一种酸降解和酶降解相结合高效制备壳寡糖的方法与流程
本发明属于生物化工技术领域,具体涉及一种酸降解和酶降解相结合的高效壳寡糖制备方法。
背景技术:
壳寡糖通常是指由2~10个氨基葡萄糖和n-乙酰氨基葡萄糖通过β-1,4糖苷键连接形成的线性寡糖,其具有降三高、调节免疫、抗肿瘤及诱导植物抗病抗逆与促进植物生长等多种生物活性。在制备工艺上,壳寡糖通常由甲壳素的脱乙酰产物壳聚糖为初始原料,经酸降解、酶降解或氧化降解制备得到。
目前能够工业化生产壳寡糖的工艺是酶降解。一般先用酸性水溶液将壳聚糖溶解,然后添加适量的酶进行降解制备壳寡糖,其中的酸性水溶液通常为醋酸、盐酸或乳酸的稀溶液,使用的酶包括特异性选择酶和非特异性选择酶。由于壳聚糖本身是一种高分子,溶解后会产生一定的粘度,其粘度随着浓度的增大而增大,当其粘度过大时则会影响酶降解的效果,所以通常酶降解制备壳寡糖时,壳聚糖溶液的浓度通常为1.0~2.5%左右,因此酶降解的生产效率较低。
壳寡糖另外一种常见的制备方法是酸降解,但目前尚无法进行工业化生产,主要原因是产品状态差和收率低。这是由于在酸降解制备壳寡糖过程中,糖苷键的断裂是随机发生的,且降解反应不能有效控制,随着降解反应的进行会不断地产生单糖,而单糖在酸性的条件下会发生多种副反应导致产品状态差。另一方面,目前壳聚糖酸降解的研究中,一般都需使用酸溶液溶解壳聚糖后,再加热进行降解反应,所以使用的试剂量普遍较大,存在排放和环境污染的问题。
技术实现要素:
本发明的目的是提供一种酸降解和酶降解相结合高效壳寡糖制备方法,有效地提高壳寡糖的生产效率和降低生产成本,从而为壳寡糖的进一步应用打下良好的基础。
本发明的技术方案是:
一种酸降解和酶降解相结合制备壳寡糖的方法,具体的工艺流程为:
(1)、将壳聚糖和酸溶液按照一定比例充分混合,在一定温度下密闭保温一段时间,使壳聚糖初步降解为中低分子量壳聚糖;
(2)、中低分子量壳聚糖加入适量的水溶解,得到高浓度的壳聚糖溶液,然后调节溶液的ph至4.2~6.0;
(3)、中低分子量壳聚糖溶液中加入适量的酶,在适宜的条件下酶解,最后得到重均分子量在400~4000的壳寡糖。
本发明首先利用酸降解对壳聚糖进行初步降解,使壳聚糖溶解后溶液的粘度大幅降低,从而大幅提高酶降解壳聚糖底物的浓度,有效地提高壳寡糖的生产效率。
本发明所述酸降解和酶降解相结合高效制备壳寡糖的方法,其特征在于,步骤(1)中,使用的壳聚糖的脱乙酰度的范围为30~99%。
本发明所述酸降解和酶降解相结合高效制备壳寡糖的方法,其特征在于,步骤(1)中,所述酸溶液是浓度为15~37%的盐酸溶液,盐酸溶液使用量为壳聚糖质量的0.2~5倍。
本发明所述的酸降解和酶降解相结合制备壳寡糖的方法,其特征在于,步骤(1)中,密闭保温的温度为40~100℃,密闭保温的时间为30~300min。作为进一步的优选,密闭保温的温度为60~80℃,密闭保温的时间为60~120min。
本发明所述酸降解和酶降解相结合高效制备壳寡糖的方法,其特征在于,步骤(1)中,使壳聚糖初步降解为重均分子量在7000~100000的中低分子量壳聚糖。
本发明所述酸降解和酶降解相结合高效制备壳寡糖的方法,其特征在于,步骤(2)中,完全溶解后中低分子量壳聚糖溶液的浓度为5~15%,优选使用壳聚糖原料或氨水调节溶液ph。
本发明所述酸降解和酶降解相结合高效制备壳寡糖的方法,其特征在于,步骤(3)中,中低分子量壳聚糖溶液中加入适量的酶,在30~70℃条件下酶解5~24h,最后得到重均分子量在400~4000的壳寡糖。
本发明的设计思想是:
研究发现,当壳聚糖酸降解的目标产物不是寡糖,而是一些分子量在几千至几万左右的中低分子量壳聚糖时,通常具有不错的效果,同时由于壳聚糖分子量的下降,其溶解后的粘度可大幅降低。另一方面,酶降解制备壳寡糖的过程中,使用的酶通常为内切酶,即当壳聚糖被降解至二糖或三糖时,糖上没有酶的结合位点,即壳二糖和壳三糖不会被进一步降解,反应更易于控制,产品收率不会大幅降低。因此在壳寡糖制备的过程中将酸降解和酶降解相结合,发挥各自的优势,回避不足,可大幅提高壳寡糖的生产效率并降低生产成本,为壳寡糖广泛应用奠定良好的基础。
本发明具有明显的优点及有益效果:
1、本发明首先利用酸降解将壳聚糖降解为中低分子量壳聚糖,使壳聚糖溶解后溶液的粘度大幅降低,再进行酶降解时,壳聚糖底物的浓度可大幅增加至10%以上,而现有工艺中酶降解制备壳寡糖中壳聚糖底物浓度通常只有1.0~2.5%左右,因此壳寡糖的生产效率可大幅提高。
2、本发明所使用的酸降解的方法,与其他酸降解的方法有明显区别,不需使壳聚糖先溶解在溶液中,而是只需使用少量的酸溶液与壳聚糖充分混合后,并密闭保温一段时间即可,因此使用的试剂量极少。
3、整个制备过程中,使用的酸溶液最后都转化成壳聚糖盐或极少量的铵盐,没有酸排放的环境污染问题。
附图说明
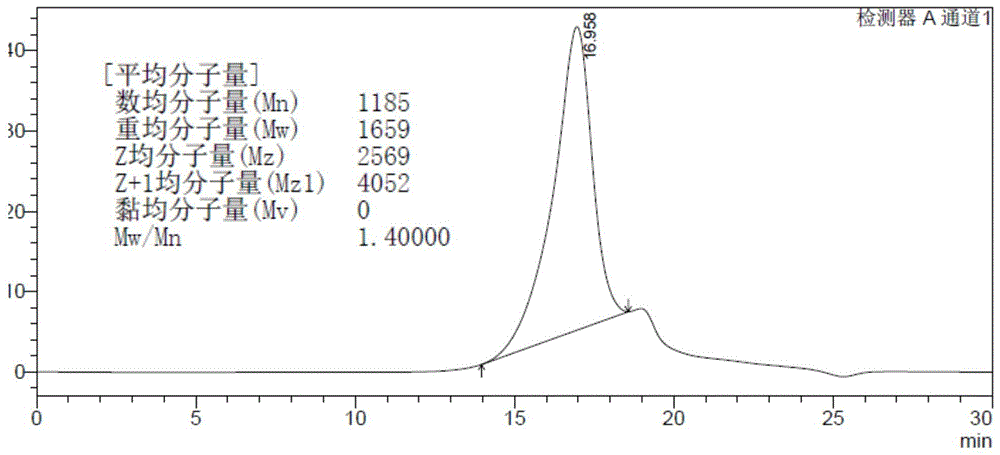
图1为本发明实施例1中的壳寡糖的gpc色谱图。
图2为本发明实施例2中的壳寡糖的gpc色谱图。
图3为本发明的工艺流程图。
具体实施方式
在具体实施过程中,如图3所示,本发明酸降解和酶降解相结合制备壳寡糖的方法,所采用的技术步骤为:
(1)、将壳聚糖和酸溶液按照一定比例充分混合,在一定温度下密闭保温一段时间,使壳聚糖初步降解为中低分子量壳聚糖;
(2)、中低分子量壳聚糖加入适量的水溶解,得到高浓度的壳聚糖溶液,然后调节溶液的ph至4.2~6.0;
(3)、中低分子量壳聚糖溶液中加入适量的酶,在适宜的条件下酶解,最后得到重均分子量在400~4000的壳寡糖。
为使本发明的技术方案和优点更加清楚,下面将结合具体实施方案进行详细描述。
实施例1
本实施例中,10g壳聚糖(重均分子量mw=78万,脱乙酰度dd=85%)与5ml37%的浓盐酸充分混合后,装入圆底烧瓶中,60℃密闭保温90min后,加入100ml蒸馏水配制成浓度大致为10%的壳聚糖溶液,测定溶液的ph=1.19,再向其中加入约1.8g壳聚糖原料,待其完全溶解后测定溶液的ph=5.25,整个过程中壳聚糖溶液的浓度可达11.8%。最后向壳聚糖溶液中加入100mg壳聚糖酶,42℃水浴下搅拌反应24h后,离心去除不溶物,清液部分冷冻干燥,得壳寡糖产品约11.8g。
称取一定量的壳寡糖样品,配成10mg/ml的溶液,用gpc色谱分析分子量数据。gpc系统组成如下:lc-20at恒流泵(岛津),cto-20a柱温箱(岛津),rid-10a示差检测器(岛津),a3000色谱柱(300mm×8.0mm,viscotek)。gpc的色谱条件为:柱温30℃,流动相为0.1mol/l的乙酸/乙酸钠缓冲溶液,流速0.5ml/min,进样量20μl,结果如图1所示。
实施例2
本实施例中,10g壳聚糖(重均分子量mw=205万,脱乙酰度dd=70%)与6ml30%的盐酸溶液充分混合后,装入圆底烧瓶中,80℃密闭保温60min后,加入120ml蒸馏水配制成浓度大致为8.3%的壳聚糖溶液,测定溶液的ph=1.35,再向其中加入约1.6g壳聚糖原料,待其完全溶解后测定溶液的ph=5.10,整个过程中壳聚糖溶液的浓度可达9.6%。最后向壳聚糖溶液中加入100mg纤维素酶,42℃水浴下搅拌反应24h后,离心去除不溶物,清液部分冷冻干燥,得壳寡糖产品约11.6g。壳寡糖样品的分子量数据分析方式和实施例1完全相同,gpc分析结果如图2所示。
实施例3
本实施例中,10g壳聚糖(重均分子量mw=78万,脱乙酰度dd=85%)与8ml25%的盐酸溶液充分混合后,装入圆底烧瓶中,60℃密闭保温90min后,加入80ml蒸馏水配制成浓度大致为12.5%的壳聚糖溶液,测定溶液的ph=1.06,再向其中加入少量氨水调节至ph=5.65左右。最后向壳聚糖溶液中加入100mg中性蛋白酶,42℃水浴下搅拌反应24h后,离心去除不溶物,清液部分冷冻干燥,得含少量氯化铵的壳寡糖产品约10g。
实施例结果表明,本发明方法能够有效地提高壳寡糖的生产效率,为壳寡糖广泛应用奠定良好的基础。
上述实施例只为说明本发明的技术构思及特点,其目的在于让熟悉此项技术的人士能够了解本发明的内容并据以实施,并不能以此限制本发明的保护范围。凡根据本发明精神实质所作的等效变化或修饰,都应涵盖在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!