一种金属有机框架材料及其制备方法和应用与流程
本发明涉及医用材料技术领域,尤其涉及一种金属有机框架材料及其制备方法和应用。
背景技术:
抗生素的持续使用不可避免地加速了细菌产生耐药性的进程,使得细菌感染面临更加严重的处境,对医疗卫生和经济发展构成严峻挑战。抗生素一般靶向作用于细菌必需的存活过程来发挥效果。然而,细菌具有通过突变和dna转移快速进化的内在能力,以克服这些抗菌药物带来的威胁。基于小分子的常规抗生素由于其自身的限制不能通过预防或消除病原微生物的生长来得到满意的效果,探索新型的抗菌药物以及治疗策略治疗多药耐药性细菌迫在眉睫。目前研制出的一类非常规的纳米抗菌材料,包括纳米银,二氧化钛,氧化铜等。基于这些纳米材料的抗菌药物已证明其对浮游细菌和生物膜感染的功效。然而,由于以下一个或多个原因,它们中的许多在临床中的使用受到限制:高毒性,高溶血率,合成或生产的复杂过程以及不能杀死多药耐药性(mdr)细菌。
光动力疗法通常需要外部光源提供能量并结合无毒光敏剂,可以将环境中三线态氧转化为包括单线态氧在内的具有杀伤性的生物活性氧(ros)。光动力治疗(pdt)策略由于其具有相对较小的诱导耐药性的可能性以及优异的生物安全性,已逐渐应用于细菌和mdr细菌感染治疗。然而应用光动力治疗原理杀菌的抗菌材料,其光敏剂分子在激发态下很容易聚集或自猝灭。
cn1695743a公开了一种医用纳米抗菌敷料的制备方法。复合纳米材料的抗菌医用敷料采有多层结构的形式组合而成,该敷料由功能层和一层支撑层所组成,其功能部分分为三层;第一层:与皮肤接触的纱布层,通过自组装技术与纳米抗菌材料(如含ag+的sio2纳米粒子、表面包覆银纳米薄层的zno纳米粒子)进行复合;第二层:用tio2或sio2纳米粉体进行超亲水处理(热浸渍技术结合紫外光照)的纱布层;第三层:具有可通透水气的多孔结构的聚氨基甲酸乙酯薄层,上表面用tio2或sio2纳米粉体进行超疏水处理。该发明的优点是广谱、长效、安全、超强杀菌、无污染、方便、可促进伤口愈合、不会产生细菌的耐药性;可有效吸收伤口部位多余水分,防止外部水分浸润,但不影响水气向外通透;可防止外部细菌的侵入。但是该发明所用的抗菌材料具有高毒性,高溶血率,对于mdr细菌的杀菌效果较差。
cn105524260b公开了一种原位聚合法制备基于氧化铜/氧化亚铜的抗菌材料的方法,包括:第一步:将氧化铜、氧化亚铜和二异氰酸酯加入到有机溶剂中,一定温度下反应1~3h,经过滤、干燥后,获得氧化铜/氧化亚铜复合抗菌粉体;第二步:将上述的氧化铜/氧化亚铜复合抗菌粉体、反应单体、稳定剂和催化剂按比例加入到聚合反应器中通过原位聚合制备基于氧化铜/氧化亚铜的抗菌树脂。该方法操作简单、高效,成本低,效用持久,应用前景广阔。但是氧化铜具有高毒性,高溶血率,生物相容性较差。
cn107828066a公开了一种四巯基卟啉修饰的金属有机框架纳米材料及其制备方法,采用uio-66作为金属有机框架纳米材料,以四巯基卟啉作为光敏剂,通过后修饰合成方法制得四巯基卟啉修饰的uio-66材料:uio-66-h2tpp-(sh)4。修饰后的uio-66-h2tpp-(sh)4既保留了uio-66内部框架结构,在水相中仍具有良好的分散性和稳定性,又保留了卟啉光敏特性。可作为一种新型的抗癌光敏材料使用。步骤简单、操作方便、实用性强。但是这种光敏材料在光动力驱动下,光敏剂分子在激发态下很容易聚集或自猝灭。
因此,本领域亟待开发一种具有很好的杀菌效果、生物相容性且光敏剂不易聚集淬灭的抗菌材料,并以此制备光驱动型抗菌敷料用于伤口细菌感染治疗。
技术实现要素:
针对现有技术的不足,本发明的目的之一在于提供一种金属有机框架材料。所述金属有机框架材料具有很好的杀菌效果、生物相容性,且在可见光驱动下不易聚集淬灭。
为达此目的,本发明采用如下技术方案:
本发明提供一种金属有机框架材料,所述金属有机框架材料包括由中心金属离子和有机配体自组装而成的纳米颗粒;
所述中心金属离子包括zr4+和ti4+,所述有机配体包括卟啉和/或金属卟啉。
金属有机框架材料(mof材料)指的是一类由无机中心金属离子或者金属团簇和有机配体自组装形成的具有分子内孔隙的有机-无机杂化材料。
本发明提供了一种新型的金属框架有机材料(pcn-224(zr/ti)),即通过在pcn-224的基础上掺杂钛离子而成,钛离子的掺入能够促进生成大量活性氧从而增强抗菌活性,可以快速有效的杀死细菌,在可见光驱动下,可以根除包括革兰氏阳性和阴性细菌在内的实验室抗生素敏感菌株和临床mdr菌株,且pcn-224(zr/ti)在激发态下不容易发生聚集或自猝灭,并且以通过其多孔结构促进生物活性氧的方便扩散,细胞毒性小。
其中,钛促进活性氧生成归因于钛-锆团簇比锆更能促进配体卟啉与团簇之间转移电子,从而进一步促进活性氧的生成、增强抗菌活性。
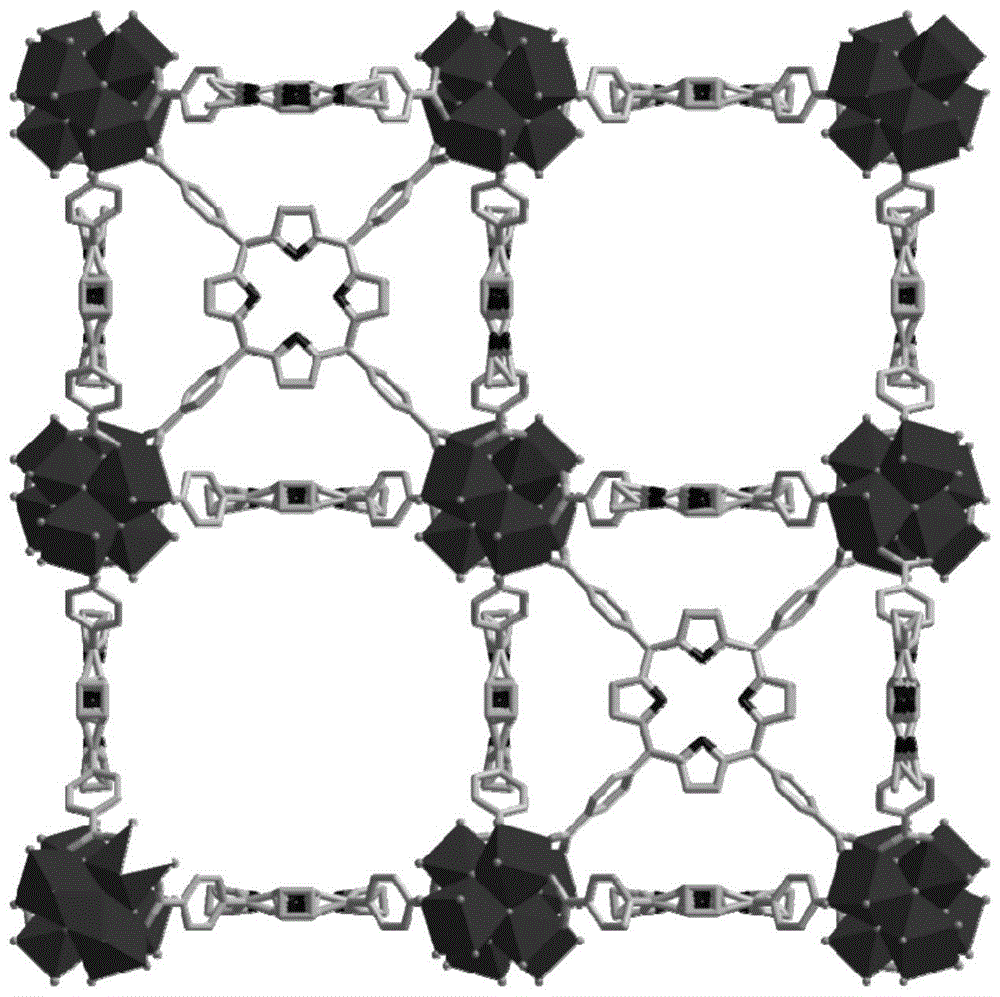
pcn-224指的是以zr4+为中心金属离子中心、以卟啉为有机配体的金属有机框架材料,即锆-卟啉金属有机框架材料,其分子结构如图1所示,其中实心球部分为中心金属离子,链状部分为卟啉有机配体。
pcn-224(zr/ti)则指本发明得到的金属框架有机材料,即在pcn-224的基础上,使ti4+取代部分zr4+,最终中心金属离子包括zr4+和ti4+,两种金属离子形成团簇。
优选地,所述中心金属离子中ti4+的质量占比为35~45%,例如36%、37%、38%、39%、40%、41%、42%、43%、44%等,优选35%。
优选地,所述有机配体包括卟啉。
优选地,所述金属卟啉包括铂卟啉(pt(ii)卟啉)、铜卟啉(cu(ii)卟啉)、铁卟啉(fe(iii)卟啉)、锌卟啉(zn(ii)卟啉)和镍卟啉(ni(ii)卟啉)中的任意一种或至少两种组合。
优选地,所述纳米颗粒的粒径为300~400nm,例如310nm、320nm、330nm、340nm、350nm、360nm、370nm、380nm、390nm等。
本发明的目的之二在于提供一种目的之一所述的金属有机框架材料的制备方法,所述制备方法包括如下步骤:
(a)将pcn-224纳米颗粒、ticp2cl2和溶剂混合,反应后得到所述金属有机框架材料。
本发明通过上述方法在pcn-224纳米颗粒中掺杂钛离子,即钛离子部分取代锆离子,从而得到抗菌材料pcn-224(zr/ti)。
优选地,步骤(a)中,所述反应的温度为100~150℃,例如105℃、110℃、115℃、120℃、125℃、130℃、135℃、140℃、145℃等,优选120℃。
优选地,步骤(a)中,所述反应的时间为1~8天,例如2天、3天、4天、5天、6天、7天等,优选2天。
优选地,步骤(a)中,所述溶剂包括n,n-二甲基甲酰胺。
优选地,步骤(a)中,所述反应在烘箱中进行。
优选地,步骤(a)中,所述pcn-224纳米颗粒和ticp2cl2的质量比为(80~90):75,例如81:75、82:75、83:75、84:75、85:75、86:75、87:75、88:75、89:75等,优选83:75。
优选地,步骤(a)还包括对所述反应的产物进行洗涤。
优选地,步骤(a)中,所述洗涤的洗涤剂包括n,n-二甲基甲酰胺和/或乙醇。
优选地,步骤(a)还包括在所述洗涤之后进行离心。
优选地,步骤(a)具体包括:
将质量比为(80~90):75的pcn-224纳米颗粒和ticp2cl2溶解于溶剂中,在100~150℃条件下反应1~8天,洗涤,离心,得到所述金属有机框架材料。
优选地,所述pcn-224纳米颗粒的制备方法包括如下步骤:
(b)将zrocl2·8h2o、四(4-羧基苯基)卟啉、苯甲酸和溶剂混合,搅拌,得到所述pcn-224纳米颗粒。
本发明进一步优化了pcn-224纳米颗粒的制备方法,苯甲酸的加入能够对pcn-224纳米颗粒的形态进行控制,最终得到分散均匀、粒径均一的pcn-224纳米颗粒,能够从常见的微米级到纳米级,利于生成的活性氧传递扩散,钛促进活性氧生成归因于钛-锆团簇比锆更能促进配体卟啉与团簇之间转移电子,从而进一步促进活性氧的生成、增强抗菌活性。
优选地,步骤(b)中,所述搅拌的温度为100~150℃,例如105℃、110℃、115℃、120℃、125℃、130℃、135℃、140℃、145℃、148℃等,优选120℃。
在优选方案中,控制搅拌温度为100~150℃,特别是120℃时,能够获得分散更加均匀,粒径更加均一的pcn-224纳米颗粒,进而提高pcn-224(zr/ti)的活性。
优选地,步骤(b)中,所述搅拌的速率为500~1300rpm,优选1300rpm。
优选地,步骤(b)中,所述搅拌的时间为0.5~2h,例如0.6h、0.7h、0.8h、0.9h、1h、1.2h、1.5h、1.6h、1.8h等,优选1h。
优选地,步骤(b)中,所述zrocl2·8h2o和四(4-羧基苯基)卟啉的质量比为(1~3):1,例如1.2:1、1.4:1、1.6:1、1.8:1、2:1、2.2:1、2.5:1、2.6:1、2.8:1等,优选2:1。
优选地,步骤(b)中,所述zrocl2·8h2o和四(4-羧基苯基)卟啉的总质量与所述苯甲酸的质量比为(0.5~2):10,例如0.6:10、0.8:10、1:10、1.2:10、1.4:10、1.6:10、1.8:10、1.9:10等,优选1:10。
优选地,步骤(b)中,所述溶剂包括n,n-二甲基甲酰胺。
优选地,步骤(b)还包括对产物进行洗涤和离心。
优选地,步骤(b)中,所述洗涤的洗涤剂包括n,n-二甲基甲酰胺和/或乙醇。
优选地,步骤(b)具体包括如下步骤:
将zrocl2·8h2o、四(4-羧基苯基)卟啉和苯甲酸加入至溶剂中,以500~1300rpm的速率搅拌0.5~2h,洗涤,离心,得到所述pcn-224纳米颗粒;
所述zrocl2·8h2o和四(4-羧基苯基)卟啉的质量比为(1~3):1;
所述zrocl2·8h2o和四(4-羧基苯基)卟啉的总质量与所述苯甲酸的质量比为(0.5~2):10。
本发明的目的之三在于提供一种敷料,所述敷料包括目的之一所述的金属有机框架材料和静电纺丝纤维。
优选地,所述静电纺丝纤维的制备原料包括聚乳酸-羟基乙酸共聚物、聚己内酯、聚乙烯醇、聚丙烯腈、聚乙酸乙烯酯、壳聚糖、聚氨酯、聚乳酸、和明胶中的任意一种或至少两种组合,优选聚乳酸-羟基乙酸共聚物。
优选地,所述金属有机框架材料和静电纺丝纤维的质量比为(2~5):650,例如2.5:650、3:650、3.5:650、4:650、4.5:650等,优选3:650。
本发明的目的之四在于提供一种目的之三所述的敷料的制备方法,所述制备方法包括如下步骤:
(1)将静电纺丝纤维原料溶解于溶剂中,搅拌,得到纺丝溶液;
(2)将目的之一所述的金属有机框架材料溶解于溶剂中,得到金属有机框架材料溶液;
(3)将所述纺丝溶液和金属有机框架材料溶液进行静电纺丝,得到所述敷料。
优选地,步骤(1)中,所述静电纺丝纤维原料包括聚乳酸-羟基乙酸共聚物、聚己内酯、聚乙烯醇、聚丙烯腈、聚乙酸乙烯酯、壳聚糖、聚氨酯、聚乳酸、和明胶中的任意一种或至少两种组合,优选聚乳酸-羟基乙酸共聚物。
优选地,步骤(1)中,所述溶剂包括六氟异丙醇、n,n-二甲基甲酰胺、n,n-二乙基甲酰胺、二氯甲烷、乙醇和丙酮中的任意一种或至少两种组合。
优选地,步骤(2)中,所述静电纺丝的电压为10~20kv,例如11kv、12kv、13kv、14kv、15kv、16kv、17kv、18kv、19kv等,优选15kv。
优选地,步骤(2)中,所述静电纺丝过程中,注射器针头的喷射距离为1~10cm,例如2cm、2.5cm、3cm、3.5cm、4cm、4.5cm、5cm、5.5cm、6cm、6.5cm、7cm、7.5cm、8cm、8.5cm、9cm、9.5cm、9.8cm等,优选8cm。
相对于现有技术,本发明具有如下有益效果:
本发明提供了一种新型的金属框架有机材料(pcn-224(zr/ti)),通过钛离子的掺入,促进生成大量活性氧从而增强抗菌活性,可以快速有效的杀死细菌,在可见光驱动下,可以根除包括革兰氏阳性和阴性细菌在内的实验室抗生素敏感菌株和临床mdr菌株,且pcn-224(zr/ti)在激发态下不容易发生聚集或自猝灭,并且以通过其多孔结构促进生物活性氧的方便扩散,细胞毒性小。
此外,还提供了一种包含pcn-224(zr/ti)和静电纺丝纤维的敷料,用于治疗细菌感染。
附图说明
图1是中pcn-224纳米颗粒的分子结构示意图。
图2是实施例1中pcn-224纳米颗粒的sem图。
图3是实施例1中pcn-224纳米颗粒的tem图。
图4的实施例1中pcn-224(zr/ti)纳米颗粒的sem图。
图5是实施例1中pcn-224(zr/ti)纳米颗粒的tem图。
图6是测试例1中荧光强度随mof纳米颗粒浓度的变化图。
图7是测试例2中不同菌株在600nm处的吸光度变化图。
图8是测试例2中不同菌株在600nm处的吸光度变化图。
图9是测试例3中细胞存活率随pcn-224(zr/ti)纳米颗粒浓度的变化图。
图10a是测试例3中加入不同样品的溶液颜色变化图
图10b是测试例3中不同样品在450nm处的吸光度变化图。
图11是实施例2中pcn-224(zr/ti)敷料的sem图。
图12是测试例4中感染mdre.coil和mrsa的小鼠的伤口愈合图像(a-感染mdre.coil,覆盖纱布7天;b-感染mdre.coil,覆盖plga空白纤维7天;c-感染mdre.coil,覆盖pcn-224(zr/ti)敷料7天;d-感染mdre.coil,覆盖纱布14天;e-感染mdre.coil,覆盖plga空白纤维14天;f-感染mdre.coil,覆盖pcn-224(zr/ti)敷料14天;g-感染mrsa,覆盖纱布7天;h-感染mrsa,覆盖plga空白纤维7天;i-感染mrsa,覆盖pcn-224(zr/ti)敷料7天;j-感染mrsa,覆盖纱布14天;k-感染mrsa,覆盖plga空白纤维14天;l-感染mrsa,覆盖pcn-224(zr/ti)敷料14天)。
具体实施方式
为便于理解本发明,本发明列举实施例如下。本领域技术人员应该明了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。
实施例1
本实施例提供一种pcn-224(zr/ti)的合成方法,具体如下:
(1)pcn-224纳米颗粒的制备:
在干燥的dmf溶液(10ml)中超声混合50mgzrocl2·8h2o、25mg四(4-羧基苯基)卟啉(tcpp)和0.75g苯甲酸。在120℃搅拌(1300rpm)混合物1小时,用dmf和乙醇洗涤产物,离心收集红棕色产物,获得pcn-224纳米颗粒;
通过透射电子显微镜(生产厂家:美国fei公司,仪器型号:tecnaig220s-twin)(tem)和扫描电子显微镜(日立高新场发射扫描电子显微镜su8200)(sem)对pcn-224纳米颗粒进行测试,结果如图2(sem)和图3(tem)所示,两幅图中均显示pcn-224纳米颗粒分布均匀且粒径均一,通过测量和计算得到的平均粒径为400nm。
(2)pcn-224(zr/ti)纳米颗粒的制备:
将83mgpcn-224纳米颗粒和75mgticp2cl2溶解在dmf溶液(12ml)中。将反应混合物置于100ml小瓶中,放入120℃的烘箱中,反应2天,使用dmf和乙醇洗涤后通过离心收集产物pcn-224(zr/ti)纳米颗粒。
通过电感耦合等离子体质谱仪icp-oes测得pcn-224(zr/ti)纳米颗粒的中心金属离子中ti4+的质量占比为35%。
通过扫描电子显微镜和透射电子显微镜对pcn-224(zr/ti)进行测试,分别得到图4所示的sem图和图5所示的tem图,图中显示pcn-224纳米颗粒分布均匀且粒径均一,通过测量和计算得到的平均粒径为400nm。
测试例1活性氧测试
通过活性氧荧光探针dcfh-da分别测量实施例1得到的pcn-224纳米颗粒和pcn-224(zr/ti)纳米颗粒在可见光照射下ros产生的含量。将100μl活性氧探针的工作液试剂和各种浓度的等体积mof纳米颗粒悬浮液置于一次性黑色板孔中,可见光照射(200mwcm-2)3分钟。荧光数据用488nm的激发波长记录。
结果如图6所示,图中显示,在相同浓度下,pcn-224(zr/ti)纳米颗粒相较于pcn-224纳米颗粒ros产生量明显提升,证明钛离子的掺杂对于ros产生量的提升起到了至关重要的作用。
测试例2体外杀菌活性测定
我们分别将不同菌株的稀释细菌悬浮液(50μl)放置于孔板中,并加入同体积的实施例1得到的pcn-224(zr/ti)纳米颗粒的pbs溶液(终浓度为50μgml-1),其中大肠杆菌(e.coil)、耐药大肠杆菌(mdre.coil)、鲍曼不动杆菌(a.baumannii)、耐药鲍曼不动杆菌(mdra.baumannii)为一组,金色葡萄球菌(s.aureus)、耐药金色葡萄球菌(mrsa)、表皮葡萄球菌(s.epidermidis)、耐药表皮葡萄菌(mrse)为一组。通过用等体积的细菌培养基替换pcn-224(zr/ti)来进行对照实验。可见光照射(200mwcm-2)测试30分钟,然后在37℃细菌培养箱中孵育。通过酶标仪在12小时和24小时测量细菌悬浮液在600nm的吸光度。
结果如图7和图8所示,图中显示,12h和24h时,加入pcn-224(zr/ti)纳米颗粒的实验组的吸光度相对于对照组均明显降低,证明pcn-224(zr/ti)纳米颗粒对于上述菌株具有良好的杀菌活性。
测试例3材料生物相容性
(1)选择人脐静脉内皮细胞(huvecs)用于pcn-224(zr/ti)细胞毒性的测定。将100μl的huvec细胞(每毫升105个细胞)在一次性96孔板中培养过夜。用不同浓度的pcn-224(zr/ti)与细胞共孵育,并继续培养细胞另外24小时。用pbs洗涤细胞,并用10μlcck-8(试剂盒)试剂在37℃下孵育4小时。通过酶标仪读取450nm处细胞的光密度(od450)。测试结果如图9所示。
图9是细胞存活率随pcn-224(zr/ti)纳米颗粒浓度的变化图,图中显示,当pcn-224(zr/ti)纳米颗粒≤80μg/ml时,细胞存活率接近100%,进一步提高至100至120μg/ml,细胞存活率仍保持在80%以上,证明本发明提供的pcn-224(zr/ti)的细胞毒性较小。
(2)选取大鼠的新鲜血液样品测试pcn-224(zr/ti)的溶血能力。将血液样品以1500rpm离心15分钟并用盐水洗涤三次以得到红细胞。将获得的红细胞重新稀释成4%悬浮液。在37℃下分别与水、生理盐水和不同浓度的pcn-224(zr/ti)生理盐水溶液混合孵育3小时。然后通过12000rpm离心15分钟获得上清液,通过uv-vis分光光度计测量540nm处的吸光度。在该实验中,水用作阳性对照,结果如图10a和图10b所示。
图10a是加入不同样品的溶液颜色变化图,从左到右样品分别为水、生理盐水(0.9%)、浓度为10μg/ml、20μg/ml、40μg/ml、80μg/ml、160μg/ml、320μg/ml的pcn-224(zr/ti)溶液,图中斜线填充代表溶液颜色变红,说明出现细胞溶血,仅添加水的对照组出现颜色的变化,由此证明,pcn-224(zr/ti)溶血率较低。
图10b是不同样品的吸光度变化图,图中显示添加水的对照组吸光度较高,而添加生理盐水以及pcn-224(zr/ti)溶液的样品的吸光度均处于较低水平,进一步证明pcn-224(zr/ti)溶血率较低。
实施例2
本实施例提供一种敷料及其制备方法,具体如下:
将1.3gplga溶解于8.7g六氟异丙醇(hfip)制备纺丝溶液,搅拌混合物直至形成澄清溶液。然后将6mg实施例1得到的pcn-224(zr/ti)溶解于3ghfip。该纺丝溶液和pcn-224(zr/ti)的hfip溶液,在15kv的电压和8.0cm的距离下共纺制备基于pcn-224(zr/ti)的静电纺丝纤维敷料。
对所述敷料进行sem测试,结果如图11所示,图中显示pcn-224(zr/ti)附着在静电纺丝纤维表面。
测试例4伤口愈合实验
通过在小鼠背部产生伤口来建立大鼠伤口模式。选择美国斯泼累格·多雷(spraguedawley,简称sd)雌性大鼠评估pcn-224(zr/ti)纳米粒子体内抗菌性能。大鼠分别用耐药金色葡萄球菌(mrsa)和耐药大肠杆菌(mdre.coil)(108cfuml-1,200μl)感染30min。每只大鼠都有三个相同大小的伤口(约直径为2厘米),分别覆盖着纱布、plga空白纤维和实施例2的pcn-224(zr/ti)敷料。在添加相应材料后,所有小鼠在可见光照射(200mwcm-2)下30分钟。在不同的时间间隔(7天和14天)观察伤口愈合情况。
结果如图12所示,其中,a-感染mdre.coil,覆盖纱布7天;b-感染mdre.coil,覆盖plga空白纤维7天;c-感染mdre.coil,覆盖pcn-224(zr/ti)敷料7天;d-感染mdre.coil,覆盖纱布14天;e-感染mdre.coil,覆盖plga空白纤维14天;f-感染mdre.coil,覆盖pcn-224(zr/ti)敷料14天;g-感染mrsa,覆盖纱布7天;h-感染mrsa,覆盖plga空白纤维7天;i-感染mrsa,覆盖pcn-224(zr/ti)敷料7天;j-感染mrsa,覆盖纱布14天;k-感染mrsa,覆盖plga空白纤维14天;l-感染mrsa,覆盖pcn-224(zr/ti)敷料14天;
图12中显示,在相同细菌和相同间隔时间下,覆盖有pcn-224(zr/ti)敷料的小鼠(c、f、i和l)的伤口愈合程度更高,由此证明,实施例2得到的pcn-224(zr/ti)敷料相较于纱布和plga空白纤维具有更好的杀菌效果。
上述测试例的结果证明,本发明提供的新型金属框架有机材料pcn-224(zr/ti)能够促进生成大量活性氧从而增强抗菌活性,可以快速有效的杀死细菌,同时具有良好的生物相容性和较小的细胞毒性。
申请人声明,本发明通过上述实施例来说明本发明的详细工艺设备和工艺流程,但本发明并不局限于上述详细工艺设备和工艺流程,即不意味着本发明必须依赖上述详细工艺设备和工艺流程才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
- 还没有人留言评论。精彩留言会获得点赞!