单体化合物、用于治疗慢性肾病的药物组合物及其应用的制作方法
本发明涉及生物医药领域,具体涉及一种单体化合物、用于治疗慢性肾病的药物组合物及其应用。
背景技术:
慢性肾脏病(chronickidneydiseases,ckd)是对影响肾脏结构和功能的异质性疾病的总称。据统计,在中国有超过10.8%的人患有肾病,在美国,晚期肾病的死亡率超过20%。近年来,慢性肾脏病在全球的发病情况逐年提高,而且预后差、花费高,成为世界范围内的严重危害人类健康的公共卫生问题。
技术实现要素:
为解决上述问题,本发明提供了单体化合物、用于治疗慢性肾病的药物组合物及其应用;所述单体化合物具有减轻炎症等引起的肾小球细胞损伤的功效,有助于减轻肾小球等细胞的形态学和功能损伤。本发明还提供了用于治疗慢性肾病的药物组合物及其应用。
第一方面,本发明提供了一种单体化合物或其药学上可接受的盐,所述单体化合物的结构式如式ⅰ所示,
可选地,所述单体化合物在药学上可接受的盐选自钠盐、钾盐、铝盐、锂盐、锌盐、钙盐、镁盐、钡盐、铵盐、三甲胺盐、四甲基铵盐、二乙胺盐、三乙胺盐、异丙基胺盐、乙醇胺盐、二乙醇胺盐、三乙醇胺盐、环己胺盐、二环己基胺盐、吡啶盐、甲基吡啶盐、2,6-二甲基吡啶盐、咖啡碱盐、普鲁卡因盐、胆碱盐、甜菜碱盐、可可碱盐、嘌呤盐、哌嗪盐、哌啶盐、n-乙基哌啶盐、聚胺树脂盐、苯明青霉素盐、盐酸盐、氢溴酸盐、硫酸盐、硝酸盐、磷酸盐、甲酸盐、乙酸盐、羟乙酸盐、丙酸盐、2-羟基丙酸盐、丙二酸盐、三氟乙酸盐、甲磺酸盐、乙磺酸盐、三氟甲磺酸盐、乙烯磺酸盐、苯磺酸盐、对甲苯磺酸盐、苯甲酸盐、苯乙酸盐、褐藻酸盐、氨茴酸盐、樟脑酸盐、马来酸盐、酒石酸盐、柠檬酸盐、琥珀酸盐、扁桃酸盐、富马酸盐、苹果酸盐、草酸盐、水杨酸盐、葡萄糖醛酸盐、半乳糖醛酸盐、枸橼酸盐、天冬氨酸盐、谷氨酸盐、肉桂酸盐或者它们的组合。
本发明第一方面提供的单体化合物或其药学上可接受的盐,具有减轻炎症等引起的肾小球细胞损伤的功效,有助于减轻肾小球等细胞的形态学和功能损伤,可以广泛用于治疗慢性肾病的药物中,或是辅助养胃的食品或保健品领域。所述单体化合物或其药学上可接受的盐可以通过天然植物经益生菌发酵制得,安全可靠。
第二方面,本发明提供了一种药物组合物,包括活性组分和药学上可接受的辅料;所述活性组分包括如式ⅰ所示的单体化合物或其药学上可接受的盐:
可选地,所述药物组合物包括由枸杞子、山茱萸、生地黄、山药、川牛膝、桑葚、淫羊藿和巴戟天的中草药复方提取液经益生菌发酵制得的发酵液,所述益生菌包括乳酸菌和双歧杆菌。
可选地,所述中草药复方提取液包括如下重量份数的原料组分:1-20份枸杞子、1-25份山茱萸、1-15份生地黄、5-20份山药、3-18份川牛膝、1-15份桑葚、2-16份淫羊藿和1-10份巴戟天。
进一步地,可选地,所述中草药复方提取液包括如下重量份数的原料组分:3-20份枸杞子、5-25份山茱萸、3-15份生地黄、5-10份山药、6-15份川牛膝、5-10份桑葚、2-5份淫羊藿和2-8份巴戟天。
可选地,所述乳酸菌为副干酪乳杆菌,所述双歧杆菌为婴儿双歧杆菌。可选地,所述乳酸菌和双歧杆菌的质量比为1:(0.1-10)。
进一步地,所述乳酸菌和双歧杆菌的质量比为1:(0.5-3)。
可选地,所述发酵液的制备方法包括:
按重量分散称取各组分并放入容器中,经加水浸泡、煎煮和灭菌后,得到中草药复方提取液;
向所述中草药复方提取液中接入含有所述益生菌的菌液发酵,发酵温度23-30℃,发酵时间16-48小时,发酵结束后,经过滤、浓缩后得到所述发酵液。
可选地,所述发酵过程中的ph为5.0-6.0。
进一步地,可选地,所述发酵过程中的ph为5.5-6.0。
例如,所述发酵过程中的ph为5.0,或为5.5,或为5.8,或为6.0。
本发明实施方式中,所述由枸杞子、山茱萸、生地黄、山药、川牛膝、桑葚、淫羊藿和巴戟天的中草药复方提取液经益生菌发酵制得的所述发酵液中含有所述单体化合物。通过将所述发酵液经过真空低温冻干后经色谱法分离及高效液相色谱法(hplc),可以获得所述单体化合物。
一具体实施方式中,从所述发酵液分离获得所述单体化合物的方法包括:
将所述发酵液经过离心7000-10000r/min获得上清液,上清液经色谱法分离及hplc法收集得到所述单体化合物。该制备工艺简单、操作方便,得到的单体化合物纯度高。
本发明一实施方式中,所述药物组合物为所述由枸杞子、山茱萸、生地黄、山药、川牛膝、桑葚、淫羊藿和巴戟天的中草药复方提取液经益生菌发酵制得的所述发酵液;其中,所述发酵液中含有的所述单体化合物作为所述药物组合物中的至少一种活性组分。
可选地,所述药物组合物中,所述单体化合物或其药学上可接受的盐的质量百分含量为0.01-90%。其中,所述药物组合物中的所述单体化合物质量百分含量还可以通过添加外加的单体化合物进行调节。
例如,所述药物组合物中,所述单体化合物或其药学上可接受的盐的质量百分含量为0.01-50%,或10-50%,或20-50%,或0.1-10%。
本发明另一实施方式中,所述药物组合物由所述发酵液和药学上可接受的辅料组成;所述发酵液由枸杞子、山茱萸、生地黄、山药、川牛膝、桑葚、淫羊藿和巴戟天的中草药复方提取液经益生菌发酵制得。
本发明第三实施方式中,所述药物组合物包括所述单体化合物或其药学上可接受的盐的活性组分和药学上可接受的辅料;其中,所述单体化合物或其药学上可接受的盐采用发酵方法分离得到和/或人工合成方法合成得到。所述发酵方法是指:先将枸杞子、山茱萸、生地黄、山药、川牛膝、桑葚、淫羊藿和巴戟天的中草药复方提取液经益生菌发酵制得的所述发酵液,然后从实施发酵液中分离提取所述单体化合物或其药学上可接受的盐。所述人工合成方法可以但不限于为通过boc固相合成法或fmoc固相合成法。
可选地,所述药物组合物还包括其他活性组分,所述其他活性组分包括维生素c、维生素e、辅酶q、谷胱甘肽、胡萝卜素和甜菜碱中的至少一种。
其中,一实施方式中,所述其他活性组分可以为维生素c、维生素e、辅酶q、谷胱甘肽、胡萝卜素或甜菜碱。另一实施方式中,所述其他活性组分可以为维生素c、维生素e、辅酶q、谷胱甘肽、胡萝卜素和甜菜碱中的至少两种。
可选地,所述药物组合物中的其他活性组分可根据所述药物组合物的具体用途进行调整。例如,所述其他活性组分也具有一定的抗慢性肾病的功效,或者所述其他活性组分具有一定的辅助抗炎症的功效等等。
可选地,所述药物组合物中,所述其他活性组分的质量百分含量可以但不限于为1%-70%。
可选地,所述药物组合物的剂型包括胶囊、微型胶囊、栓剂、粉剂、颗粒散、口服液、气雾剂、果冻和冲剂中的一种。
本发明实施方式中,所述药物组合物的剂型可以通过添加相对于的药学上可接受的辅料形成。
可选地,所述药学上可接受的辅料可以但不限于包括载体或赋形剂。可选地,所述载体包括溶剂、聚合物、脂质体和稀释剂中的至少一种。其中,所述溶剂可以但不限于包括水、生理盐水,或其他非水性溶剂。所述聚合物可以但不限于包括聚赖氨酸、聚乙烯亚胺及其改性物、壳聚糖、聚乳酸和明胶中的至少一种。可选地,所述脂质体可以但不限于包括胆固醇、豆卵磷脂和蛋黄卵磷脂中的至少一种。可选地,所述稀释剂包括淀粉类、糖类、纤维素类和无机盐中的一种或多种。可选地,所述赋形剂包括片剂中的黏合剂、填充剂、润滑剂,半固体制剂软膏剂、霜剂中的基质部分、防腐剂、抗氧剂、矫味剂、芳香剂、助溶剂、乳化剂和着色剂中的至少一种。
本发明第二方面提供了一种用于治疗慢性肾病的药物化合物,所述药物组合物中至少包括本发明第一方面所述的单体化合物的活性组分;所述药物组合物具有减轻炎症等引起的肾小球细胞损伤,有助于减轻肾小球等细胞的形态学和功能损伤的功效。具体地,所述药物组合物能显著减轻高糖引起的活性氧(ros)积累、超氧化物歧化酶(sod)活性降低及炎症因子的分泌,有助于减轻氧化因子、炎症因子对细胞的损伤。同时,所述药物组合物可通过调控tlr4/nf-κb/nlrp3炎性信号通路轴,发挥其对细胞的保护作用。
本发明第二方面提供的所述用于治疗慢性肾病的药物化合物,其可以通过将枸杞子、山茱萸、生地黄、山药、川牛膝、桑葚、淫羊藿和巴戟天的中草药复方提取液经益生菌发酵制得,所述中草药复方提取液是从天然中草药中提取出来的,其具有很好的药理活性的特点,可以避免传统药物带来的巨大的药副作用。同时,本发明中包括所述发酵液的药物组合物的制备过程中使用的益生菌是定殖在人体内,对宿主有益的活性微生物。益生菌对调节宿主免疫功能、保持肠道健康具有重要作用;在抗炎、预防肿瘤、降血脂、预防食物过敏等方面都发挥重要作用。其制备工艺简单,制得的药物组分物药效起作用较快,药效明显,能起到标本兼治的效果。
本发明所述由枸杞子、山茱萸、生地黄、山药、川牛膝、桑葚、淫羊藿、巴戟天组成的中草药复方提取液对于慢性肾病均具有很好的药理活性;同时益生菌具有很好的减毒和增加药物疗效的作用,因此,所述包括所述发酵液的药物组合物具有更小的副作用和更高的疗效。
第三方面,本发明还提供了一种如本发明第二方面所述的药物组合物在制备用于预防或治疗慢性肾病的药物或保健品中的应用。
可选地,所述慢性肾病包括糖尿病肾病、肾小动脉硬化、原发性与继发性肾小球肾炎、肾小管间质病变、肾血管病变和遗传性肾病。例如,iga肾病或igg肾病。
一实施方式中,本发明提供了一种如本发明第二方面所述的药物组合物在制备用于预防或治疗慢性肾病的药物中的应用。另一实施方式中,本发明提供了一种如本发明第二方面所述的药物组合物在制备用于预防或治疗慢性肾病的保健品中的应用。本发明所述药物组合物除了在药物或保健品中的应用之外,还可以应用与食品中。例如,在本发明实施方式中,所述药物组合物作为食品添加剂加入至食品,甚至是保健食品中,作为预防或治疗慢性肾病的有效成分。
可选地,所述保健品的物理形态可以但不限于包括凝胶状或水剂状。可选地,所述保健品中还包括添加剂,所述添加剂可以但不限于包括单糖、寡糖、多糖、氨基酸、抗氧化和ph调节剂中的至少一种。
可选地,所述药物为化学类药物和生物药物中的至少一种。进一步可选的,所述生物药物包括多肽类药物、蛋白药物和基因药物中的一种或多种。
本发明第三方面所述的药物组合物,具有减轻炎症等引起的肾小球细胞损伤,有助于减轻肾小球等细胞的形态学和功能损伤的功效,可以在食品、药物和保健品中的得到广泛应用。
附图说明
为了更清楚地说明本申请实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本申请的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
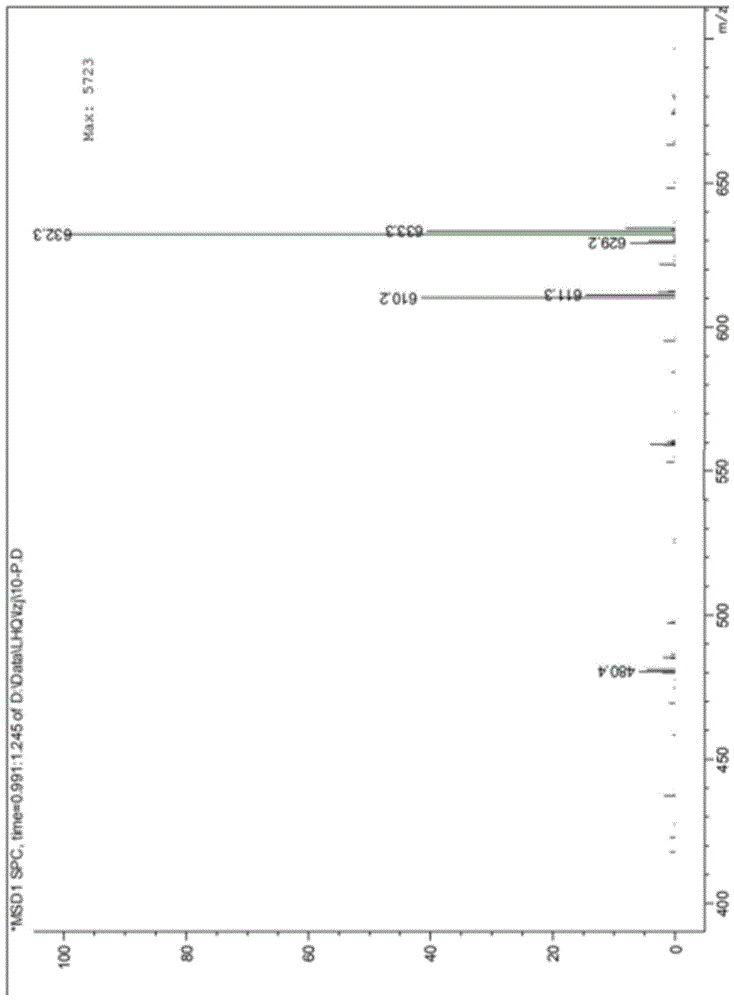
图1是本发明一实施例提供的单体化合物的质谱检测图谱;
图2是本发明另一实施例提供的单体化合物的质谱检测图谱;
图3是本发明一实施例提供的单体化合物的高效液相检测图谱;
图4是本发明一实施例提供的药物组合物及单体化合物抑制hg诱导hbzy-1的细胞增殖数据图;
图5是本发明一实施例提供的药物组合物及单体化合物抑制hg抑制hbzy-1的细胞炎症反应数据图;
图6是本发明一实施例提供的药物组合物及单体化合物抑制hg诱导的hbzy-1细胞氧化应激;
图7本发明一实施例提供的药物组合物及单体化合物抑制tlr4nf-κb/nlrp3炎症途径数据图;
图8本发明一实施例提供的药物组合物及单体化合物抑制tlr4/nf-κb通路抑制nlrp3炎症反应数据图;
图9本发明一实施例提供的药物组合物及单体化合物在hg条件下tlr4/nf-κb/nlrp3炎性轴对hbzy-1细胞的抑制作用数据图。
具体实施方式
以下所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也视为本发明的保护范围。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
若无特别说明,本发明实施例所采用的原料及其它化学试剂皆为市售商品。
实施例一
一种药物组合物的制备,包括:
按比例取3份枸杞子、5份山茱萸、5份生地黄、5份山药、8份川牛膝、10份桑葚、3份淫羊藿、2份巴戟天提取物粉共30g;经加水浸泡、煎煮和灭菌后,得到中草药复方提取液;将10g选取含有乳酸菌和双歧杆菌,乳酸菌为副干酪乳杆菌,双歧杆菌包括婴儿双歧杆菌的益生菌干粉;即得到混合物。在温度为25℃、ph为5.5的条件下发酵24h,得到发酵液。
对发酵液9000r/min离心30min,除去沉淀并保留上清液,对上清液进行冷冻干燥,得到药物组合物。
效果实施例
为了评估本发明上述方法制备得到用于治疗慢性肾病的药物组合物的效果,进行如下效果测试实施例。
(一)单体化合物的分离和检测
取由实施例1制备的60g药物组合物经真空低温冻干经多种色谱及hplc制备,得到抗慢性肾病中药益生菌发酵单体化合物,并利用质谱和高效液相色谱对其进行测定,其中质谱测定条件为esi正离子模式毛细管电压3kv,锥孔电压50v,萃取电压5v,脱溶剂温度350℃,雾化气流350l/h;高效液相色谱测定条件为采用液相波士顿液相色谱柱(bostongreenods-aq色谱柱(250*4.6mm)),以0.1%三氟乙酸水溶液为流动相a,以0.1%三氟乙酸的乙腈溶液为流动相a,流动相a:流动相b=75:25,流速为1ml/min,检测波长为220nm,进样量10μl。
结果如图1-图3所示,其中图1和图2分别为单体化合物在[m-h]-和[m+h]+下的质谱测定图谱,图3为单体化合物的高效液相色谱测定图谱,从以上结果中可以解析出所述单体化合物的化学结构如式ⅰ所示,
(二)药物组合物和单体化合物对慢性肾病的影响。
动物模型试验设计:将多只雄性sprague-dawley(sd)大鼠(180-220g)饲养在相对湿度为55±5%的22±2℃室内,光-暗循环(12-12小时),待适应1周实环境或进行试验。大鼠随机分为对照组和高果糖喂养组;其中,对照组给予标准饲料和饮用水,高果糖喂养组给予标准饲料和加入10%的果糖的饮用,服用10周,每天都更换新鲜的饮用水。期间,4周后,将高果糖喂养组的大鼠进一步分为3个亚组(n=8),分别对应给予纯净水(1ml/kg)、单体化合物(2mg/kg)和药物组合物(2mg/kg)灌胃,连续6周。
(1)血糖含量试验:在喂食的最后一周,大鼠称重并禁食14小时,然后口服葡萄糖(1.5g/kg)。尾静脉血样于0~120min不同时间采集,4℃下离心10min(4000g离心力),然后用血糖测定试剂盒测定血糖含量。
(2)尿白蛋白分析:上述(1)实验结束时,将大鼠置于代谢笼中24小时,收集尿液样本并记录体积。2000g离心10min以去除微粒污染物,上清液用于尿白蛋白分析。
(3)组织学分析和免疫印迹试验分析:上述口服葡萄糖耐量试验后,大鼠恢复3天;然后禁食16h后处死大鼠。在冰上被迅速解剖肾组织。一部分立即固定进行组织学分析,另一部分保存在液氮中进行免疫印迹试验(westernblotting)分析。采集血样并在4℃下离心(3000g)10min,血清-80℃冷冻保存,酶联免疫吸附测定(elisa)试剂盒检测尿酸、肌酐、血尿素氮、胰岛素、甘油三酯、总胆固醇和低密度脂蛋白等含量。
其中,分布将hbzy-1细胞在正常葡萄糖(ng,5.5mmd-葡萄糖)、甘露醇+葡萄糖(m+g,24.5mm甘露醇和5.5mmd-葡萄糖)或高糖(hg,30mmd-葡萄糖)条件下培养。每种培养条件下,分别设置普通无添加组、添加药物组合物组、添加单体化合物组和空白对照组(仅用缓冲液培养细胞);然后mtt法(四甲基偶氮唑盐微量酶反应比色法)检测细胞增殖水平。
结果如图4所示,其中,图4中(a)为ng培养条件下各组的细胞相对活性图;图4中(b)为m+g培养条件下各组的细胞相对活性图;图4中(c)为hg培养条件下各组的细胞相对活性图。由图4的结果可以显示hg诱导hbzy-1细胞增殖(p<0.05),而ng和m+g对hbzy-1细胞增殖无影响(p>0.05)。药物组合物可以抑制hg诱导的hbzy-1细胞增殖。
由于炎性细胞因子在慢性肾病中起重要作用,通过荧光实时定量pcr(q-rt-pcr)技术检测hbzy-1细胞炎症细胞因子(包括il-6、il-1β和tnf-α)的水平。如图5所示,其中,图5中(a)和(b)为hg培养条件下各组的il-6的mrna相对表达量和il-6相对水平数据图;图5中(c)和(d)为hg培养条件下各组的il-1β的mrna相对表达量和il-1β相对水平数据图;图5中(e)和(f)为hg培养条件下各组的tnf-α的mrna相对表达量和tnf-α相对水平数据图;
结果显示,hg刺激使il-6、il-1β和tnf的mrna-α水平显著升高(p<0.05),而药物组合物使其表达显著下降(p<0.05)。elisa法测定hbzy-1细胞上清中炎性细胞因子的含量,结果显示,hg对细胞的刺激显著诱导了炎症细胞因子的分泌(p<0.05),而药物组合物则抑制了hg诱导的炎性细胞因子产生(p<0.05)
氧化应激是hg诱导的细胞损伤的重要原因,通过检测hbzy-1细胞的活性氧(ros)、丙二醛(mda)水平,以及超氧化物歧化酶(sod)活性发现,见图6,其中,图6中(a)为hg培养条件下各组的ros相对水平数据图;图6中(b)为hg培养条件下各组的mda相对水平数据图;图6中(c)为hg培养条件下各组的sod相对水平数据图。与空白对照组比较,hg升高hbzy-1细胞ros和mda水平,降低了sod的活性(p<0.05)。经药物组合物治疗显著抑制了ros、mda的分泌(p<0.05)。此外,药物组合物也显著减弱了hg对hbzy-1细胞sod活性的抑制作用(p<0.05)。
根据报道,高糖(hg)暴露可促进慢性肾病中细胞外基质蛋白(ecm蛋白)的积累,因此,进一步研究了药物组合物对ecm蛋白表达的影响,包括层粘连蛋白、iv型胶原蛋白、纤维粘连蛋白。参见图7,q-rt-pcr结果显示,参见图hg诱导使细胞ecmmrna的表达水平升高(p<0.05),而药物组合物降低了mrna的表达(p<0.05;图7中(a))。此外,elisa结果显示hg可诱导层粘连蛋白、iv型胶原蛋白、纤维粘连蛋白的表达(p<0.05),药物组合物则抑制了其诱导作用(p<0.05;图7中(b))。
参见图8,为进一步探讨药物组合物抑制hg诱导hbzy-1细胞损伤的相关机制,采用westernblotting法检测tlr4、myd88、nf-κbp65、nf-κbp-p65和nlrp3的表达水平。如图8中(a)所示,hg刺激增加了tlr4和myd88的表达(p<0.05),而药物组合物抑制则抑制了tlr4和myd88的表达(p<0.05)。hg还诱导nf-κbp-p65的表达(p<0.05),而药物组合物抑制抑制hg诱导nf-κbp-p65的表达(p<0.05;图8中(a))。此外,药物组合物抑制减弱了hg诱导的nlrp3表达上调(p<0.05;图8中(b))。结果表明,药物组合物通过调控tlr4/myd88、nf-κb和nlrp3等的表达发挥对hbzy-1细胞的保护作用。
为进一步探讨药物组合物通过调控tlr4、myd88、nf-κbp65和nlrp3蛋白的表达发挥抗hg对hbzy-1细胞的损伤作用,分别用tlr4和nf-κb抑制剂作用于hbzy-1细胞。结果参见图9,tlr4抑制剂tak-242抑制hg诱导的nf-κbp-p65和nlrp3的表达(p<0.05)。此外,nf-κb抑制剂pdtc(1-吡咯烷二硫代羧酸铵盐)阻断hg诱导的nlrp3在hnzy-1细胞中的表达(p<0.05;图9中(b))。结果表明,tlr4、nf-κb和nlrp3炎性小体通路形成了信号转导轴,药物组合物通过该轴减弱了hg对hbzy-1细胞的损伤。
为证实tlr4/nf-κb/nlrp3轴在hg诱导的hbzy-1细胞中的作用,在加入或不加入抑制剂tak-242(tlr4抑制剂)或pdtc的情况下,用30μmd-葡萄糖处理细胞24小时,测定细胞存活率、炎性细胞因子、氧化应激和ecm的表达。图9中(a)显示tak-242和pdtc抑制hg诱导的细胞增殖(p<0.05)。hg显著诱导细胞中il-6、il-1β和tnf-α的产生(p<0.05),tak-242或pdtc可抑制其产生(p<0.05;图9中(b))。hg刺激还使ros和mda含量显著增加(p<0.05),并降低了sod的活性(p<0.05;图9中(c))。然而,tak-242或pdtc作用后,hg对氧化应激的影响是相反的(p<0.05;图9中(c))。采用elisa法分别检测层粘连蛋白、iv型胶原蛋白、纤维连接蛋白的mrna和蛋白水平发现(图9中(d)),hg增加了层粘连蛋白、iv型胶原蛋白、纤维连接蛋白的表达水平(p<0.05),tak-242或pdtc处理则减弱了hg诱导的层粘连蛋白、iv型胶原蛋白、纤维连接蛋白的表达(p<0.05)。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!