靶向肿瘤沃伯格效应的肿瘤诊断和治疗荧光探针的制作方法
本发明属于生物医药
技术领域:
,涉及一种靶向肿瘤沃伯格效应的肿瘤诊断和治疗荧光探针。
背景技术:
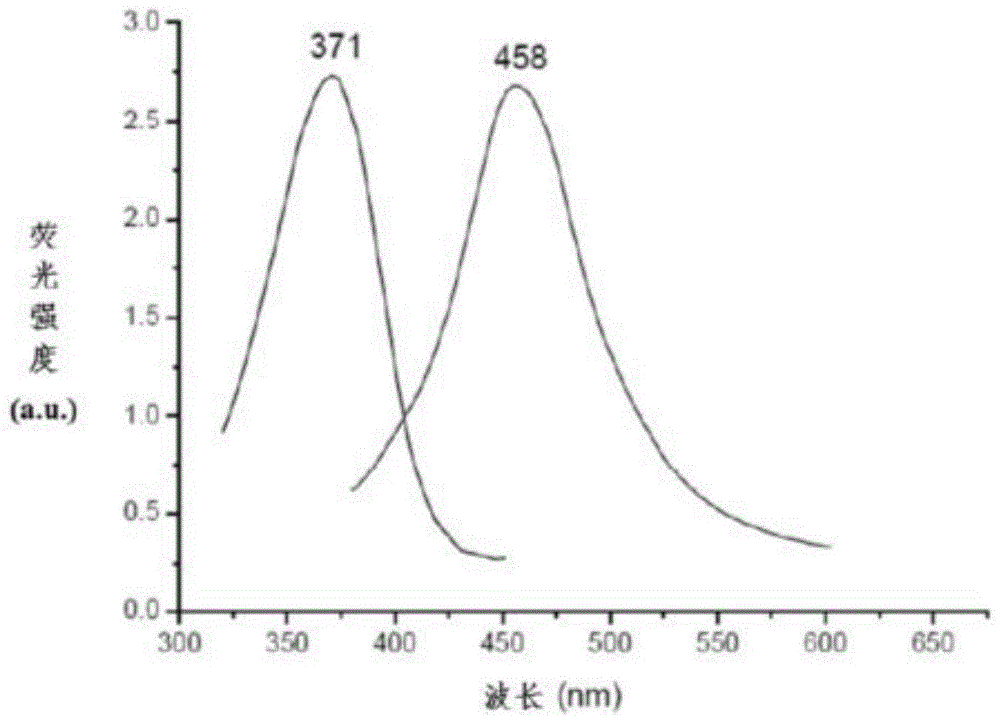
:目前,肿瘤已成为当今世界上严重威胁人类健康的重大疾病,随着抗肿瘤药物研究的发展,关于肿瘤早期诊断、靶向诊疗的研究也越来越引起人们的重视。靶向诊断和治疗肿瘤的方法有很多,其基本原理是利用肿瘤细胞或肿瘤组织特异性存在,或者与正常细胞或正常组织具有显著差异的肿瘤生物标志物,通过选择性识别、抑制这些生物标志物而达到检测或者靶向治疗肿瘤的目的。研究表明,恶性肿瘤之所以能够持续增殖、扩散和转移,其重要的生理机制之一是不断吸收和摄取它所需要的特殊营养。这些营养包括,糖分子、氨基酸、维生素、核苷等。早在1924年,德国生物化学家奥托·沃伯格就发现健康细胞能有效利用有氧代谢,从有限的糖类营养源制备足够的能量,而大多数肿瘤细胞由于处于缺氧环境,则通过大量的糖吸收和糖代谢为自身提供能源。这种现象被称为沃伯格效应。沃伯格因此于1931年获得了生理学或医学诺贝尔奖(参考文献:warburg,o.science,123:309(1956);"thenobelprizeinphysiologyormedicine1931".nobelprize.org.<http://www.nobelprize.org/nobel_prizes/medicine/laureates/1931/>)。基于肿瘤沃伯格效应,由于肿瘤细胞与健康细胞相比特异性高表达糖转运通道蛋白glut1,因此以glut1为肿瘤特异性标志物有望实现对肿瘤的靶向识别。如式(a)所示,作为现有技术,文献报道了化合物1作为glut1抑制剂能够阻止血癌细胞hl-60和u-937的糖吸收和糖积蓄(salasm.,etal.,am.j.physiol.cellphysiol.,305:c90(2013))。另有文献报道了化合物2能够选择性抑制glut1蛋白通道从而能够作为潜在的肿瘤抑制剂药物(chanda,etal.scitranslmed.2011,3(94),94ra70)。另有报道,化合物3作为glut1选择性抑制剂,但没有验证其在抑制肿瘤细胞或动物模型中的作用(siebeneicherh,etal.chemmedchem.2016,11(20):2261-2)。这些通过不同药物筛选方法获得的glut1抑制剂为进一步验证这些先导化合物的临床应用提供了物质材料。香豆素,化学名为1,2-苯并吡喃酮,其存在于天然黑香豆,兰花及野香荚兰中。不含有取代基的香豆素母体结构本身没有荧光,然而在香豆素母体结构中的7、8-位引入羟基、氨基等取代集基团时,该类化合物会出现蓝色荧光。利用香豆素这种荧光发光特征,如果能够通过精心设计,在香豆素母体结构中7、8-位引入适当的取代基,使分子整体能够成为具有荧光发光特征的glut1抑制剂,如此获得的化合物将能够实现既能够抑制肿瘤增殖,又能够通过荧光检测肿瘤的双重目的。早在十八世纪,文献v.pechmann-chemischeberichte,1884,vol.17,p.932和stuenkel-chemischeberichte,1879,vol.12,p.112就已经报道了7、8-为二苯甲酰香豆素化合物,但该化合物针对抗肿瘤效果或者化合物可能的glut1抑制作用未作任何研究和报道。技术实现要素:本发明的目的是克服现有技术的不足,提供一种既能够通过肿瘤沃伯格效应预防或者治疗肿瘤,又能够通过荧光对肿瘤细胞实施定位或检测的靶向肿瘤沃伯格效应的肿瘤诊断和治疗荧光探针。本发明的第二个目的是提供一种诊断和治疗肿瘤的药物组合物。本发明的第三个目的是提供一种检测和诊断肿瘤的试剂。本发明的第四个目的是提供上述一种药物组合物在制备诊断和治疗肿瘤药物中的用途。本发明的第五个目的是提供上述一种试剂在制备肿瘤检测和诊断试剂中的用途。本发明的技术方案概述如下:靶向肿瘤沃伯格效应的肿瘤诊断和治疗荧光探针,其特征是结构如式(i)所示:其中,xr1和xr2相同或不同;xr1表示苯环不同位置的单取代或双取代;xr2表示苯环不同位置的单取代或双取代;x选自o,s或nh;r1为氢原子,直链烷基或支链烷基;r2为氢原子,直链烷基或支链烷基。优选地,xr1和xr2相同;xr1在xr2在苯环取代位置选自(a-1)、(a-2)、(a-3)或(a-4);其中,r1为氢原子或甲基;x为o。一种诊断和治疗肿瘤的药物组合物,包括上述荧光探针、或其药学上可接受的盐、或其溶剂化物,或与药用载体、赋形剂或稀释剂的混合。一种检测和诊断肿瘤的试剂,包括上述荧光探针、或其药学上可接受的盐、或其溶剂化物,或与药用载体、赋形剂或稀释剂的混合。上述药物组合物在制备诊断和治疗肿瘤药物的用途。上述试剂在制备肿瘤检测和诊断试剂中的用途。本发明具有以下的有益效果:本发明靶向肿瘤沃伯格效应的肿瘤诊断和治疗荧光探针能够直接用在细胞系中分析和检测肿瘤细胞glut1蛋白的表达程度,从而完成对肿瘤细胞的筛选。同时通过直接阻断glut1通道抑制肿瘤对糖营养成分的摄取抑制肿瘤细胞增殖。为肿瘤早期筛选和诊断,开发新的抗肿瘤药物等提供了有效的手段和有用的工具。附图说明图1为(i)-(a-1)-1荧光探针的荧光吸收图谱;图2为(i)-(a-1)-2荧光探针的荧光吸收图谱;图3为(i)-(a-2)-1荧光探针的荧光吸收图谱;图4为(i)-(a-2)-2荧光探针的荧光吸收图谱;图5为(i)-(a-3)-1荧光探针的荧光吸收图谱;图6为(i)-(a-3)-2荧光探针的荧光吸收图谱;图7为(i)-(a-4)-2荧光探针的荧光吸收图谱;图8为本发明荧光探针针对直肠癌的抗肿瘤药效;图9为本发明荧光探针针对肺癌的抗肿瘤药效;图10为本发明荧光探针用于检测和诊断肿瘤的效果。具体实施方式下面通过具体实施例对本发明作进一步详细的说明,所述是对本发明的解释而不是限定。靶向肿瘤沃伯格效应的肿瘤诊断和治疗荧光探针,以下简称荧光探针。实施例1荧光探针(i)-(a-1)-1的合成:1、荧光发色团7,8-二羟基香豆素的合成,其合成路线如下:向焦性没食子酸(ii,2g,15.88mmol)和丙炔酸(iii,2.2g,31.76mmol)的混合物中加入两滴浓硫酸。将所得悬浮液在120℃下加热回流并搅拌1h,冷却后加入50ml乙酸乙酯,用饱和的碳酸氢钠水溶液洗涤3次后,用蒸馏水和饱和氯化钠水溶液洗涤,最后用无水硫酸钠干燥。用旋转蒸发仪将溶剂蒸干,得到浅棕色固体,粗品用无水乙醚重结晶纯化,得到浅黄色或灰白色固体(7,8-二羟基香豆素,iv)1.97g,产率70%。反应式为:2、荧光探针(i)-(a-1)-1的合成:(1)2-甲氧基苯甲酰氯的合成:在氮气的保护下向烘箱干燥后的三颈烧瓶中加入2-甲氧基苯甲酸(1.2g,7.9mmol),n,n-二甲基甲酰胺(dmf)(2滴)和干燥的二氯甲烷(dcm)(15ml)。在0℃,逐滴向反应液中加入草酰氯(0.8ml,9.48mmol)。将混合物升温至室温反应2h,用旋转蒸发仪将溶剂蒸干,所得2-甲氧基苯甲酰氯无需进一步纯化立即用于下一步反应。(2)荧光探针(i)-(a-1)的合成:将7,8-二羟基香豆素(500mg,2.81mmol)溶于无水乙腈(20ml)中,加入4-二甲氨基吡啶(dmap)(1.5g,12.36mmol),在0℃,逐滴向反应液中加入上一步反应所得的2-甲氧基苯甲酰氯(1.05g,6.18mmol)。将混合物升温至30℃反应18h,用tlc监测反应终点。反应完成后,用旋转蒸发仪除去溶剂,所得残余物溶解于乙酸乙酯(20ml)中,用饱和氯化铵水溶液(10ml)和蒸馏水(10ml)洗涤,收集有机相,用无水硫酸钠干燥。用旋转蒸发仪将溶剂蒸干,经硅胶柱色谱纯化(石油醚∶乙酸乙酯=3∶1),得到白色固体(i)-(a-1)-10.96g。收率77%1hnmr(600mhz,cdcl3)δ7.40-8.00(m,5h),7.15(1h,d,j=8.4hz,1h),6.90-7.00(m,6h),3.80(s,3h),3.73(s,3h);esi-ms:(m/z)447.11[m+1]+实施例2荧光探针(i)-(a-1)-2的合成:将荧光探针(i)-(a-1)-1(210mg,0.47mmol)溶于干燥的二氯甲烷(10ml)中,在-20℃的条件下,向反应液中缓缓加入1m三溴化硼的二氯甲烷(dcm)溶液(1ml),将混合物升温至室温反应3h,用tlc监测反应终点。反应完成后,在0℃的条件下,加入冰水(10ml)将反应淬灭,用饱和碳酸氢钠(5ml)洗涤,用二氯甲烷(2×10ml)萃取,合并有机相,用无水硫酸钠干燥。用旋转蒸发仪将溶剂蒸干,经硅胶柱色谱(石油醚∶乙酸乙酯=1∶1)和重结晶(石油醚和乙酸乙酯的混合溶剂)纯化,得到白色固体125mg。收率64%1hnmr(600mhz,cdcl3)δ9.50-10.20(m,2h),7.40-8.00(m,5h),7.15(1h,d,j=8.4hz,1h),6.90-7.00(m,6h);esi-ms:(m/z)419.07[m+1]+实施例3荧光探针(i)-(a-2)-1的合成,包括如下步骤:1)3-甲氧基苯甲酸甲酯的合成:在室温条件下,将3-羟基苯甲酸(3g,21.74mmol)溶于干燥的n,n-二甲基甲酰胺(dmf)(20ml)中,加入碳酸钾(9g,65.22mmol)和碘化钾(3ml,47.83mmol),室温反应12h,用tlc监测反应终点。反应完成后,加入乙酸乙酯(20ml),用饱和氯化铵水溶液(10ml)和蒸馏水(10ml)洗涤,水相用乙酸乙酯萃取,合并有机相,用无水硫酸钠干燥。用旋转蒸发仪除去溶剂,经硅胶柱色谱(石油醚∶乙酸乙酯=12∶1)纯化得到白色固体3-甲氧基苯甲酸甲酯3.43g,产率95%。2)3-甲氧基苯甲酸的合成:在室温条件下,将3-甲氧基苯甲酸甲酯(3.43g,20.66mmol)溶于甲醇(5ml):水(10ml)=1:2的混合溶剂中,加入氢氧化钠(1.65g,41.32mmol),室温反应3h,用tlc监测反应终点。反应完成后,用旋转蒸发仪除去溶剂,加入二氯甲烷(dcm)(30ml),用体积浓度为5%的盐酸水溶液(2×5ml)洗涤,水相用二氯甲烷(2×5ml)萃取,合并有机相,用无水硫酸钠干燥。用旋转蒸发仪将溶剂蒸干,得到白色固体3-甲氧基苯甲酸2.7g,产率87%。3)3-甲氧基苯甲酰氯的合成:在氮气的保护下向烘箱干燥的三颈烧瓶中加入3-甲氧基苯甲酸(1.2g,7.9mmol),n,n-二甲基甲酰胺(dmf)(2滴)和干燥的二氯甲烷(15ml)。在0℃的条件下,逐滴向反应液中加入草酰氯(0.8ml,9.48mmol)。将混合物升温至室温反应2h,用旋转蒸发仪将溶剂蒸干,所得3-甲氧基苯甲酰氯无需进一步纯化立即用于下一步反应。4)荧光探针(i)-(a-2)-1的合成:将7,8-二羟基香豆素(iv,500mg,2.81mmol)溶于无水乙腈(20ml)中,加入4-二甲氨基吡啶(dmap)(1.5g,12.36mmol),在0℃的条件下,逐滴向反应液中加入上一步反应所得的3-甲氧基苯甲酰氯(1.05g,6.18mmol)。将混合物升温至30℃反应18h,用tlc监测反应终点。反应完成后,用旋转蒸发仪除去溶剂,所得残余物溶解于乙酸乙酯(20ml)中,用饱和氯化铵水溶液(10ml)和蒸馏水(10ml)洗涤,收集有机相,用无水硫酸钠干燥。用旋转蒸发仪将溶剂蒸干,经硅胶柱色谱纯化(石油醚∶乙酸乙酯=3∶1),得到白色固体0.94g。收率75%1hnmr(600mhz,cdcl3)δ7.74(d,j=8.6hz,2h),7.66(d,j=7.3hz,1h),7.61(s,1h),7.53(s,1h),7.47(d,j=8.4hz,1h),7.32(ddd,j=19.1,15.1,8.2hz,3h),7.11(dd,j=12.7,8.8hz,2h),6.43(d,j=9.5hz,1h),3.79(s,3h),3.72(s,3h);13cnmr(150mhz,cdcl3)δ163.64,163.25,159.68,159.11,147.52,145.96,142.91,130.65,129.67,129.44,129.18,125.07,123.04,122.76,120.92,119.11,117.82,116.50,114.62,114.30,55.40.esi-ms:(m/z)447.09[m+1]+实施例4荧光探针(i)-(a-2)-2的合成:将荧光探针(i)-(a-2)-1(200mg,0.45mmol)溶于干燥的二氯甲烷(10ml)中,在-20℃的条件下,向反应液中缓缓加入1m三溴化硼的二氯甲烷(dcm)溶液(1ml),将混合物升温至室温反应3h,用tlc监测反应终点。反应完成后,在0℃的条件下,加入冰水(10ml)将反应淬灭,用饱和碳酸氢钠(5ml)洗涤,用二氯甲烷(2×10ml)萃取,合并有机相,用无水硫酸钠干燥。用旋转蒸发仪将溶剂蒸干,经硅胶柱色谱(石油醚∶乙酸乙酯=1∶1)和重结晶(石油醚和乙酸乙酯的混合溶剂)纯化,得到白色固体120mg。收率64%1hnmr(600mhz,dmso)δ10.03(s,1h),9.97(s,1h),8.20(d,j=9.7hz,1h),7.83(d,j=8.6hz,1h),7.56(d,j=8.6hz,1h),7.51(d,j=7.6hz,1h),7.47(d,j=7.3hz,2h),7.42(s,1h),7.37(t,j=7.9hz,1h),7.33(t,j=7.9hz,1h),7.13(dd,j=8.1,1.7hz,1h),7.10(dd,j=8.1,1.7hz,1h),6.60(d,j=9.7hz,1h).esi-ms:(m/z)419.06[m+1]+实施例5荧光探针(i)-(a-3)-1的合成,包括如下步骤:1)4-甲氧基苯甲酸甲酯的合成:在室温条件下,将4-羟基苯甲酸(3g,21.74mmol)溶于干燥的n,n-二甲基甲酰胺(dmf)(20ml)中,加入碳酸钾(9g,65.22mmol)和碘化钾(3ml,47.83mmol),室温反应12h,用tlc监测反应终点。反应完成后,加入乙酸乙酯(20ml),用饱和氯化铵水溶液(10ml)和蒸馏水(10ml)洗涤,水相用乙酸乙酯萃取,合并有机相,用无水硫酸钠干燥。用旋转蒸发仪除去溶剂,经硅胶柱色谱(石油醚∶乙酸乙酯=12∶1)纯化得到白色固体4-甲氧基苯甲酸甲酯3.5g,产率97%。2)4-甲氧基苯甲酸的合成:在室温条件下,将4-甲氧基苯甲酸甲酯(3.5g,21.08mmol)溶于甲醇(5ml):水(10ml)=1:2的混合溶剂中,加入氢氧化钠(1.69g,42.16mmol),室温反应3h,用tlc监测反应终点。反应完成后,用旋转蒸发仪除去溶剂,加入二氯甲烷(30ml),用体积浓度为5%的盐酸水溶液(2×5ml)洗涤,水相用二氯甲烷(2×5ml)萃取,合并有机相,用无水硫酸钠干燥。用旋转蒸发仪将溶剂蒸干,得到白色固体4-甲氧基苯甲酸2.7g,产率84%。3)4-甲氧基苯甲酰氯的合成:在氮气的保护下向烘箱干燥的三颈烧瓶中加入4-甲氧基苯甲酸(1.2g,7.9mmol),n,n-二甲基甲酰胺(2滴)和干燥的二氯甲烷(dcm)(15ml)。在0℃的条件下,逐滴向反应液中加入草酰氯(0.8ml,9.48mmol)。将混合物升温至室温反应2h,用旋转蒸发仪将溶剂蒸干,所得4-甲氧基苯甲酰氯无需进一步纯化立即用于下一步反应。4)荧光探针(i)-(a-3)-1的合成:将7,8-二羟基香豆素(500mg,2.81mmol)溶于无水乙腈(20ml)中,加入4-二甲氨基吡啶(dmap)(1.5g,12.36mmol),在0℃的条件下,逐滴向反应液中加入上一步反应所得的4-甲氧基苯甲酰氯(1.05g,6.18mmol)。将混合物升温至30℃反应18h,用tlc监测反应终点。反应完成后,用旋转蒸发仪除去溶剂,所得残余物溶解于乙酸乙酯(20ml)中,用饱和氯化铵水溶液(10ml)和蒸馏水(10ml)洗涤,收集有机相,用无水硫酸钠干燥。用旋转蒸发仪将溶剂蒸干,经硅胶柱色谱纯化(石油醚∶乙酸乙酯=3∶1),得到白色固体0.92g。收率74%1hnmr(600mhz,cdcl3)δ7.99(d,j=8.6hz,2h),7.92(d,j=8.6hz,2h),7.65(d,j=9.6hz,1h),7.35(d,j=8.5hz,1h),7.23(d,j=8.5hz,1h),6.78(dd,j=22.7,8.6hz,4h),6.31(d,j=9.6hz,1h),3.76(s,3h),3.74(s,3h).esi-ms:(m/z)447.09[m+1]+实施例6荧光探针(i)-(a-3)-2的合成,包括如下步骤:1)4-叔丁基二甲基硅氧基苯甲酸的合成:将4-羟基苯甲酸(3g,21mmol),叔丁基二甲基氯硅烷(tbscl)(7.2g,48mmol)和咪唑(3.3g,48mmol)溶于无水n,n-二甲基甲酰胺(dmf)(30ml)中,在室温下搅拌18h,用tlc监测反应终点。反应完成后,将丙酮(150ml)加入到反应混合物中,过滤,收集滤液,用旋转蒸发仪将溶剂蒸干,所得残余物溶于乙酸乙酯(50ml)中,用水(3×40ml)洗涤,无水硫酸钠干燥。减压除去溶剂,直接得到4-叔丁基二甲基硅氧基苯甲酸叔丁基二甲基硅烷基酯,为无色液体。将所得粗品溶于冰醋酸(50ml),四氢呋喃(15ml)和水(15ml)的混合溶剂中,在室温下搅拌5h。加入乙酸乙酯(50ml)和水(50ml),用饱和碳酸氢钠水溶液洗涤,收集有机相,用无水硫酸钠干燥。用旋转蒸发仪将溶剂蒸干,所得残余物在高真空下干燥,得到白色固体4-(叔丁基二甲基硅氧基)苯甲酸3.6g,产率66%。2)4-叔丁基二甲基硅氧基苯甲酰氯的合成:取烘箱中干燥的50ml三颈烧瓶,在氮气的保护下加入4-叔丁基二甲基硅氧基苯甲酸(1.6g,6.35mmol),n,n-二甲基甲酰胺(dmf)(2滴)和无水二氯甲烷(dcm)(20ml)。在0℃的条件下,逐滴向反应液中加入草酰氯(0.65ml,7.62mmol),在室温下搅拌3h,用旋转蒸发仪将溶剂蒸干,所得4-(叔丁基二甲基)硅氧基苯甲酰氯无需进一步纯化立即用于下一步反应。3)化合物v的合成:将7,8-二羟基香豆素(500mg,2.81mmol)溶于无水二氯甲烷(20ml)中,加入4-二甲氨基吡啶(dmap)(1.5g,12.36mmol),在0℃的条件下,逐滴向反应液中加入上一步反应所得的4-(叔丁基二甲基)硅氧基苯甲酰氯(1.67g,6.18mmol)。将混合物升温至30℃反应18h,用tlc监测反应终点。反应完成后,加入二氯甲烷(dcm)(10ml),用饱和氯化铵水溶液(10ml)和蒸馏水(2×10ml)洗涤,收集有机相,用无水硫酸钠干燥,经硅胶柱色谱(石油醚∶乙酸乙酯=10∶1→5:1)纯化,得到白色固体1.4g(化合物v)。收率78%1hnmr(600mhz,cdcl3)δ8.03(d,j=8.7hz,2h),7.95(d,j=8.7hz,2h),7.75–7.72(m,1h),7.44(d,j=8.6hz,1h),7.33–7.31(m,1h),6.83(d,j=8.7hz,2h),6.79(d,j=8.7hz,2h),6.41(d,j=9.6hz,1h),0.99–0.96(m,18h),0.24–0.20(m,12h).4)化合物(i)-(a-3)-2的合成:将化合物v(100mg,0.15mmol)溶于四氢呋喃(10ml)中,缓慢加入适量1m四正丁基氟化铵(tbaf)的四氢呋喃(thf)溶液,所得混悬液在室温下搅拌1h,用tlc监测反应终点。反应完成后,加入二氯甲烷(10ml)和饱和氯化钠溶液(10ml),有机相用蒸馏水(10ml)洗涤,收集有机相,用无水硫酸钠干燥,用旋转蒸发仪将溶剂蒸干,经硅胶柱色谱(石油醚∶乙酸乙酯=1∶1)和重结晶(石油醚和乙酸乙酯的混合溶剂)纯化,得到白色固体(化合物(i)-(a-3)-2)26mg。收率40%1hnmr(600mhz,dmso)δ10.59(s,2h),8.17(d,j=9.7hz,1h),7.90(d,j=8.7hz,2h),7.85(d,j=8.7hz,2h),7.77(d,j=8.6hz,1h),7.49(d,j=8.6hz,1h),6.87(d,j=8.7hz,2h),6.82(d,j=8.7hz,2h),6.56(d,j=9.7hz,1h);esi-ms:(m/z)419.06[m+1]+实施例7荧光探针(i)-(a-4)-1的合成,包括如下步骤:用3,5-二甲氧基苯甲酸替代实施例1步骤2(1)中的2-甲氧基苯甲酸,其它同实施例1,制备获得荧光探针(i)-(a-4)-1。得到白色固体0.97g。收率70%。1hnmr(600mhz,dmso)δ9.80(d,j=24.4hz,4h),8.18(d,j=9.5hz,1h),7.81(d,j=8.4hz,1h),7.50(d,j=8.4hz,1h),6.90(d,j=24.0hz,4h),6.50-6.60(m,3h),3.76(s,3h),3.74(s,3h).esi-ms:(m/z)507.12[m+1]+实施例8荧光探针(i)-(a-4)-2的合成:1)3,5-二(叔丁基二甲基硅氧基)苯甲酸(vi)的合成:取100ml烘箱干燥的双颈圆底烧瓶,加入3,5-二羟基苯甲酸(3g,19.5mmol)和叔丁基二甲基氯硅烷(tbscl)(9.5g,208mmol)与30ml无水甲苯,剧烈搅拌,逐滴加入三乙胺(tea)(9ml,64.35mmol),所得混合物在氮气保护下回流18h。用tlc监测反应终点。反应完成后,将混合物置于250ml分液漏斗中,用水(100ml)和饱和氯化钠水溶液(10ml)洗涤,收集甲苯层并用水(100ml)洗涤两次以上,收集有机层,用无水硫酸钠干燥,旋转蒸发仪除去溶剂,所得粗产品在减压真空干燥箱中干燥过夜,得到浅褐色固体8.5g,产率88%,使用前需储存在干燥器中。取上一步所得的浅褐色固体(6.2g,12.5mmol)溶于冰醋酸(45ml),四氢呋喃(15ml)和水(15ml)的混合溶剂中,在室温下搅拌12h。加入乙酸乙酯(50ml)和水(50ml),用饱和碳酸氢钠水溶液洗涤,收集有机相,用无水硫酸钠干燥。用旋转蒸发仪将溶剂蒸干,所得残余物在高真空下干燥,得到白色固体4.3g,产率90%。2)3,5-二(叔丁基二甲基硅氧基)苯甲酰氯(vii)的合成:取烘箱中干燥的50ml三颈烧瓶,在氮气的保护下加入3,5-二(叔丁基二甲基硅烷基)氧基苯甲酸(2.6g,6.8mmol),n,n-二甲基甲酰胺(dmf)(2滴)和无水二氯甲烷(dcm)(20ml)。在0℃的条件下,逐滴向反应液中加入草酰氯(0.7ml,8.16mmol),在室温下搅拌5h,用旋转蒸发仪将溶剂蒸干,所得3,5-二(叔丁基二甲基硅烷基)氧基苯甲酰氯(vii)无需进一步纯化立即用于下一步反应。3)化合物(viii)的合成:将7,8-二羟基香豆素iv(500mg,2.81mmol)溶于无水二氯甲烷(dcm)(30ml)中,加入4-二甲氨基吡啶(dmap)(1.5g,12.36mmol),在0℃的条件下,逐滴向反应液中加入上一步反应所得的3,5-二(叔丁基二甲基硅氧基)苯甲酰氯(2,47g,6.18mmol)。将混合物升温至30℃反应18h,用tlc监测反应终点。反应完成后,加入二氯甲烷(dcm)(10ml),用饱和氯化铵水溶液(10ml)和蒸馏水(2×10ml)洗涤,收集有机相,用无水硫酸钠干燥,用旋转蒸发仪将溶剂蒸干,经硅胶柱色谱(石油醚∶乙酸乙酯=5∶1)纯化,将所得油状液体置于冰箱中冷藏24h,重结晶析出类白色固体(化合物(19))1.89g。收率73%1hnmr(600mhz,cdcl3)δ7.74(d,j=9.6hz,1h),7.45(d,j=8.6hz,1h),7.28(d,j=8.5hz,1h),7.21(d,j=2.2hz,2h),7.15(t,j=4.4hz,2h),6.53(dt,j=4.3,2.2hz,2h),6.42(d,j=9.6hz,1h),0.95(d,j=9.1hz,35h),0.15(d,j=18.3hz,24h).4)荧光探针(i)-(a-4)-2)的合成:将化合物(19)(110mg,0.12mmol)溶于无水二氯甲烷(dcm)(10ml)中,缓慢加入四氟硼酸锂(约10mg)和浓盐酸(0.5ml),所得混悬液在室温下搅拌8h,用tlc监测反应终点。反应完成后,加入乙酸乙酯(20ml)和饱和氯化钠溶液(10ml),用碳酸氢钠水溶液(10ml)和蒸馏水(10ml)洗涤,收集有机相,用无水硫酸钠干燥,用旋转蒸发仪将溶剂蒸干,经硅胶柱色谱(石油醚∶乙酸乙酯=1∶1)和重结晶(石油醚和乙酸乙酯的混合溶剂)纯化,得到白色固体(i)-(a-4)-2)20mg。收率36%1hnmr(600mhz,dmso)δ9.80(d,j=24.4hz,4h),8.18(d,j=9.5hz,1h),7.80(d,j=8.4hz,1h),7.50(d,j=8.4hz,1h),6.95(d,j=24.0hz,4h),6.50-6.62(m,3h).esi-ms:(m/z)451.05[m+1]+试验例1:本发明荧光探针荧光光谱的测定实验1)实验仪器:thermoscientificvarioskanlux。2)实验化合物:以上各实施例制备的荧光探针(i)-(a-1)-1,(i)-(a-1)-2,(i)-(a-2)-1,(i)-(a-2)-2,(i)-(a-3)-1,(i)-(a-3)-2,(i)-(a-4)-1,(i)-(a-4)-2。测试溶剂:dmso:pbs(ph=7.2)=1:9(v:v)3)实验步骤(1)称取各化合物。(2)用dmso溶解化合物至10mm,涡旋1min,使化合物充分溶解。(3)用pbs-dmso(1:1,体积比)稀释化合物至500um,涡旋溶解。取不同化合物与测试溶剂各100ul,加入到黑色底透96孔培养板中,用多功能酶标仪检测吸收光谱、激发光谱和发射光谱。表-1:实施例1-8荧光探针吸收光谱(nm)300-800激发光谱(nm)320-520发射光谱(nm)380-6404)数据处理:用originpro8.5处理,导出吸收谱、发射谱、和吸收-发射合谱。5)结果:本发明荧光探针的激发和发射光谱如附图(图1至图7)所示。本发明所提供的荧光探针中,(i)-(a-1)-1和2的荧光探针的激发波长范围为:350nm至380nm,发射波长范围为:430nm和470nm;(i)-(a-2)-1和2的荧光探针的激发波长范围为:350nm至380nm,发射波长范围为:380nm和440nm;(i)-(a-3)-1和2的荧光探针的激发波长范围为:350nm至380nm,发射波长范围为:380nm和470nm;(i)-(a-4)-1和2的荧光探针的激发波长范围为:350nm至380nm,发射波长范围为:430nm和470nm;试验例2:荧光探针对glut1的抑制作用由于人和哺乳动物的红细胞主要表达glut1蛋白进行糖吸收,本实验采用2-脱氧葡萄糖细胞吸收测试试剂盒(cosmobioco.ltd.,日本)针对本发明荧光探针分子的glut1抑制作用进行检测。具体实验方法和结果如下:人红细胞采用常规方法采集:枸橼酸抗凝采集的肘静脉全血10ml,于1500r/min离心5分钟,弃去血浆和红细胞表面的白细胞,用10ml磷酸盐缓冲液(ph7.4)洗涤细胞3次(1500r/min,4分钟),红细胞于磷酸盐缓冲液中保存于4度冰箱中待用。将上述红细胞缓冲液悬液计数后以5x106每孔加于96孔板中,设置:①空白对照组每孔加入溶于pbs(ph7.2)中的2-脱氧葡萄糖(购于sigma)200微升(终浓度为1mm);②阳性对照组添加含有终浓度为1mm的2-脱氧葡萄糖和10μm细胞松弛素b(购于sigma)(总体积200微升);③测试组:分别添加含有终浓度1mm的2-脱氧葡萄糖和15μm本发明荧光探针化合物:(i)-(a-1)-1,(i)-(a-1)-2,(i)-(a-2)-1,(i)-(a-2)-2,(i)-(a-3)-1,(i)-(a-3)-2,(i)-(a-4)-1和(i)-(a-4)-2(总体积200微升)。上述空白对照组、阳性对照组、测试组各自分别设3孔,实验在37℃培养1小时。然后用冷却至零度的pbs(ph=7.2)洗涤细胞3次(1500r/min,4分钟),然后用5毫升含有10mm的tris-hcl缓冲液(ph8.0,购于solarbio)和0.5%的tritonx-100(购于sigma)的裂解缓冲液于80℃进行细胞裂解15分钟。裂解后细胞置于4℃经1500r/min离心20分钟。针对上清液进行2-脱氧葡萄糖吸收测试。被红细胞经glut1吸收的2-脱氧葡萄糖的细胞内浓度以2-脱氧葡萄糖-6-磷酸的形式采用2-脱氧葡萄糖细胞吸收试剂盒(2-deoxyglucose(2dg)uptakemeasurementkit,购于cosmobioco.ltd.,日本)进行测试。测试结果分别以空白对照组糖吸收为100%折算后如下表:表-2:表-2中结果显示,阳性对照化合物细胞松弛素b是已知的glut1抑制剂(procnatlacadsci.2016,113(17):4711-4716),与其相比,本发明荧光探针化合物针对红细胞的2-脱氧葡萄糖吸收显示出了同样的抑制效果。试验例3:荧光探针在肿瘤检测中的应用1,肿瘤检测试剂的制备1)称取1mg荧光探针,根据其分子量使用分析纯二甲基亚砜(dmso)将荧光探针配制成1mm溶液,然后用pbs(ph=7.2)稀释成100μm的检测试剂。2)将配制成的荧光探针试剂溶液,加入培养好的癌细胞或者健康细胞中,保持荧光探针的最终浓度为100μm,在细胞孵化条件下对细胞进行荧光染色。3)所配制的荧光探针试剂,一般在使用前配制,或者配置后置于-20℃冷冻避光保存。2,荧光探针在检测肿瘤中的应用肿瘤细胞培养:从美国模式菌种收集中心(atcc)购得人肺癌细胞a549(2018年7月购入,www.atcc.org)、人正常支气管上皮细胞beas-2b-cm(2018年7月atcc购入,www.atcc.org)。分别按照相应的细胞培养条件进行培养并使用。具体培养条件如下:a549:rpmi-1640培养基,10%胎牛血清,95%空气,5%二氧化碳,37℃;beas-2b-cm细胞:mem培养基,10%胎牛血清,10ug/ml胰岛素95%空气,5%二氧化碳,37℃。肿瘤检测及药物筛选:1,在细胞培养箱中,在不同的96孔板中分别铺设1x104肺癌细胞a549、人正常支气管上皮细胞beas-2b-cm。待细胞过夜贴壁后,分别加入100μm终浓度的荧光探针溶液于37度培养60分钟。每个浓度设复孔5个,同时设空白对照组不添加细胞只添加荧光探针溶液。2,冰冷pbs洗3遍,转移到酶标板中测量荧光强度。平均荧光强度=(每个药物浓度下测得的每个复孔荧光强度取平均值)-(空白对照组各个复孔测得的荧光强度平均值)。取小数点后2位。荧光探针在高表达glut1的人肺癌细胞a549中的荧光强度,以及荧光探针在人正常支气管上皮细胞beas-2b-cm中的荧光强度测试结果如下:表-3:表-3中结果显示,本发明荧光探针在高表达glut1蛋白的肺癌细胞中,显示出的荧光染色显著高于健康细胞。这是由于荧光探针化合物针对具有沃伯格效应的肿瘤细胞具有选择性识别功能。试验例4:荧光探针在治疗肿瘤中的应用细胞毒性测试:细胞毒性实验采用mts测试方法。收集对数期肿瘤细胞,调整细胞悬液浓度,每孔加入100μl,铺板使待测细胞调密度至1000-10000个/孔,(边缘孔用无菌pbs填充)。在5%co2,37℃孵育,至细胞单层铺满孔底(96孔平底板),加入固定浓度的荧光探针药物(50μm),每孔100μl,设5个复孔。在5%co2,37℃条件下孵育96小时,倒置显微镜下观察。向2mlmts(2mg/ml,dpbs配制)溶液中加入100μlpms(1mg/ml,dpbs配制),混匀,制成mts工作液。上述细胞培养板离心后弃去培养液,小心用pbs冲2-3遍后,在检测吸光度前,向96孔板中每孔加入100μl培养基,再加入20μlmts工作液,在37℃,5%co2条件下孵育2h后,在490nm处检测od值(光密度值)。对照组:在上述同样条件下不添加被测荧光探针药物,最后取得肿瘤细胞在490nm处检测od值,作为细胞100%生存的对照。上述每个荧光探针药物的实验重复5组,取平均od值,与对照组比较计算细胞存活率。(2)实验结果:表-4如表-4和图8、9所示,本发明荧光探针对直肠癌以及肺癌细胞都具有不同强度的抑制作用。试验例5:荧光探针在体内肿瘤检测中的应用1)细胞培养:a549细胞用含有10%的胎牛血清的rpmi1640培养基置于37℃、5%的二氧化碳培养箱培养,细胞贴壁率为85%左右时用胰酶消化、传代、换液,不断扩增细胞数量。2)建立肺癌a549细胞裸鼠(balb/cnudemice,购自北京维通利华实验动物技术有限公司)皮下注射成瘤模型:于spf级裸鼠饲养实验室,用无菌注射器抽取0.2ml在超净台中浓缩的细胞悬液(浓度为2×107/ml),接种到局部棉签消毒的裸鼠后背部皮下,观察注射处无渗液后放回笼中饲养,10-14天后成瘤(成瘤率90%以上),待肿瘤长至约1000mm3,荷瘤裸鼠分成四组,每组三只:pbs注射对照组,(i)-(a-1)-2荧光探针药物注射组、荧光探针药物注射组(i)-(a-3)-2、探针药物注射组(i)-(a-4)-2,注射测试探针药物溶液并进行成像实验。3)动物成像操作:荷瘤小鼠尾静脉注射100ul(0.06mg)(i)-(a-1)-2、(i)-(a-3)-2、(i)-(a-4)-2。注射后即成像,动物成像采用美国xenogenivisspectrum活体成像系统。分别针对上述荧光探针尾部静脉注射后的动物于6h,12h,24h进行成像观察荧光探针在动物体内的蓄积。结果见图10所示。以上内容是结合具体的实施方式对本发明所作的进一步详细说明,不能认定本发明的具体实施只局限于这些说明,对于本发明所属
技术领域:
的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干简单推演或替换,都应当视为属于本发明的保护范围。实验证明,(i)-(a-1)-1、(i)-(a-1)-2、(i)-(a-2)-1、(i)-(a-2)-2、(i)-(a-3)-1、(i)-(a-3)-2、(i)-(a-4)-1、(i)-(a-4)-2,上述所列举本发明荧光探针分子,能够针对肿瘤细胞由于沃伯格效应高表达glut1糖营养吸收蛋白的特点,对肿瘤细胞形成选择性荧光染色,从而可用于区别和检测肿瘤细胞。同时,荧光探针化合物通过有效抑制glut1通道,对肿瘤细胞的增值形成有效的抑制作用。另外,对于体内形成的肿瘤组织,本发明荧光探针能够对肿瘤形成选择性荧光标记,实现对体内肿瘤的检测和诊断。因此,本发明提供的所述荧光探针可用于检测或治疗肿瘤的制剂和抗肿瘤药物。诊断和治疗肿瘤的药物组合物,包括上述荧光探针(分别为(i)-(a-1)-1,(i)-(a-1)-2,(i)-(a-2)-1,(i)-(a-2)-2,(i)-(a-3)-1,(i)-(a-3)-2,(i)-(a-4)-1或(i)-(a-4)-2)为唯一活性成分,其余是药学可接受的辅料,如赋形剂或稀释剂的混合。诊断和治疗肿瘤的药物组合物,包括上述荧光探针(分别为(i)-(a-1)-1,(i)-(a-1)-2,(i)-(a-2)-1,(i)-(a-2)-2,(i)-(a-3)-1,(i)-(a-3)-2,(i)-(a-4)-1或(i)-(a-4)-2)的药学上可接受的盐为唯一活性成分。诊断和治疗肿瘤的药物组合物,包括上述荧光探针(分别为(i)-(a-1)-1,(i)-(a-1)-2,(i)-(a-2)-1,(i)-(a-2)-2,(i)-(a-3)-1,(i)-(a-3)-2,(i)-(a-4)-1或(i)-(a-4)-2)溶剂化物。诊断和治疗肿瘤的药物组合物,包括上述荧光探针(分别为(i)-(a-1)-1,(i)-(a-1)-2,(i)-(a-2)-1,(i)-(a-2)-2,(i)-(a-3)-1,(i)-(a-3)-2,(i)-(a-4)-1或(i)-(a-4)-2),其余为药物载体。一种检测和诊断肿瘤的试剂,包括上述荧光探针(分别为(i)-(a-1)-1,(i)-(a-1)-2,(i)-(a-2)-1,(i)-(a-2)-2,(i)-(a-3)-1,(i)-(a-3)-2,(i)-(a-4)-1或(i)-(a-4)-2)的药学上可接受的盐为唯一活性成分。诊断和治疗肿瘤的试剂,包括上述荧光探针(分别为(i)-(a-1)-1,(i)-(a-1)-2,(i)-(a-2)-1,(i)-(a-2)-2,(i)-(a-3)-1,(i)-(a-3)-2,(i)-(a-4)-1或(i)-(a-4)-2)溶剂化物。诊断和治疗肿瘤的试剂,包括上述荧光探针(分别为(i)-(a-1)-1,(i)-(a-1)-2,(i)-(a-2)-1,(i)-(a-2)-2,(i)-(a-3)-1,(i)-(a-3)-2,(i)-(a-4)-1或(i)-(a-4)-2),其余为药物载体。上述药物组合物在制备诊断和治疗肿瘤药物的用途。上述试剂在制备肿瘤检测和诊断试剂中的用途。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 氨苯砜在制备保护脑微血管的药物中的应用的制造方法与工艺
- 基于人间充质干细胞分泌的活性因子提取物的身体霜及其制备方法与流程
- 一种载VEGF抗体的眼用温敏水凝胶植入剂及其制备方法与流程
- 一种依达拉奉的制备方法与流程
- 一种新型的CCR2拮抗剂及其用途的制造方法与工艺
- 高密度脂蛋白模拟肽Reverse-D-4F在治疗LPS诱导呼吸窘迫综合症药物中的应用的制造方法与工艺
- 中药组合物联合抗生素在制备抑制炎症因子药物方面的应用的制造方法与工艺
- 芳酰肼类化合物在治疗急性心肌缺血性冠心病中的应用的制造方法与工艺
- 存在于人体外周静脉血中的脑源性微粒及其分离提纯鉴定方法和应用与制造工艺
- 使受损细胞具有复活效果的复活素的培养方法与制造工艺