一种丹磺酰衍生物荧光探针及其合成方法和应用与流程
本发明属于有机合成及生物硫醇检测技术领域,具体涉及一种丹磺酰衍生物荧光探针及其合成方法和应用。
背景技术:
硫化氢(h2s)是最简单的生物硫醇,是继一氧化碳(co)和一氧化氮(no)之后的又一种内源性气态信号分子。它广泛分布于肝脏、脾脏乃至大脑等各个器官,参与如血管舒张,细胞凋亡和神经调节等一系列生理过程,在维持正常的生理活动中起着不可替代的作用。研究表明其异常水平可引发阿尔茨海默症,唐氏综合症和糖尿病等。因此,开发一种简单可靠的、高选择性、高灵敏度的方法来检测生物样品中的硫化氢含量具有非常重要的意义。
目前,定量分析硫化氢的方法有色谱法、电化学法、比色法和荧光法等。在众多分析方法中,由于荧光法具有选择性好、灵敏度高、操作简单、可实时在线检测等特点而备受关注。尽管已有不少工作对硫化氢的选择性检测进行了报道,但现有的检测硫化氢的探针分子对分子的合成依赖性很强,而且大多探针分子疏水性较强,限制了其在水溶液中的应用。同时,基于单通道的turn-on(荧光增强)和turn-off(荧光减弱)型荧光传感器存在易受环境背景干扰的不足,急需发展具有比例型(ratiometric)响应信号的双通道荧光传感器来实现对硫化氢的传感。因此,构建可用于生物及复杂环境中h2s检测的比例型荧光传感器仍具有挑战。
技术实现要素:
本发明为了解决现有h2s的检测方法存在的操作复杂、选择性低或灵敏度低等技术问题,提供了一种丹磺酰衍生物荧光探针及其合成方法和应用,该合成方法操作简单、对设备要求低、适合放大生产。同时,将丹磺酰衍生物和市售的吡罗红y作为荧光探针,利用表面活性剂十六烷基三甲基溴化铵(ctab)增溶二者,构建了一种基于超分子共组装策略的比例型荧光传感体系。该荧光共组装体传感平台能够高选择性、高灵敏检测h2s,且操作简单、方便、结果清晰易辩。
为了达到上述目的,本发明采用了下列技术方案:
一种丹磺酰衍生物荧光探针,所述荧光探针的结构式如下:
式中,n=1、2或3。具有不同链长的丹磺酰衍生物在于表面活性剂共组装时可能呈现出不同的性能。
一种丹磺酰衍生物荧光探针的合成方法,包括以下步骤:
在惰性气氛及室温条件下,将丹磺酰氯的三氯甲烷溶液逐滴加入含溴取代醇和三乙胺的三氯甲烷溶液中,滴加完毕后,室温搅拌反应,待反应结束后将反应液洗涤、干燥,蒸除溶剂后再将反应物经过柱层析分离纯化,得到丹磺酰衍生物荧光探针。
进一步,所述惰性气氛为氮气、氩气或氖气气氛,,流速为0.6~0.8ml/s。当流速在此范围内既避免了气体的浪费又可以保证反应在惰性气氛下进行。
进一步,所述丹磺酰氯、溴取代醇、三乙胺的摩尔比为1:1~1.5:1~1.5。理论上,反应的摩尔比应为1:1:1,考虑到原料丹磺酰氯价格较昂贵,因此为了使丹磺酰氯尽可能反应完全,同时避免原料的浪费,反应物溴取代醇和缚酸剂三乙胺应稍微过量。
进一步,所述溴取代醇为4-溴-1-丁醇、6-溴-1-己醇或8-溴-1-辛醇中的一种。这些溴取代醇具有不同的链长,可以合成含不同链长的丹磺酰衍生物荧光探针,进而研究链长对其传感性能的影响。
进一步,所述室温搅拌反应的时间为3~5h。当反应时间从0h增加到3h或5h,目标产物的产率在逐渐增加;而当反应时间超过这个范围,目标产物丹磺酰衍生物的产率未见进一步提高。因此本发明中最佳的反应时间范围为3~5h。
进一步,所述洗涤为用饱和食盐水洗6~7次;所述干燥为用无水硫酸钠干燥至少4h;所述柱层析分离纯化的洗脱剂为二氯甲烷:石油醚按体积比1~2:1配成的混合溶剂。用饱和食盐水洗涤6~7次的目的是除去反应过程中生成的三乙胺盐酸盐和剩余的三乙胺,通过监测水层的ph值可以发现是否洗涤干净。实验表明,当水层呈中性时,需用饱和食盐水洗涤6~7次。用饱和食盐水洗涤的有机层可能含有少量的水,研究发现用无水硫酸钠干燥至少4h可以去除其中的水分。通过薄层色谱(tlc)实验发现,当洗脱剂二氯甲烷与石油醚体积比1~2:1,目标化合物与杂质分离效果最佳。
一种丹磺酰衍生物荧光探针的应用,以所述荧光探针与吡罗红y作为双荧光探针,利用表面活性剂ctab的增溶作用,构建超分子比例型荧光传感平台并对h2s进行选择性检测。吡罗红y可以与h2s发生迈克尔加成反应,使得其荧光发生猝灭。表面活性剂ctab增溶的丹磺酰衍生物荧光探针不仅可以促进上述反应的进行,而且可以提供另一种荧光响应信号,从而实现对h2s的比例型传感。
与现有技术相比本发明具有以下优点:
本发明公开了一种丹磺酰衍生物荧光探针,该荧光探针合成简单、对微环境敏感,可以与市售的硫化氢受体吡罗红y共组装于表面活性剂聚集体中以构建超分子荧光传感体系。该传感体系制备简单、化学稳定性好、选择性好。用本发明构建的传感平台可对h2s进行选择性检测,检出限为110nm。
附图说明
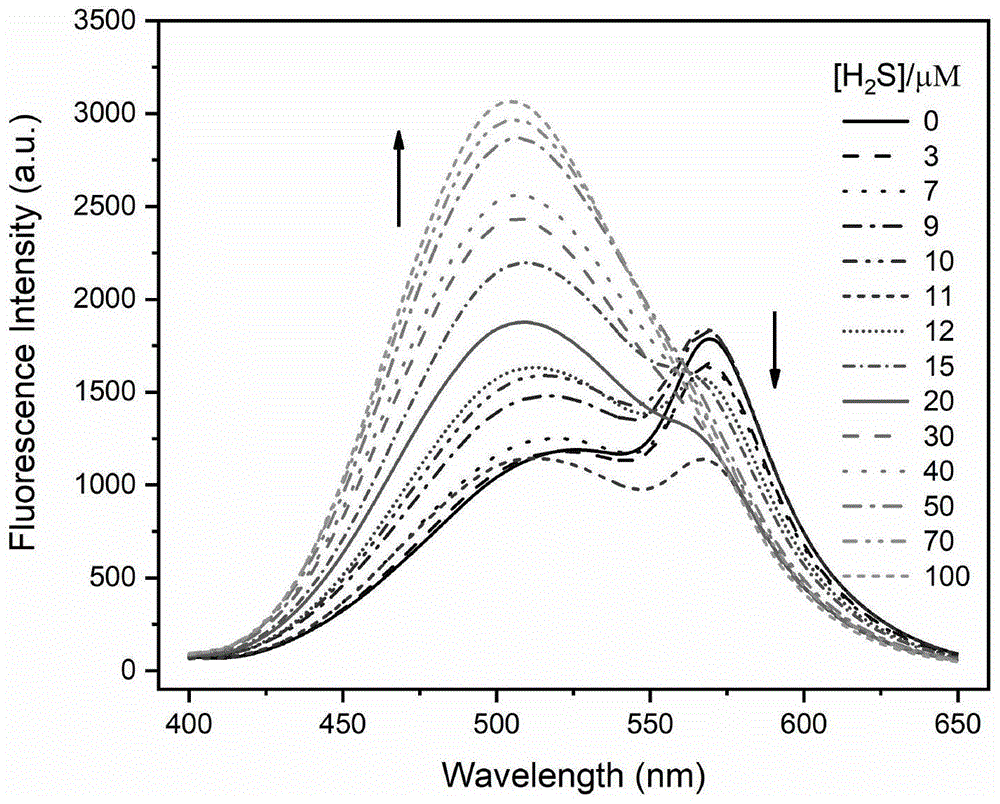
图1是本发明实施例1制备的丹磺酰衍生物荧光探针/吡罗红y/ctab组装体检测h2s的荧光强度变化曲线图;
图2是本发明实施例1制备的丹磺酰衍生物荧光探针/吡罗红y/ctab组装体检测h2s的荧光强度比值(i1/i2)与浓度关系图;
图3是本发明实施例1制备的丹磺酰衍生物荧光探针/吡罗红y/ctab组装体对16种分析物中h2s的选择性检测图;
图4是本发明实施例1制备的丹磺酰衍生物荧光探针/吡罗红y/ctab组装体在血清中检测h2s的荧光强度变化曲线图;
图5是本发明实施例1制备的丹磺酰衍生物荧光探针/吡罗红y/ctab组装体在血清中检测h2s的荧光强度比值(i1/i2)与浓度关系图。
具体实施方式
下面结合具体的实施例对本发明做进一步的详细说明,所述是对本发明的解释而不是限定。
本发明公开了一种丹磺酰衍生物荧光探针,该荧光探针的结构式如下:
式中,n为1或2或3。
上述丹磺酰衍生物荧光探针的合成步骤如下:
在流速为0.6~0.8ml/s的氮气保护条件下,按摩尔比为1:1.5:1.5将丹磺酰氯的三氯甲烷溶液滴加到含溴取代醇和三乙胺的三氯甲烷溶液中,滴加完成后室温搅拌4小时。待反应结束后,将反应液用饱和食盐水洗6~7次,然后用无水硫酸钠干燥4h。蒸除三氯甲烷,用二氯甲烷与石油醚的体积比为1.5:1的混合溶剂作为洗脱剂柱层析纯化产物,得到丹磺酰衍生物荧光探针,其反应方程式如下:
上述的溴取代醇为4-溴-1-丁醇、6-溴-1-己醇或8-溴-1-辛醇中的任意一种。
上述的丹磺酰衍生物荧光探针在检测生物硫醇中的用途,所述的生物硫醇为h2s,其检测方法如下:
1、配制溶液
向pbs缓冲溶液(10mmol/l,ph7.4)中分别加入一定量的浓度为5×10-3mol/lctab溶液、浓度为2.5×10-3mol/l丹磺酰衍生物荧光探针溶液、浓度为2.5×10-3mol/l吡罗红y溶液,继续加pbs缓冲溶液定容至刻度线,配制成丹磺酰衍生物/吡罗红y/ctab(10μm/5μm/100μm)荧光探针溶液。本发明用到的h2s是由na2s·9h2o代替的,故称取一定质量的na2s·9h2o溶于二次水中,配制成2.5mmol/lna2s·9h2o溶液。
2、绘制标准曲线
量取2.5ml荧光探针溶液于比色皿中,分别向其中滴加2.5mmol/lna2s·9h2o溶液,用毛细管搅拌使其混合均匀,所得到的溶液中na2s·9h2o的浓度为0~100μmol/l。荧光光谱的测试均在f-7000荧光光谱仪(hitachi,japan)上完成,扫描速度为1200nm/min,样品的激发波长为345nm,激发和发射狭缝分别设置为10.0和5.0nm。待上述溶液达到稳定后,分别绘制荧光强度随h2s浓度变化的荧光光谱图,并通过采集丹磺酰衍生物(i1)与吡罗红y(i2)处的荧光强度,绘制i1/i2值随h2s浓度变化的标准曲线。
3、检测待测样品
按照上述方法用荧光仪测量待测h2s样品的荧光强度,根据待测生物硫醇样品的i1/i2值和浓度,结合标准曲线的线性方程即可确定为h2s。
本发明基于丹磺酰衍生物的比例型荧光组装体的化学稳定性好、选择性好,可直接进行检测,如f-7000荧光光谱仪或其他类似的光学检测器,实现对h2s的选择性检测。
实施例1
合成结构式如下的丹磺酰衍生物荧光探针:
其合成步骤如下:
在流速为0.6ml/s的氮气保护及室温条件下,将溶有0.50g(1.85mmol)丹磺酰氯的三氯甲烷溶液逐滴加入含253μl(2.78mmol)4-溴-1-丁醇和385μl(2.78mmol)三乙胺的三氯甲烷溶液中,滴加完成后室温搅拌反应4小时。用饱和食盐水洗涤6次,然后用无水硫酸钠干燥4h,蒸除三氯甲烷,用二氯甲烷与石油醚的体积比为1.5:1的混合溶剂作为洗脱剂柱层析纯化产物,得到丹磺酰衍生物荧光探针,其收率为86%,其反应方程式如下:
上述丹磺酰衍生物荧光探针的核磁数据为:1hnmr(600mhz,cdcl3)δ8.65(s,1h),8.28(d,j=7.1hz,2h),7.59(dt,j=21.6,7.8hz,2h),7.24(s,1h),4.03(t,j=6.0hz,2h),3.26(t,j=6.4hz,2h),2.92(s,6h),1.87-1.81(m,2h),1.76(dt,j=12.0,6.0hz,2h).
实施例2
合成结构式如下的丹磺酰衍生物荧光探针:
其合成步骤如下:
在实施例1的合成步骤中,将所用的4-溴-1-丁醇用等摩尔质量的6-溴-1-己醇替换,其它步骤与相应的实施例1相同。
实施例3
合成结构式如下的丹磺酰衍生物荧光探针:
其合成步骤如下:
在实施例1的合成步骤中,将所用的4-溴-1-丁醇用等摩尔质量的8-溴-1-辛醇替换,其它步骤与相应的实施例1相同。
实施例4
实施例1合成的丹磺酰衍生物荧光探针,与市售的吡罗红y共组装于表面活性剂ctab聚集体中,构建基于非共价相互作用的超分子荧光传感平台,在水相中检测h2s的用途,其使用方法如下:
1、配制溶液
向50ml容量瓶中加入1ml浓度为5mmctab溶液后,向其中加入pbs缓冲溶液(10mmol/l,ph7.4)至距刻度线为2~3cm处,然后再向其中先后加入200μl浓度为2.5×10-3mol/l丹磺酰衍生物荧光探针的乙腈溶液、100μl浓度为2.5×10-3mol/l吡罗红y的水溶液,继续加pbs缓冲溶液定容至刻度线,配制成丹磺酰衍生物/吡罗红y/ctab(10μm/5μm/100μm)荧光探针溶液。称取一定质量的na2s·9h2o溶于二次水中,配制成2.5mmol/lna2s·9h2o溶液。
2、绘制标准曲线
量取2.5ml上述荧光探针溶液于比色皿中,分别加入2.5mmol/lna2s·9h2o溶液,用毛细管搅拌使其混合均匀,使得混合溶液中h2s的浓度分别为3、7、9、10、11、12、15、20、30、40、50、70和100μmol/l。荧光光谱的测试均在荧光光谱仪f-7000(hitachi,japan)上完成,扫描速度为1200nm/min,样品的激发波长为345nm,激发与发射狭缝分别为10.0和5.0nm。待溶液达到平衡后,绘制荧光强度随h2s浓度变化的荧光光谱图,见图1。并通过采集丹磺酰衍生物(i1)与吡罗红y(i2)处的荧光强度,绘制i1/i2值随h2s浓度变化的标准曲线,见图2。
由图1可见,传感平台的荧光强度随着体系中h2s浓度的增大,呈现出吡罗红y荧光强度降低,丹磺酰衍生物荧光强度明显增强并伴随蓝移的比例型响应现象。由图2可见,在h2s浓度为0~15μmol/l时,i1/i2随浓度呈二次方关系;在20~100μmol/l时,i1/i2随浓度呈线性关系(每个值代表三次平行实验的平均值),方程分别为:
y1=0.693(±0.010)+1.633e-5(±0.004)x+0.003(±0.0003)x2;
y2=1.391(±0.043)+0.011(±0.001)x;
式中y1和y2为h2s浓度分别为0~15μmol/l和20~100μmol/l时i1/i2值,x为h2s浓度,相关系数r2分别为0.993和0.963。经测试,该荧光传感平台对h2s的检出限为110nmol/l。
3、检测待测样品
向2.5ml荧光组装体溶液中加入不同体积的待测生物硫醇样品,用荧光仪监测传感平台的荧光强度,通过计算i1/i2值和浓度的关系,结合标准曲线的方程即可确定为h2s。
为了证明本发明的有益效果,发明人按照实施例4的方法,在丹磺酰衍生物/吡罗红y/ctab(10μm/5μm/100μm)荧光组装体溶液中加入等量的h2s、cys、hcy、gsh、cl-、br-、i-、hco3-、h2po4-、bro3-、aco-、oh-、co32-、so42-、c2o42-和s2o32-,只有h2s发生明显的比例型响应,而其他分析物荧光强度比值均未发生明显变化,说明传感平台对h2s具有很好的选择性检测,见图3(每个值代表三次平行实验的平均值)。
实施例5
实施例1合成的丹磺酰衍生物,与吡罗红y和ctab构建比例型荧光传感平台,在血清中检测h2s的用途,其使用方法如下:
1、配制溶液
将血清溶液用pbs缓冲溶液(10mmol/l,ph7.4)稀释为体积分数为1%的血清溶液。按照案例4中溶液的配制,向50ml容量瓶中加入1ml浓度为5mmctab溶液(1%血清)后,向其中加入1%血清溶液至距刻度线为2~3cm处,然后再向其中先后加入200μl浓度为2.5×10-3mol/l丹磺酰衍生物荧光探针的乙腈溶液、100μl浓度为2.5×10-3mol/l吡罗红y的水溶液,继续加1%血清溶液定容至刻度线,配制成丹磺酰衍生物/吡罗红y/ctab(10μm/5μm/100μm)荧光探针溶液。称取一定质量的na2s·9h2o溶于二次水中,配制成2.5mmol/lna2s·9h2o溶液。
2、绘制标准曲线
量取2.5ml上述荧光探针溶液于比色皿中,分别加入2.5mmol/lh2s溶液,用毛细管搅拌使其混合均匀,使得混合溶液中h2s的浓度分别为3、5、7、10、15、20、30、40、50、70和100μmol/l。荧光光谱的测试均在荧光光谱仪f-7000(hitachi,japan)上完成,扫描速度为1200nm/min,样品的激发波长为345nm,激发与发射狭缝分别为10.0和5.0nm。待溶液达到平衡后,绘制荧光强度随h2s浓度变化的荧光光谱图,见图4。并通过采集丹磺酰衍生物(i1)与吡罗红y(i2)处的荧光强度,绘制i1/i2值随h2s浓度变化的标准曲线,见图5。
由图4可见,传感平台的荧光强度随着体系中h2s浓度的增大,呈现出不同的响应程度。由图5可见,在h2s浓度为0~40μmol/l和40~100μmol/l时,i1/i2与h2s浓度呈不同的线性关系(每个值代表三次平行实验的平均值),线性方程分别为:
y1=1.697(±0.014)+0.014(±0.0005)x;
y2=2.034(±0.018)+0.006(±0.0003)x;
式中y1和y2为硫化氢浓度在0~40μmol/l和40~100μmol/l时的i1/i2值,x为人血清蛋白浓度,线性相关系数r2分别为0.992和0.993。
3、检测待测样品
向2.5ml上述荧光组装体溶液中加入不同体积的待测生物硫醇样品,用荧光仪监测传感平台的荧光强度,通过计算i1/i2值和浓度的关系,结合标准曲线的方程即可确定为h2s。
综上所述,本发明采用非共价共组装策略构建的荧光传感体系,可以大大减少对有机合成的依赖。同时,该传感平台既可以在水相中实现对h2s的高选择性检测,又可以实现在血清中的潜在应用。
实施例6
合成结构式如下的丹磺酰衍生物荧光探针:
其合成步骤如下:
在流速为0.7ml/s的氮气保护及室温条件下,将溶有0.50g(1.85mmol)丹磺酰氯的三氯甲烷溶液逐滴加入含169μl(1.85mmol)4-溴-1-丁醇和257μl(1.85mmol)三乙胺的三氯甲烷溶液中,滴加完成后室温搅拌反应3小时。用饱和食盐水洗涤6次,然后用无水硫酸钠干燥4h,蒸除三氯甲烷。用二氯甲烷与石油醚的体积比为1:1的混合溶剂作为洗脱剂柱层析纯化产物,得到丹磺酰衍生物荧光探针,其收率为80%,其反应方程式如下:
实施例7
合成结构式如下的丹磺酰衍生物荧光探针:
其合成步骤如下:
在流速为0.8ml/s的氮气保护及室温条件下,将溶有0.50g(1.85mmol)丹磺酰氯的三氯甲烷溶液逐滴加入含253μl(2.78mmol)4-溴-1-丁醇和385μl(2.78mmol)三乙胺的三氯甲烷溶液中,滴加完成后室温搅拌反应5小时。用饱和食盐水洗涤7次,然后用无水硫酸钠干燥4h,蒸除三氯甲烷。用二氯甲烷与石油醚的体积比为2:1的混合溶剂作为洗脱剂柱层析纯化产物,得到丹磺酰衍生物荧光探针,其收率为83%,其反应方程式如下:
- 还没有人留言评论。精彩留言会获得点赞!