一种生物降解性可辐射固化的(甲基)丙烯酸酯及其制备方法与流程
[0001]
本发明涉及一种生物降解性可辐射固化的(甲基)丙烯酸酯及其制备方法,属于生物基改性的可生物降解光固化材料领域。
背景技术:
[0002]
光固化技术具有快速固化、节能省时、低溶剂释放、固化温度低、设备体积小、投资低等优点,其应用领域从最初的木材涂装现已发展到塑料装饰、金属部件涂装、医疗器械、电子元件、信息记录介质、感光印刷、塑性材料和光学纤维等多个工业生产领域,它主要以uv涂料、uv油墨、uv胶粘剂等形式出现。
[0003]
紫外光固化材料由光敏预聚体(低聚物)、活性稀释单体、光引发剂和各类添加助剂(颜填料、消泡剂等)组成。预聚体是紫外光固化体系的基础树脂,在整个体系中占有较大比例。活性稀释剂是用来稀释预聚体,使树脂体系达到期望的粘度。预聚体和活性稀释单体一起一般占整个固化体系质量的90%以上,其中活性稀释单体占40-60%。它们对整个体系的性能,如硬度、附着力、柔韧性、耐久性、耐磨性、拉伸强度、耐冲击性、及耐老化性能等起着决定性作用。
[0004]
由于石油资源的日益锐减,以可再生资源为原料制备生物基高分子材料,促进高分子材料的可持续发展,受到了学术界与产业界的广泛关注。生物基材料是当今全球新材料热点之一,据occams research发布的研究报告,目前全球生物基化学品和高分子材料产量约5000万吨左右,到2021年预计产值可达到100-150亿美元。发达国家为促进本国生物基材料产业的发展和使用,纷纷出台一系列相关法律法规,如美国的优先采购生物基产品计划、欧盟第七研发框架计划(fp7)、日本的生物基材料2020计划和澳大利亚的可持续包装计划等。尤其是由荷兰、英国、德国、法国、意大利等主导的欧盟第七研发框架计划(fp7),跨行业生物基产品企业联合科技界组成的欧洲生物基产品技术开放平台。该技术平台研究整个生物基产品价值链任何环节的特定标准,从生产标准、工业标准、商业标准和监管标准到检测方法和产品标示。尤其是建立起一整套欧盟生物基产品标签制度,刺激和扩大市场消费。生物基材料作为中国战略性新兴产业之一。我国生物基材料近年来发展迅速,保持了约20%的年均增长速度,总产量已达到600万吨/年,到2020年产量有望翻番。
[0005]
木糖醇原产于芬兰,是从白桦树、橡树、玉米芯、甘蔗渣等植物原料中提取出来的一种天然甜味剂,在自然界中,木糖醇的分布范围很广,广泛存在于各种水果、蔬菜、谷类之中,但含量很低。商品木糖醇是将玉米芯、甘蔗渣等农业作物进行深加工而制得的,是一种天然、健康的甜味剂。木糖醇作为一种价廉易得的可再生资料,木糖醇可被人体代谢所吸收,是美国食品与药品管理局(fda)认可,有较好的生物相容性,若能将其应用于制备可持续发展的高分子材料,不仅符合可持续发展的要求,且能减少石化资源的消耗。
技术实现要素:
[0006]
本发明提供一种生物降解性可辐射固化的(甲基)丙烯酸酯及其制备方法,本发明
生物降解性可辐射固化的(甲基)丙烯酸酯由木糖醇缩醛成分、聚酯聚醚改性成分和(甲基) 丙烯酸酯化性化合物制备而成,在硬度、柔韧性、抗氧化性和附着力等方面提升显著,且具有生物相容性以及可生物降解性,环境友好;同时拓宽了生物资源木糖醇的利用,减少了石化资源的消耗。
[0007]
为解决上述技术问题,本发明所采用的技术方案如下:
[0008]
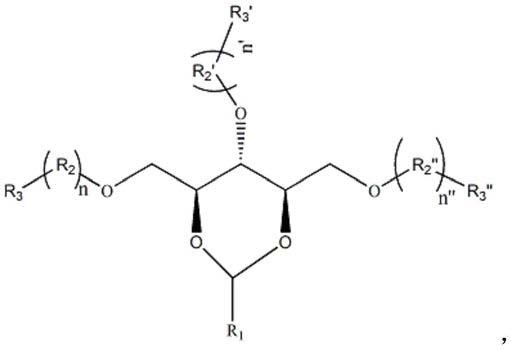
一种生物降解性可辐射固化的(甲基)丙烯酸酯,其结构式为:
[0009]
其中,r1为氢、或者c1-c10的的直链或带支链烷基、或者含c1-c4支链的苯基;r2,r2
′
,r2
″
均为聚酯聚醚改性基,聚酯聚醚改性基中包含(聚)己内酯、(聚)丙交酯、(聚)乙交酯、提供环氧化物基的化合物或提供含有2-3个碳原子的环氧烷基残基单元中的至少一种;n,n
′
和n
″
均为0-4的整数,且 n、n
′
和n
″
之和大于0;r3,r3
′
和r3
″
均为通过酯基连接在分子主链上的(甲基)丙烯酸酯化性化合物的残基。
[0010]
上述化合物主要适用于辐射固化涂料,如辐射固化油墨、辐射固化胶黏剂等。
[0011]
上述化合物在塑料(pvc,abs,pe,pp及pc等)上的附着力尤其突出。
[0012]
本申请(甲基)丙烯酸酯表示丙烯酸酯或甲基丙烯酸酯,其他各处类似表达,含义类似,如(聚)己内酯表示己内酯或聚己内酯。
[0013]
上述生物降解性可辐射固化的(甲基)丙烯酸酯,由木糖醇缩醛成分、聚酯聚醚改性成分和(甲基)丙烯酸酯化性化合物制备而成。
[0014]
上述木糖醇缩醛成分为木糖醇缩甲醛以及其缩醛衍生物,羟基官能度为2.5~3.5;优选为,木糖醇缩甲醛,木糖醇缩苯甲醛,最优选的是木糖醇缩甲醛。这样能更好地提升产品的硬度、柔韧性和附着力。
[0015]
上述聚酯聚醚改性成分为包含(聚)己内酯、(聚)丙交酯、(聚)乙交酯、提供环氧化物基的化合物或提供含有2-3个碳原子的环氧烷基残基单元中的至少一种。
[0016]
(甲基)丙烯酸酯化性化合物为:不饱和酸、不饱和的酰卤、带端(甲基)丙烯酰基的环氧化合物、带(甲基)丙烯酰基的不饱和酸或不饱和酸的烷基酯中的至少一种。如: (甲基)丙烯酸,(甲基)丙烯酸酰氯/溴/碘,甲基丙烯酸甲/乙/(正/异)丙酯,(甲基) 丙烯酸缩水甘油醚。进一步优选为:(甲基)丙烯酸酰氯、(甲基)丙烯酸、(甲基)丙烯酸甲酯或带端(甲基)丙烯酰基环氧化合物。
[0017]
上述生物降解性可辐射固化的(甲基)丙烯酸酯的制备,包括顺序相接的如下步骤:
[0018]
a、用木糖醇与带反应性羰基的醛类化合物在酸性催化剂作用下反应,采用带水溶剂共沸除去反应生成水,制得含多羟基以及取代基的木糖醇缩醛成分;带反应性羰基的醛类化合物为甲醛、或者含c1-c10的直链或带支链的烷基醛、或者含c1-c4支链的苯基醛,优选的是甲醛、苯甲醛或苯乙醛,最优选的是甲醛;
[0019]
b、木糖醇缩醛成分与聚酯聚醚改性成分在催化剂的作用下进行改性反应,制得聚酯聚醚改性木糖醇缩醛多元醇;
[0020]
c、按照如下c1-c4中的任何一种方式进行:
[0021]
c1.聚酯聚醚改性木糖醇缩醛多元醇与(甲基)丙烯酸酰氯反应,制得生物降解性可辐射固化的(甲基)丙烯酸酯,此反应过程不需加其它溶剂;
[0022]
c2.聚酯聚醚改性木糖醇缩醛多元醇与(甲基)丙烯酸在酯化催化剂、阻聚剂和脱水剂的作用下发生酯化反应,生成聚酯聚醚改性木糖醇缩醛多元醇。
[0023]
c3.聚酯聚醚改性木糖醇缩醛多元醇与(甲基)丙烯酸甲酯在酯化催化剂和阻聚剂的作用下发生酯交换反应,生成聚酯聚醚改性木糖醇缩醛多元醇。
[0024]
c4.聚酯聚醚改性木糖醇缩醛多元醇与带端(甲基)丙烯酰基的环氧化合物在催化剂的作用下发生酯交换反应,生成聚酯聚醚改性木糖醇缩醛多元醇。
[0025]
上述制备方法简单易控制,且所得产品纯度高、综合性能好。
[0026]
申请人经研究发现,上述特定结构的木糖醇缩醛与特定结构的聚酯聚醚结合,改性(甲基)丙烯酸酯,使得材料的抗氧化性、硬度、柔韧性和附着力均提升显著;由于木糖醇可被人体代谢所吸收是美国食品与药品管理局(fda)认可,有较好的生物相容性,可应用在一些食品包装涂层以及一些医疗器件材料的涂层或粘结剂,大大拓展了所得材料的应用领域;且木糖醇缩醛与可生物降解的聚酯聚醚结合改性,不仅使得材料的力学性能和抗氧化性有了更显著的提升,还能通过聚酯聚醚的亲水性改善其在使用基材上的附着力,同时具有生物降解性能,因此申请人提出了本申请。
[0027]
为了促进物料的完全反应,同时确保改性产品的性能,上述步骤a中,反应温度为 40-100℃,反应时间为6-16h;木糖醇、醛与酸性催化剂的摩尔比为(100-130):100: (3-8);
[0028]
为了提高反应速率,同时减少副反应,步骤a中,酸性催化剂为硫酸、磺酸、甲基磺酸、乙基磺酸、苯磺酸、对甲苯磺酸中的一种或两种以上任意配比的混合物,优选为甲基磺酸,酸性催化剂的摩尔用量为木糖醇摩尔数的1-6%。
[0029]
上述选择带水溶剂,不仅可分散物料,而且可共沸除去反应生成的水。为了提高反应效率,步骤a中,带水溶剂为甲醇、乙醇、苯、甲苯、c5烷烃或c6烷烃中的一种或两种以上任意配比的混合物,带水溶剂的质量用量为木糖醇和带羰基的醛类化合物质量和的 10-40%。
[0030]
为了便于反应,步骤b在环己烷、庚烷或甲苯中反应;
[0031]
为了提高反应速率,同时减少副反应,步骤b中,催化剂为二月桂酸丁基锡、钛酸四丁酯、钛酸四异丙酯、辛酸亚锡、二醋酸二丁基酯、环烷酸锌、环烷酸钴或环烷酸铋中的一种或两种以上任意配比的混合物。
[0032]
上述步骤b中,反应温度为70-120℃,反应时间为2-6小时,这样可确保反应的充分反应,同时确保所得材料的综合性能。
[0033]
为了确保反应顺利平缓的进行,同时确保产品的得率和性能,,步骤c1为:将(甲
基) 丙烯酰氯缓慢(30-60滴/min)滴入聚酯聚醚改性木糖醇缩醛多元醇中,滴加完毕后,室温下反应1-3小时,分离后即得生物降解性可辐射固化的(甲基)丙烯酸酯;其中,(甲基)丙烯酰氯的摩尔用量为聚酯聚醚改性木糖醇缩醛多元醇摩尔数的1-1.3倍。
[0034]
为了提高反应效率,在步骤c1的反应中,加入低沸点胺类碱性物中和酰氯反应后产生的盐酸,帮助加快反应,其中,低沸点胺类碱性物为甲胺、乙胺、二乙胺或三乙胺中的一种或两种以上任意配比的混合物,低沸点胺类碱性物的摩尔用量为聚酯聚醚改性木糖醇缩醛多元醇摩尔数的1-1.3倍。
[0035]
为了提高反应效率和产品的纯度,步骤c2和c3中,酯化催化剂均为硫酸、磺酸、甲基磺酸、乙基磺酸、苯磺酸或对甲苯磺酸中的一种或两种以上任意配比的混合物。
[0036]
为了确保反应的充分性和产品综合性能的优异性,步骤c2和c3中,反应温度均为 70-110℃,反应时间均为6-14h,反应结束后,经水洗、中和、脱溶,生成聚酯聚醚改性木糖醇缩醛多元醇;其中,(甲基)丙烯酸或者(甲基)丙烯酸甲酯的摩尔用量为聚酯聚醚改性木糖醇缩醛多元醇摩尔数的2.4-4倍。
[0037]
为了进一步提高产品的附着力,步骤c4中,带端(甲基)丙烯酰基的环氧化合物为丙烯酸缩水甘油醚和甲基丙烯酸缩水甘油醚任意配比的混合物;催化剂为三乙胺、卞基氯化铵、卞基溴化铵或三苯基膦中的一种或两种以上任意配比的混合物。
[0038]
本发明未提及的技术均参照现有技术。
[0039]
本发明生物降解性可辐射固化的(甲基)丙烯酸酯由木糖醇缩醛成分、聚酯聚醚改性成分和(甲基)丙烯酸酯化性化合物制备而成,在硬度、柔韧性、抗氧性和附着力等方面提升显著,且可生物降解,环境友好;同时拓宽了生物资源木糖醇的利用,减少了石化资源的消耗。
具体实施方式
[0040]
为了更好地理解本发明,下面结合实施例进一步阐明本发明的内容,但本发明的内容不仅仅局限于下面的实施例。
[0041]
实施例中,“室温”和“环境温度”为25℃;得率:实际生成的产品质量与按照木糖醇理论生成质量的百分比。
[0042]
实施例1
[0043]
(1)木糖醇缩甲醛制备:
[0044]
在室温下向装有机械搅拌、温度计的500ml四口瓶中加入d-木糖醇(152g,1mol), 35%甲醛(103g,1.2mol),70%甲基磺酸(18.2g,1.9mmol),甲醇(76.5g);反应回流温度为60-70℃,回流管中添加甲醇和氯化钙,反应8h,反应基本结束后,减压蒸馏去除多余的甲醛和甲醇,加入正庚烷40g,搅拌2h后抽滤,滤饼采用20ml热的环己烷洗涤2次,得到木糖醇缩醛成分m1,烘干得134.6g,得率82%。按照前述方法,制备2500g左右的木糖醇缩醛成分m1,用于实验。所得产品采用硅胶层析柱分离,最后产品进行1h-nmr 核磁分析,1h-nmr采用bruker av400 nmr核磁共振仪测试,tms为内标参照,1h nmr (400mhz,cdcl3)δ4.75(d,1h),4.65(d,1h),3.96(m,2h),3.79(m,2h),3.54(m,2h),3.39 (m,1h),2.0(s,3h);氢核磁共振(1h nmr)波谱分析得所得产品为如下述式i所示:
[0045][0046]
实施例2
[0047]
(2)木糖醇缩苯甲醛制备:
[0048]
在室温下向装有机械搅拌、温度计的500ml四口瓶中加入d-木糖醇(152g,1mol),苯甲醛(117g,1.1mol),70%甲基磺酸(19.2g,2mmol),甲醇(80.7g);反应回流温度为60-70℃,回流管中添加甲醇和氯化钙。反应8h,反应基本结束后,减压蒸馏去除多余的甲醇,加入40g水,搅拌2h后抽滤,滤饼采用20ml热的环己烷洗涤2次,得到木糖醇缩醛成分m2,烘干得171.1g,得率71%。按照前述方法,制备2500g左右的木糖醇缩醛成分m2,用于实验。所得产品采用硅胶层析柱分离,最后产品进行1h-nmr核磁分析,1h-nmr采用bruker av400 nmr核磁共振仪测试,tms为内标参照,1h nmr(400mhz, cdcl3)δ7.18-7.20(m,5h),5.98(s,1h),3.96(m,2h),3.79(m,2h),3.54(m,2h),3.39(m, 1h),2.0(s,3h);氢核磁共振(1h nmr)波谱分析得所得产品为如下述式ⅱ所示:
[0049][0050]
实验证明,采用盐酸,磷酸,硫酸,对甲苯磺酸替代本实施例中的甲基磺酸,也可以对反应进行催化。
[0051]
实施例3
[0052]
己内酯改性木糖醇缩甲醛:
[0053]
在室温下向装有机械搅拌、温度计的500ml四口瓶(接回流冷凝管)中加入木糖醇缩甲醛m1(82g,0.5mol),6-己内酯(171g,1.5mol),甲苯(50g),二月桂酸丁基锡(2g),升温至105℃,微回流下保持5小时,该反应基本上完成,制得己内酯改性木糖醇缩醛主链(r2n-a-r2
′
n(r2
″
n)简称中间产物m1a2),减压脱出甲苯溶剂后,用于下一步反应。
[0054]
实验证明,采用钛酸四丁酯、钛酸四异丙酯、辛酸亚锡、二醋酸二丁基酯、环烷酸锌、环烷酸钴或环烷酸铋替代本实施例中的二月桂酸丁基锡,也可以对反应进行催化;溶剂也可以为环己烷或庚烷替代本实施例中甲苯,溶剂采用环己烷时,回流温度改为88℃,时间延长至6小时。
[0055]
实施例4
[0056]
己内酯改性木糖醇缩苯甲醛:
[0057]
在室温下向装有机械搅拌、温度计的500ml四口瓶(接回流冷凝管)中加入木糖醇
缩苯甲醛m2(120g,0.5mol),6-己内酯(171g,1.5mol),甲苯(54g),二月桂酸丁基锡(2.16g),升温至105℃,微回流下保持5小时,该反应基本上完成,从而制得己内酯改性木糖醇缩苯甲醛主链(r2n-a-r2
′
n(r2
″
n)简称中间产物m2a2),减压脱出甲苯溶剂后,用于下一步反应。
[0058]
实验证明,采用钛酸四丁酯、钛酸四异丙酯、辛酸亚锡、二醋酸二丁基酯、环烷酸锌、环烷酸钴或环烷酸铋替代本实施例中的二月桂酸丁基锡,也可以对反应进行催化;溶剂也可以用环己烷或庚烷替代本实施例中甲苯,溶剂采用环己烷时,回流温度改为88℃,时间延长至6小时。
[0059]
实施例5
[0060]
乙交酯改性木糖醇缩甲醛:
[0061]
在室温下向装有机械搅拌、温度计的500ml四口瓶(接回流冷凝管)中加入木糖醇缩甲醛m1(82g,0.5mol),乙交酯(174g,1.5mol),甲苯(51g),二月桂酸丁基锡(2.04 g),升温至105℃,微回流下保持5小时,该反应基本上完成,从而制备己内酯改性木糖醇缩醛主链(r2n-a-r2
′
n(r2
″
n)简称中间产物m1a3),减压脱出甲苯溶剂后,用于下一步反应。
[0062]
实验证明,采用钛酸四丁酯、钛酸四异丙酯、辛酸亚锡、二醋酸二丁基酯、环烷酸锌、环烷酸钴或环烷酸铋替代本实施例中的二月桂酸丁基锡,也可以对反应进行催化;溶剂也可以用环己烷或庚烷替代本实施例中甲苯,溶剂采用环己烷时,回流温度改为88℃,时间延长至6小时。
[0063]
实验进一步证明,木糖醇缩甲醛m1可采用木糖醇缩苯甲醛替代进行上述乙交酯改性反应。
[0064]
实施例6
[0065]
丙交酯改性木糖醇缩甲醛:
[0066]
在室温下向装有机械搅拌、温度计的500ml四口瓶(接回流冷凝管)中加入木糖醇缩甲醛m1(82g,0.5mol),丙交酯(216g,1.5mol),甲苯(59.6g),二月桂酸丁基锡 (2.38g),升温至105℃,微回流下保持4-6小时,该反应基本上完成,从而制备己内酯改性木糖醇缩醛主链(r2n-a-r2
′
n(r2
″
n)简称中间产物m1a4),减压脱出甲苯溶剂后,用于下一步反应。
[0067]
实验证明,采用钛酸四丁酯、钛酸四异丙酯、辛酸亚锡、二醋酸二丁基酯、环烷酸锌、环烷酸钴或环烷酸铋替代本实施例中的二月桂酸丁基锡,也可以对反应进行催化;溶剂也可以用环己烷或庚烷替代本实施例中甲苯,溶剂采用环己烷时,回流温度改为88℃,时间延长至6小时。
[0068]
实验进一步证明,木糖醇缩甲醛m1可采用木糖醇缩苯甲醛替代进行上述丙交酯改性反应。
[0069]
实施例7
[0070]
环氧乙烷改性木糖醇缩甲醛:
[0071]
在室温下,向装有机械搅拌、温度计的500ml四口瓶(接回流冷凝管)中加入木糖醇缩甲醛m1(164g,1mol),氢氧化钾(57.1g,1.02mol),甲苯(40g),升温至110℃,回流下保持2-3小时,脱除水分,制得木糖醇钾;向带机械搅拌以及独立的进气排气阀的高压反应釜(可控温度0-200℃)中抽入(缩甲醛)木糖醇钾约(222g,1mol),先用氮气进行置换,置换压力不大于0.2mpa,排空后封闭反应釜,开动搅拌,料温逐步升至110℃。再将带独立的进气排气阀
的压力物料罐(环氧乙烷3mol,132g)内用氮气加压在0.5~ 0.6mpa压力,使环氧乙烷根据聚合工艺要求连续、缓慢压入聚合釜,保持釜内压力不超过0.3mpa,温度不超过120℃,低压聚合。环氧乙烷进料完毕,在搅拌下,维持釜温120℃, 0.5小时后,停止保温。待釜内压力降至0.05mpa以下,物料温度降至70℃以下,反应结束;转移至烧瓶中加入醋酸(63g,1.05mol)中和,用50ml水水洗两次,下层水分离去除,上层减压脱溶,去除多余的甲苯,从而制备环氧乙烷改性木糖醇缩醛主链(r2n-a-r2
′ꢀ
n(r2
″
n)简称中间产物m1a5)。
[0072]
实验证明,采用氢氧化钠、甲醇钠、乙醇钠、甲醇钾或乙醇钾替代本实施例中的氢氧化钾,也可以对反应进行催化;溶剂也可以用环己烷或庚烷替代本实施例中甲苯,溶剂采用环己烷时,回流温度改为88℃,时间延长至4小时。
[0073]
实验进一步证明,木糖醇缩甲醛m1可采用木糖醇缩苯甲醛替代进行上述环氧乙烷改性反应。
[0074]
实施例8
[0075]
环氧丙烷改性木糖醇缩甲醛:
[0076]
在室温下,向装有机械搅拌、温度计的500ml四口瓶(接回流冷凝管)中加入木糖醇缩甲醛m1(164g,1mol),氢氧化钾(57.1g,1.02mol),甲苯(40g),升温至110℃,回流下保持2-3小时,脱除水分;向带机械搅拌以及独立的进气排气阀的高压反应釜(可控温度0-200℃)中抽入(缩甲醛)木糖醇钾约(222g,1mol),先用氮气进行置换,置换压力不大于0.2mpa,排空后封闭反应釜,开动搅拌,料温逐步升至110℃。再将带独立的进气排气阀的压力物料罐(环氧丙烷3mol,174g)内用氮气加压在0.5~0.6mpa压力,使环氧丙烷根据聚合工艺要求连续、缓慢压入聚合釜,保持釜内压力不超过0.3mpa,温度不超过120℃,低压聚合。环氧丙烷进料完毕,在搅拌下,维持釜温120℃,0.5小时后,停止保温。待釜内压力降至0.05mpa以下,物料温度降至70℃以下,反应结束;转移至烧瓶中加入醋酸(63g,1.05mol)中和,用50ml水水洗两次,下层水分离去除,上层减压脱溶,去除多余的甲苯,从而制备环氧丙烷改性木糖醇缩醛主链(r2n-a-r2
′
n(r2
″
n) 简称中间产物m1a6)。
[0077]
实验证明,采用氢氧化钠、甲醇钠、乙醇钠、甲醇钾或乙醇钾替代本实施例中的氢氧化钾,也可以对反应进行催化;溶剂也可以用环己烷或庚烷替代本实施例中甲苯,溶剂采用环己烷时,回流温度改为88℃,时间延长至4小时。
[0078]
实验进一步证明,木糖醇缩甲醛m1可采用木糖醇缩苯甲醛替代进行上述环氧丙烷改性反应。
[0079]
实施例9:
[0080]
由己内酯改性木糖醇缩甲醛制备己内酯改性木糖醇缩甲醛丙烯酸酯:
[0081]
在将实施例3所得m1a2剩余溶液冷却至室温,加入(182g,1.8mol)三乙胺,撤去加热用的电热套,用冰水浴冷却温度至0℃,使将要反生的反应比较平缓,之后采用加样恒压滴液漏斗缓慢滴加(136g,1.5mol,30滴/min)丙烯酰氯到冰浴冷却的带电动搅拌的烧瓶中,将丙烯酰氯滴加完毕后,移去冰水浴,逐步将烧瓶温度升温至室温,反应混合物在室温下维持2h,反应结束,用300ml的1m浓度的盐酸对产品进行酸洗,酸洗结束后,用100ml蒸馏水进行洗涤,洗涤完毕后,将0.15g对羟基苯甲醚加入产品溶液中,减压蒸馏脱除少量水和多余环己烷溶液,得到己内酯改性木糖醇缩甲醛丙烯酸酯。
[0082]
实验证明,上述丙烯酰氯可以采用甲基丙烯酰氯代替制备出性质相似的丙内酯改
性甲基丙烯酸酯;也可以采用甲胺、乙胺或二乙胺替代三乙胺进行上述反应。
[0083]
实施例10:
[0084]
由乙交酯改性木糖醇缩甲醛制备乙交酯改性木糖醇缩甲醛甲基丙烯酸酯:
[0085]
在将实施例5所得m1a3剩余溶液冷却至室温,加入(182g,1.8mol)三乙胺,撤去加热用的电热套,用冰水浴冷却温度至0℃,使将要反生的反应比较平缓,之后采用加样恒压滴液漏斗缓慢滴加(157g,1.5mol)甲基丙烯酰氯到冰浴冷却的带电动搅拌的烧瓶中,将甲基丙烯酰氯滴加完毕后,移去冰水浴,逐步将烧瓶温度升温至室温,反应混合物在室温下维持2h,反应结束,用300ml的1m浓度的盐酸对产品进行酸洗,酸洗结束后,用100ml蒸馏水进行洗涤,洗涤完毕后,将0.16g对羟基苯甲醚加入产品溶液中,减压蒸馏脱除少量水和多余环己烷溶液,得到乙交酯改性木糖醇缩甲醛甲基丙烯酸酯。
[0086]
实验证明,上述甲基丙烯酰氯可以采用丙烯酰氯代替制备出性质相似的乙交酯改性丙烯酸酯;也可以采用甲胺、乙胺或二乙胺替代三乙胺进行上述反应。
[0087]
实施例11:
[0088]
由丙交酯改性木糖醇缩苯甲醛制备丙交酯改性木糖醇缩苯甲醛甲基丙烯酸酯:
[0089]
将实施例6中木糖醇缩甲醛采用木糖醇缩苯甲醛替代反应,实验所得m2a4剩余溶液冷却至室温,加入(182g,1.8mol)三乙胺,撤去加热用的电热套,用冰水浴冷却温度至0℃,使将要反生的反应比较平缓,之后采用加样恒压滴液漏斗缓慢滴加(157g,1.5 mol)甲基丙烯酰氯到冰浴冷却的带电动搅拌的烧瓶中,将甲基丙烯酰氯滴加完毕后,移去冰水浴,逐步将烧瓶温度升温至室温,反应混合物在室温下维持2h,反应结束,用300 ml的1m浓度的盐酸对产品进行酸洗,酸洗结束后,用100ml蒸馏水进行洗涤,洗涤完毕后,将0.17g对羟基苯甲醚加入产品溶液中,减压蒸馏脱除少量水和多余环己烷溶液,得到丙交酯改性木糖醇缩苯甲醛甲基丙烯酸酯。
[0090]
实验证明,上述甲基丙烯酰氯可以采用丙烯酰氯代替制备出性质相似的丙交酯改性丙烯酸酯;丙交酯改性木糖醇缩苯甲醛(m2a4)可以采用丙交酯改性木糖醇缩甲醛(m1a4) 替代制备类似的丙交酯改性(甲基)丙烯酸酯;也可以采用甲胺、乙胺或二乙胺替代三乙胺进行上述反应。
[0091]
实施例12:
[0092]
由环氧丙烷改性木糖醇缩苯甲醛制备环氧丙烷改性木糖醇缩苯甲醛甲基丙烯酸酯:
[0093]
将实施例8中木糖醇缩甲醛采用木糖醇缩苯甲醛替代反应,实验所得m2a6剩余溶液冷却至室温,加入(364g,3.6mol)三乙胺,撤去加热用的电热套,用冰水浴冷却温度至0℃,使将要反生的反应比较平缓,之后采用加样恒压滴液漏斗缓慢滴加(314g,3mol) 甲基丙烯酰氯到冰浴冷却的带电动搅拌的烧瓶中,将甲基丙烯酰氯滴加完毕后,移去冰水浴,逐步将烧瓶温度升温至室温,反应混合物在室温下维持2h,反应结束,用600ml的 1m浓度的盐酸对产品进行酸洗,酸洗结束后,用200ml蒸馏水进行洗涤,洗涤完毕后,将0.34g对羟基苯甲醚加入产品溶液中,减压蒸馏脱除少量水和多余环己烷溶液,得到环氧丙烷改性木糖醇缩苯甲醛甲基丙烯酸酯。
[0094]
实验证明,上述甲基丙烯酰氯可以采用丙烯酰氯代替制备出性质相似的环氧丙烷改性丙烯酸酯;其中环氧丙烷改性木糖醇缩苯甲醛(m2a6)可以采用环氧丙烷改性木糖醇缩
甲醛(m1a6)替代制备类似的环氧丙烷改性(甲基)丙烯酸酯;也可以采用甲胺、乙胺或二乙胺替代三乙胺进行上述反应。
[0095]
实施例13:
[0096]
由己内酯改性木糖醇缩甲醛制备己内酯改性木糖醇缩甲醛(环氧醚)丙烯酸酯:
[0097]
在将实施例3所得m1a2剩余溶液冷却至室温后,加入带电动搅拌的烧瓶中,再加入 (192g,1.5mol)丙烯酸缩水甘油醚,2.67g三苯基膦,1.78g对羟基苯甲醚,缓慢升温至95℃,保温2h,再升温至105℃,在103-107℃保持2-4小时,直到该反应基本上完成,从而制备出己内酯改性木糖醇缩甲醛(环氧醚)丙烯酸酯。
[0098]
实验证明,上述丙烯酸缩水甘油醚可以采用甲基丙烯酸缩水甘油醚代替制备出性质相似的己内酯改性甲基丙烯酸酯;也可以采用三乙胺、卞基氯化铵或卞基溴化铵替代三苯基膦进行上述反应。
[0099]
下表1为产品性能测试结果,表2为产品降解测试数据;表3为产品配方后刮涂应用性能评估结果。
[0100]
表1中,酸值的测定参照hb/fg02-2009;色度的测定参照gb 9282;阻聚剂的测定参照gb/t 17530.5-1998;粘度的测定参照gb/t 5561-1994;固化速率用临界固化速率来表示,临界固化速率定义为:使漆膜表面达到完全固化时传送带的最大允许速度,也就是说,当传送带速率高于该临界固化速率值,漆膜不完全固化;当传送带速率低于该临界固化速率值,漆膜完全固化,漆膜表面达到完全固化的判别依据是通过拇指捻压和无尘纸擦拭无擦痕,涂膜厚度为12μm,固化速率具体方法参照:陈顺凉,薛永富.烷氧化双酚a二(甲基)丙烯酸酯单体的特性.中国辐射固化年会2003论文集,16-26。
[0101]
表1实施例9-13所得产品的性能评价表
[0102][0103]
注
①
:按下列比例混合后测试固化速度:脂肪族聚氨酯丙烯酸酯开磷瑞阳ry2203 30份,实施例样40份,tmpta(三羟甲基丙烷三丙烯酸酯)18份,光引发剂184 3份,bp二苯甲酮4份,引发剂活性胺(p115)5份,流平剂eterslip 0.2份,消泡剂byk-052 0.1份;
[0104]
样品降解测试:
[0105]
在水中降解(加速降解):
[0106]
将试样制成薄膜,制成1
×
1cm2大小的样品,在80℃的真空烘箱中干燥24h,取出称其质量为w0,然后将试样置于100℃的水中,每隔相同时间更换一次水,并取出一片试样,用吸水纸吸干表面水分,在80℃的真空烘箱中干燥24h,称其剩余质量w
g
。
[0107]
根据v=(w
0-w
g
)/w0*100%(*)算出失重率。
[0108]
在pbs(磷酸盐缓冲溶液)中(ph=7.4)的降解:
[0109]
常温下,高分子材料的降解很慢,而在310k的磷酸缓冲溶液中的降解常被用来评价聚乳酸等可生物降解材料在自然条件下,特别是在动物体内的降解情况。
[0110]
制样同上,在80℃的真空烘箱中干燥24h,取出称其质量w0,然后将试样置于装有 ph=7.4的磷酸盐缓冲溶液的10ml试管中,并将试管置于37度的恒温水浴中,每隔96h 更换一次水,并取出一片试样,在80℃的真空烘箱中干燥24h,取出称重w
g
,用相同方法计算失重率。
[0111]
表2实施例9-13所得产品的降解性能评价表
[0112][0113][0114]
应用实施例1
[0115]
分别将实施例9-13所得的产品30份,开磷瑞阳pea(双酚a环氧丙烯酸酯 (20%tmpta)ry1101a80)12份,聚氨酯丙烯酸酯(开磷瑞阳ry2204)18份,1,6 己二醇二丙二醇(开磷瑞阳r206)20份,三羟甲基丙烷三丙烯酸酯(开磷瑞阳tmptar302)14份,引发剂184 4份,流平剂eterslip 0.8份,消泡剂byk-052 0.2份,参照现有技术制备涂料,所述份数为质量份数,并对所得涂料性能测试,漆膜耐冲击测定参照gb 1732-1979;漆膜附着力(abs,pp,pe,pvc,pc等塑料基材)测定参照gb 1720-1979;漆膜硬度测定参照gb6739-1986;所得涂料的应用性能见表3。
[0116]
表3实施例的应用性能
[0117]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1