针对人卷曲受体的单克隆抗体及其用途
1.本发明属于生物技术领域,具体涉及靶向人卷曲受体(frizzled receptors)的单克隆抗体及其用途。
背景技术:
2.wnt信号通路是人体中极其重要的信号转导途径,wnt配体通过结合卷曲受体(frizzled receptors,fzd)来激活下游信号通路,调控胚胎发育、器官形成、干细胞干性维持等多种生物学过程。卷曲受体具有一个富含半胱氨酸的n端结构域(cysteine-rich domain,crd)和一个由七次跨膜螺旋组成的跨膜结构域。卷曲受体作为wnt信号通路的主要受体,在人体中共发现了10种(fzd1-fzd10)。根据crd区域的序列差异,可以将卷曲受体分成四个亚家族,fzd1/2/7,fzd5/8,fzd4/9/10以及fzd3/6。卷曲受体和wnt配体之间呈现出复杂的交叉结合网络,每种受体可以和多种wnt配体相互作用,同时每种wnt配体也可以结合多种卷曲受体。
3.根据已经报道的复合物晶体结构模型,wnt配体通过氨基端的“拇指”结构域和羧基端的“食指”结构域同时结合在卷曲受体crd结构域中的两个表位,分别将其命名为i类位点和ii类位点。结构和序列分析表明,i类位点相当保守,尤其是在fzd1/2/7和fzd5/8中,而ii类位点相对不保守。
4.有研究表明,wnt信号通路参与肿瘤组织的增殖、侵袭和转移,并且能够调控肿瘤血管生成。例如,fzd2受体参与多种肿瘤的上皮-间充质转化和转移。fzd7受体异常表达于三阴性乳腺癌、非小细胞肺癌、肝癌等多种类型的癌症组织中,并通过激活经典wnt信号通路来促进肿瘤细胞增殖和转移。fzd10受体在约40%的原发性胃癌,原发性结肠癌和大多数的滑膜肉瘤组织中表达显著上调。
5.鉴于失调的wnt信号通路在肿瘤发生发展过程中的重要作用,通过抑制wnt信号通路的过度激活来治疗肿瘤一直是生命科学研究的热点。目前为止,已经有多种小分子wnt信号通路抑制剂被研制并进入临床试验,如porcupine酶抑制剂lgk-974,tankyrase抑制剂e7449等。但由于小分子药物缺乏特异性,在抑制癌症组织wnt信号通路的同时也会对机体正常的信号传导产生影响,从而导致严重的毒副反应。为了提高治疗特异性,降低副作用,抗体类药物逐渐成为科研人员研发的重点。其中美国oncomed公司开发了靶向fzd7的单克隆抗体omp-18r5,该抗体正处于i期临床试验中。加拿大的sachdev sidhu课题组开发了f2.i抗体以及相关的抗体,同时解析了f2.i抗体与fzd5 crd的复合物晶体结构。值得注意的是,这类报道的抗体均结合在卷曲受体中的i类位点,能够通过拮抗wnt配体结合卷曲受体i类位点来抑制相对应的wnt信号通路。另一方面,这两种抗体均能同时结合fzd1/2/7和fzd5/8卷曲受体亚家族,这主要是由于i类位点在fzd1/2/7和fzd5/8中高度保守。
6.目前报道的抗体仍然无法满足临床或者科研需要。一方面,omp-18r5,f2.i抗体或者相关抗体均无法结合fzd10受体。虽然目前报道了其它的抗fzd10抗体,但这些抗体的结合表位未知,多数抗体通过以抗体偶联药物的形式发挥靶向作用,无法确定这些抗体是否
能够有效抑制相对应的wnt信号通路激活。另一方面,omp-18r5,f2.i抗体或者相关抗体均能同时结合fzd1/2/7和fzd5/8两个卷曲受体亚家族,因此该类抗体在治疗过程中会出现脱靶风险。若是能够筛选获得结合在特定功能表位(例如ii类位点)并具有识别特异性的抗体,则能够降低脱靶效应,增强抗肿瘤活性。同时,这种特异性抗体也可以用来探究各卷曲受体在某一生物学过程中的不同功能,有助于wnt信号通路的基础研究。
技术实现要素:
7.本发明通过一种定向表位抗体筛选方法,开发了多种结合在卷曲受体中特定功能位点,具有不同识别特异性的单克隆抗体。经过功能实验验证,这些抗体能够调控特定受体介导的wnt信号通路。
8.一方面,本发明筛选获得了结合在fzd10受体中i类位点的抗体,其能够直接调控fzd10受体介导的wnt信号通路,可以用于fzd10受体相关的肿瘤治疗。另一方面,本发明筛选获得了结合在ii类功能表位并具有识别特异性的抗体,为实现wnt信号通路的特异性调控提供工具,用于相关疾病治疗和基础研究。
9.具体来说,本发明提供了以下技术方案:
10.一方面,本发明提供了抗体或其抗原结合片段,所述抗体或其抗原结合片段结合卷曲受体,优选人卷曲受体,其中:所述抗体包含:
11.hcdr1,其包含seq id no:8、18、28、38、48、58、68所示的序列,与所述序列具有至少90%,优选至少91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的序列,或与所述序列相比具有一个或多个(优选2个或3个)保守氨基酸突变(优选置换,插入或缺失)的氨基酸序列,或由其组成,
12.hcdr2,其包含seq id no:9、19、29、39、49、59、69所示的序列,与所述序列具有至少90%,优选至少91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的序列,或与所述序列相比具有一个或多个(优选2个或3个)保守氨基酸突变(优选置换,插入或缺失)的氨基酸序列,或由其组成,和
13.hcdr3,其包含seq id no:10、20、30、40、50、60、70所示的序列,与所述序列具有至少90%,优选至少91%,92%、93%、94%、95%、96%、97%、98%或99%序列同一性的序列,或与所述序列相比具有一个或多个(优选2个或3个)保守氨基酸突变(优选置换,插入或缺失)的氨基酸序列,或由其组成,
14.lcdr1,其包含seq id no:5、15、25、35、45、55、65所示的氨基酸,或与所述序列具有至少90%,优选至少91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的序列,或与所述序列相比具有一个或多个(优选2个或3个)保守氨基酸突变(优选置换,插入或缺失)的氨基酸序列,或由其组成,
15.lcdr2,其包含seq id no:6、16、26、36、46、56、66所示的氨基酸序列,与所述序列具有至少90%,优选至少91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的序列,或与所述序列相比具有一个或多个(优选2个或3个)保守氨基酸突变(优选置换,插入或缺失)的氨基酸序列,或由其组成,和
16.lcdr3,其包含seq id no:7、17、27、37、47、57、67所示的序列,与所述序列具有至少90%,优选至少91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的序列,
或与所述序列相比具有一个或多个(优选2个或3个)保守氨基酸突变(优选置换,插入或缺失)的氨基酸序列,或由其组成。
17.在一些实施方案中,所述抗体包括:
18.(i)重链可变区,其包含下述序列或由下述序列组成:
19.seq id no:4、14、24、34、44、54、64所示的氨基酸序列,或
20.与seq id no:4、14、24、34、44、54、64所示的序列具有至少80%、85%、90%,优选至少91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的序列,或
21.与seq id no:4、14、24、34、44、54、64所示的氨基酸序列相比具有一个或多个(优选1、2、3、4、5、6、7、8、9或10个)保守氨基酸突变(优选置换,插入或缺失)的氨基酸序列,和
22.(ii)轻链可变区,其包含下述序列或由下述序列组成:
23.seq id no:3、13、23、33、43、53、63所示的氨基酸序列,或
24.与seq id no:3、13、23、33、43、53、63所示的序列具有至少80%、85%、90%,优选至少91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的序列,或
25.与seq id no:3、13、23、33、43、53、63所示的氨基酸序列相比具有一个或多个(优选1、2、3、4、5、6、7、8、9或10个)保守氨基酸突变(优选置换,插入或缺失)的氨基酸序列。
26.在一些实施方案中,所述抗体包括:
27.(i)重链,其包含下述序列或由下述序列组成:
28.seq id no:2、12、22、32、42、52、62所示的氨基酸序列,或
29.与seq id no:2、12、22、32、42、52、62所示的序列具有至少80%、85%、90%,优选至少91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的序列,或
30.与seq id no:2、12、22、32、42、52、62所示的氨基酸序列相比具有一个或多个(优选1、2、3、4、5、6、7、8、9或10个)保守氨基酸突变(优选置换,插入或缺失)的氨基酸序列,和
31.(ii)轻链,其包含下述序列或由下述序列组成:
32.seq id no:1、11、21、31、41、51、61所示的氨基酸序列,或
33.与seq id no:1、11、21、31、41、51、61所示的序列具有至少80%、85%、90%,优选至少91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的序列,或
34.与seq id no:1、11、21、31、41、51、61所示的氨基酸序列相比具有一个或多个(优选1、2、3、4、5、6、7、8、9或10个)保守氨基酸突变(优选置换,插入或缺失)的氨基酸序列。
35.进一步地,所述抗体或其抗原结合片段,其进一步包含fc结构域,优选igg1 fc结构域,更优选人igg1 fc结构域,所述人igg1 fc结构域的序列如seq id no:73所示。
36.在一些实施方案中,所述卷曲受体包括但不限于fzd1、fzd2、fzd3、fzd4、fzd5、fzd6、fzd7、fzd8、fzd9和fzd10。
37.在一些实施方案中,所述卷曲受体选自由fzd1、fzd2、fzd3、fzd4、fzd5、fzd6、fzd7、fzd8、fzd9和fzd10组成的组。
38.在一些实施方案中,所述抗体或其抗原结合片段是人源化抗体或其抗原结合片段。
39.另一方面,本发明提供多核苷酸,其编码如上所述的抗体或其抗原结合片段。
40.另一方面,本发明提供表达载体,其包含如上所述的多核苷酸。
41.另一方面,本发明提供宿主细胞,其包含如上所述的表达载体,所述宿主细胞是用
于表达外源蛋白的宿主细胞,例如细菌、酵母、昆虫细胞、哺乳动物细胞。
42.另一方面,本发明提供制备如上所述的抗体或其抗原结合片段的方法,其包括培养如上所述的宿主细胞,以及从细胞培养物中回收所述抗体或其抗原结合片段的步骤。
43.另一方面,本发明提供药物组合物,其含有如上所述的抗体或其抗原结合片段和药用载体。
44.进一步地,其中所述药物组合物为适于通过皮下注射、皮内注射、静脉内注射、肌肉注射或病灶内注射施用的形式。
45.另一方面,本发明提供如上所述的抗体或其抗原结合片段在制备预防、治疗和/或诊断与卷曲受体相关的病症的试剂盒或药物中的用途。
46.进一步地,所述与卷曲受体相关的病症选自癌症,例如乳腺癌、肺癌、肝癌、胃癌、结肠癌、滑膜肉瘤、胰腺癌、宫颈癌、口腔鳞状细胞癌、膀胱癌、血管肉瘤、前列腺癌、肾细胞癌、卵巢癌、黑色素瘤及成骨相关病症。
47.另一方面,本发明提供试剂盒,其包括如上所述的抗体或其抗原结合片段,优选地,所述抗体还包括第二抗体,其特异性识别所述抗体或其抗原结合片段,任选地,所述第二抗体包括可检测的标记,例如放射性同位素、发光物质、有色物质、酶或聚乙二醇。
48.另一方面,本发明提供多特异性抗体,优选双特异性抗体,其包含如上所述的抗体或其抗原结合片段。
49.另一方面,本发明提供融合蛋白,其包括如上所述的抗体或其抗原结合片段。
50.进一步具体地说,本发明提供了以下内容:
51.1)本发明提供了结合在fzd10中i类位点的抗体或者抗原结合片段发明人根据已经报道的f2.i结合fzd5 crd的复合物晶体结构模型(参照raman,s.,et al.(2019)."structure-guided design fine-tunes pharmacokinetics,tolerability,and antitumor profile of multispecific frizzled antibodies."),在f2.i抗体的重链的三个cdr区域和轻链的cdr-l3区域的序列中引入定向突变,构建了噬菌体展示文库。使用体外重组表达带有人igg fc融合标签的fzd10 crd抗原进行体外筛选。本发明中分离得到了3种抗体。分别命名为f10_a9、f10_e10、f10_h7。进一步地,本发明解析了f10_a9抗体结合fzd10 crd的复合物晶体结构,确定f10_a9结合在fzd10 crd中的i类位点,该位点包括两个区域,分别是第72位丙氨酸至第77位的酪氨酸(seq id no:95)以及第120位的异亮氨酸至第124位的苯丙氨酸(seq id no:96)。进一步地,本发明通过竞争性结合的方式确定了f10_e10和f10_h7的结合表位和f10_a9的结合表位重叠。具体地,与fzd10结合的抗体或其抗原结合片段具有以下特征中的任意一种:
52.(1)与抗体重链可变区(vh)的cdr1~3所示的氨基酸序列(seq id no:8~10或seq id no:18~20或seq id no:28~30),或抗体轻链可变区(vl)的cdr1~3所示的氨基酸序列(seq id no:5~7或seq id no:15~17或seq id no:25~27)的抗体竞争性结合的抗体或其抗原结合片段;
53.(2)与抗体重链可变区(vh)的cdr1~3所示的氨基酸序列(seq id no:8~10或seq id no:18~20或seq id no:28~30),或抗体轻链可变区(vl)的cdr1~3所示的氨基酸序列(seq id no:5~7或seq id no:15~17或seq id no:25~27)的抗体所结合的表位结合的抗体或其抗原结合片段;
54.(3)与抗体重链可变区(vh)的cdr1~3所示的氨基酸序列(seq id no:8~10),或抗体轻链可变区(vl)的cdr3所示的氨基酸序列(seq id no:5~7或seq id no:15~17或seq id no:25~27)的抗体所结合的表位相同的表位结合的抗体或其抗原结合片段;
55.(4)与fzd10 crd结合的抗体或其结合片段,抗体的vh的cdr1~3分别包含显示与seq id no:8~10或seq id no:18~20或seq id no:28~30所示的氨基酸序列具有90%或以上的同一性的氨基酸序列或由其组成,或抗体的vl的cdr-l3分别包含显示与seq id no:5~7或seq id no:15~17或seq id no:25~27所示的氨基酸序列具有90%或以上同一性的氨基酸序列或由其组成。
56.2)本发明提供结合在卷曲受体中ii类位点的抗体或者抗原结合片段
57.以fzd2/7受体作为研究对象,发明人根据ii类位点的结构特征,使用已经公开的hb9l9.3抗体(seq id no:105~106)为模板定向设计了噬菌体展示文库,使得该文库中展示的抗体具有结合ii类位点的潜力。同时,发明人针对fzd7 crd中的ii类位点设计了突变体蛋白,使用该突变体蛋白优化筛选流程。对噬菌体展示文库使用野生型fzd7 crd抗原联合突变体抗原进行筛选,本发明中分离得到了pf7_a5抗体,该抗体能够同时结合fzd1/2/7。进一步地,本发明中解析了pf7_a5抗体结合fzd2 crd的复合物晶体结构,确定pf7_a5结合在fzd2 crd中的ii类位点,该位点包括两个区域,分别是101位苏氨酸至108位的脯氨酸(seq id no:97)以及140位的组氨酸至152位的甘氨酸(seq id no:98)。相对应地,在fzd1受体中,该表位分别是178位苏氨酸至185位脯氨酸(seq id no:99)以及217位赖氨酸至229位甘氨酸(seq id no:100)。在fzd7受体中,该表位分别是111位苏氨酸至118位脯氨酸(seq id no:101)以及150位天冬酰胺至162位甘氨酸(seq id no:102)。
58.进一步地,本发明根据晶体结构模型进一步对pf7_a5进行了定向进化,在不改变其结合表位的前提下来提高亲和力和特异性。通过噬菌体展示筛选后获得三种改良抗体,分别是能高亲和力结合fzd1/2/7的抗体pf7_b6,特异性结合fzd2受体的抗体sf2_c11以及偏好性结合fzd7受体的抗体sf7_a2。
59.具体地,与fzd crd中ii类位点结合的抗体或其抗原结合片段具有以下特征中的任意一种:
60.(1)与抗体重链可变区(vh)的cdr1~3所示的氨基酸序列(seq id no:38~40或seq id no:48~50或seq id no:58~60或seq id no:68~70),或抗体轻链可变区(vl)的cdr1~3所示的氨基酸序列(seq id no:35~37或seq id no:45~47或seq id no:55~57或seq id no:65~67)的抗体竞争性结合的抗体或其抗原结合片段;
61.(2)与抗体重链可变区(vh)的cdr1~3所示的氨基酸序列(seq id no:38~40或seq id no:48~50或seq id no:58~60或seq id no:68~70),或抗体轻链可变区(vl)的cdr1~3所示的氨基酸序列(seq id no:35~37或seq id no:45~47或seq id no:55~57或seq id no:65~67)的抗体所结合的表位结合的抗体或其抗原结合片段;
62.(3)与抗体重链可变区(vh)的cdr1~3所示的氨基酸序列(seq id no:38~40或seq id no:48~50或seq id no:58~60或seq id no:68~70),或抗体轻链可变区(vl)的cdr1~3所示的氨基酸序列(seq id no:35~37或seq id no:45~47或seq id no:55~57或seq id no:65~67)的抗体所结合的表位相同的表位结合的抗体或其抗原结合片段。
63.(4)与fzd1或fzd2或fzd7结合的抗体或其抗原结合片段,抗体的vh的cdr1~3分别
包含显示与seq id no:38~40或seq id no:48~50或seq id no:58~60或seq id no:68~70所示的氨基酸序列具有90%或以上的同一性的氨基酸序列,或抗体的vl的cdr1~3分别包含显示与seq id no:35~37或seq id no:45~47或seq id no:55~57或seq id no:65~67所示的氨基酸序列具有90%或以上同一性的氨基酸序列;
64.(5)与fzd1或fzd2或fzd7结合的高亲和力抗体或其抗原结合片段,抗体的vh的cdr1~3分别包含显示与seq id no:48~50所示的氨基酸序列具有90%或以上的同一性的氨基酸序列,或抗体的vl的cdr1~3分别包含显示与seq id no:45~47所示的氨基酸序列具有90%或以上同一性的氨基酸序列;
65.(6)特异性与fzd2结合的抗体或其抗原结合片段,抗体的vh的cdr1~3分别包含显示与seq id no:58~60所示的氨基酸序列具有90%或以上的同一性的氨基酸序列,或抗体的vl的cdr1~3分别包含显示与seq id no:55~57所示的氨基酸序列具有90%或以上同一性的氨基酸序列;
66.(7)偏好性结合fzd7的抗体或其结合片段,抗体的vh的cdr1~3分别包含显示与seq id no:68~70所示的氨基酸序列具有90%或以上的同一性的氨基酸序列,或抗体的vl的cdr1~3分别包含显示与seq id no:65~67所示的氨基酸序列具有90%或以上同一性的氨基酸序列。
67.有益效果
68.一方面,抗fzd10抗体均能够高亲和力结合fzd10 crd抗原。采用elisa实验表明,f10_a9,f10_e10,f10_h7结合fzd10 crd抗原的ec
50
值分别为7.73
±
1.07,7.69
±
0.39,16.73
±
4.41nm(纳摩尔每升)。采用表面等离子共振(spr)实验表明,f10_a9和f10_h7结合fzd10 crd抗原的平衡解离常数(kd)分别为6.22和18.88nm。
69.进一步地,本发明的抗fzd10抗体定向结合fzd10受体中i类位点,能够直接地阻碍wnt配体结合fzd10受体,从而有效地拮抗fzd10受体介导的wnt信号通路。采用荧光素酶报告基因实验表明,f10_a9,f10_e10,f10_h7均能有效地抑制fzd10受体介导的wnt信号通路活化,ic
50
值分别为12.62
±
0.90,19.31
±
0.92,8.47
±
1.37nm。
70.另一方面,本发明中首次鉴定出结合fzd crd ii类位点的抗体。本发明中获得的ii类位点抗体及改良抗体具有高亲和力和严谨的结合特异性。其中,pf7_a5,pf7_b6能够特异性结合fzd1/2/7亚家族,不能结合fzd5/8。特别地,sf2_c11抗体单一结合fzd2受体。采用表面等离子共振(spr)实验表明,pf7_b6结合fzd1、fzd2、fzd7的平衡解离常数(kd)分别为1.56、0.55、0.18nm。fzd2受体的特异性抗体sf2_c11不结合fzd1受体,同时该抗体结合fzd2受体的亲和力(6.51nm)比结合fzd7受体的亲和力(612nm)高100倍左右,表明该抗体是fzd2受体的单一特异性抗体。
71.进一步地,本发明的卷曲受体ii类位点抗体能够有效地调控wnt信号通路。采用荧光素酶报告基因实验表明,pf7_b6能够有效地抑制fzd2或fzd7受体介导的wnt信号通路激活,但不会干扰fzd10受体介导的wnt信号通路。该抗体抑制fzd2受体和fzd7受体的ic
50
值分别为3.33
±
0.19nm和9.31
±
0.54nm。fzd2受体的特异性抗体sf2_c11能够特异性地拮抗fzd2受体介导的wnt信号通路活化,ic
50
值为13.09
±
1.17nm,但不会干扰fzd7或者fzd10受体介导的wnt信号通路。
附图说明
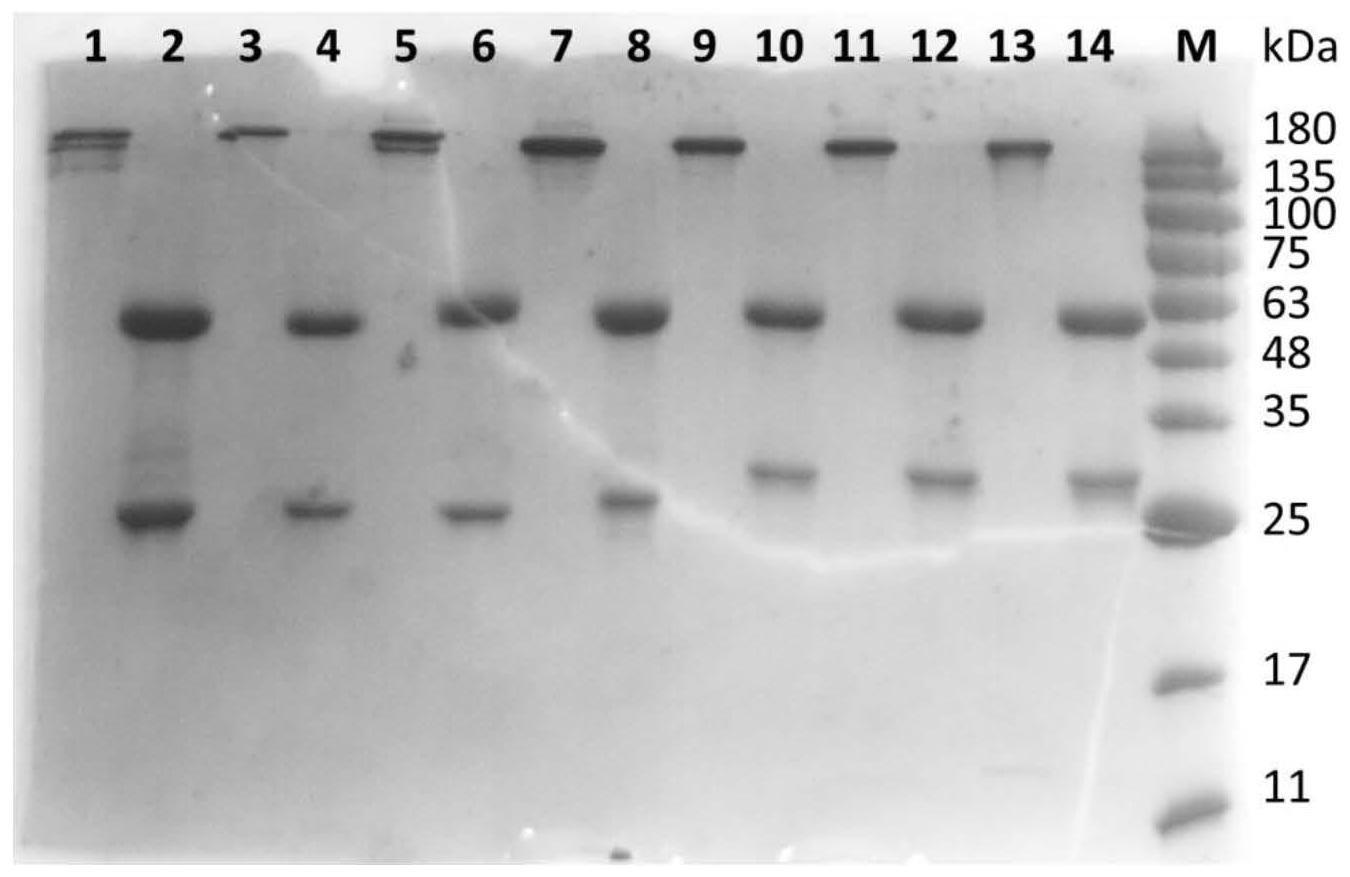
72.图1示出了本发明的抗体的sds-page凝胶电泳结果。泳道m为marker,泳道1到14依次为f10_a9抗体,还原状态下f10_a9抗体,f10_e10抗体,还原状态下f10_e10抗体,f10_h7抗体,还原状态下f10_h7抗体,pf7_a5抗体,还原状态下pf7_a5抗体,pf7_b6抗体,还原状态下pf7_b6抗体,sf2_c11抗体,还原状态下sf2_c11抗体,sf7_a2抗体,还原状态下sf7_a2抗体。
73.图2示出了抗fzd10抗体的亲和力表征结果。图a是三种抗fzd10抗体的elisa结合曲线。图b是f10_a9抗体(左)和f10_h7抗体(右)结合fzd10 crd抗原的动力学曲线。其中不同颜色的曲线代表不同抗体浓度的动力学曲线,黑色实线是采用“bivalent analyte”模型拟合后的曲线。
74.图3示出了抗fzd10抗体的表位表征结果。图a是f10_a9结合fzd10 crd的晶体结构(上),以及f10_a9抗体结合在fzd10 crd中的表位(下),表位处的氨基酸使用红色加粗标注。图b是f10_e10抗体和f10_h7抗体与f10_a9抗体的竞争性elisa结果,其中f2.i抗体是同型对照。
75.图4示出了抗fzd10抗体的功能表征结果。具体示出了f10_a9、f10_e10、f10_h7抑制fzd10介导的wnt信号通路活化的实验数据分析结果。
76.图5示出了卷曲受体ii类抗体的特异性表征结果。本发明采用elisa检测了pf7_a5抗体对多种卷曲受体的结合能力。
77.图6示出了卷曲受体ii类抗体的表位表征结果。图a是ii类位点抗体pf7_a5结合fzd2 crd的晶体结构。图b是fzd1、fzd2、fzd7受体在ii类位点处的序列比对结果。
78.图7示出了改良的卷曲受体ii类位点抗体的亲和力和特异性表征结果。图a-c分别是pf7_b6抗体的fab片段结合fzd1、fzd2、fzd7抗原的spr曲线。图d-f分别是sf2_c11抗体的fab片段结合fzd1、fzd2、fzd7抗原的spr曲线。图g-i分别是sf7_a2抗体的fab片段结合fzd1、fzd2、fzd7抗原的spr曲线。其中不同颜色的曲线代表不同抗体浓度的动力学曲线,黑色实线是采用“1:1binding”模型拟合后的曲线。
79.图8示出了改良的卷曲受体ii类位点抗体的功能表征结果。图a-c分别是pf7_b6抗体、sf2_c11抗体和sf7_a2抗体抑制fzd2、fzd7和fzd10受体介导的wnt信号通路活化的实验结果。
具体实施方式
80.为使本发明的目的、技术方案和优点更加清楚明白,以下结合具体实施例,并参照附图,对本发明作进一步的详细说明。
81.实施例1表达纯化所获得的抗体
82.1)设计引物,将抗体重链可变区的基因序列与人igg1的ch1,ch2,ch3区域(seq id no:72)融合,并在重链可变区的n端添加分泌信号肽(seq id no:71),构成重链表达载体。同时,将抗体轻链可变区的基因序列与人轻链恒定区cl融合,其中f10_a9、f10_e10、f10_h7与κ链恒定区(seq id no:74)融合,pf7_a5、pf7_b6、sf2_c11和sf7_a2与λ链恒定区(seq id no:75)融合,在轻链可变区的n端添加分泌信号肽(seq id no:71)。
83.2)将重链表达载体和轻链表达载体按照3:2的质量比,使用pei(polysciences,
inc.cat#24765)瞬时转染的方式转染至哺乳动物细胞expi293f
tm cells(thermo fisher,cat#a14527)中,培养5天后收集培养基上清,采用protein a(cytiva,cat#ge17-1279-01)柱子对上清中的抗体进行纯化,进行sds-page电泳,结果如图1所示,从上清中,我们获得了高纯度的抗体。
84.实施例2表征抗fzd10抗体的亲和力和结合表位
85.1)采用非竞争性elisa初步表征f10_a9、f10_e10和f10_h7抗体对fzd10 crd的结合能力:将带有人igg fc融合标签的fzd10 crd抗原(seq id no:84)用pbs溶液稀释至1μg/ml,按照每孔50μl的量加入到nunc maxisorb plate酶标板(thermo fisher,cat#44-2404)中,室温锚定2小时;使用封闭溶液(含有0.5%牛血清白蛋白的pbs溶液)室温封闭两小时;使用清洗溶液(含有0.05% tween-20的pbs溶液)洗三次,每次200μl,将梯度稀释的抗体溶液加入到酶标板中,每孔50μl,室温孵育一小时;使用清洗溶液洗涤四次,之后加入1:10000稀释的辣根过氧化物酶偶联的抗人ig kappa链的抗体(赫澎生物),每孔30μl,室温孵育30分钟;使用清洗溶液洗涤六次,之后每个孔加入120μl tmb溶液(碧云天),反应2分钟至10分钟,之后加入50μl硫酸溶液终止显色反应,读取每个孔在450nm处的吸光度值。结果如图2a所示,f10_a9、f10_e10和f10_h7结合fzd10 crd的ec
50
值分别为7.73
±
1.07、7.69
±
0.39和16.73
±
4.41nm。
86.2)采用spr表征f10_a9、f10_h7抗体对fzd10 crd的结合亲和力:将带有人igg fc融合标签的fzd10 crd抗原使用ph 4.5的醋酸钠溶液稀释至2μg/ml,偶联至cm5芯片的一个通道上,偶联30至100ru的抗原,同时设置一个不偶联蛋白的对照通道,采用乙醇胺封闭。将两种抗体使用缓冲液(含有0.05% tween-20的pbs溶液)进行梯度稀释,随后分别以30μl/min的速度流过以上2个通道,同时检测信号值(ru)。在一个循环完成后,采用10mm的naoh洗掉结合的抗体以再生芯片。所有操作均在biacore t200系统上完成。结果如图2b所示,采用biacore evaluation程序对结果进行分析,f10_a9和f10_h7结合fzd10 crd抗原的平衡解离常数(kd)分别为6.22和18.88nm。
87.3)采用x射线晶体衍射的方式解析f10_a9抗体结合fzd10 crd的表位:将f10_a9抗体的抗原结合片段(fab)(seq id no:91-92)表达载体与fzd10 crd抗原(seq id no:90,其中设计n48q点突变消除糖基化修饰对结晶的影响)表达载体同时转染到hek293f细胞中,其中抗体的重链片段带有组氨酸标签,便于纯化;转染5天后,收集培养基上清使用ni-nta亲和层析柱(cytiva)纯化得到抗原抗体复合物;使用superdex 200 increase 10/300层析柱(cytiva)进行精细纯化;将纯化得到的复合物浓缩至蛋白浓度大于8mg/ml,使用多种商业化晶体生长试剂盒进行筛选;根据初始出晶条件进行进一步组合优化。我们成功在0.1m hepes(ph 7.0),30% jeffamine(ph 7.0)(hampton research,hr2-597)的条件下获得了衍射分辨率为的晶体并进行了数据收集。通过分子置换解析了f10_a9-fzd10 crd复合物结构模型,确定f10_a9结合在fzd10 crd中的i类位点,该位点包括两个区域,分别是第72位丙氨酸至第77位的酪氨酸(aplvey)(seq id no:95)以及第120位的异亮氨酸至第124位的苯丙氨酸(imeqf)(seq id no:96)(图3a)。
88.4)采用竞争性elisa实验表征f10_e10和f10_h7抗体的结合表位:将带有人igg fc融合标签的fzd10 crd抗原用pbs溶液稀释至1μg/ml,按照每孔50μl的量加入到nunc maxisorb plate酶标板中,室温锚定2小时;使用封闭溶液(含有0.5%牛血清白蛋白的pbs
溶液)室温封闭两小时;使用清洗溶液(含有0.05% tween-20的pbs溶液)洗三次,每次200μl,加入50μl f10_a9噬菌体溶液,室温孵育30分钟;之后将稀释至200nm的抗体溶液(f2.i,f10_a9,f10_e10,f10_h7)(f2.i抗体的氨基酸序列如seq id no:103~104所示)加入到酶标板中,每孔50μl,室温孵育30分钟;之后加入使用清洗溶液洗涤四次,之后加入1:10000稀释的辣根过氧化物酶偶联的抗m13噬菌体的抗体(义翘神州),每孔30μl,室温孵育30分钟;使用清洗溶液洗涤六次,之后每个孔加入120μl tmb溶液(碧云天),反应2分钟至10分钟,之后加入50μl 2m硫酸溶液终止显色反应,读取每个孔在450nm处的吸光度值。结果表明,f10_e10和f10_h7抗体会抑制f10_a9噬菌体结合fzd10,这表明f10_e10和f10_h7抗体的结合表位和f10_a9的结合表位重叠或者部分重叠(图3b)。
89.实施例3表征抗fzd10抗体对wnt信号通路的调控能力
90.采用荧光素酶报告基因实验表征f10_a9、f10_e10、f10_h7抗体对wnt信号通路的调控能力。功能实验使用敲除fzd1/2/7受体的hek293t细胞系(f127-ko)(参照voloshanenko,o.,et al.(2017)."mapping of wnt-frizzled interactions by multiplex crispr targeting of receptor gene families.")作为模型细胞系。将f127-ko细胞接种到6孔板中,每孔接种1.3
×
106个细胞,培养24小时;使用polyjet
tm
转染试剂(signagen,cat#sl100688),按照标准流程进行转染,转染时细胞汇合度为70
–
90%,同时转染500ng fzd10全长表达质粒(seq id no:87),480ng tcf/lef-firefly luciferase质粒(改造自promega公司的pgl3-basic,参照tao,y.,et al.(2019)."tailored tetravalent antibodies potently and specifically activate wnt/frizzled pathways in cells,organoids and mice.")和20ng renilla luciferase质粒(promega);转染后24小时将6板中的细胞转移到96孔板中,加入40μl的mwnt3a条件培养基(参照willert,k.,et al.(2003)."wnt proteins are lipid-modified and can act as stem cell growth factors."制备)刺激wnt信号通路,同时加入梯度稀释的抗体溶液各40μl;24小时后,收集细胞使用双荧光素酶报告基因试剂盒(transgene)进行检测。结果表明,f10_a9、f10_e10和f10_h7均能有效地抑制fzd10受体介导的wnt信号通路活化,ic
50
值分别为12.62
±
0.90、19.31
±
0.92和8.47
±
1.37nm(图4)。
91.实施例4表征卷曲受体ii类位点抗体的特异性和结合表位
92.1)采用elisa表征卷曲受体ii类位点抗体pf7_a5对多种卷曲受体的结合特异性。其中,pf7_a5抗体轻链羧基端带有ha表位标签。将不同的fzd crd抗原(seq id no:76~84)用pbs溶液稀释至1μg/ml,按照每孔50μl的量加入到nunc maxisorb plate酶标板中,室温锚定2小时;使用封闭溶液(含有0.5%牛血清白蛋白的pbs溶液)室温封闭两小时;使用清洗溶液(含有0.05% tween-20的pbs溶液)洗三次,每次200μl,将稀释至10nm的pf7_a5抗体溶液加入到酶标板中,每孔50μl,室温孵育一小时;使用清洗溶液洗涤四次,之后加入1:5000稀释的辣根过氧化物酶偶联的anti-ha tag抗体(义翘神州),每孔30μl,室温孵育30分钟;使用清洗溶液洗涤六次,之后每个孔加入120μl tmb溶液(碧云天),反应2分钟至10分钟,之后加入50μl硫酸溶液终止显色反应,读取每个孔在450nm处的吸光度值。结果如图5所示,pf7_a5抗体特异性结合fzd1/2/7受体。
93.2)采用x射线晶体衍射的方式解析pf7_a5抗体结合fzd2/7 crd的表位:将pf7_a5抗体的抗原结合片段(fab)表达载体与fzd2 crd或fzd7 crd抗原表达载体(seq id no:88、
89、93、94)同时转染到hek293f细胞中;转染5天后,收集培养基上清使用ni-nta亲和层析柱(cytiva)纯化得到抗原抗体复合物;使用superdex 200increase 10/300层析柱(cytiva)进行精细纯化;将纯化得到的复合物浓缩至蛋白质浓度大于8mg/ml,使用多种商业化晶体生长试剂盒进行筛选;根据初始出晶条件进行进一步组合优化。我们成功在8% tacsimate
tm
(ph 4.0)(hampton research,hr2-823),20% peg 3350(hampton research,hr2-527)的条件下获得了衍射分辨率为的晶体并进行了数据收集。通过分子置换解析了pf7_a5-fzd2crd复合物结构模型,确定pf7_a5结合在fzd2crd中的ii类位点,该位点包括两个区域,分别是第101位苏氨酸至108位的脯氨酸(seq id no:97)以及140位的组氨酸至152位的甘氨酸(seq id no:98)。(图6a)。相对应地,在fzd1受体中,该表位分别是178位苏氨酸至186位脯氨酸(seq id no:99)以及217位赖氨酸至229位甘氨酸(seq id no:100)。在fzd7受体中,该表位分别是111位苏氨酸至118位脯氨酸(seq id no:101)以及150位天冬酰胺至162位甘氨酸(seq id no:102)(图6b)。
94.实施例5表征改良的卷曲受体ii类位点抗体的亲和力和特异性
95.采用spr表征pf7_b6、sf2_c11和sf7_a2抗体对fzd1/2/7crd的亲和力:将带有人igg fc融合标签的fzd1/2/7crd抗原(seq id no:76、77、81)使用ph 4.5的醋酸钠溶液稀释至2μg/ml,偶联至cm5芯片的一个通道上,偶联30至100ru的抗原,同时设置一个不偶联蛋白的对照通道,采用乙醇胺封闭。将三种抗体使用缓冲液(含有0.05% tween-20的pbs溶液)进行梯度稀释,随后分别以30μl/min的速度流过以上2个通道,同时检测信号值(ru)。在完成一个循环后,采用10mm的naoh溶液洗掉结合的抗体以再生芯片。所有操作均采用biacore t200系统完成。采用biacore evaluation程序对结果进行分析,亲和力和相关的动力学参数如图7所示。pf7_b6与fzd1的k
on
(m-1
×
s-1
)、k
off
(s-1
)和kd(nm)分别为2.00
×
106、3.12
×
10-3
和1.56,pf7_b6与fzd2的k
on
(m-1
×
s-1
)、k
off
(s-1
)和kd(nm)分别为3.17
×
106、1.73
×
10-3
和0.55,pf7_b6与fzd7的k
on
(m-1
×
s-1
)、k
off
(s-1
)和kd(nm)分别为4.72
×
106、8.50
×
10-4
和0.18,sf2_c11与fzd1的k
on
(m-1
×
s-1
)、k
off
(s-1
)和kd(nm)分别为n/a、n/a和n/a(说明sf2_c11不结合fzd1受体),sf2_c11与fzd2的k
on
(m-1
×
s-1
)、k
off
(s-1
)和kd(nm)分别为1.87
×
106、1.22
×
10-2
和6.51,sf2_c11与fzd7的k
on
(m-1
×
s-1
)、k
off
(s-1
)和kd(nm)分别为7.63
×
105、0.49和642,sf7_a2与fzd1的k
on
(m-1
×
s-1
)、k
off
(s-1
)和kd(nm)分别为2.22
×
106、2.11
×
10-2
和9.51,sf7_a2与fzd2的k
on
(m-1
×
s-1
)、k
off
(s-1
)和kd(nm)分别为1.36
×
106、3.20
×
10-2
和24.52,sf7_a2与fzd7的k
on
(m-1
×
s-1
)、k
off
(s-1
)和kd(nm)分别为6.55
×
106、2.65
×
10-2
和4.05。
96.实施例6表征改良的卷曲受体ii类位点抗体对wnt信号通路的调控能力
97.采用荧光素酶报告基因实验表征pf7_b6、sf2_c11和sf7_a2抗体对wnt信号通路的调控能力。将f127-ko细胞接种到6孔板中,每孔接种1.3
×
106个细胞,培养24小时;使用polyjet
tm
转染试剂,按照标准流程进行转染,转染时细胞汇合度为70
–
90%,同时转染500ng fzd2或fzd7或fzd10全长表达质粒(seq id no:85、86、87),480ng tcf/lef-firefly luciferase质粒和20ng renilla luciferase质粒;转染后24小时将6板中的细胞转移到96孔板中,加入40μl的mwnt3a条件培养基刺激wnt信号通路,同时加入梯度稀释的抗体溶液各40μl;24小时后,收集细胞使用双荧光素酶报告基因试剂盒(transgene)进行检测。结果表明,pf7_b6抗体抑制fzd2受体和fzd7受体的ic
50
值分别为3.33
±
0.19nm和9.31
±
0.54nm。
fzd2受体的特异性抗体sf2_c11能够特异性地拮抗fzd2受体介导的wnt信号通路活化,ic
50
值为13.09
±
1.17nm,但不会干扰fzd7或者fzd10受体介导的wnt信号通路。fzd7受体的偏好性抗体sf7_a2对fzd7受体具有更加显著的最大抑制效应,其对fzd7能达到96%的最大抑制效应,但对fzd2受体只能达到71%的最大抑制效应。(图8)。
98.序列
99.seq id no:1 f10_a9抗体轻链
100.diqmtqspsslsasvgdrvtitcrasqsvssavawyqqkpgkapklliysasslysgvpsrfsgsrsgtdftltisslqpedfatyycqqgwpfftfgqgtkveikrtvaapsvfifppsdsqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
101.seq id no:2 f10_a9抗体重链
102.evqlvesggglvqpggslrlscaasgfpirgssihwvrqapgkglewvaatygwpgsityadsvkgrftisadtskntaylqmnslraedtavyycarrhtyplwaldywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
103.seq id no:3 f10_a9抗体轻链可变区
104.diqmtqspsslsasvgdrvtitcrasqsvssavawyqqkpgkapklliysasslysgvpsrfsgsrsgtdftltisslqpedfatyycqqgwpfftfgqgtkveik
105.seq id no:4 f10_a9抗体重链可变区
106.evqlvesggglvqpggslrlscaasgfpirgssihwvrqapgkglewvaatygwpgsityadsvkgrftisadtskntaylqmnslraedtavyycarrhtyplwaldywgqgtlvtvss
107.seq id no:5 f10_a9抗体lcdr1
108.qsvssa
109.seq id no:6 f10_a9抗体lcdr2
110.sas
111.seq id no:7 f10_a9抗体lcdr3
112.qqgwpfft
113.seq id no:8 f10_a9抗体hcdr1
114.gfpirgss
115.seq id no:9 f10_a9抗体hcdr2
116.tygwpgsi
117.seq id no:10 f10_a9抗体hcdr3
118.arrhtyplwaldy
119.seq id no:11 f10_e10抗体轻链
120.diqmtqspsslsasvgdrvtitcrasqsvssavawyqqkpgkapklliysasslysgvpsrfsgsrsgtdftltisslqpedfatyycqqgyrpftfgqgtkveikrtvaapsvfifppsdsqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
121.seq id no:12 f10_e10抗体重链
122.evqlvesggglvqpggslrlscaasgfsipwssihwvrqapgkglewvaatyfltgsityadsvkgrftisadtskntaylqmnslraedtavyycarlhddwrsaldywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
123.seq id no:13 f10_e10抗体轻链可变区
124.diqmtqspsslsasvgdrvtitcrasqsvssavawyqqkpgkapklliysasslysgvpsrfsgsrsgtdftltisslqpedfatyycqqgyrpftfgqgtkveik
125.seq id no:14 f10_e10抗体重链可变区
126.evqlvesggglvqpggslrlscaasgfsipwssihwvrqapgkglewvaatyfltgsityadsvkgrftisadtskntaylqmnslraedtavyycarlhddwrsaldywgqgtlvtvss
127.seq id no:15 f10_e10抗体lcdr1
128.qsvssa
129.seq id no:16 f10_e10抗体lcdr2
130.sas
131.seq id no:17 f10_e10抗体lcdr3
132.qqgyrpft
133.seq id no:18 f10_e10抗体hcdr1
134.gfsipwss
135.seq id no:19 f10_e10抗体hcdr2
136.tyfltgsi
137.seq id no:20 f10_e10抗体hcdr3
138.arlhddwrsaldy
139.seq id no:21 f10_h7抗体轻链
140.diqmtqspsslsasvgdrvtitcrasqsvssavawyqqkpgkapklliysasslysgvpsrfsgsrsgtdftltisslqpedfatyycqqggyaftfgqgtkveikrtvaapsvfifppsdsqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
141.seq id no:22 f10_h7抗体重链
142.evqlvesggglvqpggslrlscaasgfnistssihwvrqapgkglewvaatyvasgsityadsvkgrftisadtskntaylqmnslraedtavyycarnhfniwlaldywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
143.seq id no:23 f10_h7抗体轻链可变区
144.diqmtqspsslsasvgdrvtitcrasqsvssavawyqqkpgkapklliysasslysgvpsrfsgsrsgtdftltisslqpedfatyycqqggyaftfgqgtkveik
145.seq id no:24 f10_h7抗体重链可变区
146.evqlvesggglvqpggslrlscaasgfnistssihwvrqapgkglewvaatyvasgsityadsvkgrftisadtskntaylqmnslraedtavyycarnhfniwlaldywgqgtlvtvss
147.seq id no:25 f10_h7抗体lcdr1
148.qsvssa
149.seq id no:26 f10_h7抗体lcdr2
150.sas
151.seq id no:27 f10_h7抗体lcdr3
152.qqggyaft
153.seq id no:28 f10_h7抗体hcdr1
154.gfnistss
155.seq id no:29 f10_h7抗体hcdr2
156.tyvasgsi
157.seq id no:30 f10_h7抗体hcdr3
158.arnhfniwlaldy
159.seq id no:31 pf7_a5抗体轻链
160.eltqppsvsvspgqtaritcsgdgsiyrvfsygwyqqkpgqapvtliylnnkrpsgiperfsgslsgstntltisgvqaedeadyycgsfgnaplafgggtkltvlgqpkaapsvtlfppsseelqankatlvclisdfypgavtvawkadsspvkagvetttpskqsnnkyaassylsltpeqwkshrsyscqvthegstvektvaptecs
161.seq id no:32 pf7_a5抗体重链
162.evqlvesggglvqpggslrlscaasgftfssfnmfwvrqapgkglewvagidddgsypnygsavkgratisrdnskntlylqmnslraedtavyycaksggwalgglitlrwidawgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
163.seq id no:33 pf7_a5抗体轻链可变区
164.eltqppsvsvspgqtaritcsgdgsiyrvfsygwyqqkpgqapvtliylnnkrpsgiperfsgslsgstntltisgvqaedeadyycgsfgnaplafgggtkltvl
165.seq id no:34 pf7_a5抗体重链可变区
166.evqlvesggglvqpggslrlscaasgftfssfnmfwvrqapgkglewvagidddgsypnygsavkgratisrdnskntlylqmnslraedtavyycaksggwalgglitlrwidawgqgtlvtvss
167.seq id no:35 pf7_a5抗体lcdr1
168.gsiyrvfs
169.seq id no:36 pf7_a5抗体lcdr2
170.lnn
171.seq id no:37 pf7_a5抗体lcdr3
172.gsfgnapla
173.seq id no:38 pf7_a5抗体hcdr1
174.gftfssfn
175.seq id no:39 pf7_a5抗体hcdr2
176.idddgsyp
177.seq id no:40 pf7_a5抗体hcdr3
178.aksggwalgglitlrwida
179.seq id no:41 pf7_b6抗体轻链
180.eltqppsvsvspgqtaritcsgdgsiyraylygwyqqkpgqapvtliylnnkrpsgiperfsgslsgstntltisgvqaedeadyycgsfgnrplafgggtkltvlgqpkaapsvtlfppsseelqankatlvclisdfypgavtvawkadsspvkagvetttpskqsnnkyaassylsltpeqwkshrsyscqvthegstvektvaptecs
181.seq id no:42 pf7_b6抗体重链
182.evqlvesggglvqpggslrlscaasgftfssfnmfwvrqapgkglewvagidddgsypnygsavkgratisrdnskntlylqmnslraedtavyycaksggwalgglitlrwidawgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
183.seq id no:43 pf7_b6抗体轻链可变区
184.eltqppsvsvspgqtaritcsgdgsiyraylygwyqqkpgqapvtliylnnkrpsgiperfsgslsgstntltisgvqaedeadyycgsfgnrplafgggtkltvl
185.seq id no:44 pf7_b6抗体重链可变区
186.evqlvesggglvqpggslrlscaasgftfssfnmfwvrqapgkglewvagidddgsypnygsavkgratisrdnskntlylqmnslraedtavyycaksggwalgglitlrwidawgqgtlvtvss
187.seq id no:45 pf7_b6抗体lcdr1
188.gsiyrayl
189.seq id no:46 pf7_b6抗体lcdr2
190.lnn
191.seq id no:47 pf7_b6抗体lcdr3
192.gsfgnrpla
193.seq id no:48 pf7_b6抗体hcdr1
194.gftfssfn
195.seq id no:49 pf7_b6抗体hcdr2
196.idddgsyp
197.seq id no:50 pf7_b6抗体hcdr3
198.aksggwalgglitlrwida
199.seq id no:51 sf2_c11抗体轻链
200.eltqppsvsvspgqtaritcsgdgsiyeaflygwyqqkpgqapvtliylnnkrpsgiperfsgslsgstntltisgvqaedeadyycgsfgnhprafgggtkltvlgqpkaapsvtlfppsseelqankatlvclisdfypgavtvawkadsspvkagvetttpskqsnnkyaassylsltpeqwkshrsyscqvthegstvektvaptecs
201.seq id no:52 sf2_c11抗体重链
202.evqlvesggglvqpggslrlscaasgftfssfnmfwvrqapgkglewvagidddgsypnygsavkgratisrdnskntlylqmnslraedtavyycaksggwalgglitlrwidawgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
203.seq id no:53 sf2_c11抗体轻链可变区
204.eltqppsvsvspgqtaritcsgdgsiyeaflygwyqqkpgqapvtliylnnkrpsgiperfsgslsgstntltisgvqaedeadyycgsfgnhprafgggtkltvl
205.seq id no:54 sf2_c11抗体重链可变区
206.evqlvesggglvqpggslrlscaasgftfssfnmfwvrqapgkglewvagidddgsypnygsavkgratisrdnskntlylqmnslraedtavyycaksggwalgglitlrwidawgqgtlvtvss
207.seq id no:55 sf2_c11抗体lcdr1
208.gsiyeafl
209.seq id no:56 sf2_c11抗体lcdr2
210.lnn
211.seq id no:57 sf2_c11抗体lcdr3
212.gsfgnhpra
213.seq id no:58 sf2_c11抗体hcdr1
214.gftfssfn
215.seq id no:59 sf2_c11抗体hcdr2
216.idddgsyp
217.seq id no:60 sf2_c11抗体hcdr3
218.aksggwalgglitlrwida
219.seq id no:61 sf7_a2抗体轻链
220.eltqppsvsvspgqtaritcsgdgsifraysygwyqqkpgqapvtliylnnkrpsgiperfsgslsgstntltisgvqaedeadyycgsfgnrplafgggtkltvlgqpkaapsvtlfppsseelqankatlvclisdfypgavtvawkadsspvkagvetttpskqsnnkyaassylsltpeqwkshrsyscqvthegstvektvaptecs
221.seq id no:62 sf7_a2抗体重链
222.evqlvesggglvqpggslrlscaasgftfssfnmfwvrqapgkglewvagidddgsypnygsavkgratisrdnskntlylqmnslraedtavyycaksggwalgglitlrwidawgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
223.seq id no:63 sf7_a2抗体轻链可变区
224.eltqppsvsvspgqtaritcsgdgsifraysygwyqqkpgqapvtliylnnkrpsgiperfsgslsgstntltisgvqaedeadyycgsfgnrplafgggtkltvl
225.seq id no:64 sf7_a2抗体重链可变区
226.evqlvesggglvqpggslrlscaasgftfssfnmfwvrqapgkglewvagidddgsypnygsavkgratisrdnskntlylqmnslraedtavyycaksggwalgglitlrwidawgqgtlvtvss
227.seq id no:65 sf7_a2抗体lcdr1
228.gsifrays
229.seq id no:66 sf7_a2抗体lcdr2
230.lnn
231.seq id no:67 sf7_a2抗体lcdr3
232.gsfgnrpla
233.seq id no:68 sf7_a2抗体hcdr1
234.gftfssfn
235.seq id no:69 sf7_a2抗体hcdr2
236.idddgsyp
237.seq id no:70 sf7_a2抗体hcdr3
238.aksggwalgglitlrwida
239.seq id no:71分泌信号肽
240.mnllliltfvaaava
241.seq id no:72人igg1 ch1-ch2-ch3序列
242.astkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
243.seq id no:73人igg1 fc序列
244.pkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
245.seq id no:74人κ链恒定区(κcl)
246.rtvaapsvfifppsdsqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
247.seq id no:75人λ链恒定区(λcl)
248.gqpkaapsvtlfppsseelqankatlvclisdfypgavtvawkadsspvkagvetttpskqsnnkyaassylsltpeqwkshrsyscqvthegstvektvaptecs
249.seq id no:76人fzd1 crd fc融合蛋白
250.mnllliltfvaaavaefqaagqgpgqgpgpgqqpppppqqqqsgqqyngergisvpdhgycqpisiplctdiaynqtimpnllghtnqedaglevhqfyplvkvqcsaelkfflcsmyapvctvleqalppcrslcerarqgceal
mnkfgfqwpdtlkcekfpvhgagelcvgqntsdkgtptpsllpefwtsnpqhediegrmdpkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgkhhhhhh
251.seq id no:77人fzd2 crd fc融合蛋白
252.mnllliltfvaaavaaqfhgekgisipdhgfcqpisiplctdiaynqtimpnllghtnqedaglevhqfyplvkvqcspelrfflcsmyapvctvleqaippcrsicerarqgcealmnkfgfqwperlrcehfprhgaeqicvgqnhsedgapalediegrmdpkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgkhhhhhh
253.seq id no:78人fzd4 crd fc融合蛋白
254.mnllliltfvaaavaeffgdeeerrcdpirismcqnlgynvtkmpnlvghelqtdaelqlttftpliqygcssqlqfflcsvyvpmctekinipigpcggmclsvkrrcepvlkefgfawpeslncskfppqndhnhmcmegpglelevlfqgpkvepkssdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
255.seq id no:79人fzd5 crd fc融合蛋白
256.mnllliltfvaaavaaskapvcqeitvpmcrgigynlthmpnqfnhdtqdeaglevhqfwplveiqcspdlrfflcsmytpiclpdyhkplppcrsvcerakagcsplmrqygfawpermscdrlpvlgrdaevlcmdynrseattapprpfpakpediegrmdpkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgkhhhhhh
257.seq id no:80人fzd6 crd fc融合蛋白
258.mnllliltfvaaavaahslftcepitvprcmkmaynmtffpnlmghydqsiaavemehflplanlecspnietflckafvptcieqihvvppcrklcekvysdckklidtfgirwpeelecdrlqycdetvpvtfdphteflgpqkkteqvediegrmdpkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgkhhhhhh
259.seq id no:81人fzd7 crd fc融合蛋白
260.mnllliltfvaaavaaqpyhgekgisvpdhgfcqpisiplctdiaynqtilpnllghtnqedaglevhqfyplvkvqcspelrfflcsmyapvctvldqaippcrslcerarqgcealmnkfgfqwperlrcenfpvhgageicvgqntsdgsggpgggptayptapylediegrmdpkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgkhhhhhh
261.seq id no:82人fzd8 crd fc融合蛋白
262.mnllliltfvaaavaaaaasakelacqeitvplckgigynytympnqfnhdtqdeaglevhqfwplveiqcspdlkfflcsmytpicledykkplppcrsvcerakagcaplmrqygfawpdrmrcdrlpeqgnpdtlcmdynrtdlttaapspprrlpppppediegrmdpkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgkhhhhhh
263.seq id no:83人fzd9 crd fc融合蛋白
264.mnllliltfvaaavaefleigrfdpergrgaapcqaveipmcrgigynltrmpnllghtsqgeaaaelaefaplvqygchshlrfflcslyapmctdqvstpipacrpmceqarlrcapimeqfnfgwpdsldcarlptrndphalcmeapenatlelevlfqgpkvepkssdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
265.seq id no:84人fzd10 crd fc融合蛋白
266.mnllliltfvaaavaaissmdmerpgdgkcqpieipmckdigynmtrmpnlmghenqreaaiqlhefaplveygchghlrfflcslyapmcteqvstpipacrvmceqarlkcspimeqfnfkwpdsldcrklpnkndpnylcmeapnngsdeptrgediegrmdpkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgkhhhhhh
267.seq id no:85人fzd2全长表达序列
268.mrprsalprlllpllllpaagpaqfhgekgisipdhgfcqpisiplctdiaynqtimpnllghtnqedaglevhqfyplvkvqcspelrfflcsmyapvctvleqaippcrsicerarqgcealmnkfgfqwperlrcehfprhgaeqicvgqnhsedgapallttapppglqpgaggtpggpggggappryatlehpfhcprvlkvpsylsykflgerdcaapceparpdgsmffsqeetrfarlwiltwsvlccastfftvttylvdmqrfryperpiiflsgcytmvsvayiagfvlqervvcnerfsedgyrtvvqgtkkegctilfmmlyffsmassiwwvilsltwflaagmkwgheaieansqyfhlaawavpavktitilamgqidgdllsgvcfvglnsldplrgfvlaplfvylfigtsfllagfvslfrirtimkhdgtkteklerlmvrigvfsvlytvpativiacyfyeqafrehwerswvsqhckslaipcpahytprmspdftvymikylmtlivgitsgfwiwsgktlhswrkfytrltnsrhgettv
269.seq id no:86人fzd7全长表达序列
270.mrdpgaaaplsslglcalvlallgalsagagaqpyhgekgisvpdhgfcqpisiplctdiaynqtilpnllghtnqedaglevhqfyplvkvqcspelrfflcsmyapvctvldqaippcrslcerarqgcealmnkfgfqwperlrcenfpvhgageicvgqntsdgsggpgggptayptapylpdlpftalppgasdgrgrpafpfscprqlkvppylgyrflgerdcgapcepgranglmyfkeeerrfarlwvgvwsvlccastlftvltylvdmrrfsyperpiiflsgcyfmvavahvagflledravcverfsddgyrtvaqgtkkegctilfmvlyffgmassiwwvilsltwflaagmkwgheaieansqyfhlaawavpavktitilamgqvdgdllsgvcyvglssvdalrgfvlaplfvylfigtsfllagfvslfrirtimkhdgtktekleklmvrigvfsvlytvpativlacyfyeqafrehwertwllqtcksyavpcppghfppmspdftvfmikylmtmivgittgfwiwsgktlqswrrfyhrlshsskgetav
271.seq id no:87人fzd10全长表达序列
272.mqrpgprlwlvlqvmgscaaissmdmerpgdgkcqpieipmckdigynmtrmpnlmghenqreaaiqlhefaplveygchghlrfflcslyapmcteqvstpipacrvmceqarlkcspimeqfnfkwpdsldcrklpnkndpnylcmeapnngsdeptrgsglfpplfrpqrphsaqehplkdggpgrggcdnpgkfhhveksascaplctpgvdvywsredkrfavvwlaiwavlcffssaftvltflidparfryperpiiflsmcycvysvgylirlfagaesiacdrdsgqlyviqeglestgctlvflvlyyfgmasslwwvvltltwflaagkkwgheaieanssyfhlaawaipavktililvmrrvagdeltgvcyvgsmdvnaltgfvliplacylvigtsfilsgfvalfhirrvmktggentdkleklmvriglfsvlytvpatcviacyfyerlnmdywkilaaqhkckmnnqtktldclmaasipaveifmvkifmllvvgitsgmwiwtsktlqswqqvcsrrlkkksrrkpasvitsggiykkaqhpqkthhgkyeipaqsptcv
273.seq id no:88人fzd2 crd表达序列
274.mnllliltfvaaavaefpdhgfcqpisiplctdiaynqtimpnllghtnqedaglevhqfyplvkvqcspelrfflcsmyapvctvleqaippcrsicerarqgcealmnkfgfqwperlrcehfprhgaeqicvgqnhsedghhhhhh
275.seq id no:89人fzd7 crd表达序列
276.mnllliltfvaaavaefpdhgfcqpisiplctdiaynqtilpnllghtnqedaglevhqfyplvkvqcspelrfflcsmyapvctvldqaippcrslcerarqgcealmnkfgfqwperlrcenfpvhgageicvgqntsdghhhhhh
277.seq id no:90人fzd10 crd表达序列(带有n48q点突变)
278.mnllliltfvaaavaefmdmerpgdgkcqpieipmckdigyqmtrmpnlmghenqreaaiqlhefaplveygchghlrfflcslyapmcteqvstpipacrvmceqarlkcspimeqfnfkwpdsldcrklpnkndpnylcmeapn
279.seq id no:91抗体f10_a9表达序列(用于制备复合物)
280.mnllliltfvaaavaevqlvesggglvqpggslrlscaasgfpirgssihwvrqapgkglewvaatygwpgsityadsvkgrftisadtskntaylqmnslraedtavyycarrhtyplwaldywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkschhhhhhhh
281.seq id no:92抗体f10_a9表达序列(用于制备复合物)
282.mnllliltfvaaavadiqmtqspsslsasvgdrvtitcrasqsvssavawyqqkpgkapklliysasslysgvpsrfsgsrsgtdftltisslqpedfatyycqqgwpfftfgqgtkveikrtvaapsvfifppsdsqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec
283.seq id no:93抗体pf7_a5表达序列(用于制备复合物)
284.mnllliltfvaaavaevqlvesggglvqpggslrlscaasgftfssfnmfwvrqapgkglewvagidddgsypnygsavkgratisrdnskntlylqmnslraedtavyycaksggwalgglitlrwidawgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepksc
285.seq id no:94抗体pf7_a5表达序列(用于制备复合物)
286.mnllliltfvaaavaeltqppsvsvspgqtaritcsgdgsiyrvfsygwyqqkpgqapvtliylnnkrpsgiperfsgslsgstntltisgvqaedeadyycgsfgnaplafgggtkltvlgqpkaapsvtlfppsseelqankatlvclisdfypgavtvawkadsspvkagvetttpskqsnnkyaassylsltpeqwkshrsyscqvthegstvektvap
tecs
287.seq id no:95抗体f10_a9结合fzd10的表位(72-77位序列)
288.aplvey
289.seq id no:96抗体f10_a9结合fzd10的表位(120-124位序列)
290.imeqf
291.seq id no:97抗体pf7_a5结合fzd2的表位(101-108位序列)
292.tvleqaip
293.seq id no:98抗体pf7_a5结合fzd2的表位(140-152位序列)
294.hfprhgaeqicvg
295.seq id no:99抗体pf7_a5结合fzd1的表位(178-185位序列)
296.tvleqalp
297.seq id no:100抗体pf7_a5结合fzd1的表位(217-229位序列)
298.kfpvhgagelcvg
299.seq id no:101抗体pf7_a5结合fzd7的表位(111-118位序列)
300.tvldqaip
301.seq id no:102抗体pf7_a5结合fzd7的表位(150-162位序列)
302.nfpvhgageicvg
303.seq id no:103抗体f2.i轻链序列
304.diqmtqspsslsasvgdrvtitcrasqsvssavawyqqkpgkapklliysasslysgvpsrfsgsrsgtdftltisslqpedfatyycqqgvylftfgqgtkveikrtvaapsvfifppsdsqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgecggs
305.seq id no:104抗体f2.i重链序列
306.evqlvesggglvqpggslrlscaasgfnihsssihwvrqapgkglewvaatyssfgsityadsvkgrftisadtskntaylqmnslraedtavyycaryhhpfgfaldywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk
307.seq id no:105抗体hb9l9.3轻链序列
308.efeltqppsvsvspgqtaritcsgdgsyagsyyygwyqqkpgqapvtliyynnkrpsgiperfsgslsgstntltisgvqaedeadyycgsadnsgaafgggtkltvlgqpkaapsvtlfppsseelqankatlvclisdfypgavtvawkadsspvkagvetttpskqsnnkyaassylsltpeqwkshrsyscqvthegstvektvaptecs
309.seq id no:106抗体hb9l9.3重链序列
310.evqlvesggglvqpggslrlscaasgftfssfnmfwvrqapgkglewvagidddgsypnygsavkgratisrdnskntlylqmnslraedtavyycaksgyggswggyiaddidawgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslsp
gk
311.以上所述的具体实施例,对本发明的目的、技术方案和有益效果进行了进一步详细说明,应理解的是,以上所述仅为本发明的具体实施例而已,并不用于限制本发明,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1