一种三氟甲硫化氮杂-8/9元环化合物的制备方法
本发明属于有机合成领域,尤其涉及一种三氟甲硫化氮杂-8/9元环化合物的制备方法。
背景技术:
1、三氟甲硫基(scf3)是一种特殊的含氟基团,由于其高电负性、亲脂性和代谢稳定性,在药物化学和材料科学中引起了广泛关注。将scf3引入有机分子将显著改善母体分子的物理、化学和生理特性。通常,agscf3参与的串联环化反应是制备多种含scf3杂环的有力策略。据我们所知,近年来在该领域已发表了50多篇文献。但研究内容主要涉及5元和6元杂环的构建,对含scf3的中环化合物的制备探索较少。
2、
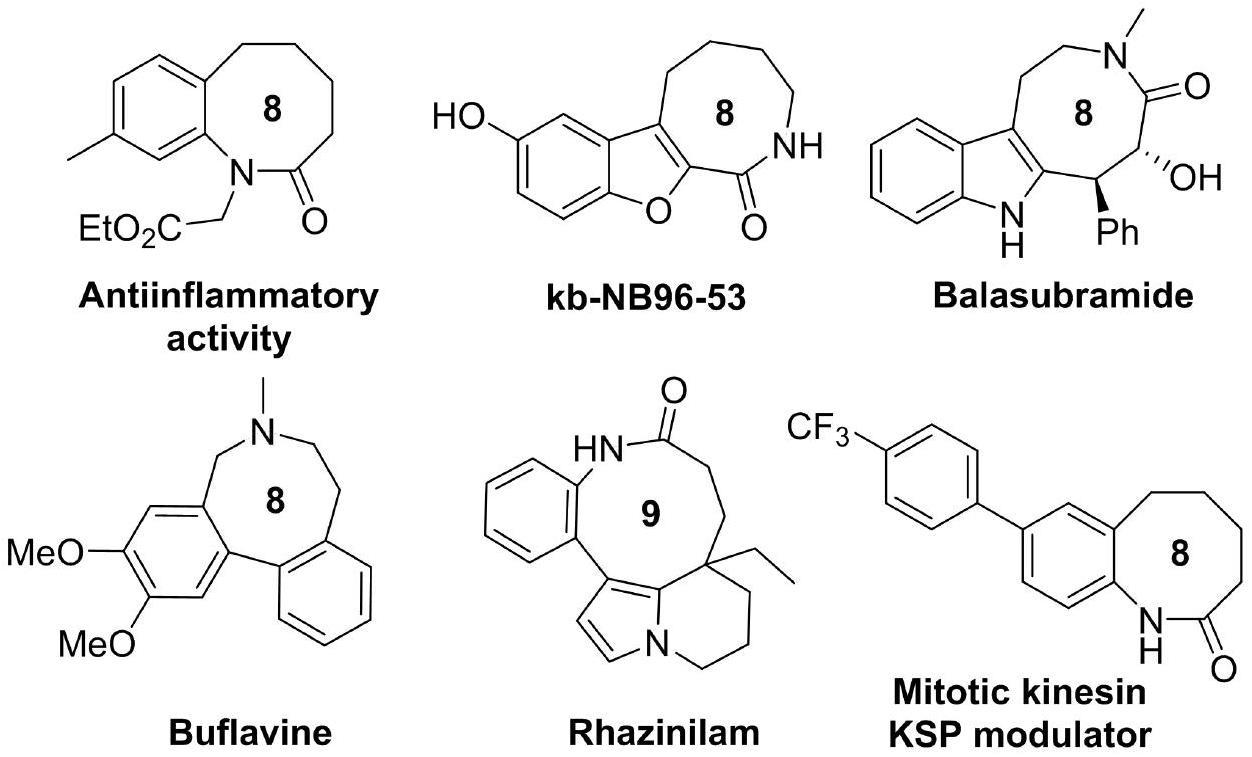
3、众所周知,中环化合物,尤其是8元和9元环化合物,在生命科学、医学、农药和材料领域具有重要意义。例如,t(+)-balasubramide具有强大的抗氧化和抗炎作用;rhazinilam可以显著抑制活化的人t细胞增殖。鉴于其丰富的应用,开发高效的三氟甲硫化中环化合物的合成方法具有重要的应用价值和前景。最近,wu和li小组独立报道使用芳基乙炔底物进行三氟甲硫化/自由基级联环化,获得含scf3的二氧二苯并噻嗪或二苯并氮嗪衍生物(chem.commun.2022,58,8674-8677;j.org.chem.2022,87,8773-8781)。但是,报道的环化反应只涵盖了7元杂环,由于反应底物局限性大,无法实现8元和9元环系分子的合成,结构类型较为单一。此外,已报道的案例采用炔基-芳基成环体系,环系需要两个芳基参与,进一步限制了该反应的底物适用性。因此,迫切需要探索普适、高效的三氟甲硫化中环分子的合成方法。
4、
技术实现思路
1、本发明的目的是提供一种简单高效的三氟甲硫化氮杂-8/9元环化合物的制备方法。
2、以可修饰的二烯底物与三氟甲烷硫醇银(agscf3)为基础原料,在过硫酸钾(k2s2o8)和六甲基磷酰三胺(hmpa)的作用下发生串联环化反应,一步得到不同取代的三氟甲硫化氮杂-8/9元环化合物。本发明的制备方法所涉及的反应过程简洁,条件温和;不需要严格的无水无氧条件,可操作性强;底物普适性高,规模化应用的潜力较高。
3、本发明的技术方案如下:
4、一种制备式(i)所示三氟甲硫化氮杂-8/9元环化合物的方法,
5、
6、其中,
7、r1选自烷基、烷氧基、卤素;
8、r2选自磺酰基;
9、r3选自芳基;
10、其中,
11、将式(ii)所示化合物(不同碳链的二烯化合物)与agscf3,在k2s2o8和hmpa的作用下,在溶剂中反应得到式(i)所示化合物:
12、
13、其中,
14、r1、r2和r3的定义同式(i)。
15、根据本发明,所述芳基可以是取代或未取代的芳基;所述芳香基可带有一个或多个取代基,对取代基的位置没有特别限制,邻位、间位、对位均可;所述取代基不以任何方式限定,常见的取代基例如烷基、烷氧基、二取代胺基、硝基、氰基、酯基、醛基、酮羰基和卤原子等;当具有多取代基时,这多个取代基可以相同或不同,相邻的两个取代基可以相互独立或成环。
16、根据本发明,所述烷基可以是取代或未取代的一级、二级或三级烷基;所述取代基不以任何方式限定,常见的取代基例如烷基、烷氧基、二取代胺基、硝基、氰基、酯基、醛基、酮羰基和卤原子等;当具有多取代基时,这多个取代基可以相同或不同,相邻或相近的两个取代基可以相互独立或成环。
17、根据本发明,所述磺酰基,硫原子可以是烷基或芳基取代。所述取代基不以任何方式限定,常见的取代基例如烷基、烷氧基、二取代胺基、硝基、氰基、酯基、醛基、酮羰基和卤原子等;当具有多取代基时,这多个取代基可以相同或不同,相邻或相近的两个取代基可以相互独立或成环。
18、根据本发明,所述烷基优选指具有1~10个碳原子的烷基,所述烷基上的取代基优选为烷氧基、硝基、氰基、酯基、醛基、酮羰基和卤原子,更优选卤原子,例如氟、氯、溴,所述烷基例如为甲基、乙基、丙基、异丙基、丁基、异丁基、叔丁基、仲丁基、戊基、新戊基、卤代c1-10烷基。
19、根据本发明,所述芳基优选为单环或双环的芳基,更优选为6-14个碳原子的芳基,例如苯基或萘基。所述芳基上的取代基优选为烷基、烷氧基、硝基、氰基、酯基、醛基、酮羰基和卤原子。
20、根据本发明,所述磺酰基优选指芳基磺酰基和烷基磺酰基,例如对甲苯磺酰基、苯磺酰基、对氯苯磺酰基、对氟苯磺酰基、邻氯苯磺酰基、间氯苯磺酰基、对甲氧基苯磺酰基、对硝基苯磺酰基、甲磺酰基、乙磺酰基、异丙基磺酰基。
21、根据本发明,所述卤原子是指氟、氯、溴或碘原子等。
22、根据本发明,所述溶剂为乙腈。
23、根据本发明,反应物优选的投料摩尔比为:
24、式(ii)化合物:agscf3=1:1~2。
25、根据本发明,所述反应的反应温度和反应时间根据不同的原料略有不同,反应温度通常为0℃至100℃,优选20℃至80℃,反应时间一般在2-24小时。若需要加热,可采用油浴(例如硅油、石蜡油等)或者其他加热方式。
26、根据本发明,所述方法还包括浓缩步骤。优选地,所述浓缩过程可采用常压蒸馏、减压蒸馏等方法。
27、根据本发明,所述方法还包括纯化步骤。优选地,所述纯化过程是通过柱层析、减压蒸馏和/或重结晶等方式得到纯净的产物。更优选地,所述纯化过程是经过柱层析后再进行减压蒸馏得到纯化后的产物。
28、本发明突出的实质性特点在于本发明采用可修饰的二烯底物与agscf3反应一步得到不同种类的三氟甲硫化氮杂-8/9元环化合物的制备方法。与前文所述方法相比,所用反应底物和生成的产物为两种截然不同的化合物。进一步分析,本发明制备路线在于二烯类化合物和agscf3,在k2s2o8和hmpa的作用下发生串联环化反应,一步得到目标产物,所用的底物可以通过延长碳链进行修饰,实现8元和9元三氟甲硫化氮杂环的合成。同时,反应制备的中环类型较为新颖,目前并未有将三氟甲硫基引入到该环系的报道。此外,本发明反应条件温和,无需严格的无水无氧条件,可操作性强,规模化应用的潜力较高。
29、本发明的方法实现了以二烯底物(式(ii)化合物)和agscf3为原料,利用k2s2o8和hmpa,在相对温和的反应条件下以较高的产率一步得到不同取代的三氟甲硫化氮杂-8/9元环化合物。
30、和现有报道相比,本发明具有下列优势:
31、1、本发明方法合成了三氟甲硫化的8或9元氮杂环分子,相比于传统5、6或7元氮杂环的合成更具挑战性和创新性。
32、2、本发明方法所涉及的底物可以修饰,通过延长烷基碳链,可选择性的进行三氟甲硫化8或9元氮杂环的合成,应用前景广泛。
33、3、本发明所涉及的反应条件相对适宜,不需要高温、不需要严格的无水无氧环境,操作非常简单;反应原子经济性高,环境友好。
34、本发明的其它特征和优点将在随后的说明书具体实施方式中阐述,并且,部分地从说明书中变得显而易见,或者通过实施本发明而了解。
- 还没有人留言评论。精彩留言会获得点赞!