一种用于组织/器官芯片集成制造的三维打印方法及装置与流程
本发明涉及三维生物打印领域,特别是关于一种用于组织/器官芯片集成制造的三维打印方法及装置。
背景技术:
细胞外微环境对组织和器官的形成、发展以及细胞行为和功能表达具有重要作用。现阶段,研究者一般通过二维单层细胞培养模型或动物模型来研究和理解人体组织生理学和病理学。由于二维单层细胞培养模型缺乏细胞与细胞间以及细胞与基质间的交互作用,而动物模型的免疫系统与细胞微环境均有别于人体,因此,两者均不能准确地表达人体内微环境的特征。目前,现有的三维模型(例如细胞支架)等基于生物胶的培养系统也难以模拟人体内组织复杂的生理结构和功能(包括组织与组织间的界面,氧气和营养的时空梯度,动态的力学性能等)。因此,二维单层细胞培养模型、动物模型和三维模型在进行生理研究和药物测试时,存在准确性差和研究周期长等问题,难以满足研究要求。因此,构建更为仿生的三维体外生物学模型已成为急需解决的问题。器官芯片是一种具有多通道的三维微流控细胞培养芯片,通过模拟完整器官的微结构、动态力学性能、生化功能以及生理响应等,实现在一个特定环境下生理学、病理学和药物测试的研究。器官芯片的技术优势主要来源于微流控技术的使用,微流控技术是指在微流道(1~1000μm)内操控微量流体(10-9~10-18L)的技术,流体流动在微流道内是层流,传质主要通过扩散来实现,基本不存在对流现象。并且粘性力起主导作用,惯性力几乎可以忽略等。利用微流体技术的这些特性,可以精确控制在微腔道内产生药物或生长因子等所需的时空梯度,并且可以实现在微观尺度可控的、动态的传递营养和化学物质到细胞或组织所在位置;同时,微流道的尺度也与人体内微血管尺度相近,因此,基于微流控技术的三维体外生物学模型(器官芯片)可以更好地模拟体内细胞微环境,具有更接近人体复杂器官的响应能力。现阶段,研究者主要采用软光刻技术制造器官芯片,该技术难以实现具有复杂三维结构的器官芯片的制造,且该技术依赖掩膜,掩膜的制造成本高,加工周期长,进而降低了系统柔性。目前无掩膜的器官芯片制造技术包括立体光刻技术、DMD(数字微镜元件)技术、PrintandPeel技术(打印和剥离技术)等,这些技术不仅难以实现复杂多层结构的器官芯片制造,而且难以实现器官芯片内细胞的可控空间分布,且细胞外基质的材料种类单一。
技术实现要素:
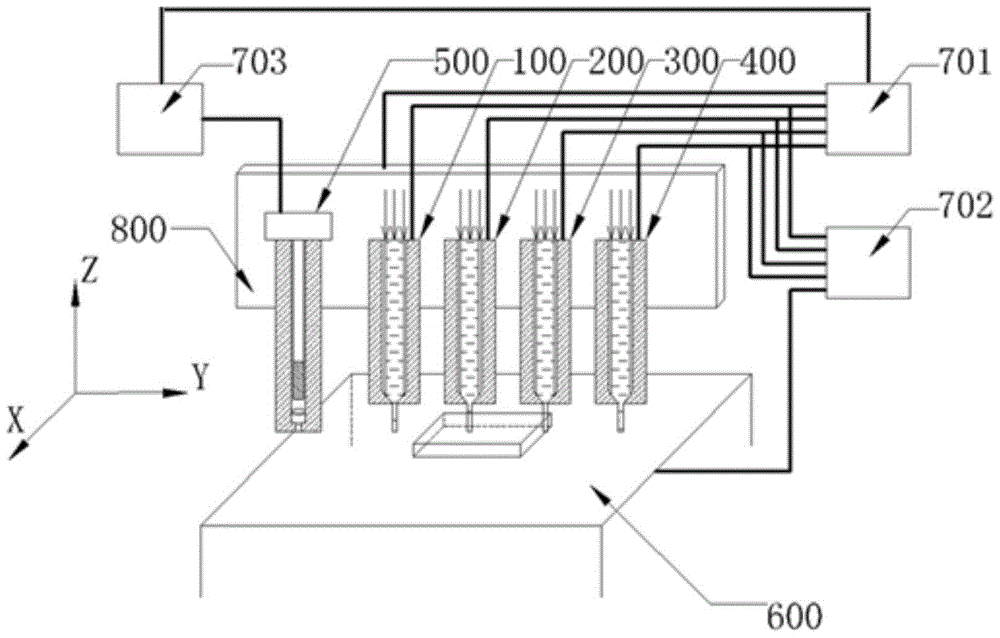
针对上述问题,本发明的目的是提供一种能够直接进行细胞打印实现复杂多层结构的器官芯片制造的用于组织/器官芯片集成制造的三维打印方法及装置。为实现上述目的,本发明采取以下技术方案:一种用于组织/器官芯片集成制造的三维打印方法,包括以下步骤:1)采用三维制图软件设计三维芯片的三维结构图,并采用分层方法将三维芯片的三维结构图转化为可以被三维打印装置识别的片层图形文件;2)首先,开启三维打印装置,并将主体材料打印墨水、牺牲材料打印墨水和多种细胞打印墨水分别吸入主体材料打印喷头、牺牲材料打印喷头和多细胞打印喷头中;然后,将步骤1)中所得到的片层图形文件导入三维打印装置;其中,主体材料打印墨水、牺牲材料打印墨水和多种细胞打印墨水均为生物材料,牺牲材料打印墨水为温敏可逆的高分子生物材料;3)三维打印装置根据片层图形文件分别通过主体材料打印喷头、牺牲材料打印喷头和多细胞打印喷头将主体材料打印墨水、牺牲材料打印墨水和不同的细胞打印墨水打印到底板系统预先设计的位置;主体材料打印墨水在底板系统形成凝胶,形成第一层三维芯片主体材料,牺牲材料打印墨水在底板系统形成通道凝胶,进而形成第一层的通道牺牲材料,不同的细胞墨水材料形成第一层多种细胞材料;4)重复步骤3)逐层累积完成三维芯片结构打印,直至片层图形文件打印完成,即三维芯片的整体打印完成;5)加热或制冷整体打印完成的三维芯片,使通道牺牲材料变为溶胶态;6)将变为溶胶态的通道牺牲材料使用移液枪吸出,去除通道牺牲材料,得到三维芯片内的通道,形成完整的三维芯片结构;7)针对不同的细胞打印墨水材料采用不同的交联方式对未被融化的细胞打印墨水材料进行交联,交联完成后在三维芯片通道中灌流培养基,对三维芯片内的细胞或组织进行长期动态培养。所述步骤3)结束后,采用紫外光源发射紫外光局部照射第一层三维芯片主体材料,使第一层三维芯片主体材料局部交联固化形成稳定不可逆的凝胶状态。所述步骤4)结束后,采用紫外光源发射紫外光照射整体打印结束后的三维芯片,透明的主体材料受紫外光照射交联固化形成稳定不可逆的凝胶状态。所述主体材料采用明胶-甲基丙烯酸。所述牺牲材料采用明胶、普朗尼克F-127和琼脂材料中的一种或多种。所述细胞打印墨水材料为细胞相容性和生物相容性好的温敏材料和/或其他生物材料的混合液;其中,生物材料采用一种或更多种天然生物材料和/或人工合成生物材料;天然生物材料采用明胶、明胶衍生物、藻酸盐、藻酸盐衍生物、琼脂、基质胶、胶原、蛋白多糖、糖蛋白、透明质酸、壳聚糖、层连接蛋白、纤连接蛋白和纤维蛋白中的至少一种;人工合成生物材料采用聚丙烯、聚苯乙烯、聚丙烯酰胺、聚丙交酯、聚乙交酯、聚乳酸、聚乳酸-羟基乙酸共聚物、聚羟基酸、聚乳酸醇酸共聚物、聚二甲基硅氧烷、聚酸酐、聚酸酯、聚酰胺、聚氨基酸、聚缩醛、聚氰基丙烯酸酯、聚氨基甲酸酯、聚吡咯、聚酯、聚甲基丙烯酸酯、聚乙烯、聚碳酸酯和聚氧化乙烯中的至少一种。一种用于组织/器官芯片集成制造的三维打印装置,其特征在于:包括三维运动系统、喷头系统、底板系统、数控系统、温控系统和紫外光源;所述喷头系统和/或所述底板系统在所述三维运动系统的带动下实现三维运动;所述数控系统分别电连接所述三维运动系统、喷头系统和紫外光源,所述数控系统将三维运动参数发送给所述三维运动系统,所述三维运动系统根据接收的三维运动参数进行三维运动;所述数控系统将喷射参数发送给所述喷头系统,所述喷头系统根据接收到的喷射参数喷射喷头内部的打印材料;所述数控系统将紫外光源参数发送给所述紫外光源,所述紫外光源根据接收到的紫外光源参数产生特定紫外功率大小和紫外光照射时间的紫外线;所述喷头系统和所述底板系统实时采集所述喷头系统和所述底板系统的温度值,并将采集的温度值发送给所述温控系统,所述温控系统根据接收到的所述喷头系统和所述底板系统的温度值,控制所述喷头系统和所述底板系统内的加热/制冷元件进行加热或者制冷,使所述喷头系统和所述底板系统的温度在设定的温度范围内。所述喷头系统包括一主体材料打印喷头、一牺牲材料打印喷头、若干细胞打印喷头和一紫外光照射探头;所述主体材料打印喷头、牺牲材料打印喷头、和细胞打印喷头用于打印墨水材料,所述紫外光照射探头用于调节紫外光照射光斑的大小,实现墨水材料的局部交联;各个打印喷头均采用一材料输送单元组成;所述材料输送单元包括一输送装置、一贯穿式螺杆、一滑块、一直线导轨、一注射器和一温度控制单元;所述输送装置、直线导轨和温度控制单元,按自上而下的顺序通过螺栓固定设置在一背板上,所述滑块滑动插设在所述直线导轨上,所述贯穿式螺杆通过螺纹贯穿连接所述输送装置,所述注射器与所述温度控制单元紧密接触;所述输送装置根据所述数控系统发送的喷射参数控制所述贯穿式螺杆做直线运动,从而推动安装在所述直线导轨上的所述滑块运动,进而推动所述注射器的运动,实现所述注射器内打印墨水的打印;所述温度控制单元用于采集所述注射器内的温度,并将采集的温度值发送给所述温控系统,所述温控系统根据接收到温度值控制所述温度控制单元对所述注射器内的打印墨水进行加热或者制冷,从而控制打印材料的温度。所述驱动装置的驱动方式采用气动、螺杆驱动、电机驱动、压电陶瓷驱动、喷墨打印驱动和激光驱动中的一种或多种组合。所述滑块安装力学传感器,用于实时采集打印过程中所述滑块推挤所述注射器所用力的大小,并将采集的值发送给所述数控系统,使所述数控系统实时监测打印过程中所述注射器的受力状态。所述温度控制单元包括一保温套筒、一导热套筒、一喷头系统温度传感器、一喷头系统半导体制冷片、一喷头系统隔热垫、一喷头系统水冷元件、一喷头系统进水管和一喷头系统出水管;所述保温套筒包裹在所述导热套筒的外部,所述注射器放置在所述导热套筒内,所述注射器与所述导热套筒紧密接触;所述喷头系统温度传感器焊接在所述导热套筒内,所述导热套筒的一侧通过导热硅胶粘连所述喷头系统半导体制冷片的一侧,所述喷头系统半导体制冷片的另一侧通过导热硅胶粘连所述喷头系统水冷元件,所述喷头系统水冷元件用于协助所述喷头系统半导体制冷片的散热;所述喷头系统水冷元件上设置有所述喷头系统进水管和所述喷头系统出水管,所述喷头系统进水管和所述喷头系统出水管连接外部的散热装置;所述保温套筒和所述喷头系统水冷元件之间通过胶粘连有所述喷头系统隔热垫;焊接在所述导热套筒内的所述喷头系统温度传感器检测到各个所述注射器内的温度后,将检测到的温度值发送给所述温控系统;所述温控系统根据接收的温度值控制所述喷头系统半导体制冷片正负电极的正接或反接,从而实现制冷或加热,热量或冷量通过所述导热套筒传递给所述注射器内被打印的材料;所述喷头系统隔热垫与所述喷头系统水冷元件及所述保温套筒通过胶粘连,用于隔住所述喷头系统半导体制冷片两端的热量交换;所述喷头系统水冷元件与所述喷头系统半导体制冷片通过导热硅胶粘连,用于协助所述喷头系统半导体制冷片另一端的散热,维持整个喷头温度稳定;所述喷头系统进水管和所述喷头系统出水管连接外部的散热装置。所述紫外光照射探头包括一紫外光纤导管固定套筒、一聚焦透镜和一紫外光纤导管;所述紫外光纤导管固定在所述紫外光纤导管固定套筒内,所述紫外光纤导管固定套筒底端设置有一通光孔,所述聚焦透镜设置在所述通光孔与所述紫外光纤导管之间,所述紫外光纤导管通过光纤与所述紫外光源连接,所述紫外光源发射紫外光后经所述紫外光纤导管到达所述聚焦透镜,紫外光经所述聚焦透镜形成光斑,通过调节所述聚焦透镜到所述底板系统的距离,从而调节紫外光的照射光斑大小。所述底板系统包括一金属底板、一底板系统温度传感器、一底板系统隔热垫、一底板系统半导体制冷片、一底板系统水冷元件、一底板系统进水管和一底板系统出水管;所述底板系统温度传感器焊接在所述金属底板内,所述金属底板的底部通过导热硅胶粘连所述底板系统半导体制冷片的顶部,所述底板系统半导体制冷片的底部通过导热硅胶粘连所述底板系统水冷元件,所述底板系统水冷元件上设置有所述底板系统进水管和所述底板系统出水管,所述底板系统进水管和所述底板系统出水管连接外部的散热装置;所述金属底板与所述底板系统水冷元件之间通过胶粘连有所述底板系统隔热垫;焊接在所述金属底板内的所述底板系统温度传感器实时采集所述金属底板的温度,并将采集的温度值发送给所述温控系统,所述温控系统根据接收到的温度值,控制所述底板系统半导体制冷片正负电极的正接或反接,从而实现所述底板系统半导体制冷片的制冷或加热,从而使所述底板系统的温度在设定的温度范围内。本发明由于采取以上技术方案,其具有以下优点:1、本发明主体材料打印喷头、牺牲材料打印喷头和多细胞打印喷头,将三维芯片主体和三维芯片内细胞直接进行三维打印,直接组装细胞和细胞外基质形成有特定空间位置排列的三维体外组织模型,可以在芯片内部实现多种细胞的特定空间排列,形成异质组织芯片(细胞共培养),突破传统芯片制造方法多种细胞排列困难的限制,因此工序简单,有利于构建更为复杂的形状。2、本发明由于基于温敏材料的变温进行打印,所有生物相容性好的温敏水凝胶均可作为细胞打印墨水,而不具备温敏特性的水凝胶可以通过修饰改性或与温敏水凝胶混合获得温敏特性,因此本发明的细胞打印墨水的具有多样性,对生物学的三维模型研究具有重要帮助。3、本发明包括紫外光照射探头,通过特殊的紫外光探头设计,控制紫外光的照射光斑大小,实现芯片主体材料的局部固化,减少整体紫外光固化对细胞的损伤;同时通过紫外光功率强度和照射时间的调控,实现控制芯片内局部材料的刚度,有利于生物学的研究。4、本发明的打印装置采用半导体制冷方式,与以往冰箱式打印机相比,大大减小了设备体积,可以使设备置于生物洁净台内使;此外,半导体制冷片的冷却方式采用水冷,而不是风冷,避免了风冷空气流动对洁净台内空气层流的扰动,降低了细菌污染的可能性。5、本发明由于加热/制冷元件仅采用单一的半导体制冷片,通过温控系统内控制电路的优化设计,实现了半导体制冷片的正负极的正接/反接,使得单一的半导体制冷片具备加热和制冷的双功能,因此可以有效的减小了设备体积和复杂性。综上所述,本发明提出的三维打印方法及装置,可以用于在芯片上构建三维体外生物学模型,并进行生理学、病理学的分析与研究,以及体外药物测试,试剂或环境的生物毒性评估等,可以应用在三维细胞/组织/器官/肿瘤芯片的集成制造与测试领域。若采用生物相容性和降解性好的芯片主体材料,也可以应用在具有微血管的组织构建,研究体内组织修复的组织工程领域。附图说明图1是本发明三维打印方法的流程示意图;图2是本发明三维打印装置的结构示意图;图3是本发明材料输送单元的结构示意图;图4是本发明喷头系统温度控制单元的结构示意图;图5是本发明紫外光照射探头的结构示意图;图6是本发明底板系统的结构示意图;图7是本发明外接水冷单元的结构示意图;图8是本发明实施例三维打印方法的流程示意图。具体实施方式下面结合附图和实施例对本发明进行详细的描述。如图1所示,本发明的用于组织/器官芯片集成制造的三维打印方法,包括以下步骤:1)采用现有的三维制图软件(例如Solidworks,但是不限于此)设计三维芯片的三维结构图,并将设计完成的三维结构图保存为STL格式,但不限于此;并采用现有的分层方法将三维芯片的三维结构图转化为可以被三维打印装置识别的片层图形文件,片层图形文件可以采用cli格式,但不限于此;2)首先,开启三维打印装置,并将主体材料打印墨水、牺牲材料打印墨水和多种细胞打印墨水分别吸入主体材料打印喷头、牺牲材料打印喷头和多细胞打印喷头中;然后,将步骤1)中所得到的片层图形文件导入三维打印装置;其中,主体材料打印墨水、牺牲材料打印墨水和多种细胞打印墨水均为生物材料,牺牲材料打印墨水为温敏可逆的高分子生物材料;3)三维打印装置根据片层图形文件分别通过主体材料打印喷头、牺牲材料打印喷头和多细胞打印喷头将主体材料打印墨水、牺牲材料打印墨水和不同的细胞打印墨水打印到底板系统预先设计的位置;主体材料打印墨水在底板系统形成凝胶,形成第一层三维芯片主体材料,牺牲材料打印墨水在底板系统形成通道凝胶,进而形成第一层的通道牺牲材料,不同的细胞墨水材料形成第一层多种细胞材料;4)采用紫外光源局部照射第一层三维芯片主体材料,使第一层三维芯片主体材料局部交联固化形成稳定不可逆的凝胶状态,此时第一层三维芯片结构打印完成;5)重复步骤3)~4)逐层累积完成三维芯片结构打印,直至片层图形文件打印完成,即三维芯片的整体打印完成;6)加热或制冷整体打印完成的三维芯片,由于牺牲材料打印墨水为温敏可逆材料,加热或制冷过程中通道牺牲材料变为溶胶态;7)将变为溶胶态的通道牺牲材料使用移液枪吸出,去除通道牺牲材料,得到三维芯片内的通道,由于三维芯片主体材料和细胞打印墨水材料仍为凝胶态而会被保留,形成完整的三维芯片结构;8)针对不同的细胞打印墨水材料采用不同的交联方式对未被融化的细胞打印墨水进行交联,交联完成后在三维芯片通道中灌流培养基,对三维芯片的细胞或组织进行长期动态培养。在一个优选的实施例中,所述步骤2)中的打印装置在使用时,可以根据实际需要分别设置三维打印装置的底板系统、主体材料打印喷头、牺牲材料打印喷头和多细胞打印喷头的温度。此外,所述步骤4)中紫外光源发射紫外光照射三维芯片主体材料,使三维芯片主体材料交联固化的过程,可以在三维芯片打印结束后进行;即紫外光源发射紫外光照射整体打印结束后的三维芯片,透明的主体材料受紫外光照射交联固化形成稳定不可逆的凝胶状态。在一个优选的实施例中,三维芯片的主体材料为可以被紫外光聚合的高分子生物温敏材料,可以采用明胶-甲基丙烯酸(GelMA)。在一个优选的实施例中,三维芯片的牺牲材料可以采用明胶、普朗尼克F-127(PluronicF-127)和琼脂等材料中的一种或多种。在一个优选的实施例中,细胞打印墨水材料为细胞相容性和生物相容性好的温敏材料和/或其他生物材料的混合液;其中,生物材料可以采用一种或更多种天然生物材料和/或人工合成生物材料;天然生物材料可以采用明胶、明胶衍生物、藻酸盐、藻酸盐衍生物、琼脂、基质胶、胶原、蛋白多糖、糖蛋白、透明质酸、壳聚糖、层连接蛋白、纤连接蛋白和纤维蛋白中的至少一种;人工合成生物材料可以采用聚丙烯、聚苯乙烯、聚丙烯酰胺、聚丙交酯、聚乙交酯、聚乳酸、聚乳酸-羟基乙酸共聚物、聚羟基酸、聚乳酸醇酸共聚物、聚二甲基硅氧烷、聚酸酐、聚酸酯、聚酰胺、聚氨基酸、聚缩醛、聚氰基丙烯酸酯、聚氨基甲酸酯、聚吡咯、聚酯、聚甲基丙烯酸酯、聚乙烯、聚碳酸酯和聚氧化乙烯中的至少一种。在一个优选的实施例中,培养基为适合一种或多种细胞生长的培养基。如图2所示,实现上述三维打印方法的用于组织/器官芯片集成制造的三维打印装置,包括三维运动系统800、喷头系统、底板系统600、数控系统701、温控系统702和紫外光源703;喷头系统和/或底板系统600在三维运动系统800的带动下实现三维运动;数控系统701分别电连接三维运动系统800、喷头系统和紫外光源703,数控系统701将三维运动参数发送给三维运动系统800,三维运动系统800根据接收的三维运动参数进行三维运动;数控系统701将喷射参数发送给喷头系统,喷头系统根据接收到的喷射参数喷射喷头内部的打印材料;数控系统701将紫外光源参数发送给紫外光源703,紫外光源703根据接收到的紫外光源参数产生特定紫外功率大小和紫外光照射时间的紫外线;喷头系统和底板系统600实时采集喷头系统和底板系统600的温度值,并将采集的温度值发送给温控系统702,温控系统702根据接收到的喷头系统和底板系统600的温度值,控制喷头系统和底板系统600内的加热/制冷元件进行加热或者制冷,使喷头系统和底板系统600的温度在设定的温度范围内;其中,三维运动参数包括运动速度、运动加速度、运动距离和运动时间中的一种或多种;喷射参数包括喷射速度、喷射力大小、喷射时间、喷射加速度和喷射材料体积;紫外光源参数包括紫外功率大小和紫外光照射时间。在一个优选的实施例中,喷头系统和底板系统600均安装在三维运动系统800上,在三维运动系统800的带动下实现三维运动。在一个优选的实施例中,喷头系统安装在三维运动系统800上,并随三维运动系统800的运动实现空间的三维运动,而底板系统固定安装在一个独立于三维运动系统800的支架上,不随三维运动系统800的运动而运动。在一个优选的实施例中,底板系统安装在三维运动系统800上,并随三维运动系统800的运动实现空间的三维运动,而喷头系统固定安装在一个独立于三维运动系统800的支架上,不随三维运动系统800的运动而运动。在一个优选的实施例中,喷头系统包括一主体材料打印喷头100、一牺牲材料打印喷头200、若干细胞打印喷头和一紫外光照射探头500;本实施例中包括第一细胞打印喷头300和一第二细胞打印喷头400两个细胞打印喷头;主体材料打印喷头100、牺牲材料打印喷头200、第一细胞打印喷头300和第二细胞打印喷头400用于打印墨水材料,紫外光照射探头500用于调节紫外光照射光斑的大小,实现墨水材料的局部交联。如图3所示,各个打印喷头均采用一材料输送单元组成,材料输送单元用于实现打印墨水的打印,其输送方式通过步进电机推挤注射器实现,但是不限于此,还可以采用气动、螺杆驱动、压电陶瓷驱动、喷墨打印驱动和激光驱动中的一种或多种组合的输送方式;下面以步进电机具体进行说明:材料输送单元包括一步进电机2001、一贯穿式螺杆2002、一滑块2003、一直线导轨(未标出)、一注射器2004和一温度控制单元2005;步进电机2001、直线导轨和温度控制单元2005,按自上而下的顺序通过螺栓固定设置在一背板2000上,滑块2003滑动插设在直线导轨上,贯穿式螺杆2002通过螺纹贯穿连接步进电机2001,注射器2004与温度控制单元2005紧密接触,实现良好的温度传递;步进电机2001根据数控系统701发送的喷射参数控制贯穿式螺杆2002做直线运动,从而推动安装在直线导轨上的滑块2003运动,进而推动注射器2004的运动,实现注射器2004内打印墨水的打印;温度控制单元2005用于采集注射器2004内的温度,并将采集的温度值发送给温控系统702,温控系统702根据接收到温度值控制温度控制单元2005对注射器2004内的打印墨水进行加热或者制冷,从而控制打印材料的温度。在一个优选的实施例中,滑块2003可以安装力学传感器,用于实时采集打印过程中滑块2003推挤注射器2004所用力的大小,并将采集的值发送给数控系统701,使数控系统701实时监测打印过程中注射器2004的受力状态。在一个优选的实施例中,如图4所示,温度控制单元2005包括一保温套筒1001、一导热套筒1002、一喷头系统温度传感器(未标出)、一喷头系统半导体制冷片1003、一喷头系统隔热垫1004、一喷头系统水冷元件1005、一喷头系统进水管1006和一喷头系统出水管1007;保温套筒1001包裹在导热套筒1002的外部,用于减小导热套筒1002的热量损失,注射器2004放置在导热套筒1002内,注射器2004与导热套筒1002紧密接触,实现良好的温度传递;喷头系统温度传感器焊接在导热套筒1002内,导热套筒1002的一侧通过导热硅胶粘连喷头系统半导体制冷片1003的一侧,喷头系统半导体制冷片1003的另一侧通过导热硅胶粘连喷头系统水冷元件1005,喷头系统水冷元件1005用于协助喷头系统半导体制冷片1003的散热,维持整个喷头温度稳定;喷头系统水冷元件1005上设置有喷头系统进水管1006和喷头系统出水管1007,喷头系统进水管1006和喷头系统出水管1007连接外部的散热装置;保温套筒1001和喷头系统水冷元件1005之间通过胶粘连有喷头系统隔热垫1004,喷头系统隔热垫1004用于隔住喷头系统半导体制冷片1003两端的热量交换;焊接在导热套筒1002内的喷头系统温度传感器检测到各个注射器2004内的温度后,将检测到的温度值发送给温控系统702;温控系统702根据接收的温度值控制喷头系统半导体制冷片1003正负电极的正接或反接,从而实现制冷或加热,热量或冷量通过导热套筒1002传递给注射器2004内被打印的材料;在一个优选的实施例中,保温套筒1001的材料可以采用气凝胶,导热套筒1002的材料可以采用紫铜,喷头系统隔热垫1004可以采用海绵;喷头系统水冷元件1005可以采用紫铜的水冷头;喷头系统进水管1006和喷头系统出水管1007可以采用硅胶管;在一个优选的实施例中,如图5所示,紫外光照射探头500包括一紫外光纤导管固定套筒5001、一聚焦透镜5002和一紫外光纤导管5003;紫外光纤导管5003固定在紫外光纤导管固定套筒5001内,紫外光纤导管固定套筒5001底端设置有一通光孔,聚焦透镜5002设置在通光孔与紫外光纤导管5003之间,紫外光纤导管5003通过光纤与紫外光源703连接,紫外光源703发射紫外光后经紫外光纤导管5003到达聚焦透镜5002,紫外光经聚焦透镜5002形成光斑,通过调节聚焦透镜5002到底板系统600的距离,从而调节紫外光的照射光斑大小,即当聚焦透镜5002离成形三维芯片位置远时,光线散焦,光斑直径更大;当聚焦透镜离成形三维芯片位置近时,光线聚焦,光斑直径更小;其中,紫外光的功率强度和照射时间可由紫外光源703调控。在一个优选的实施例中,如图6所示,底板系统600用于对打印的三维芯片进行制冷或加热,它包括一金属底板6001、一底板系统温度传感器(未标出)、一底板系统隔热垫6002、一底板系统半导体制冷片6003、一底板系统水冷元件6004、一底板系统进水管6005和一底板系统出水管6006;底板系统温度传感器焊接在金属底板6001内,金属底板6001的底部通过导热硅胶粘连底板系统半导体制冷片6003的顶部,底板系统半导体制冷片6003的底部通过导热硅胶粘连底板系统水冷元件6004,底板系统水冷元件6004上设置有底板系统进水管6005和底板系统出水管6006,底板系统进水管6005和底板系统出水管6006连接外部的散热装置;金属底板6001与底板系统水冷元件6004之间通过胶粘连有底板系统隔热垫6002;焊接在金属底板6001内的底板系统温度传感器实时采集金属底板6001的温度,并将采集的温度值发送给温控系统702,温控系统702根据接收到的温度值,控制底板系统半导体制冷片6003正负电极的正接或反接,从而实现底板系统半导体制冷片6003的制冷或加热,从而使底板系统600的温度在设定的温度范围内;其中,底板系统隔热垫6002可以采用海绵。底板系统水冷元件6004可以采用紫铜的水冷头。底板系统进水管6005和底板系统出水管6006可以采用硅胶管。金属底板6001可以采用铝合金底板;底板系统隔热垫6002可以采用海绵。底板系统水冷元件6004可以采用紫铜的水冷头。喷头系统半导体制冷片1003和底板系统半导体制冷片6003为达到良好的制冷效果,需要配备散热装置。散热装置可以采用水冷方式,即外部设置一水冷单元,喷头内部的喷头系统水冷单元包括喷头系统水冷元件1005,喷头系统进水管1006和喷头系统出水管1007。如图7所示,喷头外部的水冷单元为现有器件,它包括水泵出水管8001,水泵8002,储水槽8003,连接水管8004,风冷散热排8005和回水管8006。水泵出水管8001与喷头系统进水管1006或底板系统进水管6005相连,回水管8006与喷头系统出水管1007或底板系统出水管6006相连,形成完整循环回路。如图8所示,下面以打印两种细胞墨水为具体实施例,采用本发明的三维打印装置对本发明的器官芯片集成制造的三维打印方法进行详细描述。1、本发明的打印墨水可以通过商业途径购买,也可以根据实际需要进行制备,本实施例要打印尺寸为50mm*30mm*10mm的三维芯片,在进行三维芯片打印前制备打印材料(打印墨水),具体制备过程为:①制备主体材料打印墨水(明胶-甲基丙烯酸)将1g明胶(G1890,Sigma,美国)粉末加入10mLDPBS(杜氏磷酸缓冲液)溶液中,70℃水浴加热,均匀搅拌至完全融化后,以0.5mL/min缓慢加入1mL甲基丙烯酸甲酯(276685,Sigma,美国),反应2小时后取下,待溶液冷却至室温,加入40mLDPBS溶液稀释,用截留分子量12000-14000的透析袋在去离子水中60℃透析3天,冷冻干燥2天,形成白色蓬松泡沫状固体,即为明胶-甲基丙烯酸甲酯聚合物,-80℃干燥保存。将制备好的明胶-甲基丙烯酸甲酯溶于杜氏改良培养液(DMEM培养液,11965092,Invitrogen,美国)中,60℃助溶3小时,形成浓度为0.05g/ml明胶-甲基丙烯酸甲酯溶液,再添加0.005g/ml的光引发剂(I2959,2-羟基-4-(2-羟乙氧基)-2-甲基苯丙酮,106797-53-9,英力,中国)粉末溶于0.05g/ml明胶-甲基丙烯酸甲酯溶液中,Votex(涡旋振荡器)振荡混匀,用0.2μm滤膜过滤后分装成1ml/管备用,避光4℃低温保存。并且之后的相关操作均在避光的条件下进行。打印前,37℃融化30分钟,得到5%GelmA溶液,作为主体材料打印墨水(GelMA)。②制备牺牲材料打印墨水(明胶)将0.2g明胶(G1890,Sigma,美国)粉末加入10mLDPBS溶液中,70℃水浴加热,均匀搅拌至完全融化后,用0.2μm滤膜过滤后分装成1ml/管备用,4℃低温保存。打印前,37℃融化30分钟,得到2%明胶溶液,作为牺牲材料打印墨水。③制备细胞打印墨水(明胶,海藻酸钠与细胞混合液)将2g明胶(G1890,Sigma,美国)粉末加入10mL生理盐水溶液中,70℃水浴加热,均匀搅拌至完全融化后,用0.2μm滤膜过滤后分装成1ml/管备用,4℃低温保存。打印前,37℃融化30分钟,得到20%的明胶溶液。将0.4g海藻酸钠(A0682,Sigma,美国)粉末加入10mL生理盐水溶液中,70℃水浴加热,均匀搅拌至完全融化后,用0.2μm滤膜过滤后分装成1ml/管备用,4℃低温保存。打印前,37℃融化30分钟,得到4%的海藻酸钠溶液。将待打印细胞A和B分别消化,计数,离心,重新吹打悬浮后得到4*10^6/ml的细胞悬浮液A和B。将37℃的20%的明胶溶液,4%的海藻酸钠溶液和4*10^6/ml的细胞悬浮液A按体积比2:1:1混合,得到细胞打印墨水A。将37℃的20%的明胶溶液,4%的海藻酸钠溶液和4*10^6/ml的细胞悬浮液B按体积比2:1:1混合,得到细胞打印墨水B。本实施例所制备的四种打印墨水均为温敏材料,且均是低温凝胶态,高温溶胶态;不同材料浓度墨水凝胶点温度存在差异性,四种打印墨水在10℃时均为凝胶态,因此可以打印出结构良好的芯片,而主体材料打印墨水(GelMA)可以被紫外线交联,其余三种打印墨水不能被紫外线交联;细胞打印墨水A和B在20℃处于凝胶态,而牺牲材料明胶在20℃处于溶胶态,所以可以在20℃的情况下以溶胶态形式被吸出,而其余三种打印墨水打印的结构得到保留。2、采用现有的Solidworks三维制图软件设计肺芯片的三维结构图,并将设计的三维结构图保存为STL格式,再采用现有的分层方法将肺芯片的三维结构图转化成可被打印机识别的cli格式;3、开启三维打印装置,将底板系统600的温度设定为10℃,将主体材料打印喷头100的温度设置为20℃,将牺牲材料打印喷头200温度设定为15℃,将第一细胞打印喷头300和第二细胞打印喷头400的温度设定为25℃;将制备的四种打印墨水,分别吸入打印机的四个打印喷头中,再将构建的含有将打印芯片数据信息的cli文件导入三维细胞打印机中;4、三维细胞打印装置根据片层图形文件将主体材料打印墨水从高温的主体材料打印喷头100打印到底板系统600预先设计的位置,主体材料打印墨水在底板系统600形成凝胶,形成第一层的芯片主体材料;5、第一层的芯片主体材料打印完成后,将牺牲材料打印墨水从高温的牺牲材料打印喷头200打印到底板系统600,牺牲材料打印墨水在底板系统600形成凝胶,形成第一层的牺牲材料;6、第一细胞打印喷头300和第二细胞打印喷头400在特定位置打印不同的细胞墨水材料;7、紫外光源703发射的紫外光通过紫外光照射探头500照射三维芯片主体材料打印墨水30秒,使其局部交联固化形成稳定不可逆的凝胶状态,第一层结构打印完成;其中局部交联固化的具体过程为:利用细小的紫外光光斑,局部照射三维芯片主体材料,使得被照射局部材料交联固化;紫外光源703通过控制紫外光功率与照射时间,从而控制芯片内局部材料的刚度;8、逐层重复步骤4~7,直至完成三维芯片的整体打印;9、加热三维芯片整体到20℃融化牺牲材料,使牺牲材料变为溶胶态;将已经融化的明胶牺牲材料通过通道口吸出来,去除牺牲材料,得到三维芯片内的通道,而片主体材料和细胞打印墨水材料仍为凝胶态而会被保留,形成完整的三维芯片结构;10、在完整的三维芯片结构中通过通道灌流100mMCaCl2,交联未被融化的细胞打印墨水A和B;交联保持3分钟后吸出CaCl2,并用DPBS清洗三维芯片内的通道3次;在三维芯片通道中灌流培养基对细胞打印墨水A和B包含的细胞A和细胞B进行长期动态培养。上述各实施例仅用于说明本发明,其中各部件的结构、连接方式和制作工艺等都是可以有所变化的,凡是在本发明技术方案的基础上进行的等同变换和改进,均不应排除在本发明的保护范围之外。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1