装备疏液性多孔膜的电化学反应器的制作方法
本发明利用疏液性多孔质膜的耐液压性,将其应用到电解精炼装置、实际电池和电容器的电化学反应装置。
背景技术:
元素周期表第1族、第2族、以及第13族内的易氧化金属元素与水接触后,离子化并立即自放电,产生氢气。因此这些金属严禁与水接触,他们的析出方法除了熔融盐电解,没有其它的制造方法。在实际电池中,与水反应强烈的第1族及第2族元素中的Ca、Ba、Sr,它们的电解质水溶液不能用于原电池或充电电池。此外,周期表第2族元素Be和Mg或者第13族中的Al,虽然可以用于原电池,但是没有充电电池。作为充电电池,使用第1族元素的锂离子电池或者钠离子电池中已经开发了非电解质水溶液(有机电解质)或是固体电解质。而且,将第1族元素的钠用于电池,可以将其用作熔融盐电解质,目前已经开发了300摄氏度以上高温操作的钠硫电池(NS)电池。
我们希望实际电池的电极材料是轻的,具有高电动势,而且具有大的放电容量。因此,元素周期表第1族元素是理想的负极材料,但是其自放电是很难避免的。导致这些实际电池、电解精炼或电容器自放电的原因是负极或正极存在于同一电解质水溶液中。因此,急切需要能够将电解质和电极分离,抑制自放电,并且将元素周期表第1、第2及第13族所属易氧化金属与水隔绝的技术。
我们希望电力贮存用电容器是大容量的,并且能够快速充电放电。电化学电容器是满足该要求的理想电容器。此外双电层电容器、氧化还原容器、混合电容器也可以满足该要求。但是这类电容器的缺点是会漏电和自放电。因此,我们急需开发抑制漏电的技术。
自放电时和负极金属溶解同时发生时,产生的电子与氢离子反应生成氢气,此时电子不会向正极移动,因此也不会产生电流。一般情况下,抑制电解质水溶液自放电的方法有一下几类。专利文献1中,碱性蓄电池的正极上设置了镍基孔构件,这个镍基孔构件中充填了镍和其它活性粒子,证实可以减少自放电。专利文献2中,将碱性蓄电池电极的相对面积增大,实际反应面积没有减少的电极形状,从而抑制了自放电。专利文献3中,磺化聚烯烃树脂纤维作为主成分制成片层,未磺化处理的片层亲水化处理,制成层积体隔板。从而减少自放电并保证了容量,是长寿命的碱性电池。专利文献4中,公开展示了将微结晶硅膜和非结晶硅膜等锂吸收和释放活性物质薄膜作为中间层铺设在集电体上,作为锂电池用电极。专利文献5公开展示了多孔质肽酸是锂电池上的电极活性物质,对非水电解质的浸渍性良好,具有更好的充放电循环特性。专利文献6中,公开展示了将具有吸收和释放阴离子的碳活性物质作为正极,将吸收和释放Na的负极活性材料Sn、Zn作为负极的钠充电电池。为了熔融钠,钠硫电池需要在300摄氏度时才能形成熔融盐。但是在专利文献7中,将双氟磺酰亚胺(FSI)作为阴离子,碱金属M作为阳离子,使用以上两种熔融盐组成物时,熔融盐MFSI生成温度只要60~130度,从而能够用于电池。
关于电解质和电极之间的隔离膜,专利文献8公开了孔径0.1μm以下的聚烯烃微多孔膜具有热稳定性,适合用于高容量/高放电电池的隔板。专利文献9中,公开了将二氧化硅、氧化铝等之制成的鳞片状无机多孔膜放置在正负电极和隔板中间,不会影响离子传导,能够维持了电池的性能。专利文献10中。公开展示了非水系二次电池使用的隔离膜。其可以是含有卤素的耐热性多孔质膜,或是耐热性树脂和多孔质聚烯烃制成的叠层膜,还可以是耐热性树脂和短片组成的层与多孔质聚烯烃制成层压薄膜。
专利文献11公开展示了,将孔隙率60-90%,通气度20秒以下的氟素疏水性多孔质膜用于固体高分子型燃料电池。专利文献12、专利文献13和专利文献14,公开展示了氟系疏水性多孔质膜在结合能量为128kcal/mol的原子和亲水基化合物存在的条件下,经准分子激光的照射,变为氟系疏水性多孔质膜的制造方法。另外,专利文献15中氟系疏水性多孔质膜的内孔经紫外线照射后产生光反应,亲水基团置换。呈现亲水性的内壁孔可以培养多巴胺产生细胞,成纤维细胞,产胶原蛋白细胞,干细胞,髓核细胞,胰岛素产生细胞等。可以为帕金森氏病,阿尔茨海默氏病,糖尿病,骨软化症患者提供立体细胞营养素的培养方法。另外村原正隆等根据非专利文献1,报道了孔径33μm的疏水性多孔质氟树脂膜的耐水压有1500torr,但是将细孔内部的亲水性用光改变后,耐水压可以降至20torr。因此他提出这种改良的膜可以用于青光眼患者,用作房水压调节器。
【现有技术文献】
【专利文献】
【专利文献1】日本专利9-180714
【专利文献2】日本专利2009-181710
【专利文献3】日本专利2002-63890
【专利文献4】国際公開WO01/031724
【专利文献5】日本专利2012-12261
【专利文献6】日本专利2013-54987
【专利文献7】日本专利2009-67644
【专利文献8】日本专利2013-32535
【专利文献9】日本专利2011-222129
【专利文献10】日本专利2009-224097
【专利文献11】国际申请公开WO2007/80763
【专利文献12】日本专利2005-253305
【专利文献13】美国专利6167497
【专利文献14】欧洲专利0644227
【专利文献15】日本专利2011-184260
【专利文献16】日本专利2009-295789
【专利文献17】日本专利2013-138050
【专利文献18】日本专利2006-193612
【专利文献19】日本专利2012-30637
【专利文献20】日本专利2013-166406
【非专利文献】
【非专利文献1】Proceeding of SPIE Vol.4245,P.221-227(2001)
【非专利文献2】電気二重層キャパシタと蓄電システム日刊工業新聞社(1999)
【非专利文献3】再生可能エネルギーを考える《原発に有終の美を》パワー社出版(2011)
【非专利文献4】“風力よ”エタノール化からトウモロコシを救え《風力発電による海洋資源回収と養生工場》パワー社出版(2007)
技术实现要素:
【本发明要解决的问题】
元素周期表中第1、2和13族的易氧化金属元素溶解于水时,会产生电子,与水分子电离产生的氢离子反应生成氢气。氢气产生后,易氧化金属(负极)产生的电子减少,电流从负极向正极移动。这种现象被称为自放电。本研究想要解决问题是:生产能够抑制自己放电的实际电池电池,并且对水中溶解的易氧化金属元素电离分解,直接回收易氧化金属元素。
电化学电容器中,如非专利文献2公开所示,双电层电容器、氧化还原电容器或混合型电容器等使用强酸或强碱的水溶液作为电解质。专利文献16公开展示了,将第1电极和第2电极及第1和第2隔板从扁平的形状转变成卷曲的形状,提供卷绕芯以增加两个电极的表面上的压力,并且增厚隔板抑制内部电阻,从而抑制漏电。专利文献17展示了将码头电容器的电极材料从镍或不锈钢改变为铝和铜,以减少内部电阻。本课题想要解决的问题是抑制这些电化学容器的内部阻力,减少了电流的泄漏。
金属电解精炼时,电解液中希望的金属在负极析出的情况下,可以是离子化能量比氢小,容易被水和酸侵蚀的易氧化金属。比如说锂、钾、钡、钙、钠、镁、铝、钛、锰、锌、铬、铁、镉、钴、镍、锡和铅。这些中,一开始会与水发生激烈的反应。然后与水反应逐渐变难,但是会与酸产生反应。然而,镁、铝、钛等放置在空气中会在表面形成稳定的氧化膜。当形成这样的膜后,便可以在水中表现出很强的耐腐蚀性。特别是元素周期表中的第1族元素锂、钠或钾,第二族元素钡、钙或镁,第13族元素铝,为了使它们与水激烈反应,并且金属盐的水溶液不会发生电解,将这些金属盐在高温熔融,电流通过这熔融盐,使用熔融盐电解法进行电解精炼。本研究想要解决的问题在电解质水溶液中进行将熔融盐电解。
一般情况下,不能充电的电池被称为原电池,既能放电又能充电的电池称为充电电池。我们希望对这类电池使用了少量的活性物质后,能够有更多的电和更高的电动势。电极的电位差,根据电极组成物质和电解质中离子浓度不同存在差异。如果将氢离子(H+)的电极电位差作为±0V,Li=-3.045V>K=-2.925V>Ba=-2.925V>Ca=-2.840V>Na=-2.714V>Mg=-2.356V>Be=-1.84V>Al=-1.67V>Pb=-1.26V>Mn=-1.26V>Zn=-0.76V>Ni=-0.72V>S=-0.55V>Cr=-0.509V>Fe=-0.44V>Cd=-0.4V>Sn=-0.14V>Cd=-0.4V>Co=-0.28V,这些是负极材料。(H=±0V)以上的有Cu=+0.337V>O2=+0.401V>Tc=+0.4V>Ru=+0.46V>I2=+0.5346V>Rh=+0.758V>Ag=+0.7991V>Pd=+0.915V>Br2=+1.0874V>Ir=+1.16V>Pt=+1.19V>Cl2=+1.3583V>Au=+1.68V>F2=+2.87V这些是正极材料。实际的电池的负极必须使用容易离子化的金属,正极则使用离子化倾向极小的金属和氧化剂(包括气体状或液体状氧化剂)是必要的。将电极电位考虑进去、本发明想要解决的课题是开发实际充电电池使用的电解质水溶液的。
电极精炼及实际电池的电解质在电解时,需要使用隔离膜(隔板防止生成的金属、金属化合物或气体等正极生成物和负极生成物混合。这类隔离膜所要具备的条件是,离子能够通过,最重要的是物质和电解质是不能通过的。我们还追求隔离膜有更好的绝缘性、耐酸耐碱、对热和震动抵抗力强,有机械强度,寿命长。以前,隔离膜使用未上釉材料,固体电解质或滤纸。这当中分离电解质水溶液和负极生成物使用矾土等陶制估计电解质是合适的,但是这些陶制固体电解质在高温下才能发挥作用。固体中虽然能够对电解质水溶液使用未上釉的隔膜,但是未上釉内部的水溶液会自由浸透,不能遮断水分。滤纸也是同样的俄问题。因此本发明想要解决的问题是,开发一种能够遮断电极部和电解质水溶液,并且根据需要,能够控制离子出入的膜。
【解决问题的手段】
本发明想要解决的问题与常规方法不同之处在于将疏水性多孔质氟树脂膜用作隔离膜,发挥压力开关的效果。以往,在电解质水溶液中放置正负极,从而发生电化学反应。这样的电化学反应时,电解质水溶液与电极和交接面产生的气体造成的绝缘现象很难回避。本发明将电解质水溶液中的正极和负极之间用疏水性多孔质膜做绝缘隔离,发生电化学反应时只对电解质水溶液加压,疏水性多孔质膜内部的细孔由电解质水溶液充填,只有加压作为绝缘体的隔离膜才会变为导电体,发挥电路的开关作用。特别是实际电池中将电解质水溶液使用疏水性多孔质膜制成的袋子密闭,对该疏水性多孔质膜加压时可以进行充放电,加压解除时就可以蓄电。加压解除后,电极与电解质是绝缘的、避免了自放电和内阻增大。另外在电解(电解精炼)时也可以使电极和电解质水溶液不接触,电极上电解质析出概率减少,而且能避免电极上生成的气体和电极及电解质水溶液之间产生的绝缘现象。此外,在所述的疏水性多孔质膜隔离电解质水溶液和油的界面之间放置网状的负电极,对电解质水溶液加压时,电解质水溶液发生电解,在电极网背面的油中析出负极生成物。如果这里的电解质使用易氧化金属盐溶液、碱金属(周期表中第一族和第二族与水激烈反应的元素)能够在油中析出,而且可以重液分选(比重选矿)。
阻断易氧化金属元素化合物与水接触的最简便方法是使用易氧化金属元素的熔融盐。熔融盐是不存在水时最理想的电解质溶液。但是,需要保持易氧化金属元素的盐在熔点以上的高温,才能制得熔融盐。为此,我们不能忽视消耗的热量。为了降低盐的熔融温度,目前广泛将金属盐与其它的金属盐混合,制成混合熔融盐。专利文献15中,混合盐与熔点的关系在图二表示。自然界中存在的常温液体元素只有汞和溴,其它的元素在常温不是液体的。如果将易氧化金属与碱金属盐的电解质水溶液在隔离状态电解时,能够进行电解精炼和用于充电电池。开发这种隔离膜是本发明的任务。这种隔离膜的充分必要条件是:隔离膜在电解液中有很好的保湿性,并且电阻非常小。本发明为了解决这一问题,采用了对水溶液具有疏水性的氟树脂膜。这种氟树脂膜对电解质具有很好的保湿性是毋庸置疑的,还能保证电阻只有零。而且这种氟树脂膜可以用做多孔质膜,可以在内部通过离子。换句话说,如果对这种疏水性多孔质氟树脂膜施加电解质水溶液耐水压想的的压力时,可以实现离子渗透膜效果。施加这种水压后,可以起到电阻为零/电导的机械开关作用。
因此,在电解精炼、实际电池和电容器充电和放电时,对电解质水溶液施加耐水压相等的压力后,因为蓄电时不施加压力,可以保持电解质的保液性。也就是说,蓄电时,正负极的活性物质都是绝缘状态。因为活性物质不发生反应,自然也就没有放电。另外隔离膜的材质是氟树脂材料,即使80摄氏度,耐碱性、耐酸性和耐化学药品的特性也是优异的。此外,该树脂膜的机械强度和柔软性以及耐热性也是优异的。而且充放电时在电解质水溶液侧施加压力,操作过程中膜与电极紧密接触。我们认为使用疏水性电解质多孔质膜作为隔膜是解决本问题的最好的方法。
电容器(冷凝器)的电介质如果只有油类等绝缘体时,可以无视正负极之间的电阻,但是电介质和导电体的电路串联或并联组合构成等效电路时,电阻也会泄漏电流。特别是双层电容器、氧化还原电容器或混合型电容器等电化学电容器,电极内部或两电极之间的电解质造成的电阻增大很难避免。如果电解质是水溶液是还会泄漏。因此本发明为了防止蓄电时漏液和漏电,在疏水性多孔质氟树脂膜制成的袋中封入强酸或强碱电解质水溶液。将这个疏水性多孔质树脂膜制成的袋子放在正极和负极之间,充放电时对疏水性多孔质膜施加耐水压,使两个电极面和电解质水溶液接触。另外,在疏水性多孔质氟树脂膜制成的袋子内部加入金属纤维或碳纤维等有空隙的导电材料,对电解质水溶液加压时充放电,电解质水溶液间的电阻变小,电解质水溶液加压解除蓄电时,疏水性多孔质氟树脂膜孔内的电解质水溶液被排除。内部具有空隙,可以作为低电介质,抑制自放电。另一方面,充电放电时,电解质水溶液加压后,疏水性多孔质氟树脂膜孔内充填电解质,导电性发生变化,双电层电容器或氧化还原电容器的高电荷交换也可以进行。
非专利文献1中图6的疏水性多孔质膜细是孔径在3μm,厚度为100μm的疏水性多孔氟树脂质膜(ePTFE),如果将液体浸没后膜两侧施加的压力差计为耐水压,溶液是生理盐水(BSS)时耐水压为300mmHg,如果达到该值以上,生理盐水的流量就会上升。一次可以将这个疏水性氟多孔质膜视为电绝缘膜,膜两侧压力比耐水压低时,可以作为绝缘膜。与耐水压相等时,在液体刚浸没时发挥导电膜的作用。本发明的要旨将这种疏水性多孔质膜的渗透压用做是离子通过的开关。特别是氟树脂具有疏水性,膜两侧的压力差为达到耐水压时水溶液不会进入多孔质膜的细孔内。另外,根据细孔直径的大小、电解质的盐溶液浓度,渗透压也会有差异。多孔氟树脂膜(细孔直径3um)的盐溶液与膜两侧渗透压的关系为:水(不含盐;以下相同)的耐水压是430mmHg,10%氯化钠溶液为330mmHg、20%NaCl为280mmHg,随着溶液浓度升高耐水压下降。另外多孔质氟树脂膜(细孔直径10μm)的盐溶液与膜两侧渗透压的关系为:水渗透压10mmHg、1%NaCl为7mmHg、2%NaCl为mmHg。对这种疏水性多孔质膜的渗透压进行开/关操作后、可以用于电解精炼和实际的电池。
实际电池作为负极材料的电势差为:Li=Li+=-3.045V、K=K+=-2.925V、Ba=Ba2+=-2.925V、Sr=Sr2+=-2.89V、Ca=Ca2+=-2.840V、Na=Na+=-2.714V、Mg=Mg2+=-2.356V、Al=Al3+=-1.67V。比重分别为Li:0.54、K:0.86、Na:0.97、Ca:1.55、Mg:1.74、Sr:2.54、Al:2.6、Ba:3.51、Fe:7.87、Cu:8.96、Pb:11.35。另一方面,从电流供给量来看,产生3价离子的是铝(Al),产生二价离子的是镁(Mg)的,钡(Ba)和钙(Ca)。而且对实际电池来说,可以降低储蓄的的电量随着时间慢慢自放电减少,内部电阻减少。此外对于充电电池,充电时不会产生氢气,充电时欧姆电阻和极化都很小,具有实用性,充电后再生状态良好,可以反复使用。但是,满足所有这些条件的电极材料是没有的。以负极材料为例来看,电动势最高的锂在有水的情况下,会与水发生激烈的反应产生自己放电,阻碍电子的流动。
因此,本发明设想是,理论上的发电效率、负极的离子化电位(V)、电流密度=电子数(I)、比重(g/cm3),定义公式VI/g。金属VI/g的高低顺序为:Li=-3.045×1÷0.54=-5.64、Ca=-2.84×2÷1.55=-3.66、K=-2.925×1÷0.86=-3.40、Na=-2.724×1÷0.97=-2.81、Mg=-2.356×2÷1.74=-2.71、Al=-1.67×3÷2.6=-1.92、Ba=-2.925×2÷3.51=-1.67、Sr=-2.89×2÷2.54=-1.57、S(-2价)=-0.55×2÷2.07=-0.53、Mん=-1.1×2÷7.42=-0.3、Zn=-0.76×2÷7.12=-0.27、Pb=-0.13×2÷11.34=-0.23、Cr=-0.51×3÷7.2=-0.21、Fe(2价)=-0.44×2÷7.876=-0.11、Sn=-0.14×2÷7.28=-0.04、Fe(3价)=-0.04×3÷7.86=-0.015。
实际电池的正极中,必须选用离子化倾向小的金属和氧化剂(氧化剂包括气体状和液体状)。金属有Sb=Sb3+=+0.2V、Bi=Bi3+=+0.28、Cu=Cu2+=+0.345、Hg=Hg2+=+0.793、Ag=Ag+=+0.808、Hg=Hg3+=+0.86,氧化气体和液体包括O2=OH-=+0.4V、Br2=Br-=+1.08V、Cl2=Cl-=+1.36V、F2=F-=+2.87,过锰酸盐,铬酸,硝酸盐,卤素,过氧化物,氧化物,金属盐,酸和硫酸盐也是可以的。他们的比重为Sb:6.69、Bi:8.8、Cu:8.93、Hg:13.59、Ag:10.5、O2:1.429、Br2(液体):3.14、Cl2:3.21、F2:1.696。因此理论上的发电率,正极离子化电势(V)、电流强度=电价(I)、比重(g/cm3),VI/g按高低顺序排列为F2=+2.87×1÷1.696=+1.692、Cl2=+1.36×1÷3.21=+0.424、Br2=+1.08×1÷3.14=+0.344、O2=+0.4×1÷1.429=+0.28、Hg(3价)=+0.86×3÷13.59=+0.19、Hg=+0.793×2÷13.59=+0.117、Bi=+0.28×3÷8.8=+0.095、Sb=+0.2×3÷6.69=+0.09、Cu=+0.345×2÷8.93=+0.077、Ag=+0.808×1÷10.5=+0.077。因此要获得最高电动势的理想电极组合为:负极Li、正极F2,电动势为5.915V(=+2.87-(-3.045))。不过虽然正极电动势最高的是F2(F2=-2.87V),但是其有很强的毒性,一般正极还是用氧气(O2=-0.4V)。而且,氧气(空气)/碱金属电池的正极是空气,容量为无限的。但是即使在氧/易氧化金属电池,负极材料如果使用镁(Mg)、铝(Al)、锌(Zn)等,电极表面会发生氧化,在负极表面形成电绝缘膜,阻止电流流动。然而,本发明使用疏水性多孔质氟树脂膜。抑制自己放电,能够防止电极面的氧化。
电解精炼时,电解质电解,在负极生成产物,1g金属析出(分解)需要的电量为1法拉第(F)=96500库伦(Eq=分子量(M)/离子价(n))。1库伦表示一秒流过的电流强度是1安培,A安培的电流在t秒通过的电量(q库伦)公式表示为Q=At,作为负极产物析出的金属量m=Eq×Q/96500=Eq×At/96500(m:Q=Eq:96500)。
实际电池储蓄的能量与电解精炼所需要的电子量是一样的,因此1秒内m(g)金属析出需要的电流量(A)、A=m×96500/Eq×t。因此1小时内1Kg金属析出需要的电流A为A=1000×96500/(Eq×3600)=26806/Eq。
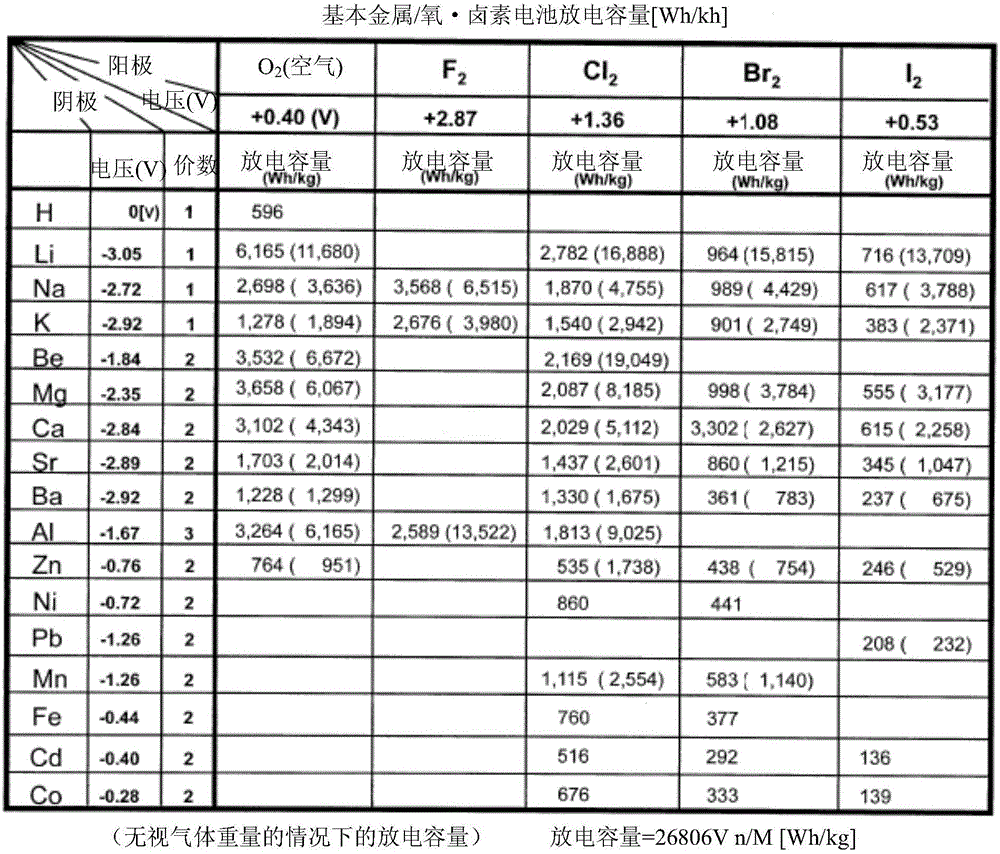
因此,实际电池在单位时间·单位重量的放电容量(电池内储蓄的能量密度W×时间(h)/kg)=电压(V)×点流量(A×h)÷电极密度(kg)=AVh/kg=W·h/kg)即26806×V×n/M[Wh/kg](V电压,M反应物的质量,n:价数)。实际电池应用这个公式后,各种易氧化金属负极材料及各种气体正极材料(氧气或卤素)组合后的放电容量Wh/kg)如图1所示。但是正极材料气体重量可以无视无视(质量为0)的放电容量在括号内表示。特别是易氧化金属/卤素电池具有很高的电动势,十分具有前景。比如Li/Cl2(16,888)>Li/Br2(15,815)>Li/I2(13,709)>Al/F2(13,522)>Al/Cl2(9,025)>Mg/Cl2(8,185)>Na/F2(6,515)>CaBr2(5,254)>Ca/Cl2(5,112)>Na/Br2(4,429)>K/F2(3,980)>Na/I2(3,788)>Mg/Br2(3,784)>Mg/I2(3,177)。不过卤素气体操作处理时具有危险性,需要十分小心。在这方面,易氧化金属/氧气电池正极实用空气,具有安全性和轻量的特点。正极使用氧气时,电池的电动势按降序排列:Li/O2(11,680)>Be/O2(6,672)>Al/O2(6,165)>Mg/O2(6,067)>Ca/O2(4,343)>Na/O2(3,636)。
根据上面的结果,本发明首先在正电极有第一主侧面,第二主侧面位于第一主侧面的对侧。负电极也有第一主表面和第二主表面,第二主表面位于第一主表面的对侧。正极和负极的第一主表面之间有空隙隔开。间隙中填满了导电液和/或电解质液体;第一个将正极从液体分开的装置是在正极的第一主表面上,第二个用于分离负极和液体的装置位于阴极的第一祝表面上。第一个分离装置包括疏液性多孔质膜含有多个小孔,第二个分离装置包括包括疏水性多孔质膜包含多个小孔。这个装置还包括压力加压工具来将液体推入疏水性多孔质膜的小孔中,继而正极和负极产生电化学反应。
本发明的一个实施方案是,前面提到的疏水性多孔质膜可以用氟树脂,聚丙烯树脂或聚乙烯树脂制成,前面提到的液体是电解质水溶液,并且对液体施加与疏液性多孔质膜耐水压相等的压力。
另一个实施方案是前面的提到的疏水性多孔质膜用氟树脂制成,液体使用油,并且对液体(油)施加与疏液性多孔质膜渗透压相等的压力进行加压。
在另一个实施方案中,前面提到的疏水性多孔质膜使用多孔质碳素,液体则是熔融盐电解质。
本发明的另一个实施方案是将前面提到的第一多孔质膜和第二多孔质膜,合在一起构成一个密闭容器。密闭容器的内部也有前面提到的间隙。此外,另一个实施方案是将前面提到的第1疏水性多孔质膜和第2多孔质膜用别的膜替代。此外,将正电极和负电极面对面开口,将疏水性多孔质膜封闭在正电极室和负电极室中。
本发明使用的电化学反应装置包括电分解装置,原电池,充电电池和电容器。
前面提到的电化学反应装置内,对导电性液体或电介质施加指定的压力后,液体流入各个疏水性多孔质膜的细孔内,从而完成各个电极与该液体的接触,发生希望的电化学反应(正极、负极参与)。然后将上述压力解除后,各电极与该液体的接触被解除。也就是说,隔离膜根据是否施加了指定压力从而发生或停止电化学反应,相当于开关ON/OFF的作用。
这个疏水性多孔质膜(隔离膜)的开关ON/OFF原理如图2所示。在疏水性多孔质膜11制成的密闭容器1中,包括了容纳负极的负极电极室3和容纳正极的正极电极室4,电解质水溶液14也容纳在密闭容器1中。然后,如图2(A)所示,使用压力加压工具6(如圆柱状砝码)对电解质水溶液14施加未到疏水性多孔质膜11耐水压的压力(图中未加压)时,因为疏水性多孔质膜11的细孔内并没有浸入电解质溶液,电压计VM指示为0,电路处于绝缘状态。与之相对,如图2(B)所示,使用压力加压工具6对电解质水溶液14施加压力后,疏水性多孔质膜11的细孔内有电解质水溶液浸入,电压计VM向正极一侧震动,指示有电压。
这个疏水性多孔质膜并非限定在电学范围,电解槽、实际电池或者冷凝器(蓄电器)都可以使用(如图3A,图3B作为对照)。本发明的电化学反应装置(电分解装置、实际电池装置和冷凝器),对液体施加指定的压力(耐水压)可以进行充放电,如果压力未满则停止充放电。这样,对疏水性多孔质膜(隔离膜)施加与液体耐水压相等的压力时,细孔内有溶液或离子,起到电子开关ON/OFF的作用。
这里的疏水(液)性多孔质膜的耐水(液)压指的是,疏水性多孔质膜压入侧(1次侧)的压力和出侧(2次侧)的压力存在压差侧,液体按照浸入该多孔质膜的细孔内最小压差来计算。一侧是液体,而另一侧可以是气体或液体。液体包括电解质,非电解质等水溶液,或者油或者纯水等导电性液体,或者可以是碱金属熔融盐溶液。气体是由水溶液电解、或者在正极或负极生成的氢气、氧气和卤素,还可以是向熔融盐内加入的氢气。
液体根据电学性质,可以分为导电体和电介质。导电性液体包括电解质水溶液和熔熔融盐电解质,电解质水溶液在电解、电池或者电化学容器中使用。在这种情况下,疏水性多孔质膜可以由氟树脂、聚丙烯树脂、聚乙烯树脂制成。如同前面提到的那样,疏水性多孔质膜起到电子开关的作用。溶液是熔融盐导电体的情况下,多孔质碳膜可以用作为熔融盐的隔离膜兼负电极使用,负电极侧的氢气的阴离子向熔融盐的正极移动时,产生了金属的氢化物。另一方面,电介质液体多为油性液体和水性液体、油性液体用于负极生成物回收,或者用作油电容器兼负极生成物的回收,或是油电容器兼负极生成物的回收及油性电容器。尤其是负极生成物回收时,将元素周期表第一族元素从水中分离在油中比重选矿。油电容器兼负极生成物的回收时,对油侧施加电荷,将电解质溶液和油的交界面作为负电极面,对负极生成物进行比重选矿。
如果仅仅供应电容器,将导电率高的硝基苯或油用作油系电容器,纯水或甲酸作为水性电容器,电容器的构造为正极版,疏水性多孔质膜,电介质溶液,疏水性多孔质膜,负极板按顺序排列。充放电时对疏水性多孔质膜施加电解质溶液耐液压相等的压力,使疏水性多孔质膜内部充满电介质溶液,蓄电时去除电解质溶液的液压。疏水性多孔质膜内部的电解质溶液被去除。疏水性多孔质膜自身变为低导电率电容器。像这样蓄电时,高诱导率电容器夹在两个低导电率的电容器中间,形成3个串联的电容器结构,充放电时,一个电容器就能发挥作用。
另一方面,隔离膜是表现为疏油性的固体导电体的场合时,特别是氟树脂的情况下,如果在水溶液中混入油,氟树脂会表现出亲油性,氟树脂表面会有油吸附。利用这一性质,水性导电体中加入少量的油,氟树脂的电解质溶液一侧会形成极薄的油层,氟树脂另一侧面与电极紧密粘附变成高电介体、可以成为控制电极间电子移动的电化学反应装置。
本发明的电化学反应装置,前面提到的疏水性多孔质膜是由高分子树脂组成时,为了改变该膜耐水压的压力值,在已经存在的多孔质膜表面或细孔壁内导入疏水性或亲水性基团、或者选用不同细孔直径的材料、或者改变电解质水溶液的盐浓度和液温、或者给予该疏水性电解质膜间电位,与电解质水溶液的水压相对应,可以控制通过疏水性多孔质膜的电解质溶液和/或离子量。
如果想要提高耐水压,可以增大疏水性多孔质膜的孔径大小。但是膜的细孔径增大后,机械强度就会减弱。因此,将呈现出疏水性和疏油性的氟树脂亲水性改良后,可以增加亲水性同时降低耐水压。然而如果氟多孔质膜两侧的亲水性改变后,该膜容易被水溶液浸透,电极也容易被水湿润,会损坏电气的绝缘性。专利文献12、专利文献13、专利文献14中氟疏水性多孔质膜,在结合能量为128kcal/mol的原子和亲水基化合物存在时,用准分子激光照射后,可以制得氟疏水性多孔质膜。专利文献15阐述了氟疏水性多孔质膜的内孔用紫外线照射后发生光反应,亲水基团置换,内壁具有亲水性的方法。非专利文献1中,33μm的疏水性多孔质氟树脂膜的渗透压为1500torr,用光改变细孔内部的亲水性后,渗透压可以降至20torr。此外非专利文献1中,电解质水溶液盐浓度变高时,耐水压会下降。而且专利文献18中,提高电解质水溶液的液温会降低耐水压,或者是给予疏水性多孔质膜间电势,使亲水性增高。这样与水溶液的水压相应,可以对通过疏水性多孔质膜离子量进行有效的控制。
本发明的电化学反应装置,如果用作实例的话,可以在海,盐湖,温泉地狱,矿泉池,含水废物贮存池,贮温水箱,蓄水池,水,游泳池等开放容器或者袋子、管子、小型容器密闭容器或是密闭容器中插入更小的密闭容器中插入疏水性多孔质膜(隔离膜),在上述的空间内对电解质溶液施加压力,电解质水溶液从疏水性多孔质膜渗出在,在正极和负极之间电解质水溶液中发生电化学反应。
对这些隔离装置内电解质水溶液用压力加压器施加压力后,电解质水溶液从疏水性多孔质膜渗出,正极和负极发生解除,产生电化学反应。隔离器具如图4所致、密闭容器和开放容器是有区别的。
密闭容器用的电化学反应装置如图4(A)所示,正负一对电极接触面为疏水性多孔质膜制成的袋子或小瓶,密闭容器中封有电解质或电介质等溶液。在外面任意一面,用图5的压力施加工具6直接加压(图5(A))、或是图5(B)以连接管为媒介用注射器6或滴管或移液器向密闭容器手动加压、或者用电动或棘轮8加压、或者在与等耐水压的高处放置,用连接管5与储水罐9连接,进行加压。
如图4B所示,开放容器11如充满大量电解质的大海、盐湖、温泉、矿泉池或废弃的水溶液、电解质、贮藏池、保温槽、贮水池、泳池等水槽。一般情况下,大海、湖泊每深10米,水压会增加1个大气压。当达到一定水深后,与溶液压力相等。此处的隔离器具可以视作放图开放容器中。在这样大的电解质溶液中,将疏水性多孔质膜放在正极和负极中间,形成电极产物回收室,保持一定间隔距离和深度,放置在与疏水性多孔质膜相等的耐水压的位置,可以直接对电解质水溶液电离分解。
开放容器中放入密闭容器的电化学反应装置如图4(C)所示,开放容器2中放入密闭容器1,对开放容器2内的密闭容器1加压,密闭容器1与正极和负极紧密接触,直接在电解室间电离分解。密闭容器1内的一对电极之间放置2块疏水性多孔质膜,或者至少可以放一张多孔质膜a,并且在密闭容器1中提前加入硫酸或苛性钠(氢氧化钠)等导电性高的水溶液。通过开放容器的水压使电解质水溶液通过疏水性多孔质膜,从而在密闭容器1中进行电解。作为替代开放容器,在大型密闭容器中放置密闭容器1,形成二重密闭容器,改变大型容器内的水压对密闭容器1加压,密闭容器1与正负极接触进行电离分解。这种双重容器结构组成的氢气发生装置可以在大海等不是电解质的水中发高效率的制造氢气,在湖和沼等淡水或是矿泉等盐水的低浓度电解质水溶液中放入该化学反应装置也可以制造氢气。这是本发明的一个鲜明特征。或者前面提到疏液性多孔质膜组成的密闭容器内部充填气体然后用压力加压工具加压,从而是疏液性多孔质膜的细孔中有熔融盐浸透。
然后说明了向由疏水性多孔质膜组成的中空密闭袋内注入电解质水溶液的方法。疏水性多孔质膜的材质可以是氟树脂、聚丙烯树脂、聚乙烯树脂。但是最耐化学药物腐蚀、耐热温度最高的此材料还是氟树脂。如图6所示,向疏水性多孔质膜11组成的中空密闭袋内1加入电解质水溶液14.方法有:使用注射器6直接注入(图6(A));利用疏水性多孔质膜11水不能通过,只能通过气体的特性,将化学药物如溶质15提前封入中空密闭袋,将中空密闭袋1放置在水蒸气的氛围中。溶质与水接触后溶解。内部的水保留方法,预先将化学药物溶质封入中空密闭袋的内部,使用连通管连接外部大气,然后插入密闭容器中,施加与密闭容器内部相等的渗透压,使溶质分解,得到电解质水溶液(图6(B));或者将中空密闭袋一侧的疏水性多孔质膜11在吸气口94用真空泵吸气,形成负压,为了将密闭容器1内的电解质水溶液14拘禁在密闭容器中,从其它侧的疏水性多孔质膜11注入电解质溶液14(图6(C));或者中空密闭容器一侧壁用乙醇13涂布、这种乙醇涂布面浸入电解质水溶液14等溶媒后,自然静置或加热,乙醇挥发后,可以将袋内的电解质水溶液保留(图6(D))。关于乙醇的涂布方法,在非专利文献1和专利文献12有描述。水的表面张力是72.3dyn/cm,氟树脂是8.5dyn/cm,甲醇则是22.3dyn/cm,多孔质氟树脂膜比氟树脂膜表面张力大,水不会浸透多孔质的细孔。比氟树脂表面张力低的甲醇的多孔质会被浸透。另一方面乙醇与水具有很高的亲和力,乙醇醇浸透的多孔质氟树脂膜上加入水后,在有乙醇存在的情况下,水会从多孔质的细孔内浸入。
如图7所示,电解质水溶液在发生电化学反应时,由正极和负极组成的一对电。电池时内部由电极板组成,电分解装置时,为了回收电极生成物会配置电极室,电容器的场合时由电极板组成
电极由电池提供的情况时,电极板的负极是两性元素和Mg,或是第1族和第2族元素中除去离子化倾向比氢大的金属元素,并且正极是氧气或是氟化物、或是离子化倾向比氢小的金属。两电极直接暴露在外部空气中,负极由第1族、第2族元素组成,并且正极是卤素或卤化物的场合时,需要对两电极的外气遮蔽形成电极室。
电极用于电离分解时,电极室根据气体透过性电极室、充填油的易氧化金属回收室,填充水的酸碱水溶液回收室分类。电极生成物是气体的场合时,两电极内部是由金属或碳组成的网状、纤维状、多孔质装或粒状的空隙电极,或是在空隙电极的背面有间隙的狗仔,形成气体透过性电解室。当电极生成物是第1族、第2族或第13族的元素时,负极是由油充填的电极室,并且为了对负极生成物重液鉴别,在该空隙电极的空隙部和空隙电极背面的空隙部装满油,或者在油的背面放置导电体电容器和供给电力贮藏用媒体的电极室(油充填电极室),水和通离子的反应后电极生成物是酸性溶液时,预先在正极板加入稀酸。如果电极生成物是碱性水溶液,则提前在负极板加入稀碱性水溶液。并且两电极的水充填电极室内水的供给口及及生成的酸性溶液和碱性溶液取出口及水充填电极室上部配置气体采集口。或者正极生成的是卤素、亚硫酸、亚硝酸等气体溶解于水,用碳素组成的空隙电极的空隙和背面的间隙安置加入水循环构造,形成水充填电极室。
当电极用于电容器时,正负电极板是裸电极,同时疏水性多孔质膜介导的是油或水等导电体,形成的单板型多孔质膜,或者活性炭电极表面有机分子附着的双层电型,或者金属氧化物、导电聚合物、活性炭等氧化还原型电极,将疏水性多孔质膜隔离,两个氧化还原电极之间充填电解质,使导电纤维发生短路。这种氧化还原构造能够在正负极电路板的氧化膜中储存高电荷,并且为了保留疏水性多孔质密闭容器(袋)内部的酸或醇等电解质溶液,会封入到店纤维,这样可以减少内部电阻。
一种实施方案是,电化学反应装置是如图8所示的等价电路。这种电路被成为[村元电路]。这个电化学反应装置中,如图8所示的等效电路,电解质水溶液面与油面之间交界面为的负电极,对电解质水溶液电离分解,阴极生成物在油层内析出,并且能够重液选别(比重选矿)。为了使成为电阻(R)的电解质水溶液14发生电离分解,在油充填电极室16内析出碱金属,设定了虚拟负电极19。虚拟负电极19位于油面和水面的交界处,这个界面只有在油面同水面与地面垂直时才能成立,其它场合都需要使用疏水性多孔质膜。如果将疏水性多孔质膜11(S)考虑为开关,对电解质水溶液施加与疏水性多孔质膜11相等的压力,使开关(S)短路,发生电离分解。更详细来说,将油充填电极室16的油层液面和电解质水溶液之间的交接面认为是虚拟负电极19,油层是油电容器(C1+C2),电解质水溶液14是电阻R的电路。油层同电解质水溶液的交接面最为油电容器的负极19,油电容器正极的17和负极19之间放置中间电极18,正极17和中间电极18之间为电介体C1,中间电极18和负极19之间是电介体C2。
这里,本发明的一个特征是,在油层和电解质水溶液之间有负极起到作用。也就是说,对正极17和中间电极18之间的电介体1持续施加电压20,并且油电容器的正极17在电解质水溶液是14正极的状态与疏水性多孔质膜11的开关(S)短路,形成串联电路,油电容器(C1+C2)内储存的电荷向电解质水溶液14转移。对导电体2施加电压20,可以对油层内的负极生成物进行重液筛选。此处将电介体1(C1)用固定电容器替代,对电介体1(C1)施加电荷,同时将电介体2(C2)的负极19和导电体1(C1)的正极16之间的水电阻R与电解质水溶液14连接。对电介体(C2)施加分解电压20后,可以对有层内的负极生成物进行重液筛选。
前面提到的将油面和电解质水溶液面的交界面作为负极的油电容器概念图如图9所示。图9(A)是虚拟电极使用疏水性多孔质膜的概念图,油与电解质水溶液的界面不受地轴影响。图9(B)为假想负极垂直于地轴,油比重未达到1时的构造图。图9(c)为假想电极与地轴垂直,油的比重超过1时的概念图。
如图9(A)所示,虚拟电极(油面和电解质水溶液的交接面)19相对于地轴形成任意方向时,在油面与电解质水溶液面19之间插入疏水性多孔质膜11,对电解质水溶液14施加压力后形成虚拟电极19,虚拟电极19与地轴垂直时并不一定需要疏水性多孔质膜11,并且油密度(比重)比电解质水溶液14的密度低(未满比重1)时,在电解质水溶液14上层形成油层23。油密度高于电解质水溶液14时(比重超过1),会在电解质水溶液14的下部形成油层14。并且对电介体1(图8(A)的C1)施加电压20,同时对电介体2(图8(A)的C2)的负极19与电介体1的正极17之间的电解质水溶液14接触,施加分解电压20时,电介体2(图7(A)的C2)内的油中的负极生成物可以从回收口26取出。
一个实施方案中,在海水或盐湖等低浓度电解质中放入正负一对气体透过电极室,可以直接从海水生成氢气、氧气和卤素(氢气制造装置,参照图10)。一般情况下,海水面或水面每深10米就会上升1个大气压。利用这一自然现象,将气体透过性正负极电极室下沉到疏水性多孔质膜相等的水压时,就不需要认为的施加压力。比如说将正极和负极隔开的一组电极室下沉到与疏水性多孔质膜渗透压相等的深度,对正负两极施加电压后,可以生成氢气、氧气和卤素。例如,如图10(A)所示,将开放容器2放入大海或盐湖等低密度的电解质水溶液14中,在负极电极室3和正极电极室4之间放油疏水性多孔质膜11。使用气体透过电极室3和4,盐水发生电解,在负极电极室3生成氢气,在正极电极室4生成氧气和卤素。正负电极室由网状、纤维状、多孔质状或粒状的金属或碳空隙电极组成,并且在电极室3、4上都有生成气体的回收软管12。两电极室3、4在电解质水溶液(海水)14中形成一组电极室、这样一组或多组连接后形成正负电极室群,将正负电极室群放入与疏水性多孔质膜水压相等的海水中,在两电极间给予电压后,产生电离,分别对负电极室的氢气、正电极室的氧气和卤素进行回收。本发明,因为电极并不直接插入电解质水溶液,根据电极生成物的不同,电极和电解质不会发生绝缘状态。而且,以疏水性多孔质膜作为边界,因为电解质侧的压力比电极生成物侧压力高,所以电极生成物的回收效率很高。如果将开放容器2用密闭容器1替代后,如图10(B)所示可以在地上使用。用压力加压器6对密闭容器1中的电解质水溶液(盐水)14施加压力后,并且通过连接管5在水头位置10放置储水槽9收集海水,或是浓缩海水或含有电解质的水都可以直接电离分解,可以分别在负电极室3回收氢气,正电极室4回收氧气和卤素。
一个实施方案中,密闭容器中装入浓缩的电解质溶液,在密闭容器外侧加入淡水,向疏水性多孔质膜27(淡水渗透用)施加压力,发生电离分解,可以直接高效率的生成氢气、氧气和卤素。
如图11(A)所示,将稀硫酸或苛性钠等高浓度/高导电率的电解质水溶液(高浓度电解质水溶液)装填的疏水性多孔质膜制成的密闭容器中,作为氢气制备装置30。将其放入淡水湖,池,海水,温泉等开放容器2中,将淡水或海水或温泉水或高温排出水压入密闭容器1的疏水性多孔质膜内侧,水溶液发生电离分解产生氢气。因为密闭容器1内装有稀硫酸或氢氧化钠水溶液等高浓度电解质水溶液,密闭容器1外壁上的疏水性多孔质膜(淡水渗透用)向密闭容器1内部提供电解质水溶液14,从而连续长生氢气。为了使密闭容器1内部同外部两种不同的电解质水溶液在同一渗透压对疏水性多孔质膜浸透。疏水性多孔质膜a(11)、b(27)在不同的场合,疏水性多孔质膜a(11)是比疏水性多孔质膜b(27)的细孔径更大的膜。也就是说,疏水性多孔质膜a(11)、b(27)是同一种类的场合下,疏水性多孔质膜b(27)与低浓度电解质水溶液接触面的孔壁被水浸润后,亲水基置换。低浓度电解质水溶液和高浓度电解质水溶液达到相同的置,使疏水性多孔质膜a和疏水性多孔质膜b可能浸透。疏水性多孔质膜a(11),b(27)是同一种类时,最简单的方法是,低电解质水溶液一侧水压增大,或者高浓度电解质水溶液的出口处压力改为负压。负压与疏水性多孔质膜a(11)接触,将负极电极室3货正极电极室4等气体透过电极室生成的气体用真空泵吸引。对低浓度电解质水溶液施加压力,的气体可渗透电极室的出口侧产生的气体的压力的斥水性多孔膜b的差压的水压力(27)它是在大于或等于被吸入成为范围作为斥水性多孔膜(11)的水的压力的总和。这个气体透过电极室在电分解是生成大量的气体,因此需要同时对生成气体的回收和气压控制。为此,负极电极室3和正极电极室4等气体透过电极室生成的气体在气体回收口12处需要添加压力调节泵。
特别是,低浓度电解质水溶液14或淡水88等通过疏水性多孔质膜b(27)与密闭容器1内的稀硫酸或碱类的高浓度电解质水溶液混合后,与疏水性多孔质膜a(11)接触后在负极电极室和正极电极室4电离分解,各气体透过电极室后产生的透过电极室的压力(Pg),低浓度电解质水溶液14对疏水性多孔质膜b(27)施加的水压Plb同高浓度电解质水溶液对疏水性多孔质膜a(11)施加的水压Pla之间额压力差,是疏水性多孔质膜a(11)的渗透压Plba,并且高浓度电解质水溶液的水压P3lag和气体透过电极室的压力(Pg)的压差是疏水性多孔质膜a(11)的渗透压Plag,必须同时满足Plb-Pla≧P1baおよびPla-Pg=P1ag。也就是说为了满足Plb-Pg≧Plba+Plag,提高低电解质水溶液14施加的水压力Plb,或者为了维持气体透过电极室内的压力(Pg),需要使用压力调节阀93介导真空泵吸气,将气体透过电极室的压力(Pg)降压后,一组疏水性多孔质膜的渗透压累加起来,可以调整水压Plb和最后的气压Pg,从而引起水电离分解,产生氧气、氢气和卤素。实际操作中,对疏水性多孔质膜a(11)、b(27)使用同一种疏水性多孔质膜,对低浓度电解质水溶液14施加水压Plb,或者对气体透过装置内的压力Pg进行降压等简便的操作,使电离分解,可以直接在海水中和湖中产生氢气。即将封有稀硫酸或稀碱的高浓度电解质水溶液的密闭容器1放入大海、湖泊等开放容器2中,在密闭容器下降到一定压力水位后,连续建立分解。
本方法如图11(B)所示也能在地上使用。将密闭容器1插入大型密闭容器29,将水道28的水压改成对疏水性多孔质膜11及疏水性多孔质膜(淡水渗透用)27耐水压以上的压力,同时不断提供水,就可以连续产生氢气。这种自来水也可以用装有淡水或是海水的容器替代,或者温泉的保温槽内施加疏水性多孔质膜耐水压以上的压力,机械加压或是在水源通过连接管对供水施加压力也是可以的。这里重要的是疏水性多孔质氟树脂膜(电极隔离膜)11的渗透压和淡水渗透用的疏水性多孔质膜88的渗透压是相同或相近的。将这些由一组气体透过用电极室3,4组成的氢气制造装置30组成一对或多个集合,将电解质水溶液放置在与疏水性多孔质膜在相等的渗透压条件下,施加高于水分解电压以上的电压进行电离分解,在负电极生成氢气,在正电极生成氧气和卤素。
在一个实施方案中,没有使用先前添加隔膜或离子交换膜的方法,疏水性多孔质膜在有水压存在的条件下进行电离分解,在负电极室内部直接获得苛性钠。如图12所示,对苛性钠31施加疏水性多孔质膜11耐水压以上的水压后,对氯化钠,智利硝石,硫酸盐等易氧化金属水溶液发生电离分解,疏水性多孔质膜11隔离的水充填电极室40内生成易氧化金属氧化物31(苛性钠)。
如图12(A)所示,对密闭容器1内的易氧化金属盐水溶液(氯化钠水溶液)32施加与耐水压相等的渗透压,并且在水充填电极室40内部填充镍等金属或碳电极,并且水供给口34提供最高80摄氏度的水。这里提供的水也可以是室温的,因为高温时苛性钠溶解度会增加,为了高效率的制造苛性钠,80摄氏度左右是最佳的。特别是电解开始时水充填电极室40内水的电阻较高,所以需要预先加入稀氢氧化钠溶液。水充填电极室40由水供给口34提供水,负极产物回收口35回收浓缩的基本金属氧化物(浓缩苛性钠水溶液),最上部回收管12回收产生的气体(氢气)。另一方面,正极由气体透过电极室41组成、疏水性多孔质膜与配备碳素纤维、碳素里或多孔质碳素等的正电极37紧密接触,正极表面生成的氯气、亚硝酸器、亚硫酸器等气体由回收管12回收。但是考虑到产品输送,液体比气体更便于运输。因此如图12(B)所示,正极采用水充填电极室40,为了使阴离子和水发生反应,在水供给口34提供的水中加入稀盐酸水溶液,疏水性多孔质膜介导正电极板36和负电极板38之间产生电解,反应试2Cl-+2H2O→2HCl+O2。这里生成的酸(盐酸)33是从浓酸(盐酸)出口42出来,氧气则从气体回收管12回收。
在一个实施方案中,因为使用了疏水性多孔质膜的离子开关ON/OFF,水中析出了最讨厌水的易氧化金属金属元素,使水溶液的电解反应能够发生(易氧化金属回收装置)。如图13(A)(B)所示,密闭容器1内,为了使易氧化金属卤化物的水溶液发生电解,在负极生成基本金属。密闭容器1的负极侧疏水性多孔质膜11组成的隔离膜与金属、碳组成的网状负电极接触,他的背面是充满油23的油充填电极室16,负极产物是比油比重轻的基本金属(Li、K、Na),在油充填电极室16的上部的负极回收口35回收。比油重的基本金属(Mg、Ca、Ba、Sr)在油充填电极室16最下部的负极产物回收口35回收。正极产物的取出方法分为气体回收和液体回收。气体的取出方法如图13(A)所示,正极由气体透过电极室41组成,疏水性多孔质膜11与碳纤维、碳元素、多孔质碳素等正电极37接触,正极表面生成的正极气体(氯气)由气体回收管12回收。但是,如果考虑产品输送,水溶液比气体更为方便。因此如图13(B)所示,正极采用水充填电极室40的构造,为了使阴离子和水反应,水供给口34提供的室温水中预先添加稀盐酸水溶液,疏水性多孔质膜11介导网状负电极板42和正电极板38之间进行电解、离子反应式(2Cl-+2H2O→2HCl+O2)。这里生成的浓盐酸从42口取出,氧气从气体回收管12分别回收。
在一个实施方案中,将元素周期表第1族或第2族元素组成的易氧化金属盐水溶液的液面与油面之间的交接面用作虚拟的负电极面,金属盐溶液发生电解,阴极生成物可以在油层内析出。图14(A)和(B)表示,密闭容器1和疏水性多孔质膜11隔开,放置油充填电极室16,油23和易氧化金属盐水溶液32之间的接触面为虚拟负极面19和正极37(使用气体透过电极室时)或与正电极38(使用水充填电极室时)之间金属盐水溶液32发生电解,使油充填电极室16中的油23内有负极产物析出。图13表示了正极使用气体回收电极41,也可以使用水充填电极室40。图14(A)中油充填电极室16内两个电容器C1和C2为串联排列的构造,油充填电极室16的疏水性多孔质膜11相对面放置正极板17,并且在疏水性多孔质膜11和正极版17之间放入中间电极板18。对油缸内的中间电极板18和油缸内正电板17之间形成的电容器C1提供电压(E)20。另一方面,对密闭容器1内的易氧化金属盐水溶液施加压力,疏水性多孔质膜11渗出的易氧化金属盐水溶液32的水液面与油面的交接面形成虚拟的负极面19。如果将油充填电极室16内的正极板17和气体回收电极41内的正电极37或水充填电极室40内的正电极板分别短路后,油槽内中间电路板18和虚拟负极面19之间形成电容器C2。并且对易氧化金属盐水溶液32施加与疏水性多孔质膜耐水压相等的压力时,发生电解,在油充填电极室16的油中析出易氧化金属。图14(B)中,油充填电极室16的油罐中没有放置中间电极板18,油充填电极室16外准备了固体电容器C1,将油罐内的正极板17和气体回收电极41内的正电极37或水充填电极室40内的正电极板分别短路后,油罐内的正电极板17和虚拟负电极面19之间形成电容器C2,对正电极37(气体回收电极41)或正电极板38(水充填电极室40)与虚拟负极面19之间的疏水性金属盐溶液32施加与疏水性多孔质膜耐水压相等的压力后,发生电解。在油充填电极室16的油中析出易氧化金属。像这样如果保持对金属盐水溶液32施加与疏水性多孔质膜11耐水压相等的压力,在油充填电极室16的油中可以对希望得到的易氧化金属进行重液筛选。正极使用气体透过用电极室时,可以在正极生成气体,或者使用水电解室时,可以连续的收集浓盐酸、浓缩无机酸或者氧气等在正极生成的气体。
在一个实施方案中,将多孔质碳素膜用作做熔融盐的隔离膜兼负电极,负极产生的氢气阴离子向熔融盐的正极侧移动,形成金属的氢化物。如图15所示那样,易氧化金属氢氧化物熔融盐(苛性钠)46经熔融盐加热器48加热,电离产生Na++OH-。另一方构成负极的电极室是气体透过电极室41,向气体透过电极室41氢气压入口47压入氢气,氢气经过多孔质碳素板兼隔离膜44,压入易氧化金属氢氧化物熔融盐(苛性钠)46。这种状态下多孔质碳素负极板兼隔离膜44和正电极板38之间施加生成氢负离子生成的分解电压以上的电压(E)20,可以生成H负离子(H-)50。氢负离子与易氧化金属氢氧化物熔融盐(苛性钠)的离子状态Na++OH发生离子反应,生成氢化金属(Na++H-=NaH)。因为苛性钠熔融盐(NaOH)的比重是2.13,氢化钠的比重是0.92,更加轻。氢化纳一边洁净固化一边从易氧化金属氢氧化物熔融盐(苛性钠46)上浮,在氢化金属回收口51对氢化金属(氢化纳)回收。这些氢化易氧化金属与水发生激烈的加水分解反应,与易氧化金属元素单体相比可以生成两倍的氢气。而且,如图16所示易氧化金属元素内第1族元素(Li,K,Na),第2族元素(Mg,Ca,Sr,Br),第13族元素(Al)的氢氧化物熔点比氧化物低。不过其中,Mg和Al需要除去,它们的氢化物的熔点比氢氧化物高。而且氢化物的比重比氢氧化物的比重低。因此除Mg和Al以外,其他的可以在低温下形成熔融盐,与氢负离子反应后生成氢化物,可以浮在表面进行简单的比重筛选。特别是第1族元素元素本身的熔点比氢化物低。Na的熔点是98摄氏度,氢化纳(NaH)的熔点是800摄氏度,K是64摄氏度,KH的熔点是417摄氏度。因此,操作熔点很低的K或Na需要十分注意。而如果是氢化物,熔点变高,比重变低,加水分解后可以产生两倍氢气,可以用于氢气发电和氢燃料汽车等氢气发生装置。根据消防法,Na是第三类危险品,是自燃物质和禁水物质,但是氢化纳(NaH)的熔点与Na的98摄氏度相比就很安全,但是也会与大气中的水分发生反应并爆炸,因此操作时十分需要注意。一般将金属Na与氢化纳氢化纳(NaH)的安全性进行比较,他们都是消防法里禁水的物品,会与水发生激烈的反应,是第3类危险品。但是,与金属Na的危险等级1级相比,氢化纳(NaH)是II级,相对安全一些,是可以操作的药物。一般来说金属Na需要用煤油保存,氢化纳(NaH)粒子只要表面涂有石蜡,就可以相对安全的使用。另外,金属钠在与水反应时生成0.5莫尔的氢气(Na+H2O→1/2H2+NaOH)。但是氢化纳(NaH)反应时可以生成1摩尔(2倍)的氢气,反应式NaH+H2O→H2+NaOH)。从而氢化纳(NaH)有望成为氢气(H2)的再生装置。这样,原来不安全的Na,只有在油中保存才安全,并且还有爆炸的危险性。但是如果将其氢化后,变成氢化纳(NaH),熔点变为800摄氏度,又安全,并可以长期保存,需要时与水反应生成氢气,使用十分方便。另一方面,使用比氢氧化物熔点低的MgH2和AlH3时,可以在熔融盐的槽上部配置冷却壁,采用蒸汽冷却回收的方法。但是氟树脂膜与金属Na接触后,会腐蚀氟树脂,所以疏水性多孔质氟树脂膜与金属钠接近后,必须要混入轻油或石油等油类。
在一个实施方案中,将填充电解质水溶液的疏水性多孔质膜夹在正极和负极的电极板之间,放入密闭容器(信封型),形成原电池和充电电池。这种电池在充电和放电时,对电解质水溶液施加与疏水性多孔质膜耐水压相等的压力,正负电极间就会发生电化学反应。蓄电时解除对电解质水溶液压力,可以避免两电极之间的自放电。如图17所示,密闭容器中(信封型)55中有两块疏水性多孔质膜11,中间封有电解质水溶液14,将密闭容器夹在负电极室(电池用)52和正电极室(电池用)53之间。充电时图17(A)所示,对密闭容器(信封型)55内的电解质水溶液14使用压力加压工具6施加与疏水性多孔质11耐水压相等的压力,疏水性多孔膜11渗出的电解质水溶液14介导负电极室(电池用)52和正电极室(电池用)53电力供应,进行充电。充电完毕后对密闭容器(信封型)55内的电解质水溶液解除压力,避免两电极之间自己放电(图17(B)),维持蓄电状态。放电时(如图17(C))所示,对疏水性多孔质膜密闭容器(信封型)55内的电解质水溶液14再度施加与耐水压相等的压力。电池电极的安全性和长期稳定是最重要的因素。因此在电极构造上需要考虑的是,负极电极板上使用两性元素(Zn,Al,Sn,Pb)或Mg及第1族和第2族中除去离子化倾向比氢元素大的金属(Ti,Mn,Cr,Ga,Fe、Cd,Co,Ni,Fe),疏水性多孔质膜与电极板紧密解除,该电极板周围也不用与外界隔断。负极是第1族或第2族元素,并且第1族和第2族元素组成固体板电极时及第1族和第2族元素的负极生成物在碳素组成的空隙电极内部的空隙驻留时,需要对电极周围的盒子,容器,疏水性处理膜用树脂膜与涂布外界隔断。如果是正极的场合,正极电极是比氢更具离子化倾向的轻金属和金属氧化物或空气或氢氧化物使用的场合时,与疏水性多孔质膜解除的电极不一定要与外界隔断。正极用除氟以外的卤素气体货卤化金属时,疏水性多孔质膜接触的电路板周围盒子,容器,疏水性处理膜需要用树脂涂层覆盖,或者对电池与外界隔断,但是,正极板电极是疏水性材料或是经疏水处理以后,不需要疏水性多孔质膜,可以直接插入电解质水溶液。
本发明对原电池和充电电池,如果负极使用易氧化金属,正极用氧气或卤素,可以获得更高的电动势和电容量(图1)。在该电池中,易氧化金属元素和氧气和卤素是化合物,可以制成电解质水溶液。这种情况下,这些化合物在室温水中溶解度越高,放电容量也越高。为了进行高效率充电,充电开始时需要提高氢氧化金属(图18)或卤化金属(图19)在室温时的溶解度,放电开始时为了让大容量电力能长时间持续放出,氢氧化金属或卤化金属的溶解密度在放电开始时要低,放电完成时溶解密度又增高,并且最好能接近饱和,而且,高速充电和放电时最好能对该电解质水溶液升温(温泉、工业废热、内燃机冷却循环水)。这些化合物,除了NaCl与温度上升没有关系,其它化合物与温度升高时溶解度液升高。特别是Ba(OH)2在40摄氏度时溶解度只有5%,80摄氏度时溶解度有60%。这些化合物在60摄氏度时溶解度如图20所示。图2中,溶解度为80%时标记为4重圆圈,溶解度60~80%标记为三重圆圈,溶解度30~60%溶解度标记为两重圆圈,溶解度10~30%溶解度标记为1个圆圈,溶解度1~10%标记为小圆圈,溶解度1%以下标记为x,如果加入乙醇溶解化合物时用三角△表示。这些在图18所示的高溶解度,并且图1所示放电容量高的电解质水溶液是最有希望的。
本发明使用的电池,包括氧/碱金属电池。为了使电池变轻,负极使用比重较轻的金属,正极使用大气中的空气。如图1显示的易氧化金属/氧气电池放电容量值,Li/O电池考虑氧气的重量计算得到6,165Wh/kg,因为氧气可以从大气中获得,如果不考虑这个重量,可以得到很高得放电容量(11,680Wh/kg)。同样Mg/O电池是3,658Wh/kg,如果不考虑空气(6,067Wh/kg),Al/O电池是3,264Wh/kg,如果不考虑空气,是(6,165Wh/kg)。然而根据图18得氢氧化金属的溶解度和温度的关系,Mg(OH)2和Al(OH)3不溶于水,最后会在负极形成氧化物,使电子流动受阻。Ca(OH)2也是同样的情况。在属于两性元素Al的电解质水溶液中加入苛性钠,反应式Al(OH)3+NaOH→Na[Al(OH)4]),Al也能以这种形式溶解。但是本发明只考虑Na/O、K/O、Ba/O、Li/O、Sr/O电池。理由是在室温环境下的电池的效率顺序是K/O>Na/O>Li/O>Ba/O>Sr/O(温泉等其它高温场所,还会有Ba/O电池。放电容量的效率顺序是Li/O>Be/O>Al/O>Mg/O>Ca/O>Na/O>Sr/O>K/O>Ba/O。考虑到这些结果,电池的构造如图21所示。这里,正电极室(电池用)53使用氧气或空气、负电极室(电池用)52使用第1族、第2族和/或第13族金属。此外,两侧壁是由疏水性多孔质膜11组成的密闭容器(信封型)55,密闭容器55内的电解质水溶液14可以使用苛性钠、苛性钾(氢氧化钾)、氢氧化钡等碱类或是硫酸、盐酸、硝酸等酸类。尤其是正电极室(电池用)53的氧气电极是碳素制的空隙板电极(活性炭)58,里面可以吸附空气和氧气,正极为集电极板64、并且疏水性多孔质膜11和碳素空隙板电极(活性炭)58之间放置充电用辅助正电极(网状电极)56,使碳素制空隙板电极(活性炭)58不会产生发热(图21(A)),或者说与正电极的疏水性多孔质膜11接触面放置金属板60(CuO或Al2O3),从而作为氧气的提供源。
另一方面,负电极(电池用)52使用第1族、第2族及/或第13族元素的固体电极,或是碳素制的空隙电极内部和表面的空隙内吸附第1族、第2族及/或第13族元素的负极产物的外气遮蔽型负电极57,并且负电极周围用树脂涂层61覆盖,或者负电极内部加入油22,与外界遮蔽。
这种电池(原电池或充电电池),对电解质水溶液14加压后进行充电。充电完成时,解除对电解质水溶液14的加压,维持蓄电状态。放电时对电解质水溶液14加压后就可以开始放电,
本发明中的电池,包含金属/卤素电池,这种电池的电极可以做到免维护。一般来说,卤素气体是有毒的。因此本发明将金属卤化物(固体)作为正极。如图22所示,两边由疏水性多孔质膜11组成的密闭容器(信封型)55内封入金属卤化物水溶液14作为电解质水溶液。与疏水性多孔质膜11连接的电极室52内有负电极板(电池用)62/65,正电极室53有金属卤化物63制成的金属板(电池用)64。在正极的金属卤化物63与多孔质膜11直接接触。对该电池(原电池或充电电池),使用压力加压工具6对电解质水溶液14施加压力,进行充电。在负极板62内析出构成电解质水溶液14的金属阳离子,在正极配备的金属板64的表面,当该金属的金属卤化物63生成后,充电完成,解除对电解质水溶液14的加压,保持蓄电状态。放电时对电解质水溶液14用压力加压工具6加压。图22(A)是单层电池的概念图,图22(B)是层叠电池的概念图。
层叠电池(图22(B))是将单层电池图22(A)串联排列起来。单层电池的正电极室内的金属板与疏水性多孔质膜接触的部分是卤化的金属卤化膜63,没有卤化的金属部分作为集电极板64。层叠电池的一层和两层之间的电极是与1层接触的正极(负极使用金属卤化物)66,单层电池的集电极板64用作第2层的负电极板65,以后每层都是一样的。如果是原电池,电解质水溶液14可以是包含氯化钠的任意金属卤化物,单层电池负极与正极的组合是Zn、Mg、Al、Ni、Pb等可以选择任意金属,正极可以是任意金属的卤化物。层叠原电池负极和正极使用同一种金属,正极和负极用金属的氯化物组成。充电电池是电解质水溶液14用负极的金属卤化物,并且单层蓄电池负极和正极的的组合有Zn、Mg、Al、Ni、Pb,他们可以是同一金属货随便选择。顺便说一下,密闭容器(信封型)55的两面正极的电极面粗糙处理后增大表面积,并且在正电极室外壁和全部的电池装置都用金属卤化物覆盖防湿。这些金属/卤素电池,如图19所示那样,按照金属卤化物在室温溶解度的高低顺序排列ZnCl2>CdCl2>LiCl>BeCl2>CaCl2>MnCl2>NiCl2>FeCl2>CoCl2>MgCl2>AlCl3>BaCl2>KCl>NaCl,放电量如图1所示,按多少顺序排列BeCl2>LiCl>AlCl3>MgCl2>CaCl2>NaCl>KCl>SrCl2>ZnCl2>BaCl2。因此本发明推荐能在空气中使用的负极板Zn、Mg、Al、Ni、Pb。第1族和第2族金属都是可以使用的。这种场合下负极是1、2族元素的固体电极或是碳素制的空隙电极板或是表面具有空隙,可以吸附1、2族元素负极生成物的电极,并且该负电极的周围有树脂涂层覆盖,或者该负电极内部含有油,必须对外界具有屏蔽作用。
本发明的电池,进一步包括金属/溴和金属/碘电池。一般卤素气体是有毒气体,如果放在室温,溴(沸点58.8摄氏度),仍然是液体;碘(沸点113.6摄氏度),仍然是固体。而且将金属溴化物按室温的溶解度高低排列ZnBr2>LiBr>CaBr2>MnBr2>NiBr2>FeBr2>CoBr2>SrBr2>CdBr2>NaBr>KBr。放电量如图1所示按多少排列CaBr2>MgBr2>NaBr>LiBr>KBr>SrBr2>MnBr2>NiBr2>FeBr2>BaBr2。并且按金属碘化物在室温的溶解度高低排列ZnI2>CaI2>BaI2>NaI>SrI2>LiI>KI>MgI2>CaI2>CoI2>PbI2。放电容量按图1所示的高低排列LiI>NaI>CaI2>MgI2>KI>SrI2>ZnI2>BaI2>PbI2>CoI2>CdI2。因此本发明中,考虑将能够将卤素存贮在固体内部空隙中的电极室。正极如图22(A)(B)所示,为了将正极电极室53与外界隔断,在容器中混入活性炭颗粒和碳素纤维67,并混入溴溶液68和碘颗粒69,密闭容器(圆筒形)55的疏水性多孔质膜正极的背面有集电极板64。另一方面,负极使用两性元素和Mg或1、2族元素除去离子化倾向比氢大的金属元素组成裸板电极,或是第1族、第2族元素使用固体电极,或者在碳素空隙电极板内部的空隙中储存第1族、第2族元素的负极生成物,并且负电极的周围由树脂涂层包围,或者该电极的内部含油,必要时与外界隔断。该电池的电解质水溶液14中,负极使用金属元素的溴化物或碘化物的水溶液,通常需要保证正极在沸点以下的环境温度。负极如图22(A)所示,负极电极板(裸板电极)62暴露在外界也不会受到影响,该裸板电极可以使用两性元素(Zn,Al,Sn,Pb)及Mg或者是1、2元素除去离子化倾向比氢大的金属(Ni、Pb、Ti、Mn、Cr、Ga、Fe、Cd、Co、Ni、Fe)。并且如图22B所示使用第1、2族金属时,负电极室(电池用)52是1、2族元素(Li,Na,K,Ca,Sr,Ba)的固体电极或碳制的空隙电极板,表面和内部有1、2族元素的负极生成物吸附,并且负电极周围有树脂涂层61包围,或者负电极内部有油22对外界产生遮蔽作用。这种电池(原电池和蓄电电池),对电解质水溶液14加压进行充电,充电完成后解除对电解质水溶液14的压力,维持蓄电状态,放电时对电解质水溶液14加压,开始放电。
本发明的电池也可以是金属/氟电池,一般氟气有剧毒很难使用,但是如图1所示氟的电极电位是+2.87V,是氧气+0.4V的7.175倍。放电容量是NaF(3,568Wh/kg)>KF(2,676Wh/kg)>AlF3(2,589Wh/kg,放电容量与之相近的物质种类是很少的。而且氟化物的结合能力强,大部分是微溶于与水的,但是室温时溶解度KF为50%、NaF为4%、AlF3为0.5%,这些是例外。因此有望成为负极材料的只有K,Na和Al,但是它们效率都很低。另一方面如果使用氟化石墨避免使用氟气,也可以制成K/F、Na/F、Al/F。这些电池的电解质溶液14中,使用氟化钾水溶液是最合适的,因为氟化铝很难溶解,在电解质水溶液14中添加苛性钠或苛性钾可以获得发电力达4.54V的Al/F原电池。K/F原电池和二次电池的发电力达5.79v,并且是轻质的高电容量电池,是十分有希望的。正极如图24(A,B)所示,正极电极室53是石墨70,密闭容器55(信封型)与疏水性多孔质膜11紧密接触的正极背面有电极板64。另一方面,负电极的Al负极电极板71与密闭容器(信封型)55的疏水性多孔质膜11紧密接触,氟化铝电解质水溶液中加入可行钠或苛性钾,可以作为原电池使用。原电池和蓄电池中,如图24B所示,如果使用钾(K)或钠(Na)时候,负电极室(电池用)52用第1族元素和/或第2族元素(Li、Na、K、Ca、Sr、Ba)形成的固体电极或碳素制成的空隙电极板内部货表面的空隙中吸附有第1族元素和/或第二族元素的负极生成物吸附的外气遮蔽型负电极57将电子从集电极板64取出,并且负电极的周围有树脂涂层包围或者负电极内部混有油22,与外界隔离。在这里,对密闭容器(信封型)55的电解质水溶液14加压后进行充电和放电。
本发明的电容器,包括将电介质液体或电解质水溶液封入疏水性多孔质膜制成的密闭容器(信封型),在密闭容器的对面分别铺设了正电极和负电极。在这种电容器中,充电和放电时对该电解质溶液施加疏水性多孔质膜耐水压相等的压力,使两电极间产生电化学反应,蓄电时解除对电解质溶液的加压。这种电容器如图25(概念图)所示,将油和水导电性液体或电解质水溶液14封入疏水性多孔质膜密闭容器(信封型)55中,在密闭容器55的外侧面放置正电极室53和负电极室52。疏水性多孔质膜制密闭容器(信封型)55的两侧配置电极室52、53两电极,板电极73或表面为活性炭、石墨、纳米碳等碳电极74,表面能够吸附有机分子的双层电容器。或者是电导电体的表面由氧化物膜、导电聚合物、活性炭等组成的氧化还原电容器电极75、或活性炭、多酚、等石墨锂钛酸等构成混合电容器电极。在该电容器中,充电时对电介质液体72或电解质溶液14施加与疏水性多孔质膜11耐水压压相等的压力,对两电极间给予电荷(图25(A))、蓄电时解除压力(图25(B))、放电时施加与耐水压相等的压力。如图25(B)所示,虚线包围处77内,疏水性多孔质膜11和电极室52、53的电极73、74、75、76为了方便描述是分开的,其实它们是接触在一起的。如果没有加压疏水性多孔膜11的细孔内是没有液体的。因此,可以考虑疏水性多孔质膜11使用低导电率膜。
因此,如图25(D)所示,细孔内渗入电介质溶液后,根据加压,电路为可变电容器(C2)、细孔内电解质水溶液浸入后展示为可变电阻(R)。也就是说,蓄电时,疏水性多孔质膜11的细孔内没有电解质液体、只有空气存在,为了储存电荷,可以考虑将电荷导电体(C1)的两端用低导电率的电容器(C2)串联排列。如果在这里施加压力,电解质液体如果C1=C2,电解质溶液R接近于零,可以进行充电和放电。本发明的电容器,包括电双层电容器和氧化还原电容器。在电容器装置中,正电极和负电极室使用高导电率的电容器,属随性多孔质膜制成的密闭容器(信封型)内部有导电体和电解质),疏水性多孔质膜的正负电极间的传导有ON/OFF开关。图26是双层电容器的概念图,图27是氧化还原电容器的概念图。如图26、27所示,正负一对电极室52、53之间的疏水性多孔质膜密闭容器(信封型)55中充填有金属纤维、碳素纤维和活性炭等含空隙的导电材料78,浸泡在稀硫酸79或苛性钠80等电解质水溶液14中,对电解质水溶液14用压力加压工具6施加与疏水性多孔质膜11耐水压压相等的压力后,疏水性多孔质膜11的细孔内有电解质水溶液通过,进行充电(图26(A),图27(A))、蓄电时解除对电解质水溶液14的加压(图26(B)、图27(B),放电时再次用压力加压工具6施加与耐水压相等的压力。如图26(B)、27(B)所示,虚线包围处77内,疏水性多孔质膜11和电极室52、53为了方面描述是分开的,实际上它们是接触的。施加压力后疏水性多孔质膜11的细孔内没有液体。这种情况下,可以将疏水性多孔质膜11视为低导电率膜。因此,如果考虑等效电路,图26(D)和图27(D)所示,对电解质水溶液14不加压时,疏水性多孔质膜11的细孔内因为疏水性电解质溶液14没有渗入,此时仍为低导电率电容器C2,如果对电解质水溶液14加压后,疏水性多孔质膜11的细孔内电解质水溶液渗入后,电路开关(S)变为打开的,正极室和负极室在疏水性多孔质膜密闭容器55(信封型)的介导下短路,2个高导电率电容器(C1)串联排列充放电,如果对电解质水溶液14的压力接触后,两个低导电率的电容器(C2)和两个高导电率的电容器(C1)串联排列保持蓄电。另一方面,负电极室52和正电极室53虽然构造是相同的,但是双层电容器和氧化还原电容器则是不同的。
双电层电容器的负极室52和正极室53的构造如图26(A)、(B)、(C)所示,疏水性多孔质膜11与活性炭67密切接触,它的反面设置有集电极板64,正负电极室52、53与外部空气屏蔽。
氧化还原电容器的负电极室52和正电极室53的构造如图27(A)、(B)、(C)所示,氧化还原电容器如果使用金属板(Al)108,这个金属板与疏水性多孔质膜11面对的面使用电氧化的氧化氧化还原电容器用金属氧化物膜(Al2O3)作为电介质。起到正负电极作用的每个金属板108,在金属氧化物膜109的介导下与多孔质膜11紧密接触。
本发明中,可以从混合的易氧化金属盐水溶液中对每个易氧化金属元素分离回收。将前面提到的氢气制造装置和易氧化金属回收装置数台串联排列并连接起来。从氢气生成装置开始,从混有多种易氧化金属盐的电解质水溶液中,按被析出金属的分解电压从低到高的顺序进行电解精炼,未反应的电解质水溶液转移至后面的易氧化金属回收装置,对该电解质水溶液加压时进行电解精炼,按金属分解电压从低到高的顺序对这些易氧化金属进行回收操作。
本发明的另一个实施方案,是以海水作为原料,使用海上获得的自然能源或临海电力发电厂的深夜电力等电力,生产出氢气和苛性钠直接提供给海上工厂和临海工厂。根据这个方案,海上及/或临海工厂进行前面提到的氢气和苛性钠制造,这些生产出的氢气和苛性钠,按前面提到的在海上和陆地上制造氢化纳,然后在陆地上对氢化钠注水后制得氢气,副产物苛性钠再次生产为氢化钠,建立苛性钠燃料循环方法。而且作为中间生成物的氢氧化钠可以作为充电电池的电解质水溶液被利用起来。
此外根据本发明,对疏水性多孔质膜形成的容器中加入指定的物质,这个容器中的能加入电解质或非电解质以及液体水溶液。在对疏水性多孔质膜施加耐水压相等的液压条件下,该液体浸入疏水性多孔质膜的的细孔,与容器内部的物质发生电解反应、加水分解反应或是溶解反应。
比如说,根据本发明,疏水性多孔质膜制成的容器(反应室)中,加水分解或与水接触后产生气体的物质,加水分解或与水接触后生成产热的物质,加水分解或与水接触后生成吸热的物质,或是加水分解或与水接触后产生的吸热物质或水溶性有机化合物都能在反应室中收集。而且,反应室的外压和内压之差,可以成为疏水性多孔质膜耐水压以上的压力世嘉在疏水性多孔质膜上,将该液体导入反应室内。于是,反应室内容纳的物质与该水溶液反应,发生气体,发生热,吸收热,及溶解反应都会发生,获得的气体或水溶液可以用于医药或营养剂向生物运输或是向水溶液中添加有机化合物。
此外根据本发明,疏水性多孔质膜可以制成药物散布的软管,向指定场所给药。药物供给口至药品水溶液供给源之间的管子用软管固定,药品供给口根据需要连续或间歇施加疏水性多孔质膜渗透压以上的压力,使药品水溶液向希望的位置供给。药品的水溶液包括药物、营养和肥料等水溶液。
而且,根据本发明,内窥镜前端的胶囊内封入加水分解加热剂,通过施加疏水性多孔质膜耐水压以上的压力,介导加水发热分解反应发生,利用这些热量可以对对器官内癌细胞进行加热。
【发明效果】
如前面所说,根据本发明,可以在海水或盐湖水等电解质水溶液中放入高度电绝缘的多孔质氟树脂膜,对多孔质氟树脂膜施加渗透压以上的水压,使多孔质氟树脂膜的细孔内部有电解质水溶液和/或离子通过,通过对水压的调节,可以有效的控制通过疏水性多孔质膜的水溶液或离子量,可以起到开关的作用。这个疏水性多孔质膜放置在电解质水溶液中,可以在正负电极室之间起到隔离膜的使用。对电解质水溶液施加压力时,水溶液发生电解反应,在正极和负极分别生成电极生成物,可以从电解质水溶液中分离回收。这样就能从海水或盐湖等电解质水溶液中直接提取氢气、苛性钠、易氧化金属元素等。这个技术不仅在电解精炼,而且在实际电池或大容量电容器都能使用。以前电解精炼时,只能使用大电力,在高温下对熔融盐进行分解,没有其他办法。有了本发明,只要在常温,而且水溶液中就能电离分解,具有很好的经济效益。特别是从海水中获得金属钠可以作为石油的替代能源,不必担心它们的枯竭,而且是没有地域差异的能源,可以为创造没有资源战争的世界提供贡献。此外,电解质只使用水溶液,将锂、钠和钙等原料用作易氧化金属/空气电池或易氧化金属元素/卤素电池,根据气候条件可以将再生能源储藏在电池中。此外制成的电池是轻量且高效率的,可以用作电动自行车,我们希望它也对二氧化碳和放射线没有的氢气社会发展。
附图说明
图1比较了基本金属/氧电池和基本金属/卤素电池的放电容量。
图2是疏水性多孔质膜(隔离膜)的压力开关原理说明图。A表示电解质水溶液在渗透压以下,B表示电解质水溶液在渗透压以上。
图3A疏水性多孔质膜(隔离膜)的电子开关与溶液的电性质和疏水性多孔质膜的效果比较。
图3B疏水性多孔质膜(隔离膜)的电子开关与溶液的电性质和疏水性多孔质膜的效果比较。
图4简单的示意了正负电极间配置电解质溶液隔离器具的化学反应装置。A是隔离器具是疏水性多孔质膜组成的密闭容器的场合,B化学反应装置是开放容器的场合,C隔离器具是疏水性多孔质膜组成的密闭容器,这个密闭容器在开放容器中位置示意。
图5简略示意了压力加压工具,(A)对疏水性多孔质膜组成的密闭容器直接加压的场合,(B)使用连通管,在水源处用手动或电动加压的情况下。(C)开放容器中放置密闭容器,并且给予水压的情况。
图6说明了在疏水性多孔质膜制成的中空密闭容器(袋)内部充填电解质水溶液的方法,A是中空密闭容器直接加入电解质水溶液的情况,B中空密闭容器(袋)放入溶质,压入水或水蒸气的场合,C是中空密闭容器(袋)内多孔质疏水性多孔质膜介导的压入电解质水溶液,D,中空密闭容器(袋)的疏水性多孔质膜用醇类涂布,抑制羁留电解质水溶液的情况。
图7用疏水性多孔质膜隔离正极和负极的构造示意图和关系说明。
图8是电解质水溶液层和油层的交接面作为负电极面,电解质水溶液电离分解的等价电路。A表示了村元电路概念图,B表示了电路(计算式)。
图9是将油和电解质水溶液的交界面作为负极的油电容器。A是使用疏水性多孔质膜的虚拟负极构造图,B是虚拟电极与地轴垂直,油比重不到1时的构造图,C是假想负极与地轴垂直,油比重超过1的时候的构造图。
图10将气体透过电极室沉入海面下直接与海水电解,产生氢气的装置概念图,A是利用水下水压的电解装置示意图,B是在地上对盐水加压的电解装置示意图。
图11是在开放容器和大型密闭容器中仿佛密闭容器,对水进行电气分解,氢气制造装置的概念图,A是利用淡水湖水面下的水压的电解装置示意图,B是对自来水加压的电解装置示意图。
图12是基本金属氢氧化物(苛性钠)制造装置的概要图,A是负极制造基本金属氢氧化物(苛性钠),正极生成气体(卤素)的装置示意图,B是在负极在负极制造基本金属元素氢氧化物(苛性钠),正极制造酸(盐酸)的装置示意。
图13是基本金属回收装置的概略图,A是负极油充填电极室的油罐中制备基本金属,正极生成气体(氯气)的装置示意图,B是负极油充填电极室的油罐中制备基本金属,正极产生酸(盐酸)的制造装置示意图。
图14是在油和电解质水溶液的交界面形成假想电极的电解精炼装置,A是将中间电极板插入油充电电极室中的电解精炼装置,B是在油充填电极室外配置固体电容器的电解精炼装置。
图15是氢负离子和熔融盐的离子反应,制备氢氧化物金属的装置图。
图16是基本金属氢氧化物和基本金属氢氧化物的熔点和比重比较示意图。
图17是电池的概略图,A是充电时的电池,B是蓄电时电池的示意图,C是放电时电池的示意。
图18是氢氧化基本金属的溶解度和温度关系的示意图。
图19是卤化(氯化)基本金属的溶解度和温度关系的示意图。
图20是基本金属/氧电池和基本金属/卤素电池使用的电解质在水中的溶解度示意图。
图21是基本金属/空气电池的概略图,A是在正极的空隙中放置碳素版作为充电用辅助电极的示意图,B是将金属的氧化物作为电池的正极。
图22是,基本金属/氯电池的概略图,A表示单层电池,B表示层叠电池。
图23是,基本金属/溴和基本金属/碘电池的概略图,A是不受空气影响的金属作为负极的电池示意图,B是负极易受金属影响元素周期表第1族和第2族的金属元素作为负极的电池。
图24是,基本金属/氟电池的概略图,A是Al/F电池的示意图,B是Al/F电池的示意图,B是K/F和Na/F电池的示意图。
图25是电容器(冷凝器)的概念图,A是充电时的电容器示意图,B是蓄电时电容器,C是放电时电容器,D是充电、蓄电、放电的动态电路说明图。
图26是双电层电容器的概略图,A是充电时的电容器,B是蓄电时的电容器,C是放电时的电容器,D是充电、蓄电、放电的动作电路说明图。
图27是氧化还原电容器的概念图,A是充电时的电容器,B是蓄电时的电容器,C是放电时的电容器,D是充电、蓄电、放电的动作电路说明图。
图28是多孔质氟树脂膜的渗透压和盐浓度的关系示意图,A多孔质氟树脂膜的细孔径是3um的情况是,B是多孔质氟树脂膜的细孔径是10um的情况下。
图29是海面下氢气制造装置的概略图。
图30是多级海面下氢气制造装置的概略图。
图31是湖面下氢气制造装置的概略图。
图32是利用自来水的建议氢气制造装置概略图。
图33是从氯化钠的直接制备苛性钠和氯气的装置概略图。
图34是从氯化钠水溶液直接制备苛性钠和盐酸的装置概略图。
图35是从基本金属氯化物水溶液中直接制备基本金属元素的装置概略图。
图36是从基本金属氯化物水溶液中直接制备基本元素和盐酸的装置概略图。
图37是利用虚拟电极的基本金属制造装置概略图,A示意了该装置,B是等价电路的示意图。
图38是今本金属制造装置的概略图。
图39是封桶型密闭容器内电解质水溶液截流装置的概略图,A是电解质水溶液截流前的示意图,B是电解质水溶液截流后的示意图。
图40是电解质加压型充电电池的概略图,A是电解质水溶液不加压时的示意图,B是电解质水溶液加压的场合的示意图。
图41是层叠型钠蓄电电池的概略图,A是截面图,B是外观图。
图42是氧化还原电容器的概略图,A是截面图,B是等效电路。
图43是混合基本金属盐的水溶液中分别提取基本金属的装置概略图。
图44是苛性钠循环燃料的概略图。
图45是加水分解反应装置的概略图。
图46是水培用水分燃料供给装置的示意图。
图47是内窥镜医疗装置的说明图,A是人体断面,B是营养药物胶囊的示意图,C是癌症温热治疗胶囊的示意图。
【符号说明】
1…密闭容器
2…开放容器
3…负极电极室
4…正极电极室
5…连通管
6…压力加压器(气缸)
7…橡胶滴管、移液器
8…带棘轮电动加压装置
9…储水槽
10…水头位置
11…疏液(水)性多孔质膜(隔离膜)
12…生成气体回收软管
13…酒精
14…电解质水溶液
15…溶质(药品)
16…油充填电极室
17…正极板(油槽内)
18…中间电极板(油槽内)
19…虚拟电极面(油和电解质的交界面)
20…电荷(电压)
21…电解质内的正极版
22…油
23…油(比重1以下)
24…油(比重1以上)
25…酸(如果是氯化物即盐酸)
26…阴极生成物回收口
27…疏水性多孔质膜(淡水渗透用)
28…水(利用睡呀)
29…大型密闭容器
30…氢气制造装置
31…(基本金属氢氧化物苛性钠)
32…基本金属卤化物水溶液(氯化钠水溶液)
33…浓酸(盐酸)
34…水供给口
35…负极产物回收口
36…负电极板
37…正电极(碳素纤维、碳素粒、多孔质碳素)
38…正电极板
39…易氧化金属水溶液供给槽
40…水充填电极室
41…气体透过电极室
42…正极生成物回收口(取出盐酸用)
43…网状负电极(碳素纤维、金属网)
44…多孔质碳素负极板兼隔离膜
45…氢气
46…易氧化金属氢氧化物熔融盐(苛性钠)
47…氢气压入口
48…熔融盐加热器
49…氢化易氧化金属(氢化纳)
50…氢负离子
51…氢化易氧化金属回收口
52…负极电极室(电池、电容器用)
53…正极电极室(电池、电容器用)
55…信封型密闭容器
56…充电用辅助正电极(网状金属)
57…外气遮蔽型负电极室
58…碳素制空隙板电极(活性炭)
59…金属氧化膜(电池正极用)(CuO,AlO3,ZnO2)
60…电池板(电池用)(Cu,Al)
61…树脂膜
62…负电极板(电池用)(Al,Mg,Ca,Zn,Ni,Pb)
63…金属卤化物膜(电池正极用)(ZnCl2)
64…集电极板(电池用)(Cu,Al)
65…负极电极板(Al,Mg,Zn)
66…正极(负极使用金属卤化物)
67…活性炭和碳素纤维
68…溴液体
69…碘液体
70…石墨板
71…铝(负极)电极板
72…电介质溶液(油性、水性)
73…板电极(电容器)
74…电双层电极(电容器)
75…氧化还原电极
76…混合电容器电极
77…虚线宝汇出
78…含空隙的导电材料(金属纤维、碳素纤维、活性炭)
79…电化学电容器用水溶液(稀硫酸)
80…稀苛性苏打(电化学电容器用电解质水溶液)
81…不锈钢纤维
82…碳素纤维
83…电极间距离(d)
84…海面下氢气制造装置
85…多级型海面下氢气制造装置置
86…湖面下(海面下)氢气制造装置
87…四角柱形密闭容器
88…淡水(水)
89…利用自来水的简易氢气制造装置
90…从氯化钠水溶液中直接制造苛性钠和氯气的装置
91…从氯化钠水溶液中直接制造苛性钠和盐酸的装置
92…易氧化金属制造装置
93…1次压力调节器(气体透过用电极室)
94…吸引口(用真空泵降至渗透压以下)
95…易氧化金属和盐酸直接制造装置
96…利用虚拟负电极的易氧化金属制造装置
97…氢化易氧化金属制造装置
98…电解质水溶液截流装置
99…吸引口(真空泵)
100…疏水性多孔质膜(11a)
101…疏水性多孔质膜(11b)
102…截留用电解质溶液
103…电解质加压型充电电池
104…锤子
105…空气进入口
106…层叠型苛性钠电池
107…氧化还原电容器
108…氧化还原电容器用金属板
109…氧化还原电容器用金属氧化膜
110…海上工厂
111…临海工厂(临海发电厂)
112…氢气发生装置
113…浮力重力发电装置
114…加水分解反应控制装置
115…疏水性多孔质氟树脂密闭袋
116…药品
117…气体
118…水溶液补给用管(软管)
119…植物(蔬菜、果蔬)
120…药品散布喷壶(疏水性多孔质膜制成的袋子和管子)
121…补给用营养(蔬菜大棚))
122…控制室
123…导管(管)
124…发热剂(CaO)
125…胶囊。
具体实施方式
接下来,根据图28~47,对本发明有效的实施方法进行说明。
本发明的根本是关于疏水性多孔质氟树脂膜的测定,电解质水溶液能够通过疏水性多孔质氟是指膜的最小压力(疏水性多孔质服树脂膜两侧的压力差,是电解质水溶液透过疏水性多孔质氟树脂膜的最小压力差,这个也称为渗透压)和电解质水溶液的电解质浓度的关系曲线。渗透压记载在日本工业规格(JIS)L1092:2009。
图28(A)是细孔径3um的氟树脂制疏水性多孔质膜(日東電工製PTFE多孔質膜NTF-1133)在使用不同浓度的氯化钠水溶液作为电解质水溶液的结果。一般情况下,渗透压是相对于水的树脂。此外。一般的海水的盐分(氯化钠)的浓度约3%(重量),氯化钠在水中的饱和浓度是25%(重量)。于是,向水中加入氯化钠的浓度从0%-25%,在室温时测定了氯化钠浓度与渗透压的关系。前面提到的氟树脂制疏水性多孔质膜的渗透压,氯化钠浓度0%时为430mmHg(0.57気圧)、氯化钠浓度10%为320mmHg(0.42気圧)、氯化钠浓度20%为280mmHg(0.37気圧)、氯化钠浓度25%为270mmHg(0.36気圧)。氯化钠浓度越高渗透压相应下降。此外,电解质水溶液温度上升,渗透压也会变小。
如图28(B)所示,细孔径为10um的氟树脂制疏水性多孔质膜(フロン工業F3011-3)与电解质水溶液相对应,不同浓度的氯化钠水溶液使用时的结果。这种氟树脂制疏水性多孔质膜的渗透压在氯化钠浓度0%时为120mmHg(0.16気圧),氯化钠浓度2%为50mmHg(0.07気圧)。
将图28(A)所示结果和图28(B)所示结果结合起来,可以得知,多孔质膜细孔径越大渗透压就会越小。此外电解质浓度越高,渗透压越低。同样的渗透压下,疏水性多孔质膜分割的不同浓度电解质,浓度高的一侧会向低的一侧流动。也就是说,疏水性多孔质膜形成的密闭容器中存在高浓度的电解质溶液,密闭容器外侧有低浓度的电解质水溶液,密闭容器的外侧会有电解质水溶液的泄漏。为了阻止这一情况,降低密闭容器内紧密接触的电极室的压力,密闭容器的外侧的低浓度电解质水溶液通过疏水性多多孔质膜进入密闭容器内部,另一侧疏水性多孔质膜通过后进入电极室采用的线路和和压力差控制是必须的。
图29所示的是海面下氢气制造装置的概略图。如图7所示,气体透过电极室内的负极电极室和正极电极室的电极都用空隙。将他们沉入海面下后直接对海水进行电解,制造氢气。
图29所示的是海面下氢气制造装置84,正负电极室52、53的外壁上,纵向的二分之一是由盐化氯乙烯树脂管制成,二分之一是很多开口的33um的PTEE多孔质膜((日東電工NTF-1133)11。如图负极电极室52的截面图所示,负极电极室52内,放入了不锈钢纤维81(日本精線株式会社ナスロン(登録商標)「ウエブ」),另一个正极电极室53的截面图内,正极电极室53内,放入了碳布(碳素纤维)82。此外,电极室52、53的最上部连接着回收管12对生成气体分别回收,回收管12的内部分别铺设正极和负极的的引线。
这里的电解质水溶液14是海水,海水的平均盐浓度为3.5%重量。另外如图28A水师,细孔径3um的多孔质氟树脂膜的渗透压与盐浓度的关系,3.5%的氯化钠水溶液对多孔质膜的渗透压为380mmHg。水深10米是水压是1个大气压(760mmHg),将位置水头放置在海面下5m。海水温度在23摄氏度,导电率为0.03s/cm。在这里将电极间距离d(83)设定为10mm,在两电极间施加1.5v电压,产生1m3氢气,0.5m3的氧气需要的电力是8.3kWh。顺便说一下,这里使用的氢气制造装置在体电视,使用25%的氯化钠电解质水溶液(导电率0.18s/cm),电极间距离d(83)固定为10mm,两电极间给予1.5v电压,产生1m3氢气,0.5m3氧气所需的电力为10kwh。
图30是在海面下电解海水生成氢气的多级海面下氢气制造装置构造图。如图7所示,将电极中有空隙的气体透过电极室组成的负极电极室52和正极电极室53沉入海面下直接对海水电解制造氢气。电解质水溶液14使用对俄海水平均浓度在3.5%。图28A所示的细孔径3um多孔质氟树脂膜的渗透压和盐浓度的关系可以看出,3.5%氯化钠的渗透压是380mmHg。因此多级型海面下氢气制造装置84放置在海面下(位置水头(h)10)约5米以下的地方。
图30的多级型海面下氢气制造装置85中,正负电极室52、53的氟树脂疏水性多孔质膜11使用细孔径3um的PTEE多孔质膜(日東電工NTF-1133),正负电极室的外壁使用氯乙烯制作,电极室52的最上部用回收软管收集生成的氢气,负极电极室52和正极电极室53交替连接排列,每个负极电极室52生成的氢气和正极电极室53生成的氧气使用管子一起回收。本实验使用的多级海面下氢气制造装置84是由正负3族氢气回收用的电极室52和氧气回收用的电极室53并列排列,每个电极室间距d(83)10mm。负极电极室52的电极材料时不锈钢纤维81日本精線株式会社ナスロン(登録商標)「ウエブ」),正极点击室内使用的是碳布(碳纤维)82。海水中电解质的盐浓度是3.5%,海水的温度是23摄氏度,导电率为0.03s/cm。这里对两电极施加的电压是1.5v,生成1m3的氢气和0.5m3的氢气所需要的电力是17kwh。
图31是湖面下氢气制造装置示意图。原理如图11所示,疏水性多孔质膜制成的密闭容器中封入高浓度的电解质水溶液,将密闭容器外侧的水溶液压入疏水性多孔质膜,直接高效率的生成氢气和氧气及氯气。将疏水性多孔质膜制成的容器沉入充满高浓度电解质水溶液(高溶解度,高导电率电解质水溶液)的淡水湖、池塘或海水中,将淡水等低浓度电解质水溶液压入疏水性多孔质膜后,水溶液发生电离分解产生氢气。
如图31所示,湖面下(海面下)的氢气制造装置86中,负极电极室52和正极电极室53之间装备有四角柱形密闭容器87,四角柱形密闭容器87中,四个侧面中的两个侧面(与正负电极室52、53接触的侧面)分别有疏水性多孔质11,或者至少一个侧面由疏水性多孔质膜(淡水渗透用)27组成。四角柱型密闭容器87内放置约规定3的硫酸或规定4的苛性钠水溶液使电离增强,四角柱型密闭容器87的淡水渗透用疏水性多孔质膜27从外部将淡水88和低浓度电解质水溶液压入后在正负电极室电解生成氢气和氧气,这里使用的酸或碱被称为电离催化剂。但是图28A的疏水性多孔质氟树脂膜(细孔径33um)的氯化钠水溶液对水的渗透压是430mmHg,与10%氯化钠水溶液的330mmHg相比,存在100mmHg的压力差。因此,疏水性多孔质氟树脂膜(电离隔离膜)11的细孔径使用比疏水性多孔质膜(淡水渗透用)27的细孔径更小的孔径,也就是对疏水性多孔质氟树脂膜(电极隔离膜)进行亲水性处理,将盐浓度的疏水性多孔质氟树脂膜(电极隔离膜)11的渗透压和淡水的疏水性多孔质膜(淡水渗透用)27的渗透压等值或近似值是本发明的特征。这里的氢气制造装置86也可以用于海水或温泉水。本发明的装置构造是在水面上对正读电极室生成的气体进行回收,可以在水面上进行吸引。因此,如过对正负电极室的气体使用真空管进行吸引,不需要将氢气制造装置87下降到水头位置。此外,正负电极室52、53的气体压比推入疏水性多孔质膜(淡水渗透用)27的淡水或稀电解质水压低,因此硫酸不会从密闭容器的疏水性多孔质膜(淡水渗透用)88向外部淡水流失。而且,正负电极室的气体使用真空管吸引,因为要控制正负电极室的气体呀,疏水性多孔质氟树脂膜(电极隔离膜)11、27也可以是同种东西。此外,装有疏水性多孔质膜(淡水渗透用)27的密闭容器外的水压变高,电极室侧的气体压会变低,因此有必要维持压力差。而且,为了保持气体生成处的压力在一定数值以下,产生的气体在出口处放置压力调节器93,这是对气体透过电极室52、53生成的气体进行压力调整的最简单方法。如果将这种构造用于湖面下氢气制造装置86,四角柱密闭容器87内先放入1~5规定的硫酸或1~10规定的苛性钠,从外部供给生成氢气或氧气相当量的淡水产生电解反应,可以连续制造氢气和氧气。本发明将硫酸或苛性钠称为电离催化剂。这个只眼在正负电极间放置10~100mm宽度的四角柱形密闭容器87,负极电极室52的电极材料横断面所示为不锈钢纤维81(日本精線株式会社ナスロン(登録商標)「ウエブ」),正极使用碳布(碳素纤维82)。四角形密闭容器87内放入2.5规定的硫酸和2.5当量的苛性钠,分为两种情况,将氢气制造装置86放入深3m的水池中,负极电极室52和正电极室53的气体压分别保持在200~400mmHg,使用压力调节器93对进入的真空排气,测定氢气的生成效率。将高浓度电解质水溶液79中加入硫酸后的导电率是0.8/cm,加入2.5当量的苛性钠的导电率是0.3s/cm。因此对氢气制造装置86的两电极间施加1.5V的电压,高浓度电解质溶液中有硫酸的情况时为生成1m3氢气、0.5m3的氧气需要电力2.3kwh,苛性钠为5.2kwh。
图32是利用自来水的简易氢气制造装置构造图。原理如图11(B)所示,将疏水性多孔质膜制成的密闭容器插入大型密闭容器中,对自来水施加疏水性多孔质膜渗透压以上的水压,一边进行自来水的供给,一边可以连续制造氢气。
如图32所示的利用水压的简易氢气制造装置89,将疏水性多孔质膜组成的密闭容器1放入大型密闭容器29,对自来水管28施加疏水性多孔质膜(淡水渗透)27渗透压以上的压力,同时将淡水(自来水)88经疏水性多孔质膜(淡水渗透用)27介导,持续压入3N(约8%)的硫酸溶液,同时在正负电极室3,4(气体透过电极室52,53)进行电解反应,负极电极室生成的气体用回收软管收集氢气,正极电极室4生成的氧气使用回收软管12回收。这种气体再此回收,如果对淡水(自然水)进行压力调整,为了保持气体生成侧的压力在一定数值一下,制造的氢气在取出钱,配置压力调整器93,对气体透过电极室52、53生成的气体进行压力调整。特别是硫酸的浓度在2~5规定时导电率最高,为了维持这种浓度需要对自来水出水口的淡水压力进行调整,产生的氢气和氧气的平衡通过真空排气和压缩机气缸等装置调节。
图33说明了从氯化钠水溶液制直接备苛性钠和卤素的装置。原理如图12(A)(B)所示,将正负电极室分别连接,对疏水性多孔质膜构成的密闭容器是假渗透压相等的压力,对氯化钠溶液加压发生电极反应,是负极电极室内部生成苛性钠。疏水性多孔质膜内的对氯化钠水溶液施加渗透压相等的压力。
图33所示的氯化钠水溶液中直接制造可行钠和氯气的装置90中,在中央放置密闭容器1,里面隔开放置了两个疏水性多孔质膜11。密闭容器1的一侧放置的负极电极室3是有充满水的电极室40构成,负电极板36是由碳素或镍组成。密闭容器1的另一侧设有正极电极室4,正极电极室4是由气体透过性的电极室41构成的。配置的是有空隙的电极材料。并且,密闭容器1内充满了浓度为26%的氯化钠水溶液32.氯化钠的溶解度几乎不受环境温度影响,生成的苛性钠受到环境温度的影响。如图18所示,苛性钠的溶解度在40摄氏度时为56%,80摄氏度时溶解度达到74%,为了制备高浓度苛性钠31,可以向电极室40内注入热水或对电极室40进行加热。本实验使用的简单方法是向负极电极室3的水供给口34注入100摄氏度一下的热水。在这里,一个独创性的方法在电解开始时预先在负极电极室3的水中加入苛性钠,提高电解效率。因此,一边维持着氯化钠水溶液32的浓度在26%,一边用压力加压工具施加与疏水性多孔质膜11渗透压相等的压力,在负电极40生成苛性钠,腹肌生成物收集口35回收浓缩的苛性钠,对顶端放置有回收软管12手机生成的氢气。此外在正极电极室4的最上部放置有气体回收软管12回收氯气。为了保证氯气生成侧的压力在一定值一下,产生的气体在取出前,需要配置压力调节器93,调节苛性钠生成室31的气体压力不超过1以上。在两电极间施加4v的电压,电流强度为20A,生成1Kg的苛性钠需要3kWh。
图34表示了从氯化钠水溶液直接制造苛性钠和盐酸的装置。原理如图12(B)所示,正负电极室分别连接,对氯化钠水溶施加与密闭容器内的疏水性多孔质膜渗透压相等的压力,发生电解反应,在负极电极室内部制备苛性钠。疏水性多孔质薄施加与氯化钠水溶液相等的渗透压。
如图34所示的从氯化钠水溶液中直接制造苛性钠和氯气的装置91,在中间放置了密闭容器1,里面分别配置了两块疏水性多孔膜11。密闭容器1的一侧配置有负极电极室3,里面有水充填构成了电极室40,负电极板配置有碳素和镍。密闭容器1的另一侧放置有正极电极室4,里面有水充填构成电极室40,正电极板38配置有碳素。然后密闭容器1内装满了浓度为26%的氯化钠水溶液32,向正极电极室4的水供给口34和负极电极室3的水供给口34注入100摄氏度以下的热水。而且在电解开始时,向负极电极室3的水中预先加入氢氧化钠水溶液31,向正极电极室4的水中预先加入盐酸可以分别提高电解效率。一边维持着氯化钠水溶液的浓度维持在26%,使用压力加压器对氯化钠水溶液是假疏水性多孔质膜11渗透压想的的压力,在负电极室生成苛性钠31,负极生成物回收口35回收浓缩的氢氧化钠溶液,最顶端放置的生成气体回收软管收集氢气。此外正极电极室40的正极生成物回收口(盐酸取出口)42对浓缩盐酸进行回收,在最顶端的气体回收软管12回收氧气。负极电极室3的电极室40制造苛性钠31,电极室41制造盐酸33,这些物质都是电传导率很高被疏水性多孔质膜11隔离。如果对密闭容器1内的电解质水溶液14(氯化钠水溶液32)施加与渗透压相等的电解质水溶液,可以很好的电解。
图35是从基本金属卤化物水溶液中直接制备基本金属的装置。原理如图13A所致,密闭容器负极侧的疏水性多孔质膜组成的隔离膜接到与碳素制空隙电极接触,他的背面充满油,比油比重轻的基本金属(Li、Na、K)的上层收集,比油比重重的金属(Mg,Ca,Ba,Sr,Al)在下部回收。
如图35所示,基本金属元素制造装置92,在装有疏水性多孔质膜11的密闭容器内根据所要制备的金属,选择相对应的卤化物。比如从NaCl、KCl、LiCl、MgCl2、CaCl2、BaCl2、SrCl2、AlCl3选择一种。如图19所示,金属卤化物出了NaCl以外,随着溶液温度的升高,溶解度也有上升的倾向。比如说如果将密闭容器1内的基本金属卤化物水溶液32的液体文丛使用内部加热器加热到60摄氏度是,NaCl是27%、KCl是31%、LiCl是50%、MgCl2是38%、CaCl2是58%、BaCl是は32%、SrCl2是47%、AlCl3是32%。从这些结果可以看出基本金属卤化物水溶液32的液体温度从25摄氏度上升到80摄氏度,达到饱和溶解度在施压压力,进行电力分解是非常有利的。图35所示的基本金属元素制造装置92的负极电极室3充填油构成电极室16,点击哪使用由碳素纤维组成的网状负电极43,油23使用比重为0.8的轻油。另一方面,正极电极室4是由气体透过性电极室41构成的,使用碳素纤维组成的正电极37,正极电极室4使用回收软管12手机产生的气体。基本金属卤化物水溶液32使用LiCl时,因为80摄氏度时溶解度为53%,并且Li的熔点是179摄氏度,比重0.54(图16),大约50%的LiCl在80摄氏度电解,金属Li漂浮在负极电极室3的轻油23的最上部,从负极电极室3的最上部的负极生成物口35进行回收。另一方面,正极电极室最上层生成的氯气通过气体回收软管12回收。为了保持氯气生成侧的压力在一定数值一下,产生气体在生成口处放置压力调节器93.预备实验室,28%浓缩的氯化钠水溶液25摄氏度是,正负电极间压力4~5v,电流密度为10A,通电1h,油充填电极室16内的轻油中析出8g金属Na。
图36是从基本金属卤化物水溶液中直接制造基本金属元素和盐酸的装置构造图。原理如图13AB所示,密闭容器的负极侧经疏水性多孔质膜组成的隔离膜介导与空隙电极接触,背面有油充填,比油比重轻的基本金属(Li,K,Na)会在上面,比油23比重重的基本金属(Mg,Ca,Ba,Sr,Al)在最下部回收。负极产物的生成法如前面所述。一方面正极制备的盐酸,图36的基本金属和盐酸直接制造的装置95和正极电极室4内采用水充填电极室40,为了使负离子与水反应,再向水供给口34预先添加了稀盐酸水溶液后,疏水行多孔质膜11介导网状负电极板43和正极板38之间进行电极反应,离子反应式为イオン反応(2Cl-+2H2O→2HCl+O2)。这里生成的盐酸33为浓盐酸从取出口42回收,氧气通过气体回收软管12装置回收。
图37是基本金属卤化物水溶液中利用虚拟电极的基本金属制造装置的示意图。原理如图14(B)所示,周期表第1、2族的元素组成基本金属盐水溶液和油面的交界面形成虚拟电极,对基本金属盐水溶液进行电解,在油层内回收负极生成物。油和电解质水溶液的交界面形成虚拟电极是十分容易考虑到的。但是,这种虚拟电极必须是负极才能得到负极生成物。因此将虚拟电极变为负极的方法如图37B的等效电路[村元电路]和图37利用假想电极制造基本金属的装置所示。通过压力加压器6使电解质水溶液14的渗透压为ON/OFF的状态,图37B的等价电路表明了了开关(S)、电解质水溶液14(R),油充填电极室16内的油23(C2)、电压(E)、外部放置了大容量电容器(C1)。先对大容量电容器C1施加电压后(E),施加渗透压的压力使两电极室面的开关(S)是ON的状态,C1内储蓄的电荷供应串联电容器C1和C2,虚拟电极面19作为负极,R作为电位,发生电解反应,在虚拟负极的电极面19中,比油比重轻的基本金属(Li,K,Na)浮在上层,比油比重重的金属(Mg,Ca,Ba,Sr,Al)在最下层回收.同时正极电极室4的气体透过电极室41的最上部有生成气体会后软管12回收氢气。为了在氯气生成一侧保持一定值一下的压力,制造的气体在取出口前放置压力调节器93,还有利用虚拟电极的基本金属制造装置。
图38表示的是氢化基本金属制造装置。一般的,氢化纳是对苛性钠的熔融盐电离分解,获得的金属钠在高温与氢气化合制造。这种金属钠的制造费用十分高昂。如图15所记载,苛性钠的熔点在318摄氏度。因此将苛性钠放入容器加热到318摄氏度以上时,会形成离子化的熔融盐。如图38的氢化金属制造装置97所示,苛性钠的熔融盐(Na++OH-)与氢气的阳离子(H+)和氢气的阴离子(H-)50反应,反应式为Na++OH-+H-+H+→NaH+H2O。因此,为了在苛性钠熔融盐46中生成氢气的负离子(H-)50,在气体透过电极室41的多孔质碳素负极兼隔离膜44内,将氢气从丫入口47压入,这种多孔质碳素负极兼隔离膜44组成的负电极44和正电极板38放置苛性钠熔融盐46,并且在两电极间给予氢气阴离子50的生成电位,苛性钠熔融盐中的钠(Na)和氢负离子反应生成氢化钠(NaH)49,不需要热反应只用离子反应就能制造。而且氢化纳(NaH)49的比重比苛性钠熔融盐46的比重轻,而且熔点比苛性钠46的熔点高很多,可以作为固体漂浮在液面上,十分容易回收的装置。
图39是展示了信封型密闭容器内的电解质水溶液拘禁装置。封筒形密闭容器55是2层疏水型多孔质11膜重叠,四周使用350摄氏度热熔融制造的。这个封筒型密闭容器55在电池的电解质水溶液潴留容器用途很多。因此,这种封筒形密闭容器55内为了拘禁电解质水溶液14,102需要电解质水溶液拘禁装置98.。封筒形密闭容器55的两面如图39(A)(B)所示,具有疏水性多孔质氟树脂膜100和疏水性多孔质氟树脂膜101。这些疏水性多孔质膜100,101的渗透压如图28所示,随着电解质水溶液的浓度有差异。这里如图39(B)所示,用压力加压工具6加压后,拘禁用电解质水溶液的102水压设为(WP102),信封型密闭容器55内的电解质水溶液的水压设为(WP55),拘禁用电解质水溶液102一侧的疏水性多孔质氟树脂膜100的渗透压设为(WP100)、吸引口99侧的疏水性多孔质氟树脂膜101的渗透压设为(WP101),吸引口99的空气设为(P99)。拘留用电解质水溶液102通过疏水性多孔质氟树脂膜100的细孔进入密闭容器55内部的条件是WP102≧WP55+WP100,为了潴留封筒型密闭容器55内的电解质水溶液,使用吸引口99吸引的负压条件是WP101≧P99≧-WP101。如果两面使用的疏水性多孔质氟树脂膜100,101是同一种材质,即WP100=WP101。因此如图39B所示电解质水溶液拘禁装置98在吸引口99一侧,负压维持在疏水性多孔质氟树脂膜101的渗透压以上(-WP101),使用压力加压器6开始对拘禁用电解质水溶液102加压后,同时吸引口99的压力变换为(+WP101),封筒型密闭容器55内可以封入拘留用电解质水溶液。
图40表示的是电解质水溶液加压型蓄电电池。图40(A)表示的是电解质加压型蓄电电池103的构造,疏水性多孔质氟树脂膜11作为电极的隔离膜的封筒型密闭容器55内封入电解质水溶液55,夹在负极电极室52和正极电极室53之间,使用锤子104增加重量,出现如图40(A)(B)所示的电路。如果去掉锤子104点位又会变为0V。本实验中负极电极室52的负电极板36使用铝板,正极电极室53的正电极板38使用AlCl3、ZnCl2、MgCl2等的金属氯化物63。首先用原电池做预备实验,在内部封有10%氯化钠盐溶液的信封型密闭容器55的两面,镁板制成的负电极和电极面形成氧化膜的锌板组成的正殿脊之间放置细孔径33um的疏水性多孔质氟树脂膜11,如图28所示使用锤子104施加相当于330mmHg的压力,可以获得3.5v的发电力,去除锤子104后电压值为0.接下来用充电电池做预实验,封筒形密闭容器55内封入浓度为25%的氯化铝溶液,两面都夹有氯化铝电极板,施加与疏水性多孔质氟树脂膜11的相等的渗透压,六十分钟可以进行10安培的直流充电。如果此时去除锤子104,充电结束。这是封筒形密闭容器55内部的氯化铝水溶液浓度为23%,理论上可以充10%的电力。如果此时将锤子104取出,1个月后,对电解质加压型充电电池103再度用锤子104加压,可以产生3.5v的发电力,去除锤子104后电压值为0。如果反复对锤子104安装和接触,封筒形密闭容器55内部的氯化铝水溶液的浓度没有变化,证实内部没有发生自放电。
图41表示层叠型苛性钠充电电池。如图21所示,电解质使用苛性钠水溶液,正电极使用空气,负电极使用碳素纤维,充电时在碳素的空隙中有钠析出。如图41A的断面图所示,层叠型苛性钠充电电池106为封筒型密闭容器55,容器内夹着负极电极室52和正极电极室53,封筒形密闭容器55两侧为疏水性多孔质氟树脂11制成的袋子,内部封入的电解质水溶液14为1~8当量的苛性钠,负极电极室52,57是Na板状电池或碳素制空隙电极板内部或表面有Na吸附,并且负电极周围有树脂膜61包围,或者是负电极内部有油22的负极电极室。另一方面,正电极室53的氧气电极是碳素制成的,在空隙板电极(活性炭)58内有空气吸附,并且疏水性多孔质膜11和碳素制多孔质膜11和碳素制空隙板电极(活性炭)58之间配置有充电用辅助正电极(网状电极)56,谈素质空隙板电极(活性炭)58不会发热,电力由碳素制空隙板电极(活性炭)58背面的集电极板64提供。这个电池的概览如图41(B)所示,层叠型苛性钠充电电池106的周围有树脂膜61包裹与外界隔绝,对封筒形密闭容器55内的电解质水溶液14使用锤子104加压时进行充电,充电完成后解除对电解质水溶液14的加压,维持蓄电状态,放电时对电解质水溶液14加压。苛性钠水溶液如图18所示在水中的溶解度很高,室温达到50%。首先在疏水性多孔质氟树脂膜11组成的封筒形密闭容器55的内部封入50%的苛性钠水溶液,负极电极室52,57周围用树脂膜61包围,并且含油的碳素制空隙电极组成空气遮蔽型负极电极室57,正极用树脂膜61包围,摒弃人空气出入的空气出入口105的活性炭为空隙电极板58,并且疏水性多孔质膜11和活性炭制成的碳素制空隙板电极58之间为具备网状的充电用辅助正电极56的正电极室53。
这些外部遮蔽型负极电极室57和正电极53之间有疏水性多孔质氟树脂膜11组成的封筒形密闭容器55.这里首先作为预备实验在苛性钠电极106上部的11用锤子施加与疏水性多孔质氟树脂膜渗透压相等的压力,在这种状态下,充电用辅助正电极56和外气遮蔽型负极电极室57内的碳素制空隙板电极之间10A充电60分钟后,去除锤子,充电完成。此时封筒形密闭容器55内部的苛性钠水溶液浓度为43%,理论上可以充电10分钟。这里外气遮蔽型负极电极室57内的碳素制空隙板电极和铜板组成的集电极板64之间施加电荷,此时再次用锤子104加重,放电开始,起电力为3v。此时取出锤子104,1个月后,再度对锤子104施加压力,发电力显示为3v,将锤子104取出后电压值为0v。如果重复对锤子104施加和解除,封筒形密闭容器55内部的苛性钠水溶液浓度没有变化,内部没有自放电可以实证。
图42显示了氧化还原电容器的构造。工作原理如图27所示,正负两电极的金属板表面预先形成极薄的氧化膜,,配置强导电体电容器,构造上正极和负极是一样的。对氧化还原电容器107的电路说明,图42B所示的等价回路,C1是负极电极室52,图42A的截面图说明氧化还原电容器用的金属板108的表面有极薄的氧化还原电容器用氧化膜109,从而形成强导电体。但是正极电极室53和负极电极室52构造相同材料也相同。这些正负一对的电极室52、53中间夹有疏水性多孔质膜1的封筒形密闭容器。这个疏水性多孔质膜11的等价回路是42B的低导电率电容器(C2)和开关(S)。特别是本发明的封筒形密闭容器55的内部是碳素纤维或金属纤维等组成的含空隙导电材料78,而且那些空隙中有电化学电容器用电解质水溶液(稀硫酸)79浸泡。此时用压力加压工具6施加渗透压相等的水压,稀硫酸侵入疏水性多孔质膜11的细孔内,电路开关(S)为ON,正极室和负极室被封筒形密闭容器55的内部的碳素纤维或金属纤维等组成的含空隙导电体78短路,2个高导电率电容器(C1)呈串联状态进行充放电,对电解质水溶液14的加压解除后,2个低导电率电容器(C2)和2个高导电率电容器(C1)呈串联状态保持蓄电。电解质水溶液14在未加压时,疏水性多孔质膜11的细孔内没有电解质水溶液浸入,所以是低导电率电容器(C2),对电解质溶液14加压后,疏水性多孔质膜11的细孔内电解质水溶液浸入,电路开关(S)变为ON,正极室和负极室在疏水性多孔质膜制密闭容器(封筒形)55介导下短路,两个额高导电率电容器(C1)呈串联状态进行充放电。如果解除对电解质水溶液14的加压,2个低导电率电容器(C2)和2个高导电率电容器(C1)串联排列,保持蓄电状态。这里氧化还原电容器使用金属板108为铝(Al),氧化还原用金属氧化膜109为氧化铝(Al2O3)。
图43是海水或盐湖水或是温泉水或工业排水等的混合盐水溶液中对第1族元素Na,K,Li或第二族元素Mg、Ca、Sr、Ba等基本金属元素的选择回收方法,盐浓度高的溶液回收效率也高。因此首先要做的是,使用热或反渗透膜法脱水后,或海水电解制得氢气后对废液(浓缩盐水)进行电解。但是,如图19所示,基本金属卤化物的溶解度跟随元素有很大的不同,溶解温度升高后,溶解度也会上升。比如说,80摄氏度是ZnCl2溶解度为84.4%、CaCl2为60%、LiCl为53%、KCl为34%、NaCl为28%である。虽然希望析出的元素溶解度越高越好,实际上需要从分解电压低的溶质开始。所以首先是水的分解电压1.4v以上,MgSO4:1.62V、CaSO4:1.904V、MgCl2:3.952V、NaCl:4.11V、CaCl2:4.23V、SrCl2:4.286V、BaCl2:4.316V、KCl:4.317V、LiCl:4.441V逐渐提高电压,每种元素洗出后,将废液转移到后面的析出装置,从多个基本金属元素中选择回收单个元素称为可能。
图44是苛性钠燃料循环的模式图。本发明想要将这个燃料循环在海上实施。能量资源、材料资源、大海是资源的宝库。如本发明人在非专利文献3和4所述的那样,地球全部的70.8%是海洋,海水的3.5%是盐,1升海水中含有2.18gNaCl。而这个钠(Na)证实下一代化石燃料或核燃料的可替代能源。钠制成的氢燃料不会释放CO2和放射能,是干净的能源,而且不用担心它的枯竭,也不会受到资源生产国的霸权主义和政策影响,可以创造没有资源战争的和平世界。产业与其在消费地设立不如在原料位置设立更好。而且因为要对原料加工,电力在原料采集地的附近是更有希望的。因此在海洋上建立海洋工厂110,直接对海水作为原料使用,这里处理所用的电力可以有海洋风力发电或太阳能发电提供。或者如专利文献19、20本发明人展示的浮力重力发电装置113在海底和海面之间往返,可以获得风力1000倍的电量。图31所示的是氢气制造装置86,利用海面下的水压制造氢气,图33或图34显示的是苛性钠制造装置90、91,生产苛性钠和盐酸还有氯气。电力出了自然能源发电获得,也可以从临海火力发电厂或核电厂的剩余电力或深夜电力,在临海工厂111制作氢气和苛性钠。苛性钠熔点如图16所示为318摄氏度,为了降低该温度,对氢化基本金属制造装置97加热后,苛性钠呈熔融状态,两端配置正负电极,并且对氢气施加逆电压,生成的氢气的负离子和钠在正极发生反应,在正极生成氢化纳49。此外,氢化纳通过离子反应制造,消耗很少的电力。而且如图16所示氢化纳的比重为0.92比苛性钠熔融盐的比重2.13小,并且氢化纳的熔点为800摄氏度,比苛性钠的熔点318摄氏度高,氢化纳的渣宰会上浮,很简单就能比重筛选。这里制造的氢化纳放入氢气发生装置112,注入水后,比金属钠的加水分解反应多生成1倍氢气。制造的氢气通过管子可以送到火力发电厂和氢气站。另一方面氢气发生装置112生产的废弃物(副产物)苛性钠31可以用于氢化基本金属制造装置97,再次制成氢化钠49。这完全是核燃料循环以外的苛性钠燃料循环。一方面苛性钠制造装置90,91制得的苛性钠的一部分如图41所示用于装有层叠型苏打电池的车载电池和电力储藏用电池。此外,将氢化钠浸入油中,将氢气发生装置112安装到车上,成为不会积攒氢气炸弹的氢气电动车,构建不需要化石燃料的氢气社会,我们需要苛性钠燃料循环。
图45是加水分解反应控制装置的模式图。加水分解反应控制装置114内部有疏水性多孔质密闭袋115,里面容纳有药品116,疏水性氟树脂膜密闭袋115的外侧将水浸入,产生加水分解反应,可以进行气体发生,热发生,吸热或溶解反应。本发明最显著的现象是将第一族元素Na、K、Li等药品116放入疏水性多孔质氟树脂密闭袋115中,渗透压以上压力会将水浸入产生氢气。但是氟树脂会被第一族元素腐蚀,发生退化。为了防止这一现象,安全的进行加水分解反应,疏水性多孔质氟树脂膜密闭袋115的内侧同时将轻油等油类和第一族元素共同插入,氟树脂在水中呈亲油性,疏水性多孔质氟树脂膜密闭袋115内侧的Na、K、Li等不会与氟树脂膜直接接触,所以不用担心退化。比如,将小苏打和柠檬酸(1:1)作为药物116插入后,可以产生二氧化碳(CO2),专利文献19,20中本发明人展示的浮力重力发电装置113(图44)的浮力用气体使用该CO2,可以在水深1300m是获得上浮的气体。如果将氧化钙(CaO)和铝(Al)作为药品116插入,如反应式,2CaO+2Al+4H2O→2Ca(OH)2+2Al+2H2O+63.3kJ/mol→2CaO+Al2O3+H2+390.1kJ/mol所示,同时获得高温和氢气,这些药品装到潜水艇沉降到海底后,使用锤子敲打后,利用深海底部的海水作为水源产生氢气,并且同时产热后会使气体的容积越变越大,可以用于潜水艇的浮力气体。这个热量可以使干冰作为浮力剂,在1300m的深海底部升华。将尿素((NH2)2CO)作为药品116插入后,(NH2)2CO+H2O→2NH3+CO2产生氨和二氧化碳。如果使用碳化钙(电石),CaC2+2H2O→Ca(OH)2+C2H,可以直接制得乙炔气体。如果将非电解质如砂糖,调味料,营养剂等医疗药物插入水88也可以发生溶解反应。
图46是水培作物的水分和营养物质供给方式示意图。营养补给装置121对植物工厂或蔬菜工厂的蔬菜和果蔬等植物119控制水压从而间歇性的给予养分的装置,药品散布喷壶(疏水性多孔质树脂袋或管子)120与水溶液补给管(软管)118连接,在植物工厂控制室122,肥料或水分等补给养分121通过压力施加工具间接向需要的场所配送,有效率的向植物的根部提供水分和营养物质(肥料),可以有效抑制水分过多导致根部腐烂和营养过多。
图47是内窥镜型医疗装置的概略图。图47(A)所示,向脏器内部插入导管123,插入脏器的胶囊内部有压力加压工具6,进行吸引(负压)和加压(正压),可以对患部投送药物或营养物水溶液,并且对患部加热。向患部投送药物和营养剂的方法如图47B,疏水性氟树脂密闭袋115内的营养剂或药品116使用软管123投送,对溶液(正压)加压,使用压力加压工具6对疏水性多孔质膜施加渗透压以上的压力,有效的将营养物质或药物投送,不想现在的静脉输液或营养管理每时每刻投送,与生活节奏相符,高效率的投送。患部治疗时可以根据目的,只对患部投递药物。图47C是消灭按细胞的温热治疗胶囊的工作模式图。癌细胞在39~43摄氏度时耐受力最差。因为该温度比洗澡的温度低,并且患者不能长时间直接加热。因此预实验在机器上进行。首先将水88封入胶囊125中,将水分解发热剂124封入疏水性多孔质氟树脂膜密闭袋115,密闭袋也插入胶囊中,疏水性多孔质氟树脂膜密闭袋115内部使用软管123获得睡呀,如果是负压是,胶囊125内部的水88向疏水性氟树脂密闭袋115中浸透,与加水分解发热剂124反应产生热量,该热量对胶囊126内部水88加热。临床实验时可以对患部的癌细胞直接加热。如果持续维持负压平衡,该负压对加水分解发热剂提供水分,加水分解发热剂124与水88反应,39摄氏度~43摄氏度可以维持30分钟。这里使用的加水分解发热剂124的发热量是CaO 65kJ/mol、P2O3+ZnCl2+Ba(OH)2是18.1kJ/mol、NaOH是12.6kJ/mol、KOH是39.5kJ/mol、硫酸是37kJ/mol、CaCl2是97.4kJ/mol、Al2O3是126kJ/mol、CuSO4是27.5kJ/mol、CaO+Al是390.1kJ/mol。如果考虑胶囊的用量、到达温度和持续温度,临床使用的CaO发热剂是最适合的。
【工业上利用可能性】
石油和煤炭可采年数是有限的,而且还会产生二氧化碳。核燃料会释放放射能。与这些相比,氢气的采集年数是无限的,不会产生二氧化碳和放射能,是一种干净的并且有益环境的燃料。但是氢气自生很轻很难拘束,如果将氢气储存在容器(气缸)或合金中又会太重,不利于搬运。因此将氢气转换为氢气的源头(钠)。钠在全世界的海水和岩盐中广泛分布,不需要担心枯竭和分布不均。但是,回收钠必须要出去水。因此除了熔融盐电解之外没有其他的回收方法。本发明直接对海水电解获得金属钠。苛性钠可以通过离子交换不需要树脂就能生产。此外如果将正负电极沉入海面下,只需要施加电位就能制造氢气和氧气。并且锂,钠,钾,钙的电解质是水溶液,可以制造基本金属/空气充电电池或基本金属/卤素充电电池,具有很大的经济效益。特别是海水获得的金属钠可以替代石油的作为能源,不需要担心枯竭,地域分布不均,不需要电力就能生产资源,此外可以用作发电效率高的基本金属水溶液的蓄电池,为我国的工业做出巨大的贡献。
- 还没有人留言评论。精彩留言会获得点赞!