一种用于水中重金属和多环芳烃协同高效吸附去除的方法与流程
本发明属于水处理领域,涉及一种用于水中重金属和多环芳烃协同高效吸附去除的方法。
背景技术:
重金属和多环芳烃(PAHs)是环境中常见的两类典型的持久性污染物,多环芳烃的化学结构极其稳定,生物可利用性极低,且可经由食物链进入人的体内,极大的增加人类患癌的风险。重金属不能生物降解,即使痕量水平也对人类和野生生物有很强的毒性,且它们在工业上应用及其广泛,导致废水中重金属浓度很高,最终经由各种途径进入到水环境中。
很多研究发现重金属和多环芳烃往往在环境中可同时被检出,其中有关土壤、河湖及其底泥的两者复合污染效应报道较多,且有研究表明重金属和多环芳烃联合作用产生的复合污染物极其复杂,且毒性更强,危害性更大,因而由重金属和多环芳烃在环境中联合作用引起的复合污染现象已经引起各国科学家的高度关注。
近年来,人们对环境介质中重金属和多环芳烃复合污染的修复给予了很大的关注,尤其是土壤环境,而面对我国水环境中重金属和多环芳烃污染程度加剧,逐年递增的现象,研究者们大多数只制定了针对单独污染物的去除方案,但对同时去除重金属和多环芳烃的关注较少。如专利201510390223.8公开了一株耐重金属的多环芳烃降解菌、组合物及其用途。所述菌为浅黄分枝杆菌Mycobacterium gilvum,保藏号为CGMCC No.10941。所述菌可用于去除或降解多环芳烃,尤其是去除或降解土壤、水环境中的多环芳烃;还可以用于在多环芳烃污染的土壤、水环境中生物修复,尤其是重金属及多环芳烃复合污染的土壤或水。同时所述菌与表面活性剂协同可增强去除或降解多环芳烃的能力。该专利只能去除水中的多环芳烃。并且随着时间的累积,其中的重金属和多环芳烃是否存在迁移和转化等问题也不清楚。因此,开发一种能同时去除重金属和多环芳烃的方法具有重要意义。
技术实现要素:
为了克服现有技术的不足,本发明提供一种用于水中重金属和多环芳烃协同高效吸附去除的方法。该方法建立一种同步、高效去除水环境中重金属和多环芳烃复合污染的新方法,为水污染控制提供应用技术。
本发明提供了如下的技术方案:
一种用于水中重金属和多环芳烃协同高效吸附去除的方法,所述方法采用吸附剂为Fe-SBA15介孔分子筛。
在上述方案中优选的是,所述水中重金属为铜。
在上述任一方案中优选的是,所述水中多环芳烃为芘。
在上述任一方案中优选的是,所述铜在水中浓度为5~50mg/L。
在上述任一方案中优选的是,所述铜在水中浓度优选为20mg/L。
在上述任一方案中优选的是,所述芘在水中浓度为25~200μg/L。
在上述任一方案中优选的是,所述芘在水中浓度优选为100μg/L。
在上述任一方案中优选的是,所述水中加入Fe-SBA15介孔分子筛的量为0.1~2g/L。
在上述任一方案中优选的是,所述水中加入Fe-SBA15介孔分子筛的量优选为0.5g/L。
在上述任一方案中优选的是,所述吸附剂加入水中后搅拌,搅拌的转速为650~900r/min,时间为0~300min。
在上述任一方案中优选的是,所述吸附剂加入水中后搅拌,搅拌的转速优选为850r/min。
在上述任一方案中优选的是,所述水中加入离子溶液。
在上述任一方案中优选的是,所述离子溶液为氯化钾溶液。
在上述任一方案中优选的是,所述氯化钾溶液加入水中后,氯化钾的浓度为0.005~0.1mol/L。
在上述任一方案中优选的是,所述氯化钾溶液加入水中后,氯化钾的浓度优选为0.005~0.025mol/L。
在上述任一方案中优选的是,控制水溶液的pH值为2~5。
在上述任一方案中优选的是,发生吸附作用时,避光震荡或搅拌。
本发明中的吸附剂Fe-SBA15介孔分子筛,是以三嵌段聚合物聚氧乙烯-聚氧丙烯-聚氧乙烯(简称P123)为模板剂,正硅酸乙酯(TEOS)为硅的前驱物,FeCl3·6H2O为Fe前驱物,于高压釜中直接水热合成制备Fe-SBA15介孔分子筛,后于马弗炉中煅烧得到淡黄棕色粉末。
本发明的方法操作方法简单,易于操作。各种参数容易控制,可根据需要随时调节运行参数。Fe-SBA15介孔分子筛吸附剂对水中重金属和多环芳烃进行吸附处理的过中,两种污染物的去除具有协同(相互促进)作用。Fe-SBA15固体吸附剂再生后可连续数次使用而不影响吸附效果,降低了长期使用处理成本。对于待处理水的pH值和离子强度无特殊要求,适用范围较大。
附图说明
图1是本发明一种用于水中重金属和多环芳烃协同高效吸附去除的方法中不同接触时间条件下Fe-SBA15对铜和芘的吸附效果示意图;
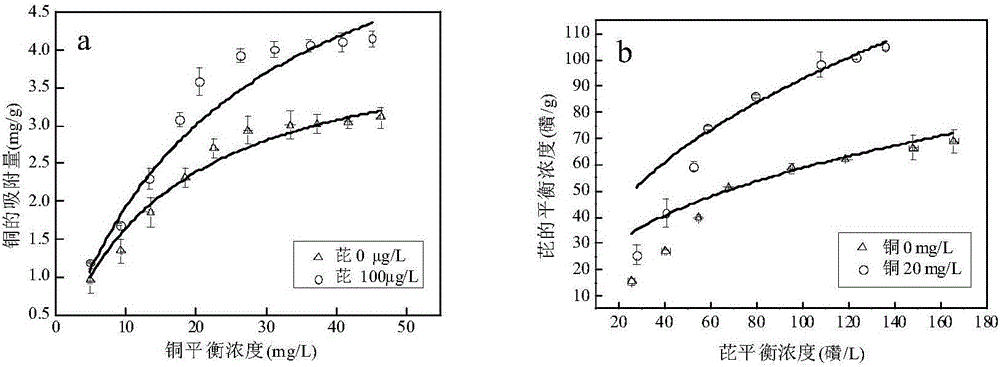
图2是本发明一种用于水中重金属和多环芳烃协同高效吸附去除的方法中不同初始浓度条件下Fe-SBA15对铜和芘的吸附效果示意图;
图3是本发明一种用于水中重金属和多环芳烃协同高效吸附去除的方法中不同离子强度条件下Fe-SBA15对铜和芘的吸附效果示意图;
图4是本发明一种用于水中重金属和多环芳烃协同高效吸附去除的方法中不同pH值条件下Fe-SBA15对铜和芘的吸附效果影响示意图;
图5是本发明一种用于水中重金属和多环芳烃协同高效吸附去除的方法中不同吸附剂Fe-SBA15投加量对铜和芘的吸附效果影响示意图。
具体实施方式
为了进一步了解本发明的技术特征,下面结合具体实施例对本发明进行详细地阐述。实施例只对本发明具有示例性的作用,而不具有任何限制性的作用,本领域的技术人员在本发明的基础上做出的任何非实质性的修改,都应属于本发明的保护范围。
本发明的Fe-SBA15介孔分子筛可由合成获得,具体方法是以三嵌段聚合物聚氧乙烯-聚氧丙烯-聚氧乙烯(简称P123)为模板剂,正硅酸乙酯(TEOS)为硅的前驱物,FeCl3·6H2O为Fe前驱物,于高压釜中直接水热合成制备Fe-SBA15介孔分子筛。
本发明提供了一种用于水中重金属和多环芳烃协同高效吸附去除的方法,所述方法采用吸附剂为Fe-SBA15介孔分子筛。
进一步地,所述水中重金属为铜。
更进一步地,所述水中多环芳烃为芘。
更进一步地,所述铜在水中浓度为5~50mg/L。优选20mg/L。
更进一步地,所述芘在水中浓度为25~200μg/L。优选100μg/L。
更进一步地,所述水中加入Fe-SBA15介孔分子筛的量为0.1~2g/L。优选为0.5g/L
更进一步地,所述吸附剂加入水中后搅拌,搅拌的转速为650~900r/min,时间为0~300min。转速优选为850r/min。
更进一步地,所述水中加入离子溶液。
更进一步地,所述离子溶液为氯化钾溶液。
更进一步地,所述氯化钾溶液加入水中后,氯化钾的浓度为0.005~0.1mol/L。优选为0.005~0.025mol/L。
更进一步地,控制水溶液的pH值为2~5。
更进一步地,发生吸附作用时,避光震荡或搅拌。
本发明的实施例1-5分别配制重金属溶液、多环芳烃溶液以及两者的混合溶液,加入吸附剂Fe-SBA15,通过控制污染物与吸附剂的接触时间、污染物的初始浓度、pH值、离子强度及吸附剂投加量等条件,实现水中重金属与多环芳烃的高效协同吸附去除,来说明本发明的效果。
实施例1:
在3个容积为500ml的玻璃烧杯内分别加入典型多环芳烃(芘)溶液、典型重金属(铜)溶液和两者的混合溶液500ml,放置在磁力搅拌器上,以850r/min的转速搅动溶液,待转速稳定后加入吸附剂Fe-SBA15 0.25g,开始计时,进行吸附反应,此时作为0时刻。控制污染物与吸附剂的接触时间,在下述条件下进行吸附处理:
反应目标溶液体积:500ml
反应目标溶液浓度:1、芘:100μg/L;2、铜:20mg/L;3、芘:100μg/L+铜:20mg/L
反应目标溶液温度:25℃
反应溶液体系:0.01M氯化钾溶液
吸附剂投加量:0.5g/L
吸附材料:Fe-SBA15粉末
取样时间点:0、5、15、25、35、45、60、75、90、120、150、180、210、270、300min。
取样后,于高速离心机中5000rmp条件下离心两分钟,取上清液,测定剩余的污染物浓度。结果如图1所示。
由图1可知,Fe-SBA15对铜和芘进行吸附,开始时污染物的吸附量均随着接触时间的增长而增加,最终趋于稳定。由图1a可知,当加入芘后,铜的吸附量明显增大,平衡吸附量由2.54mg/g增大到3.78mg/g,增幅达48.8%,即芘对铜的吸附具有促进作用;由图1b可得,当芘溶液中加入铜后,芘的吸附量也有明显的提高,平衡吸附量由44μg/g增大到58μg/g,增幅为32%,即铜对芘的吸附同样具有促进作用。综上所述,在吸附过程中,铜和芘具有明显的相互促进的作用,可高效协同去除。
实施例2:
在一系列容积为30ml的离心管中分别加入一定浓度梯度的芘溶液(加或不加铜)和一定浓度梯度的铜溶液(加或不加芘)25ml,一式两份。之后均加入吸附剂Fe-SBA15 0.0125g,将离心管置于摇床上,150rpm条件下避光震荡。通过控制污染物的初始浓度,在下述条件下进行吸附处理:
反应目标溶液体积:25ml
反应目标溶液浓度:芘:25、50、75、100、125、150、175、200μg/L(加或不加20mg/L的铜溶液);铜:5、10、15、20、25、30、35、40、45、50mg/L(加或不加100μg/L的芘溶液)
反应目标溶液温度:25℃
反应溶液体系:0.01M氯化钾溶液
吸附剂投加量:0.5g/L
吸附材料:Fe-SBA15粉末
取样时间点:24h
取样后,于高速离心机中5000rmp条件下离心两分钟,取上清液,测定剩余的污染物浓度。结果如图2所示,并用Langmuir模型对数据进行拟合,得到最大吸附容量,公式如下:
Qe=QmaxbCe/(1+bCe)
式中,Ce为平衡浓度(mg/L或μg/L);Qmax为最大吸附量(mg/g或μg/g);b为吸附系数。拟合后所得结果如下表所示。
表中Cu表示铜,Pyr表示芘。
由图2a可知,铜的吸附量随着溶液初始浓度的增大而增大,且当溶液中加入芘时,铜的吸附量就会明显的增大,由表可得,经拟合后,最大吸附量由4.31mg/g增加到6.77mg/g,增幅为57.1%,即芘对铜的吸附具有促进作用;由图2b可得,与铜的吸附情况相似,芘的吸附量也随着溶液初始浓度的增大而增大,且当芘溶液中加入铜后,芘的吸附量会有极大的增加,由表可得,拟合后,最大吸附量由单独吸附时的93μg/g增大到161μg/g,增幅达73.1%,即铜对芘的吸附同样具有促进作用。由上可知,在吸附过程中,铜和芘具有及其明显的相互促进的作用,可高效协同去除。
实施例3:
配制一系列氯化钾溶液作为反应溶液的体系,浓度分别为0、0.001、0.005、0.01、0.025、0.05、0.1mol/L。吸附处理分为三组同时进行,第一组含有100μg/L的芘,第二组含有20mg/L的铜,最后一组含有100μg/L的芘和20mg/L铜。每种溶液均取25ml于容积为30ml的离心管中,一式两份。之后均加入吸附剂Fe-SBA15 0.0125g,将离心管置于摇床上,150rpm条件下避光震荡。通过控制溶液体系的离子强度,进行吸附处理。其他条件参见实施例2。结果如图3所示。
由图3a可知,随着离子强度的增大,铜的吸附量降低,且加入芘之后,铜的吸附量出现明显的增加,其中氯化钾浓度为0.005mol/L时,铜的吸附量由2.13mg/g增加到3.02mg/g,增幅最小,为31.3%,氯化钾浓度为0.1mol/L时,铜的吸附量由0.51mg/g增大到1.84mg/g,增幅最大,高达260%。;由图3b可得,芘的吸附量随着离子强度的增加而增加,且加入铜之后,芘的吸附量也出现不同程度的增加,其中氯化钾浓度为0.005mol/L时,芘的吸附量由25.04μg/g增加为30.8μg/g,增幅最小,为23%,氯化钾浓度为0.025mol/L时,芘的吸附量由35.18μg/g增大到58.17μg/g,增幅最大,为65.3%。综上所述,在吸附过程中,当反应体系的离子强度发生变化时,铜和芘具有极其明显的相互促进的作用,可高效协同去除。
实施例4:
配制100μg/L的芘溶液、20mg/L铜溶液和芘(100μg/L)与铜(20mg/L)的混合溶液,每种溶液均取25ml于容积为30ml的离心管中。分别将溶液pH值调到2、3、4、5,一式两份。之后均加入吸附剂Fe-SBA15 0.0125g,将离心管置于摇床上,150rpm条件下避光震荡。通过控制溶液体系的pH值,进行吸附处理。其他条件参见实施例2。结果如图4所示。
由图4a可知,铜的吸附量随着pH值的增大而增大,且加入芘后,铜的吸附量会有不同程度的增加,其中pH值为4时,铜的吸附量从9.03mg/g增加到10.11mg/g,增幅最小,为12%,pH值为2时,铜的吸附量由1.97mg/g增大至4.41mg/g,增幅最大,高达124%;图4b显示,随着pH值的升高,芘的吸附量会降低,同时当有铜存在时,芘的吸附量会出现略微的增大。由上可得,在吸附过程中,当反应体系的pH值发生变化时,铜和芘仍具有明显的相互促进的作用,可高效协同去除。
实施例5:
配制芘(100μg/L)与铜(20mg/L)的混合溶液,每种溶液均取25ml于容积为30ml的离心管中。按照吸附剂投加量0.1、0.3、0.5、1.0、1.5、2.0g/L分别加入一定量的Fe-SBA15,一式两份。将离心管置于摇床上,150rpm条件下避光震荡。通过控制吸附剂的投加量,进行吸附处理。其他条件参见实施例2。结果如图5所示。
由图5可知,吸附剂投加量由0.1g/L增加到0.3g/L时,铜和芘的吸附量都明显增大,且在0.3g/L时两者的吸附量都达到最大值,分别为5.05mg/g和99.52μg/g,之后随着吸附剂投加量的增大,两种污染物的吸附量都出现明显的降低,因此考虑污染物的去除率及吸附剂的利用率,吸附剂的投加量优选为0.5g/L。
- 还没有人留言评论。精彩留言会获得点赞!
- 重金属离子吸附系统及其宿主菌、重金属离子回收方法与流程
- 一种吸附重金属离子的改性苎麻纤维多孔微球吸附剂及其制备方法与应用与流程
- 一种用于重金属离子去除的L‑半胱氨酸改性纤维素的制备方法与制造工艺
- 一种用于吸附重金属的改性纤维素衍生物吸附材料及其制备方法与应用与制造工艺
- 一种利用花生壳制备的重金属吸附材料及其制备方法与制造工艺
- 一种利用稻草制备的重金属吸附材料及其制备方法与制造工艺
- 一种环境友好型重金属离子吸附材料及其制备方法与制造工艺
- 一种基于罗丹明衍生物的重金属离子多重检测传感器制备方法与制造工艺
- 一种基于硅藻土的重金属复合吸附材料及其制备方法与制造工艺
- 一种基于凹凸棒土的重金属吸附材料及其制备方法与制造工艺