样本分离转印装置和样本分析方法与流程
本发明涉及电泳技术,特别是,涉及通过电泳分离受检体,将分离后的受检体转印到转印膜,并进行其后的处理的样本分离转印装置。
背景技术:
人类基因组计划结束后,到现在为止,各种疾病与生物体高分子的关系性逐渐变得清楚。特别是,作为生物体高分子之一的蛋白质与生物体的细胞、器官、以及脏器的功能直接相关,存在因氨基酸排列和立体结构的不同、糖链和磷酸化等化学修饰等而引起许多的疾病的可能性这种状况开始变得清楚。
在这样的状况中,进行许多的蛋白质组解析。蛋白质组是指在特定的细胞、器官、以及脏器中翻译生产的蛋白质整体,作为其解析,能够列举蛋白质的蛋白谱和功能解析等。其中,已知在蛋白质经过翻译后在生物体内合成的蛋白质,通过磷酸化等翻译后修饰,进行蛋白质的功能的控制,与蛋白质的化学修饰有关的信息的得到在今后的蛋白质组解析中能够成为重要事项之一。因此,以高精度分离和检测混有多种蛋白质的样品的方法受到重视,用于此的装置的开发正在发展。
现在,作为有益的蛋白质的分离方法,有凝胶电泳、毛细管电泳、以及液相色谱等,但从其简易性和分离性能的高低来看,一般来说广泛地利用凝胶电泳。
现在,蛋白质的化学修饰的检测主要采取在电泳后进行免疫印迹法的方法。利用被称为转印(印迹)的方法,使通过电泳分离出的蛋白质的样品吸附于转印膜并固定化。其后,若将吸附到转印膜的蛋白质覆盖到进行了荧光标记、放射性标记的特定的抗体或者探测器,则能够基于抗原抗体反应检测特定的蛋白质。将该一系列的流程称为免疫印迹。转印膜使用试样容易结合,并且疏水性较高的硝化纤维膜或者PVDF(Polyvinylidene difluoride:聚偏氟乙烯)膜等。
这样电泳与免疫印迹法的组合是在蛋白质组解析中非常有效的方法(例如,参照非专利文献1)。
以往,电泳和免疫印迹法通过研究者的手工操作使用各自独立的装置进行。例如,一般来说在电泳装置进行了等电点电泳和SDS-PAGE之后,从装置取出凝胶并移至转印装置,设置转印膜进行转印(印迹),并利用手动将抗体或者探测器覆盖到转印膜。由于该操作所使用的凝胶不容易利用非常柔软的材料进行处理,所以操作繁琐,该作业需要熟练度。因此,开发了使这些作业自动化的技术。例如,专利文献1和2公开了使从电泳到印迹的一系列的操作自动化的装置。另外专利文献3公开了用于同时进行电泳和转印的凝胶盒。另外专利文献4公开了自动地处理转印了生物体样本的转印体的装置。
专利文献1:美国专利第5234559号说明书(1993年8月10日专利)
专利文献2:日本国公开专利公报“日本特开2011-80842(2011年4月21日公开)”
专利文献3:日本国公表专利公报“日本特表平9-501774(1997年2月18日公表)”
专利文献4:日本国公开专利公报“日本特开2011-58968(2011年3月24日公开)”
非专利文献1:蛋白质实验笔记(下):从分离鉴定到功能解析(羊土社,2005年,第38~47项)
然而,上述那样的现有技术存在不能够自动地进行受检体的分离、转印以及之后的处理这样的问题。
技术实现要素:
本发明是鉴于上述课题而完成的,主要目的在于提供用于自动地进行受检体的分离、转印以及之后的处理的新的技术。
为了解决上述的课题,本发明的一方式所涉及的样本分离转印装置是通过电泳分离受检体,从缓冲槽内的排出部排出分离出的该受检体,通过使转印膜与该排出部抵接并移动来将分离后的该受检体转印到该转印膜的样本分离转印装置,具备对填充该缓冲槽的液体进行更换的送液泵。
根据本发明的一方式,能够自动地进行受检体的分离、转印以及之后的处理,因此起到使免疫印迹实验高效这样的效果。
附图说明
图1是表示本发明的实施方式1所涉及的样本分离转印装置的概略结构的立体图。
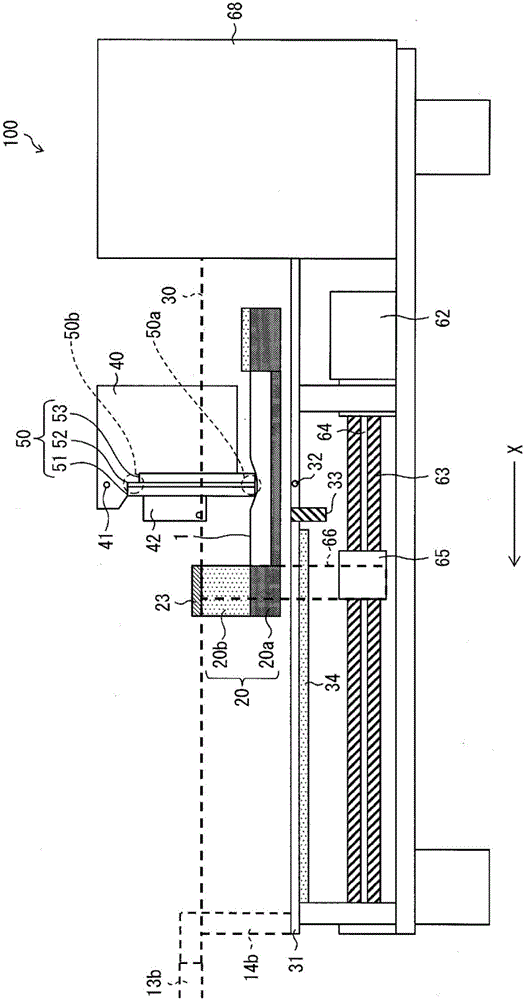
图2是表示本发明的实施方式1所涉及的样本分离转印装置的概略结构的剖视图。
图3是表示本发明的实施方式1中的管嘴的位置的立体图。
图4是用于说明本发明的实施方式1中的隔板的功能的示意图。
图5是表示本发明的实施方式2中的管嘴的位置的立体图。
图6是表示本发明的实施方式3中的阳极缓冲槽的底面的亲水性和疏水性区域的位置的俯视图。
图7是表示本发明的实施方式2、3的变形例中的设在阳极缓冲槽的底面的槽的俯视图。
图8是用于说明本发明的实施方式4中的升降板的功能的示意图。
图9是表示本发明的实施方式5所涉及的样本分离转印装置的概略结构的立体图。
具体实施方式
〔实施方式1〕
若基于附图对本发明的一实施方式(实施方式1)进行说明,则如以下那样。
首先,参照图1~图4对实施方式1所涉及的样本分离转印装置100的概略的构成进行说明。图1是示意地表示样本分离转印装置100的构成的立体图。图2是示意地表示样本分离转印装置100的构成的剖视图。图3是表示样本分离转印装置100中的管嘴的位置的立体图。图4是用于说明样本分离转印装置100中的隔板的功能的示意图。
如图1、图2所示,样本分离转印装置100是在通过电泳分离受检体,从排出部排出分离出的该受检体,通过使转印膜与该排出部抵接并移动来将分离出的该受检体转印到该转印膜之后,使用泵,更换阳极缓冲槽内的溶液,进行其后的处理、即、清洗、封闭、抗体反应以及检测反应(显色或者发光等)的样本分离转印装置,具备泵(送液泵)11a、11b、储液罐12a~12f、软管13a~13h、管嘴14a、14b、框架20、滑架(臂部)23、阳极缓冲槽(缓冲槽)30、桌台31、珀尔帖元件34、阴极缓冲槽40、分离部50、马达(驱动部)62、滚珠丝杠(驱动部)63、导轴(驱动部)64、轴架(驱动部)65、导柱(臂部)66、以及控制部68。另外,虽然为了说明而未图示,但为了安全,还具备在动作时覆盖整体的盖。
这里,分离部50收纳分离凝胶(分离介质)52,具有在阳极缓冲槽30内开口的第一开口(排出部)50a和在阴极缓冲槽40内开口的第二开口50b。另外,在阳极缓冲槽30内以与第一开口50a对置的方式配置有转印膜1。另外,在阳极缓冲槽30内配置有阳极32,在阴极缓冲槽40内配置有阴极41。
因此,在样本分离转印装置100中,通过在阴极缓冲槽40和阳极缓冲槽30填满缓冲液,阴极缓冲槽40内的阴极41与阳极缓冲槽30内的阳极32经由两个槽中的缓冲液、分离凝胶52、以及转印膜1电连接。即,样本分离转印装置100是通过对阴极41与阳极32之间施加电压,使从第二开口50b导入的样本被分离凝胶52分离,使分离后的各成分从第一开口50a排出并吸附于转印膜1的装置。
以下,参照图1~图4对主要的各部件进行详细说明。
(阳极和阴极)
阳极32配置在阳极缓冲槽30内,阴极41配置在阴极缓冲槽40内。阳极32和阴极41由金属等具有导电性的材料形成。例如从抑制电极的离子化的观点来看,作为形成阳极32和阴极41的材料优选白金。
关于这些电极配置,只要阳极32配置在阳极缓冲槽30内,阴极41在阴极缓冲槽40内以浸入阴极缓冲液的方式配置即可,并不特别限定,但是,也可以是例如阴极41、第一开口50a、以及阳极32配置在大致一条直线上。在这样的配置中若如图1所示那样配置转印膜1,则通过第一开口50a的电力线相对于转印膜1大致垂直,所以能够提高样本的吸附的精度。
另外,优选阳极32离开转印膜1配置。由此,能够抑制从阳极32产生的气泡带给针对转印膜1形成的分离成分的吸附负面影响。
阳极32和阴极41例如,既可以与控制部68连接进行使用,也可以与外部的电源供应器(直流电源装置)连接进行使用。在与外部的电源供应器连接进行使用的情况下,在对该电源供应器设置时间、电流以及电压之后,在与电源供应器的动作开始同时,操作控制部68使样本分离转印装置100动作开始即可。
(阳极缓冲槽和阴极缓冲槽)
阳极缓冲槽30和阴极缓冲槽40是使缓冲液(缓冲)滞留的绝缘性的容器。阴极缓冲槽40相对于阳极缓冲槽30设在上方。此外,在实施方式1中,阳极缓冲槽30固定在桌台31上,阴极缓冲槽40固定于阳极缓冲槽30,但本发明并不限定于该构成。
装入阳极缓冲槽30和阴极缓冲槽40的缓冲液可以是具有导电性的所有的缓冲液,特别是,能够合适地使用在弱酸性~弱碱性具有缓冲带的缓冲液。作为那样的缓冲液,例如,能够使用Tris/甘氨酸系缓冲液、乙酸缓冲溶液、炭酸钠系缓冲液、CAPS缓冲液、Tris/硼酸/EDTA缓冲液、Tris/乙酸/EDTA缓冲液、MOPS、磷酸缓冲液、Tris/右Tricine系缓冲液等缓冲液。
阳极缓冲槽30在底面收纳有隔板33。隔板33相对于阳极缓冲槽30的底面在竖直方向可动。如图4所示,隔板33从阳极缓冲槽30的底面向阳极缓冲槽30内突出,从而将阳极缓冲槽30分隔为两个区域(第一区域35和第二区域36)。第一区域35是具备阴极缓冲槽40的一侧的空间。第二区域36是不具备阴极缓冲槽40的一侧的空间。隔板33不透水,装入第二区域36的液体不会漏到第一区域35。第二区域36成为足够收纳框架20的大小。通过这样的构成,能够仅在第二区域36进行转印后的处理工序,所以对于转印后的处理工序能够以最小限的液体量高效地促进反应。此外,第一区域35称为进行电泳和转印的区域,第二区域36称为进行转印后的处理的区域。
在阳极缓冲槽30内,如图3所示,在第二区域36的内侧表面具备管嘴14a、14b。管嘴14a的一端(开口部15a)与阳极缓冲槽30的底面对置并离开阳极缓冲槽30的底面5mm~50mm左右。管嘴14a向阳极缓冲槽30外延伸,管嘴14a的另一端(连接部16a)在阳极缓冲槽30外与软管13a连接。另外,管嘴14b的一端(开口部15b)与阳极缓冲槽30的底面对置并离开阳极缓冲槽30的底面5mm~50mm左右。管嘴14b向阳极缓冲槽30外延伸,管嘴14b的另一端(连接部16b)在阳极缓冲槽30外与软管13b连接。
通过这样的构成,能够将管嘴14a、14b中的一者作为排出用,将另一者作为注入用。因此,能够容易地更换填充阳极缓冲槽30的液体。
另外,管嘴14a、14b设在阳极缓冲槽30中进行转印时转印膜1移动方向上的端部的内侧表面。另外,管嘴14a、14b向阳极缓冲槽30外向该移动方向延伸。因此,不会成为转印膜1的移动的障碍,能够顺利地进行各工序。此外,管嘴14a、14b的位置并不限定于此,只要是不成为转印膜1的移动的障碍的位置则也可以是其它的位置。
优选管嘴14a、14b由绝缘性的材料例如塑料构成。若使用这样的材料,则能够不会阻碍阳极周边的电力线的配置,顺利地进行电泳。
阳极缓冲槽30在第二区域36的底面外表面具备珀尔帖元件34。通过具备珀尔帖元件34,在各工序中能够将阳极缓冲槽30内的液体的温度调节到在该工序中合适的温度。
(分离部)
分离部50在其内部收纳分离凝胶52。在实施方式1中,分离部50以在大致竖直方向直立,其下部配置在阳极缓冲槽30内,其上部单面与阴极缓冲槽40接触的方式配置。由此,分离凝胶52被阳极缓冲槽30内的缓冲液和阴极缓冲槽40内的缓冲液的至少一者水冷,而能够充分地冷却。
另外,分离部50具有在阳极缓冲槽30内开口的第一开口50a和在阴极缓冲槽40内开口的第二开口50b。由此,分离凝胶52经由第一开口50a面向阳极缓冲槽30内,并经由第二开口50b面向阴极缓冲槽40内。此外,在实施方式1中,分离部50通过设于阴极缓冲槽40的锁止件42固定于阴极缓冲槽40,但本发明并不限定于该构成。
分离部50能够由利用玻璃或者丙烯酸等绝缘体形成的两块绝缘板51、53构成。在一实施方式中,分离部50在第二开口50b中绝缘板53的局部缺失,而使分离凝胶52暴露,由此,能够将样本容易地导入分离凝胶52。
分离凝胶52是用于将从第二开口50b导入的样本成分根据分子量分离的凝胶。分离凝胶52能够在分离部50向样本分离转印装置100安装前,或者在进行了安装之后,填充在分离部50内。另外,也可以使用填充了分离凝胶52的市售的页片(page chip)作为分离部50。作为分离凝胶52的例子,能够列举丙烯酰胺凝胶和琼脂糖凝胶等。分离凝胶52的横向宽度例如,能够是能够使10~12道的样本分离的长度。此外,在本发明中分离介质并不限定于凝胶,也可以是能够进行受检体的分离的其它的介质。
此外,在实施方式1中,采用在分离部50内填充分离凝胶52的构成,但也能够采用在绝缘板51与绝缘板53之间设有被称为纳米柱的许多的超微细柱的构成。
另外,分离部50的第一开口50a包含其四周,也可以被由导电性的多孔质材料(例如,亲水性PVDF膜、亲水性PTFE(Polytetra fluoro ethylene:聚四氟乙烯)膜等)形成的覆盖部覆盖。由此,在转印膜1接触或者被按压到第一开口50a的情况下(在第一开口50a与转印膜1之间不设有距离的情况下),能够减少在输送转印膜1时转印膜1从分离部50和分离凝胶52受到的摩擦阻力和损伤。
此外,分离部50在大致竖直方向直立,所以与分离部50设置在大致水平方向的构成相比,能够使样本导入量增大。这是因为在水平型的样本分离转印装置中,不容易改变设于分离凝胶的井的深度,但在竖直型的样本分离转印装置中,能够容易地改变井的深度,所以能够容易地使样本导入量增大。
(转印膜1)
优选转印膜1是能够长期间稳定地保存被分离凝胶52分离出的样本,并且,使之后的分析变得容易的样本的吸附、保持体。作为转印膜1的材质,优选具有较高的强度,并且样本结合能力(每个单位面积能够吸附的重量)较高的材质。作为转印膜1,在样本为蛋白质的情况下,PVDF膜等适合。此外,优选PVDF膜预先使用甲醇等进行亲水化处理。除此以外,也能够使用硝化纤维膜或者尼龙膜等以往利用于蛋白质、DNA以及核酸的吸附的膜。
此外,作为能够在样本分离转印装置100中进行分离和吸附的样本,并不限定于这些,能够列举来自生物材料(例如,生物个体、体液、细胞株、组织培养物、或组织碎片)的调制物,或者,市售的试剂等。例如,能够列举多肽或者多核苷酸。
转印膜1以在阳极缓冲槽30内浸渍到缓冲液的状态使用。
在实施方式1中,转印膜1具有供一次电泳、转印使用的长度,换句话说,在只要是具有在进行一次电泳、转印时在阳极缓冲槽30内移动的距离的长度即可。通过使转印膜1这样构成,不需要在每一次电泳、转印,进行切断转印膜1的操作,能够使样本分离转印装置100的使用性提高。另外,转印膜1的横向宽度是与分离凝胶52的横向宽度对应的长度即可。
(框架)
在实施方式1中,转印膜1以被框架20保持的状态使用。在一个例子中,框架20由框架下部20a、和框架上部20b构成,在转印膜1的移动方向上的两端部,转印膜1夹在框架下部20a和框架上部20b之间并被保持。框架20并不限定于此,但例如,能够由特氟龙(注册商标)、丙烯酸树脂、PEEK树脂那样的合成树脂构成。
但是,本发明并不限定于此,只要能够固定转印膜1,则也可以是其它的构成(例如,利用保持部件按住转印膜1并以能够拆装的方式进行保持的构成等)。
(臂部)
在实施方式1中,框架20装于臂部。臂部使转印膜1移动、以及与第一开口50a抵接。在实施方式1中,臂部由作为连结起来的一系列的部件的框架20、滑架23以及导柱66构成。
导柱66是以与后述的驱动部(轴架65)连结,并通过阳极缓冲槽30的侧壁的外侧的方式配置的杆部件。滑架23是与导柱66连结,并绕到阳极缓冲槽30的侧壁的上端,与框架20连结的部件。
如以上那样,臂部从与驱动部连结的位置起,通过阳极缓冲槽30的侧壁的外侧,绕到该侧壁的上端,并与该侧壁的内侧连接。
此外,在实施方式1中,导柱66在阳极缓冲槽30的侧壁的外侧,延伸到与该侧壁的上端并排的位置,这并不构成对本发明进行限定。而且,滑架23与导柱66嵌合,并跨过阳极缓冲槽30的侧壁的上端延伸到该侧壁的内侧。
通过像这样构成,滑架23能够容易地相对于驱动部进行拆装。导柱66配置在阳极缓冲槽30的侧壁的外侧,并不成为根据需要进行的、阳极缓冲槽30的取下、电极的设置等各种操作的障碍。因此,通过适当地取下滑架23,能够顺利地进行各种操作。
(驱动部)
驱动部在水平方向驱动臂部,在实施方式1中,由马达62、滚珠丝杠63、导轴64以及轴架65构成。
马达62使滚珠丝杠63旋转。马达62既可以使用能够使转速变化的马达,也可以是将转速固定的马达与齿轮组合起来使用。滚珠丝杠63贯通轴架65,并且与轴架65螺纹配合。导轴64贯通轴架65,轴架65构成为能够沿导轴64移动。而且,马达62通过使滚珠丝杠63旋转,从而向图中X轴方向(大致水平方向)驱动轴架65。轴架65与臂部(导柱66)连结,由此,驱动部能够向图中X轴方向(大致水平方向)驱动臂部。而且,臂部保持转印膜1,所以转印膜1项图中X轴方向(大致水平方向)移动。
但是,本发明并不限定于此,只要能够向大致水平方向驱动臂部,则也可以由其它的驱动机构(例如,传动带、齿轮等)构成驱动部。
另外,驱动部设在阳极缓冲槽30下。由此,能够防止从阳极缓冲槽30飞溅的缓冲液使驱动部的耐用性降低的担心、以及驱动部成为针对样本分离转印装置100的各种操作的障碍的担心。
(储液罐)
储液罐12a~12e是用于储存转印后的处理所需要的试剂或者清洗缓冲液的容器。储液罐12f是用于储存废液的容器。例如,在储液罐12a能够填充清洗缓冲液(例如包含表面活性剂的PBS缓冲液、TBS缓冲液),在储液罐12b能够填充封闭溶液(例如BSA溶液、酪蛋白溶液、脱脂乳溶液、高分子封闭溶液),在储液罐12c能够填充初级抗体溶液(例如识别目的蛋白质的抗体溶液、多肽配体溶液、核酸配体溶液、具有相互作用的蛋白溶液),在储液罐12d能够填充二级抗体溶液(例如显色物质、荧光物质或者放射性同位体等所标志的识别初级抗体的抗体溶液),在储液罐12e能够填充检测反应溶液(例如西洋山葵过氧化物酶、碱性磷酸酶等显色或者发光溶液等)。
优选储液罐12a~12f能够取下。若能够取下,则能够在使用后取下并容易地对储液罐内进行清洗,所以能够在下次使用时防止试剂的混入。
此外,在本发明中储液罐的数目并不限定于此,也可以具备更多的储液罐,也可以具备更少的储液罐。
(泵和软管)
泵11a经由软管13c、13d、13e、13f以及13g分别与储液罐12a、12b、12c、12d以及12e连接,另外,经由软管13a与管嘴14a连接。泵11a能够将装入储液罐12a、12b、12c、12d以及12e的液体任意地注入阳极缓冲槽30。
泵11b经由软管13h与储液罐12f连接,另外,经由软管13b与管嘴14b连接。泵11b能够将阳极缓冲槽30内的液体排出到储液罐12f。
泵并不特别限定于11a、11b,例如能够使用隔膜泵等能够自动控制的公知的泵等。
虽然软管13a~13h并不特别限定,但优选是硅酮软管等柔软的材质的软管。另外,软管13a~13h也可以能够相对于储液罐12a~12f、泵11a、11b以及管嘴14a、14b拆装。若为能够拆装的构成,则在软管的劣化情况下或者产生了堵塞的情况下等能够更换为新的软管。
[(控制部)
控制部68是进行样本分离转印装置100的各种控制(臂部的位置的控制、施加给阳极32以及阴极41的电流、电压的控制、泵11a、11b的控制、珀尔帖元件34的控制、隔板33的动作的控制等)的控制面板。控制部68也可以具备用于接受来自用户的输入的按钮、开关,或者用于向用户通知动作状态的灯、显示部等。
(样本的电泳、转印以及转印后的处理)
接下来,参照图1~4对实施方式1的样本分离转印装置100中的样本的电泳、转印以及转印后的处理的流程进行说明。如图1所示,在样本的电泳和转印时,转印膜1以配置在与第一开口50a抵接的位置的状态被框架20保持。
在阳极缓冲槽30和阴极缓冲槽40装入缓冲液。在实施方式1中,例如,在阳极缓冲槽30装入400mL的缓冲液,在阴极缓冲槽40装入170mL的缓冲液。
然后,将样本从分离部50的第二开口50b导入分离凝胶52。优选样本除了作为分析对象的生物体分子之外,还有用于确认电泳的进行状态的可视分子量标记。
利用以上的状态,进行样本的由电泳形成的分离。控制部68控制马达62,将转印膜1的位置设定在开始位置,并在阳极32与阴极41之间流通电流,开始电泳。作为在阳极32与阴极41之间流通的电流值,并不特别限定,但优选在50mA以下,更优选在20mA以上、且在30mA以下。此外,可以以电流值恒定的方式进行控制,也可以以电压恒定的方式进行控制,也可以以其它的方式控制电流、电压。控制部68控制珀尔帖元件34,冷却阳极缓冲槽30。由此,样本分离转印装置100整体被冷却,能够防止电泳时的微笑现象。
转印膜1配合分离部50中的电泳的进行,因利用驱动部形成的臂部的驱动而朝向图1的箭头的方向在X轴上逐渐移动。X轴方向是与第一开口50a的长边方向正交的方向。转印膜1的移动速度并不特别限定,但例如,能够是在60~120分钟间,移动5cm~10cm的速度。
然后,由于电泳而排出的样本(在分离凝胶52内分离的样本)从第一开口50a,吸附到转印膜1上的遵从排出的时刻的位置(在排出的时刻与第一开口50a对置的位置)。由此,在转印膜1转印分离后的样本。
转印后,臂部将被框架20保持的转印膜1移动到第二区域36内的位置。此时,为了框架20与分离部50不干扰,臂部也可以使框架20上下活动。
接下来,进行转印后的处理。在实施方式1中通过免疫印迹法对转印膜1进行免疫染色。在实施方式1中,例如,在储液罐12a预先填充有清洗缓冲液,在储液罐12b预先填充有封闭溶液,在储液罐12c预先填充有初级抗体溶液,在储液罐12d预先填充有二级抗体溶液,在储液罐12e预先填充有检测反应溶液。
首先,控制部68控制泵11b,将阳极缓冲槽30内的缓冲液排出到储液罐12f。具体而言,阳极缓冲槽30内的缓冲液从管嘴14b的开口部15b起依次通过管嘴14b、软管13b、泵11b以及软管13h,移动到储液罐12f。接下来,通过控制部68的控制,隔板33从阳极缓冲槽30的底面突出,将阳极缓冲槽30分为第一区域35和第二区域36。
接下来,控制泵11a,将储液罐12a内的清洗缓冲液注入阳极缓冲槽30内。具体而言,储液罐12a内的清洗缓冲液依次通过软管13c、泵11a、软管13a、管嘴14a,并从管嘴14a的开口部15a移动到阳极缓冲槽30内。清洗缓冲液的量例如是100mL。清洗例如进行5分钟。此时,优选控制部68控制臂部,使转印膜1在X轴方向前后移动进行摇晃。由此,能够高效地进行清洗,能够实现时间的缩短和灵敏度的提高。其后,控制泵11b,将阳极缓冲槽30内的溶液排出到储液罐12f。清洗例如进行三次。
清洗后,控制部68控制泵11a,将储液罐12b内的封闭溶液注入阳极缓冲槽30内。具体而言,储液罐12b内的封闭溶液依次通过软管13d、泵11a、软管13a、管嘴14a,并从管嘴14a的开口部15a移动到阳极缓冲槽30内。封闭溶液的液体量例如是100mL。由此,能够进行封闭。封闭例如花费一小时进行。此时,优选控制部68控制臂部,使转印膜1在X轴方向前后移动进行摇晃。由此,能够高效地进行封闭,能够实现时间的缩短和灵敏度的提高。
在封闭结束后,控制部68控制泵11b,将阳极缓冲槽30内的封闭溶液排出到储液罐12f。接下来,控制部68控制泵11a,将储液罐12c内的初级抗体溶液注入到阳极缓冲槽30。具体而言,储液罐12c内的初级抗体溶液依次通过软管13e、泵11a、软管13a、管嘴14a,并从管嘴14a的开口部15a移动到阳极缓冲槽30内。初级抗体溶液的量例如是10mL。反应例如花费一小时进行。此时,优选控制部68控制臂部,使转印膜1在X轴方向前后移动进行摇晃。由此,受检体与初级抗体接触的机会增加,能够实现时间的缩短和灵敏度的提高。另外,控制部68控制珀尔帖元件34,对阳极缓冲槽30进行加温(例如37℃)。由此,能够促进与初级抗体进行反应,实现时间的缩短和灵敏度的提高。
在反应结束后,控制部68控制泵11a,将储液罐12a内的清洗缓冲液注入到阳极缓冲槽30内。清洗缓冲液的量例如是100mL。清洗例如进行五分钟。此时,优选控制部68控制臂部,使转印膜1在X轴方向前后移动进行摇晃。其后,控制泵11b,将阳极缓冲槽30内的溶液排出到储液罐12f。清洗例如进行三次。
清洗后,控制部68控制泵11a,将储液罐12d内的二级抗体溶液注入阳极缓冲槽30。具体而言,储液罐12d内的二级抗体溶液依次通过软管13f、泵11a、软管13a、管嘴14a,并从管嘴14a的开口部15a移动到阳极缓冲槽30内。二级抗体溶液的量例如是10mL。反应例如花费一小时进行。此时,优选控制部68控制臂部,使转印膜1在X轴方向前后移动进行摇晃。由此,受检体与二级抗体接触的机会增加,能够实现时间的缩短和灵敏度的提高。控制部68控制珀尔帖元件34,对阳极缓冲槽30进行加温(例如37℃)。由此,能够促进与二级抗体的反应,实现时间的缩短和灵敏度的提高。
在反应结束后,控制部68控制泵11a,将储液罐12a内的清洗缓冲液注入阳极缓冲槽30内。清洗缓冲液的量例如是100mL。清洗例如进行五分钟。此时,优选控制部68控制臂部,使转印膜1在X轴方向前后移动进行摇晃。其后,控制泵11b,将阳极缓冲槽30内的溶液排出到储液罐12f。清洗例如进行三次。
清洗后,控制部68控制泵11a,将储液罐12e内的检测反应溶液注入阳极缓冲槽30内。具体而言,储液罐12e内的检测反应溶液依次通过软管13g、泵11a、软管13a、管嘴14a,并从管嘴14a的开口部15a移动到阳极缓冲槽30内。检测反应溶液的量例如是10mL。反应例如进行一小时。
在反应结束后,控制部68控制泵11a,将储液罐12a内的清洗缓冲液注入到阳极缓冲槽30内。清洗缓冲液的量例如是100mL。清洗例如进行五分钟。此时,优选控制部68控制臂部,使转印膜1在X轴方向前后移动进行摇晃。其后,控制泵11b,将阳极缓冲槽30内的溶液排出到储液罐12f。清洗例如进行三次。
此外,转印膜1的免疫染色的顺序并不限定于上述方式,能够适当地省略清洗,或者追加清洗。
回收这样得到的转印膜1,并通过荧光检测器等,检测转印到转印膜1的成分的分离图案。这样的荧光检测器也可以装于样本分离转印装置100,由此能够使电泳、转印、转印后的处理、以及检测所有工序自动化。
〔实施方式2〕
若基于图5对本发明的其它的实施方式(实施方式2)进行说明,则如以下那样。此外,为了方便说明,对于具有与在实施方式1中说明的部件相同的功能的部件,标相同的附图标记,并省略其说明。
实施方式2与实施方式1的区别是管嘴14a、14b的形状、以及阳极缓冲槽30的底面的构成。其它的点与实施方式1相同。
(管嘴)
在实施方式2中,如图5所示,对于管嘴14a、14b来说,具有开口部15a、15b的端部沿阳极缓冲槽30内的侧面和底面折弯为L字,开口部15a、15b相对于阳极缓冲槽30的底面在竖直方向开口。
由此,通过管嘴14b进行的对阳极缓冲槽30内的废液(使用完毕的液体)的回收变得更容易。特别是,虽然附图未明示,但通过使阳极缓冲槽30的底面形成角度,使废液向管嘴14b侧流动,从而能够进一步使废液的回收容易。
另外,在变形例中,也可以在阳极缓冲槽30的底面设有槽73,从而废液流到管嘴14b的四周。槽73例如是,如图7的(a)所示,优选以管嘴14b的开口部15b为起点放射状地设置。通过成为这样的构成,能够使废液从阳极缓冲槽30的底面的整体高效地流入到开口部15b。因此,能够减少残留在阳极缓冲槽30的废液,能够实现灵敏度的提高。并且,也可以将管嘴14b设在槽73内。由此,能够进一步使废液的回收变得容易。槽73例如,能够使深度为0.1mm~1mm,使横向宽度为11mm。
(样本的电泳、转印以及转印后的处理)
实施方式2的样本分离转印装置100中的样本的电泳、转印以及转印后的处理的流程与实施方式1相同。
〔实施方式3〕
若基于图6对本发明的其它的实施方式(实施方式3)进行说明,则如以下那样。此外,为了方便说明,对于具有与在实施方式1中说明的部件相同的功能的部件,标相同的附图标记,并省略其说明。
实施方式3与实施方式1的区别是阳极缓冲槽30的底面的材料、构成。其它的点与实施方式1相同。
(阳极缓冲槽的底面)
在实施方式3中,如图6所示,在阳极缓冲槽30的底面存在亲水性区域(一部分区域)71以及疏水性区域(其它区域)72。更具体而言,亲水性区域71存在于第二区域36。即,阳极缓冲槽30(具体而言是第二区域36)的底面具备亲水性区域71和以包围该亲水性区域71的方式配置的疏水性区域72。
亲水性区域71例如由玻璃、进行了等离子体处理的树脂材料等构成。疏水性区域72例如由树脂材料(丙烯酸、聚碳酸酯、聚氯乙烯、聚乙烯、聚丙烯、聚苯乙烯、丙烯腈-苯乙烯、聚乙烯、对苯二酸盐(或酯)等)构成。
亲水性区域71存在于与进行转印后的处理时的转印膜1的位置对置的位置。优选亲水性区域71的大小与转印膜1大致相同。另外,开口部15a和15b存在于与亲水性区域71接触的位置。根据该构成,在从开口部15a注入了少量的液体的情况下,能够使该液体高效地保持于亲水性区域71。因此,能够减少高价格的试剂(抗体溶液等)的使用量。另外,能够均匀地使试剂反应。在实施方式3中,例如,能够使初级抗体溶液、二级抗体溶液以及检测反应溶液的使用量在10mL以下,优选在5mL以下,更优选在3mL以下。
在这样实施方式3中,能够在阳极缓冲槽30内以各自更优选的液体量自动地进行使用优选电泳用的缓冲液、清洗缓冲液以及封闭溶液那样一次使用量较多的液体的工序、和使用优选抗体溶液和检测反应溶液那样一次使用量较少的液体的工序双方。
另外,在变形例中,也可以在阳极缓冲槽30的底面设有槽73,使废液流入到管嘴14b的四周。槽73是例如,如图7的(b)所示,优选设在亲水性区域71与疏水性区域72的边界。更具体而言,以包围亲水性区域71的方式设置。此时,优选槽73为亲水性。通过成为这样的构成,能够使保持于亲水性区域71的液体高效地流入开口部15b。因此,能够减少残留在阳极缓冲槽30的废液,能够实现灵敏度的提高。并且,也可以将管嘴14b设在槽73内。由此,能够进一步使废液的回收变得容易。槽73是例如,能够使深度为0.1mm~1mm,使横向宽度为11mm。
(样本的电泳、转印以及转印后的处理)
实施方式3的样本分离转印装置100中的样本的电泳、转印以及转印后的处理的流程与实施方式1相同。另外,虽然实施方式3的样本分离转印装置100中的管嘴与实施方式2相同地进行说明,但也可以与实施方式1相同。
〔实施方式4〕
若基于图8对本发明的其它的实施方式(实施方式4)进行说明,则如以下那样。此外,为了方便说明,对于具有与在实施方式1~3中说明的部件相同的功能的部件,标相同的附图标记,并省略其说明。
实施方式4与实施方式3的区别是阳极缓冲槽30的底面的结构以及开口部15a、15b的位置。其它的点与实施方式3相同。
(升降板)
在实施方式4中,如图8所示,在阳极缓冲槽30的底面具备沿相对于转印膜1接近分离的方向移动的升降板82。即,在相当于实施方式2中的亲水性区域71的位置具备升降板82。这里,升降板82的大小比转印膜1大。即,升降板82的大小比框架20的内径大。因此,若升降板82向与转印膜1接近的方向移动,则升降板82与框架20抵接,由升降板82、框架20以及转印膜1形成封闭的空间83。若以使注入到阳极缓冲槽30的液体载置于升降板82的状态下,向相对于转印膜1接近的方向移动,则能够将该液体保持于空间83。该情况下,与没有升降板82的情况相比较,与转印膜1间的距离较短,所以即使是较少的液体量,也能够使该液体与转印膜1接触。因此,能够进一步减少高价格的试剂(抗体溶液等)的使用量。另外,能够均匀地使试剂反应。在实施方式4中,例如,能够使初级抗体溶液、二级抗体溶液以及检测反应溶液的使用量在5mL以下,优选在3mL以下,更优选为1mL。
在实施方式4中,升降板82通过设于下部的滚珠丝杠81升降。滚珠丝杠81被控制部68控制。但是,本发明并不限定于滚珠丝杠81,也可以通过使升降板82升降的其它的方法(例如螺线管等)。
升降板82优选上表面的外边缘部为疏水性,其它区域为亲水性。该情况下,升降板82更优选与框架20接触的部分以及比这部分靠外侧部分为疏水性的区域。若为这样的构成,则能够更可靠地将液体保持在升降板82的上表面的内侧(即亲水性的区域)。
另外,如图8所示,优选在框架20的底面设有垫片24。若为这样的构成,则能够防止保持于空间83的液体从升降板82与框架20间的间隙漏出。因此,能够更可靠地将液体保持于空间83。
(管嘴)
实施方式4中的管嘴14a、14b具备在不与升降板82重叠的位置。即,开口部15a、15b与阳极缓冲槽30的底面中未设有升降板82的部分接触。开口部15a越处于接近升降板82的位置,越容易使液体配置在亲水性区域71,所以优选。
(样本的电泳、转印以及转印后的处理)
对实施方式4的样本分离转印装置100中的样本的电泳、转印以及转印后的处理的流程进行说明。
样本的电泳以及转印与实施方式1相同。
转印后,转印膜1直接移动到第二区域36内的位置。更具体而言,移动到与升降板82对置的位置。此时,升降板82是下降到阳极缓冲槽30的底面的高度的状态(图8的(a))。
首先,控制部68控制泵11b,将阳极缓冲槽30内的缓冲液排出到储液罐12f。接下来,通过控制部68的控制,隔板33从阳极缓冲槽30的底面突出,将阳极缓冲槽30分为第一区域35和第二区域36。
接下来,与实施方式1相同,控制部68控制泵11a,将储液罐12a内的清洗缓冲液注入到阳极缓冲槽30内,进行清洗。其后,控制泵11b将阳极缓冲槽30内的溶液排出到储液罐12f。清洗例如进行三次。
接下来,控制部68控制泵11a,将储液罐12b内的封闭溶液注入到阳极缓冲槽30内,进行封闭。封闭结束后,与实施方式1相同,控制部68控制泵11b将阳极缓冲槽30内的溶液排出到储液罐12f。
接下来,控制部68控制泵11a,将储液罐12c内的初级抗体溶液注入到阳极缓冲槽30。初级抗体溶液的量例如是1mL。此时,升降板82的上表面成为载置了初级抗体溶液的状态。接下来,控制部68控制滚珠丝杠81,将升降板82推到与框架20(更正确地说是垫片24)接触(图8的(b))。由此,进行受检体与初级抗体的反应。这里,虽然一方面,受检体存在于转印膜1的上表面侧,另一方面,初级抗体溶液存在于转印膜1的下下表面侧,但转印膜1也能够从下表面侧反应。反应例如花费一小时进行。
在反应结束后,控制部68控制滚珠丝杠81,将升降板82下降到阳极缓冲槽30的底面的高度。接下来,控制部68控制泵11a,将储液罐12a内的清洗缓冲液注入到阳极缓冲槽30内。清洗缓冲液的量例如是100mL。与实施方式1相同地进行清洗,控制部68控制泵11b,将阳极缓冲槽30内的溶液排出到储液罐12f。
清洗后,控制部68控制泵11a,将储液罐12d内的二级抗体溶液注入到阳极缓冲槽30。二级抗体溶液的量例如是1mL。此时,升降板82的上表面成为载置了二级抗体溶液的状态。接下来,控制部68控制滚珠丝杠81,将升降板82推到与框架20(更正确地说是垫片24)接触。由此,进行受检体与二级抗体的反应。
在反应结束后,控制部68控制滚珠丝杠81,将升降板82下降到阳极缓冲槽30的底面的高度。接下来,控制部68控制泵11a,将储液罐12a内的清洗缓冲液注入到阳极缓冲槽30内。清洗缓冲液的量例如是100mL。与实施方式1相同地进行清洗,控制部68控制泵11b,将阳极缓冲槽30内的溶液排出到储液罐12f。
清洗后,控制部68控制泵11a,将储液罐12e内的检测反应溶液注入到阳极缓冲槽30。检测反应溶液的量例如是1mL。此时,升降板82的上表面成为载置了检测反应溶液的状态。接下来,控制部68控制滚珠丝杠81,将升降板82推到与框架20(更正确地说是垫片24)接触。由此,进行与检测反应溶液的反应。
在反应结束后,控制部68控制滚珠丝杠81,将升降板82下降到阳极缓冲槽30的底面的高度。接下来,控制部68控制泵11a,将储液罐12a内的清洗缓冲液注入到阳极缓冲槽30内。清洗缓冲液的量例如是100mL。与实施方式1相同地进行清洗,控制部68控制泵11b,将阳极缓冲槽30内的溶液排出到储液罐12f。
此外,转印膜1的免疫染色的顺序并不限定于上述方式,能够适当地省略清洗,或者追加清洗。
回收这样得到的转印膜1,并通过荧光检测器等,检测转印到转印膜1的成分的分离图案。这样的荧光检测器也可以装于样本分离转印装置100,由此能够使电泳、转印、转印后的处理、以及检测的所有工序自动化。
在这样实施方式4中,能够在阳极缓冲槽30内以各自更优选的液体量自动地进行优选使用电泳用的缓冲液、清洗缓冲液以及封闭溶液那样一次使用量较多的液体的工序、和优选使用抗体溶液和检测反应溶液那样一次使用量较少的液体的工序双方。
〔实施方式5〕
若基于图9对本发明的其它的实施方式(实施方式5)进行说明,则如以下那样。此外,为了方便说明,对于具有与在实施方式1中说明的部件相同的功能的部件,标相同的附图标记,并省略其说明。
实施方式5与实施方式1的区别是注入用的储液罐、软管、泵以及管嘴的连接方法。其它的点与实施方式1相同。
(储液罐、软管、泵以及管嘴)
在实施方式5中,具备相当于实施方式1的储液罐12a~12f的储液罐92a~92f。这里,如图9所示,在阳极缓冲槽30内在第二区域36的内侧表面具备管嘴94a~94f。储液罐92a~92f分别经由软管93g~93l、泵91a~91f、软管93a~93f与管嘴94a~94f连接。即,储液罐92a~92f分别具备软管、泵以及管嘴。这样,在实施方式5中,注入用的储液罐(储液罐92a~92e)分别具备软管、泵以及管嘴。在这样的构成中,各液体以独立的路径注入到阳极缓冲槽30内,所以有试剂的混入的担心较少这样的优点。
此外,管嘴的开口部的位置和方向并不限定于图9所示的方式,也可以与实施方式2相同,也可以是其它的方式。
〔变形例〕
在实施方式1、5的样本分离转印装置100中,也可以与实施方式2相同,在阳极缓冲槽30的底面存在亲水性区域71和疏水性区域72。
另外,在实施方式1、5的样本分离转印装置100中,也可以与实施方式3相同,在阳极缓冲槽30的底面具备升降板82。
另外,在实施方式1~5的样本分离转印装置100中,也可以阳极缓冲槽30的底面倾斜。优选管嘴14b或者94f的开口部所在的部分较低。若为这样的构成,则在从阳极缓冲槽30排出液体时,能够使该液体聚集在较低的部分。因此,液体的回收变得容易。
另外,在实施方式1~5的样本分离转印装置100中,也可以不具备储液罐12b~12e或者92b~92e。该情况下,能够形成将在储液罐12a或者92a装入清洗缓冲液进行到转印后的清洗工序的装置。
另外,在实施方式1~5的样本分离转印装置100中,也可以不具备储液罐12c~12e或者92c~92e。该情况下,能够形成将在储液罐12a或者92a装入清洗缓冲液,在储液罐12b或者92b装入封闭溶液,进行到转印后的清洗和封闭工序的装置。
另外,在实施方式1~5的样本分离转印装置100中,也可以不具备储液罐12d~12e或者92d~92e。该情况下,能够形成将在储液罐12a或者92a装入清洗缓冲液,在储液罐12b或者92b装入封闭溶液,在储液罐12c或者92c装入初级抗体溶液,进行到转印后的清洗、封闭、以及初级抗体反应工序的装置。
另外,在实施方式1~5的样本分离转印装置100中,也可以不具备储液罐12e或者92e。该情况下,能够形成将在储液罐12a或者92a装入清洗缓冲液,在储液罐12b或者92b装入封闭溶液,在储液罐12c或者92c装入初级抗体溶液,在储液罐12d或者92d装入二级抗体溶液,进行到转印后的清洗、封闭、初级抗体反应以及二级抗体反应工序的装置。
另外,在实施方式1~5的样本分离转印装置100中,也可以不将储液罐作为构成要素。该情况下,在样本分离转印装置100的使用时,使用者准备储液罐,并使之与软管连接即可。
另外,在实施方式1~5的样本分离转印装置100中,转印后的处理并不限定于使用了抗体的免疫染色,也可以是基于能够进行蛋白质或者多肽的检测的其它的方法的处理。另外,在样本不为蛋白质或者多肽的情况下,利用适合该样本的方法进行处理。
〔总结〕
本发明的方式1所涉及的样本分离转印装置100是通过电泳分离受检体,从缓冲槽(阳极缓冲槽30)内的排出部(第一开口50a)排出分离出的该受检体,通过使转印膜1与该排出部抵接并移动来将分离后的该受检体转印到该转印膜1的样本分离转印装置,该样本分离转印装置具备对填充该缓冲槽的液体进行更换的送液泵(泵11a、11b或者91a~91f)。
根据上述的构成,能够通过送液泵更换填充缓冲槽的液体。由此,能够自动地进行通过电泳分离受检体的工序、将受检体转印到转印膜的工序、以及转印后的处理(清洗、封闭、抗体反应、检测反应等)工序。因此,能够简便地进行免疫印迹。
本发明的方式2所涉及的样本分离转印装置可以是,在上述方式1中,上述送液泵在从由阳极缓冲液、清洗液、封闭溶液、抗体溶液以及检测反应溶液构成的组选择的两种液体间更换填充上述缓冲槽的液体。
根据上述的构成,能够简便地进行免疫印迹。
本发明的方式3所涉及的样本分离转印装置可以是,在上述方式1或者2中,对于上述缓冲槽的底面来说,一部分区域为亲水性,包围该一部分区域的区域为疏水性。
根据上述的构成,在缓冲槽填充少量的液体情况下,能够将该液体高效地保持在亲水性的区域。若使转印膜1与保持于亲水性的区域的液体接触,则能够高效地促进反应。因此,能够减少高价格的试剂的液体量。
本发明的方式4所涉及的样本分离转印装置可以是,在上述方式1或者2中,上述缓冲槽的底面具备向相对于上述转印膜1接近分离的方向移动的升降板(升降板82)。
根据上述的构成,上述缓冲槽的底面的局部(即升降板)与转印膜1之间的距离变短。因此,通过在升降板保持有液体的状态下向相对于转印膜1接近的方向移动,即使是较少的液体量,也能够使液体与转印膜1接触。因此,能够进一步减少高价格的试剂的液体量,另外,能够高效地促进反应。
本发明的方式5所涉及的样本分离转印装置可以是,在上述方式4中,上述升降板(升降板82)的上表面的外边缘部为疏水性,其它区域为亲水性。
根据上述的构成,能够更可靠地将液体保持在升降板的上表面的内侧(即亲水性的区域)。
本发明的方式6所涉及的样本分离转印装置可以是,在上述方式1~5中,具备收纳在上述缓冲槽的底面,且能够通过突出将该缓冲槽分为两个区域(第一区域35和第二区域36)的隔板33。
根据上述的构成,通过隔板33将缓冲槽分为两个区域。通过仅在一个区域进行电泳、转印后的操作,能够减少使用的液体量。因此,能够实现高价格的试剂的节约和时间的缩短。
本发明的方式7所涉及的样本分离转印装置可以是,在上述方式1~6中,上述缓冲槽的底面倾斜。
根据上述的构成,在液体的更换时能够将填充缓冲槽的液体聚集在缓冲槽的较低的区域。因此,能够高效地进行填充缓冲槽的液体的更换。
本发明的方式8所涉及的样本分离转印装置可以是,在上述方式1~7中,在缓冲槽的底面设有槽(槽73)。
根据上述的构成,在液体的更换时能够将填充缓冲槽的液体在缓冲槽的底面聚集在槽。因此,能够高效地进行填充缓冲槽的液体的更换。
本发明的方式9所涉及的样本分离转印装置可以是,在上述方式1~8中,具备保持上述转印膜1并进行摇晃的臂部。
根据上述的构成,在转印后的处理中,臂能够保持转印膜1并使其摇晃。因此,能够高效地进行反应。
本发明的方式10所涉及的样本分析方法是,使用上述方式1~9中任意一个所涉及的样本分离转印装置,进行受检体的分离、向转印膜的转印、以及免疫染色(例如,清洗、封闭、抗体反应、检测反应等)的方法,在缓冲槽内进行向转印膜1的转印和免疫染色。
根据上述的构成,起到与上述方式1~9同等的效果。
本发明并不限定于上述的实施方式,在权利要求示出的范围能够进行各种变更,对不同的实施方式分别适当地组合公开的技术手段得到的实施方式也包含于本发明的技术范围。并且,通过对各实施方式分别组合公开的技术手段,能够形成新的技术特征。
本发明能够在生物体分子等的分析领域中进行利用。
附图标记说明
1…转印膜,11a、11b…泵(送液泵),12a~12f…储液罐,13a~13h…软管,14a、14b…管嘴,15a、15b…开口部,16a、16b…连接部,20…框架,20a…框架下部,20b…框架上部,23…滑架(臂部),24…垫片,30…阳极缓冲槽(缓冲槽),31…桌台,32…阳极,33…隔板,34…珀尔帖元件,35…第一区域,36…第二区域,40…阴极缓冲槽,41…阴极,42…锁止件,50…分离部,50a…第一开口(排出部),50b…第二开口,51、53…绝缘板,52…分离凝胶(分离介质),62…马达(驱动部),63…滚珠丝杠(驱动部),64…导轴(驱动部),65…轴架(驱动部),66…导柱(臂部),68…控制部,71…亲水性区域(一部分区域),72…疏水性区域(包围一部分区域的区域),73…槽,81…滚珠丝杠,82…升降板,83…空间,91a~91f…泵(送液泵),92a~92f…储液罐,93a~93l…软管,94a~94f…管嘴,100…分离转印装置。
- 还没有人留言评论。精彩留言会获得点赞!