基于SERS检测技术和微流控芯片的多种肿瘤标志物检测平台及方法与流程
本发明属于光谱学和生物分析技术领域,具体涉及一种基于SERS检测技术和微流控芯片的多种肿瘤标志物检测平台及方法。
背景技术:
近年来,尽管目前人们越来越了解乳腺癌的演变过程,医疗方式也在不断的进步,但是乳腺癌患者的死亡率依然非常高。其中的一个原因就是乳腺癌患者被诊断出患有乳腺癌比较晚,所以提高乳腺癌患者的早期诊断准确性显得至关重要,这能提高乳腺癌患者的存活率。
到目前为止,已经有大量的实验证明肿瘤标志物对于癌症早期诊断和监控有很大的潜力。然而只检测一种肿瘤标志物从而判断患者是否患有癌症是往往不准确的,同时检测多种肿瘤标志物能够增加癌症早期诊断的准确性。如同时检测三种乳腺癌肿瘤标志物(antigen 15-3)CA153、(antigen 12-5)CA125、(carcinoembryonic antigen)CEA能够提高乳腺癌诊断的准确性已经被证明,所以我们需要一个平台能够同时检测多种肿瘤标志物。
目前对于癌症肿瘤标志物的检测主要有SERS、ELISA、LSPR、SPR、RIA、CLEIA等等。由于标志物在早期癌症患者体内的含量很少,如乳腺癌肿瘤标志物(CA153<30u/ml CA125<35u/ml CEA≤5.9ng/ml),而SERS能够提高探测的灵敏度,所以使用SERS检测技术。基于SERS的检测方法主要分为无标和有标检测,无标探测是指生物分子被直接的检测,而有标检测为使用连接上拉曼报告分子的探针间接的检测目标分子。由于有标检测相比无标检测能大幅度的提高检测的灵敏度,所以有标检测方法被采用。
近年来,由于微流控芯片具有液体流动可控、消耗试样和试剂极少、分析速度成十倍上百倍地提高,以及可以在几分钟甚至更短的时间内进行上百个样品的同时分析,并且可以在线实现样品的预处理及分析全过程等的优点,使得基于微流控芯片进行DNA、蛋白质等微量物质的探测得到了越来越广泛的应用。于此同时微流控芯片由于其体积小便于集成,使用样品和试剂少的同时还能获得高通道,试剂在微流控通道内反应速度快等特点以及在生物、化学、医学等领域获得了大量的使用。考虑到实际应用中的便携性和患者样品量少等原因,我们选用了PDMS芯片。
技术实现要素:
发明目的:为了克服现有技术中存在的不足,提高早期癌症诊断的准确性和灵敏度,本发明提供一种基于SERS检测技术和微流控芯片的多种肿瘤标志物检测平台,能同时检测多种肿瘤标志物并能提高检测灵敏度,可以极大的增强肿瘤标志物的检测灵敏度,为早期癌症的诊断提供有力的技术支持。
技术方案:为实现上述目的,本发明采用的技术方案为:
一种基于SERS检测技术和微流控芯片的多种肿瘤标志物检测平台,包括由微流控芯片制成的微流控通道及其内的SERS衬底,以及SERS探针和探测抗体;
所述微流控通道为十字交叉形,横向通道内为所述SERS衬底,垂直的纵向通道内通入所述SERS探针和探测抗体,交叉区域即为检测区域;
所述SERS衬底由金属纳米粒子通入所述微流控通道内得到,所述SERS衬底上连接有捕获抗体;
所述SERS探针由金属纳米粒子分别与拉曼报告分子、二抗连接,然后用BSA进行金属表面空隙的填补制成。
进一步的,所述微流控芯片为PDMS芯片。
进一步的,所述捕获抗体不少于两种。
一种基于SERS检测技术和微流控芯片的多种肿瘤标志物检测平台的方法,包括以下步骤:
首先,制备SERS探针:
步骤1).制备金属纳米粒子;
步骤2).在步骤1)中得到的金属纳米粒子表面接上拉曼报告分子;
步骤3).在步骤2)中将连接有拉曼报告分子的金属纳米粒子表面连接上捕获抗体;
步骤4).在步骤3)后使用BSA填补金属纳米粒子表面的空隙形成SERS探针;
其次,制备SERS衬底:
步骤5).将PDMS芯片贴合在羟基化的玻璃片上,形成微流控通道;
步骤6).向所述微流控通道内通入带正电的溶液;
步骤7).将步骤1)中的金属纳米粒子通入所述微流控通道内,得到SERS衬底;
步骤8).重复步骤6)和步骤7)两到三次,形成多层SERS衬底;
步骤9).在步骤8)得到的SERS衬底上连接上捕获抗体;
步骤10).在步骤9)的基础上通入BSA进行填补金属表面空隙;
然后,抗体检测:
步骤11).取下PDMS芯片等待玻璃表面干燥后,在与原来PDMS芯片垂直的方向贴合上新的PDMS芯片;
步骤12).在步骤11)的基础上通入BSA;
步骤13).在步骤12)后进一步向新的微流通道内通入待测溶液;
步骤14).在步骤13)的基础上向新的微流控通道内通入与步骤9)对应的探测抗体;
步骤15).在步骤14)后将步骤4)所制备的SERS探针通入到新的微流控通道内;
最后,SERS光谱成像:
步骤16).对步骤11)所形成的通道交叉区域进行SERS光谱成像。
进一步的,所述步骤2)、3)、4)、9)、10)、12)中的拉曼报告分子、捕获抗体、BSA通过化学键插入到金属纳米粒子表面。
进一步的,所述步骤6)、7)、8)、9)、10)、12)、13)、14)、15)中向微流控通道内通入试剂的方法为通过注射泵将装有试剂的注射器中的试剂通过PE管连接钢针,然后钢针插入到所述微流控通道内的方式注射,通过调注射泵参数控制注射的试剂量和注射速率。
进一步的,所述步骤7)中的所述SERS衬底是利用静电吸附的原理形成。
进一步的,所述步骤13)和步骤14)中,待测溶液中的肿瘤标志物与捕获抗体间的连接为抗原和抗体间的特异性识别。
进一步的,所述步骤15)中所述SERS探针与探测抗体的识别为SERS探针上的二抗与所述探测抗体的特异性识别。
进一步的,所述步骤13)~16)中所述待测试剂中若含有肿瘤标志物,则通入探测抗体,会形成“三明治”结构;继续通SERS探针,即可检测该“三明治”结构是否已形成。
有益效果:本发明提供的基于SERS检测技术和微流控芯片的多种肿瘤标志物检测平台,具有以下优点:
1、所设计的平台可以同时检测多种肿瘤标志物,提高癌症早期诊断的准确性;
2、所设计的平台所使用的SERS衬底可以提高检测的灵敏度;
3、所设计的平台在抗体-抗原-抗体形成“三明治”结构的基础上通过连接有二抗的SERS探针进行探测,由于二抗可以检测一抗的存在并放大信号,并且和SERS技术联用可以极大的增加检测的灵敏度。
4、由于与肿瘤标志物相关的抗体价格相对都较高,而二抗普遍价格较低,所以二抗的使用可以在达到较高检测灵敏度的同时节约成本。
5、所设计的平台由于微流控芯片的使用,使得使用样品和试剂少的同时还能获得高通量,并且试剂在微流控通道内反应时具有反应速度快等特点。
6、所设计的平台尺寸小巧便于携带和集成。
附图说明
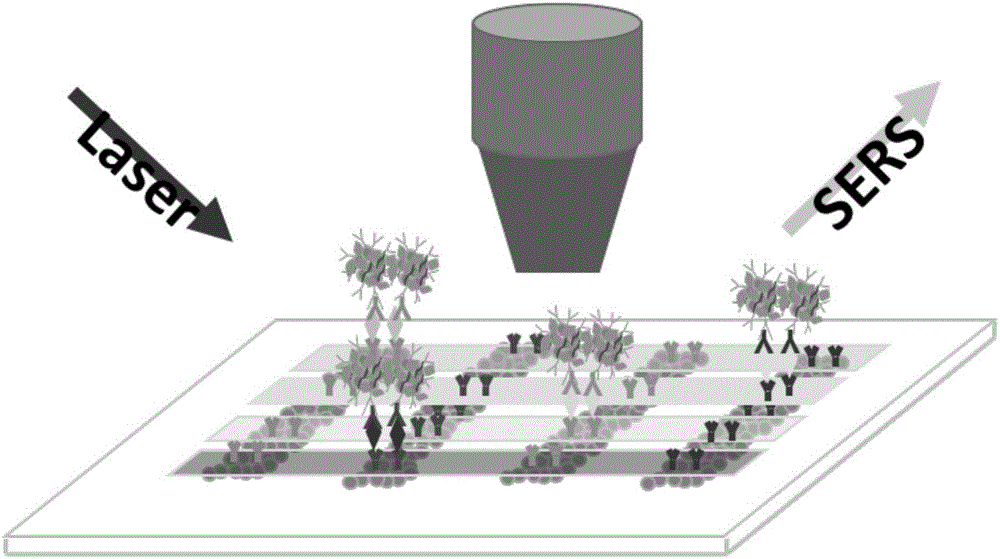
图1为本发明检测原理示意图;
图2为本发明所设计的一种同时检测多种肿瘤标志物示意图。
具体实施方式
下面结合附图对本发明作更进一步的说明。
如图1所示为一种基于SERS检测技术和微流控芯片的多种肿瘤标志物检测平台,本发明为一种基于表面增强拉曼散射(SERS)检测技术和微流控芯片能同时检测多种肿瘤标志物并能提高检测灵敏度的平台,该平台通过先在微流控通道内形成SERS衬底来提高检测的灵敏度,然后在SERS衬底上形成经典的“三明治”结构以检测待测试剂中是否含有特定的肿瘤标志物。通过先用PDMS芯片在衬底上连接上特定的捕获抗体,然后将新的PDMS芯片的放置位置垂直于之前的放置位置以达到在交叉区域可以同时检测多种肿瘤标志物的作用。通过通入连接有二抗和拉曼报告分子的SERS免疫探针以达到定性以及定量探测待测试剂中肿瘤标志物的作用,由于二抗可以放大信号,所以可以进一步的提高检测的灵敏度。整个平台可以同时定性定量检测多种肿瘤标志物,对癌症患者早期诊断出患有癌症并提高存活率提供了有利的技术支持。
如图1所示的SERS探针,该探针由金属纳米粒子分别与拉曼报告分子、二抗连接,然后用BSA进行金属表面空隙的填补制成。图1所示为本发明基于SERS检测技术和微流控芯片平台的检测原理,在微流控通道中形成SERS衬底用于增强检测的灵敏度,然后在衬底上连接上特定的抗体用以捕获待测试剂中的特定肿瘤标志物,若待测试剂中含有特定的肿瘤标志物,则会在接下来通探测抗体时形成金典的“三明治”结构,如果待测试剂中未含有特定的肿瘤标志物时则不会形成该种“三明治”结构。然后在后续的通SERS探针时若形成了“三明治”结构则会由于二抗识别一抗而形成如图1所示的4层结构,如果没有则不会形成该种特殊结构,通过检测探针上的拉曼分子信号即可间接定性的判断待测试剂中是否含有特定的肿瘤标志物。
如图2所示,通过先用PDMS芯片在衬底上连接上特定的捕获抗体,然后将新的PDMS芯片的放置位置垂直于之前的放置位置,若在不同的微流控通道中通不同的捕获抗体,则可以在交叉区域同时检测多种肿瘤标志物。
本发明设计了一种基于SERS检测技术和微流控芯片能同时检测多种肿瘤标志物并能提高检测灵敏度的平台,利用微流控芯片所提供的特殊环境以及SERS极高的信号增强作用,再通过形成SERS衬底以及SERS探针来极大的增加检测的灵敏度以及可以同时检测多种肿瘤标志物。
本发明的一种基于SERS检测技术和微流控芯片能同时检测多种肿瘤标志物并能提高检测灵敏度的平台检测方法过程,具体可以分为以下步骤:
步骤1).制备金属纳米粒子;
步骤2).在步骤1)中得到的金属纳米粒子表面接上拉曼报告分子;
步骤3).在步骤2)中将连接有拉曼报告分子的金属纳米粒子表面连接上特定捕获抗体;
步骤4).在步骤3)后使用BSA填补金属纳米粒子表面的空隙形成SERS探针;
步骤5).将PDMS芯片贴合在羟基化过的玻璃片上;
步骤6).向微流控通道内通入带正电的溶液;
步骤7).利用步骤1)中的金属纳米粒子通入微流控通道内,利用静电吸附的原理形成SERS衬底;
步骤8).重复步骤6)和步骤7)两到三次,形成多层SERS衬底;
步骤9).在步骤8)得到的SERS衬底上连接上特定捕获抗体;
步骤10).在步骤9)的基础上通入BSA进行填补金属表面空隙;
步骤11).取下PDMS芯片等待玻璃表面干燥后在与原来PDMS芯片垂直的方向贴合上新的PDMS芯片;
步骤12).在步骤11)的基础上通入BSA;
步骤13).在步骤12)后进一步向新的微流控通道内通入待测溶液;
步骤14).在步骤13)的基础上向新的微流控通道内通入与步骤9)对应的特定探测抗体;
步骤15).在步骤14)后将步骤4)所制备的SERS探针通入到微流控通道内;探针与探测抗体的识别为探针上的二抗与特定的探测抗体的特异性识别;
步骤16).对步骤11)所形成的通道交叉区域进行SERS光谱成像。
其中,步骤2)、3)、4)、9)、10)、12)中的拉曼报告分子、抗体、BSA通过化学键插入到金属纳米粒子表面。
其中,步骤6)、7)、8)、9)、10)、12)、13)、14)、15)中向微流控通道内通入试剂的方法为通过注射泵将装有试剂的注射器中的试剂通过PE管连接钢针,然后钢针插入到微流控通道内的方式注射,通过调注射泵参数可以控制注射的试剂量和注射速率。
步骤13)、14)中肿瘤标志物与特定抗体间的连接为抗原和抗体间的特异性识别。
实施例
如图1和如图2所示,本发明一种基于SERS检测技术和微流控芯片能同时检测多种肿瘤标志物并能提高检测灵敏度的平台检测的过程包括以下步骤:
1)银纳米粒子的制备,首先,将390ml去离子水和0.072g AgNO3以130℃在搅拌状态下加热至沸腾,然后加入10ml,1%的柠檬酸钠,继续加热至溶液呈黄绿色,停止加热,在室温下让溶液冷却,从而制成银胶以备后用.
2)SERS探针的制备,取6ml银胶用离心机以11000rpm的速率离心30分钟,去掉上层清液加入4ml去粒子水。然后,向4ml的银胶溶液中加入40μl的10mmol的4MBA并在搅拌状态下让其混合至少两个小时。最后,取1.5ml混合后溶液以900rpm的速率离心20分钟,去掉上清液然后加入1ml的BBS缓冲液。将50ul的1mg/ml的羊抗小鼠加入到之前处理好的1ml 4-MBA标记的银胶中,让其在4℃下放置2h。然后,以6500rpm的速率离心12min,去掉上清液中多余的抗体并向沉淀中加入1ml的BBS缓冲液。接着,加入10μl 5%的BSA溶液以填补银纳米粒子表面未被4-MBA和羊抗小鼠覆盖的空隙,然后将其放置在4℃下1h。最后以6500rpm的速率离心12min,去掉上清液并加入200μl的BBS缓冲液。
3)玻璃片和PDMS芯片预处理,所使用的玻璃预先浸泡在98%H2SO4和30%H2O2以体积比3:1混合的溶液中,在使用时用大量的去离子水冲洗,然后用氮气吹干,置于温度设定为80℃的烘箱中。所使用的PDMS芯片预先浸没在浓度为99%的酒精中,并密封好放置于超声机中超洗2h,然后将PDMS芯片从酒精中取出并用大量的去离子水冲洗,然后用氮气吹干,重复上述步骤至少两次,然后置于80℃的烘箱中2h。从烘箱中取出PDMS芯片并将其与玻璃片贴合,确保芯片与玻璃片之间没有气泡。
4)免疫检测,如图2所示首先使用注射泵将1%的PDDA以0.8μl/min的速率注射到PDMS芯片上的微流控通道内25min,然后向微流控通道内以相同的速率通入浓缩了20倍的银胶通25min。重复上述步骤。然后我们向微流控通道内以0.8μl/ml的速率通抗体兔抗CA153、兔抗CA125、兔抗CEA 25min,然后静置25min以使抗体充分连接到银纳米粒子上,通抗体的目的是捕获待测试剂中的肿瘤标志物CA153、CA125、CEA。接着以速率为2μl/min通5%BSA持续3min以冲掉未连接到纳米粒子上的抗体,然后速率改为0.8μl/m通25min为了防止非特异性吸附。然后,小心的拿下PDMS芯片并等待玻璃片上的液体在室温下自然风干。从烘箱中取出一块新的PDMS芯片并使PDMS芯片与玻璃片贴合,PDMS上的通道方向与玻璃片上的衬底方向垂直。向微流控通道内依次用注射泵注BSA、待测试剂、特定的对应探测抗体小鼠抗CA153、小鼠抗CA125、小鼠抗CEA、SERS探针,每一种反应物都是以0.8μl/m的速率,注射时间都是25min,并且注射完都让其静置25min,而且每次在静置完之后都用注射泵以2μl/m的速率注射PBST持续3分钟。等上述步骤全部做完之后将微流控通道中的液体用空气将其排出之后就可以SERS测量了。
上述实施例的结果为:当衬底上修饰了不同的捕获抗体时,含有与衬底上捕获抗体相对应的肿瘤标志物的待测试剂,当最终进行SERS测量时其SERS信号相对较强,而待测试剂中含有与衬底上捕获抗体不对应的肿瘤标志物其SERS信号则相对较弱。上述结果说明所述基于SERS检测技术和微流控芯片的多种肿瘤标志物检测平台及方法可以很好的通过SERS信号的测量来判断待测试剂中是否含有特定的乳腺癌肿瘤标志物,而且该平台相较与现有技术其在使用样品和试剂少的同时还能获得高通量,并且试剂在微流控通道内反应时具有反应速度快等特点,而且由于二抗的使用可以使得整个检测的成本降低。
以上所述仅是本发明的优选实施方式,应当指出:对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 普适型用于同时检测多种肿瘤标志物的微流控芯片装置的制造方法
- 男性适用的典型肿瘤标志物联合检测用微流控芯片装置的制造方法
- 女性适用的典型肿瘤标志物联合检测用微流控芯片装置的制造方法
- 一种检测口腔癌的标志物及其试剂盒的制造方法与工艺
- microRNA 标志物组及其在制备检测胃癌淋巴结转移试剂盒中的应用的制造方法与工艺
- 基于弹性蛋白酶荧光底物检测乳腺癌肿瘤标志物CA153的酶联免疫试剂盒制备方法与制造工艺
- 检测和评价力量训练效果的miRNA标志物或其组合及其应用的制造方法与工艺
- 一种最优超平面的构建方法、动态优化系统和构建装置与制造工艺
- 癌症标志物及癌症的判定方法与制造工艺
- 检测尿液中单羟酚类代谢物的试剂盒及其制备方法与制造工艺