达格列净中间体A中葡萄糖酸内酯残留量的检测方法与流程
本发明属于药物分析领域,具体涉及一种达格列净中间体a中葡萄糖酸内酯的残留量的检测方法。
背景技术:
达格列净是由百时美施贵宝公司和阿斯利康公司开发的钠-葡萄糖转运蛋白(sglt)抑制剂,化学名为2-氯-5-(β-d-吡喃葡萄糖-1-基)-4′-乙氧基二苯甲烷。2012年12月在欧盟上市,2014年1月在美国上市,2017年3月在我国上市,商品名为farxiga。研究显示,sglt(主要是sglt2)可调节血糖在肾小球的滤过重吸收过程,因此达格列净通过对sglt2的抑制作用,阻止葡萄糖在肾脏的重吸收,增加葡萄糖在尿液中的排泄从而起到降低血糖的作用,是非常有效的sglt2抑制剂。
根据文献报道的达格列净的合成工艺(j.med.chem.2008,51,1145–1149),路线如下:
达格列净合成路线
其关键中间体为达格列净中间体a(cas号:461432-24-6),结构如下:
达格列净中间体a。
该步骤以2,3,4,6-四-o-三甲基硅基-d-葡萄糖酸内酯(以下简称葡萄糖酸内酯)和(5-溴-2-氯苯基)(4-乙氧基苯基)甲烷为原料,首先将葡萄糖酸内酯在正丁基锂催化下得到tms基保护的葡萄糖酸内酯,再与(5-溴-2-氯苯基)(4-乙氧基苯基)甲烷反应,得到中间体a。其中,该步骤的主要杂质为起始物料之一的葡萄糖酸内酯。因中间体a中葡萄糖酸内酯的存在会造成进一步的杂质传递,且在后续反应中很难去除,因此在反应中为了避免传递杂质的产生,需要严格控制中间体a中葡萄糖酸内酯的含量。
葡萄糖酸内酯性状为白色结晶或结晶性粉末,几乎无臭味,先甜后酸,易溶于水。稍溶于乙醇,几乎不溶于乙醚。目前,国际上尚未有统一的检测葡萄糖酸内酯的标准方法。从已发表的国内外文献来看,检测方法有多种,既有化学分析方法也有仪器分析方法。前者主要是化学滴定法,后者则包括气液色谱、高效液相色谱、质谱和红外光谱等多种方法。检测物种类也有所不同,有些方法侧重于分析葡萄糖氧化产物,即由葡萄糖、葡萄糖酸和葡萄糖酸内酯等构成的混合物中的内酯含量,有些方法侧重于分析食品中的内酯含量。由于检测物种类不同,因此检测方法往往也随之不同。
文献记载,葡萄糖酸内酯的检测分析方法主要有比色法、气相色谱法和高效液相色谱法。比色法操作复杂且灵敏度低,气相色谱法要求样品具有良好的挥发性和热稳定性,而糖类化合物含有大量的羟基,不能在高温下直接挥发,需要对样品进行衍生处理,导致操作繁琐,并且在高温条件下分析可能导致样品分解。高效液相色谱法主要有正相色谱法和反相法:正相色谱法一般用氨基柱进行分离,但灵敏度低,一般只用于样品的定性分析。若进行定量分析则需对样品进行衍生处理,以提高检测灵敏度和避免葡萄糖酸内酯的羰基与氨基柱上键合的氨基发生亲核加成反应而影响检测结果并保护氨基柱。鉴于上述几种检测方法在实际检测中的缺陷与不足,开发一种方便、灵敏、无干扰的分析方法具有重要的意义。
技术实现要素:
针对现有技术中的上述技术问题,本发明提供了一种达格列净中间体a中葡萄糖酸内酯的残留量的检测方法,该方法使用反相高效液相色谱法,具有柱效高,重现性好,可用于梯度洗脱操作,应用范围广等优点,解决了现有技术中存在的问题,弥补了现有技术不足,为葡萄糖酸内酯的检测提供了一种通用方法。
具体而言,本发明提供一种达格列净中间体a中葡萄糖酸内酯的残留量的检测方法,该方法采用高效液相色谱分析仪,选用十八烷基键合硅胶为填充剂的色谱柱,规格4.6mm×250mm,5μm;流动相为乙腈和水的混合液、乙腈和磷酸盐缓冲液的混合液、甲醇和水的混合液、甲醇和磷酸盐缓冲液的混合液中的一种;流速0.5-1.2ml/min;柱温为20-30℃;紫外检测器波长为190nm;进样体积为20μl;先出峰的化合物为葡萄糖酸内酯,后出峰的化合物为达格列净中间体a。
进一步地,所述色谱柱的规格为4.6mm×250mm,5μm。
进一步地,所述流动相由乙腈和水组成,乙腈和水的体积比为1~10:99~90。
进一步地,所述流动相由乙腈和磷酸盐缓冲液组成,乙腈和磷酸盐缓冲液的体积比为5~15:95~85。
进一步地,所述流动相由甲醇和水组成,甲醇和水的体积比为1~10:99~90。
进一步地,所述流动相由甲醇和磷酸盐缓冲液组成,甲醇和磷酸盐缓冲液的体积比为5~15:95~85。
进一步地,所述磷酸盐缓冲液由磷酸二氢钠和磷酸氢二钠组成,其ph值为6.5-7.5。
进一步地,所述流动相的流速为1ml/min,色谱柱温度为25℃。
本发明的达格列净中间体a中葡萄糖酸内酯的残留量的检测方法实现了葡萄糖酸内酯含量的测定,使关键中间体a的纯度得到了保证,减少了后续反应中杂质生成的概率。该方法操作简单,专属性强,灵敏度高,线性范围良好,为葡萄糖酸内酯含量测定提供了有效的技术手段,可满足国内外法规的限量要求。
本发明的方法方便、灵敏、无干扰,弥补了现有技术的缺陷,适用于葡萄糖酸内酯含量的一般测定,为工业化生产带来了巨大的社会意义,具有很强的实用性。
附图说明
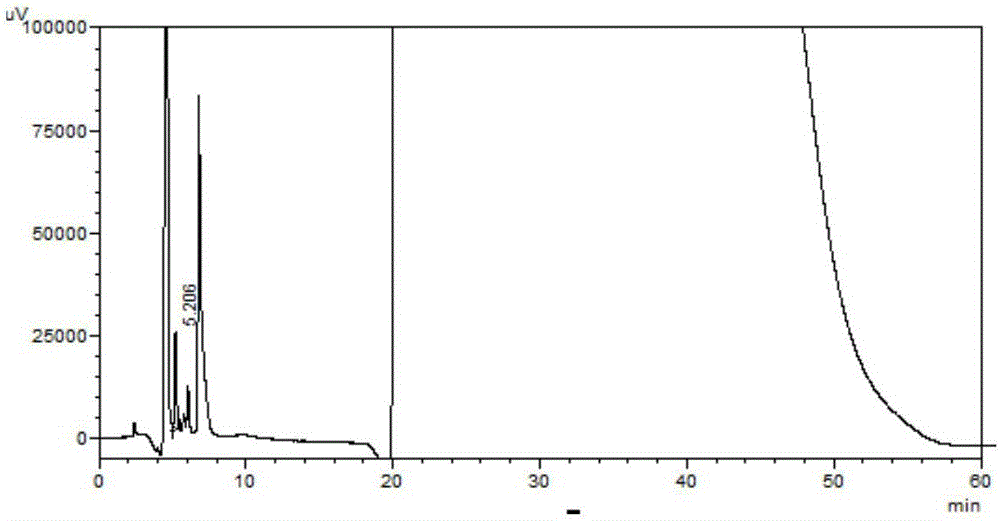
图1为实施例1的色谱分离图,保留时间为5.206min的是葡萄糖酸内酯,保留时间大于20min的是中间体a。
图2为实施例2的色谱分离图,保留时间为5.210min的是葡萄糖酸内酯,保留时间大于20min的是中间体a。
图3为实施例3的色谱分离图,保留时间大于20min的是中间体a,葡萄糖酸内酯未检出。
图4为实施例4的色谱分离图,保留时间大于20min的是中间体a,葡萄糖酸内酯未检出。
图5为实施例5的色谱分离图,保留时间为4.600min的是葡萄糖酸内酯,保留时间大于20min的是中间体a。
图6为实施例6的色谱分离图,保留时间大于20min的是中间体a,葡萄糖酸内酯未检出。
具体实施方式
下面通过具体的实施例并结合附图对本发明做进一步阐述,但并不限制本发明。
实施例所用到的仪器与条件:
仪器:日本岛津高效液相色谱仪(spd-20av紫外检测器,sil-20a进样器,lc-20at泵),
tb-215d电子天平(丹佛仪器)
色谱柱:采用welthultimateaq-c18柱(4.6×250mm,5μm)
在葡萄糖酸内酯测定结束后,采用梯度洗脱的方式将色谱柱中残留的中间体a进行有效的洗脱。
测试样品:按照前述达格列净合成路线分别合成6批次中间体a,编号分别为dg-a-1,dg-a-2,dg-a-3,dg-a-4,dg-a-5,dg-a-6。
经过筛选,确定葡萄糖酸内酯溶液(即对照品溶液)的配制方法为:称取葡萄糖酸内酯约25mg置50ml容量瓶中,加溶剂1(乙腈:水=1:1)溶解并稀释至刻度,摇匀,作为对照品储备液,精密量取对照品储备液1.0ml置20ml量瓶中,加溶剂2(乙腈:水=9:1)稀释至刻度,摇匀,作为对照品溶液。
实施例1
一种达格列净中间体a中葡萄糖酸内酯的残留量的检测方法,其步骤如下:
取dg-a-1批次合成的中间体a样品25mg,置于50ml的容量瓶中,加乙腈-水溶解稀释定容至刻度,摇匀,作为供试品溶液;采用高效液相色谱仪,以十八烷基键合硅胶为填充剂的色谱柱,以乙腈和水组成的混合液为流动相,采用如下色谱分离条件进行分离:
流动相流速:1.2ml/min
色谱柱温度:25℃
检测波长:190nm
所述流动相中,按体积百分比计算,乙腈:水为5:95
精密移取上述各溶液20μl,注入液相色谱仪,记录色谱图。
色谱分离结果见图1所示,从图1可以看出,与对照品溶液相比,保留时间为5.206min的是葡萄糖酸内酯,大于20min的为中间体a,该批次样品含有检测限以上的葡萄糖酸内酯。
实施例2
一种达格列净中间体a中葡萄糖酸内酯的残留量的检测方法,其步骤如下:
取dg-a-2批次合成的中间体a样品25mg,置于50ml的容量瓶中,加乙腈-磷酸盐缓冲液溶解稀释定容至刻度,摇匀,作为供试品溶液;采用高效液相色谱仪,以十八烷基键合硅胶为填充剂的色谱柱,以乙腈和磷酸盐缓冲液组成的混合液为流动相,采用如下色谱分离条件进行分离:
流动相流速:0.8ml/min
色谱柱温度:20℃
检测波长:190nm
所述流动相中,按体积百分比计算,乙腈:磷酸盐缓冲液为8:92,所述磷酸盐缓冲液的ph值为6.5
精密移取上述各溶液20μl,注入液相色谱仪,记录色谱图。
色谱分离结果见图2所示,从图2可以看出,与对照品溶液相比,保留时间为5.210min的是葡萄糖酸内酯,大于20min的为中间体a,该批次样品含有检测限以上的葡萄糖酸内酯。
实施例3
一种达格列净中间体a中葡萄糖酸内酯的残留量的检测方法,其步骤如下:
取dg-a-3批次合成的中间体a样品25mg,置于50ml的容量瓶中,加乙腈-磷酸盐缓冲液溶解稀释定容至刻度,摇匀,作为供试品溶液;采用高效液相色谱仪,以十八烷基键合硅胶为填充剂的色谱柱,以乙腈和磷酸盐缓冲液组成的混合液为流动相,采用如下色谱分离条件进行分离:
流动相流速:0.5ml/min
色谱柱温度:20℃
检测波长:190nm
所述流动相中,按体积百分比计算,乙腈:磷酸盐缓冲液为15:85,所述磷酸盐缓冲液的ph值为7
精密移取上述各溶液20μl,注入液相色谱仪,记录色谱图。
该测试条件下,对照品溶液中葡萄糖酸内酯的保留时间为4.501min。
色谱分离结果见图3所示,从图3可以看出,与对照品溶液相比,保留时间大于20min的是中间体a,未检出葡萄糖酸内酯的峰,说明该批次的中间体a中葡萄糖酸内酯的残留量接近0,该批次产品合格。
实施例4
一种达格列净中间体a中葡萄糖酸内酯的残留量的检测方法,其步骤如下:
取dg-a-4批次合成的中间体a样品25mg,置于50ml的容量瓶中,加甲醇-水溶解稀释定容至刻度,摇匀,作为供试品溶液;采用高效液相色谱仪,以十八烷基键合硅胶为填充剂的色谱柱,以甲醇和水组成的混合液为流动相,采用如下色谱分离条件进行分离:
流动相流速:0.8ml/min
色谱柱温度:25℃
检测波长:190nm
所述流动相中,按体积百分比计算,甲醇:水为5:95。
精密移取上述各溶液20μl,注入液相色谱仪,记录色谱图。
该测试条件下,对照品溶液中葡萄糖酸内酯的保留时间为5.124min。
色谱分离结果见图4所示,从图4可以看出,与对照品溶液相比,保留时间大于20min的是中间体a,未检出葡萄糖酸内酯的峰,说明该批次的中间体a中葡萄糖酸内酯的残留量接近0,该批次产品合格。
实施例5
一种达格列净中间体a中葡萄糖酸内酯的残留量的检测方法,其步骤如下:
取dg-a-5批次合成的中间体a样品25mg,置于50ml的容量瓶中,加甲醇-磷酸盐缓冲液溶解稀释定容至刻度,摇匀,作为供试品溶液;采用高效液相色谱仪,以十八烷基键合硅胶为填充剂的色谱柱,以甲醇和磷酸盐缓冲液组成的混合液为流动相,采用如下色谱分离条件进行分离:
流动相流速:1.2ml/min
色谱柱温度:30℃
检测波长:190nm
所述流动相中,按体积百分比计算,甲醇:磷酸盐缓冲液为15:85,所述磷酸盐缓冲液的ph值为7.5
精密移取上述各溶液20μl,注入液相色谱仪,记录色谱图。
色谱分离结果见图5所示,从图5可以看出,与对照品溶液相比,保留时间为4.6min的是葡萄糖酸内酯,保留时间大于20min的是中间体a,该批次样品含有检测限以上的葡萄糖酸内酯。
实施例6
一种达格列净中间体a中葡萄糖酸内酯的残留量的检测方法,其步骤如下:
取dg-a-6批次合成的中间体a样品25mg,置于50ml的容量瓶中,加甲醇-水溶解稀释定容至刻度,摇匀,作为供试品溶液;采用高效液相色谱仪,以十八烷基键合硅胶为填充剂的色谱柱,以甲醇和水组成的混合液为流动相,采用如下色谱分离条件进行分离:
流动相流速:1.0ml/min
色谱柱温度:20℃
检测波长:190nm
所述流动相中,按体积百分比计算,甲醇:水为10:90
精密移取上述各溶液20μl,注入液相色谱仪,记录色谱图。
该测试条件下,对照品溶液中葡萄糖酸内酯的保留时间为4.208min。
色谱分离结果见图6所示,从图6可以看出,与对照品溶液相比,保留时间大于20min的是中间体a,未检出葡萄糖酸内酯的峰,说明该批次的中间体a中葡萄糖酸内酯的残留量接近0,该批次产品合格。
综上所述仅为本发明的较佳实施例而已,并非用来限定本发明的实施范围。即凡依本发明申请专利范围的内容所作的等效变化与修饰,都应为本发明的技术范畴。
- 还没有人留言评论。精彩留言会获得点赞!