一种同时定量血浆内、外源性葡萄糖的二维核磁共振方法与流程
本发明属于分析化学方法领域,具体涉及一种基于稳定性同位素稀释法(isotopedilution,id)结合二维核磁共振技术用于快速、准确测定血浆中内、外源性葡萄糖浓度的定量方法。更具体地说,涉及一种以d-[u-13c]-葡萄糖作为标记物(示踪物),改编单量子相关核磁实验(hsqc)以测定血浆中内、外源性葡萄糖浓度的方法(id-hsqc)。
背景技术
葡萄糖是人及动物的重要能源物质,在能量代谢中扮演着重要角色。血糖的监测对多种疾病的诊断和治疗具有重要意义,通常血糖浓度的测定是利用酶反应的方法在自动分析仪上测试完成的。然而该方法并不能区分血样中内、外源性葡萄糖,而内、外源性葡萄糖的含量测定是在临床上研究葡萄糖代谢,胰岛素敏感性等实验中的重要参数。目前用于这些临床实验的方法主要方法有:气相色谱-质谱联用方法(gc-ms)、气相色谱-同位素比值质谱联用方法(gc-irms)、液相色谱-同位素比值质谱联用方法(lc-irms)以及液相色谱-串联质谱联用方法(lc-ms/ms)。但这些方法大多需要除蛋白,衍生化等繁琐的前处理步骤,以及需要相对较大量的同位素示踪物等缺点。因此开发样品前处理简单、同位素标记物用量较少又能准确测定血样中内、外源性葡萄糖的定量方法将具有重要实际应用价值。
技术实现要素:
本发明的目的在于提供一种基于稳定性同位素稀释法(isotopedilution,id)结合二维核磁共振技术用于快速、准确测定血浆中内、外源性葡萄糖浓度的定量方法。更具体地说,涉及一种以d-[u-13c]-葡萄糖作为标记物(示踪物),改编单量子相关核磁实验(hsqc)以测定血浆中内、外源性葡萄糖浓度的方法(id-hsqc)。本发明利用较低浓度的d-[u-13c]-葡萄糖(~0.035mm)作为标记物的同位素稀释法(isotopedilution),结合改编的单量子相关核磁实验(hsqc),简单、准确、快速地同时测定血浆中内、外源性葡萄糖浓度。
为了实现本发明的上述目的,本发明提供了如下的技术方案:
一种同时定量血浆内、外源性葡萄糖的二维核磁共振方法,利用少量d-[u-13c]葡萄糖作为示踪物和内标的同位素稀释法,结合适应性改编的核磁单量子相关实验(id-hsqc),测定相应的双峰和单峰的积分比值,以此计算血浆中内、外源性葡萄糖浓度。
一种同时定量血浆内、外源性葡萄糖的二维核磁共振方法,该方法包括下述步骤:
样品制备:取适量的血浆,加入少量氘代试剂,混匀后转移到核磁管;
核磁实验:在常规灵敏度增强单量子相关实验的脉冲序列基础上,将碳通道的180度非选择性重聚脉冲改为葡萄糖1号位13c1化学位移选择性重聚脉冲,从而消除δ1,δ2及随后2τ时间内碳碳耦合
浓度计算:利用核磁实验获得的积分值,通过下面的公式计算出内、外源葡萄糖摩尔浓度比值,
如所述的一种同时定量血浆内、外源性葡萄糖的二维核磁共振方法,该方法结合了同位素稀释法和hsqc核磁方法并对其进行了适应性改编,样品制备过程简单、标记葡萄糖用量少、能同时准确测定血浆内、外源性葡萄糖浓度。
如所述的一种同时定量血浆内、外源性葡萄糖的二维核磁共振方法,该方法在样品的制备过程中使用了氘代二甲基亚砜作为锁场试剂,在核磁实验的脉冲序列中利用了选择性重聚脉冲避免相位扭曲。
如所述的一种同时定量血浆内、外源性葡萄糖的二维核磁共振方法,样品制备只需往待测血浆中加入少量的锁场试剂,混匀后转移到核磁管,操作简单。
如所述的一种同时定量血浆内、外源性葡萄糖的二维核磁共振方法,该方法使用了氘代二甲基亚砜作为锁场试剂避免活泼氢交换。
如所述的一种同时定量血浆内、外源性葡萄糖的二维核磁共振方法,该方法对常规的hsqc脉冲序列进行适应性改编,采用了葡萄糖1号位13c化学位移选择性重聚脉冲,消除了同核13c1-13c2一键耦合对图谱相位的影响,从而保证图谱积分和定量分析的准确性。
本发明的方法可以更具体地描述为:
样品制备:取适量的血浆(如480ul),加入少量氘代试剂(核磁实验锁场用,如20uldmso-d6),混匀后转移到核磁管。
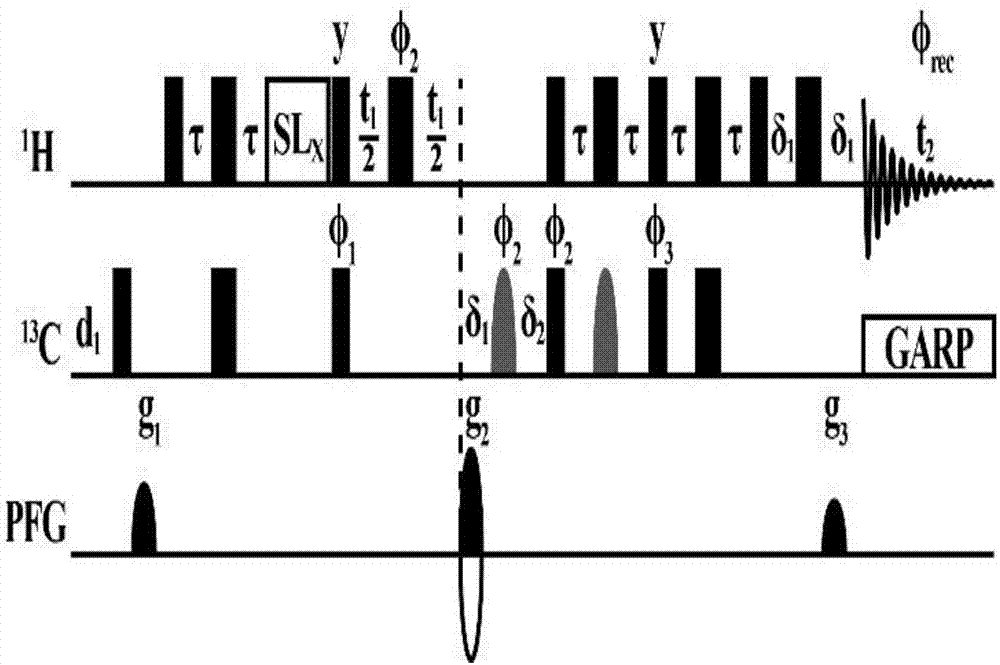
核磁实验:为了实现天然丰度和碳-13全标记葡萄糖的同时定量检测,在常规灵敏度增强单量子相关实验的脉冲序列基础上,将碳通道的180度非选择性重聚脉冲改为葡萄糖1号位13c1化学位移选择性重聚脉冲(图1,灰色正弦波型脉冲),从而消除δ1,δ2及随后2τ时间内碳碳耦合
浓度计算:利用核磁实验获得的积分值,通过下面的公式可以计算出内、外源葡萄糖摩尔浓度比值。
与现有技术相比,本发明的优点在于:(1)样品制备简单,只需要取适量血浆后直接加入少量氘代试剂便可以进行检测,而现有的方法的大多需要除蛋白及衍生化等繁琐的前处理步骤。(2)具有较大的同位素稀释比(~1%水平),同位素标记的示踪物用量少,从而可以降低实验成本。区别于一般的同位素稀释法,为了获得较为准确的定量结果,一般要求检测到的示踪物和被测物的信号强度相当,因而需要的同位素标记的示踪物的用量较大。(3)本发明使用改编的单量子相关核磁实验(hsqc),使用了葡萄糖1号位13c1化学位移选择性重聚脉冲(refocusingpulses),消除了同核一键耦合(13c1-13c2)对图谱相位的影响,以提高图谱积分及定量分析的准确性。
附图说明
图1用于内、外源性葡萄糖定量的改编的灵敏度增强hsqc脉冲序列图。
图2血浆id-hsqc图谱(α-d-吡喃型葡萄糖的1号基团信号区域局部放大图)。a)三维图;b)等高线图,中间单峰为α-d-吡喃型葡萄糖的1h-13c1(-12c2)基团信号,两边的双峰为d-吡喃型葡萄糖的1h-13c1(-13c2)基团信号。
图3标准曲线。横坐标为标样的理论摩尔浓度比值,纵坐标为通过实验测得的摩尔浓度比值。
图4同时定量血浆内、外源性葡萄糖的二维核磁共振方法(id-hsqc)技术路线图。
具体实施方式
下面结合附图,用本发明的实施例来进一步说明本发明的实质性内容,但并不以此来限定本发明。
本发明实施例的数据采集和处理按以下方法进行:
该发明所涉及的所有核磁实验均在配置qci-p低温探头的布鲁克avanceiii800核磁谱仪上进行。脉冲序列如图1,操控软件topspin3.2。使用topspin3.5进行数据处理。利用本研究组之前开发的lc-ms/ms方法对测量结果进行验证。液质联用数据处理使用dataanalysis4.1(bruker)。
实施例1:
为了证实利用本发明方法测定血浆内、外源性葡萄糖浓度的准确性,本发明首先制备一系列不同浓度比例的d-葡萄糖和d-[u-13c]葡萄糖混合物标准样品,考察该发明方法定量动态范围、准确性和精确度。
分别称量90.6mg天然葡萄糖和95.4mgd-[u-13c]葡萄糖于5ml容量瓶中,加水定容,得到母液浓度分别为100.4mm和99.5mm。取20ul99.5mm的d-[u-13c]葡萄糖母液,加水稀释至2ml,得浓度为1mm的d-[u-13c]葡萄糖溶液。
分别用移液枪取20μl、40μl、70μl、100μl、140μl、170μl、200μl99.9mm天然葡萄糖母液于2ml的ep管,每个ep管中加入等量35μl1mmd-[u-13c]葡萄糖溶液,加适量的水和500μldmso-d6稀释至1ml,涡旋混匀、充分平衡,制备得到天然葡萄糖(浓度分别为2、4、7、10、14、17、20mm)与d-[u-13c]葡萄糖(0.035mm)不同浓度比例的混合标准溶液。依次取480ul标准溶液于1.5ml的ep管,加入20μldmso-d6,涡旋混匀,将混匀的溶液转移到5mm的核磁管,每支样在不同的时间重复测试三次。
使用topspin3.5软件对实验数据进行处理、积分,利用获得的积分数值根据浓度计算公式(1)计算得到天然葡萄糖与d-[u-13c]葡萄糖的摩尔浓度比值,并与理论的摩尔浓度比例进行比较(表1)。所有的样品测试相对标准偏差(relativestandarddeviation,rsd)均小于9%,相对误差(relativeerror,re)均小于3%,结果显示本发明方法具有良好的精确度和准确度(图2)。
表1id-hsqc方法测定标准样品的定量性能
a平均值±标准偏差,n=3
实施例2:
精确度:为了考察测定血浆中葡萄糖的精确度和准确度,取猴血浆样品,滴加0.035mm的[u-13c]葡萄糖,加入20μldmso-d6,涡旋混匀,将混匀后的样品转移到5mm的核磁管。三天内测试8次,相对标准偏差为4.02%。
回收率:
样品制备:四份相同的猴血浆样品,其中三份样品分别加入2mm,4mm,6mm(均为加入后的浓度)的d-葡萄糖,另一份不加d-葡萄糖作为对照(基质)。然后每份样品均加入20μldmso-d6,涡旋混匀,将混匀后的样品转移到5mm的核磁管。每支洋nmr测试三次。按公式(2)计算回收率(表2)。
式中cn,m(加入),cn,m(基质)为滴加d-葡萄糖之后和之前的测得的葡萄糖浓度,cn(滴加)为加入的葡萄糖浓度。
表2加样回收率实验结果
a平均值±标准偏差,n=3
实施例3:
测定健康猴和ii型糖尿病模型猴血浆样品(以d-[u-13c]葡萄糖作为外源性葡萄糖的示踪物的钳夹实验血浆样品)中内、外源性葡萄糖的浓度:
核磁样品制备步骤:
取480ul血浆于1.5ml的ep管,加入20μldmso-d6,涡旋混匀,将混匀后的样品转移到5mm的核磁管用于核磁测试。
液质联用验证实验样品处理和制备过程包括以下三个步骤:
(1)血浆样品沉淀蛋白处理:取100μl血浆,加入400μl乙腈,涡旋30s,在4℃下以12000×g离心10min,取上层清液,使用真空离心浓缩仪旋转干燥,再用100μl超纯水重新溶解。
(2)衍生化反应:取20μl以上经过沉淀蛋白处理的血样,加100μl混合衍生化试剂(配置过程:称取0.385g对氨基苯甲酸丁酯,0.625g氰基硼氢化钠于4ml甲醇),于80℃水浴锅中反应1h,取出,冷却至室温。
(3)纯化处理:用c18填料的固相萃取小柱纯化衍生化反应得到的混合样品,固相萃取小柱活化、平衡后,将样品转移至固相萃取小柱,用1ml乙腈-水(5:95,v/v)洗两次,再用1ml乙腈-水(30:70,v/v)洗脱,洗脱液收集于进样小瓶中,进行lc-ms/ms实验。
测试结果(表3)表明id-hsqc方法与lc-ms/ms方法结果一致,因此id-hsqc方法可以用于血浆样品的内、外源葡萄糖测定。
表3id-hsqc和lc-ms/ms定量健康猴(1~6)和ii型糖尿病模型猴(7~12)血浆样品中的内外源性葡萄糖(cendo/cexo)结果的比较
a血浆中葡萄糖的浓度范围为3~5.5mm(b)或10~15mm(c)
实施例4:
为了进一步评价id-hsqc在测定血浆样品的性能(准确度和精确度)。三份相同的患糖尿病猴血浆样品(无d-[u-13c]葡萄糖示踪物):其中两份分别滴加0.5mm、10mm(滴加后在血样中的终浓度,选择这两个浓度是为了使分别采用核磁共振和液质联用两种检测方法检测到的天然葡萄糖和标记葡萄糖的信号强度相当,以提高测量结果的准确度)的d-[u-13c]葡萄糖作为参照样品。另一份血浆样品中滴加0.035mm的d-[u-13c]葡萄糖(滴加后在血样中的终浓度)作为测试样品,用以考察本发明方法id-hsqc测试血浆样品的定量精确度和准确度。以实施例2的步骤,分别用id-hsqc和lc-ms/ms方法检测参照样品,两种检测方法获得结果的平均值看作血糖的“理论浓度”。取480ul测试样品置于1.5ml的ep管,加入20μldmso-d6,涡旋混匀,将混匀的溶液转移到5mm的核磁管用本发明方法id-hsqc进行测试(重复测试三次)。表4显示id-hsqc测量的相对误差(re)为2.1%,相对标准偏差(rsd)为5.2%。
表4id-hsqc方法针对真实血样的葡萄糖定量性能
- 还没有人留言评论。精彩留言会获得点赞!