血浆阿莫西林浓度的HPLC-MS/MS检测方法与流程
本发明涉及抗生素类药物的血药浓度监测技术领域,特别是涉及血浆阿莫西林浓度的hplc-ms/ms检测方法。
背景技术:
阿莫西林(amoxicillin),青霉素类、β-内酰胺类抗生素,杀菌作用强,穿透细胞壁的能力也强,是目前应用较为广泛的口服青霉素之一。临床应用阿莫西林的不良反应发生率约为5~6%,因反应而停药者约2%,具有安全范围小、体内代谢个体差异大、毒性较强等特点,且其疗效和不良反应与血浆中药物浓度密切相关,需要根据血药浓度调整给药方案,故有必要对其进行临床血药浓度监测。
药典中规定的阿莫西林含量测定方法为高效液相色谱法,具体实验方法如下:取装量差异项下的内容物,混合均匀,精密量取(约相当于阿莫西林0.125g),加流动相溶解并稀释成每1ml中约含0.5mg的溶液,滤过,取续滤液,精密量取20μl注入液相色谱仪,记录色谱图;另取阿莫西林对照品适量,同法测定。按外标法以峰面积计算出供试品中c16h19n3o5s的含量。
色谱条件与系统适用性试验:
用十八烷基硅烷键合硅胶为填充剂;以0.05mol/l磷酸二氢钾溶液(用2mol/l氢氧化钾溶液调节ph值至5.0)-乙腈(97.5∶2.5)为流动相;流速为每分钟约1ml;检测波长为254nm。理论板数按阿莫西林计算不低于2000。
上述药典中规定分析方法涉及大量的化学预处理步骤,操作相对繁琐,特别是磷酸缓冲液的配制和标定,耗时较长,给实际工作带来许多不便。
目前,阿莫西林血药浓度测定的常见方法有:高效液相色谱法和液相色谱-质谱联用法。由于阿莫西林极性较大且热稳定性差,不能通过液液萃取后挥干复溶来纯化浓集,早期检测采用繁琐的超滤方法处理,后期研究中的样本前处理则往往采用2-3倍量的甲醇或乙腈或高氯酸用以沉淀蛋白。但沉淀蛋白无法完全纯化样本,而且采用lc-ms检测时的基质效应会产生干扰;加入沉淀剂离心后取上清液进行检测往往会因为稀释倍数过大而灵敏度不够,为保证定量灵敏度,导致进样体积需要20μl以上,上清液与流动相的不匹配造成的溶剂效应往往会对色谱峰形产生较大干扰,需要在上样时加入一定比例的特定溶剂来消除溶剂效应。这些问题使得阿莫西林的检测仍然存在问题,导致在lc-ms普及的今天仍然有研究者采用hplc来进行检测。
阿莫西林微溶于水,在乙醇中几乎不溶。游离态分子式与分子量为c16h19n3o5s/365.40g/mol,水合物分子式与分子量为c16h19n3o5s·3h2o/419.45g/mol,具体结构如式(i)所示。其结构特点有:稠环张力导致该类化合物不稳定,内酰胺环易开环分解。
本发明方法所选用内标为维拉帕米(verapamil),为罂粟碱类衍生物,常用其盐酸盐;可溶于水,在甲醇、乙醇或氯仿中易溶。游离态分子式与分子量为c27h38n2o4/454.60g/mol,盐酸盐分子式与分子量为c27h38n2o4·hcl/491.07g/mol,具体结构如式(ii)所示。
技术实现要素:
基于此,本发明提供一种血浆阿莫西林浓度的hplc-ms/ms检测方法。该方法准确、快速、特异性强,具有较高的分离度。
一种血浆阿莫西林浓度的hplc-ms/ms检测方法,包括以下步骤:
(a)储备液的制备:
a1:取阿莫西林溶解于(50±5)%乙腈中,制得阿莫西林储备溶液;
a2:取维拉帕米溶解于乙腈中,制得维拉帕米储备溶液;
(b)工作溶液的制备:
b1:用(50±5)%乙腈稀释阿莫西林储备溶液,制得混合标准曲线样本工作溶液和混合质控样本工作溶液;
b2:用(50±5)%乙腈稀释维拉帕米储备溶液,制得混合标准曲线样本工作溶液和混合质控样本工作溶液;
(c)标准曲线样本和质控样本的制备:
向空白血浆中加入混合标准曲线工作溶液混合均匀,制备阿莫西林标准曲线样本和阿莫西林质控样本;
(d)样本前处理:取血浆样本,加入维拉帕米储备溶液,混匀;加入乙腈,混匀;离心,取上清液;加入甲酸水溶液,混匀,得到待测样品溶液;
(e)液相色谱分离:将待测样品溶液进行液相色谱分离;
(f)进行质谱分析:将液相色谱分离后的样品进行质谱检测。
与现有技术相比,本发明具有以下有益效果:
本发明取待测血浆样本加入内标工作液,再用乙腈沉淀蛋白后,离心后取上清,再加入稀释液,之后只需要极少的进样量进行分析就可以满足定量要求,样本预处理过程被大大简化。色谱检测过程中避免了溶剂效应的影响,色谱峰形极佳。本发明的血浆中阿西莫林浓度的检测方法操作简单、分析快速、特异性高、分离度高。
附图说明
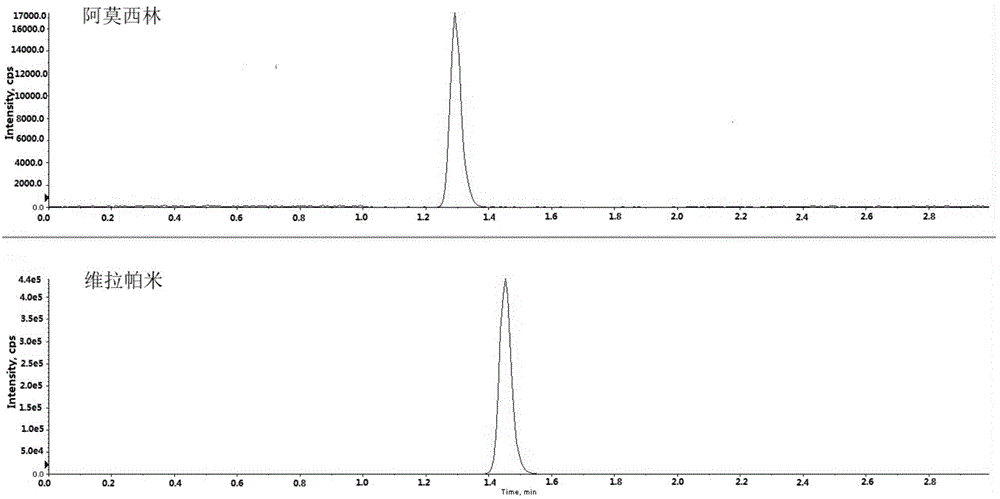
图1为阿莫西林标准品和维拉帕米标准品的检测结果图。
具体实施方式
为了便于理解本发明,下面将参照实施例对本发明进行更全面的描述,以下给出了本发明的较佳实施例。但是,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施例。提供这些实施例的目的是使对本发明的公开内容的理解更加透彻全面。
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。本文所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。
本发明提供一种血浆阿莫西林浓度的hplc-ms/ms检测方法,包括以下步骤:
(a)储备液的制备:
a1:取阿莫西林溶解于(50±5)%乙腈中,制得阿莫西林储备溶液;
a2:取维拉帕米溶解于乙腈中,制得维拉帕米储备溶液;
(b)工作溶液的制备:
b1:用(50±5)%乙腈稀释阿莫西林储备溶液,制得混合标准曲线样本工作溶液和混合质控样本工作溶液;
b2:用(50±5)%乙腈稀释维拉帕米储备溶液,制得混合标准曲线样本工作溶液和混合质控样本工作溶液;
(c)标准曲线样本和质控样本的制备:
向空白血浆中加入混合标准曲线工作溶液混合均匀,制备阿莫西林标准曲线样本和阿莫西林质控样本;
(d)样本前处理:取血浆样本,加入维拉帕米储备溶液,混匀;加入乙腈,混匀;离心,取上清液;加入甲酸水溶液,混匀,得到待测样品溶液;
(e)液相色谱分离:将待测样品溶液进行液相色谱分离;
(f)进行质谱分析:将液相色谱分离后的样品进行质谱检测。
在其中一个实施例中,步骤(d)中,所述乙腈与血浆样本的体积比为:2-5:1,优选比为4-5:1;所述甲酸水溶液的浓度为(0.1±0.02)%。在样品预处理过程中,沉淀剂的量远大于血浆量,进样溶液体系与初始流动相比例接近,且进样量十分低,完全可以忽略溶剂效应的影响,使得分离效果极佳。
在其中一个实施例中,步骤(d)中,所述离心的温度为2-8℃,所述离心的转速为2500-3500rpm,所述离心时间为5min-15min。
在其中一个实施例中,步骤(e)中,所述液相色谱分离条件为:
流动相:流动相a为0.1%甲酸水溶液;流动相b为乙腈;采用梯度洗脱;所述梯度洗脱过程为:0~1.3分钟,(50±5)%流动相a-流动相b;1.3~1.5分钟,(50±5)%流动相a-流动相b;1.5~2.3分钟,(5±2)%流动相a-流动相b;2.3~2.4分钟,(5±2)%流动相a-%流动相b;2.4~3分钟,(50±5)%流动相a-流动相b;流速0.4ml/min-0.8ml/min;进样体积为2μl.00-4.00μl;柱温设置为25-35℃;自动进样器温度为2-6℃;洗针液:(50±5)%乙腈。洗冲速度:30-40μl/sec;洗针液体积:400-600μl。
在其中一个实施例中,步骤(e)中,所述梯度洗脱过程为:0~1.3分钟,50%流动相a-流动相b;1.3~1.5分钟,50%流动相a-流动相b;1.5~2.3分钟,5%流动相a-流动相b;2.3~2.4分钟,5%流动相a-流动相b;2.4~3分钟,50%流动相a-流动相b;流速0.6ml/min;进样体积为3.00μl;柱温设置为30℃;自动进样器温度为4℃;洗针液:50%乙腈;洗冲速度:35μl/sec;洗针液体积:500μl。
在其中一个实施例中,步骤(f)中,所述质谱分析条件为:
质谱检测条件:离子化模式:电喷雾离子源;正离子模式;多反应监测;
离子源参数:气帘气:25psi;离子源气体1:50psi;离子源气体2:50psi;离子源喷雾电压:5500v;离子源温度:550℃;分辨率q1/q3:unit/unit;碰撞气:medium;暂停时间:20msec;质谱采集时间为3.00min;
监测离子对四极杆参数:阿莫西林:离子对:366.2→208.1;去簇电压:30.0v;入口电压:10.00v;出口电压:25.00v;碰撞能量:14.00ev;停留时间:200.0msec;维拉帕米:离子对:455.2→165.1;去簇电压:30.0v;入口电压:10.00v;出口电压:25.00v;碰撞能量:36.00ev;停留时间:200.0msec。
在其中一个实施例中,步骤b1中,所述混合标准曲线样本工作溶液中,阿莫西林的浓度分别为:300ng/ml、600ng/ml、2000ng/ml、10000ng/ml、50000ng/ml、100000ng/ml、250000ng/ml和300000ng/ml;和/或
步骤b2中,所述混合质控样本工作溶液中,阿莫西林的浓度分别为:定量下限质控300ng/ml、低浓度质控800ng/ml、几何平均值中浓度质控15000ng/ml、算术平均值中浓度质控150000ng/ml、高浓度质控225000ng/ml。
在其中一个实施例中,步骤(c)中,所述标准曲线样本中,阿莫西林的浓度分别为:15.0ng/ml、30.0ng/ml、100ng/ml、500ng/ml、2500ng/ml、5000ng/ml、12500ng/ml和15000ng/ml;和/或
所述质控样本中,阿莫西林的浓度分别为:定量下限质控15ng/ml、低浓度质控40.0ng/ml、几何平均值中浓度质控750ng/ml、算术平均值中浓度质控7500ng/ml、高浓度质控11250ng/ml。
在其中一个实施例中,步骤(e)中,所采用的液相色谱质谱联用仪的型号为shimadzulc30ad液相色谱联合sciexqtrap5500质谱仪,所采用的操作系统为analyst1.6.3;所采用的色谱柱为nacalai的cosmosil5c18-paq;其规格为4.6×100mm,5.0μm;本发明使用的sciexqtrap5500型质谱仪,其灵敏度较以前的仪器有了数量级的提升。
在其中一个实施例中,步骤(d)中,所述样本前处理为:取40.0μl血浆样本,加入40.0μl内标工作溶液,涡旋混匀1min,再加入520μl的乙腈,于室温下振摇混匀10min,之后于4℃、3000rpm下离心10min;取100μl上清液,加入200μl0.1%的甲酸水溶液,振摇混匀3min,得到待测样品溶液。
以下结合具体实施例对本发明作进一步详细的说明。
实施例1
(1)溶液的配制:
储备液的制备:取阿莫西林标准品(羟氨苄青霉素三水合物),溶解于50%乙腈配制浓度为1.00mg/ml的阿莫西林储备溶液;
取适量的维拉帕米标准品(盐酸维拉帕米),溶解100%乙腈中,制得浓度为1.00mg/ml的维拉帕米储备溶液;
用50%乙腈稀释上述阿莫西林储备溶液制得混合标准曲线样本工作溶液:300ng/ml、600ng/ml、2000ng/ml、10000ng/ml、50000ng/ml、100000ng/ml、250000ng/ml和300000ng/ml浓度的阿莫西林溶液;
用50%乙腈稀释上述阿莫西林储备溶液制得混合质控样本工作溶液:分别为含有300ng/ml(定量下限质控)、800ng/ml(低浓度质控)、15000ng/ml(几何平均值中浓度质控)、150000ng/ml(算术平均值中浓度质控)、225000ng/ml(高浓度质控)浓度的阿莫西林溶液。
用50%乙腈稀释上述维拉帕米储备溶液制得内标工作溶液,内标工作溶液浓度为:50.0ng/ml。
向380μl的空白血浆中加入20.0μl混合标准曲线工作溶液,混合均匀。得到八种不同浓度的标准曲线样本分别为含有15.0ng/ml、30.0ng/ml、100ng/ml、500ng/ml、2500ng/ml、5000ng/ml、12500ng/ml和15000ng/ml浓度的阿莫西林溶液。
向380μl的空白血浆中加入20.0μl混合标准曲线工作溶液,混合均匀。得到五种不同浓度的质控样本,分别为含有15ng/ml(定量下限质控)、40.0ng/ml(低浓度质控)、750ng/ml(几何平均值中浓度质控)、7500ng/ml(算术平均值中浓度质控)、11250ng/ml(高浓度质控)浓度的阿莫西林溶液。
(2)样本前处理
取40.0μl人血浆低浓度样本,加入40.0μl内标工作溶液,涡旋混匀1min,再加入520μl的乙腈,于室温下振摇混匀10min,之后于4℃、3000rpm下离心10min。取100μl上清液,加入200μl0.1%的甲酸水溶液,振摇混匀3min,待进样分析。
(3)液相色谱条件
仪器设备:shimadzulc-30ad液相色谱系统。
色谱柱:cosmosil5c18-paq(4.6×100mm,5.0μm),nacalai,柱温设置为30℃,自动进样器温度设置为4℃。
流动相a为0.1%甲酸水溶液;流动相b为100%乙腈。总流速为0.60ml/min。
流动相洗脱程序为:0至1.3分钟,流动相a为50%体积份,流动相b为50%体积份;大于1.3分钟至1.5分钟,流动相a为50%体积份,流动相b为50%体积份;大于1.5分钟至2.3分钟,流动相a为5%体积份,流动相b为95%体积份;大于2.3分钟至2.4分钟,流动相a为5%体积份,流动相b为95%体积份;大于2.4分钟至3分钟,流动相a为50%体积份,流动相b为50%体积份。
质谱切换阀程序为:0至1分钟,b阀(进入废液);1至2分钟,a阀(进入质谱);2至3分钟,b阀(进入废液)。
洗针液为50%乙腈。洗针模式为外部冲洗;冲洗速度:35μl/sec;冲洗端口液体:r1;冲洗液体积:500μl;冲洗模式:进针前后冲洗;冲洗浸润时间:0秒;冲洗方法:仅端口冲洗;冲洗时间:2秒;
进样体积为3.00μl,阿莫西林保留时间约为1.29min;维拉帕米保留时间约为1.47min。
(5)质谱条件
仪器设备:sciexqtrap5500质谱系统。
离子化模式:电喷雾离子源(esi);正离子模式(positive);多反应监测(mrm)。
离子源参数:气帘气(cur):25psi;离子源气体1(gas1):50psi;离子源气体2(gas2):50psi;离子源喷雾电压(is):5500v;离子源温度(tem):550℃;分辨率q1/q3(resolutionq1/q3):unit/unit;碰撞气(cad):medium;暂停时间(mrpause):20msec;质谱采集时间为3.00min。
监测离子对四极杆参数:
阿莫西林:离子对:366.2→208.1;去簇电压(dp):30.0v;入口电压(ep):10.00v;出口电压(cxp):25.00v;碰撞能量(ce):14.00ev;停留时间(dwell):200.0msec。
维拉帕米:离子对:455.2→165.1;去簇电压(dp):30.0v;入口电压(ep):10.00v;出口电压(cxp):25.00v;碰撞能量(ce):36.00ev;停留时间(dwell):200.0msec。
在此条件下,测得人血浆中低浓度阿莫西林的浓度为15.0ng/ml。阿莫西林标准品和维拉帕米标准品的检测结果如图1所示。
实施例2
(1)溶液的配制过程与实施例1一致。
(2)样本前处理
取40.0μlbeagle犬血浆中浓度样本,加入40.0μl内标工作溶液,涡旋混匀1min,再加入320μl的乙腈,于室温下振摇混匀10min,之后于4℃、3000rpm下离心10min。取100μl上清液,加入200μl0.1%的甲酸水溶液,振摇混匀3min,待进样分析。
(3)液相色谱条件
仪器设备:shimadzulc-30ad液相色谱系统。
色谱柱:cosmosil5c18-paq(4.6×100mm,5.0μm),nacalai,柱温设置为30℃,自动进样器温度设置为4℃。
流动相a为0.1%甲酸水溶液;流动相b为100%乙腈。总流速为0.60ml/min。
流动相洗脱程序为:0至1.3分钟,流动相a为50%体积份,流动相b为50%体积份;大于1.3分钟至1.5分钟,流动相a为50%体积份,流动相b为50%体积份;大于1.5分钟至2.3分钟,流动相a为5%体积份,流动相b为95%体积份;大于2.3分钟至2.4分钟,流动相a为5%体积份,流动相b为95%体积份;大于2.4分钟至3分钟,流动相a为50%体积份,流动相b为50%体积份。
质谱切换阀程序为:0至1分钟,b阀(进入废液);1至2分钟,a阀(进入质谱);2至3分钟,b阀(进入废液)。
洗针液为50%乙腈。洗针模式为外部冲洗;冲洗速度:35μl/sec;冲洗端口液体:r1;冲洗液体积:500μl;冲洗模式:进针前后冲洗;冲洗浸润时间:0秒;冲洗方法:仅端口冲洗;冲洗时间:2秒;
进样体积为3.00μl,阿莫西林保留时间约为1.29min;维拉帕米保留时间约为1.47min。
(4)质谱条件
仪器设备:sciexqtrap5500质谱系统。
离子化模式:电喷雾离子源(esi);正离子模式(positive);多反应监测(mrm)。
离子源参数:气帘气(cur):25psi;离子源气体1(gas1):50psi;离子源气体2(gas2):50psi;离子源喷雾电压(is):5500v;离子源温度(tem):550℃;分辨率q1/q3(resolutionq1/q3):unit/unit;碰撞气(cad):medium;暂停时间(mrpause):20msec;质谱采集时间为3.00min。
监测离子对四极杆参数:
阿莫西林:离子对:366.2→208.1;去簇电压(dp):30.0v;入口电压(ep):10.00v;出口电压(cxp):25.00v;碰撞能量(ce):14.00ev;停留时间(dwell):200.0msec。
维拉帕米:离子对:455.2→165.1;去簇电压(dp):30.0v;入口电压(ep):10.00v;出口电压(cxp):25.00v;碰撞能量(ce):36.00ev;停留时间(dwell):200.0msec。
在此条件下,可测得beagle犬血浆中中浓度阿莫西林的浓度为11250ng/ml。
实施例3
(1)溶液的配制过程与实施例一致。
(2)样本前处理
取40.0μl人血浆低浓度样本,加入40.0μl内标工作溶液,涡旋混匀1min,再加入520μl的乙腈,于室温下振摇混匀10min,之后于4℃、3000rpm下离心10min。取100μl上清液,加入200μl0.1%的甲酸水溶液,振摇混匀3min,待进样分析。
(3)液相色谱条件
仪器设备:shimadzulc-30ad液相色谱系统。
色谱柱:cosmosil5c18-paq(4.6×100mm,5.0μm),nacalai,柱温设置为30℃,自动进样器温度设置为4℃。
流动相a为0.1%甲酸水溶液;流动相b为100%乙腈。总流速为0.60ml/min。
流动相洗脱程序为:0至1.3分钟,流动相a为50%体积份,流动相b为50%体积份;大于1.3分钟至1.5分钟,流动相a为50%体积份,流动相b为50%体积份;大于1.5分钟至2.3分钟,流动相a为5%体积份,流动相b为95%体积份;大于2.3分钟至2.4分钟,流动相a为5%体积份,流动相b为95%体积份;大于2.4分钟至3分钟,流动相a为50%体积份,流动相b为50%体积份。
质谱切换阀程序为:0至1分钟,b阀(进入废液);1至2分钟,a阀(进入质谱);2至3分钟,b阀(进入废液)。
洗针模式为外部冲洗;冲洗速度:35μl/sec;冲洗端口液体:r1;冲洗液体积:500μl;冲洗模式:进针前后冲洗;冲洗浸润时间:0秒;冲洗方法:仅端口冲洗;冲洗时间:2秒;
进样体积为5.00μl,阿莫西林保留时间约为1.29min;维拉帕米保留时间约为1.47min。
(4)质谱条件
仪器设备:sciexqtrap5500质谱系统。
离子化模式:电喷雾离子源(esi);正离子模式(positive);多反应监测(mrm)。
离子源参数:气帘气(cur):25psi;离子源气体1(gas1):50psi;离子源气体2(gas2):50psi;离子源喷雾电压(is):5500v;离子源温度(tem):550℃;分辨率q1/q3(resolutionq1/q3):unit/unit;碰撞气(cad):medium;暂停时间(mrpause):20msec;质谱采集时间为3.00min。
监测离子对四极杆参数:
阿莫西林:离子对:366.2→208.1;去簇电压(dp):30.0v;入口电压(ep):10.00v;出口电压(cxp):25.00v;碰撞能量(ce):14.00ev;停留时间(dwell):200.0msec。
维拉帕米:离子对:455.2→165.1;去簇电压(dp):30.0v;入口电压(ep):10.00v;出口电压(cxp):25.00v;碰撞能量(ce):36.00ev;停留时间(dwell):200.0msec。
在此条件下,可测得人血浆中高浓度阿莫西林的浓度为25000ng/ml。
实施例4
(1)溶液的配制过程与实施例一致。
(2)样本前处理
取40.0μl人血浆各标准曲线浓度样本,加入40.0μl内标工作溶液,涡旋混匀1min,再加入520μl的乙腈,于室温下振摇混匀10min,之后于4℃、3000rpm下离心10min。取100μl上清液,加入200μl0.1%的甲酸水溶液,振摇混匀3min,待进样分析。
(3)液相色谱条件
仪器设备:shimadzulc-30ad液相色谱系统。
色谱柱:cosmosil5c18-paq(4.6×100mm,5.0μm),nacalai,柱温设置为30℃,自动进样器温度设置为4℃。
流动相a为0.1%甲酸水溶液;流动相b为100%乙腈。总流速为0.60ml/min。
流动相洗脱程序为:0至1.3分钟,流动相a为50%体积份,流动相b为50%体积份;大于1.3分钟至1.5分钟,流动相a为50%体积份,流动相b为50%体积份;大于1.5分钟至2.3分钟,流动相a为5%体积份,流动相b为95%体积份;大于2.3分钟至2.4分钟,流动相a为5%体积份,流动相b为95%体积份;大于2.4分钟至3分钟,流动相a为50%体积份,流动相b为50%体积份。
质谱切换阀程序为:0至1分钟,b阀(进入废液);1至2分钟,a阀(进入质谱);2至3分钟,b阀(进入废液)。
洗针模式为外部冲洗;冲洗速度:35μl/sec;冲洗端口液体:r1;冲洗液体积:500μl;冲洗模式:进针前后冲洗;冲洗浸润时间:0秒;冲洗方法:仅端口冲洗;冲洗时间:2秒;
进样体积为3.00μl,阿莫西林保留时间约为1.29min;维拉帕米保留时间约为1.47min。
(4)质谱条件
仪器设备:sciexqtrap5500质谱系统。
离子化模式:电喷雾离子源(esi);正离子模式(positive);多反应监测(mrm)。
离子源参数:气帘气(cur):25psi;离子源气体1(gas1):50psi;离子源气体2(gas2):50psi;离子源喷雾电压(is):5500v;离子源温度(tem):550℃;分辨率q1/q3(resolutionq1/q3):unit/unit;碰撞气(cad):medium;暂停时间(mrpause):20msec;质谱采集时间为3.00min。
监测离子对四极杆参数:
阿莫西林:离子对:366.2→208.1;去簇电压(dp):30.0v;入口电压(ep):10.00v;出口电压(cxp):25.00v;碰撞能量(ce):14.00ev;停留时间(dwell):200.0msec。
维拉帕米:离子对:455.2→165.1;去簇电压(dp):30.0v;入口电压(ep):10.00v;出口电压(cxp):25.00v;碰撞能量(ce):36.00ev;停留时间(dwell):200.0msec。
在此条件下,可测得人血浆中阿莫西峰面积与浓度的关系为:y=0.0002346+0.0006688x,r2=0.9970,最低检测限为10ng/ml,定量下限为15ng/ml。
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!