一种获取导致皮肤瘢痕疙瘩治疗靶点的方法与流程
本发明涉及生物医学工程和蛋白质组学领域,具体为诊断皮肤瘢痕疙瘩生物标志物组合,以及新的治疗皮肤瘢痕疙瘩的潜在靶点。
背景技术:
皮肤由表皮和真皮组成,是人体最大的器官,在保护身体免受外界干扰方面起着重要作用。皮肤损伤后,伤口愈合过程迅速开始,包括炎症、增殖和重塑。虽然伤口愈合的理想结果是无瘢痕愈合,颜色和质地与正常皮肤相似,但最好的结果通常是扁平、柔韧的瘢痕,轻微变色。然而,伤口愈合异常会导致病理性瘢痕,如增生性瘢痕和瘢痕疙瘩(1、tredget,e.e.,levi,b.,anddonelan,m.b.(2014)biologyandprinciplesofscarmanagementandburnreconstruction.surgclinnortham94,793-815;2、xue,m.,andjackson,c.j.(2015)extracellularmatrixreorganizationduringwoundhealinganditsimpactonabnormalscarring.advwoundcare(newrochelle)4,119-136)。尽管近几十年来在伤口护理、康复和管理方面取得了进展,但病理性瘢痕仍然很难用外科方法和药物治愈(vanderveer,w.m.,bloemen,m.c.,ulrich,m.m.,molema,g.,vanzuijlen,p.p.,middelkoop,e.,andniessen,f.b.(2009)potentialcellularandmolecularcausesofhypertrophicscarformation.burns35,15-29)。
瘢痕疙瘩是一种纤维增生性肿瘤,与细胞外基质(ecm)成分过度积聚有关,尤其是真皮和皮下组织中的胶原沉积,对皮肤损伤起反应(andrews,j.p.,marttala,j.,macarak,e.,rosenbloom,j.,anduitto,j.(2016)keloids:theparadigmofskinfibrosis-pathomechanismsandtreatment.matrixbiol51,37-46。瘢痕疙瘩最常见的部位是前胸、肩部、上背部和耳垂。瘢痕演变成瘢痕疙瘩伴随着瘙痒、疼痛、毁容和关节挛缩,很少消退。特别是,瘢痕疙瘩的缺陷可能与严重的功能和心理负担有关。虽然已经描述了几种病理病因,但瘢痕疙瘩形成的机制仍不清楚。
ecm是由数百种蛋白质组成的复合体,它构成了所有多细胞生物的支架,并提供了一种生物活性结构,通过化学和机械信号从根本上控制细胞的行为。人们普遍认为ecm降解和沉积之间的不平衡在病理过程中对瘢痕形成起着重要作用(sidgwick,g.p.,andbayat,a.(2012)extracellularmatrixmoleculesimplicatedinhypertrophicandkeloidscarring.jeuracaddermatolvenereol26,141-152)。例如,病理性瘢痕中胶原、纤维连接蛋白和层粘连蛋白的表达显著增加,而透明质酸和decorin则下调。转化生长因子-β(tgf-β)和纤维连接蛋白外区a(fn-eda)被证实参与瘢痕疙瘩形成过程中的胶原沉积。然而,人们对ecm在病理性瘢痕形成中的具体作用的了解非常有限,导致人们不了解瘢痕疙瘩的形成机制,阻碍新的诊断和治疗方法的建立。
技术实现要素:
本发明的目的是提出一种获取导致皮肤瘢痕疙瘩治疗靶点的方法,通过揭示瘢痕疙瘩形成的病理机制,鉴定诊断标志物,找出作为导致皮肤瘢痕疙瘩的激素受体,以之作为治疗靶点。
为了实现上述目的,本发明采用下述技术方案:
一种获取导致皮肤瘢痕疙瘩治疗靶点的方法,包括以下步骤:
1)利用脱细胞方法获得人瘢痕疙瘩的皮肤基质支架;
2)提取皮肤基质支架的蛋白质,利用串联质谱鉴定皮肤瘢痕疙瘩皮肤的基质蛋白成份;
3)比较瘢痕疙瘩与正常皮肤的基质蛋白成份,筛选瘢痕疙瘩诊断标志物即用于辅助诊断瘢痕疙瘩的早期形成的基质蛋白;
4)对用于辅助诊断瘢痕疙瘩的早期形成的基质蛋白进行免疫荧光染色,从瘢痕疙瘩形成的潜在机制中确认瘢痕疙瘩形成的具体机制;
5)根据上述确认的瘢痕疙瘩形成的具体机制,筛选作为瘢痕疙瘩潜在的治疗靶点的激素受体,并通过病理染色和动物实验验证,找出作为导致皮肤瘢痕疙瘩的治疗靶点的激素受体。
进一步地,步骤1)中的脱细胞方法为:用电动皮肤采集器切割采集皮肤组织,皮肤组织去除表皮;将去细胞真皮样品清洗,然后利用酶进行脱细胞。
进一步地,步骤1)中脱细胞后,通过定量胶原的数量来测试生物支架的完整性,并使用胶原检测试剂盒定量胶原蛋白含量,具体地通过测定胶原蛋白的吸光度来测量其浓度;然后用硫酸化糖胺聚糖法测定gag含量,通过测定指示剂的吸光度来测量其浓度;当上述测量的浓度达到一预设标准时,则认定获得的基质支架具备完整性。
进一步地,步骤2)中提取皮肤基质支架的蛋白质的方法为:将脱细胞后的皮肤基质支架匀浆,用蛋白提取试剂(sigma-aldrich)提取蛋白质。
进一步地,步骤2)中提取蛋白质以后,离心30分钟后,将上清液转移到干净的试管中并在-80℃下储存。
进一步地,步骤2)中提取皮肤基质支架的蛋白时,裂解蛋白,提取肽段,并将肽段混合物使用配备有简易nlc纳米流液相色谱系统(thermofisherscientific)的orbitrapq-exactive质谱仪(thermofisherscientific)进行分析。
进一步地,步骤3)中利用matrisome数据库对质谱鉴定瘢痕疙瘩的基质蛋白进行比对,获得瘢痕疙瘩脱细胞支架的基质蛋白成分;然后与正常皮肤相比,找出用于辅助诊断瘢痕疙瘩的早期形成的基质蛋白。
进一步地,用于辅助诊断瘢痕疙瘩的早期形成的基质蛋白包括col11a1、col26a1、col2a1、cilp、creld1、fndc1、crispld2、edil3、spon2、mmrn1、igfbp7、cilp2、ltbp2、tnfaip6、sparcl1、tnn、slit1、acan、hapln1、p4ha2、serpinb4、mmp12、ctsk、elane、timp1、plod2、serpinb13、serpinb3、mmp14、ctsa、serpine2、adam12、ctss、loxl2、bmp1、gpc6、colec12、s100a12、sfrp2、wnt4、wnt3、tchh、fgf2、sfrp4、sfrp1、fstl1、tgfb1、mst1、cthrc1、thbs4、srpx2、thbs2、tnc、sparc、comp、fbln7、plod1、p4ha1、htra1、c1qtnf5、clec11a、s100a8、s100a9、angptl2、cxcl14。
进一步地,步骤4)中瘢痕疙瘩形成的潜在机制包括:瘢痕的皮肤微环境止血、炎症、血管生成、ecm重塑、酶活性、细胞粘附、皮肤发育、细胞骨架发育和碳水化合物等的一种或几种为生物学过程失调因素,炎性蛋白、促血管生成的蛋白、酶和纤维化相关的蛋白中的一种或几种为瘢痕疙瘩的基质蛋白,以及弹性蛋白、酶抑制剂和基底膜成分的一种或几种为导致瘢痕疙瘩丧失抗血管生成的成分。
进一步地,步骤4)中对潜在导致瘢痕形成的代表性蛋白sparc、htra1、clec11a、s100a9、mfap4和ogn进行免疫荧光染色。
进一步地,步骤5)作为瘢痕疙瘩潜在的治疗靶点的激素受体包括催乳素受体、促性腺激素释放激素受体、催产素受体、甲状腺素受体、胰岛素受体、雌激素受体中的一种或几种。
本发明具有以下优点:
1本发明首次阐明了皮肤瘢痕疙瘩的病理形成机制,揭示瘢痕疙瘩微环境失调的生物学过程,以及ecm在皮肤瘢痕疙瘩形成中的具体作用。
2.本发明提出了65个瘢痕疙瘩临床诊断的生物标志物,为瘢痕疙瘩的早期预防提供诊断方法。
3.本发明发现的瘢痕疙瘩治疗的潜在靶点,以不同激素受体作为治疗靶点,可利用相应激素受体抑制剂治疗瘢痕疙瘩,为瘢痕疙瘩的治疗提供了新方向。
附图说明
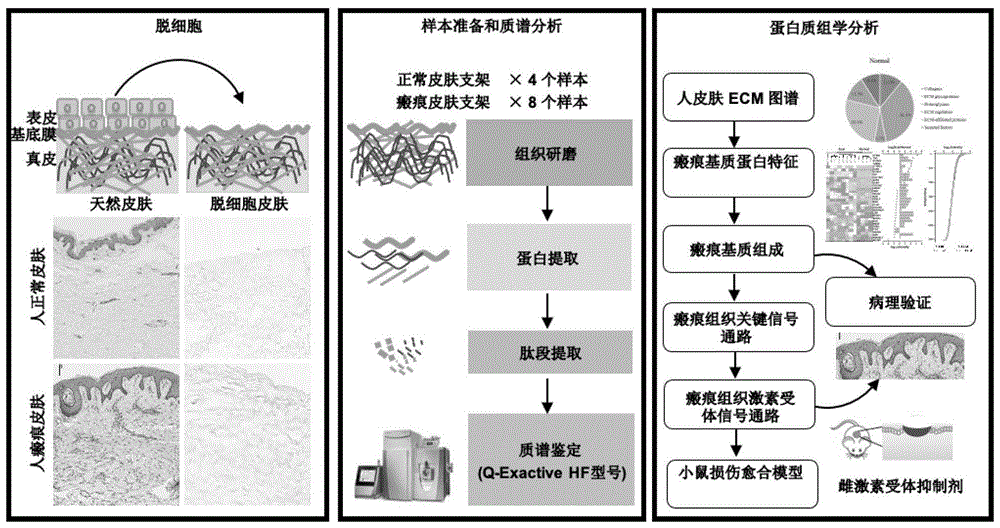
图1是实例的一种获取导致皮肤瘢痕疙瘩治疗靶点的流程图。
图2是皮肤瘢痕疙瘩生物标志物代表性蛋白示例图。
图3是皮肤瘢痕疙瘩治疗靶点激素受体的示例图。
具体实施方式
为使本发明的技术方案能更明显易懂,特举实施例并结合附图详细说明如下。
本实施例公开一种获取导致皮肤瘢痕疙瘩治疗靶点的方法,包括以下步骤:
1)利用脱细胞方法获得人瘢痕疙瘩的皮肤基质支架;脱细胞方法为:用电动皮肤采集器切割采集皮肤组织,皮肤组织去除表皮;将去细胞真皮样品清洗,然后利用酶进行脱细胞。脱细胞后,通过定量胶原的数量来测试生物支架的完整性,并使用胶原检测试剂盒定量胶原蛋白含量,具体地通过测定胶原蛋白的吸光度来测量其浓度;然后用硫酸化糖胺聚糖法测定gag含量,通过测定指示剂的吸光度来测量其浓度;当上述测量的浓度达到一预设标准时,则认定获得的基质支架具备完整性。
2)将脱细胞后的皮肤基质支架匀浆,用蛋白提取试剂(sigma-aldrich)提取皮肤基质支架的蛋白质,提取皮肤基质支架的蛋白时,裂解蛋白,提取肽段,并将肽段混合物使用配备有简易nlc纳米流液相色谱系统(thermofisherscientific)的orbitrapq-exactive质谱仪(thermofisherscientific)进行分析。利用串联质谱鉴定皮肤瘢痕疙瘩皮肤的基质蛋白成份;提取的蛋白质可在离心30分钟后,将上清液转移到干净的试管中并在-80℃下储存,以备下次使用。
3)瘢痕疙瘩与正常皮肤比较基质蛋白成份,筛选瘢痕疙瘩诊断标志物即用于辅助诊断瘢痕疙瘩的早期形成的基质蛋白,具体地,利用matrisome数据库对质谱鉴定瘢痕疙瘩的基质蛋白进行比对,获得瘢痕疙瘩脱细胞支架的基质蛋白成分;然后与正常皮肤相比,找出用于辅助诊断瘢痕疙瘩的早期形成的基质蛋白;这些基质蛋白包括col11a1、col26a1、col2a1、cilp、creld1、fndc1、crispld2、edil3、spon2、mmrn1、igfbp7、cilp2、ltbp2、tnfaip6、sparcl1、tnn、slit1、acan、hapln1、p4ha2、serpinb4、mmp12、ctsk、elane、timp1、plod2、serpinb13、serpinb3、mmp14、ctsa、serpine2、adam12、ctss、loxl2、bmp1、gpc6、colec12、s100a12、sfrp2、wnt4、wnt3、tchh、fgf2、sfrp4、sfrp1、fstl1、tgfb1、mst1、cthrc1、thbs4、srpx2、thbs2、tnc、sparc、comp、fbln7、plod1、p4ha1、htra1、c1qtnf5、clec11a、s100a8、s100a9、angptl2、cxcl14。
4)对用于辅助诊断瘢痕疙瘩的早期形成的基质蛋白进行免疫荧光染色,优选地,对潜在导致瘢痕形成的代表性蛋白sparc、htra1、clec11a、s100a9、mfap4和ogn进行免疫荧光染色。从瘢痕疙瘩形成的潜在基质中确认瘢痕疙瘩形成的具体机制,该潜在机制包括瘢痕的皮肤微环境止血、炎症、血管生成、ecm重塑、酶活性、细胞粘附、皮肤发育、细胞骨架发育和碳水化合物等的一种或几种为生物学过程失调因素,炎性蛋白、促血管生成的蛋白、酶和纤维化相关的蛋白中的一种或几种为瘢痕疙瘩的基质蛋白,以及弹性蛋白、酶抑制剂和基底膜成分的一种或几种为导致瘢痕疙瘩丧失抗血管生成的成分。
5)根据上述确认的瘢痕疙瘩形成的具体机制,筛选作为瘢痕疙瘩潜在的治疗靶点的激素受体,该激素受体包括催乳素受体、促性腺激素释放激素受体、催产素受体、甲状腺素受体、胰岛素受体、雌激素受体中的一种或几种,然后并通过病理染色和动物实验验证,找出作为导致皮肤瘢痕疙瘩的治疗靶点的激素受体。
以下列举一具体实例:
本实例利用本发明方法找出瘢痕疙瘩的治疗靶点,过程如图1所示,具体为:对瘢痕疙瘩皮肤和健康皮肤进行脱细胞处理,获得细胞外基质支架。通过对两组支架进行基质组学鉴定,获得二者蛋白表达的差异成份。利用生物信息学工具和数据库(davidbioinformaticsresources6.8)对这些差异成分进行功能分析和相互作用网络分析,发现在瘢痕疙瘩中上调和下调的蛋白,例如上调蛋白sparc和下调蛋白mfap4,这些蛋白可能是形成瘢痕疙瘩的原因。发现雌激素受体通路为瘢痕形成机制的关键通路,因此,通过抑制剂抑制雌激素受体erα或erβ可能对瘢痕疙瘩有治疗作用。
图2是皮肤瘢痕疙瘩生物标志物代表性蛋白示例图,图中显示的是皮肤瘢痕疙瘩相对正常皮肤中高表达基质蛋白(sparc、htra1、clec11a、s100a9)和低表达基质蛋白(mfap4、ogn、ambp)的情况。图3是皮肤瘢痕疙瘩治疗靶点激素受体的示例图,图中显示的是雌激素核受体erα和erβ在真皮组织中细胞的入核情况,与正常皮肤相比,瘢痕疙瘩组真皮中的细胞入核更多,说明雌激素通路激活更强。
以上实施例仅用以说明本发明的技术方案而非对其进行限制,本领域的普通技术人员可以对本发明的技术方案进行修改或者等同替换,本发明的保护范围以权利要求所述为准。
- 还没有人留言评论。精彩留言会获得点赞!