抗药性癌症的治疗方法与流程
本申请案是主张于2014年6月2日提申的美国临时专利申请号62/006,630的优先权,其揭示内容在此并入本案以作为参考数据。
技术领域
本发明涉及以止吐药(anti-emetic drug)与化疗药物组合治疗抗药性癌症的方法。
背景技术:
化学疗法,具体而言是与抗癌药剂的组合,为非定域肿瘤的治疗选择,所述肿瘤无法以手术或放射线治疗。然而,一些病患甚至于很短时间内复发,且对第二疗程的化疗无反应。
大多数恶性肿瘤对细胞毒性药物展现某些敏感性。据此,以该些药物治疗通常能缓解并使肿瘤收缩,其可能持续数周至数月。尽管如此,在许多情况下,肿瘤会再生,且此再生对进一步的细胞毒性疗法具抗性。
理论上,藉组合投予不同作用方式的药物,应能解决此问题。此疗法是基于在相同细胞自发性出现二或多个不同药物的抗药性的机率极小。合并性化学治疗(combination chemotherapy)似乎能避免抗药性肿瘤细胞的问题。
后续研究是针对与抗癌药物组合投药的方法。新开发的药物和数十年前的合并性化学治疗,于一些儿童白血病和何杰金氏病(Hodgkin's disease)产生高治愈率。然而,主要致死癌症,如肺癌、乳癌、和肠胃道癌症,仍对化疗具抗性。合并性化学治疗的失效未被厘清。为解释所述现象,有许多理论被提出,但该些理论中仅少数可被适当验证。
尽管治疗癌症的医药组合物的开发已有长足进展,新的抗药性癌症的治疗方法仍是需要的。
技术实现要素:
根据本发明,意外发现,普洛陪拉幸(prochlorperazine)与化疗药物的组合展现出协同效应,可减少癌细胞的体积与数目,且抑制具抗药性的癌细胞的生长。
在一方面,本发明是提供一种治疗具有对化疗药物具抗药性的癌症的个体的方法。所述方法包含对所述个体组合投予一治疗有效量的普洛陪拉幸或其类似物或代谢物、或其医药上可接受盐类,和化疗药物。
再一方面,本发明提供一种预防癌症转移的方法。所述方法包含对有需求的个体组合投予一治疗有效量的普洛陪拉幸或其类似物或代谢物、或其医药上可接受盐类,和化疗药物。
又一方面,本发明提供一种医药组合物或组合,以治疗具有对化疗药物具抗药性的癌症的个体或预防癌症转移,其特征为一治疗有效量的普洛陪拉幸或其类似物或代谢物、或其医药上可接受盐类,和与化疗药物的组合。
又另一方面,本发明是提供一种普洛陪拉幸或其类似物或代谢物、或其医药上可接受盐类,用于制造治疗具有对化疗药物具抗药性的癌症的个体的药剂,并与化疗药物组合的用途。
又再一方面,本发明提供一种普洛陪拉幸或其类似物或代谢物、或其医药上可接受盐类,用于制造预防癌症转移的药剂,并与化疗药物组合的用途。
于本发明的一具体实施例,化疗药物是选自于由吉非替尼(gefitinib)、厄洛替尼(erlotinib)、阿法替尼(afatinib)、培美曲塞(pemetrexed)、顺铂(cisplatin)、紫杉醇(paclitaxel)、欧洲紫杉醇(docetaxel)、吉西他滨(gemcitabine)、长春瑞宾(navelbine)、伊立替康(irinotecan)、阿瓦斯丁(avastin)、5-氟尿嘧啶(5-fluorouracil)、胺甲喋呤(methotrexate)、奥沙利铂(oxaliplatin)、替加氟-吉玛瑞西-欧特拉西儿(tegafur-gimeracil-oteracil potassium;TS-1)、表皮生长因子受体(EGFR)-酪胺酸激酶抑制剂和其组合组成的群组。
附图说明
前面的摘录,以及本发明的下列详尽说明,结合附图时将被更好地理解。于图式中:
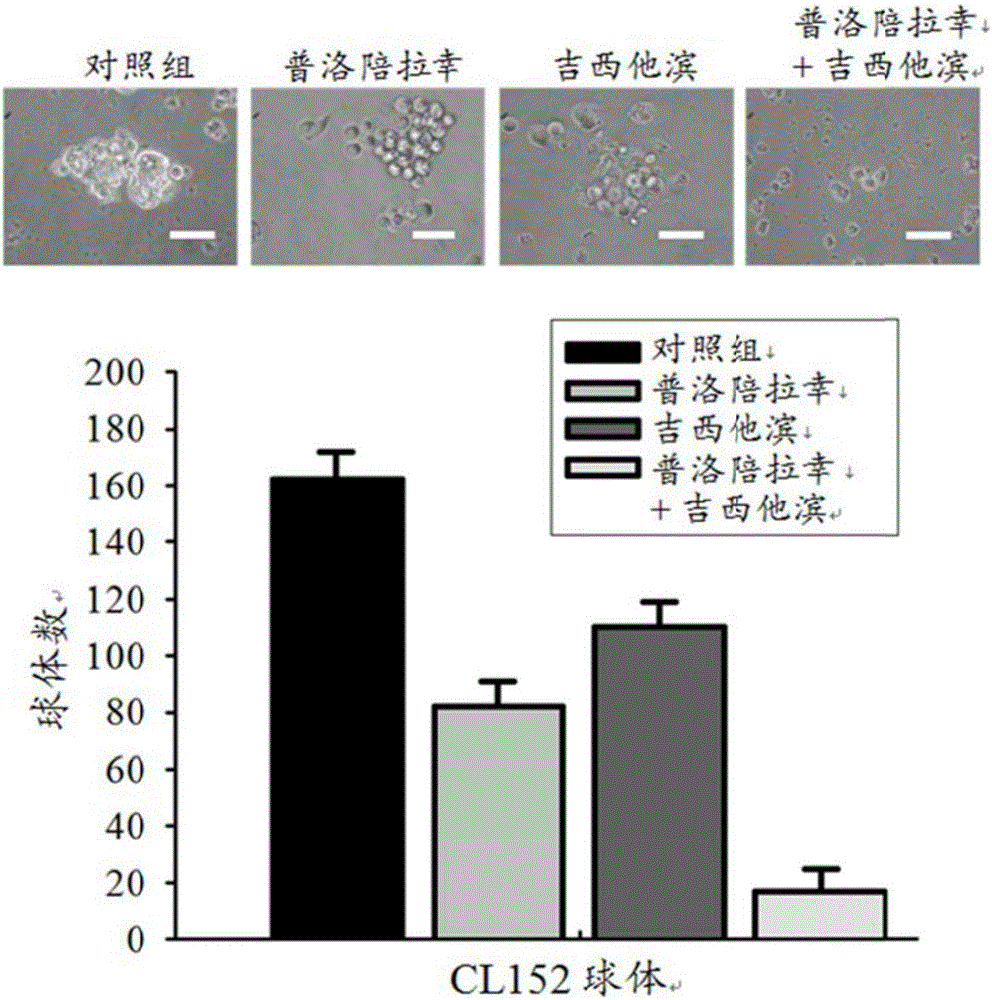
图1显示普洛陪拉幸诱导肺鳞状细胞癌细胞株CL152球体细胞凋亡,且结合吉西他滨可协同性增进细胞毒性;其中
图1A显示以普洛陪拉幸治疗48小时后,收集肺鳞状上皮细胞癌细胞株CL152球体并以流式细胞仪分析。普洛陪拉幸导致剂量依赖性增加的细胞凋亡。
图1B显示普洛陪拉幸与吉西他滨对于肺鳞状上皮细胞癌细胞株CL152球体具协同效应。
图1C显示于普洛陪拉幸治疗后,普洛陪拉幸抑制细胞迁移。
图1D显示普洛陪拉幸增加β-半乳糖苷酶阳性细胞的数目,且于以普洛陪拉幸处理24小时的A549细胞诱导老化。肺腺癌细胞株A549细胞以50μM白藜芦醇(resveratrol)处理,作为老化(senescent)阳性对照组。
图2显示普洛陪拉幸减少癌症类干细胞的百分比,且强化化疗药剂与吉非替尼诱导的细胞毒性;其中
图2A显示普洛陪拉幸减少肺腺癌细胞株CL141癌症类干球体细胞的细胞存活,且增进培美曲塞的抗癌活性;
图2B显示普洛陪拉幸减少肺腺癌细胞株CL97癌症类干球体细胞的细胞存活,且增进吉非替尼的抗癌活性;
图2C显示普洛陪拉幸抑制肺腺癌细胞株HCC827细胞的球体形成活性,且增进顺铂的抗癌活性;
图2D显示普洛陪拉幸抑制非小细胞肺癌细胞株H1299细胞的球体形成活性,且增进顺铂的抗癌活性;
图3是提供体内监测普洛陪拉幸介导的抗肿瘤功效,其为单独和与标准化疗药剂组合;其中:
图3A显示5x105个H441肿瘤实质细胞是皮下注射至NOD/SCID小鼠右腹侧,其随后分成载体组(对照组)和普洛陪拉幸组(5mg/kg/天,每周5次)。以测径器测量肿瘤负荷(tumor burden),并绘制随时间的肿瘤大小倍数变化;我方初步结果证实,于此浓度时,单独的普洛陪拉幸抑制(或推迟)体内肿瘤形成。于后续实验中,我方以普洛陪拉幸和标准化疗药剂的组合探讨肿瘤抑制功效。
图3B指出,相较于对照组、培美曲塞单独组(1mg/kg,每周5次)、和培美曲塞(1mg/kg,每周5次)与顺铂(1mg/kg,每周2次)的组合组,培美曲塞(1mg/kg,每周5次)与普洛陪拉幸的组合组(1mg/kg,每周5次)提供最显著的肿瘤抑制功效。
图3C显示腺癌肿瘤模式的实验结果,其中以标准化疗法是培美曲塞(50mg/kg)与顺铂(3mg/kg)的组合;且结果显示,以普洛陪拉幸(5mg/kg)加入标准疗法产生最小肿瘤负荷,接着为普洛陪拉幸单独组(5mg/kg)、培美曲塞(50mg/kg)与顺铂的组合组(3mg/kg)、和载体对照组。
图3D显示以标准治疗和吉西他滨与顺铂的组合于鳞状模式的实验结果;其指出,以普洛陪拉幸(5mg/kg)加入标准治疗(60mg/kg吉西他滨与3mg/kg顺铂的组合)提供最大肿瘤抑制功效,接着为普洛陪拉幸单独组(5mg/kg)、吉西他滨与顺铂组合组、和载体对照组。
图3E显示以吉非替尼加上普洛陪拉幸于吉非替尼抗药性NSCLC模式的治疗结果;其中吉非替尼(100mg/kg)与普洛陪拉幸(5mg/kg)的组合组显示最高程度的肿瘤抑制,接着为普洛陪拉幸单独组(5mg/kg);吉非替尼单独组(100mg/kg)和载体对照组显示相似的肿瘤负荷。
图4提供一些影像,显示以普洛陪拉幸用于肺鳞状细胞癌病患的个案研究结果,其中,所述病患为右下肺罹患肺鳞状细胞癌的81岁男性,并转移至右上肺。病患由于咳血,故右下肺原发病灶接受放射线治疗;接着自2010年5月19日起接受TarcevaTM(含厄洛替尼为活性成分)。病情维持稳定且首次CT显示0.5cm的右上肺转移。此病灶于2013年5月20日发展为2cm,伴随恶化的咳嗽与呼吸困难。由于高龄且整体状况差,所述病患选择继续服用TarcevaTM,且仅加入普洛陪拉幸。于服用普洛陪拉幸后,咳嗽与呼吸困难获改进,且三个月后的追踪CT显示病情稳定。疗法继续,直到2014年6月10日的最终追踪CT,显示肿瘤恶化。病患死于2014年终。
图5提供一些影像,显示以普洛陪拉幸用于肺腺癌病患的个案研究结果。具EGFR-L858R突变的肺腺癌病患(50岁女性,LUL),自2012年起首先以吉非替尼治疗(具恶性胸腔积液),且自2013年8月24日起以培美曲塞治疗。病患之后于2013年11月11日服用普洛陪拉幸伴随培美曲塞。疗法继续,直到2014年7月19日的最终追踪CT,显示肿瘤和胸腔积液明显减少。病患现仍存活。
图6提供一些影像,显示以普洛陪拉幸用于戒指细胞癌病患的个案研究结果。戒指细胞癌病患(58岁女性),具多重腹腔内转移,其平均中位数存活期为7-8个月,为自2012年7月16日起以数种化疗药物治疗(顺铂、5-氟尿嘧啶、伊立替康、紫杉醇、吉西他滨、阿瓦斯丁、TS-1、奥沙利铂、紫杉醇/5-氟尿嘧啶、和阿瓦斯丁/吉西他滨/TS-1)。病患于2013年2月25日服用普洛陪拉幸。疗法继续,直到2014年6月18日的最终追踪CT,显示肿瘤稳定。病患死于2014年终。
图7A和图7B显示临床过程和添加普洛陪拉幸作为维持疗法。所有个案是根据临床指导方针治疗。所有病患的预期寿命低于3个月。加入普洛陪拉幸以作为抢救治疗,延长其有效时间以防抗药性。此维持疗法的目的为协助控制疾病免于恶化,使病患活得更久。于普洛陪拉幸治疗后,客观反应率(objective response rate;ORR)、无恶化存活期(progression-free survival;PFS)、和整体存活期(overall survival;OS)显示,使用维持治疗的确有效维持疾病状态稳定且延长存活期。中位数ORR为-6.2%(-79.8%~4.3%)。于普洛陪拉幸治疗后,中位数PFS和OS分别为12.8(7.0-20.1)个月和13.5(7.4-21.4)个月。
具体实施方式
除非另有定义,本文使用的所有技术性和科学性术语,具有本发明领域具通常知识者所能常规理解的意义。
除非另有指明,本文使用的单数形式“一”、“一者”、和“所述”包括复数参考体。因此,举例而言,参考“一样本”包括复数个本领域具通常知识者习知的此类样本和其等同物。
本文使用的“普洛陪拉幸”乙词是指多巴胺(D2)受体拮抗剂,其是用于恶心和眩晕的止吐治疗。普洛陪拉幸的结构为
本文使用的“医药上可接受盐类”乙词是指普洛陪拉幸的任何医药上可接受盐类。医药上可接受盐类包括铵盐、碱金属盐如钾和钠(包括单、二、三钠)盐(其为较佳)、碱土金属盐如钙和镁盐、有机碱盐如二环己基胺盐、N-甲基-D-葡糖胺、和氨基酸盐如精胺酸、离胺酸等。
本文使用的“代谢物”乙词是指代谢作用的任何中间物和产物。普洛陪拉幸代谢物的一些实例包括但不局限于,N-去甲基普洛陪拉幸、普洛陪拉幸亚砜、和普洛陪拉幸亚砜4'-N-氧化物。于一特定实例,所述代谢物为N-去甲基普洛陪拉幸。
本文使用的“类似物”乙词是指任何具相同功能或活性的化学结构改变的化合物。普洛陪拉幸类似物的一些实例包括但不局限于,具下列结构的化合物:
本文使用的“个体”乙词是指任何温血物种,如人类和动物。欲根据本发明治疗的个体(如人类)实际上可为任何人类群体、男性或女性的个体,其可分成孩童、成人、或老年人。该些病患族群的任一者是与本发明的具体实施例相关。
本发明提供一种具有对化疗药物具抗药性的癌症的个体的治疗方法。本方法包含投予所述个体一治疗有效量的普洛陪拉幸或其类似物或代谢物、或其医药上可接受盐类,并结合化疗药物。
于本发明的一些实例,普洛陪拉幸与化疗药物的组合呈现协同效应,减少癌细胞的大小和数目。于本发明的其他实例,普洛陪拉幸与化疗药物的组合呈现协同效应,抑制癌细胞生长。
本文使用的“化疗药物”乙词是指任何提供抗癌功效的药物,包括但不限于,吉非替尼、厄洛替尼、阿法替尼、培美曲塞、顺铂、紫杉醇、欧洲紫杉醇、吉西他滨、长春瑞宾、伊立替康、阿瓦斯丁、5-氟尿嘧啶、胺甲喋呤、奥沙利铂、替加氟-吉玛瑞西-欧特拉西儿(TS-1)、表皮生长因子受体(EGFR)-酪胺酸激酶抑制剂和其组合。较佳的实例包括吉非替尼、厄洛替尼、阿法替尼、培美曲塞、顺铂、5-氟尿嘧啶、伊立替康、紫杉醇、吉西他滨、阿瓦斯丁、TS-1、奥沙利铂。于一特定实例中,化疗药物为吉非替尼。
于本发明的实例中发现,一些代谢物具如同普洛陪拉幸的细胞毒性活性,如表2所示。
于本发明的实例中亦发现,一些类似物具如同普洛陪拉幸的成株活性(clonogenic activities),如表3所示。
本文使用的“治疗有效量”乙词是指足以提供癌症治疗功效的量,其取决于投予方式和欲治疗的条件,包括年龄、体重、症状、疗效、投予途径、和治疗时间。
于本发明中,可以本发明方法治疗各种癌症。于一些具体实施例中,癌症为实体癌,如实体瘤。于其他具体实施例中,癌症为“液体”癌症或血液癌症。所述癌症是选自于由肺癌、肝癌、大肠癌、脑癌、乳癌、胰腺癌、胃癌、腺癌、鳞状细胞癌、和大细胞癌组成的群组。
于本发明的实例中发现,普洛陪拉幸于各类型癌症呈现细胞毒性,所述癌症包括腺癌、鳞状细胞癌、大细胞癌、肝癌、肠腺癌、脑癌、乳癌、胰腺癌、和骨髓瘤,参见表1。
本发明提供一种治疗具有对化疗药物具抗药性的癌症的个体的方法。所述方法包含对所述个体组合投予一治疗有效量的普洛陪拉幸或其类似物或代谢物、或其医药上可接受盐类,和化疗药物。于本发明的一实例中,癌症为肺癌,如非小细胞肺癌(NSCLC)。
另一方面,本发明提供一种预防癌症转移的方法。所述方法包含对有需求的个体组合投予一治疗有效量的普洛陪拉幸或其类似物或代谢物、或其医药上可接受盐类,和化疗药物。于本发明的一实例中,癌症为肺癌,如肺鳞状细胞癌。于本发明的另一实例中,癌症为胃癌,如戒指细胞癌。
于本发明的一实例中,普洛陪拉幸和厄洛替尼的组合提供预防肺癌(如肺鳞状细胞癌)转移的功效。于本发明的另一实例中,普洛陪拉幸和化疗药物,其是选自于由顺铂、5-氟尿嘧啶、伊立替康、紫杉醇、吉西他滨、阿瓦斯丁、TS-1、奥沙利铂、和其结合物组成的群组,的组合提供预防胃癌(如戒指细胞癌)转移的功效。
此外,本发明提供普洛陪拉幸或其类似物或代谢物、或其医药上可接受盐类,用于制造治疗具有对化疗药物具抗药性的癌症的个体的药剂的用途。本发明亦提供普洛陪拉幸或其类似物或代谢物、或其医药上可接受盐类,用于造预防癌症转移的药剂的用途。
于本发明中,普洛陪拉幸或其类似物或代谢物、或其医药上可接受盐类(“活性化合物”)可配制成医药组合物或制剂,其可以任何适当途径投予,包括但不限于,口服或非经口投予。于本发明的一实例中,含有普洛陪拉幸或其类似物或代谢物、或其医药上可接受盐类的组合物或制剂是经由口服途径投予,其可为固体或液体形式。固体组合物或制剂包括片剂、丸剂、胶囊、可分散粉剂、颗粒剂、和其类似物。口服组合物亦包括漱口剂,其是黏于口腔,和舌下片剂。胶囊包括硬胶囊和软胶囊。于此口服用固体组合物或制剂,活性化合物之一或多者可仅混合或伴随稀释剂、黏合剂、崩解剂、润滑剂、安定剂、增溶剂,且随后以常规方法配制成制备物。当有需要时,此类制备物可以涂布剂涂布,或其可以二或多个涂层涂布。另一方面,口服投予的液体组合物包括医药上可接受水溶液、悬浮液、乳液、糖浆、酏剂、和其类似物。于此类组合物,活性化合物之一或多者可溶解、悬浮、或乳化于常用的稀释剂(如纯水、乙醇、或其混合物等)。除了此类稀释剂以外,所述组合物亦可含有润湿剂、悬浮剂、乳化剂、甜味剂、调味剂、香料、防腐剂、缓冲剂、和其类似物。
非经口投予的医药组合物包括溶液、悬浮液、乳液、和固体注射组合物,其是于使用前立即溶解或悬浮于溶剂。注射剂可藉将活性成分之一或多者溶解、悬浮、或乳化于稀释剂而制备。所述稀释剂的实例为注射用蒸馏水、生理盐液、植物油、酒精、和其组合。此外,注射剂可含有安定剂、增溶剂、悬浮剂、乳化剂、抚慰剂、缓冲剂、防腐剂等。注射剂是于最终配制步骤除菌,或藉无菌程序制备。本发明的医药组合物亦可配制成无菌固体制备物,例如,藉冷冻干燥,且可于除菌后使用,或于使用前立速溶于无菌注射水或其他无菌稀释剂。
下列实施例应当解释为仅具说明性,而非以任何方式局限本发明的其余部分。毋须进一步详尽说明,据信本领域具通常知识者可基于本文的描述,最大限度地使用本发明。
实施例
I.细胞培养和化学物质
A549、CL141、和H441为EGFR野生型肺腺癌细胞株;HCC827具EGFR外显子19缺失;且CL97为EGFR T790M与G719A点突变肺腺癌细胞株。CL152、H2170、和H226为肺鳞状细胞癌细胞株,且H1299为非小细胞肺癌细胞株。A549-ON细胞株是A549细胞过度表达Oct4与Nanog,发明人视其为类干细胞癌症细胞株(22)。所有细胞株皆维持于RPMI培养基,且补充10%胎牛血清(FBS,Invitrogen)、2mM L-麸酰胺酸、100U/mL青霉素、和100μg/mL链霉素。于细胞培养实验方面,10mM普洛陪拉幸储液是溶于二甲基亚砜(DMSO;Sigma)。普洛陪拉幸、顺铂、吉西他滨是购自Sigma。
II.细胞毒性和磺基玫瑰红B(sulforhodamine B)试验
细胞以每孔2000个细胞的密度三重复分盘于96孔培养盘。细胞于第三天(以确保适当分盘效率和活力)处理指定药剂48小时。细胞是以不同浓度的普洛陪拉幸、顺铂、吉西他滨、或例如,普洛陪拉幸与吉西他滨的组合处理。以磺基玫瑰红B(SRB)试验评估细胞毒性(23)。简言之,移除培养基,且各孔的附着细胞是于4℃下以100μl的冷的10%三氯乙酸(w/v)固定1小时。于固定后,细胞于室温下以每孔100μl的0.4%(w/v,溶于1%乙酸)SRB溶液染色30分钟,随后以1%乙酸清洗5次。于空气风干后,将100μl的10mM Tris碱加入各孔,并于530nm读取吸光值。细胞毒性是以药物处理孔中相对于仅溶剂的对照组细胞数目(设定为100%)的细胞百分比表示。各实验以三重复单独进行至少2次,且细胞毒性以平均值±SD表示。
III.成株试验
受测细胞是分别种植于6孔培养盘中14天,其中每孔104个细胞。于细胞种植后24小时,加入普洛陪拉幸和其他受测药物。每隔4天置换培养基和普洛陪拉幸。于处理后,细胞以PBS清洗,且细胞群落以固定液(甲醇:乙酸=3:1)固定,并以溶于甲醇的0.5%结晶紫染色。于小心移除结晶紫且以自来水清洗后,手动计数细胞群落。各实验以三重复独立进行至少2次,且细胞毒性以平均值±SD表示。
IV.肿瘤球体试验
简言之,单类细胞是分盘于6孔超低附着培养盘(Corning Inc.),其以每毫升2,000个细胞的密度培养于肿瘤球体培养基DMEM/F12,并补充1%N2补给物(Invitrogen)、10ng/mL碱性纤维细胞生长因子(Sigma-Aldrich)、10ng/mL表皮生长因子(Invitrogen)、和1%青霉素/链霉素(Invitrogen),培养条件为37℃的95%空气与5%CO2的潮湿环境,细胞每周培养2次。当继代培养时,收取肿瘤球体。球体是以TrypLETM(Invitrogen)分离。以台酚蓝排除法(Trypan Blue Exclusion method)计数球体细胞。
V.以流式细胞术进行侧群分析和纯化
细胞的单类细胞悬浮液是以胰蛋白酶-EDTA(Invitrogen)自培养盘分离,并以每毫升1×106个细胞悬浮于补充3%胎牛血清和10mM Hepes的汉克氏平衡盐液(Hank’s balanced salt solution;HBSS)。该些细胞随即于37℃下以20μg/mL Hoechst33342(Sigma Chemical,St.Louis,MO)培养90分钟。将ABC运输蛋白抑制剂维拉帕米(verapamil)(Sigma)加入,使其最终浓度为50μM,以确认流式细胞术的闸控区域。以指定药物培养90分钟后,细胞立即于300g和4℃下离心5分钟,并再悬浮于冰冷的HBSS。将细胞保持于冰上,以防Hoechst染料流出,并加入1μg/mL碘化吡啶(PI,BD),以区分死细胞。最终,该些细胞是过滤通过40μm细胞过滤器(BD),以取得单类悬浮细胞。于双雷射FACS Vantage SE(BD)进行细胞双波长分析和纯化。Hoechst 33342可于355nm紫外光下激发,并以450/20带通(BP)滤波器发散蓝色荧光,和以675nm边缘滤波器长通(EFLP)发散红色荧光。以610nm分色镜短通(DMSP)分开所述发散波长。将PI阳性(死)细胞排除于分析之外。
VI.Aldefluor试验
高醛去氢酶(ALDH)酵素活性是用于检测肺癌干细胞群。根据制造商指导方针进行Aldefluor试验(StemCell Technologies)。简言之,取自细胞培养基的单类细胞是于37℃下培养于Aldefluor试验缓冲液50分钟,所述缓冲液含有ALDH受质(乙醛缩-胺基乙醛(bodipy-aminoacetaldehyde,BAAA))。作为阴性对照组,取自各样本的一部分细胞是于ALDH抑制剂(二乙基胺基苯甲醛,DEAB)存在下培养于相同条件。以流式细胞术测量ALDH阳性细胞群。
VII.普洛陪拉幸介导的抗肺癌功效的体内检验
于第一试验中,人类肺腺癌细胞株NCI-H441(购自ATCC,1百万个细胞/注射)细胞是皮下注射至NOD/SCID小鼠右腹侧(雌性,4-6周大)。当肿瘤变得可触知时,以测径器记录其大小,且小鼠是随机分成对照组(DMSO载体)和普洛陪拉幸处理组(5mg/kg,5天/周,腹腔注射)。经过4周时间,于两组别形成的肿瘤是每周以测径器测量。肿瘤大小的变化是以倍数改变表示,并随时间绘图。相较于载具对照组,以普洛陪拉幸处理似乎抑制和/或推迟肿瘤生长(**p<0.01)。
于第一药物结合测试中,表达萤火虫荧光素酶的NCI-H441细胞(6x105个细胞/注射)是经由侧尾静脉注射至NOD/SCID小鼠(4-6周龄),以建立肿瘤模式。于肿瘤注射后一周,小鼠是随机分成不同组别:载体组、普洛陪拉幸(1mg/kg)与培美曲塞(1mg/kg)组合组(NSCLC的标准化疗药剂)、培美曲塞(1mg/kg)+顺铂(1mg/kg)治疗组、和培美曲塞(1mg/kg)+普洛陪拉幸(1mg/kg)治疗组。以测径器记录不同组别的肿瘤负荷。肿瘤大小的变化是以倍数改变表示,并随时间绘图。随后,我们进行另一组药物结合测试。我们以二主要标准化疗法结合普洛陪拉幸。于肺腺癌方面,标准药物组合为培美曲塞与顺铂,而吉西他滨与顺铂则用于肺鳞状癌。于带有CL97(肺腺癌)肿瘤的小鼠,结合培美曲塞+顺铂+普洛陪拉幸提供最显著的肿瘤抑制功效,其优于培美曲塞+顺铂组和普洛陪拉幸单独组。于带有CL152(肺鳞状细胞癌)肿瘤的小鼠,标准疗法(吉西他滨+顺铂)加上普洛陪拉幸似乎亦抑制肿瘤形成,其优于普洛陪拉幸单独组和吉西他滨+顺铂组。接着,我们证实,吉非替尼抗药性CL97肺癌细胞于体内对普洛陪拉幸具敏感性。CL97癌细胞(1.5x106个细胞/注射)是皮下注射至NOD/SCID小鼠,以建立体内肿瘤模式。小鼠是随机分成4个组别:对照组、吉非替尼单独组(100mg/kg,PO,5次/周)、普洛陪拉幸单独组(5mg/kg,IP,5次/周)、和吉非替尼+普洛陪拉幸组。于肿瘤注射后5周,观察到普洛陪拉幸单独组和吉非替尼+普洛陪拉幸组产生显著的肿瘤抑制功效。于肿瘤注射后第6周,吉非替尼+普洛陪拉幸组显示最显著的肿瘤抑制功效,接着为普洛陪拉幸单独组,其后对照组和吉非替尼单独组两者显示类似肿瘤负荷。
结果
普洛陪拉幸于NSCLC细胞株的细胞毒性
我们首先探讨普洛陪拉幸于各种NSCLC细胞株的细胞毒性功效。A549、A549-ON、CL97、CL141、HCC827、和H441为肺腺癌细胞株。CL152、H2170、和H226为肺鳞状细胞癌细胞株。以SRB试验测定细胞存活力。以各浓度的普洛陪拉幸处理48小时后,所有癌细胞株的IC50值为约20μM(参见表1)。进行成株试验,以测定普洛陪拉幸的抗肿瘤活性。曝露于不同浓度的普洛陪拉幸后,NSCLC细胞株的成株性(clonogenicity)以浓度依赖性方式降低。癌症干细胞(CSC)是假定存在独特拥有自我更新能力和治疗抗性的肿瘤细胞群。由于普洛陪拉幸预期偏好抑制肺脏CSC,我们接着检测是否NSCLC(具野生型EGFR的肺鳞状细胞癌细胞)球体的比例可藉普洛陪拉幸处理而减少。欲测定是否侧群(SP)细胞,是指具CSC特性的细胞群,存在于NSCLC细胞株,我们以荧光染料Hoechst 33342将细胞染色,并以流式细胞术分析细胞。根据散射信号排除死细胞和细胞碎片后,NSCLC细胞含有一小群具SP细胞特性的细胞。以2.5、5、和10μM的普洛陪拉幸培养48小时后,SP细胞的比例为剂量依赖性减少(参见表1)。
普洛陪拉幸减少侧群细胞和ALDH+细胞的比例
普洛陪拉幸处理是否能消耗ALDH表达细胞的百分比(ALDH为造血和NSCLC CSCs两者的习知标记)亦被探讨。如表1所示,普洛陪拉幸处理亦以剂量依赖方式减少ALDH+CL152群体。总结,普洛陪拉幸于NSCLC细胞显示低或最小细胞毒性功效。
表1
普洛陪拉幸于各类癌症的细胞毒性
此外,以SRB试验和台酚蓝排除法检验普洛陪拉幸代谢物于NSCLC亲代和球体细胞的细胞毒性。其发现N-去甲基普洛陪拉幸于NSCLC细胞株显示优于其他受测代谢物的细胞毒性功效(参见表2)。
表2
普洛陪拉幸代谢物的IC50
同时,检验普洛陪拉幸类似物对CL141成株性的功效,其中将大约1,000个细胞种植于6孔培养盘并以不同类似物处理;于14天后,细胞群落以结晶紫染色、拍摄、和计数。结果显示于表3,显示四种普洛陪拉幸类似物降低NSCLC细胞成株性。
表3
普洛陪拉幸类似物的成株试验
普洛陪拉幸诱导CL152球体细胞凋亡且与吉西他滨组合协同性地增进细胞毒性
以普洛陪拉幸处理48小时后,收集CL152球体并以流式细胞术分析。普洛陪拉幸导致细胞凋亡呈现剂量依赖性增加(图1A)。吉西他滨为常用于NSCLC治疗的化疗药剂。接着,以球体形成试验探讨普洛陪拉幸与吉西他滨组合的功效。结果证实,普洛陪拉幸与吉西他滨于CL152球体显示协同效应(图1B)。
普洛陪拉幸抑制肺癌细胞迁移和诱导老化
历经表皮间质转化(epithelial-mesenchymal transition;EMT)的癌细胞被发现显示增加的细胞凋亡和特定化疗药物的抗性。EMT于调节癌症干性上亦扮演关键角色。EMT的特征在于增进的细胞迁移和侵袭。以透孔迁移试验(transwell migration assay)测定是否普洛陪拉幸的亚细胞毒性浓度能抑制A549细胞的体外细胞活动。相较于DMSO对照组(图1C),于24小时后,以10μM普洛陪拉幸处理明显抑制A549细胞的细胞迁移。此外,我们检验了普洛陪拉幸对A549细胞老化的功效。以老化检测套组(BioVision Inc.)检测β-半乳糖苷酶(SA-β-Gal)活性。以1μM普洛陪拉幸和作为阳性对照组的50μM白藜芦醇处理24小时后,A549细胞增加β-半乳糖苷酶活性且诱导β-半乳糖苷酶活性,阳性细胞是以200x视野的显微镜计数(图1D)。该些数据显示,普洛陪拉幸于低浓度时能诱导NSCLC细胞老化。
普洛陪拉幸显著抑制NSCLC癌症球体的自我更新
欲评估是否单独的普洛陪拉幸或与临床药物、化疗药剂、和EGFR-酪胺酸激酶抑制剂吉非替尼的组合的治疗,能体外抑制NSCLC癌症类干球体细胞。CL141球体细胞(图2A)和CL97球体细胞(图2B)是以单独的普洛陪拉幸、单独的培美曲塞(CL141球体)或吉非替尼(CL97球体)、或组合治疗48小时。普洛陪拉幸(1、2.5、5、和10μM)是浓度依赖性减少CL141和CL97细胞球体数目(图2A和图2B)。相较于单独的培美曲塞或吉非替尼,以普洛陪拉幸与临床药物的组合共治疗亦明显减少球体细胞数目(图2A和图2B)。欲进一步探索普洛陪拉幸与顺铂的组合于CSC的功效,我们进行二NSCLC细胞株(包括HCC827和H1299)的球体形成试验。普洛陪拉幸抑制球体形成能力(图2C和图2D)。有趣的是,与顺铂组合时,该些NSCLC细胞的球体数目似乎比以单独的普洛陪拉幸或顺铂治疗的细胞的低。总之,该些数据显示,普洛陪拉幸于该些受测球体具抗CSC能力,且普洛陪拉幸与化疗药剂或EGFR-酪胺酸激酶抑制剂的组合对癌症治疗具效益。
体内检验普洛陪拉幸的肿瘤抑制功效
于第一试验中(图3A),NCI-H441(1x 106个细胞/注射)细胞是皮下注射至NOD/SCID小鼠右腹侧(雌性,4-6周大)。当肿瘤变得可触知时,以测径器记录其大小,且小鼠是随机分成对照组(DMSO载具)和普洛陪拉幸处理组(5mg/kg,5天/周,腹腔注射)。于处理后四周,清楚发现,相较于载体对照组,普洛陪拉幸于5mg/kg时有效抑制肿瘤生长(**p<0.01)。
于药物组合测试中(图3B),表达萤火虫荧光素酶的NCI-H441细胞(6x105个细胞/注射)是经由侧尾静脉注射至NOD/SCID小鼠(4-6周龄),以建立肿瘤模式。于肿瘤注射后一周,小鼠是随机分成不同组别:对照组、普洛陪拉幸(1mg/kg)与培美曲塞(1mg/kg)(NSCLC的标准化疗药剂)的组合组、培美曲塞(1mg/kg)与顺铂(1mg/kg)结合组、和培美曲塞(1mg/kg)与普洛陪拉幸(1mg/kg)的组合组。有趣的是,我们发现,使用我们的投剂疗法,顺铂(1mg/kg)与培美曲塞的组合的肿瘤生长抑制功效未明显异于培美曲塞单独组(1mg/kg)(参见图3B)。然而,普洛陪拉幸与培美曲塞的组合提供明显比其他组别更好的肿瘤抑制功效(*p<0.05)。
于其他药物结合测试中,CL97(图3C)和CL152(图3D)细胞是皮下注射至NOD/SCID小鼠右腹侧(雌性,4-6周大)。于肿瘤注射后一周,小鼠是随机分成不同组别:对照组(DMSO载体)与普洛陪拉幸处理组(5mg/kg)、标准治疗组(50mg/kg培美曲塞或60mg/kg吉西他滨与3mg/kg顺铂组合)、和组合组(标准治疗与5mg/kg普洛陪拉幸组合)。由动物数据可知,普洛陪拉幸单独组可抑制肿瘤生长(*p<0.05,***p<0.001);标准治疗与普洛陪拉幸的组合显示比其他处理组更显著的肿瘤生长抑制功效(**p<0.01,***p<0.001)。
欲检验是否普洛陪拉幸可克服抗药性问题,CL97(EGFR T790M与G719A突变)细胞是皮下注射至NOD/SCID小鼠右腹侧(雌性,4-6周大)。于肿瘤注射后一周,小鼠是随机分成不同组别:对照组(DMSO载体)与普洛陪拉幸处理组(5mg/kg)、标靶治疗组(100mg/kg吉非替尼)、和组合组(100mg/kg吉非替尼与5mg/kg普洛陪拉幸组合)。于图3E中,吉非替尼单独组无法有效抑制肿瘤生长。然而,普洛陪拉幸单独组或与吉非替尼的组合显示显著的肿瘤生长抑制功效(***p<0.001)。由证据可知,经由增加化疗或标靶治疗敏感性,普洛陪拉幸可解决抗药性问题。此发现显示,普洛陪拉幸可视为未来化疗或标靶治疗的临床佐剂治疗剂。
普洛陪拉幸治疗后的临床个案
为证明本发明的概念,进行普洛陪拉幸(于图中以药物P标示)的临床观察研究(参见图4-图6)。病患包括以TarcevaTM(含有厄洛替尼以作为活性成分)治疗的肺鳞状细胞癌病患(如图4所示)、以培美曲塞治疗的肺腺癌病患(如图5所示)、和以数种化疗药剂的组合治疗的戒指细胞癌病患,该些化疗药剂包括顺铂、5-氟尿嘧啶、伊立替康、紫杉醇、吉西他滨、阿瓦斯丁、TS-1、奥沙利铂、紫杉醇/5-氟尿嘧啶、和阿瓦斯丁/吉西他滨/TS-1(如图6所示),其亦服用普洛陪拉幸。观察到,病患呈现稳定或肿瘤减少情况。所述观察显示,以现有治疗加上普洛陪拉幸对病患具效益。于其他情况下,数个病患服用普洛陪拉幸一年以上,显示现有剂量可于副作用最小的情况下耐受。此外,加入普洛陪拉幸可视为一种维持疗法,其有助于病患控制疾病而无癌症恶化,使病患活得更久。于普洛陪拉幸治疗后,鉴于包括中位数客观反应率(ORR)、无恶化存活期(PFS)、和整体存活期(OS)等数据,观察到病患的疾病状态可有效维持稳定,且存活期延长(图7A和图7B)。
可结论的是,以普洛陪拉幸与化疗组合,可对各种癌症病患提供治疗效益,具体而言是克服抗药性问题和预防癌症转移。
据信,本发明领域具通常知识者可基于本文的阐述最大限度利用本发明,而毋须进一步说明。因此,应理解到,所提供的说明和权利要求仅用于示例的目的,而非以任何方式局限本发明的范畴。
- 还没有人留言评论。精彩留言会获得点赞!