多流体组织切除方法及设备与流程
本申请是2011年02月04日提交的发明名称为“多流体组织切除方法及设备”的第201180014687.9号中国专利申请(国际申请号pct/us2011/023781)的分案申请。发明背景1.发明领域。本发明总体上涉及医疗方法和设备。具体地,本发明涉及用于向尿道和前列腺施加能量以实现组织减容术的方法和设备。多种医学状况会影响男性尿道,从而导致包括排尿疼痛或排尿困难、前列腺肿大、尿血、腰痛等在内的多种症状。这些状况中的一些状况,比如前列腺炎,是细菌感染,可用抗生素和其他药物治疗。然而,其他状况,比如良性前列腺增生(bph)和前列腺癌,造成前列腺增大和尿道梗阻,有时会导致膀胱功能的完全丧失。尽管用于治疗bph的各种药物疗法已被证明有效,但它们的有效性往往持续时间有限,并且经常需要诸如外科手术治疗等另外干预。bph的外科手术治疗包括根治性前列腺切除术或部分前列腺切除术的几种形式,涉及前列腺的电外科全切或部分电外科切除。前列腺切除术是用于减轻压迫性前列腺增大继发的尿流梗阻的、最具侵入性和最有效的治疗。虽然其在泌尿外科实践中的使用已由于引入了创伤更小的技术而迅速下降,但其仍被美国泌尿外科学会(americanurologyassociation,aua)认为是急性症状性bph处置的黄金护理标准。基于开放式外科手术的根治性前列腺切除术很少在bph治疗中采用,其几乎只被用于前列腺癌适应症。前列腺切除术可经由开放式途径、腹腔镜途径或者经尿道途径来实现。后者优选用于部分前列腺切除术,该手术通常在患有急性症状性bph的患者身上进行。已建立的技术包括基于电烙术的经尿道前列腺切除术(turp)、经尿道前列腺汽化术(tuvp)以及经尿道前列腺切开术(tuip),但后一种技术不常使用。在turp中,将电切环插入尿道并用其来清除多余的前列腺组织,而tuip则依赖于切割与前列腺相邻的肌肉来松弛膀胱口,以便缓解排尿困难。tuvp被开发用于在减少手术发病率和住院时间的同时,产生与标准turp相仿的结果。在tuvp中,用能够输送足以使前列腺组织汽化的能量的滚球来代替电切环。在过去十年中,医疗设备制造商们已开发出若干种针对bph的基于微创(mi)定向能的技术,这些技术旨在减少伴随电外科手术途径的发病率和并发症,允许以更经济的门诊方式进行治疗,并使其适合于药物疗法失败但又没有严重到足以有理由进行诸如turp等电外科手术干预的患者。在这些mi技术中,有经尿道微波热疗术(tumt)、基于rf的经尿道针刺消融术(tuna)、水致热疗(wit)以及使用经尿道光纤的几种激光消融技术,诸如间质激光前列腺凝固术(ilc)、钬激光前列腺剜除术(holep)和光选择性前列腺汽化术(pvp)。虽然tump、tuna和wit总体上是成功的,但它们不足以治疗所有的患者和所有的状况。特别是,患有由bph或前列腺癌所造成的组织严重侵入尿道腔中的患者难以用依靠组织收缩而非切除的上述方法来治疗。因此,这些患者中的许多人最终将需要传统的外科手术切除。相反,holep和pvp能够通过汽化而主动地清除组织。然而,holep受限于漫长的手术时间和相对较高的学习曲线,这限制了它的广泛使用。因此,泌尿学界近来已接受相对而言在技术上不那么苛刻的pvp,其中,将具有60w至120w的输出功率的激光束从尿道导向前列腺组织,以实现超过被称为汽化阈值的一定体积功率密度的辐照(功率密度)水平,在该汽化阈值之下发生组织凝固而不是汽化。当辐照水平增至汽化阈值之上时,组织汽化会增加,而凝固会减少。然而,从pvp系统中的探头发射的光束是发散的。因此,激光斑点大小随着探头与组织的距离增加而增大,并且功率密度降低,从而降低汽化速率。因而,为使组织汽化的速率最大化并从而限制以术后所留下的组织凝固为特征的热损伤区的范围,医生必须稳定地将光纤与组织保持固定的距离(例如,1-2mm),并且在不改变该距离的情况下缓慢地将光束在靶组织上扫过。随着手术的进行,组织变得碳化并且更加难以消融。因此,pvp的严重限制在于随着手术进行而逐渐下降的组织清除速率,这显著增加了手术时间、患者花费和风险。另外,该手术的有效性和持续时间高度依赖于主治医生的技能以及非常昂贵的高功率激光系统的使用。此外,以上所述的大多数手术要求非常高的能量来使组织凝固和/或汽化,这样高的能量只能用庞大而昂贵的高功率器材来产生。另外,目前对bph的治疗往往伴有高并发症风险。例如,turp与以下并发症有关:逆行射精、术后刺激、勃起功能障碍、严重血尿、以及急性尿潴留和失禁,以及其他并发症。治疗后并发症可以归因于切除、消融或者以其他方式损伤前列腺-尿道区域内的非腺体组织,诸如精囊、括约肌、前列腺内血管、神经组织或者肌纤维间质。另外,利用选择性热解来使靶组织消融、凝固或变性从而充分缩减前列腺体积的治疗方式很可能造成广泛的组织热损伤区。后果是热治疗后的前列腺组织水肿和肿胀,这往往会导致无法向患尿潴留的患者提供即时症状缓解,以及需要术后插入导管和住院治疗。此外,由于诸如bph之类的前列腺疾病的症状时常导致尿道梗阻,因此经尿道前列腺治疗方法和设备很可能受阻于异常的组织闭塞。这是因为设备可能无法在闭塞空间内正确移动以治疗期望的区域,因此阻碍了治疗设备正确地或最佳地发挥功能。另外,异常的组织闭塞还可能限制治疗过程的可视性,并且一般会妨碍最佳治疗。由于这些原因,期望提供如下微创方法和设备——该微创方法和设备增加尿道周围组织的切除体积和/或尿道管腔面积。如果此类方法和设备提供对组织的无加热清除从而允许在不对组织造成热损伤的情况下进行组织切除,则将会是特别期望的。如果此类方法和设备提供对尿道周围此类组织的清除或破坏,其中即使在清除大体积的组织时仍然可以将切除的产物或破坏产物从管腔清除从而缓解尿道上的压力,则将会是特别期望的。此外,期望此类方法和设备通过选择性地切除腺体组织而保持非腺体组织不受损伤,来使治疗后并发症最小化。另外,期望此类方法和设备通过形成工作空间以支持更好的设备移动和更好的治疗区域可视性,来扩大治疗区域。备选地或附加地,该方法和设备应当提供治疗设备相对于尿道的锚固,以便为治疗方案提供稳定的平台。用于执行此类方案的方法和设备应当给患者带来最小风险,应当相对地易于由主治医生执行,并且应当即使在患者患有严重疾病时仍然允许以最小的并发症来缓和症状。以下所描述的本发明将会满足这些目标中的至少一些目标。
背景技术:
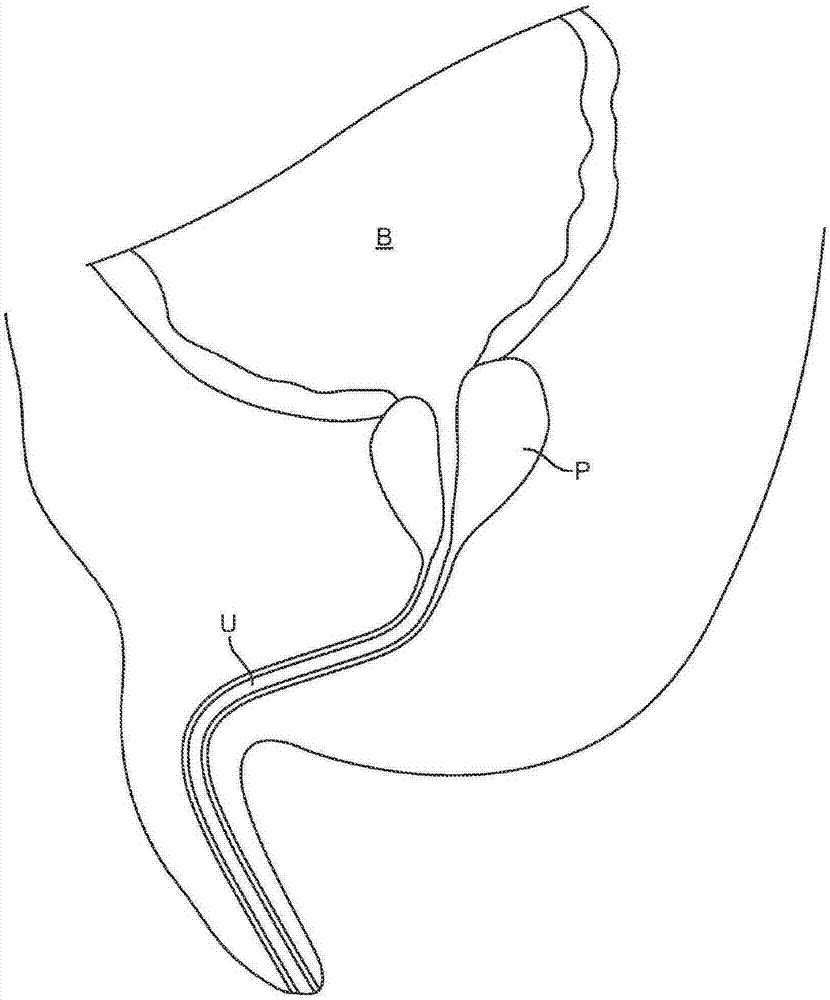
:。在boffo等人(2001)j.endourol.15:313-316中描述了使用经尿道内窥镜进行双极射频前列腺汽化。在woloszko等人(2002)ieeetrans.plasmasci.30:1376-1383和stalder等人(2001)appl.phys.lett.79:4503-4505中讨论了用于产生组织消融性等离子体的盐水溶液中的射频放电。在jian和jiajun(2001)trans.asme246-248中描述了用于切除组织的空气/水射流。us20050288639描述了可以通过膀胱中的球囊而锚固尿道中基于导管的系统上的针式注射器。美国专利号6,890,332;6,821,275;和6,413,256各自描述了用于产生针对组织消融的rf等离子体的导管。在美国专利公开号20020128637中描述了使用激光来切割生物组织,并且在美国专利号5,257,991;5,514,669;和6,986,764中描述了使用激光来消融前列腺组织。在美国专利号7,122,017;5,620,414;和5,505,729中描述了用于产生外科手术切口的加压水流。在美国专利公开号20070278195、加拿大公开申请2,330436a1、pct公开wo99/56907和美国专利号7,163,875;5,902,499;和5,773,791中描述了使用水或其他流体射流作为波导来携带用于切割和其他制造操作的激光束。美国专利号6,960,182描述了使用液体射流仪器来切除诸如膝盖关节囊等组织,其中喷嘴形成液体射流,而该射流由射流接收开口接收。美国专利号5,135,482描述了用于消除部分或完全阻塞人体血管的有机沉淀物的流体动力设备。所述专利未披露使用流体流来切除在诸如前列腺-尿道区域之类的封闭组织区域内的组织。美国专利号5,782,848描述了使用水射流来切除凝固的组织。该专利未披露使用流体流来切除未凝固组织或其他未经治疗的组织。美国专利号5,207,672描述了通过使用球囊来压缩部分前列腺以及利用激光束来消融组织。该专利未披露扩张尿道并继而使用流体流来切除组织。美国专利号4,560,373;3,818,913;4,913,698;5,505,729;以及美国专利公开号20090149712和20090157114描述了使用流体流来处理各种组织。所述专利和专利申请未描述使用流体流在诸如前列腺-尿道区域之类的封闭组织区域中切除组织。在美国专利号5,037,431;6,720,745;美国专利公开号20070129680、20080038124、20080243157、20080221602和20090060764中描述了诸如泵、涂药器等流体射流外科手术装置的各其他方面。gruber等人的美国专利公开号20080097470披露了在妇科手术中使用机械扩张和流体射流剖割。该申请未描述使用流体流来切除一定体积的组织。美国专利公开号20080188868、20080249526和20090287045披露了在例如腹腔镜手术中使用流体射流切除组织。众所周知,腹腔镜手术在腹腔中形成工作空间,并且该工作空间不是在经受外科手术的器官内形成。上述公开未描述向器官中插入设备,并在该器官内形成工作空间,以及使用流体流来切除器官组织。技术实现要素:根据本实施方式的方法、设备和系统提供对前列腺组织的治疗,以便缓解诸如bph、前列腺炎和前列腺癌等状况的症状,其中前列腺的增大可能阻塞尿道并压迫尿道以及导致尿道的部分或完全闭塞。在第一方面,一种用于切除前列腺组织的方法包括将具有流体输送元件的设备置于前列腺内的尿道管腔之中。从流体输送元件向外引出流体流并将其引向尿道腔的壁。流体流足够有力以便清除组织。移动流体输送元件以将流体流在所述的壁上扫过,从而清除管腔周围一定体积的组织,以便缓解与管腔堵塞相关联的症状。流体输送元件可以输送水、盐水或其他流体——它们可选地与治疗活性物质相结合,以便将治疗与诸如化疗等其他疗法或者与麻醉剂、抗生素、血管收缩剂和抗炎剂或者包含治疗用放射性同位素的放射性药物等的引入结合起来。流体可与气体、可溶物或晶粒相结合,以便提高切除效率。根据本实施方式,使用流体流来切除组织提供了多种优点。根据诸如流体源压强、流体流形、治疗时间和治疗模式等选定的设置参数,组织切除被非常迅速地进行。本流体流技术切除组织比诸如激光消融等传统技术快大约一个数量级。另外,由于组织切除不需要热源,本方法基本上无需加热,因此不会在治疗的组织上留有热损伤区。因而,将不会存在或者存在很小的术后肿胀,从而消除或减少了对导管插入的需要,并能立即缓解症状。使用流体流来切除组织还通过避免在体内使用原本可导致神经损伤的其他能量源而降低了患者风险。本流体流切除技术还提供了以适当压强进行选择性组织切除的优点,其中可将流体压强和其他特性设置成使得软组织得到清除,而诸如结缔组织之类的较硬组织则基本上不受流体流的影响。另外,可将流体流设置成发散的流,从而减少对距离流体输送元件较远处的组织的冲击,这保护前列腺囊以及大动脉和大静脉在外科手术期间免受损伤。为了在尿道内获得工作空间,本发明的方法还可以包括在输送流体流以切除组织之前或当中引入流体喷注治疗区域中的尿道。这样的喷注可以用来帮助控制从加压流体源到正在治疗的组织表面的距离。此外,可选择喷注流体为比切除流体粘度更低的介质,从而降低切除流体在组织切除期间遭遇的阻力,以及保持切除流体流形的完整性。另外,可以选取这两种流体使得它们的折射率之差提供在切除流体中的内反射,特别是全内反射,以及允许切除流体充当电磁能传输的管道,例如用于对组织的烧灼或其他能量输送。可选地,可以使用机械方式来形成工作空间。本发明的方法还可以包括清除已输送到治疗区的流体以及清楚切除所产生的组织碎屑和流体。还可以在用流体流进行治疗之前、当中或之后,利用盐水或其他流体来冲洗或喷射治疗区。虽然根据本实施方式的组织切除通常将会使用有力的流体流来实现,但是在一些实例中,在有力流体流的输送之前、当中或之后输送他治疗能量的可能是有益的。在此类其他方法中,流体流对于切除组织可能不够有力。这样的能量可被输送用于增强组织切除,但通常将会被输送用于提供对组织的烧灼——通常在使用有力流体流的治疗完成之后输送。合适的能量源包括激光能、射频能、热、冷等,并且可以宽泛地包括应用任何电磁能、机械能、振动能、热能和/或电能。加压流体源的定位通常将会包括向尿道推入探头,引导加压流体经过可移动地安装在探头上的流体输送元件(诸如一个喷嘴或多个喷嘴),以及相对于探头移动流体输送元件以便将流体流在壁上扫过。探头可由探头远端上的球囊或者其他可扩张元件来锚固,以及/或者通过配置用于非创伤性地接合诸如阴茎根部之类身体外部表面区域的外部锚固框来锚固,从而稳定探头以防近端变位和远端变位。通过在膀胱中如此锚固探头的远端,探头上的流体输送元件相对于膀胱颈的位置将会被精确限定,从而有助于将流体输送元件精确地定位在尿道内前列腺组织处。锚固件的使用特别有利,这是因为其允许在无内窥镜、荧光镜或其他成像的情况下进行本手术——尽管本手术也可以与成像技术结合使用。由锚固件所提供的设备稳定性还允许流体输送元件精确移动,而这转而有助于手术的自动化。流体输送元件通常将会被置于如下的腔或管的末端处,该腔或管穿过或越过探头并且允许流体输送元件相对于探头的轴进行平移和/或旋转。流体流可在其离开流体输送元件之后发散、汇聚或者保持恒定的横截面积。通常,流体输送元件将会以预定方式移动,以覆盖和治疗尿道周围柱形体积的前列腺组织。备选地,可以扫描流体输送元件以覆盖作为治疗靶标的尿道内非柱形并且可选地非对称的区域。通常,加压流体源将会包括动力泵,该动力泵可以被可控地驱动,以便经流体输送元件输送期望的压强。本发明还提供用于治疗前列腺的设备。此类设备包括具有近端和远端的细长元件(例如,轴杆)。诸如可膨胀球囊之类的可扩张锚固件在细长元件的远端处或者靠近该远端处紧固,用于将元件锚固在膀胱中,并且外部锚固框可以通过接合诸如阴茎根部之类的身体外部表面而提供额外的稳定性。至少一个流体输送元件耦合至细长元件,并且靠近锚固件而安设。流体输送元件可相对于细长元件移动,通常能够以相对于细长元件的轴向运动、旋转运动或者摆动运动而移动。可以以相对于细长元件的直角或法线角来引导流体,并且还可以以相对于细长元件的其他角度来引导流体。细长元件可包括一个或多个管腔,用于执行本发明的方案的附加部分。例如,可以提供管腔来向尿道输送加压气体或其他流体用于喷注尿道。可以提供其他管腔,用于从治疗区清除切除的碎屑、用于输送冲洗流体,等等。细长元件将会的尺寸适合经过尿道而被引入到前列腺。细长元件可包括用于输送在此关于本方法所讨论的包括激光能、射频能、热、冷等在内的任何能量源的装置。虽然本发明特别针对经尿道治疗前列腺,但是本发明的某些方面亦可用于治疗和改造诸如脑、心、肺、肠、眼、皮肤、肾、肝、胰腺、胃、子宫、卵巢、睾丸、膀胱、耳、鼻等其他器官,诸如骨髓、脂肪组织、肌肉、腺体组织、脊髓组织等软组织,诸如牙齿、骨骼等硬生物组织,以及诸如鼻窦、输尿管、结肠、食道、肺道、血管等体腔及通道。在此所披露的设备可以通过已存在的体腔插入,或者通过实体身体组织而插入。附图说明本发明具有其他优点和特征,这些优点和特征在以下结合附图对本发明的详细描述和随附权利要求中将会更容易理解,在附图中:图1是根据本发明原理适合用于尿道内前列腺组织减积术的设备的示意图。图2a-图2d图示了在进行前列腺组织减积术中使用图1的设备。图3图示了特定的前列腺组织治疗设备,其包括使用射频盐水等离子体进行前列腺组织减积术。图4图示了适合在本发明的设备中使用的能量源,其中该能量源输送流体流用于组织切除。图5图示了适合在本发明的设备中使用的能量源,其中该能量源包括偏转光波导用于向前列腺组织输送激光能。图6图示了与图5中所示设备类似的设备,区别在于光波导在横向偏转激光能的光镜处引导激光能。图7图示了适合在本发明的设备中使用的能量源,其中该能量源包括横向凸出电极,该电极可接合尿道壁及前列腺组织,以便输送射频能用于组织消融。图8是展现临界压强的组织切除速率的曲线图。图9a是选择性且受控的切除流程图。图9b是选择性切除的流程图,其中流体流被设置成在切除前列腺组织之前穿透尿道壁。图10a图示了柱状流体流和发散流体流。图10b图示了被设置成发射柱状流体流的组织改造设备的横截面图。图10c图示了被设置成发射发散流体流的组织改造设备的横截面图。图11是作为组织与流体输送元件之间距离的函数的,使用发散流体流的穿透时间曲线图。图12是作为压强和组织与流体输送元件之间的距离的函数的,由切除速率变化所显示的使用发散流体流的临界压强的曲线图。图13是作为压强和组织与流体输送元件之间的距离的函数的,腺体组织切除速率的曲线图。图14是腺体组织与囊组织的切除速率之比的曲线图。图15图示了使用流体流进行组织切除的组织改造设备,其中流体流可选地可以充当电磁能的管道。图16图示了置于尿道中的组织改造设备,其中组织与该设备的接触导致低效的设备操作。图17图示了如图16中所见的置于尿道中的组织改造设备,其中该设备使周围的组织扩张并且形成工作空间。图18是图示组织改造设备的操作流程图。具体实施方式虽然详细描述包含许多细节,但这些细节不应理解为对本发明的范围加以限制,而是仅仅说明本发明的不同示例和方面。应当明白,本发明的范围包括未在上文详细讨论的其他实施方式。在本文所披露的本发明的方法和装置的布置、操作和细节中可以做出本领域技术人员所显而易见的各种其他更改、改变和变动,而不偏离在此所述本发明的精神和范围。参照图1,根据本发明的原理构建的示例性前列腺组织减积设备10包括导管组装件,该导管组装件一般包括具有远端14和近端16的轴杆12。轴杆12通常将会是聚合物挤压件,其包括从近端16处的毂(hub)18延伸到远端14附近位置的一个、两个、三个、四个或者更多个轴向管腔。轴杆12一般将会具有范围从15cm到25cm的长度和范围从1mm到10mm——通常从2mm到6mm的直径。轴杆将会具有足够的柱强度,从而使其可以如以下更详细描述的那样向上经男性尿道引入。轴杆将会包括置于能量输送区域20中的能量源,其中能量源可以是如以下所更详细讨论的多种具体组件中的任何一种。位于能量输送区域远端的可膨胀锚固球囊24将会被置于轴杆的远端14处或者非常靠近该远端14。球囊将会通过多个轴向管腔中的一个连接至通过毂18连接的球囊膨胀源26。除了能量源22和球囊膨胀源26之外,毂可选地还将包括用于灌注/冲洗源28、吸引(真空)源30和/或喷注(加压co2或其他气体)源32的连接。在示例性实施方式中,灌注或冲洗源28可以通过(未示出的)轴向管腔连接至一个或多个输送端口34,所述端口34位于球囊锚固件24的近端和能量输送区域20的远端。吸引源30可以连接至通常位于能量输送区域20近端的第二端口或开口36,而喷注源32可以连接至通常也位于能量输送区域近端的附加端口38。应当明白,端口34、36和38的位置并不是关键的,尽管某些位置可能导致本文所述的特定优点,并且管腔和输送装置可由附加的导管、管等来提供,这些附加的导管、管等例如包括可位于轴杆12之上的同轴套筒、鞘套等。虽然本实施方式是参照人前列腺来描述的,但是应当理解,其可以通用地用于治疗哺乳动物前列腺。现参照图2a-图2d,前列腺组织减积设备10通过男性尿道u引入到位于紧贴膀胱b远端的前列腺p内的区域。在图2a中示出了解剖结构。一旦导管10已被定位成使得锚固球囊24位于紧靠膀胱颈bn的远端处(图2b),则球囊可以膨胀,优选地基本上占据整个膀胱内部,如图2c中所示。一旦锚固球囊24被膨胀,则前列腺组织减积设备10的位置将会固定和稳定在尿道u内,以便将能量输送区域20定位在前列腺p内。应当明白,能量输送区域20的正确定位仅依赖于锚固球囊24在膀胱内的膨胀。由于前列腺位于紧靠膀胱颈bn近端之处,因此通过将能量输送区域的远端置于非常靠近球囊的近端,通常在从0mm到5mm,优选地在从1mm到3mm的范围内,可以正确地定位输送区域。如图2中的箭头所示,在锚固球囊24已经膨胀之后,可以向前列腺中输送能量用于减积。如图2d中所示,一旦能量已在期望的表面区域上输送了一段时间,则可以停止能量区域,并且前列腺将会得到减积从而缓解尿道上的压力。此时,如图2d中所示,可以通过端口34输送冲洗流体,并将其吸入端口36。可选地,在治疗之后,可使用烧灼球囊和/或支架来烧灼该区域,所述烧灼球囊和/或支架可使用经改进的或单独的导管设备来放置。现将参照图3-图7,描述多个有代表性的能量输送区域。现参照图3,根据本发明原理而构建的第一示例性前列腺切除设备110包括轴杆112,该轴杆112具有近端114和远端116。多个喷嘴118安装在轴杆112上与远端116间隔开1cm到5cm的很短距离的位置处。喷嘴通常是能够生成等离子体的陶瓷芯或者是能够引导径向向外的导电流体流的端口,其可以安装到结构120上,这样允许喷嘴118径向地向外移动,如图3中的虚线所示。图示为可膨胀球囊的锚固件122安装在轴杆112的远端116上介于喷嘴118与远尖端124之间的位置处。如以下所更详细地描述,可扩张结构122将能够在膀胱内扩张以便锚固轴杆112,从而使喷嘴阵列118居于前列腺内。轴杆112将会包括管腔、通路、导电线等,以便从轴杆的近端114向远端116输送能量和物质。例如,rf能量源126将会连接至轴杆112,通常连接至喷嘴118,以便向从源128(通常经轴杆112内的管腔)输送到喷嘴118的导电流体输送rf能。将会提供其他管腔、通道或管道,以便允许通常连接至一个或多个吸引端口132的真空源130产生吸引。可以在轴杆112内提供其他管道,以便允许从源134向端口136引入冲洗流体,诸如盐水。在其他实例中,将会有可能把吸引源130和冲洗源134连接至公共端口,从而可以按顺序而非同时地进行吸引和冲洗。此外,可选地,可以提供内管腔、管道等,以便将喷注源140连接至轴杆上处于阵列118的区域中的一个或多个喷注端口142。最后,可以提供内管腔、管道等,用于将球囊122连接至球囊膨胀源144。如图4中所示,在安设于轴杆12内的输送管380上所承载的高压喷嘴200可以形成示例能量输送区域20。载携管380可以如箭头204所示地轴向平移以及/或者如箭头206所示地旋转,从而使从喷嘴200发出的流体流208可以在前列腺内尿道的所有部分或选定部分上扫过或掠过。此类高压水治疗的特定压强和其他细节例如在上述的jian和jiajun中有述。现参照图5,能量输送区域20内的能量源可以包括承载于旋转和平移轴杆380上的光纤波导或光纤束220。光波导220在光束222中传输激光或其他相干光能,该光束222可通过旋转和/或平移载携管380而在尿道壁和前列腺组织上扫过或掠过。如图6中所示,可以将来自光波导或光纤束230的激光能轴向地导向光镜232,其中波导和光镜全都被承载于旋转和轴向平移载携管380上。再一次地,通过旋转和/或平移载携管380,发出的光束234可以扫过或掠过尿道壁之上。现参照图7,在另一实施方式中,旋转和轴向平移管380可以承载电极240,该电极240从该管横向地凸出。电极240将会适配成连接射频能量源,从而使得当电极接触尿道壁和前列腺组织时,射频能可以在单极模式或者双极模式下得到输送。因此,射频能可以在选定体积和区域的前列腺组织上对组织进行消融。可选地,通过改变射频能的性质,电极240还可用于在组织已得到治疗后对其进行烧灼。在本发明的一个实施方式中,设备被设置成用于选择性地切除组织,从而造成一些组织成分的清除,而保持其他组织成分完好无损。例如,前列腺及附近区域包含多种组织成分,包括腺体前列腺组织、前列腺内血管、肌纤维间质、囊组织、括约肌、精囊等。当治疗bph或其他前列腺状况时,期望清除腺体前列腺组织并保持诸如血管和囊组织等其他组织基本上不受损伤。正如本文所指,术语“切除”旨在包括对组织的任何切除——包括对一团或多团组织细胞的清除,对组织细胞的部分清除,等等。通过选择性组织切除来治疗bph的一个优点在于减少对烧灼的需求(或者对其没有需求),这是因为对前列腺内血管存在很少的损伤或者不存在损伤,并且因此出血有限。另一优点在于降低失禁或阳痿的可能性,这是因为选择性切除降低了刺穿或以其他方式损伤诸如前列腺囊、括约肌、精囊等周围组织的风险。当使用流体流来切除组织时,通过改变流体流的一个或多个参数——诸如喷嘴或其他流体输送元件内的压强或者流体流中流体的流速,从而使其切除一些组织成分而保持其他组织成分基本上不受损伤,可以实现选择性组织切除。在一个实施方式中,可将流体流参数设置成即使当非靶组织长时间(即,通常是一段足以实现期望的切除的时间)暴露于流体流时,仍然保持这些组织基本上不受损伤。在另一实施方式中,可将流体流参数设置成以大大高于切除非靶组织的速率来切除靶组织,从而限制对非靶组织的损伤。此类参数可根据所要选择性切除的靶组织来调节。在一个实施方式中,切除速率被设置成对于腺体组织比对于非腺体组织更高。可以通过更改流体的压强,或者通过如上所述地调节其他流体参数来设置切除速率。特别是,针对腺体组织的切除速率可被设置成显著高于针对非腺体组织的切除速率,从而有效地保持非腺体组织在治疗期间不受损伤。例如,腺体组织的切除速率可被设置成高达针对非腺体组织的切除速率的至少两倍。作为另一示例,针对腺体组织的切除速率可被设置成高达针对非腺体组织的切除速率的至少10倍。应当注意,组织切除具有临界压强(低于该压强,组织不会被切除;而高于该压强,组织会被切除),这是因为清除过程涉及对组织的撕裂,其中将组织在微观尺度上拉伸到使组织基质破裂或撕裂的程度。由于组织是有弹性的,因此将会存在临界断裂点。不同类型的组织将会具有不同的临界断裂点,并因此具有与其相关联的不同的临界压强。实际上,给定具体的流体输送元件大小(诸如喷嘴直径),每种组织类型通常具有流体流源的临界压强(下文亦称为pcrit)——低于该压强,切除速率趋近于零,而高于该压强,切除速率一般单调增大,并且有可能呈指数增大。特别地,由于组织成分的差异,可将流体流源的压强设置用于选择性地切除特定类型的组织,而保持具有更高临界压强的其他组织类型基本不受损伤。根据本实施方式在多组织环境中切除组织的一个重要方面在于,有可能以一种组织类型被切除而另一组织类型保持基本上不受损伤的方案进行操作。这最强烈地发生在以介于两种组织类型的临界压强之间的压强进行操作之时。如图8中所见,流体流的操作压强po可被设置成大于组织1的临界压强(po>pcrit1)从而使组织1经受大于零的切除速率,同时保持压强po小于组织2的临界压强(po<pcrit2)从而使组织2经受基本上接近于零的切除速率。在这样的设置中,将流体流称为被设置用于选择性地切除组织1而不是切除组织2。在设置成用于治疗bph的一个实施方式中,将流体流源压强设置成高于腺体前列腺组织的临界压强但低于非腺体前列腺组织的临界压强。在这样的实施方式中,压强高至足以切除腺体组织,但对于实质上切除或损伤诸如前列腺内血管、肌纤维间质、囊组织等非腺体组织而言则过低。在一个实施方式中,流体在离开流体输送元件之前被加压至大约1-30000磅/平方英寸(psi)范围内的压强,更优选地加压至大约50-1500psi范围内的压强,并且最优选地加压至大约100-1000psi范围内的压强。以下实施例说明了针对流体流切除的一些组织临界压强。应当注意,以下设置作为示例而提供,而不应理解为具有限制性。实施例1:不同肾脏组织成分的示例性临界压强。在猪肾脏中测量了组织临界压强。选择肾脏组织是因为其组成类似于前列腺组织。使用了直径约为200微米的柱状流体流来进行组织切除。腺体组织(肾脏的粉色外围部分)非常软,并且很容易用手指的压力撕裂,而肾脏的内部包含更坚韧的血管组织。据发现,该流体流对于腺体组织的临界压强为大约80psi,而对于血管组织则为大约500psi,如以下的表1中所见。组织pcrit(psi)腺体80血管500表1:猪肾脏中腺体组织和血管组织的不同临界压强例如,实验表明,当使用直径约200微米的喷嘴以大约500psi的液体源压强来切除猪肾脏时,在10cm2面积上的切除速率对于腺体组织为大约每30秒1cm(即,每30秒清除10cc),而对于血管组织则为大约每180秒0.1cm,这是大约6倍的切除速率差异。因此,在相同的切除时间段中,将会有比血管组织更多的腺体组织得到切除。藉此,可将切除时间段设置成允许在不会明显地损伤血管组织的情况下对腺体组织的切除。切除的速率可通过改变流体源压强和/或喷嘴大小而得到调节。例如,可以将针对腺体组织的切除速率调节成大约每分钟1cc、每分钟5cc、每分钟10cc、每分钟30cc,或者其他速率。如上所述,在此应当理解,改变喷嘴的大小可能使改变流体源压强成为必需,以便导致流体流以足够的力量撞击在组织上,从而实现期望的切除速率。图9a是根据一个实施方式、用于选择性前列腺切除的方法流程图。在步骤700处,如上文所述地将设备定位和锚固在尿道中。在步骤701处,对诸如流体源的压强、流体流的形状等各种流体参数进行设置以便切除诸如腺体前列腺组织等特定组织类型。通过设置流体参数,可以控制流体的力度、切除速率、治疗时间、要切除的组织面积等,以便实现受控和选择性的切除。在设置了参数之后,在步骤702处,对设备进行设置以排放出流体流来切除靶组织。在步骤703处,如果确定治疗已完成,则在步骤704处将设备从尿道u撤出。然而,如果在步骤703处确定治疗尚未完成,则可以如步骤701中所述那样,根据需要来重新设置流体参数,并且重复步骤循环直到治疗完成。特别地,在其中期望针对完整的治疗而切除两种不同类型组织的实施方式中,流体参数的重新设置是有利的。在这样的实施方式中,可以调节流体参数以顾及所要切除的靶组织类型的变化。通常,在已切除一些或所有的腺体组织之后,诸如血管组织或囊组织等其他组织类型将会暴露于流体流。虽然流体流参数被设置成用于选择性地切除腺体组织,但是还考虑到可在切除手术期间动态地调节流体参数,以便顾及非腺体组织的逐渐暴露以及根据需要而对切除选择性进行微调。在步骤701处如此重新设置了流体参数之后,继而在步骤702处发射经重新设置的流体流以便继续进行组织切除,并且该操作继续,直到治疗完成。特别地,应当注意,当从尿道内治疗前列腺时,尿道壁介于流体流的源(诸如喷嘴或其他流体输送元件)与要切除的靶腺体前列腺组织之间。因此,在一个实施方式中,将流体流参数初始设置成用于切除和穿透尿道组织的一部分(例如,尿道壁)。然而,由于腺体前列腺组织的成分比尿道组织的成分要薄弱,因此期望避免使用与用来切除尿道壁的力相同的流体流力来切除腺体组织。为了做到这一点,可以在足以切除和穿透尿道壁的一段时间,而不是更长时间中使用流体流。此后,可以使用强度降低的流体流来切除腺体前列腺组织。图9b是根据一个实施方式、用于选择性前列腺切除的方法流程图,其中流体流被设置成用于首先穿透和切除尿道壁。在步骤801处,如上文所述那样将设备定位和锚固在尿道中。在步骤802处,对设备进行设置,以便排放出足够有力的流体流来切除和穿透尿道壁。在步骤803处,在流体流已穿透尿道壁之后,将流体流调节至选择性地切除期望的前列腺组织而保持前列腺内血管、囊以及其他非腺体组织基本上不受损伤的水平。另外,考虑到流体流的形状也影响到选择性切除。虽然在图10a中将流体流示例性地示为柱状流体流333或者发散流体流334,但还考虑到流体流可以是允许根据本实施方式进行切除的任何形状或设置。特别地,如将在下文进一步描述,对于柱状流体流设置和发散流体流设置而言,存在多种优点。在柱状流体流配置333中,设备将流体流发射成发散角基本上为零的基本上聚焦的棒状流体柱。在一个实施方式中,将柱状流体流配置成总体上笔直或不发散的流体流。在这样的配置中,设备基本上将流体流发射成筒状或其他不发散的形状,从而在很大程度上在与流体输送元件和组织之间距离无关的面积或斑点大小上向组织传输能量。可选地,可以例如在流体输送元件包括多个喷嘴时或者在流体包含气泡时调节流体流以使其汇聚,以便使输送到组织的能量集中。图10b示出了发射柱状流体流以改造诸如前列腺等组织的设备的横截面图。设备的细长元件310(诸如上文所述的轴杆)被放置在尿道u内。放置在细长元件310内的载携管(未示出)上的流体输送元件320被设置成发射柱状流体流333。如本文所理解的,流体输送元件320可以包括如上文所述的喷嘴,或者设置用以发射流体的任何其他元件。柱状流体流333被设置成在切除区ra内切除组织,诸如尿道壁uw和前列腺组织p。柱状流体流设置的一个特性是:由于切除区ra的宽度基本上与距离流体输送元件320的距离无关,因此切除区ra在距流体输送元件320的一段距离内保持基本恒定。这样是有利的,因为当流体流333离开流体输送元件320时,切除区ra保持集中和恒定,从而以集中的面积向组织传输能量。当切除或穿透诸如尿道壁uw等坚韧组织时,能量聚集在集中的切除区ra内特别有利。在一个实施方式中,可以通过在流体输送中引入压强波动而改变流体流的柱形。例如,可以通过在流体输送路径中——诸如在流体输送元件320的孔隙之后或者在流体流离开流体输送元件320孔隙之后的路径中——机械地和可控地引入大致坚实的物体,来改变流体流的柱形。在另一示例中,可以通过在流体路径中引入诸如压电元件等振动元件以形成压强波动,来改变流体流的柱形。在另一实施方式中,将流体流配置成如图10a中所见的发散流体流334。发散流体流334是这样的:在其中,流体离开诸如流体输送元件320之类的流体流源,并基本上以锥形发散,其中锥体的尖端处于流体流源。发散流体流334的切除速率可以表示成从发射流体的流体输送元件320到要切除的组织的距离z的函数。如图10a中所示,z2比z1更加远离孔口,并且因此,在z1处的切除速率高于在z2处的切除速率。发散流体流334可由流体流的发散角来加以表征。在一个实施方式中,将发散角配置成约0-90度,优选地约2-45度,更优选地约4-20度,并且最优选地约7度,同时还考虑到可以根据需要来改变发散角。另外,发散流体流334可由流体流的横截面形状来加以表征。一般而言,距流体流源(例如,流体输送元件320)的距离越远发散流体流334的横截面积或斑点面积越大,从而成比例地减小流体流在每单位面积上的力。斑点面积的这种增大一般导致靠近流体流源组织的切除速率更大。在一个实施方式中,将发散流体流334的横截面形状配置成大体上为窄矩形(以产生扇形流体流)。在另一实施方式中,将发散流体流334的横截面形状配置成大体上为圆形(以产生锥形流体流),其中最小横截面积位于流体流源。应当注意,发散流体流334的横截面形状可以被设置成封闭非零面积的任何形状(例如,椭圆形或者不规则形状)。图10c示出了发射发散流体流以改造诸如前列腺等组织的设备的横截面视图。设备的细长元件310放置在尿道u内。安设在细长元件310内的载携管(未示出)上的流体输送元件320被设置成发射发散的流体流334。发散流体流334被设置成在切除区ra内切除诸如尿道壁uw和前列腺组织p等组织。由发散流体流334所覆盖的切除区ra随着流体流远离流体输送元件320而增大,从而成比例地降低每单位面积的流体流强度。发散流体流334的特性在于,切除宽度作为从流体输送元件320起的距离的函数而增大,同时每单位面积的切除速率作为从流体输送元件320起的距离的函数而降低。这是因为在流体流中输送的总能量总体上是恒定的(不考虑流体速度的任何减小),但能量却被输送到更大的面积上。因此,每单位面积所输送的能量减少,这是切除速率所依赖于的关键参数。因而,每单位面积的切除速率作为距离的函数而降低。此外,在发散流体流334中,切除的体积速率可以作为距离的函数而基本上恒定。亦即,尽管每单位面积的切除速率降低,但所切除的总面积成比例地增大,因而总切除体积基本上保持不变。应当注意,如果作为面积能量密度的函数的切除面积速率是非线性的并且随能量单调地增大,则切除的体积速率将会作为从流体输送元件320起的距离的函数而降低。还应当注意,流体流粒子(例如,液滴)的任何减速也将使体积切除速率作为距离的函数而降低。以下实施例说明了使用发散流体流进行的组织切除。应当注意,以下设置是作为示例提供的,而不应被理解为限制性的。实施例2:使用发散流体流进行的前列腺穿透。在图11中示出了与切除犬前列腺囊组织有关的测量数据。穿过囊的穿透时间是作为组织与流体输送元件之间距离的函数而测量的。流体流的发散角大约为7度。穿透时间标绘成用以穿透囊的时间,其中囊具有小于1mm的厚度。图11示出了穿透时间随着组织与流体输送元件之间的距离增大而增加。应当注意,该效应在较低的流体源压强下更强。还应当注意,柱状流体流的穿透时间一般与组织与流体输送单元之间的距离无关。实施例3:使用发散流体流的临界压强和前列腺组织切除。在图12中示出了在犬前列腺囊组织上测量的、在发散流体流切除中临界压强作为不同距离的函数的变化。切除速率作为切除(即,穿透)囊的整个厚度所用时间的倒数而测量。切除速率作为流体源压强以及组织与流体输送元件之间距离的函数而测量。切除速率在距流体输送元件更大的距离和更高的压强下增大。切除速率的这种增大指示出临界压强。临界压强作为距离的函数的增大显示,在发散流体流中切除有效性随距离增大而减小。图13图示了作为源压强以及组织与流体输送元件之间距离的函数的、发散流体流对犬腺体组织的切除速率。在临界压强(大约300psi)之上,在靶组织较靠近流体输送元件时对压强变化的敏感性较大。这有助于选择性地切除腺体组织而保留囊组织,因为可以使用较高的压强来切除流体输送元件附近的腺体组织,而保留处于离流体输送元件更远距离处的囊组织。在图14中将两种不同组织的切除相对速率示为腺体组织切除速率与囊组织切除速率之比。如图14中所见,在中间压强(大约500psi)下存在明显的最大比率。这指示出如上所述地在两个临界压强之间操作,并且示出选择性组织切除可通过设置适当的压强范围来实现。实施例4:使用发散流体流切除的临界距离。如下表中所示,对于给定压强,当进行发散流体流切除时,还存在临界切除距离。如表2中所见,当流体流距离组织大约10mm以上时,不发生发散流体流对犬膀胱的穿透,这进一步说明了出于选择性切除目的而使用发散流体流的优点。表2:使用发散流体流的犬膀胱切除本发明的一个有利方面在于,其允许切除诸如前列腺组织等组织,而无需在切除之前消融、弱化、机械地改变或者以其他方式处理组织。虽然可以进行诸如组织消融之类的处理,主要通过将靶组织从身体区域的组织基质分离来弱化靶组织,并从而允许使用较低强度的流体流而容易地清除经预处理的组织,但此类处理需要两步过程(弱化组织,随后将经弱化的组织从组织基质分离),并且可能导致诸如炎症加重等不期望的不良副作用。因此,一个有利方面在于,本发明允许使用流体流来进行靶组织的切除而无需预先消融、改造或处理组织。如上所述,可以使用流体喷注尿道腔,以便在将能量导向前列腺组织之前或当中形成工作空间。图15示出了配置用于喷注和切除组织的示例性组织改造设备。封闭组织系统内的组织改造所固有的一个挑战是,在组织改造设备与身体区域的周围组织之间缺乏足够的工作空间。此类工作空间的存在是有利的,因为其将会帮助提高能量传输效率、实现碎屑产物的有效清除、以及使组织区域更好的可视化,以及其他优点。在下文中更加详细地描述了用于通过形成工作空间和利用工作空间来进行组织改造的设备和方法,以及此类设备和方法的优点。虽然以下实施方式是在前列腺治疗的背景下示例性描述的,但是还考虑到本发明可以用于改造如下封闭组织系统内的任何组织:在该组织系统中,一个组织或解剖结构大幅度侵犯或挤压另一组织或解剖结构,并且其中在组织改造之前形成工作空间是有利的。现参照图15,设备包括细长元件310,诸如轴杆,被设置成插入到身体区域之中。细长元件310包括暴露出载携管380和以下所述其他组件的窗口。该窗口展露出载携管380和安设在载携管380上的高压流体输送元件320。流体输送元件320经由流体管腔390连接至流体源(未示出),所述流体管腔390将流体从源输送到流体输送元件320。可选地,当经过尿道引入细长元件310时,可通过鞘套或其他遮蔽物(未示出)来覆盖细长元件310。当完全用鞘套覆盖时,该窗口得到保护,从而减少了在细长元件310推进时对尿道的刮擦和损伤。一旦就位,则收回鞘套,从而暴露出窗口。继而可以旋转以及推进和/或收回载携管380,以便通过流体输送元件320输送流体。附加地或可选地,该设备可以包括遮蔽元件(未示出),该元件被定位成基本上覆盖流体输送元件320,同时在流体输送元件320与遮蔽元件之间保持空间。这反过来有效地在流体输送元件320与可能撞击遮蔽元件的任何组织之间保持该空间。在一个实施方式中,遮蔽元件是置于流体输送元件320之上的基本上平坦的片状元件。遮蔽元件被定位或塑形成使其允许载携管380根据需要而在细长元件310内移动。例如,遮蔽元件可以是弯曲的,以遵循载携管380的曲率。遮蔽元件包括开口,使流体输送元件320所发射的流体流通畅地穿越该开口并撞击在组织上。开口可以是圆形,或者其可以包括其他形状。此类遮蔽元件的一个优点在于,其保护流体输送元件320在插入或移除程序期间以及/或者在治疗期间免遭损坏。遮蔽元件的另一优点在于,在流体发射期间或在此之后,向流体输送元件320返回的流体可以穿越遮蔽元件开口(或者通过遮蔽元件周围的其他路径)并进入遮蔽元件与流体输送元件320之间的空间。继而,可将这样的返回流体引导出该空间,以使得流体发射不被这样的返回流体所阻塞或阻碍。遮蔽元件还可被配置成使得遮蔽元件与流体输送元件320之间的空间经由低流阻流体路径而持续地与废物处置腔相连通。这在流体输送元件320与此类废物的外部目的地之间形成了低流阻路径,从而使离开流体输送元件320的废物和流体可以容易地离开流体输送元件320周围的区域。在这种情况下,低阻力应当理解为与流体输送元件320的流阻相比较低的流阻。这种配置有利地防止在流体输送元件320处产生回压,否则该回压会减小流动,并从而允许由流体输送元件320所发射的流体流基本上不受废物和返回流体干扰。流体输送元件320可以是单一喷嘴、多个喷嘴,或者是各种配置的喷嘴阵列。流体输送元件320被设置成以足够的力量将流体作为流体流331径向向外地发射出,以便在流体流331与组织相接触时切除组织。流体流331可以垂直于细长元件310,或者其可以被设置成相对于细长元件310的各种角度。载携管380可相对于细长元件310轴向平移、旋转、摆动或者旋转摆动,从而使流体流331可以扫过或掠过期望的组织面积或体积以进行切除。期望的面积或体积可以是球形、柱形,或者是任意形状和尺寸的任何其他预定面积或体积。附加地并且可选地,当设备不用于切除组织时,可将载携管380定位成使得流体输送元件320和/或任何其他元件(诸如可视化元件或者烧灼元件)远离窗口,从而降低此类元件的损坏风险,以及降低任何意外切除组织的风险。设备还包括安设在细长元件310上的至少一个喷注端口340。喷注端口340经由一个或多个管腔而连接至喷注源(未示出),其中该喷注源通过喷注端口340将流体330输送到身体区域之中,以便扩张周围组织和形成工作空间。设备还包括至少一个清除端口360,用于清除碎屑产物,诸如切除产物、切除流体、其他废弃产物或者其混合物。细长元件310可以包括管腔、通路、导电线等,被设置成从细长元件310的近端向远端输送能量,以及/或者用于清除碎屑和废弃产物,其详情在上文有述。可选地,除了流体输送元件320之外,设备可以包括电磁能输送端口350,该端口350安设在载携管380上并且位于流体输送元件320之中或附近。如也在上文中更详细描述地那样,电磁能332依靠一个或多个管道351——诸如载携管380和细长元件310内的光纤或其他波导——而被输送到能量输送端口350。电磁能332可以是射频能、相干光或非相干光、或者任何其他形态的电磁能。能量输送端口350被设置成通过流体流331的内部来输送能量332,从而使电磁能332可以代替流体切除或者与流体切除相结合地对组织进行切除。附加地并且可选地,上述各种电磁能形态可以被设置成与组织切除相结合,或者独立于组织切除而烧灼组织。由于本文所披露的选择性组织切除一般会对诸如血管组织等其余组织造成很小的损伤或者不造成损伤,并且从而造成有限的出血或者不造成出血,因此倘若需要这样的烧灼的话,也只需在有限的基础上对其加以使用。当通过流体流331将电磁能输送到组织用于烧灼时,可将流体源压强调节成大体上低于针对组织切除的临界压强,从而不切除额外的组织。备选地或附加地,烧灼可以使用其他方式来实现,举例而言,使用如上所述的使用导管设备放置成与组织相接触的烧灼球囊和/或支架。此外,设备可以包括可选的偏转元件,其例如被置于窗口内部或细长元件310内并且远离窗口,偏转元件被设置成将流体输送元件320所发射的流体朝向流体输送元件320偏转回来,从而清除在组织切除期间可能堆积在流体输送元件320和/或能量输送端口350上的任何碎屑。此外,流体输送元件320与偏转元件相结合,可以被设置成清洁基本上整个的流体输送元件320、任何可视化元件或烧灼元件和/或载携管380,或者清洁其一部分。偏转元件可以被设置成基本上是平坦的或者凹面的。备选地,偏转元件可被设置成任何形状或设计。另外,偏转元件可以被设置成起到针对流体输送元件的保护元件的作用。流体输送元件可以被置于相对于保护元件的特定位置,该保护元件保护前列腺免遭意外流体发射,并且例如保护流体输送元件320免遭组织的堵塞或阻塞,特别是在插入身体和从身体移除时尤为如此。现参照图16,示出了插入到身体区域之中的组织改造设备。身体区域示例性地图示为前列腺-尿道区域pu。由于诸如bph等异常或者其他组织特性,设备可能被周围组织t所阻塞,这使得治疗复杂化。如图16中所示,在已将细长元件310引入尿道中之后,周围组织t可能阻塞流体输送元件320并且阻止载携管380相对于细长元件310正常地轴向平移、旋转、摆动或者旋转摆动。如图17中所见,为了解决这个缺点,设备被设置成对周围组织t加以扩张,从而形成工作空间ws,在该工作空间ws中设备可以使用流体流311来切除组织t。周围组织t的扩张可以通过多种方式来实现。在一个实施方式中,设备被设置成通过喷注端口340输送第一流体330而扩张周围组织t。流体330接触并扩张周围组织t,藉此在载携管380和流体输送元件320周围形成工作空间ws。在另一实施方式中,设备被设置成通过机械方式来扩张周围组织t。在一个此类实施方式中,可将一个或多个支架或机械结构安设在细长元件310上并且在身体区域内扩张。可以通过使用一个或多个膨胀球囊,或者通过对支架进行配置以使支架从受限空间释放后展现出扩张形状的记忆效应(诸如镍钛记忆合金支架),来实现扩张。备选地,如本领域中技术人员应当知晓,支架可以通过其他方式来扩张。在又一实施方式中,使用安设在细长元件310上的一个或多个膨胀球囊来扩张周围组织t。可以通过诸如气体或液体等流体来使球囊膨胀。可以考虑使用在身体区域中形成工作空间ws可以包括扩张周围组织t、拉伸周围组织t、重新定位周围组织t、展开周围组织t以及/或者在身体区域内形成工作空间ws的任何其他方式。一旦工作空间ws形成,载携管380就可以相对于细长元件310轴向平移、旋转、摆动或者旋转摆动,并且在流体输送元件320不再被周围组织t所堵塞的情况下在工作空间ws内不受阻碍。此时,设备可以输送第二流体331作为流体流来有效地开始治疗,以便切除周围组织t。如下文将更详细描述,让流体330和331成为不同的介质具有多个优点。在一个示例实施方式中,用于扩张组织和形成工作空间ws的第一流体330是气体,诸如加压的co2、co、n2、he、ar、其他生物相容性气体或者它们的组合。用于切除组织的第二流体331是液体,诸如水、盐水、其他生物相容性液体或者它们的组合。附加地并且可选地,第二流体331可包括一种或多种可溶性物质,诸如氯化钠或者硫酸钡。使用此类可溶性物质的一个优点在于,其通过向第二流体301添加腐蚀性能力而提高了切除效率。实际上,根据存在于第二流体301中的可溶性物质的浓度,提高切除效率可使切除所必需的流体压强降低。使用此类可溶性物质的另一优点在于,它们可以帮助防止或减少出血。备选地并且可选地,第二流体331一般还可以包括晶粒,所述晶粒可以提高切除效率以及使切除所必需的流体压强降低。在一个实施方式中,晶粒可以是钙、镁、铝、锰、铁、镍、铜、锌、锶、钡、铋、铬、钒、镧、它们的盐或者它们的组合。在另一实施方式中,晶粒可以是阳离子盐,诸如甲酸盐、富马酸盐、乙酸盐、丙酸盐、丁酸盐、辛酸盐、戊酸盐、乳酸盐、柠檬酸盐、苹果酸盐、葡糖酸盐、氯化物、钾盐、磷酸盐或者它们的组合。在又一实施方式中,晶粒可以是柠檬酸钙、酒石酸钙、丁二酸钙、富马酸钙、己二酸钙、苹果酸钙、乳酸钙、葡萄糖酸钙、二水磷酸氢二钙、二磷酸钙、无水磷酸氢二钙、氯化钙、一水合乙酸钙或者它们的组合。此外,晶粒可以是任何固体颗粒。晶粒可具有至少30天、至少10天、至少1天、至少1分钟、至少10秒或者至少1秒的寿命。此外,晶粒的尺寸可以小于流体输送元件320的孔隙的尺寸,从而使颗粒小至足以穿过流体输送元件320。另外,可将颗粒设置成足够小,以使得流体输送元件320不被阻塞或堵塞。为了实现这一点,颗粒的最大尺寸一般可以是流体输送元件的一个开口或多个开口的最小尺寸的分数,其中该分数优选地处于大约1/10至1/2的范围中。在一个实施方式中,晶粒的最大尺寸一般小于流体输送元件320的孔隙的最小尺寸的1/2。在另一实施方式中,晶粒的最大尺寸一般小于流体输送元件320的孔隙的最小尺寸的1/4。在又一实施方式中,晶粒的最大尺寸一般小于流体输送元件320的孔隙的最小尺寸的1/10。另外,第二流体331可包括一种或多种溶解气体,以便提高切除的效率。此类溶解气体可以包括co2、co、n2、he、ar、其他生物相容性气体或者它们的组合。在一个实施方式中,将设备设置成使得在第二流体331从流体输送元件320的发射之后但在流体331抵达组织之前形成气泡。在另一实施方式中,将设备设置成使得在第二流体331碰撞组织时在其中形成气泡。设备可以被设置成使用此类效应的组合——其中一些气泡在碰撞之前形成,而另一些气泡在碰撞时形成。可选地,第二流体331的温度可以被设置成显著低于组织温度,以便造成血管收缩并从而减少或抑制出血。另外,第二流体331的温度可被设置成具有升高的温度,例如具有足够的升高以便协助切除或烧灼。被配置成气体的第一流体330的压强处于约0.1-5.0psi的范围内,优选地处于约0.5-2.5psi的范围内。可选地,可以提供压强传感器来监控第一流体330的压强,以便使压强可以保持在期望的范围内。还可以使被配置成液体的第二流体的源压强处于约1-2000psi的范围内,更优选地处于约50-1500psi的范围内,而最优选地处于约100-1000psi的范围内。可选地,喷注端口340可以被安设在细长元件310上十分靠近流体输送元件320之处。在这样的配置中,通过喷注端口340输送到工作空间ws中的一些第一流体(例如,气体)330被包含第二流体(例如,液体)331的流体流向外带出,以便在切除流体流周围形成包封,从而帮助保持流体流的完整性。喷注端口340靠近流体输送元件320还可以保护流体输送元件320免遭流体和组织的堆积,从而维持流体流的完整性。图18为图示设备的示例操作的流程图。在步骤1101处,将细长元件310引入到诸如前列腺-尿道区域pu等身体区域中。在步骤1102处,将细长元件310操纵就位并接合锚固元件(未示出),以便在手术的剩余过程中稳定细长元件310。锚固元件可以包括锚固球囊和/或外部锚固框,其中锚固球囊和外部锚固框被设置成通过将细长元件310稳定在治疗区域内而基本上防止细长元件310的近端变位和远端变位。锚固球囊被设置成紧靠膀胱颈的远端膨胀。锚固球囊可以膨胀以占据膀胱的足够部分,以便防止细长元件310在手术期间(在远离膀胱的方向上)显著移动超出治疗区域。锚固球囊的膨胀可通过上述各种方式来实现。备选地,可将其他扩张结构,诸如镍钛记忆合金半拱支架等,代替球囊用作锚固元件。外部锚固框被配置用于接合身体外部表面区域,例如,阴茎根部的表面区域。外部锚固框通常包括用于接合身体外部表面区域的非创伤性环。在一个实施方式中,一旦已将细长元件310引入治疗区域之中并扩张锚固球囊占据膀胱的一部分,则外部锚固框自动地或手动地在阴茎上同轴推进,从而使非创伤性环在阴茎根部接合身体外部表面区域。一旦外部锚固框接合了身体外部表面区域,就防止了细长元件310(在朝向膀胱的方向上)显著移动超出治疗区域。锚固元件,包括锚固球囊和外部锚固框在内,被配置用于通过使细长元件310基本上被压缩在治疗区域内而防止其近端和远端变位超出治疗区域,以次来稳定细长元件310。由锚固元件所提供的设备稳定性还允许流体输送元件的精确移动,而这转而有助于治疗过程的自动化。有利地,应注意到,在被配置成与球囊相结合地使用外部锚固框的此类实施方式中,球囊无需基本上填充整个膀胱来稳定设备,这是因为使球囊膨胀填充膀胱的一部分就可以提供足够的稳定。锚固过程还在共同待决专利申请公开号2009/0227998中有述。在步骤1103处,可以在细长元件310被稳定在其位置之后将细长元件310上的窗口遮盖收回,以便展露喷注端口340、清除端口360和载携管380。在步骤1104处,喷注端口340向身体区域中输送第一流体330并造成周围组织t扩张,从而形成工作空间ws。在步骤1105处,流体输送元件320输送第二流体331作为流体流,以便在工作空间ws内切除周围组织t。如上文所述,使第一流体330和第二流体331是不同的介质具有多种优点。例如,当扩张流体330是粘度低于切除流体331的介质时,使用第二流体331切除组织所需的流体源压强或流速小于使用与第二流体331相同(或粘度更高的)的介质填充工作空间ws时的情况。这是因为,如果第二流体331要行进穿过填充有相同或更高粘度介质的第一流体330的工作空间ws时,则第二流体331在抵达靶组织之前将需要在工作空间ws中克服更大的阻力。双介质实施方式的另一优点与流体流的完整性有关。在工作空间ws中的第一流体330与包含第二流体331的流体流之间的摩擦或阻力致使第二流体331的一部分从流中分散出来,而导致流体流逐渐丧失其结构完整性。这样的分散可能是不期望的,因为遭受显著分散的流体流到达周围组织t时可能切除有效性已经降低,并且可能由于切除准确性降低而额外地导致对周围健康组织的损伤。为了在这样的高阻力工作空间ws中保持流体流完整性,将必须向流体331施加增大的压强,以力图抵消流体分散的速率。与此相反,通过利用介质粘度更低的第一流体(例如,气体)形成包含介质粘度比流体流331低的第一流体(例如,气体)的工作空间ws,可以在保持足够的流体流完整性和切除有效性的同时,对流体流331使用较低的源压强或流速配置。备选地,可以设置第一流体330与第二流体331之间的阻力以便分散流体流,从而使得在远离流体输送元件320的期望距离处减小切除力。可以调节第一流体330(例如,调节气体的压强),以便以期望的方式对分散影响切除速率的距离加以配置。双介质实施方式的又一优点与两种介质的折射率的差异有关。在可选实施方式中,在步骤1105处,可经流体流的内部输送电磁能332,用以烧灼组织、切除组织或者用于其组合。在这样的实施方式中,切除流体流充当电磁能传输的管道,并且可以设置工作空间ws中的流体与切除流体流之间的折射率差异,来允许在切除流体流的内部之中实现更高效的能量传导。还考虑到,当流体流充当用于电磁能传输的管道时,可将其设置成具有足以向组织传输能量而又不足以切除组织的流和力。具体而言,当第一流体330的折射率被设置成小于第二流体331的折射率时(例如,分别为气体和液体时),可在流体流内实现全内反射或近全内反射。在此类设置中,会有更多经流体流行进的电磁能在期望的位置抵达靶组织,而更少的电磁能有可能会向工作空间ws中扩散出去。因此,作为传导效率提高的结果,可以在保持烧灼和/或消融有效性的同时减少源处的电磁能332的量,从而降低设备的功耗以及降低对患者的任何有害辐射效应。本发明所考虑使用的电磁能类型包括射频能和光能,诸如相干光(例如,激光能)或者非相干光。在步骤1106处,通过清除端口360将切除碎屑产物(连同用于切除的流体)从工作空间ws清除。在一个实施方式中,可以通过在清除端口360与喷注端口340之间形成正压差以使碎屑产物行进穿过清除端口360并从而得到清除,来经清除端口360清除碎屑产物。在另一实施方式中,可以通过向清除端口360附接真空源并向工作空间ws施加抽吸,来实现清除。可选地,可以使用所述两种清除方法的组合。上述步骤1103、1104、1105和1106可以彼此同时地实施。例如,步骤1105中所述的组织切除可以与步骤1106中所述的碎屑产物清除同时地进行。可选地,可以通过在扩张的工作空间ws内提供可视化元件而使治疗可视化。此类可视化元件可以包括内窥相机或者其他合适的可视化元件。在一个实施方式中,可视化元件可以安设在细长元件310上或者安设在载携管380上。在另一实施方式中,可视化元件可以单独地插入到工作空间ws中。附加地并且可选地,可以在治疗期间持续向身体区域中输送第一流体330以维持工作空间ws。此外,当在第一流体330输送之前就已经有足够的工作空间ws存在于身体区域中时,可以向身体区域中输送第一流体330以维持这样的工作空间ws。本实施方式还考虑到,可将第二流体331与治疗剂相结合,来治疗周围组织t。可以利用治疗剂来最小化患者不适和出血,以及/或者提供对癌症、前列腺炎或者其他疾病的局部治疗。治疗剂可以包括可溶性物质,诸如盐(例如,上文所描述的盐)、抗生素、凝结剂、麻醉剂、血管收缩剂、抗炎剂、化疗剂、抗癌剂、其他添加剂或药物,或者它们的组合。另外,治疗剂可以是固定剂,诸如戊二醛,用于收缩组织t,以便使出血最小化。应当注意,戊二醛还可通过造成组织紧缩和尿道腔增大而帮助增大工作空间ws。治疗剂可以在组织切除期间、在组织切除之前、在组织切除之后、或者独立于组织切除而输送到组织t。当治疗剂在切除期间输送至组织t时,可以使用具有如上所述压强配置的第二流体331。当治疗剂在组织切除之前和/或之后或者独立于组织切除而输送至组织t以便灌洗工作空间ws时,可将第二流体331的压强调节至低于切除组织t所需的临界压强。在这样的实施方式中,在组织切除之前和/或之后的第二流体源的压强可以处于约1-50psi的范围内,或者备选地小于约10psi。备选地并且可选地,可以使用对组织t损伤最小而将药剂有效地注入组织t的、高于临界压强的第二流体331的短脉冲发射,来将治疗剂输送到组织t。根据期望的治疗,可以设置此类发射的强度,使得药剂注入到组织t中的适当深度。虽然已主要参考经尿道治疗前列腺而描述了本实施方式,但是还可使用实施方式的某些方面来治疗和改造诸如脑、心、肺、肠、眼、皮肤、肾、肝、胰腺、胃、子宫、卵巢、睾丸、膀胱、耳、鼻等其他器官,诸如骨髓、脂肪组织、肌肉、腺体组织、脊髓组织等软组织,诸如牙齿、骨骼等硬生物组织,以及诸如鼻窦、输尿管、结肠、食道、肺道、血管等体腔及通道。本文所披露的设备可以通过已存在的体腔插入,或者通过实体身体组织而插入。虽然以上是对本发明优选实施方式的完整描述,但也可以使用各种替代、修改和等同物。因此,以上描述不应认为是对本发明范围的限制——该范围由随附权利要求所限定。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1