一种化合物A8作为组蛋白甲基转移酶NSD3活性抑制剂及其应用的制作方法
本发明属于医药技术领域,具体的涉及一种组蛋白甲基转移酶nsd3活性抑制剂及其应用。
背景技术
组蛋白甲基化是表观遗传修饰最重要的修饰机制之一。组蛋白甲基化及其调控者组蛋白甲基转移酶的异常表达与遗传病、自身免疫性疾病、衰老和癌症等多种疾病的发生密切相关,尤其在肿瘤的发生发展中具有重要意义。因此,组蛋白甲基转移酶被视为潜在的抗肿瘤治疗新靶点。
近年来,以组蛋白甲基转移酶为靶点的抑制剂研发取得了突破性的进展。目前,组蛋白甲基转移酶ezh2抑制剂epz-6438(epizyme公司)于2014年进入i/ii期临床试验,用于治疗非霍奇金淋巴瘤,晚期实体肿瘤,和恶性间皮瘤患者;组蛋白甲基转移酶dot1l抑制剂epz-5676(epizyme公司)亦于2014年进入i期临床试验,用于治疗急性白血病患者。此外,还有多个组蛋白赖氨酸甲基转移酶的小分子抑制剂,如setd7抑制剂pfi-2,g9a(ehmt2)和glp(ehmt1)抑制剂unc0638、a-366,smyd2抑制剂lly-507等处于临床前研究阶段,这些研究对于抗肿瘤靶向治疗药物研发至关重要,具有广阔的应用前景。组蛋白甲基转移酶nsd3(又名whsc1l1,wolf-hirschhornsyndromecandidate1-like1)可使组蛋白h3第36位赖氨酸(h3k36)二甲基化(me2)及三甲基化(me3)。nsd3基因定位于人染色体8p11.23位置上,与多种恶性肿瘤的发生发展具有重要关系。首先,nsd3所在的8p11-12染色体区间在乳腺癌,肺癌,胰腺癌和血液肿瘤等癌症中高度扩增,揭示该区间与肿瘤发生发展具有强烈相关性。其次,多项研究表明nsd3基因本身在恶性肿瘤的发生发展中发挥重要作用。在乳腺癌、膀胱癌、头颈鳞状细胞癌等肿瘤中nsd3被发现高度表达,具有促进肿瘤形成的作用;在急性髓性白血病患者中发现t(8;11)(p11.2;p15)nup98-nsd3融合基因,具体的作用机制尚不清楚;在nut中线癌(nutmidlinecarcinoma)中发现nsd3-nut融合基因,其表达的融合蛋白通过结合brd4蛋白在肿瘤细胞分化阻滞和增殖方面发挥重要的作用;在急性髓细胞白血病(aml)细胞中,只含有n端第一个pwwp结构域的nsd3异构体介导brd4-chd8蛋白质结合,直接影响肿瘤细胞的增殖与分化。
nsd3由1个set(su(var),enhancerofzeste,andtrithorax)结构域、2个pwwp(pro-trp-trp-promotif)结构域和4个phd结构域(planthomeodomain,)组成。其中set结构域为催化中心,pwwp和phd结构域通常参与染色质相关的转录调控及dna修复等诸多生物过程。
迄今为止,发现的组蛋白甲基转移酶大约有60多种,其中包括50多种组蛋白赖氨酸甲基转移酶。在已发现的组蛋白赖氨酸甲基转移酶中,有50%的甲基转移酶活性通过实验方法得到验证,且大部分与肿瘤发生密切相关。然而,在组蛋白赖氨酸甲基转移酶抑制剂研究领域中,大部分研究主要集中于ezh1和ezh2、dot1l、setd7、ehmt1和ehmt2等组蛋白赖氨酸甲基转移酶,对于其他已被证实与人类肿瘤发生发展密切相关的组蛋白甲基转移酶的研究相对而言较少。组蛋白甲基转移酶nsd3在肿瘤发生发展过程中十分重要,是一个潜在的抗肿瘤新靶标。因此发现高活性的nsd3抑制剂对于nsd3在癌症靶向治疗中的应用尤为重要和迫切,针对这些组蛋白甲基转移酶寻找高活性的特意性抑制剂对于抗肿瘤靶向治疗药物研发具有重要意义。
技术实现要素:
本发明提供一种组蛋白甲基转移酶nsd3活性抑制剂,所述抑制剂为式i化合物或其药学可接受的盐
本发明提供了抑制剂在制备治疗肿瘤药物中的新应用。
本发明还提供了式i化合物在制备治疗肿瘤药物中的新应用。
优选的本发明所述肿瘤为肺癌、乳腺癌、胰腺癌、骨肉瘤、头颈部癌,所述肺癌优选为非小细胞肺癌。
优选的本发明所述药物为式i化合物其水合物、药学上可接受的盐、互变异构体、立体异构体或前体化合物和一种或多种药学上可接受的载体制成的药物。所述载体包括药学领域常规的稀释剂、赋形剂、填充剂、粘合剂、湿润剂、崩解剂、吸收促进剂、表面活性剂、吸附载体、润滑剂等。
本发明药物可以制成注射液、片剂、粉剂、颗粒剂、丸剂、胶囊、口服液、膏剂、霜剂等多种形式。上述各种剂型的药物均可以按照药学领域的常规方法制备。
所述药物是通过抑制组蛋白甲基转移酶nsd3活性来治疗肿瘤,可通过注射、喷射、滴鼻、滴眼、渗透、吸收、物理或化学介导的方法导入机体如肌肉、皮内、皮下、静脉、粘膜组织;或是被其他物质混合或包裹后导入机体。
本发明采用整合虚拟筛选与实验测定的方法从从chemdiv化合物库中寻找并发现了式i化合物(以下简称a8)可抑制nsd3酶活性,并结合细胞实验验证化合物的抗肿瘤活性,虽然关于抑制剂a8的研究还未成熟到进入临床阶段,但这些研究对于最终研制出抗nsd3药物至关重要,具有重要的应用前景。
本发明采用计算机模拟方法对药物分子的有效性进行先期评估,并采用生物学实验方法检测并验证活性,获得了有效的nsd3酶抑制剂a8(化学名:6-amino-9-(2-(p-tolyloxy)ethyl)-9h-purine-8-thiol),其酶学水平ic50值为0.69±0.06μmol/l;对h460非小细胞肺癌细胞系具有抑制生长作用,其ic50值分别在5~10μmol/l,具有良好的nsd3酶抑制效果。
附图说明
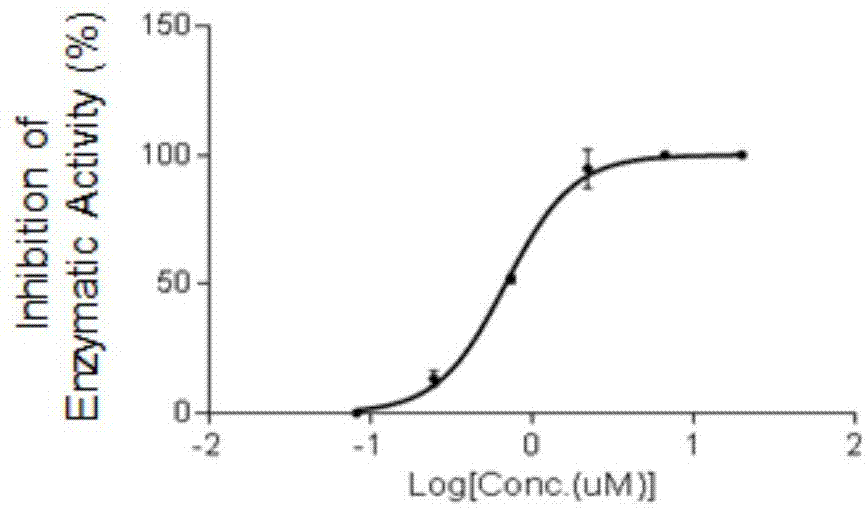
图1:a8在nsd3蛋白水平上的ic50值图。
图2:a8在细胞内抑制nsd3酶活性。
图3:a8对h460非小细胞肺癌细胞生长抑制作用。
具体实施方式
为了证实本发明化合物的抗肿瘤效果,下面将结合附图及具体实施例对本发明做出进一步的描述。
1.实验方法
1.1基于受体的虚拟筛选
首先采用
在采用分子对接方法进行虚拟筛选之前,首先需要验证所采用的glide对接方法的有效性,定义nsd3活性位点,以晶体结构中配体分子s-adenosylmethionine(sam)的质心为中心,设定
采用glidehtvs(highthroughputvirtualscreening)模式对chemdiv库化合物进行对接和打分,选出打分靠前的三十万个化合物;再采用glidesp模式进行重新对接和打分,保留打分靠前的3万个小分子结合模式。在sam与nsd3的结合的晶体结构中,与活性区域残基his1224,his1274形成三个关键的氢键相互作用。对于对接产生的3万个小分子结合模式,采取氢键标准作为筛选条件,选出与his1224,his1274形成2个以上氢键的结合模式,获得了697个符合条件的化合物分子。为了充分考虑化合物的结构多样性,采用schrodinger中的canvas模块进行聚类分析,挑选一批化合物进行实验测定。发现式i化合物,(以下简称a8)具有较好的组蛋白甲基转移酶抑制活性。
式i化合物化学结构式(式i化合物以下简称a8)
1.2nsd3体外酶活性检测实验步骤
1)nsd3蛋白的表达纯化:通过pcr方法从hek293细胞系cdna中扩增获得nsd3部分基因(1021-1320aa),亚克隆于原核表达载体pgex-4t1中,构建具有gst标签的重组质粒,经测序鉴定后,转化于大肠杆菌rossetta中诱导表达(用0.5mmiptg诱导后,在16℃持续培养20小时),用gst树脂进行纯化,获得gst标签的nsd3蛋白。
2)nsd3体外酶活性检测步骤:
①将化合物和2.3μgnsd3蛋白混匀,并在30℃放置15分钟;
②分别加入组蛋白h3k36me1多肽片段
(atkaarksapatggv-k(me1)-kphryrpg-gk(biotin))(最终浓度为0.2μm)和s-adenosylmethioninesam(最终浓度为1.0μm),并在50mmtris-hclph8.5、50mmnacl、5mmmgcl2、1mmdtt和0.01%tween反应液中,30℃反应1小时;
③结合cisbiohtrf组蛋白甲基转移酶检测试剂盒,利用多功能酶标仪在620nm和665nm波长检测相应的荧光数值,计算nsd3活性。
1.3细胞内nsd3酶活性检测实验
1)6孔板种植细胞,16小时后加入化合物,并继续培养48小时后用ripa裂解液裂解细胞收获蛋白样品;蛋白质免疫印迹实验测定h3k36me3和h3蛋白表达。
1.4细胞水平肿瘤抑制实验
1)肿瘤细胞生长抑制率:在96孔板种植5000个细胞,16小时后加入对照dmso或不同浓度的化合物,在37℃,5%二氧化碳培养箱中继续培养;72小时后加入dojindocellcountingkit-8试剂,37℃反应1小时后450nm测定吸光度,最终测定该化合物的肿瘤细胞抑制作用.
2.实验结果
测定了a8在蛋白和细胞水平上针对组蛋白甲基转移酶nsd3的活性抑制作用,以及a8在细胞水平上针对h460非小细胞肺癌细胞生长增殖的抑制效果。
a8在体外蛋白酶学水平上具有良好的nsd3酶抑制效果,其ic50值为0.69±0.06μm,见图1。
分别采用0、2.5、5μm化合物a8分别处理h460和h1299细胞48小时,检测化合物在细胞内对h3k36me3修饰的抑制作用,组蛋白h3为参考蛋白。结果表明,与不加化合物的对照组相比,在2.5μm浓度下,化合物在h460和h1299细胞株中对h3k36me3修饰的抑制率分别为37.3%,38.1%;在5μm浓度下,化合物在h460和h1299细胞株中对h3k36me3修饰的抑制率分别为87.7%和70.0%,说明a8在细胞水平上可有效地抑制nsd3酶活性,降低h3k36me3修饰,见图2。
检测不同浓度的a8对非小细胞肺癌细胞h460的肿瘤生长抑制实验,a8浓度梯度分别是0、2.5、5.0、10.0和20.0μm。结果表明,a8在h460非小细胞肺癌细胞系中对细胞生长增殖抑制效果明显,且抑制作用随作用浓度增加而增强,与对照组相比有统计学意义(不同浓度的a8对肿瘤细胞抑制率分别为21.7%,41.3%,48.3%和54.5%,p<0.05),见图3。
综上,本发明所述化合物a8为有效的组蛋白甲基转移酶nsd3抑制剂,a8在细胞内可明显抑制nsd3酶活性,降低h3k36me3水平,对非小细胞肺癌细胞系的生长增殖亦有显著的抑制作用。可见本发明所述的a8化合物作为组蛋白甲基转移酶抑制剂能够明显抑制肿瘤细胞增殖,具有潜在的抗肿瘤作用,可望作为活性成分用于制备抗肿瘤药物,尤其可望用于制备抗肺癌的药物,具有药用前景。
- 还没有人留言评论。精彩留言会获得点赞!