用于癌症治疗和代谢介入疗法的组合物、方法、试剂盒和系统与流程
交叉引用
本申请要求于2017年12月11日提交的美国临时申请号62/597,392的权益,该申请通过引用全文纳入本文。
背景技术:
癌症和肥胖是主要的公共卫生问题。癌症是全球第二大死亡原因,2012年造成880万人死亡。在全球范围内,大约有六分之一的死亡是由于癌症造成的。癌症是由正常细胞转化为肿瘤细胞的多阶段过程而产生的,该过程通常从癌前病变发展为恶性肿瘤。癌症的一个定义性特征是迅速产生异常细胞,这些细胞生长超出其正常边界,然后可以侵入人体的相邻部位并扩散至其他器官。
癌细胞采用一种独特的新陈代谢类型,即“瓦伯格效应(warburgeffect)”,以促进生长、存活、增殖以及长期维持。这种改变的新陈代谢涉及不相关的细胞糖酵解和线粒体有氧呼吸,这可能导致需要正常细胞不需要的某些营养素。
当前可用的治疗方法具有许多严重的缺陷。例如,当前可用于患者的癌症治疗是昂贵的。癌症的经济影响是巨大的,并且会继续增加。在2010年,癌症的年度经济总成本估计约为1.16万亿美元。而且,传统的治疗癌症的方法,例如化学疗法和放射疗法,倾向于对于癌症具有高毒性和/或非特异性,这导致有限的功效和有害的副作用。
肥胖症是一种多余的体脂积累到可能对健康产生负面影响的程度的医学病症。该病症通常是由食物摄取过多、缺乏体育活动和遗传易感性共同造成的。肥胖症增加了各种疾病和病症的可能性,例如心血管疾病、2型糖尿病、阻塞性睡眠呼吸暂停、癌症、骨关节炎和抑郁症。
当前许多肥胖症治疗方法,例如限制卡路里的饮食调控、行为矫正、锻炼、药物治疗和手术面临许多弊端。许多肥胖症治疗方法无效,只能提供短期效果,尤其是对于那些病态肥胖的患者。
因此,仍然非常需要新的癌症治疗方法和肥胖症治疗方法。
技术实现要素:
癌症和代谢性疾病例如肥胖症仍然是主要的健康问题,目前需要新的、替代的和有效的治疗方法。本公开内容解决了这样的需求并且提供了许多优点。本公开内容涉及向受试者提供包括控制受试者的营养饮食和/或透析的治疗。例如,治疗有需要的患者可以包括给患者安排半胱氨酸贫化的饮食并且安排患者进行透析。本公开内容提供了贫化了一种或多种营养素例如非必需氨基酸的固体和液体组合物,以及使用所述组合物治疗癌症、肾脏疾病和代谢性疾病例如肥胖症的方法。本公开内容提供了与所描述的组合物和方法的分布和/或性能有关的设施、系统和试剂盒。
本公开内容利用血液透析和腹膜透析作为通过施用缺乏一种或多种营养素的组合物来消耗受试者中的这种或多种营养素的方式。血液透析包括从体内抽血并在体外血液回路中对其进行清洁,然后将清洁后的血液返回到体内。体外血液回路包括透析器,该透析器包括半透膜。在该透析器内,废物和多余的液体通过半透膜被去除,并且透析器内的半透膜具有血液侧和透析液侧。腹膜透析涉及在人的腹部中使用腹膜作为膜,通过该膜流体和溶解的物质与血液交换。腹膜透析用于去除多余的液体、纠正电解质问题以及去除肾衰竭患者的毒素。在腹膜透析中,溶液通过下腹部中的永久管引入,然后去除。这可以全天定期进行,称为连续非卧床透析,也可以在夜间借助机器进行,称为自动腹膜透析。此外,本公开内容设想利用血液透析和腹膜透析作为通过消耗和/或恢复受试者中一种或多种营养素来向有需要的受试者提供特定营养组成的方式。本公开内容提供了透析系统及其设备。
在一些方面,本公开内容提供了一种液体组合物,其包含:(a)碳水化合物;(b)至少一种维生素;(c)至少一种选自钠、钙、镁、氯和乳酸根的离子;(d)至少一种必需氨基酸;以及(e)水溶液,其中所述液体组合物任选地包含谷氨酸,其中所述液体组合物包含0-5μm的半胱氨酸和/或胱氨酸,其中所述液体组合物的ph为4.0-6.5,并且其中所述液体组合物具有300-720mosmol/l的同渗容摩。
在一些方面,本公开内容提供了一种液体组合物,其包含:(a)碳水化合物;(b)至少一种维生素;(c)至少一种选自钠、钙、镁、氯和乳酸根的离子;(d)至少一种必需氨基酸;以及(e)水溶液,其中所述液体组合物任选地包含谷氨酸,其中所述液体组合物基本上不含选自丙氨酸、天冬酰胺、天冬氨酸、半胱氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸和酪氨酸的非必需氨基酸,其中所述液体组合物包含0-5μm的半胱氨酸和/或胱氨酸,其中所述液体组合物的ph为4.0-6.5,并且其中所述液体组合物具有300-720mosmol/l的同渗容摩。
在一些方面,本公开内容提供了一种液体组合物,其包含:(a)右旋糖;(b)至少一种选自钠、钙、镁、氯和乳酸根的离子;(c)至少一种必需氨基酸;以及(d)水溶液,其中所述液体组合物包含至少10μm的必需氨基酸,其中所述液体组合物包含0-5μm的半胱氨酸和/或胱氨酸,其中所述液体组合物的ph为4.0-6.5,并且其中所述液体组合物具有300-720mosmol/l的同渗容摩。
在一些实施方案中,所述碳水化合物选自右旋糖和葡萄糖。所述碳水化合物可以是右旋糖。在某些实施方案中,所述右旋糖的量是1.0-4.5%w/v。所述右旋糖的量可以是1.5-4.25%w/v。所述右旋糖的量可以是1.7-4.0%w/v。在另一个实施方案中,所述右旋糖的量是0.05-0.50%w/v。所述右旋糖的量可以是0.05-0.25%w/v。所述右旋糖的量可以是0.08-0.22%w/v。所述右旋糖的量可以是0.1-0.2%w/v。
对于所述液体组合物,在某些实施方案中,所述液体组合物包含至少10μm的所述必需氨基酸。在一些实施方案中,至少一种所述必需氨基酸的量为10-300μm。例如,至少一种所述必需氨基酸的量为20-250μm。所述必需氨基酸可以选自组氨酸、异亮氨酸、亮氨酸、赖氨酸、甲硫氨酸、苯丙氨酸、苏氨酸、色氨酸、缬氨酸和精氨酸。在一些实施方案中,至少一种所述必需氨基酸为甲硫氨酸。在一些实施方案中,至少一种所述必需氨基酸为精氨酸。所述液体组合物可以包含至少两种必需氨基酸。所述液体组合物可以包含至少三种必需氨基酸。所述液体组合物可以包含至少四种必需氨基酸。所述液体组合物可以包含至少五种必需氨基酸。所述液体组合物可以包含至少六种必需氨基酸。所述液体组合物可以包含至少七种必需氨基酸。所述液体组合物可以包含至少八种必需氨基酸。所述液体组合物可以包含至少九种必需氨基酸。所述液体组合物可以包含至少十种必需氨基酸。
所述液体组合物可以进一步包含至少一种维生素。所述维生素可以选自维生素a、维生素b、维生素c、维生素d、维生素e、维生素k和胆碱,例如所述维生素是维生素c。在一些实施方案中,所述维生素的量为约0.000010至200μm。在一些实施方案中,所述液体组合物包含至少1μm的维生素c。例如,所述液体组合物可以包含至少7μm的维生素c。在一些实施方式中,所述维生素是维生素b。所述液体组合物可以包含0.000003至1500μm的所述维生素b。
所述液体组合物可以进一步包含必需脂肪酸。所述必需氨基酸可以是ω-3脂肪酸。
在一些实施方案中,谷氨酸的量为约2-500μm。谷氨酸的量可能会使血液中的谷氨酸增加至少150μm。
在某些实施方案中,所述液体组合物进一步包含至少一种矿物质。所述矿物质可以选自铁、铜、铬、氟化物、碘、锰、钼、硒和锌。所述液体组合物可以包含至少5nm的矿物质。在一些实施方案中,至少一种矿物质的量为5nm-5μm。
在某些实施方案中,所述液体组合物存储在容器中。所述容器可以是透析袋。所述透析袋可以旨在一次性使用。在一些实施方案中,所述容器容纳1500至5000ml的所述液体组合物。例如,约2000ml的所述液体组合物是单个单元。在另一个实施方案中,约2500ml的所述液体组合物是单个单元。
对于所述液体组合物而言,在某些实施方案中,至少一种离子的量为至少约0.1meq/l。至少一种离子的量可以为0.1-150meq/l。
在一些实施方案中,液体组合物不含除谷氨酸以外的非必需氨基酸。或者,所述液体组合物可以进一步包含至少一种非必需氨基酸。在一些实施方案中,所述非必需氨基酸的量为至少约5μm。所述非必需氨基酸的量可以是5-600μm。所述非必需氨基酸可以选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸和酪氨酸。
在某些实施方案中,所述液体组合物包含0-4μm的半胱氨酸和/或胱氨酸。例如,所述液体组合物可以包含0-1μm的半胱氨酸和/或胱氨酸。
在某些实施方案中,所述液体组合物的ph为约5.0-6.5。所述液体组合物的ph可以为约5.5-6.0。所述液体组合物的ph可以为约6.0。液体组合物的ph可以为约5.5。所述液体组合物的ph可以为约5.0。
在某些实施方案中,所述液体组合物的同渗容摩为300-500。例如,所述液体组合物的同渗容摩可以为300-400。所述液体组合物的同渗容摩可以为400-500。所述液体组合物的同渗容摩可以为300-350。
对于所述液体组合物而言,在某些实施方案中,所述水溶液是无菌的。在另一个实施方案中,所述水溶液是非无菌的。在一些实施方案中,所述液体组合物是透析溶液。
在一些方面,本公开内容提供了一种干燥组合物,其包含:(a)碳水化合物;(b)至少一种维生素;(c)至少一种选自钠、钙、镁、氯和乳酸根的离子;(d)至少一种必需氨基酸;以及(e)水溶液,其中所述干燥组合物任选地包含谷氨酸,其中所述干燥组合物包含0-5μm的半胱氨酸和/或胱氨酸。
在一些方面,本公开内容提供了一种干燥组合物,其包含:(a)碳水化合物;(b)至少一种维生素;(c)至少一种选自钠、钙、镁、氯和乳酸根的离子;(d)至少一种必需氨基酸;以及(e)水溶液,其中所述干燥组合物任选地包含谷氨酸,其中所述干燥组合物基本上不含选自丙氨酸、天冬酰胺、天冬氨酸、半胱氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸和酪氨酸的非必需氨基酸,其中所述干燥组合物包含0-5μm的半胱氨酸和/或胱氨酸。
在一些实施方案中,所述碳水化合物选自右旋糖、葡萄糖、蔗糖、果糖和乳糖。所述碳水化合物可以是右旋糖。
在一些方面,本公开内容提供了一种干燥组合物,其包含:(a)右旋糖;(b)至少一种选自钠、钙、镁、氯和乳酸根的离子;以及(c)至少一种必需氨基酸,其中所述干燥组合物包含至少2μg的必需氨基酸,并且其中所述干燥组合物包含0-10mg的半胱氨酸和/或胱氨酸。
对于所述干燥组合物而言,在某些实施方案中,右旋糖的量为至少约10g。右旋糖的量可以是10-50g,例如约50g。在另一个实施方案中,右旋糖的量为至少约0.5g。右旋糖的量可以是0.5-2.5g,例如约2g。
对于所述干燥组合物而言,在某些实施方案中,所述必需氨基酸选自组氨酸、异亮氨酸、亮氨酸、赖氨酸、甲硫氨酸、苯丙氨酸、苏氨酸、色氨酸、缬氨酸和精氨酸。在一些实施方案中,至少一种必需氨基酸是甲硫氨酸。在一些实施方案中,至少一种必需氨基酸是精氨酸。在一些实施方案中,所述干燥组合物包含至少两种必需氨基酸。所述干燥组合物可以包含至少四种必需氨基酸。所述干燥组合物可以包含至少五种必需氨基酸。所述干燥组合物可以包含至少六种必需氨基酸。所述干燥组合物可以包含至少七种必需氨基酸。所述干燥组合物可以包含至少八种必需氨基酸。所述干燥组合物可以包含至少九种必需氨基酸。所述干燥组合物可以包含至少十种必需氨基酸。在一些实施方案中,所述干燥组合物包含至少2μg的必需氨基酸。
所述干燥组合物可以包含至少一种维生素。所述维生素可以选自维生素a、维生素b、维生素c、维生素d、维生素e、维生素k和胆碱。在一些实施方案中,所述维生素的量为约0.01-1500μg。例如,所述维生素是维生素c。所述干燥组合物可以包含至少1000μg的维生素c。在一些实施方案中,所述干燥组合物包含至少2500μg的维生素c。在一些实施方案中,所述干燥组合物包含至少0.01μg的所述维生素b。所述干燥组合物可以包含至少1μg的维生素b。
在一些实施方案中,所述谷氨酸的量为约0.1mg至50mg。所述液体组合物可以不含除谷氨酸以外的非必需氨基酸。
所述干燥组合物可以进一步包含必需脂肪酸,例如ω-3脂肪酸。
所述干燥组合物可以进一步包含至少一种矿物质。所述矿物质可以选自铁、铜、铬、氟化物、碘、锰、钼、硒和锌。在一些实施方案中,所述干燥组合物包含至少0.3μg的矿物质。例如,所述干燥组合物可以包含至少1μg的矿物质。
在某些实施方案中,所述干燥组合物储存在容器中。所述容器可以是透析袋。所述透析袋可以旨在一次性使用。所述干燥组合物可以是透析混合物。在一些实施方案中,所述干燥组合物在容器中进一步包含水溶液,从而产生混合物。所述容器可以包含约2000ml的水溶液。所述容器可以包含约2500ml的水溶液。所述混合物的ph可以为4.0-6.5。所述混合物的同渗容摩可以为300-720mosmol/l。
在某些实施方案中,至少一种离子的量为至少100μmol。
在某些实施方案中,所述干燥组合物进一步包含至少一种非必需氨基酸。非必需氨基酸的量可以为至少1μg。在一些实施方案中,非必需氨基酸的量为1-100μg。
所述干燥组合物可以包含0-5mg的半胱氨酸和/或胱氨酸。在一些实施方案中,所述干燥组合物包含0-1mg的半胱氨酸和/或胱氨酸。
在一些方面,本公开内容提供了浓缩的组合物,所述浓缩的组合物包含本文所述的干燥组合物和初始的水溶液,其中所述干燥组合物溶解在所述初始的水溶液中。
在一些方面,本公开内容提供了一种食品组合物,其包含:(a)不含半胱氨酸的蛋白质源;(b)至少一种必需氨基酸;以及(c)至少一种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的非必需氨基酸,其中每种非必需氨基酸为所述食品组合物中蛋白质的0-1%wt/wt,其中所述食品组合物包含为所述食品组合物中蛋白质的0-1%wt/wt的半胱氨酸和/或胱氨酸,并且其中所述食品组合物包含至少6%wt/wt的蛋白质。
对于所述食品组合物而言,在某些实施方案中,选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的非必需氨基酸的量为所述食品组合物中蛋白质的0-0.1%wt/wt。在一些方面,所述食品组合物包含至少两种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的非必需氨基酸。所述食品组合物可以包含至少三种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的非必需氨基酸。所述食品组合物可以包含至少四种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的非必需氨基酸。所述食品组合物可以包含至少五种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的非必需氨基酸。所述食品组合物可以包含至少六种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的非必需氨基酸。在一些实施方案中,所述非必需氨基酸是甘氨酸。在一些实施方案中,所述非必需氨基酸是脯氨酸。
在某些实施方案中,半胱氨酸的量为所述食品组合物中蛋白质的0-0.1%wt/wt。
在一些方面,本公开内容提供了一种食品组合物,其包含:(a)不含半胱氨酸的蛋白质源;(b)至少一种必需氨基酸;以及(c)至少六种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸的非必需氨基酸,其中每种非必需氨基酸为食品组合物中蛋白质的0-1%wt/wt,并且其中所述食品组合物包含至少6%wt/wt的蛋白质。
对于所述食品组合物而言,在某些实施方案中,选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸的每种非必需氨基酸的量为0-50%。在一些实施方案中,所述食品组合物包含至少七种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸的非必需氨基酸。所述食品组合物可以包含至少八种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸的非必需氨基酸。所述食品组合物可以包含至少九种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸的非必需氨基酸。所述食品组合物可以包含至少十种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸的非必需氨基酸。在一些实施方案中,至少六种非必需氨基酸选自甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸。在一个示例性的实施方案中,至少一种非必需酸是半胱氨酸。半胱氨酸和/或胱氨酸的量可以是所述食品组合物中蛋白质的0-0.04%wt/wt。
在一些方面,本公开内容提供了一种食品组合物,其包含(a)至少一种必需氨基酸;和(b)谷氨酸,其中所述食品组合物基本上不含除谷氨酸以外的非必需氨基酸。
在本文公开的任何食品组合物中,所述不含半胱氨酸的蛋白质源的量为所述食品组合物的至少1%wt/wt。所述不含半胱氨酸的蛋白质源的量可以为所述食品组合物的1-5%。在一个示例性的实施方案中,所述不含半胱氨酸的蛋白质源是明胶。
在本文公开的任何食品组合物中,其进一步包含谷氨酸。在一些实施方案中,所述食品组合物包含约0.1mg至50mg的谷氨酸。
在本文公开的任何食品组合物中,所述必需氨基酸选自精氨酸、组氨酸、异亮氨酸、亮氨酸、赖氨酸、甲硫氨酸、苯丙氨酸、苏氨酸、色氨酸和缬氨酸。在一个示例性的实施方案中,所述必需氨基酸是甲硫氨酸。所述必需氨基酸可以为所述食品组合物的至少1.0wt/wt。例如,必需氨基酸的量可以为所述食品组合物的2.0-75%wt/wt。在一些实施方案中,所述食品组合物包含至少两种必需氨基酸。所述食品组合物可以包含至少三种必需氨基酸。所述食品组合物可以包含至少四种必需氨基酸。所述食品组合物可以包含至少五种必需氨基酸。所述食品组合物可以包含至少六种必需氨基酸。所述食品组合物可以包含至少七种必需氨基酸。所述食品组合物可以包含至少八种必需氨基酸。
在某些实施方案中,本文所述的任何食品组合物进一步包含药物活性剂。所述药物活性剂可以是抗癌治疗剂。
在本文公开的任何食品组合物中,所述食品组合物包装为固体食物、半固体食物或饮料。所述食品组合物包装为选自零食棒、谷物产品、烘焙产品和乳制品的食品。例如,所述食品组合物可以是婴儿配方。所述食品组合物可以是软饮料。所述食品组合物可以是营养奶昔。所述食品组合物为燕麦棒。
在一些实施方案中,所述食品组合物包含10-20%w/w的总氨基酸。所述食品组合物可以包含约17%w/w的总氨基酸。
在一些方面,本公开内容提供了一种设施,其包括多种本文所述的液体组合物。所述设施可以是制药厂。所述设施可以是配送中心。所述设施可以是医院或诊所。
在一些方面,本公开内容提供了多种本文所述的干燥组合物。所述设施可以是制药厂。所述设施可以是配送中心。所述设施可以是医院或诊所。
在一些方面,本公开内容提供了多种本文所述的食品组合物。所述设施可以是食品制造场所。所述设施可以是配送中心。所述设施可以是商业厨房、餐厅或就餐设施。
在一些方面,本公开内容提供了一种试剂盒,其包含:(a)本文所述的预包装的液体组合物;和(b)使用所述预包装液体组合物的说明书。在一些实施方案中,所述试剂盒提供至少一周的完整治疗。例如,所述试剂盒可以提供至少四周的完整治疗。
在一些方面,本公开内容提供了一种试剂盒,其包含:(a)本文所述的预包装的干燥组合物或浓缩组合物;和(b)使用所述预包装的干燥组合物或浓缩组合物的说明书。在一些实施方案中,所述试剂盒提供至少一周的完整治疗。例如,所述试剂盒可提供至少四周的完整治疗。
在一些方面,本公开内容提供了一种试剂盒,其包含:(a)本文所述的预包装的食品组合物;和(b)使用所述预包装食品组合物的说明书。在一些实施方案中,所述试剂盒提供至少一日的全餐。例如,所述试剂盒可以提供至少五日的全餐。在一些实施方案中,所述试剂盒进一步包含本文所述的预包装液体组合物。所述试剂盒可以进一步包含使用所述预包装液体组合物的说明书。在另一个实施方案中,所述试剂盒进一步包含本文所述的预包装干燥组合物。所述试剂盒进一步包括使用所述预包装干燥组合物的说明书。
在一些方面,本公开内容提供了一种用于在有需要的受试者中治疗癌症的方法,所述方法包括向所述受试者施用本文所述的任何食品组合物,以及向所述受试者施用本文所述的液体组合物、浓缩组合物或干燥组合物。
在一些方面,本公开内容提供了一种在有需要的受试者中治疗癌症的方法,所述方法包括向所述受试者施用本文所述的液体组合物、浓缩组合物或干燥组合物。
在一些方面,本公开内容提供了一种用于在有需要的受试者中治疗癌症的方法,所述方法包括向所述受试者施用本文所述的任何食品组合物。
在任何用于治疗癌症的所述方法中,所述癌症可以选自肝癌、乳腺癌、肺癌、白血病、前列腺癌和结肠癌。所述受试者可以是人类。所述受试者可以是动物。在一些实施方案中,所述受试者具有癌症的遗传易感性。所述受试者可能具有升高的半胱氨酸生物合成基因表达水平。
在某些实施方案中,治疗癌症的特征在于肿瘤大小的减小。所述肿瘤可以减小至少30%。所述肿瘤可以减小至少50%。所述肿瘤可以减小至少80%。
在一些实施方案中,治疗癌症的特征在于血浆半胱氨酸水平的降低。所述血浆半胱氨酸水平可以降低至少30%。所述血浆半胱氨酸水平可以降低至少50%。所述血浆半胱氨酸水平可以降低至少80%。所述血浆半胱氨酸水平可以降低至少90%。在一个示例性的实施方案中,所述血浆半胱氨酸水平降低至少95%。
在一些方面,本公开内容提供了一种用于在有需要的受试者中减小肿瘤大小的方法,所述方法包括向所述受试者施用任何本文所述的食品组合物,以及向所述受试者施用本文所述的液体组合物、浓缩组合物或干燥组合物。
在一些方面,本公开内容提供了一种用于在有需要的受试者中减小肿瘤大小的方法,所述方法包括向所述受试者施用本文所述的液体组合物、浓缩组合物或干燥组合物。
在一些方面,本公开内容提供了一种用于在有需要的受试者中减小肿瘤大小的方法,所述方法包括向所述受试者施用任何本文所述的食品组合物。
在任何用于减小肿瘤大小的所述方法中,所述受试者可以是人类。所述受试者可以是动物。在一些实施方案中,所述受试者具有癌症的遗传易感性。所述受试者可能具有升高的半胱氨酸生物合成基因表达水平。
在某些实施方案中,减小肿瘤大小的特征在于肿瘤大小的减小。所述肿瘤可以减小至少30%。所述肿瘤可以减小至少50%。所述肿瘤可以减小至少80%。
在一些方面,本公开内容提供了一种用于治疗肥胖症的方法,所述方法包括向所述受试者施用本文所述的任何食品组合物。
在任何治疗肥胖症的所述方法中,所述受试者可以是人类。所述受试者可以是动物。在一些实施方案中,所述受试者具有肥胖症的遗传易感性。
在一些实施方案中,治疗肥胖症的特征在于受试者减轻了所述受试者初始体重的至少10%。治疗肥胖症的特征可在于受试者减轻了所述受试者初始体重的至少20%。治疗肥胖症的特征可在于受试者减轻了所述受试者初始体重的至少30%。
在一些方面,本公开内容提供了一种用于治疗肾脏疾病的方法,所述方法包括向用于受试者施用本文所述的液体组合物、浓缩组合物或干燥组合物。
在任何用于治疗肾脏疾病的所述方法中,所述受试者可以是人类。所述受试者可以是动物。在一个示例性的实施方案中,所述受试者被诊断患有慢性肾脏疾病。
在包括向所述受试者施用本文所述的液体组合物、浓缩组合物或干燥组合物的任何所述方法中,所述方法进一步包括利用膜。在某些实施方案中,所述膜包含改性的二乙酸纤维素或聚砜。在一个示例性的实施方案中,所述膜是低通量膜。所述低通量膜可允许小分子交换。在一些实施方案中,所述低通量膜包括多个孔,并且所述多个孔包括第一端和第二端。所述多个孔可以具有约1.8nm的平均孔径。
在某些实施方案中,所述低通量膜允许约50%或以上的重约500道尔顿或以下的分子穿过所述多个孔从所述第一端移动到所述第二端。所述低通量膜可允许约75%或以上的重约500道尔顿或以下的分子穿过所述多个孔从所述第一端移动到所述第二端。所述低通量膜可允许约90%或以上的重约500道尔顿或以下的分子穿过所述多个孔从所述第一端移动到所述第二端。所述低通量膜可允许约95%或以上的重约500道尔顿或以下的分子穿过所述多个孔从所述第一端移动到所述第二端。
在某些实施方案中,约20%的至少1000道尔顿的分子穿过所述多个孔从所述第一端通过到所述第二端。例如,约10%的至少1000道尔顿的分子可以从第一侧通过到第二侧。约1%的至少1000道尔顿的分子可以从第一侧通过到第二侧。
在包括施用施用所述液体组合物、浓缩组合物或干燥组合物的任何所述方法中,在某些实施方案中,每周至少一次向所述受试者施用所述组合物。可以每周至少三次向所述受试者施用所述组合物。可以每周至少五次向所述受试者施用所述组合物。在某些实施方案中,在至少一周的过程中向所述受试者施用所述液体组合物、浓缩组合物或干燥组合物。可以在至少四周的过程中向所述受试者施用所述组合物。可以在至少2个月的过程中向所述受试者施用所述组合物。在一个示例性的实施方案中,在至少3个月的过程中向所述受试者施用所述组合物。
在包括施用本文所述的任何食品组合物的任何所述方法中,在某些实施方案中,每周至少一次向所述受试者施用所述食品组合物。可以每周至少三次向所述受试者施用所述食品组合物。可以每周至少五次向所述受试者施用所述食品组合物。可以每周至少21次向受试者施用所述食品组合物。
在某些实施方案中,在至少一周的过程中向所述受试者施用所述食品组合物。可以在至少四周的过程中所述受试者施用所述食品组合物。可以在至少2个月的过程中向所述受试者施用所述食品组合物。可以在至少3个月的过程中所述受试者施用所述食品组合物。
在包括施用液体组合物、浓缩组合物或干燥组合物以及任何食品组合物的任何所述方法中,可以向所述受试者顺序地施用所述组合物。在另一个实施方案中,可以向受试者同时施用所述组合物。在一些实施方案中,每周至少一次向所述受试者施用所述组合物。例如,可以每周至少三次向所述受试者施用所述组合物。在一些实施方案中,在至少一周的过程中向所述受试者施用所述组合物。例如,可以在至少四周的过程中向所述受试者施用所述组合物。
在本文所述的任何方法中,在某些实施方案中,所述方法进一步包括施用药物活性剂。所述药物活性剂可以是抗癌治疗剂。可以以亚治疗量提供所述药物活性剂。
在本文所述的任何方法中,在某些实施方案中,所述方法进一步包括施用营养补充剂。所述营养补充剂可以包含至少一种选自精氨酸、组氨酸、异亮氨酸、赖氨酸、甲硫氨酸、苯丙氨酸、苏氨酸、色氨酸和缬氨酸的氨基酸。在一些实施方案中,所述营养补充剂为所述受试者提供的营养素水平符合推荐膳食摄入量(rda)、适宜摄入量(ai)和/或每日量值(dv)。
在一些方面,本公开内容提供了一种在已接受低半胱氨酸饮食的受试者中治疗癌症的方法,所述方法包括:给所述受试者进行透析,其中所述透析减少或消耗所述受试者体内的半胱氨酸。
在一些方面,本公开内容提供了一种在已接受低半胱氨酸饮食的受试者中消耗半胱氨酸的方法,所述方法包括:给所述受试者进行透析,其中所述透析减少或消耗所述受试者体内的半胱氨酸。
在一些方面,本公开内容提供了一种在已接受透析程序以减少血液中的半胱氨酸的受试者中治疗癌症的方法,所述方法包括:为所述受试者安排低半胱氨酸饮食。
在一些实施方案中,所述透析包括施用本文公开的液体组合物、本文公开的浓缩组合物或本文公开的干燥组合物。在一些实施方案中,所述低半胱氨酸饮食是本文公开的食品组合物。
在一些方面,本公开内容提供了一种透析系统,其包括:透析容器,所述透析容器包含本文公开的液体组合物、本文公开的浓缩组合物或本文公开的干燥组合物。
在一些方面,本公开内容提供了一种透析系统,其包括:透析容器,所述透析容器包含本文公开的液体组合物、本文公开的浓缩组合物或本文公开的干燥组合物;以及透析机,所述透析机被配置为施用所述液体组合物、所述浓缩组合物或所述干燥组合物。在一些实施方案中,所述透析机包括泵、压力监测器、气阱、空气检测器、夹具和/或过滤器。
援引并入
在本说明书中提到的所有出版物、专利和专利申请都通过引用并入本文,其程度如同特别地和单独地指出每个单独的出版物、专利或专利申请均通过引用而并入。
附图说明
下文参考附图简要描述本文提供的各个方面、特征、实施方案和实例。附图可以整体或部分地示出一个或多个方面、特征、实施方案和/或实例。附图是说明性的,不一定按比例绘制。
在所附的权利要求书中具体阐述本发明的新颖性特征。通过参考下文阐述了说明性的实施方案的详细说明和附图,可以更好地理解本发明的特征和优点,在这些说明性的实施方案中利用了本发明的原理,在附图中:
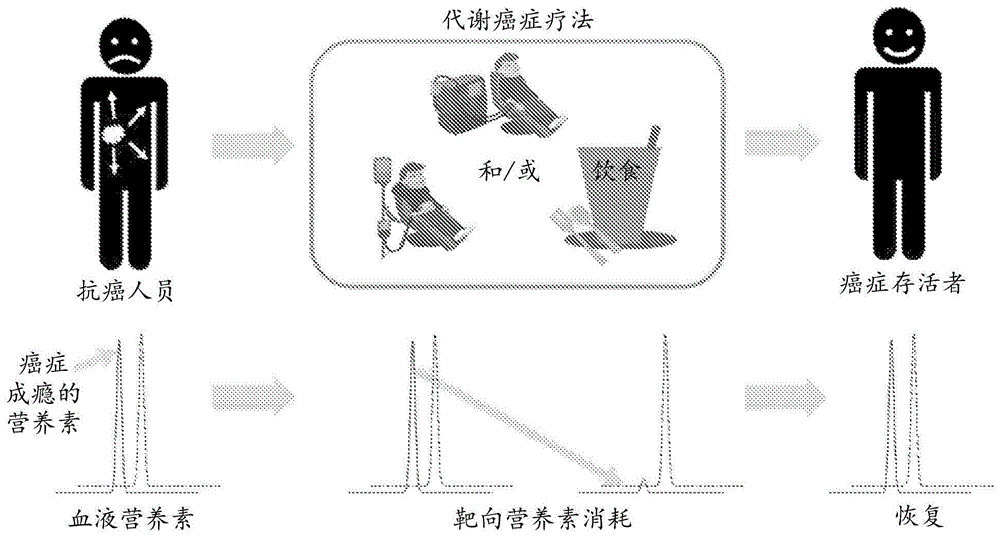
图1描绘了代谢癌症疗法,其中用透析和/或营养饮食治疗癌症患者以消耗靶向营养素。
图2显示了结肠癌、乳腺癌、前列腺癌和胰腺癌研究中所用饮食的概况。
图3示出了在本公开内容的研究中使用的饮食组合物的概况。用于本研究的小鼠是正常的和活跃的(而不是荷瘤的)。
图4描绘了显示完全饮食和mead202对结肠癌(hct116)的肿瘤体积(mm3)的影响的图。植入hct116细胞的小鼠在第7天接受饮食治疗。每周监测肿瘤大小3次。每组有5只小鼠。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。
图5a描绘了显示完全饮食(ctrl)和治疗饮食在三阴性乳腺癌(mda-mdb-231)中随时间(肿瘤植入后的天数)对肿瘤体积(mm3)的影响的图。植入mda-mdb-231细胞的小鼠在第20天接受饮食治疗。每周监测肿瘤大小3次。每组有5只小鼠。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。图5b描绘了显示完全饮食(ctrl)、mead202和mead203在三阴性乳腺癌(mda-mdb-231)中随时间(肿瘤接种后的天数)对肿瘤体积(mm3)的影响的图。植入mda-mdb-231细胞的小鼠在第7天接受饮食治疗。每周监测肿瘤大小3次。每组有5只小鼠。显示了显著性:*为p<0.05,**为p<0.0l,***为p<0.001。
图6描绘了显示完全饮食(ctrl)和mead203在前列腺癌(pc3)中随时间(肿瘤接种后的天数)对肿瘤体积(mm3)的影响的图。植入pc-3细胞的小鼠在第5天接受饮食治疗。每周监测肿瘤大小3次。每组有5只小鼠。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。
图7描绘了显示完全饮食(ctrl)和治疗饮食在胰腺癌(miapaca-2)中随时间(治疗后的天数)对肿瘤体积(mm3)的影响的图。植入miapaca-2细胞的小鼠在第0天接受饮食治疗。每周监测肿瘤大小2次。每组有5只小鼠。显示了显著性:*为p<0.05,**为p<0.0l,***为p<0.001。
图8示出了在本公开内容的研究中使用的透析组合物的概况。
图9描绘了显示完全饮食(ctrl)、mead203+透析、mead203在胶质母细胞瘤(et87mg,单只小鼠研究)中随时间(肿瘤接种后的天数)对肿瘤体积(mm3)的影响的图。植入et87mg细胞的小鼠在第5天接受饮食治疗。每天监测肿瘤大小。每个治疗组有1只小鼠。在第7、8、9、13、14、28、37和40天,透析流体为mead101(ctrl)。在第23、26、27、30、31、33、34、35、36、41和42天,透析流体为mead102。在第43、44、47、48、49、50、51、54、55、56、57和58天,透析流体为mead103。
图10描绘了显示完全饮食、仅饮食、仅透析和饮食+透析在胶质母细胞瘤(u87mg)中随时间(治疗后的天数)对肿瘤体积(mm3)的影响的图。植入u87mg细胞的小鼠在第1天接受饮食治疗。每天监测肿瘤大小。每组有6只小鼠。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。
图11a描绘了显示完全饮食(ctrl)、mead203、mead202和天然食物在三阴性乳腺癌(mda-mb-231)中随着时间(肿瘤接种后的天数)对体重(%)的影响的图。植入mda-mdb-231细胞的小鼠在第20天接受饮食治疗。每周监测肿瘤大小3次。每组有5只小鼠。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。图11b描绘了显示完全饮食(ctrl)和mead203在前列腺癌(pc3)中随时间(肿瘤接种后的天数)对体重(%)的影响的图。植入pc-3细胞的小鼠在第5天接受饮食治疗。每周监测肿瘤大小3次。每组有5只小鼠。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.01。
图12a描绘了显示天然食物、完全饮食、mead202、mead203在三阴性乳腺癌(mda-mb-231)中对葡萄糖(mg/dl)的影响。用novamax葡萄糖试纸测量血浆中的葡萄糖。植入mda-mdb-231细胞的小鼠在第20天接受饮食治疗。在治疗开始之前和治疗完成之后收集血浆样品。每组有5只小鼠。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。图12b描绘了显示完全饮食和mead203在前列腺癌(pc3)中对葡萄糖(mg/dl)的影响的图。用novamax葡萄糖试纸测量血浆中的葡萄糖。植入pc-3细胞的小鼠在第5天接受饮食治疗。在治疗开始之前和治疗完成之后收集血浆样品。每组有5只小鼠。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。
图13a描绘了显示天然食物、完全饮食、mead202、mead203在三阴性乳腺癌(mda-mb-231)中对β-酮(mmol/l)的影响。用novamax酮试纸测定血浆中的β-酮体。植入mda-mdb-231细胞的小鼠在第20天接受饮食治疗。在治疗开始之前和治疗完成之后收集血浆样品。每组有5只小鼠。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。图13b描述了显示完全饮食和mead203在前列腺癌中对β-酮(mmol/l)的影响的图。用novamax酮试纸测定血浆中的β-酮体。植入pc-3细胞的小鼠在第5天接受饮食治疗。在治疗开始之前和治疗完成之后收集血浆样品。每组有5只小鼠。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。
图14a和图14b分别示出了配置用于施用本文所述的组合物的示例性的透析系统、capd和ccpd。
图15示出了配置为用于施用本文所述的组合物的用于血液透析的示例性透析系统。
图16描绘了典型的血液透析过程。
具体实施方式
下面参考用于说明的示例应用来描述本发明的几个方面。应当理解,阐述了许多具体细节、关系和方法以提供对本发明的全面理解。然而,相关领域的普通技术人员将容易地认识到,可以在没有一个或多个特定细节或通过其他方法的情况下实践本发明。除非另有说明,否则本发明不受动作或事件的所示顺序的限制,因为某些动作可以以不同的顺序发生和/或与其他动作或事件同时发生。此外,并非所有示出的动作或事件都是实施本发明的方法所必需的。所公开的组合物中各种组分的浓度是示例性的,并不意在限于所述浓度本身。
将理解的是,以单数形式出现在本文中的单词包括其复数形式,并且以复数形式出现在本文中的单词包括其单数形式,除非隐含或明确地理解或另有说明。此外,将理解的是,对于本文所述的任何给定的组分,为该组分所列出的任何可能的候选物或替代物通常可以单独使用或与彼此任意组合使用,除非隐含或明确地理解或另有说明。另外,将理解的是,这样的候选物或替代物的任何列表仅是说明性的,而不是限制性的,除非隐含地或明确地理解或另有说明。更进一步,将理解的是,本文呈现的任何数字、数值或量都是近似的,并且任何数值范围均包括限定所述范围的最小数值和最大数值,无论是否使用单词“包含”等,除非隐含或明确地理解或另有说明。通常,在提及数字、数值或量时,术语“大约”或“约”或符号“~”包括落入其±5%的范围内的数值,除非隐含或明确地理解或另有说明。此外,将理解的是,所采用的任何标题都是为了方便而不是限制。另外,将理解,任何宽容式(permissive)、开放(open)或开放式(open-ended)语言分别包含对限制语言的任何相对宽容、对封闭语言的较小开放或对封闭式语言的较小开放,除非隐含或明确地理解或另有说明。仅作为示例,单词“包括”可以包括“包括”、“基本上由……组成”和/或“由……组成”类型语言。
如本文所用,除非另有说明,否则本文的一些发明性实施方案考虑数值范围。本发明的各个方面可以以范围形式呈现。应当理解,范围形式的描述仅仅是为了方便和简洁,而不应被解释为对本发明范围的刻板限制。因此,范围的描述应该被认为已经明确公开了所有可能的子范围以及该范围内的各个数值,就好像它们被明确写出一样。例如,应该将对范围如1到6的描述视为已具体公开了如从1到3、从1到4、从1到5、从2到4、从2到6、从3到6等的子范围,以及该范围内的单个数字,例如1、2、3、4、5和6。无论范围的广度如何,这都适用。如果存在范围,则范围包括范围端点。
定义
术语“施用(administer)”、“施用(administered)”、“施用(administers)”和“施用(administering)”被定义为通过本领域已知的途径向受试者提供组合物,所述途径包括但不限于静脉内、动脉内、口服、肠胃外、经颊、局部、经皮、直肠、肌内、皮下、骨内、经粘膜或腹膜内施用途径。在本申请的某些实施方案中,可以优选施用组合物的口服途径。在某些实施方案中,可以优选通过透析施用组合物。
如本文所用,“药剂”或“生物活性剂”是指生物学、药学或化学的化合物或其他部分。非限制性实例包括简单或复杂的有机或无机分子、肽、蛋白质、肽核酸(pna)、寡核苷酸(包括例如适体和多核苷酸)、抗体、抗体衍生物、抗体片段、维生素衍生物、碳水化合物、毒素、游离氨基酸形式的支链氨基酸或其代谢产物,或化疗化合物。如本文所用,术语蛋白质包括包含一个或多个氨基酸的氨基酸混合物。可以合成各种化合物,例如小分子和寡聚物(例如寡肽和寡核苷酸),以及基于各种核心结构的合成有机化合物。另外,各种天然来源可以提供用于筛选的化合物,例如植物或动物提取物等。技术人员可以容易地认识到,对于本发明的药剂的结构性质没有限制。
如本文所用,术语“共同施用”,“与……联合施用”及其语法等同物意指涵盖将本发明组合物和另外的治疗剂施用给每个受试者。共同施用可以包括向动物施用两种或更多种药剂,使得两种药剂和/或其代谢产物同时存在于受试者中。共同施用可以包括其中通过相同或不同的施用途径或在相同或不同的时间施用组合物和另外的治疗剂的治疗方案。共同施用包括同时施用单独的组合物,在不同时间施用单独的组合物,或施用存在两种药剂的组合物。共同施用可以包括同时施用单独的组合物中的药剂,在不同的时间施用单独的组合物,和/或施用包含要共同施用的每种药剂的单一组合物。
术语“确定”、“测量”、“评估”、“评价”、“测定”、“询问”和“分析”在本文中可互换使用,以指代任何形式的测量,并且包括确定元素是否存在。这些术语包括定量和/或定性确定。评估可以是相对的,也可以是绝对的。
术语“有效量”或“治疗有效量”是指足以实现预期应用的本文所述化合物的量,该应用包括但不限于如下定义的疾病治疗。治疗有效量可根据预期应用(体外或体内)或所治疗的受试者和疾病状况而变化,例如,受试者的体重和年龄、疾病状况的严重程度、施用方式等等,这可以由本领域普通技术人员容易地确定。该术语还适用于将在靶细胞中诱导特定应答的剂量,例如减少增殖或下调靶蛋白的活性。具体剂量将根据所选的特定化合物、要遵循的给药方案、是否与其他化合物联合施用、施用时间、将其施用的组织以及携带其的物理递送系统而变化。
术语“必需氨基酸”或“必不可少的氨基酸”是指生物体不能从头合成的氨基酸。必需氨基酸包括精氨酸、组氨酸、异亮氨酸、亮氨酸、赖氨酸、甲硫氨酸、苯丙氨酸、苏氨酸、色氨酸和缬氨酸。必需氨基酸可以包括其盐。
如本文所用,术语“不含”是指具有约0%的特定组分的组合物。
术语“非必需氨基酸”或“不必要的氨基酸”是指可以由生物体从头合成的氨基酸。非必需氨基酸包括丙氨酸、天冬酰胺、天冬氨酸、半胱氨酸(或胱氨酸)、谷氨酸、谷氨酰胺、甘氨酸、脯氨酸、丝氨酸和酪氨酸。术语“半胱氨酸”和“胱酸氨”在本文中可互换使用。非必需氨基酸还可以包括其盐。
术语“预防”是指在病症发作之前提供治疗。如果在患有病症的受试者中开始治疗,则预期这种治疗可以预防病症的医学后遗症或预防病症的医学后遗症的发展。
如本文所用,术语“受试者”或“个体”包括哺乳动物。哺乳动物的非限制性实例包括人和动物,例如小鼠,包括转基因和非转基因小鼠。本文所述的方法可用于人类治疗、临床前应用和兽医应用。在一些实施方案中,受试者是动物,在一些实施方案中,受试者是人类。其他哺乳动物包括但不限于猿、黑猩猩、猩猩、猴子;驯养的动物(宠物),例如狗、猫、豚鼠、仓鼠、小鼠、大鼠、兔子和雪貂;驯养的农场动物,如牛、水牛、野牛、马、驴、猪、绵羊和山羊;或通常在动物园中发现的外来动物,例如熊、狮子、老虎、豹、大象、河马、犀牛、长颈鹿、羚羊、树懒、瞪羚、斑马、牛羚、草原土拨鼠、考拉熊、袋鼠、熊猫、大熊猫、鬣狗、海豹、海狮和象海豹。
如本文所用,术语“基本上不含”是指具有小于约10%、小于约5%、小于约1%、小于约0.5%、小于0.1%或甚至更少的指定组分。
药剂、活化剂或疗法的“亚治疗量”是小于该药剂、活化剂或疗法的有效量的量,但当与另一种药剂或疗法的有效量或亚治疗量组合时,由于例如所产生的有效作用中的协同作用和/或减少的副作用,可产生期望的结果。药剂或组分的亚治疗量可以使得低于该量的量将被认为是治疗性的。例如,fda指南可以建议治疗特定病症的指定剂量水平,并且亚治疗量可以是低于fda建议的剂量水平的任何水平。亚治疗量可以比被认为是治疗量的量少约1%、5%、10%、15%、20%、25%、30%、35%、50%、75%、90%或95%。可以针对每个受试者或受试者组评估治疗量。受试者组可以是所有潜在的受试者,或具有特定特征(例如年龄、体重、种族、性别或体育锻炼水平)的受试者。
组合物
如本文所用,“组合物”是指干燥组合物、浓缩组合物、液体组合物和/或食品组合物。本公开内容提供了有效治疗癌症、其他代谢疾病(包括肥胖症和肾脏疾病)的组合物,例如干燥组合物、浓缩组合物、液体组合物和食品组合物。就一种或多种氨基酸或其他营养素而言,组合物可以是消耗的或减少的,和/或就一种或多种其他氨基酸或营养素而言,组合物可以是补充的。消耗或减少的营养素可以是与非癌细胞相比,某些癌细胞中更高程度地需要的营养素酸。例如,与非癌细胞相比,癌细胞对于某些非必需氨基酸可能具有更高的营养或代谢要求,因此可以配制出就那些非必需氨基酸而言被消耗或减少的组合物,同时保持正常量或补充量的其他营养素。组合物可以是用于透析或营养饮食的组合物。如本文所用,干燥组合物、浓缩组合物或液体组合物也可以称为“透析液组合物”、“透析液”、“透析溶液”或“透析组合物”。如本文所用,食品组合物也可以被称为“营养饮食”或“饮食”。
液体组合物
本公开内容提供了透析组合物。透析组合物可以是液体组合物的形式。在一些方面,本公开内容提供了包含谷氨酸的液体组合物。在一些实施方案中,液体组合物包含谷氨酸和至少一种必需氨基酸。本公开内容还提供了包含至少一种维生素的透析组合物。在一些实施方案中,液体组合物包含至少一种维生素和至少一种必需氨基酸。在一些实施方案中,液体组合物基本上不含半胱氨酸和/或胱氨酸。
在一些方面,本公开内容提供了一种液体组合物,其包含:(a)碳水化合物;(b)谷氨酸;(c)至少一种维生素;(d)至少一种选自钠、钙、镁、氯和乳酸根的离子;(e)至少一种必需氨基酸;以及(f)水溶液,其中所述液体组合物包含0-5μm的半胱氨酸和/或胱氨酸,其中所述液体组合物的ph为4.0-6.5,并且其中所述液体组合物的同渗容摩为300-720mosmol/l。在一些方面,本公开内容提供了一种液体组合物,其包含:(a)碳水化合物;(b)至少一种维生素;(c)至少一种选自钠、钙、镁、氯和乳酸根的离子;(d)至少一种必需氨基酸;以及(e)水溶液,其中所述液体组合物任选地包含谷氨酸,其中所述液体组合物包含0-5μm的半胱氨酸和/或胱氨酸,其中所述液体组合物的ph为4.0-6.5,并且其中所述液体组合物的同渗容摩为300-720mosmol/l。
在一些方面,本公开内容提供了一种液体组合物,其包含:(a)碳水化合物;(b)谷氨酸;(c)至少一种选自钠、钙、镁、氯和乳酸根的离子;(d)至少一种必需氨基酸;以及(e)水溶液,其中所述液体组合物基本上不含除谷氨酸以外的非必需氨基酸,其中所述液体组合物包含0-5μm的半胱氨酸和/或胱氨酸,其中所述液体组合物的ph为4.0-6.5,并且其中所述液体组合物的同渗容摩为300-720mosmol/l。在一些方面,本公开内容提供了一种液体组合物,其包含:(a)碳水化合物;(b)至少一种维生素;(c)至少一种选自钠、钙、镁、氯和乳酸根的离子;(d)至少一种必需氨基酸;以及(e)水溶液,其中所述液体组合物任选地包含谷氨酸,其中所述液体组合物基本上不含选自丙氨酸、天冬酰胺、天冬氨酸、半胱氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸和酪氨酸的非必需氨基酸,其中所述液体组合物包含0-5μm的半胱氨酸和/或胱氨酸,其中所述液体组合物的ph为4.0-6.5,并且其中所述液体组合物的同渗容摩为300-720mosmol/l。
在一些方面,本公开内容提供了一种液体组合物,其包含:(a)碳水化合物;(b)至少一种选自钠、钙、镁、氯和乳酸根的离子;(c)至少一种必需氨基酸;和水溶液,其中所述液体组合物包含0-50μm的半胱氨酸和/或胱氨酸,其中液体组合物的ph为4.0-6.5,并且其中所述液体组合物的同渗容摩为300-720mosmol/l。
在一些方面,本公开内容提供了一种液体组合物,其包含:(a)右旋糖;(b)至少一种选自钠、钙、镁、氯和乳酸根的离子;(c)至少一种必需氨基酸;和水溶液,其中所述液体组合物包含至少10μm的必需氨基酸,其中所述液体组合物包含0-50μm的半胱氨酸和/或胱氨酸,其中液体组合物的ph为4.0-6.5,并且其中所述液体该组合物的同渗容摩为300-720mosmol/l。
在一些方面,本公开内容提供了一种液体组合物,其包含:(a)碳水化合物;(b)至少一种必需氨基酸;和水溶液,其中所述液体组合物包含0-50μm的半胱氨酸和/或胱氨酸,并且其中所述液体组合物基本上不含非必需氨基酸。
在一些实施方案中,碳水化合物选自右旋糖、葡萄糖、蔗糖、果糖和乳糖。在一个示例性的实施方案中,碳水化合物是右旋糖。本文公开的液体组合物可以包含0.1-4.5%w/v的右旋糖的量。在某些实施方案中,右旋糖的量为1.0-4.5%w/v。右旋糖的量可以为1.5-4.25%w/v。在一个示例性的实施方案中,右旋糖的量为1.7-4.0%w/v。在另一个实施方案中,右旋糖的量为0.05-0.25%w/v。右旋糖的量可以是0.08-0.22%w/v。在一个示例性的实施方案中,右旋糖的量为0.1-0.2%w/v。液体组合物中的右旋糖的量可以为至少、大约或不大于0.05、0.1、0.5、1.0、1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9、2.0、2.1、2.2、2.3、2.4、2.5、2.6、2.7、2.8、2.9、3.0、3.1、3.2、3.3、3.4、3.5、3.6、3.7、3.8、3.9、4.0、4.1、4.2、4.3、4.4、4.5、4.6、4.7、4.8、4.9或5.0%w/v。液体组合物中的右旋糖的量可以取决于其预期的应用,例如用于腹膜透析(pd)或用于血液透析(hd)。例如,当用于腹膜透析时,液体组合物中的右旋糖的量可以为1.0-4.5%w/v,例如1.5-4.25%w/v或1.7-4.0%w/v。当用于血液透析时,液体组合物中的右旋糖的量可以为0.05-0.50%w/v,例如0.08-0.25%w/v或0.1-0.25%w/v。
在某些实施方案中,液体组合物包含至少一种必需氨基酸,其选自组氨酸、异亮氨酸、亮氨酸、赖氨酸、甲硫氨酸、苯丙氨酸、苏氨酸、色氨酸、缬氨酸和精氨酸。在一个示例性的实施方案中,至少一种必需氨基酸是甲硫氨酸。在一个示例性的实施方案中,至少一种必需氨基酸是精氨酸。在某些实施方案中,至少一种必需氨基酸的量为至少10μm。至少一种必需氨基酸的量可以是10-300μm。至少一种必需氨基酸的量可以是20-250μm。至少一种必需氨基酸的量可以为至少、大约或不超过1、5、10、20、30、40、50、60、70、80、90、100、110、120、130、140、150、160、170、180、190、200、210、220、230、240、250、260、270、280、290或300μm。
在某些实施方案中,液体组合物包含至少两种必需氨基酸。液体组合物可以包含至少三种必需氨基酸。液体组合物可以包含至少四种必需氨基酸。液体组合物可以包含至少五种必需氨基酸。液体组合物可以包含至少六种必需氨基酸。液体组合物可以包含至少七种必需氨基酸。液体组合物可以包含至少八种必需氨基酸。液体组合物可以包含至少九种必需氨基酸。液体组合物可以包含至少十种必需氨基酸。
在某些实施方案中,液体组合物包含至少一种维生素。维生素可以选自维生素a、维生素b、维生素c、维生素d、维生素e、维生素k和胆碱。在一些实施方案中,维生素的量为至少、大约或不大于约0.00001、0.0001、0.001、0.01、0.1、1、25、50、75、100、125、150、175或200μm。维生素的量可以为约0.000010至200μm。在一些实施方案中,液体组合物包含约至少0.001、100或1000μm的至少一种维生素。在一个示例性的实施方案中,维生素是维生素c。在一个实施方案中,液体组合物包含至少约1μm的维生素c。液体组合物可以包含至少约7μm的维生素c。液体组合物可以包含至少约1、2、3、4、5、6、7、8、9或10μm的维生素c。在一个示例性的实施方案中,维生素是维生素b。在一些实施方案中,液体组合物包含0.000005至1500μm的所述维生素b,例如0.00005、0.0005、0.005、0.05、0.5、1、10、100、1000或1500μm。维生素b可以包括生物素、维生素b1、维生素b2、维生素b3、维生素b5、维生素b6、维生素b9和/或维生素b12。
在某些实施方案中,液体组合物包含谷氨酸。谷氨酸的量可以是至少、大约或不大于1、5、20、50、100、200、300、400、500、750或1000μm。谷氨酸的量可以是大约2-500、20-400、75-300或100-200μm。在一些实施方案中,谷氨酸的量使血液中的谷氨酸增加至少、大约或不超过25、50、75、100、125、150、175、200或300μm。在某些实施方案中,谷氨酸的量使血液中的谷氨酸增加至少150μm。
在某些实施方案中,液体组合物进一步包含必需脂肪酸,例如ω-6和ω-3脂肪酸。在一个实施方案中,必需脂肪酸是ω-3脂肪酸。必需脂肪酸的量可以是约100、150、200、250、300、350、400、450、500、600、700、800、900、1000、1500或2000mg/l。在一些实施方案中,必需氨基酸的量为200-350mg/l。
在某些实施方案中,液体组合物进一步包含至少一种矿物质。矿物质可以选自铁、铜、铬、氟化物、碘、锰、钼、硒和锌。在一个实施方案中,液体组合物包含至少5nm的矿物质。至少一种矿物质的量可以是5nm-5μm。在一个示例性的实施方案中,液体组合物包含1μm或更高。
本文所述的液体组合物包含至少一种离子。在某些实施方案中,至少一种离子的量为至少约0.1meq/l。至少一种离子的量可以为0.1-150meq/l。至少一种离子的量可以为至少约0.1、0.5、1、5、10、15、20、50、75、100、125或150meq/l。
在一些实施方案中,液体组合物基本上不含至少一种选自丙氨酸、天冬酰胺、天冬氨酸、半胱氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸和酪氨酸的非必需氨基酸。液体组合物可以基本上不含至少2、3、4、5、6、7、8或9种非必需氨基酸。液体组合物可以不含至少一种非必需氨基酸。液体组合物可以不含至少2、3、4、5、6、7、8或9种非必需氨基酸。液体组合物可以不含除谷氨酸以外的非必需氨基酸。或者,在某些实施方案中,液体组合物进一步包含至少一种非必需氨基酸。非必需氨基酸可以选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸和酪氨酸。在一个实施方案中,液体组合物包含至少两种非必需氨基酸。液体组合物可以包含至少三种非必需氨基酸。液体组合物可以包含至少四种非必需氨基酸。液体组合物可以包含至少五种非必需氨基酸。液体组合物可以包含至少六种非必需氨基酸。液体组合物可以包含至少七种非必需氨基酸。液体组合物可以包含至少八种非必需氨基酸。液体组合物可以包含至少九种非必需氨基酸。在一个实施方案中,非必需氨基酸的量为至少约5μm,例如5、10、50、75、100、125、150、175、200、225、250、275、300、325、350、375、400、425、450、475、500、525、550、575、600、625、650、675或700μm。非必需氨基酸的量可以是5-600μm。
液体组合物可以包含小于约5μm的半胱氨酸和/或胱氨酸。例如,半胱氨酸和/或胱氨酸的量可以是0、0.1、0.5、1、1.5、2、2.5、3、3.5、4、4.5或5μm。在某些实施方案中,液体组合物包含0-4μm的半胱氨酸和/或胱氨酸。液体组合物可以包含0-2.5μm的半胱氨酸和/或胱氨酸,例如0-1μm的半胱氨酸和/或胱氨酸。在一个示例性的实施方案中,液体组合物基本上不含半胱氨酸和/或胱氨酸。液体组合物可以不含半胱氨酸和/或胱氨酸。
在某些实施方案中,液体组合物的ph为5.0-6.5。液体组合物的ph可以为5.5-6.0。例如,液体组合物的ph可以为约6.0。液体组合物的ph可以为约5.5。液体组合物的ph可以为约5.0。
在某些实施方案中,液体组合物的同渗容摩为300-500。液体组合物的同渗容摩可以为300-400。在一个实施方案中,液体组合物的同渗容摩为300-350。液体组合物的同渗容摩可以为400-500。
液体组合物包含水溶液,该水溶液可以是无菌溶液或非无菌溶液。在一些实施方案中,水溶液是无菌的。在其他实施方案中,水溶液是非无菌的。液体组合物可以储存在由受试者即用的容器中。容器可以包含足够量的液体组合物,以用于本文所述的任何方法中。例如,该容器可以容纳大约1、2或2.5升的液体组合物。液体组合物可以作为即用型透析溶液获得。
干燥组合物/浓缩组合物
本公开内容提供了透析组合物。透析组合物可以是干燥组合物或浓缩组合物的形式。在一些方面,本公开内容提供了包含谷氨酸的干燥组合物或浓缩组合物。在一些实施方案中,干燥组合物或浓缩组合物包含谷氨酸和至少一种必需氨基酸。本公开内容还提供了包含至少一种维生素的透析组合物。在一些实施方案中,干燥组合物或浓缩组合物包含至少一种维生素和至少一种必需氨基酸。在一些实施方案中,干燥组合物或浓缩组合物基本上不含半胱氨酸和/或胱氨酸。
在一些方面,本公开内容提供了一种干燥组合物,其包含:(a)碳水化合物;(b)至少一种维生素;(c)至少一种选自钠、钙、镁、氯和乳酸根的离子;(d)至少一种必需氨基酸;以及(e)水溶液,其中所述干燥组合物任选地包含谷氨酸,其中所述干燥组合物包含0-5μm的半胱氨酸和/或胱氨酸。在一些方面,本公开内容提供了一种干燥组合物,其包含:(a)碳水化合物;(b)谷氨酸;(c)至少一种维生素;(d)至少一种选自钠、钙、镁、氯和乳酸根的离子;以及(e)至少一种必需氨基酸,其中所述干燥组合物包含0-10mg的半胱氨酸和/或胱氨酸。
在一些方面,本公开内容提供了一种干燥组合物,其包含:(a)碳水化合物;(b)至少一种维生素;(c)至少一种选自钠、钙、镁、氯和乳酸根的离子;(d)至少一种必需氨基酸;以及(e)水溶液,其中所述液体组合物任选地包含谷氨酸,其中所述干燥组合物基本上不含选自丙氨酸、天冬酰胺、天冬氨酸、半胱氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸和酪氨酸的非必需氨基酸,并且其中所述干燥组合物包含0-5μm的半胱氨酸和/或胱氨酸。在一些方面,本公开内容提供了一种干燥组合物,其包含:(a)碳水化合物;(b)谷氨酸;(c)至少一种选自钠、钙、镁、氯和乳酸根的离子;以及(d)至少一种必需氨基酸,其中所述干燥组合物基本上不含除谷氨酸以外的非必需氨基酸,并且其中所述干燥组合物包含0-10mg的半胱氨酸和/或胱氨酸。
在一些方面,本公开内容提供了一种干燥组合物,其包含:(a)右旋糖;(b)至少一种选自钠、钙、镁、氯和乳酸根的离子;以及(c)至少一种必需氨基酸,其中所述干燥组合物包含至少2μg的必需氨基酸,并且其中所述干燥组合物包含0-10μg的半胱氨酸和/或胱氨酸。
在一些方面,本公开内容提供了一种干燥组合物,其包含:(a)碳水化合物;(b)至少一种必需氨基酸,其中所述干燥组合物包含0-10μg的半胱氨酸和/或胱氨酸。
本文所述的干燥组合物可能是有利的,因为其可以使水的存储空间、重量和运输最小化,并且还可以增加稳定性,并因此还增加透析组分的保存期限。干燥组合物对于长期储存和运输可以是稳定的。干燥组合物可以在容器中获得,其中可以将水溶液添加到容器中以重构其中的内容物。容器可以具有容纳大约1、2、2.5、4或10升水溶液的容积。在将组合物施用于受试者以进行透析之前,可以将水溶液添加到容器中。
在一些实施方案中,碳水化合物选自右旋糖、葡萄糖、蔗糖、果糖和乳糖。在一个示例性的实施方案中,碳水化合物是右旋糖。干燥组合物中右旋糖的量可以在0.1g至75g的范围内。在某些实施方案中,右旋糖的量为约5-75g。右旋糖的量可以是约5、10、15、20、25、30、35、40、45、50、55、60、65、70或75g。右旋糖的量可以是10-50g。在一个实施方案中,右旋糖的量为约10g。在一个实施方案中,右旋糖的量为约50g。在另一个实施方案中,右旋糖的量为0.1g-5g。右旋糖的量可以是约0.1、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5或5.0g。右旋糖的量可以是0.5-2.5g。在一个实施方案中,右旋糖的量为约0.5g。在一个实施方案中,右旋糖的量为约2g。在某些实施方案中,右旋糖的量为总组合物的约10-99.5%。例如,右旋糖的量可以是总组合物的10、20、30、40、50、60、70、75、80、85、90、95或99.5%。在一个示例性的实施方案中,右旋糖的量为总组合物的70-95%。
在某些实施方案中,干燥组合物包含至少一种必需氨基酸,该必需氨基酸选自组氨酸、异亮氨酸、亮氨酸、赖氨酸、甲硫氨酸、苯丙氨酸、苏氨酸、色氨酸、缬氨酸和精氨酸。在一个示例性的实施方案中,至少一种必需氨基酸是甲硫氨酸。在一个示例性的实施方案中,至少一种必需氨基酸是精氨酸。在某些实施方案中,每种必需氨基酸的量为至少2μg。每种必需氨基酸的量可以为至少、大约或不超过1、2、5、10、15、20、25、30、40、50、60、70、80、90、100、300、500、1000或1500μg。必需氨基酸的总量可以是至少、大约或不大于100、150、200、250、300、500、1000、2000、3000、5000、6000、7000、7500或8000μg。
在一个实施方案中,干燥组合物包含至少两种必需氨基酸。干燥组合物可以包含至少三种必需氨基酸。干燥组合物可以包含至少四种必需氨基酸。干燥组合物可以包含至少五种必需氨基酸。干燥组合物可以包含至少六种必需氨基酸。干燥组合物可以包含至少七种必需氨基酸。干燥组合物可以包含至少八种必需氨基酸。干燥组合物可以包含至少九种必需氨基酸。干燥组合物可以包含至少十种必需氨基酸。
在某些实施方案中,干燥组合物包含至少一种维生素。维生素可以选自维生素a、维生素b、维生素c、维生素d、维生素e、维生素k和胆碱。在某些实施方案中,维生素的量至少为、大约或不超过0.01、0.05、0.1、0.5、1、10、50、100、500、750、1000、1250或1500μg。维生素的量可以为约0.01至1500μg。在一个示例性的实施方案中,维生素是维生素c。干燥组合物可以包含至少约1000μg的维生素c,例如约1000、1300、1400、1500、1600、1700、1800、1900、2000、2100、2200、2300、2400,2500、2600、2700、2800、2900或3000μg维生素c。在一个实施方案中,干燥组合物包含至少约2500μg维生素c。干燥组合物可以包含至少、大约或不超过0.01μg的维生素b,例如约0.01、0.05、0.1、0.5、1、1.5、5、10、50或100μg的维生素b。维生素b可以包括生物素、维生素b1、维生素b2、维生素b3、维生素b5、维生素b6、维生素b9和/或维生素b12。
在某些实施方案中,干燥组合物包含至少、大约或不超过0.1mg的谷氨酸,例如大约0.1、1、5、10、15、20、25、30、35、40、45或50mg。谷氨酸的量可以是0.1-50mg、5-25mg或25-45mg。
在某些实施方案中,干燥组合物进一步包含必需脂肪酸,例如ω-6和ω-3脂肪酸。在一个实施方案中,必需脂肪酸是ω-3脂肪酸。在一个实施方案中,必需脂肪酸是ω-3脂肪酸。必需脂肪酸的量可以是大约100、150、200、250、300、350、400、450、500、750、1000、1100、1200、1300、1400、1500、1600、1700、1800、1900或2000mg/l。在一些实施方案中,必需氨基酸的量是1200-1600mg/l。
在某些实施方案中,干燥组合物进一步包含至少一种矿物质。矿物质可以选自铁、铜、铬、氟化物、碘、锰、钼、硒和锌。在一个实施方案中,干燥组合物包含至少0.3μg的矿物质。例如,干燥组合物包含约0.1、1、10、50、75、100、150、200、250、300、350、400、450、500、750、1000、1250、1500、2000、2500、3000、3500、4000、4500、5000或7500μg。在一个示例性的实施方案中,干燥组合物包含约400μg。在另一个实施方案中,干燥组合物包含约800μg。
本文所述的干燥组合物包含至少一种离子。离子可以是但不限于钠、钙、镁、氯、乳酸根或其组合。在某些实施方案中,至少一种离子的量为至少约0.1μg。在一个实施方案中,至少一种离子的量为至少约0.5μg。离子的量可以为至少约0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0、1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9或2.0μg。在某些实施方案中,离子的量为至少约50μmol。在一个实施方案中,离子的量为至少约100μmol。离子的量可以为至少约200μmol。离子的量可以为至少约250μmol。离子的量可以是50-300μmol,例如50、60、70、80、90、100、110、120、130、140、150、160、170、180、190、200、210、220、230、240、250、260、270、280、290或300μmol。
在一些实施方案中,干燥组合物基本上不含至少一种选自丙氨酸、天冬酰胺、天冬氨酸、半胱氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸和酪氨酸的非必需氨基酸。干燥组合物可以基本上不含至少2、3、4、5、6、7、8或9种非必需氨基酸。该干燥组合物可以不含至少一种非必需氨基酸。干燥组合物可以不含至少2、3、4、5、6、7、8或9种非必需氨基酸。干燥组合物可以不含除谷氨酸以外的非必需氨基酸。或者,在某些实施方案中,干燥组合物进一步包含至少一种非必需氨基酸。非必需氨基酸可以选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸和酪氨酸。在一个实施方案中,干燥组合物包含至少两种非必需氨基酸。干燥组合物可以包含至少三种非必需氨基酸。干燥组合物可以包含至少四种非必需氨基酸。干燥组合物可以包含至少五种非必需氨基酸。干燥组合物可以包含至少六种非必需氨基酸。干燥组合物可以包含至少七种非必需氨基酸。干燥组合物可以包含至少八种非必需氨基酸。干燥组合物可以包含至少九种非必需氨基酸。在一个实施方案中,非必需氨基酸的量为至少1mg。非必需氨基酸的量可以是1-100mg。在一些实施方案中,非必需氨基酸的量是1-300mg,例如1、50、100、150、200、250或300mg。
本公开内容提供了包含少于10mg的半胱氨酸和/或胱氨酸的干燥组合物。例如,干燥组合物可以包含约0、0.5、1、1.5、2、2.5、3、3.5、4、4.5、5、5.5、6、6.5、7、7.5、8、8.5、9、9.5或10mg的半胱氨酸和/或胱氨酸。在某些实施方案中,干燥组合物包含0-10mg的半胱氨酸和/或胱氨酸。在一个实施方案中,干燥组合物包含0-2.5mg的半胱氨酸和/或胱氨酸。在一个示例性的实施方案中,干燥组合物基本上不含半胱氨酸和/或胱氨酸。干燥组合物可以不含半胱氨酸和/或胱氨酸。
在一个示例性的实施方案中,液体组合物或干燥组合物包含甲硫氨酸。液体组合物或干燥组合物的右旋糖与甲硫氨酸的摩尔比可以大于或小于约1、50、100、250、500、1,000、2,000、3,000、4,000、5,000、6,000、7,000、8,000、9,000、10,000、10,500、20,000、30,000、40,000、50,500、60,000、70,000、80,000、90,000或100,000。在一个示例性实施方案中,液体组合物或干燥组合物的右旋糖与甲硫氨酸的摩尔比大于或小于约250、500、1,000、2,000、3,000、4,000、5,000、6,000、7,000、8,000、9,000、10,000或10,500。在一个实施方案中,组合物的右旋糖与甲硫氨酸的摩尔比为约250。在另一个实施方案中,组合物的右旋糖与甲硫氨酸的摩尔比为约10,500。
液体组合物或干燥组合物的半胱氨酸与必需氨基酸的摩尔比可以小于0.01、0.02、0.03、0.04、0.05、0.06、0.08、0.09、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4、5、10、15、20、50或100。在一个实施方案中,半胱氨酸与甲硫氨酸的摩尔比小于0.01、0.02、0.03、0.04、0.05、0.06、0.08、0.09、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。
液体组合物或干燥组合物的甲硫氨酸与氨基酸的摩尔比可以大于约0.01、0.02、0.03、0.04、0.05、0.06、0.08、0.09、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4、5、10、15、20、50或100。在一些实施方案中,液体组合物和干燥组合物的甲硫氨酸与其他氨基酸的摩尔比可以大于约0.01、0.02、0.03、0.04、0.05、0.06、0.08、0.09、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。
在一些实施方案中,液体组合物或干燥组合物中的甲硫氨酸与丙氨酸的摩尔比大于约0.06、0.08、0.09、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与精氨酸的摩尔比大于约0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与天冬酰胺的摩尔比大于约0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与天冬氨酸的摩尔比大于约2、3、4、5、10、15、20、50或100。在一些实施方案中,甲硫氨酸与β-丙氨酸的摩尔比大于约1、2、3、4、5、10、15、20、50或100。在一些实施方案中,甲硫氨酸与胱氨酸的摩尔比大于约0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与谷氨酸的摩尔比大于约0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与谷氨酰胺的摩尔比大于约0.04、0.05、0.06、0.08、0.09、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与甘氨酸的摩尔比大于约0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与组氨酸的摩尔比大于约0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与异亮氨酸的摩尔比大于约0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与亮氨酸的摩尔比大于约0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与苯丙氨酸的摩尔比大于约0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与脯氨酸的摩尔比大于约0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与丝氨酸的摩尔比大于约0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与苏氨酸的摩尔比大于约0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与色氨酸的摩尔比大于约0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与酪氨酸的摩尔比大于约0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。在一些实施方案中,甲硫氨酸与缬氨酸的摩尔比大于约0.09、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4或5。
在某些实施方案中,干燥组合物或液体组合物中的甲硫氨酸与矿物质如铁、铜、铬、氟化物、碘、锰、钼、硒和锌的摩尔比大于约1、5、7、8、9、10、40、50、75、90、100、500、1,000、1,100、1,500、1,900、2,000、2,300、2,500、2,800、3,000、4,000、5,000、6,000、7,000、8,000、9,000或10,000。甲硫氨酸与铁的摩尔比可以大于约9、10、40、50、75、90、100、500或1,000。甲硫氨酸与铜的摩尔比可以大于约90、100、500、1,000、1,100、1,500、1,900或2,000。甲硫氨酸与铬的摩尔比可以大于约2,300、2,500、2,800、3,000、4,000、5,000、6,000、7,000、8,000、9,000或10,000。甲硫氨酸与氟化物的摩尔比可以大于约7、8、9、10、40、50、75、90、100、500或1,000。甲硫氨酸与碘化物的摩尔比可以大于约1,100、1,500、1,900、2,000、2,300、2,500、2,800、3,000、4,000、5,000、6,000、7,000、8,000、9,000或10,000。甲硫氨酸与锰的摩尔比可以大于约40、50、75、90、100、500或1,000。甲硫氨酸与钼的摩尔比可以大于约2,800、3,000、4,000、5,000、6,000、7,000、8,000、9,000或10,000。甲硫氨酸与硒的摩尔比可以大于约1,900、2,000、2,300、2,500、2,800、3,000、4,000、5,000、6,000、7,000、8,000、9,000或10,000。甲硫氨酸与锌的摩尔比可以大于约8、9、10、40、50、75、90、100、500或1,000。
一些实施方案中,干燥组合物、浓缩组合物或液体组合物包含一种或多种组分,例如右旋糖、离子、缓冲剂、氨基酸、维生素和矿物质,以摩尔比(右旋糖:组分)计,如下表1所示。
表1:干燥组合物、浓缩组合物和液体组合物组分
干燥组合物也可以浓缩形式获得。在一些方面,本发明提供了浓缩组合物,其包含本文所述的干燥组合物和初始水溶液。本文所述的浓缩组合物可能是有利的,因为其可以使水的储存空间、重量和运输最小化,并且还可以增加稳定性,并因此还增加透析组分的保存期限。浓缩组合物对于长期储存和运输而言可能是稳定的。浓缩组合物可以在容器中获得,其中可以向该容器中添加另外的水溶液以使溶液达到一定体积,在该体积下,该浓缩组合物可以被受试者即用。该容器可以具有容纳大约1、2、2.5、4或10升的总水溶液的容积。在施用于受试者以进行透析之前,可以将另外的水溶液添加至浓缩组合物。
食品组合物
在一些方面,本公开内容提供了一种食品组合物,其包含:(a)不含半胱氨酸的蛋白质源;(b)至少一种必需氨基酸;以及(c)至少一种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的非必需氨基酸,其中每种非必需氨基酸是食品组合物的蛋白质的0-1%wt/wt,其中食品组合物包含为食品组合物的蛋白质的0-1%wt/wt的半胱氨酸和/或胱氨酸,并且其中食品组合物包含至少6%wt/wt的蛋白质。
在某些实施方案中,选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的每种非必需氨基酸的量为食品组合物中蛋白质的0-2%wt/wt。每种非必需氨基酸的量可以为蛋白质的大约0.01、0.02、0.03、0.04、0.05、0.06、0.07、0.08、0.09、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0、1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9或2.0%wt/wt。每种非必需氨基酸的量可以为食品组合物中蛋白质的0-1%wt/wt。在一个实施方案中,每种非必需氨基酸的量为食品组合物中蛋白质的0-0.1%wt/wt。在一些实施方案中,食品组合物包含至少两种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的非必需氨基酸。食品组合物可以包含至少三种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的非必需氨基酸。食品组合物可以包含至少四种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的非必需氨基酸。食品组合物可以包含至少五种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的非必需氨基酸。食品组合物可以包含至少六种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸和脯氨酸的非必需氨基酸。在一些实施方案中,至少一种非必需氨基酸是甘氨酸。在一些实施方案中,至少一种非必需氨基酸是脯氨酸。
在某些实施方案中,半胱氨酸和/或胱氨酸的量为食品组合物中蛋白质的0-2%wt/wt。半胱氨酸和/或胱氨酸的量可以是食品组合物中蛋白质的0-1%wt/wt,例如蛋白质的0、0.01、0.02、0.03、0.04、0.05、0.06、0.07、0.08、0.09、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9或1%wt/wt。在一个示例性的实施方案中,半胱氨酸和/或胱氨酸的量为食品组合物中蛋白质的0-0.2%wt/wt。在一个实施方案中,半胱氨酸和/或胱氨酸的量为食品组合物中蛋白质的约0-0.1%wt/wt。在另一个实施方案中,半胱氨酸和/或胱氨酸的量为食品组合物的0-0.04%wt/wt,例如食品组合物的约0、0.01、0.02、0.03或0.04%wt/wt。
在一些方面,本公开内容提供了一种食品组合物,其包含:(a)不含半胱氨酸的蛋白质源;(b)至少一种必需氨基酸;以及(c)至少六种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸的非必需氨基酸,其中每种非必需氨基酸为食品组合物中蛋白质的0-1%wt/wt,并且其中食品组合物包含至少6%wt/wt的蛋白质。
在一些方面,本公开内容提供了一种食品组合物,其包含:(a)至少一种必需氨基酸;和(b)谷氨酸,其中食品组合物基本上不含除谷氨酸以外的非必需氨基酸。在一些方面,本公开内容提供了一种食品组合物,其包含:(a)至少一种必需氨基酸;(b)谷氨酸;以及(c)精氨酸,其中食品组合物基本上不含除谷氨酸以外的非必需氨基酸。
在某些实施方案中,选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸的每种非必需氨基酸的量为食品组合物中蛋白质的0-2%wt/wt。每种非必需氨基酸的量可以为蛋白质的大约0.01、0.02、0.03、0.04、0.05、0.06、0.07、0.08、0.09、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0、1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9或2.0%wt/wt。每种非必需氨基酸的量可以为食品组合物中蛋白质的0-1%wt/wt。在一个实施方案中,每种非必需氨基酸的量为食品组合物中蛋白质的0-0.1%wt/wt。
在一些实施方案中,食品组合物包含至少七种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸的非必需氨基酸。食品组合物可以包含至少八种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸的非必需氨基酸。食品组合物可以包含至少九种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸的非必需氨基酸。食品组合物可以包含至少十种选自丙氨酸、天冬酰胺、天冬氨酸、谷氨酸、甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸的非必需氨基酸。食品组合物可以包含至少六种非必需氨基酸,所述非必需氨基酸选自甘氨酸、脯氨酸、谷氨酰胺、丝氨酸、酪氨酸和半胱氨酸。在一些实施方案中,至少一种非必需氨基酸是甘氨酸。在一些实施方案中,至少一种非必需氨基酸是脯氨酸。在一个示例性的实施方案中,至少一种非必需氨基酸是半胱氨酸。当食品组合物包含半胱氨酸时,半胱氨酸和/或胱氨酸的量为食品组合物中蛋白质的0-2%wt/wt。半胱氨酸和/或胱氨酸的量可以为食品组合物中蛋白质的约0-1%wt/wt,例如蛋白质的约0、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9或1%wt/wt。在一个示例性的实施方案中,半胱氨酸和/或胱氨酸的量为食品组合物中蛋白质的0-0.2%wt/wt。在一个实施方案中,半胱氨酸和/或胱氨酸的量为食品组合物中蛋白质的0-0.1%wt/wt。在另一个实施方案中,半胱氨酸和/或胱氨酸的量为食品组合物的0-0.04%wt/wt,例如食品组合物的约0、0.01、0.02、0.03或0.04%wt/wt。在一个示例性的实施方案中,食品组合物基本上不含半胱氨酸和/或胱氨酸。食品组合物可以不含半胱氨酸和/或胱氨酸。
在某些实施方案中,如本文所述的任何食品组合物,不含半胱氨酸的蛋白质源的量为食品组合物的至少1%wt/wt。不含半胱氨酸的蛋白质源可以是明胶。不含半胱氨酸的蛋白质源的量可以是食品组合物的0.1、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5、8.0、8.5、9.0、9.5或10.0%wt/wt。在一些实施方案中,不含半胱氨酸的蛋白质源的量为食品组合物的1-5%。
在某些实施方案中,如本文所述的任何食品组合物,蛋白质的量为食品组合物总重量的至少约5%。食品组合物中蛋白质的量可以为食品组合物总重量的大约5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或25%。在一个实施方案中,蛋白质的量为食品组合物总重量的约6%。在另一个实施方案中,蛋白质的量为食品组合物总重量的约16%。
在某些实施方案中,如本文所述的任何食品组合物,必需氨基酸选自精氨酸、组氨酸、异亮氨酸、亮氨酸、赖氨酸、甲硫氨酸、苯丙氨酸、苏氨酸、色氨酸和缬氨酸。在一个示例性的实施方案中,必需氨基酸是甲硫氨酸。在一个示例性的实施方案中,必需氨基酸是精氨酸。必需氨基酸可以是食品组合物的大约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、45、50、55、60、65、70或75%wt/wt。在一些实施方案中,必需氨基酸为食品组合物的至少约2%wt/wt。必需氨基酸的量可以为食品组合物的2-30%wt/wt。在一个示例性的实施方案中,必需氨基酸的量为食品组合物的约8%wt/wt。
在一个实施方案中,食品组合物包含至少两种必需氨基酸。食品组合物可以包含至少三种必需氨基酸。食品组合物可以包含至少四种必需氨基酸。食品组合物可以包含至少五种必需氨基酸。食品组合物可以包含至少六种必需氨基酸。食品组合物可以包含至少七种必需氨基酸。食品组合物可以包含至少八种必需氨基酸。食品组合物可以包含至少九种必需氨基酸。食品组合物可以包含至少十种必需氨基酸。
本文所述的任何食品组合物可以进一步包含至少一种维生素。维生素可以选自维生素a、维生素b、维生素c、维生素d、维生素e、维生素k和胆碱。在一个示例性的实施方案中,维生素是维生素c。在一个实施方案中,食品组合物包含至少约10mg的维生素c/千克的食品组合物。食品组合物可以包含约10、15、20、25、30、40、45、50、55或60mg的维生素c/千克的食品组合物。在一个示例性的实施方案中,食品组合物包含约40mg的维生素c/千克的食品组合物。
在某些实施方案中,本文所述的任何食品组合物进一步包含必需脂肪酸,例如ω-6脂肪酸和ω-3脂肪酸。在一个实施方案中,必需脂肪酸是ω-3脂肪酸。必需脂肪酸的量可以是大约100、150、200、250、300、350、400、450、500、750、1000、1100、1200、1300、1400、1500、1600、1700、1800、1900或2000mg/l。在一些实施方案中,必需氨基酸的量是1200-1600mg/l。在一些实施方案中,必需氨基酸的量为100-200mg/l。
在某些实施方案中,本文所述的任何食品组合物进一步包含至少一种矿物质。矿物质可以选自铁、铜、铬、氟化物、碘、锰、钼、硒和锌。在一个实施方案中,食品组合物包含在食品组合物中的至少约1%w/w的矿物质,例如1、2、3、4或5%w/w的矿物质。至少一种矿物质的量可以是0.05mg-20g/千克食品组合物,例如大约0.1、1、10、50、100、500、1,000、5,000、10,000或20,000mg的矿物质/千克食品组合物。
本文所述的任何食品组合物进一步包含至少一种离子。在某些实施方案中,至少一种离子的量为食品组合物中离子的至少0.1%w/w,例如0.1、0.5、1.0、1.5、2.0、2.5、3.0%w/w。至少一种离子的量可以是0.05-20g/千克食物,例如约0.05、0.1、1、5、10、15或20g离子/千克食品组合物。
本文所述的任何食品组合物进一步包含谷氨酸。在一些实施方案中,食品组合物包含至少、大约或不超过0.1mg的谷氨酸,例如大约0.1、1、5、10、15、20、25、30、35、40、45或50mg。谷氨酸的量可以是0.1-50mg、5-25mg或25-45mg。
在一些实施方案中,本文所述的任何食品组合物包含至少约10%wt/wt的氨基酸,例如10、11、12、13、14、15、16、17、18、19或20%w/w的氨基酸。在一些实施方案中,食品组合物包含约14%wt/wt的氨基酸。在一些实施方案中,食品组合物包含约17%wt/wt的氨基酸。在一些实施方案中,食品组合物包含10-20%w/w的总氨基酸。食品组合物可以包含14-17%w/w的总氨基酸。
在某些实施方案中,如本文所述的任何食品组合物,食品组合物进一步包含药物活性剂。本文所述的食品组合物中使用的药剂或任何其他组分的量可以以治疗有效量使用。可以针对每个受试者或受试者组评估治疗量。受试者组可以是所有潜在受试者,或具有特定特征(例如年龄、体重、种族、性别或体育锻炼水平)的受试者。药物活性剂可以包括抗癌治疗剂,例如美司钠(mesna)。提供给受试者的药物活性剂可以是约5、10、50、100、500、1000、1200、1500、2000、2500或3000mg。在一些实施方案中,提供给受试者的药物活性剂是10-2000mg。在一些实施方案中,提供给受试者的美司钠为200-1200mg。在一些实施方案中,药物活性剂是抗肥胖治疗剂。
使用方法
本发明提供了在有需要的受试者中治疗(包括预防)癌症、代谢性疾病例如肥胖症和/或肾脏疾病的方法。该方法可以包括减少、消耗和/或补充受试者饮食中的某些营养素。该方法可以包括向受试者施用本文所述的具有不超过特定量的预选营养素的食品组合物。减少或耗尽的营养素可以是与非癌细胞相比,癌细胞对其具有更高水平或更高程度的需求的某些营养素。可以通过向受试者施用食品组合物来控制受试者的饮食,其中受试者除了是该食品组合物的一部分或在该方案允许的范围内的那些之外不食用任何其他食物或营养素。因此,食品组合物可以由提供给受试者的所有食物组成,并且食品组合物可以仅具有一定量的预选营养素。可以设计食品组合物,使得以每小时、每天、每周或每月为基础来评估或确定提供给受试者或由受试者摄取的营养。对于本文提供的以每天为基础所描述的任何数值,本发明在每小时、每周或每月的基础上提供所述量按比例缩放的数值。可以将食品组合物单独提供给受试者或与干燥组合物、浓缩组合物或液体组合物组合提供给受试者,直到在受试者中看到一致且显著的改善,并且可以在治疗的任何时候对其进行修改以适应受试者的需求。
本文所述的方法还包括通过透析来减少、消耗和/或补充受试者系统(例如血液水平)中的某些营养素。本公开内容设想了执行透析的方法。用于执行透析的透析机,例如freedomcycler(freseniusmedicalcare)、homechoiceprotm(baxterhealthcarecorporation)、homechoicetm(baxterhealthcarecorporation)、
可以设计干燥组合物、浓缩组合物或液体组合物,使得以每小时、每天、每周或每月为基础评估或确定提供给受试者的营养素。对于本文提供的以每天为基础所描述的任何数值,本发明在每小时、每周或每月的基础上提供所述量按比例缩放的数值。可以将干燥组合物、浓缩组合物或液体组合物单独或与食品组合物一起提供给受试者,直到在受试者中看到一致且显著的改善,并且可以在治疗的任何时候对其进行修改以适应受试者的需求。
在一些实施方案中,受试者经历腹膜透析。腹膜透析可涉及将诸如导管的柔性管插入受试者中。导管可以通过受试者皮肤的切口进入受试者的腹部或胸腔,再到达受试者的体外。导管可以用透析液填充腹部。图14示出了示例性的透析系统。
在一些实施方案中,受试者经历血液透析。
治疗癌症
本文所述的方法可以包括提供本文所述的组合物。在一些方面,本公开内容提供了一种用于在有需要的受试者中治疗癌症的方法,该方法包括向受试者施用本文所述的任何食品组合物,以及向受试者施用本文所述的液体组合物、本文所述的干燥组合物,或本文所述的浓缩组合物。
在一些方面,本公开内容提供了一种用于在有需要的受试者中治疗癌症的方法,该方法包括向受试者施用本文所述的液体组合物、本文所述的干燥组合物或本文所述的浓缩组合物。
在一些方面,本公开内容提供了一种用于在有需要的受试者中治疗癌症的方法,该方法包括向受试者施用本文所述的任何食品组合物。
在某些实施方案中,治疗癌症的特征在于肿瘤大小的减小。肿瘤大小可以减小治疗前初始肿瘤大小的至少10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或100%。肿瘤可以减小至少30%。肿瘤可以减小至少50%。肿瘤可以减小至少80%。肿瘤大小的减小可以是10-100%。肿瘤大小的减小可以是30-100%。
在某些实施方案中,治疗癌症的特征在于循环癌细胞计数的减少。循环癌细胞计数可以减少治疗前的初始循环癌细胞计数的至少10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或100%。循环癌细胞计数可以减少至少30%。循环癌细胞计数可以减少至少50%。循环癌细胞计数可以减少至少80%。循环癌细胞计数的减少可以是10-100%。循环癌细胞计数的减少可以是30-100%。
本公开内容的方法包括监测受试者血液中半胱氨酸和/或胱氨酸的水平。监测半胱氨酸和/或胱氨酸可用于修改现有治疗,以将半胱氨酸和/或胱氨酸的水平降低至治疗水平。
在某些实施方案中,治疗癌症的特征在于血浆半胱氨酸水平降低。血浆半胱氨酸水平可以降低治疗前的初始血浆半胱氨酸水平的至少10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或100%。血浆半胱氨酸水平可以降低至少30%。血浆半胱氨酸水平可以降低至少50%。血浆半胱氨酸水平可以降低至少80%。血浆半胱氨酸水平可以降低至少90%。血浆半胱氨酸水平可以降低至少95%。血浆半胱氨酸水平可以是30-100%。
施用本文所述的组合物可导致半胱氨酸和/或胱氨酸的血液水平降低。可以以治疗量施用所述组合物。在施用本文所述的组合物之后,受试者血液中的半胱氨酸水平可以降低至低于半胱氨酸的平均水平,例如低于约10μm的半胱氨酸。在某些实施方案中,受试者血液中半胱氨酸的水平低于约9μm、8μm、7μm、6μm、5μm、4μm、3μm、2μm或1μm。在一个示例性实施方案中,受试者血液中半胱氨酸的水平大约低于1μm。在施用本文所述的组合物之后,受试者血液中的胱氨酸水平可以降低至低于胱氨酸的平均水平,如低于约40μm的胱氨酸。在某些实施方案中,受试者血液中的胱氨酸水平可以降低至低于约39μm、38μm、37μm、36μm、35μm、34μm、33μm、32μm、31μm、30μm、29μm、28μm、27μm、26μm、25μm、24μm、23μm、22μm、21μm、20μm、19μm、18μm、17μm、16μm、15μm、14μm、13μm、12μm、11μm、10μm、9μm、8μm、7μm、6μm、5μm、4μm、3μm、2μm或1μm。在一个示例性实施方案中,受试者血液中的胱氨酸水平约为低于5μm。
减小肿瘤大小
在一些方面,本公开内容提供了一种用于减小有需要的受试者的肿瘤大小和/或循环癌细胞计数的方法,该方法包括向受试者施用本文所述的任何食品组合物,以及向受试者施用本文所述的液体组合物、本文所述的干燥组合物或本文所述的浓缩组合物。
在一些方面,本公开内容提供了一种用于减小有需要的受试者中的肿瘤大小和/或循环癌细胞计数的方法,该方法包括向受试者施用权利要求1的液体组合物、本文所述的干燥组合物或本文所述的浓缩组合物。
在一些方面,本公开内容提供了一种用于减小有需要的受试者中的肿瘤大小和/或循环癌细胞计数的方法,该方法包括向受试者施用本文所述的任何食品组合物。
本公开内容的方法可以导致抑制受试者的肿瘤生长。在某些实施方案中,如初次施用本文所述的任何食品组合物并向受试者施用本文所述的液体组合物、本文所述的干燥组合物或本文所述的浓缩组合物之前和施用本文所述的任何食品组合物并向受试者施用本文所述的液体组合物、本文所述的干燥组合物或本文所述的浓缩组合物后6周所测得,受试者的肿瘤大小不增加大于0-100%,例如约0、10、20、30、40、50、60、70、80、90或100%。如初次施用本文所述的任何食品组合物并向受试者施用本文所述的液体组合物、本文所述的干燥组合物或本文所述的浓缩组合物之前和施用本文所述的任何食品组合物并向受试者施用本文所述的液体组合物、本文所述的干燥组合物或本文所述的浓缩组合物后6周所测得,受试者的肿瘤大小不会增加大于约100%。如初次施用前和施用后6周所测得,受试者的肿瘤大小不会增加大于约70%。如初次施用前和施用后6周所测得,受试者的肿瘤大小不会增加大于约60%。如初次施用前和施用后6周所测得,受试者的肿瘤大小不会增加大于约40%。如初次施用前和施用后6周所测得,受试者的肿瘤大小不会增加大于约20%。如初次施用前和施用后6周所测得,受试者的肿瘤大小不会增加大于约0%。
在某些实施方案中,如初次施用本文所述的任何食品组合物并向受试者施用本文所述的液体组合物、本文所述的干燥组合物或本文所述的浓缩组合物之前和施用本文所述的任何食品组合物并向受试者施用本文所述的液体组合物、本文所述的干燥组合物或本文所述的浓缩组合物后6周所测得,受试者的肿瘤大小减小至少10%,如初次施用前和初次施用后6周所测得,受试者的肿瘤大小可减小至少20%。如初次施用前和初次施用后6周所测得,受试者的肿瘤大小可减小至少30%。如初次施用前和施用后6周所测得,受试者的肿瘤大小可减小至少40%。如初次施用前和施用后6周所测得,受试者的肿瘤大小可减小至少50%。
本公开内容的方法可以导致循环癌细胞计数的减少。循环癌细胞计数可减少治疗前的初始循环癌细胞计数的至少10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或100%。循环癌细胞计数可减少至少30%。循环癌细胞计数可减少至少50%。循环癌细胞计数可减少至少80%。循环癌细胞计数可减少10-100%。循环癌细胞计数可减少30-100%。
治疗肥胖症
在一些方面,本公开内容提供了一种用于在有需要的受试者中治疗肥胖症的方法,该方法包括向受试者施用本文所述的任何食品组合物。
治疗肥胖症的特征可以在于受试者的体重减轻。从使用本文公开的食品组合物进行营养饮食开始,受试者可以经历至少或大约5%、10%、15%、20%、25%、30%、35%、40%、45%或50%的体重减轻。在某些实施方案中,如开始控制饮食之前和开始控制饮食之后6周所测得,受试者的体重减轻大于5%。控制饮食包括向有需要的受试者施用本文所述的食品组合物。如开始控制饮食之前和开始控制饮食之后6周所测得,受试者的体重减轻可大于10%。从开始控制饮食之前和开始控制饮食之后6周所测得,受试者的体重减轻可大于15%。如开始控制饮食之前和开始控制饮食之后6周所测得,受试者的体重减轻可大于20%。从开始控制饮食之前和开始控制饮食之后6周所测得,受试者的体重减轻可大于25%。从开始控制饮食之前和开始控制饮食之后6周所测得,受试者的体重减轻可大于30%。
治疗肾脏疾病
在一些方面,本公开内容提供了一种用于在有需要的受试者中治疗肾脏疾病的方法,该方法包括向受试者施用本文所述的液体组合物、本文所述的干燥组合物或浓缩组合物。本公开内容的方法可以向受试者提供或消耗某些营养素。受试者可能由于透析而经历营养不良、营养不足或其他副作用,而施用液体组合物、干燥组合物或浓缩组合物的可以预防、减缓、减轻或消除此类副作用。其他副作用可能包括但不限于低血压、恶心、呕吐、皮肤干痒、下肢不宁综合征、肌痛性痉挛或其组合。对于本文所述的施用液体组合物或干燥组合物的方法,在某些实施方案中,该方法进一步包括利用膜。膜可以包括改性的二乙酸纤维素或聚砜。在一个示例性的实施方案中,该膜是允许小分子交换的低通量膜。在一些实施方案中,低通量膜包括多个孔,其中多个孔包括第一端和第二端。在一些实施方案中,低通量膜包括多个孔。多个孔可以具有约1.8nm的平均孔径。在一些实施方案中,低通量膜允许约50%或以上的重约500道尔顿或以下的分子穿过多个孔从第一端移动到第二端。低通量膜可以允许约75%或以上的重约500道尔顿或以下的分子穿过多个孔从第一端移动到第二端。在一些实施方案中,低通量膜允许约90%或以上的重约500道尔顿或以下的分子穿过多个孔从第一端移动到第二端。低通量膜可以允许约95%或以上的重约500道尔顿或以下的分子穿过多个孔从第一端移动第二端。在一些实施方案中,约20%的至少1000道尔顿的分子穿过多个孔从第一端到第二端。约10%的至少1000道尔顿的分子可以从第一侧通过到第二侧。约1%的至少1000道尔顿的分子可以从第一侧通过到第二侧。
对于本文所述的任何方法,该方法可以进一步包括施用药物活性剂。药物活性剂可以是抗癌治疗剂。抗癌药的实例包括
在一个实施方案中,以亚治疗量提供药物活性剂。本文所述的组合组合物中使用的药剂或任何其他组分的量可以以亚治疗量使用。在一些实施方案中,使用亚治疗量的药剂或组分可以减少该药剂的副作用。亚治疗量的使用仍然可以有效,特别是与其他药剂或组分协同使用时。药剂或组分的亚治疗量可以使得低于该量的量将被认为是治疗性的。例如,fda指南可以建议治疗特定病症的指定剂量水平,并且亚治疗量可以是低于fda建议剂量水平的任何水平。亚治疗量可以比被认为是治疗量的量的少约1%、5%、10%、15%、20%、25%、30%、35%、50%、75%、90%或95%。可以针对每个受试者或受试者组评估治疗量。受试者组可以是所有潜在受试者,或具有特定特征(例如年龄、体重、种族、性别或体育锻炼水平)的受试者。
对于本文所述的任何方法,在某些实施方案中,所述方法可以进一步包括施用营养补充剂。在一些实施方案中,营养补充剂包含一种或多种营养素,该营养素可以包括维生素、矿物质、水、碳水化合物、脂肪、蛋白质及其组合。营养补充剂可以包装为维生素、矿物质、草药、膳食补充剂、运动营养产品、天然食品补充剂和强化食品。该营养补充剂可以包含至少一种选自精氨酸、组氨酸、异亮氨酸、赖氨酸、甲硫氨酸、苯丙氨酸、苏氨酸、色氨酸和缬氨酸的氨基酸。营养补充剂可以按照膳食参考摄入量(dri)、参考每日摄入量(rdi)、世界卫生组织(who)指南、推荐膳食摄入量(rda)、适宜摄入量(ais)和/或每日量值(dv)的水平向受试者提供营养素。成人、儿童、男人和女人所需的营养素水平可以相同或不同。在某些实施方案中,营养补充剂包含一种或多种选自维生素a、硫胺素、核黄素、烟酸、泛酸、维生素b6、生物素、叶酸、氰钴胺素、维生素c、维生素d、维生素e、维生素k和胆碱的营养素。在某些实施方案中,营养补充剂包含一种或多种选自钙、氯化物、铬、铜、氟化物、碘、铁、镁、锰、钼、磷、钾、硒、钠和锌的营养素。在某些实施方案中,营养补充剂包含一种或多种选自水、碳水化合物、蛋白质、纤维、脂肪、胆固醇和脂肪酸的营养素。
剂量、治疗方案和施用
仅透析
本公开内容提供了向有需要的受试者提供透析疗法的方法。对于本文所述的施用本文所述的液体组合物、干燥组合物或浓缩组合物的方法,所述液体组合物、干燥组合物或浓缩组合物可以通过传统的透析方法施用。例如,可以通过血液透析、腹膜透析、血液滤过、血液透析滤过和肠道透析来施用所述组合物。在一个示例性的实施方案中,通过血液透析或腹膜透析(例如连续不卧床pd(capd)和连续循环仪辅助pd(ccpd))施用所述组合物。透析治疗可以与其他治疗癌症、肥胖症和肾脏疾病的常规方法(例如外科手术、放射疗法、免疫疗法、抗癌疗法、抗肥胖疗法或肾脏疾病疗法)联合使用。
对于本文所述的施用本文所述的液体组合物、干燥组合物或浓缩组合物的方法,在某些实施方案中,每周至少一次向受试者施用所述组合物。可以每周至少三次向受试者施用所述组合物。可以每周至少五次向受试者施用所述组合物。在一些实施方案中,在至少一周的过程中向受试者施用所述组合物。可以在至少四周的过程中向受试者施用所述组合物。可以在至少2个月的过程中向受试者施用所述组合物。可以在至少3个月的过程中向受试者施用所述组合物。
在一些实施方案中,可以在透析中心、医院、诊所、保健设施、在家中或在任何清洁且干燥的地方将透析提供给有需要的受试者。
仅饮食
对于本文所述的方法,可以每周多次施用本文所述的任何食品组合物,例如每周1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30或更多次。在某些实施方案中,每周至少一次向受试者施用所述食品组合物。可以每周至少三次向受试者施用所述食品组合物。可以每周至少五次向受试者施用所述食品组合物。在一个实施方案中,可以每周至少21次向受试者施用所述食品组合物。在一些实施方案中,可以在至少一周的过程中向受试者施用所述食品组合物。可以在至少四周的过程中向受试者施用所述食品组合物。可以在至少2个月的过程中向受试者施用所述食品组合物。可以在至少3个月的过程中向受试者施用所述食品组合物。
透析与饮食
在本文描述的任何方法中,在某些实施方案中,将本文所述的液体组合物、干燥组合物或浓缩组合物与本文所述的任何食品组合物顺序地施用于受试者。在另一个实施方案中,将本文所述的液体组合物、干燥组合物或浓缩组合物与本文所述的任何食品组合物同时施用于受试者。在一些实施方案,至少每周一次将食品组合物以及液体组合物、干燥组合物或浓缩组合物施用于受试者。可以每周至少三次将食品组合物以及液体组合物、干燥组合物或浓缩组合物施用于受试者。可以在至少一周的过程中将食品组合物以及液体组合物、干燥组合物或浓缩组合物施用于受试者。可以在至少四周的过程中将食品组合物以及液体组合物、干燥组合物或浓缩组合物施用于受试者。
药物组合物和制剂
饮食
本文所述的任何食品组合物可以具有预选的热值。例如,食品组合物可以包含至少10、20、50、100、200、300、400、500、600、700、800、900、1000或1500kcal。食品组合物可以具有0-100、0-200、200-400、400-600、600-800、800-1000或500-1000kcal的热值。食品组合物可以具有至少5、10、50、100、200、300、400、500、600、700或1000克的质量。食品组合物可以具有0-100、100-200、200-400、400-600或100-500克的质量。
本文所述的任何食品组合物可以在包装容器中出售给受试者。在某些实施方案中,食品组合物包装为固体食物、半固体食物或饮料。食品组合物可以是营养成分的调制品、速食混合物、可微波的冷冻糊剂、可烘烤或可烘焙的面团,或几种营养素模块与香料品种的可定制混合物。在一些实施方案中,食品组合物可以被烹饪、部分烹饪或未烹饪。例如,食品组合物可以是婴儿配方、软饮料、无果肉果汁、营养奶昔、燕麦棒、甜点或糖果。在一些实施方案中,食品组合物用维生素、矿物质、草药、营养素及其组合强化。食品组合物可以包装为选自零食棒、谷物产品、烘焙产品和乳制品的食品。例如,食品组合物可以是婴儿配方或婴儿食品。食品组合物可以是软饮料。食品组合物可以是营养奶昔或营养小吃,例如燕麦棒。食品组合物可以是代餐饮料或小吃。食品组合物可以具有适口性增强剂。适口性增强剂可以是msg,或一些其他形式的谷氨酸盐。
在一些实施方案中,食品组合物是宠物食品。宠物食品可以是湿的或干的宠物食品。宠物食品可以形成为可以被包覆的粗磨食物。包衣可以是在形成粗磨食物之后施加到粗磨食物上的聚合物包衣。
在施用本文所述的任何食品组合物的任何方法中,在某些实施方案中,其进一步包含添加剂、填充剂或赋形剂。添加剂、填充剂和赋形剂可以添加到任何食品组合物中的饮料、固体食品、半固体食品和其他消耗性物质。添加剂、填充剂和赋形剂可以包括酸化剂、酸度调节剂、防结块剂、消泡剂和发泡剂、抗氧化剂、填充剂、食用色素、保色剂、乳化剂、调味剂、增香剂、四种处理剂、上光剂、保湿剂、示踪剂气体、防腐剂、稳定剂、甜味剂和增稠剂。在一个示例性的实施方案中,添加剂、填充剂和赋形剂包括一种或多种玉米淀粉、麦芽糖糊精10、纤维素、复合矿物质s10001、碳酸氢钠、复合维生素v10001和胆碱酒石酸氢盐。在一些实施方案中,添加剂是食用色素。食用色素可以包括fd&c蓝色#1、fd&c蓝色#2、fd&c柑橘红#2、fd&c绿色#3、fd&c红色#3、fd&c红色#40、fd&c黄色#5和fd&c黄色#6。在一个示例性的实施方案中,食品组合物中的染料包括一种或多种fd&c红色#40、fd&c蓝色#1和fd&c黄色染料#5。
在施用本文所述的任何食品组合物的任何方法中,在某些实施方案中,所述方法进一步包含防腐剂。可以将防腐剂添加到食品组合物中的饮料、固体食物、半固体食物和其他消耗性物质。防腐剂可以包括天然食品防腐剂、化学食品防腐剂或人工防腐剂。例如,防腐剂可以包括乙酸、抗坏血酸、抗坏血酸钙、异抗坏血酸(erythrobicacid)、异抗坏血酸(isoascorbicacid)、硝酸钾、亚硝酸钾、抗坏血酸钠、异抗坏血酸钠(sodiumerythorbate)、异抗坏血酸钠(sodiumisoascorbate)、硝酸钠、亚硝酸钠、木焦油(woodsmoke)、苯甲酸、山梨酸钙、广布肉杆菌(carnobacteriumdivergensm35)、麦芽香肉杆菌(carnobacteriummaltaromaticumcb1)、月桂酰精氨酸乙酯、4-己基间苯二酚、肉色明串珠菌(leuconostoccarnosum4010)、对羟基苯甲酸甲酯、尼泊金甲酯、乙酸钾、苯甲酸钾、亚硫酸氢钾、二乙酸钾、乳酸钾、偏亚硫酸氢钾、山梨酸钾、对羟基苯甲酸丙酯、尼泊金丙酯、乙酸钠、苯甲酸钠、亚硫酸氢钠、二乙酸钠、乳酸钠、偏亚硫酸氢钠、对羟基苯甲酸甲酯的钠盐、对羟基苯甲酸丙酯的钠盐、山梨酸钠、亚硫酸钠、连二亚硫酸钠、山梨酸、亚硫酸、丙酸钙、山梨酸钙、二甲基二碳酸盐、那他霉素、山梨酸钾、丙酸、双乙酸钠、丙酸钠、山梨酸钠、山梨酸、抗坏血酸、抗坏血酸棕榈酸酯、抗坏血酸硬脂酸酯、丁基羟基茴香醚、丁羟甲苯、单甘油酯的柠檬酸酯和二甘油酯的柠檬酸酯、愈创木胶、卵磷脂、柠檬酸卵磷脂、柠檬酸单甘油酯、柠檬酸单异丙酯、没食子酸丙酯、焦亚硫酸钠、酒石酸、叔丁基对苯二酚和生育酚。在一个实施方案中,防腐剂选自亚硫酸盐、维生素e、维生素c和丁羟甲苯。在某些实施方案中,饮料、固体食物、半固体食物和其他可消耗物质的防腐可以通过物理防腐,例如通过冷冻、煮沸、烟熏和脱水来实现。
透析
在某些实施方案中,液体组合物存储在容器中。例如,容器可以是透析袋。在一个实施方案中,透析袋旨在一次性使用。容器可以容纳约1500至5000ml的液体组合物。在一个实施方案中,大约2000ml的液体组合物是单个单元。在另一个实施方案中,大约2500ml的液体组合物是单个单元。
在某些实施方案中,干燥组合物或浓缩组合物储存在容器中。例如,容器可以是透析袋。在一个实施方案中,透析袋旨在一次性使用。在一些实施方案中,干燥组合物或浓缩组合物在容器中进一步包含水溶液,从而产生混合物。水溶液可以是无菌或非无菌流体。在一个实施方案中,容器包含约2000ml的水溶液。在另一个实施方案中,容器包含约2500ml的水溶液。在某些实施方案中,混合物的ph为约4.0-6.5。在某些实施方案中,混合物的同渗容摩为约300-720mosmol/l。
应用
癌症
在本文描述的用于治疗癌症的任何方法中,在某些实施方案中,本公开内容提供了一种使用本文公开的食品组合物和/或透析组合物治疗癌症和预防癌症的方法。在一些实施方式中,该方法涉及癌症的治疗,所述癌症是例如急性髓性白血病、青少年癌症、儿童肾上腺皮质癌、与aids有关的癌症(例如淋巴瘤和卡波济氏肉瘤)、肛门癌、阑尾癌、星形细胞瘤、非典型畸胎瘤、基底细胞癌、胆管癌、膀胱癌、骨癌、脑干神经胶质瘤、脑肿瘤、乳腺癌、支气管肿瘤、伯基特淋巴瘤、类癌瘤、非典型畸胎瘤、胚胎瘤、生殖细胞瘤、原发性淋巴瘤、宫颈癌、儿童癌症、脊索瘤、心脏肿瘤、慢性淋巴细胞白血病(cll)、慢性髓性白血病(cml)、慢性骨髓增生性疾病、结肠癌、结直肠癌、颅咽管瘤、皮肤t细胞淋巴瘤、原位肝外导管癌(dcis)、胚胎瘤、中枢神经系统癌、子宫内膜癌、室管膜瘤、食道癌、成感觉神经细胞瘤、尤因肉瘤、颅外生殖细胞瘤、性腺外生殖细胞瘤、眼癌、骨纤维组织细胞瘤、胆囊癌、胃癌、胃肠道类癌、胃肠道间质瘤(gist)、生殖细胞瘤、妊娠滋养细胞肿瘤、多毛细胞白血病、头颈癌、心癌、肝癌、霍奇金淋巴瘤、下咽癌、眼内黑色素瘤、胰岛细胞瘤、胰腺神经内分泌肿瘤、肾癌、喉癌、唇和口腔癌、肝癌、小叶原位癌(lcis)、肺癌、淋巴瘤、原发性隐匿性转移性鳞状颈癌、中线癌、口腔癌、多发性内分泌肿瘤综合征、多发性骨髓瘤/浆细胞瘤、蕈样真菌病、骨髓增生异常综合征、骨髓增生异常/骨髓增生性肿瘤、多发性骨髓瘤、默克尔细胞癌、恶性间皮瘤、骨恶性纤维组织细胞瘤和骨肉瘤、鼻腔和鼻旁窦癌、鼻咽癌、神经母细胞瘤、非霍奇金淋巴瘤、非小细胞肺癌(nsclc)、口癌、唇和口腔癌、口咽癌、卵巢癌、胰腺癌、乳头状瘤病、副神经节瘤、鼻旁窦和鼻腔癌、甲状旁腺癌、阴茎癌、咽癌、胸膜肺母细胞瘤、原发性中枢神经系统(cns)淋巴瘤、前列腺癌、直肠癌、移行细胞癌、视网膜母细胞瘤、横纹肌肉瘤、涎腺癌、皮肤癌、胃癌、小细胞肺癌、小肠癌、软组织肉瘤、t细胞淋巴瘤、睾丸癌、喉癌、胸腺瘤和胸腺癌、甲状腺癌、肾盂和输尿管的移行细胞癌、滋养细胞肿瘤、儿童期的罕见癌症、尿道癌、子宫肉瘤、阴道癌、外阴癌或病毒引起的癌症。在一些实施方案中,癌症选自白血病、血液恶性肿瘤、实体瘤癌症、前列腺癌、乳腺癌、肝癌或脑肿瘤。在一个示例性的实施方案中,癌症选自肺癌、肝癌、乳腺癌、前列腺癌、结肠癌、淋巴瘤和白血病。
在某些方面,本公开内容提供了一种在已接受低半胱氨酸饮食的受试者中治疗癌症的方法,该方法包括:给受试者进行透析,其中透析减少或消耗受试者体内的半胱氨酸。
在某些方面,本公开内容提供了一种在已接受低半胱氨酸饮食的受试者中消耗半胱氨酸的方法,该方法包括:给受试者进行透析,其中透析减少或消耗受试者体内的半胱氨酸。
在一些方面,本公开内容提供了一种在已接受透析程序以减少血液中的半胱氨酸的受试者中治疗癌症的方法,该方法包括:为受试者安排低半胱氨酸饮食。
在一些实施方案中,透析包括施用本文公开的液体组合物、本文公开的浓缩组合物或本文公开的干燥组合物。在一些实施方案中,低半胱氨酸饮食是本文公开的食品组合物。
肥胖症
在本文描述的用于治疗肥胖症的任何方法中,在某些实施方案中,本公开内容提供了一种用于治疗肥胖症和预防肥胖症的方法。在一些实施方案中,该方法涉及对可能导致肥胖或由肥胖引起的疾病的治疗或预防,该疾病是例如暴饮暴食和贪食症、多囊卵巢疾病、颅咽管瘤、帕-魏二氏综合征(prader-willisyndrome)、frohlich综合征、ii型糖尿病、gh缺乏的受试者、正常变异性矮小、turner综合征,以及表现出代谢活动减少或静息能量消耗占总无脂肪质量的百分比减少的其他病理状况,例如患有急性成淋巴细胞性白血病的儿童。在一些实施方案中,该方法涉及治疗至少一种与肥胖有关的健康状况,包括但不限于心血管疾病、2型糖尿病、阻塞性睡眠呼吸暂停、癌症、骨关节炎和抑郁症。
肾脏疾病
在本文描述的用于治疗肾脏疾病的任何方法中,在某些实施方案中,本公开内容提供了一种用于治疗肾脏疾病和预防肾脏疾病的方法。在示例性的实施方案中,肾脏疾病是慢性肾脏疾病。在一些实施方案中,该方法涉及治疗通过病史、体格检查结果和实验室检查确定的被诊断患有肾脏疾病的受试者。例如,可以诊断该受试者患有急性或慢性肾衰竭,该肾衰竭是由糖尿病、局部缺血、药物诱导的毒性、需要或不需要透析的移植后排斥引起的;肾小球肾炎;肾小球硬化;间质性肾炎;和急性肾小管坏死。受试者可能有体格检查结果,如无尿、嗜睡、昏迷和总体生长速度下降。受试者可具有增加的肌酐、尿素和尿酸(bun)的血浆水平、蛋白尿、降低的gfr、rpf和肾脏大小,如通过尿路图、改变的酸/碱平衡和尿比重的变化所确定。
受试者
癌症
在本文所述的用于治疗癌症和/或减小肿瘤大小的任何方法中,在某些实施方案中,受试者是人类。例如,人类受试者可以是成人、儿童或婴儿。在一个示例性的实施方案中,人类受试者是成人。人类受试者可以是18岁或更大的成人。人类受试者可能在18至90岁之间。在某个实施方案中,人类受试者为40至85岁。在一个示例性的实施方案中,人类受试者为65至80岁。
在本文所述的用于治疗癌症和/或减小肿瘤大小的任何方法中,在某些实施方案中,受试者是动物。动物受试者可以是家养动物,例如狗或猫。动物受试者可以是小鼠或大鼠。动物受试者可以是至少7周龄的小鼠或大鼠。动物受试者可以是7至15周龄的小鼠或大鼠。动物受试者可以是10至11周龄的小鼠或大鼠。
可以用本公开内容的食品组合物、液体组合物、浓缩组合物和/或干燥组合物治疗的受试者包括已被诊断为患有以下病症的受试者:急性髓性白血病、急性髓性白血病、青少年癌症、儿童肾上腺皮质癌、与aids有关的癌症(例如淋巴瘤和卡波济氏肉瘤)、肛门癌、阑尾癌、星形细胞瘤、非典型畸胎瘤、基底细胞癌、胆管癌、膀胱癌、骨癌、脑干神经胶质瘤、脑肿瘤、乳腺癌、支气管肿瘤、伯基特淋巴瘤、类癌瘤、非典型畸胎瘤、胚胎瘤、生殖细胞瘤、原发性淋巴瘤、宫颈癌、儿童癌症、脊索瘤、心脏肿瘤、慢性淋巴细胞白血病(cll)、慢性髓性白血病(cml)、慢性骨髓增生性疾病、结肠癌、结直肠癌、颅咽管瘤、皮肤t细胞淋巴瘤、原位肝外导管癌(dcis)、胚胎瘤、中枢神经系统癌、子宫内膜癌、室管膜瘤、食道癌、成感觉神经细胞瘤、尤因肉瘤、颅外生殖细胞瘤、性腺外生殖细胞瘤、眼癌、骨纤维组织细胞瘤、胆囊癌、胃癌、胃肠道类癌、胃肠道间质瘤(gist)、生殖细胞瘤、妊娠滋养细胞肿瘤、多毛细胞白血病、头颈癌、心癌、肝癌、霍奇金淋巴瘤、下咽癌、眼内黑色素瘤、胰岛细胞瘤、胰腺神经内分泌肿瘤、肾癌、喉癌、唇和口腔癌、肝癌、小叶原位癌(lcis)、肺癌、淋巴瘤、原发性隐匿性转移性鳞状颈癌、中线癌、口腔癌、多发性内分泌肿瘤综合征、多发性骨髓瘤/浆细胞瘤、蕈样真菌病、骨髓增生异常综合征、骨髓增生异常/骨髓增生性肿瘤、多发性骨髓瘤、默克尔细胞癌、恶性间皮瘤、骨恶性纤维组织细胞瘤和骨肉瘤、鼻腔和鼻旁窦癌、鼻咽癌、神经母细胞瘤、非霍奇金淋巴瘤、非小细胞肺癌(nsclc)、口癌、唇和口腔癌、口咽癌、卵巢癌、胰腺癌、乳头状瘤病、副神经节瘤、鼻旁窦和鼻腔癌、甲状旁腺癌、阴茎癌、咽癌、胸膜肺母细胞瘤、原发性中枢神经系统(cns)淋巴瘤、前列腺癌、直肠癌、移行细胞癌、视网膜母细胞瘤、横纹肌肉瘤、涎腺癌、皮肤癌、胃癌、小细胞肺癌、小肠癌、软组织肉瘤、t细胞淋巴瘤、睾丸癌、喉癌、胸腺瘤和胸腺癌、甲状腺癌、肾盂和输尿管的移行细胞癌、滋养细胞肿瘤、儿童期的罕见癌症、尿道癌、子宫肉瘤、阴道癌、外阴癌、病毒引起的癌症、白血病、血液恶性肿瘤、实体瘤癌症、前列腺癌、去势抵抗性前列腺癌、乳腺癌、尤因肉瘤、骨肉瘤、原发性骨肉瘤、t-细胞幼淋巴细胞白血病、神经胶质瘤、胶质母细胞瘤、肝细胞癌、肝癌或糖尿病、相关的病症,及其组合。在一些实施方案中,使用本公开内容的食品组合物、液体组合物和/或干燥组合物治疗的受试者包括已被诊断为患有非癌性过度增殖性疾病例如皮肤的良性增生(例如牛皮癣)、再狭窄和前列腺增生(例如,良性前列腺肥大(bph))的受试者。
在某些实施方案中,人类受试者已经诊断出患有白血病、肺癌、肝癌、乳腺癌、结肠癌、前列腺癌、胃癌、宫颈癌、食道癌、膀胱癌、非霍奇金淋巴瘤及其组合。在某些实施方案中,动物受试者已经诊断出患有恶性淋巴瘤、皮肤癌、乳腺肿瘤、乳腺癌、软组织肉瘤、骨癌及其组合。
在某些实施方案中,受试者具有癌症的遗传易感性。
在某些实施方案中,受试者具有升高的半胱氨酸生物合成基因表达水平。
肥胖症
如本文所用,术语“肥胖症”是指个体被认为是“超重”或“肥胖”的病症。术语“肥胖”或“肥胖症”包括“极端肥胖”、“严重肥胖”和“超级肥胖”。
在本文所述的用于治疗肥胖症的任何方法中,在某些实施方案中,受试者是人类。例如,人类受试者可以是成人或儿童。在某些实施方案中,人类受试者是人类儿童。例如,人类儿童的年龄可能在2到5岁之间,6到11岁之间以及12到17岁之间。在某些实施方案中,人类受试者是人类成人。人类受试者可以是18岁或更大的成人。人类受试者可以是18-90岁。在某个实施方案中,人类受试者是30-80岁。在一个示例性的实施方案中,人类受试者为45-65岁。
在某些实施方案中,受试者是动物。动物受试者可以是家养动物,例如狗或猫。动物受试者可以是小鼠或大鼠。动物受试者可以是至少7周龄的小鼠或大鼠。动物受试者可以是7-15周龄的小鼠或大鼠。动物受试者可以是10-11周龄的小鼠或大鼠。
可以用本公开内容的食品组合物、液体组合物、浓缩组合物和/或干燥组合物治疗的受试者包括已经被诊断为超重或肥胖并且/或者体重指数(bmi)至少为25kg/m2的受试者。可以使用体重指数(bmi)测量来评估受试者的肥胖症。可以通过将受试者的体重(以kg为单位)除以受试者的身高的平方(m2)来计算受试者的bmi。如果受试者的bmi超过25kg/m2、超过26kg/m2、超过27kg/m2、超过28kg/m2、超过29kg/m2、超过30kg/m2、超过31kg/m2、超过32kg/m2、超过33kg/m2、超过34kg/m2、超过35kg/m2、超过36kg/m2、超过37kg/m2、超过38kg/m2、超过39kg/m2、超过40kg/m2、超过41kg/m2、超过42kg/m2、超过43kg/m2、超过44kg/m2、超过45kg/m2、超过46kg/m2、超过47kg/m2、超过48kg/m2、超过49kg/m2或超过50kg/m2则被认为是肥胖。受试者可以诊断为i级肥胖、ii级肥胖、iii级肥胖或其等效项。受试者的bmi可以为至少30kg/m2、至少35kg/m2、至少40kg/m2、至少45kg/m2或至少50kg/m2。受试者的bmi可以在25kg/m2至50kg/m2之间。受试者可以经历至少一种与肥胖有关的健康状况,包括但不限于心血管疾病、2型糖尿病、阻塞性睡眠呼吸暂停、癌症、骨关节炎和抑郁症。如果受试者表现出腹部肥胖,也可以认为该受试者表现出发展nash或肝脂肪变性的倾向。可以通过测量受试者的腰围来评估腹部肥胖。例如,如果受试者是成年男性,则如果受试者的腰围为102cm或更大,则可以认为该受试者表现出腹部肥胖。例如,如果受试者是成年女性,则如果受试者表现出88cm或更大的腰围,则可以认为该受试者表现出腹部肥胖。
在某些实施方案中,受试者习惯性地食用过量的食物、具有肥胖的遗传易感性、日常缺乏身体活动、对药物具有不良反应、患有精神疾病、患有内分泌疾病,及其组合。在某些实施方案中,受试者具有肥胖的遗传易感性。在某些实施方案中,受试者中的肥胖症是由于一个或多个基因的多态性所致。在某些实施方案中,受试者习惯性地食用过量的食物。
在某些实施方案中,治疗肥胖症的特征在于受试者减轻了受试者初始体重的至少5%、10%、15%、15%、20%、25%、30%、35%、40%、45%或50%。治疗肥胖症的特征可在于受试者减轻了受试者初始体重的至少10%。治疗肥胖症的特征可在于受试者减轻了受试者初始体重的至少20%。治疗肥胖症的特征可在于受试者减轻了受试者初始体重的至少30%。
肾脏疾病
如本文所用,术语“肾脏疾病”包括但不限于肾疾病、肾病变、肾炎、肾病、慢性肾疾病、慢性肾衰竭、急性肾病和急性肾损伤。
在本文所述的用于治疗肾脏疾病的任何方法中,在某些实施方案中,受试者是人类。例如,人类受试者可以是成人或儿童。在某些实施方案中,人类受试者是人类儿童。在某些实施方案中,人类受试者是人类成人。人类受试者可以是18岁或更大的成人。在某些实施方案中,人类受试者为至少30、35、40、45、50、55、60、65、70、75或80岁。人类受试者可以为至少60岁。人类受试者可以在18至90岁之间。在一个示例性的实施方案中,人类受试者为55至75岁。
在某些实施方案中,受试者是动物。动物受试者可以是家养动物,例如狗或猫。动物受试者可以是小鼠或大鼠。动物受试者可以是至少7周龄的小鼠或大鼠。动物受试者可以是7至15周龄的小鼠或大鼠。动物受试者可以是10-11周龄的小鼠或大鼠。
可以使用本公开内容的食品组合物、液体组合物和/或干燥组合物治疗的受试者包括已经被诊断出患有肾脏疾病和/或相关病症的受试者。在某些实施方案中,该受试者先前或同时被诊断出患有高血压和/或糖尿病、对药物具有不良反应、具有肾脏疾病的遗传易感性、经历泌尿系统的阻塞、经历炎症(例如肾小球肾炎)和/或经历感染(例如肾盂肾炎)。
设施
在一些方面,本公开内容提供了一种包含多种液体组合物的设施。在某些实施方案中,该设施制造本文所述的液体组合物或其组分。在一个实施方案中,该设施是制药厂。在某些实施方案中,该设施分配本文所述的液体组合物或其组分。例如,该设施可以是配送中心。在某些实施方案中,该设施施用本文所述的液体组合物或其组分。在一个实施方案中,该设施是医院、透析中心、家庭或诊所。该设施可以通过透析向受试者施用液体组合物。
在一些方面,本公开内容提供了一种包含多种干燥组合物或浓缩组合物的设施。在某些实施方案中,该设施生产本文所述的干燥组合物或浓缩组合物或其组分。在一个实施方案中,该设施是制药厂。在某些实施方案中,该设施分配本文所述的干燥组合物或浓缩组合物或其组分。例如,该设施可以是配送中心。在某些实施方案中,该设施施用本文所述的干燥组合物或浓缩组合物或其组分。在一个实施方案中,该设施是医院或诊所。该设施可以通过透析向受试者施用干燥组合物或浓缩组合物。
在一些方面,本公开内容提供了一种包含多种食品组合物的设施。在某些实施方案中,该设施生产本文所述的食品组合物或其组分。在一个实施方案中,该设施是食品制造场所。在某些实施方案中,该设施分配本文所述的食品组合物或其组分。例如,该设施可以是配送中心。在某些实施方案中,该设施向受试者提供本文所述的食品组合物及其组分。在一个实施方案中,该设施可以将食品组合物出售给受试者。在另一个实施方案中,该设施可以制备食品组合物。在另一个实施方案中,该设施可以向受试者施用食品组合物。例如,该设施可以是配送中心、商业厨房、饭店、就餐设施或医疗设施。在一些实施方案中,该设施位于向医院、诊所或患者提供餐饮或食品递送服务的位置。该设施可以位于医院或诊所的内部或附近,例如在医院或诊所的0.1、0.5、1或5英里之内。
试剂盒
饮食
本发明还提供了试剂盒。在一些方面,本公开内容提供了一种试剂盒,其包含:(a)如本文所述的预包装食品组合物;和(b)使用预包装食品组合物的说明书。试剂盒以合适的包装包括一种或多种本文所述的食品组合物,并且可以进一步包括书面材料,该书面材料可以包括使用说明书、临床研究的论述、副作用列表等。说明书可以包括描述该食品组合物在治疗癌症、肥胖症或肾脏疾病中的用途和伴随的益处的信息包。这样的试剂盒还可以包括信息,例如科学文献参考、包装插页材料、临床试验结果和/或这些信息的摘要等,其指示或确定食品组合物的活性和/或优点,并且/或者描述剂量、用法、饮食方案、副作用、药物相互作用或其他对医疗保健提供者有用的信息。这样的信息可以基于各种研究的结果,例如,使用涉及体内模型的实验动物的研究和基于人类临床试验的研究。试剂盒可以包含本文所述的食品组合物的一个或多个全餐和/或零食。在一些实施方案中,试剂盒包含食品组合物的约、小于约或大于约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、30、31、60、90、120、150、180、210或更个全餐和/或零食。试剂盒可提供恰好或至少1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、17、18、19、20、30、31、60、90、120或更多天的全餐和/或零食。使用说明书可以包括饮食方案说明,例如每天进食1、2、3、4、5、6、7、8、9、10或更多次的全餐和/或1、2、3、4、5、6、7、8、9、10或更多次的零食。例如,试剂盒可以包括作为食品提供的食品组合物的全餐和/或零食,其中每种食品分别包装,多种食品根据每次施用的食品组合物(例如成对的组分)的全餐和/或零食的数量分开包装,或所有食物包装在一起(例如在容器中)。作为另一个实例,试剂盒可以包括作为瓶装饮料的食品组合物的全餐和/或零食,试剂盒包括1、2、3、4、5、6、7、8、9、10、11、12、13、14、24、28、36、48、72或更多瓶。在替代的实例中,试剂盒可以包括作为营养棒的食品组合物的全餐和/或零食,试剂盒包含1、2、3、4、5、6、7、8、9、10、11、12、13、14、24、28、36、48、72或更多的营养棒。试剂盒可以包括作为单独组合物提供或包装在试剂盒内的单独容器中的食品组合物的组分。在一些实施方案中,试剂盒可以包含作为单一组合物提供或包装在试剂盒的容器内的食品组合物的组分。
试剂盒可以进一步包含另一种药剂。在一些实施方案中,食品组合物或其组分以及药剂作为单独的组合物提供或包装在试剂盒内的单独容器中。在一些实施方案中,食品组合物或其组分以及药剂作为单一组合物提供或包装在试剂盒中的容器内。适用的包装和其他物品(例如,用于液体制剂的量杯、将空气暴露最小化的箔包装等)在本领域中是已知的,并且可以包括在试剂盒中。可以向包括医生、护士、药剂师、处方官等的健康提供者提供、销售和/或推广本文所述的试剂盒。在一些实施方案中,试剂盒也可以直接销售给消费者。
试剂盒可以进一步包含本文所述的预包装的液体组合物、预包装浓缩组合物或预包装干燥组合物。试剂盒可以包括指导预包装的液体组合物,或预包装的浓缩组合物,或干燥组合物的施用的说明书。在一些实施方案中,试剂盒包含约、小于约或大于约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、30、31、60、90、120、150、180、210或更多种预包装的液体组合物、预包装的浓缩组合物或预包装的干燥组合物。
在一些实施方案中,试剂盒可以包含多日供应量的本文所述的食品组合物的全餐和/或零食。试剂盒可以包含指导在几天的时间内施用多日供应量的食品组合物的全餐和/或零食的说明书。多日供应量可以是一个月供应量、两个月供应量或多周供应量。多日供应量可以是90天、180天、3个月或6个月的供应量。试剂盒可以包括食品组合物的包装的每日全餐和/或零食,例如食品组合物的1、2、3、4或5个全餐和/或零食的包装。试剂盒可与其他膳食补充剂、维生素和/或代餐棒、混合物和饮料包装在一起。
透析
在一些方面,本公开内容提供了一种试剂盒,其包含:(a)如本文所述的预包装的液体组合物;和(b)使用预包装液体组合物的说明书。在一些方面,本公开内容提供了一种试剂盒,其包含:(a)如本文所述的预包装的干燥组合物或浓缩组合物;和(b)使用预包装的干燥组合物的说明书。试剂盒以合适的包装包括一种或多种本文所述的液体组合物、浓缩组合物或干燥组合物,并且可以进一步包括书面材料,该书面材料可以包括使用说明书、临床研究的论述、副作用列表等。说明书可以包括描述该液体组合物或干燥组合物在治疗癌症、肥胖症或肾脏疾病中的用途和伴随的益处的信息包。这样的试剂盒还可以包括信息,例如科学文献参考、包装插页材料、临床试验结果和/或这些信息的摘要等,其指示或确定液体组合物、浓缩组合物或干燥组合物的活性和/或优点,并且/或者描述剂量、用法、副作用、药物相互作用或其他对医疗保健提供者有用的信息。这样的信息可以基于各种研究的结果,例如,使用涉及体内模型的实验动物的研究和基于人类临床试验的研究。试剂盒可以包含一个或多个透析袋,该透析袋包含本文所述的液体组合物、浓缩组合物或干燥组合物。在一些实施方案中,试剂盒包含约、小于约或大于约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、30、31、60、90、120、150、180、210或更多个含有液体组合物、浓缩组合物或干燥组合物的透析袋。试剂盒可提供含有用于恰好或至少1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、30、31、60、90、120或更多天的液体组合物、浓缩组合物或干燥组合物的透析袋。使用说明书可以包括透析方案说明书,例如每天1、2、3、4、5、6、7、8、9、10或更多次使用1、2、3、4、5、6、7、8、9、10或更多个含有液体组合物、浓缩组合物或干燥组合物的透析袋的说明书。例如,试剂盒可以包括透析袋,该透析袋含有作为一次性透析袋提供的液体组合物、浓缩组合物或干燥组合物,其中每个一次性透析袋分别包装,多个一次性透析袋根据含有每次施用的液体组合物、浓缩组合物或干燥组合物的透析袋的数量(例如成对的一次性透析袋)分别包装或所有一次性透析袋包装在一起(例如在容器中)。试剂盒可以包括透析袋的组分,该透析袋含有作为单独的组合物提供或包装在试剂盒内的单独容器中的液体组合物、浓缩组合物或干燥组合物。在一些实施方案中,试剂盒可以包括透析袋的组分,该透析袋含有作为单一组合物提供或包装在试剂盒的容器内的液体组合物、浓缩组合物或干燥组合物。
该试剂盒可以进一步包含另一种药剂。在一些实施方案中,将包含液体组合物、浓缩组合物或干燥组合物或其组分以及药剂的透析袋作为单独的组合物提供或包装在试剂盒内的单独容器中。在一些实施方案中,液体组合物、浓缩组合物、干燥组合物或其组分以及药剂作为单一组合物提供或包装在试剂盒中的容器内。适用的包装和其他物品(例如,用于重构干燥组合物或浓缩组合物的水溶液、用于液体制剂的量杯、将空气暴露最小化的包装等)是本领域已知的,并且可以包含在试剂盒中。可以向包括医生、护士、药剂师、处方官等在内的健康提供者提供、销售和/或推广本文所述的试剂盒。在一些实施方案中,试剂盒也可以直接销售给消费者。
试剂盒可以进一步包含本文所述的预包装的液体组合物、预包装的浓缩组合物或预包装的干燥组合物。试剂盒可以包含指导预包装的液体组合物、预包装的浓缩组合物或预包装的干燥组合物施用的说明书。在一些实施方案中,试剂盒包含约、小于约或大于约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、30、31、60、90、120、150、180、210或更多个预包装的液体组合物、预包装的浓缩组合物或预包装的干燥组合物。
在一些实施方案中,试剂盒可以包括多日供应量的透析袋,该透析袋含有本文所述的液体组合物、浓缩组合物或干燥组合物。试剂盒可以包括指导在多天的时间内施用多日供应量的透析袋的说明书,该透析袋含有液体组合物、浓缩组合物或干燥组合物。多日供应量可以是一个月供应量、两个月供应量或多周供应量。多日供应量可以是90天、180天、3个月或6个月的供应量。试剂盒可以包括含有液体组合物、浓缩组合物或干燥组合物的包装的透析袋,例如含有液体组合物、浓缩组合物或干燥组合物的1、2、3、4或5个透析袋的包装。试剂盒可以与本文所述的食品组合物、膳食补充剂、维生素和/或代餐棒、混合物和饮料一起包装。
系统
本公开内容提供了一种使用本文公开的组合物给受试者进行透析和/或营养饮食以帮助治疗或预防疾病的系统。该系统可以执行本文公开的任何方法,并且可以使用本文公开的任何组合物。
可以控制和修改本公开内容的透析系统,以根据需要提供各种透析疗法。透析系统可以被修改(例如增加/减少交换次数,增加/减少每次交换中使用的透析液量,和/或使用调整后的透析液配方)以调节受试者的医疗进度。透析系统可以促进腹膜透析、血液透析和其他形式的透析。透析系统可以包括(a)包含本文公开的组合物的透析容器,(b)管道,和(c)收集容器。在一些实施方案中,透析系统进一步包括用于促进和/或自动化流体交换的机器。在一些方面,本公开内容提供了一种透析系统,包括:透析容器,其包含本文公开的液体组合物、本文公开的浓缩组合物或本文公开的干燥组合物;以及透析机,其被配置为施用所述液体组合物、浓缩组合物或干燥组合物。在一些实施方案中,透析机包括泵、压力监测器、气阱、空气检测器、夹具和/或过滤器。在一些方面,本公开内容提供了一种透析系统,包括:透析容器,其包含本文公开的液体组合物、本文公开的浓缩组合物或本文公开的干燥组合物。
腹膜透析。
腹膜透析(pd)是一种使用受试者腹部的内衬(即腹膜)和透析液来清洗受试者的血液的治疗方法。液体组合物、浓缩组合物和干燥组合物中的任何一种均可用作pd中的透析液。透析液使用腹膜作为过滤器吸收血液中的废物和液体。在一些实施方案中,透析系统包括连续不卧床pd(capd)或连续循环仪辅助pd(ccpd)。
capd是“连续的”,无需计算机,可以随时执行。该治疗可以包括将约两夸脱的清洁液置于受试者的腹部,然后将其排干。在一些实施方案中,capd可以通过将清洁液的塑料袋接合在腹膜中的管上来完成。受试者可以将透析袋抬高到大约肩水平,以将透析流体引入腹膜。排空后,将透析袋取出并丢弃。交换完成(放入和取出液体)后,将液体将从受试者的腹部排出。在一些实施方案中,此过程在24小时内执行几次,例如1、2、3、4、5、6或7次,或者根据需要执行。每次交换可能花费大约30分钟、45分钟、1小时、2小时、3小时、4小时、5小时或6小时。图14a示出了示例性的capd过程(来源:https://www.niddk.nih.gov/health-information/kidney-disease/kidney-failure/peritoneal-dialysis)。如图14a所示,经历capd的患者可以通过放置在患者腹膜中的导管和连接管104接合透析袋101和废物容器105。转移装置103将导管连接到透析袋101以进行透析交换,并且可以被设计成降低感染的风险。转移装置可以是“y形的”,并且y管的一个分支可以连接至废物容器105,而另一分支可以连接至含有本文所述的透析溶液的透析袋101。在一些实施方案中,在受试者使用之前将透析溶液温热。将透析袋101以允许透析袋中的流体进入患者的方式放置在患者腹膜上方,如图14a所示放置在柱上。
ccpd(也称为自动腹膜透析(apd))与capd的不同之处在于,机器(循环仪)输送并排出受试者的清洁液。该治疗可以在任何时间进行,尤其是在晚上。透析系统例如在患者入睡的夜间自动对患者进行透析治疗。受试者可能会长时间与机器连接,例如每天8、9、10、11或12个小时。图14b显示了示例性的ccpd的流程(来源:https://www.niddk.nih.gov/health-information/kidney-disease/kidney-failure/peritoneal-dialysis)。如图14b所示,经历ccpd的患者可以接合到本文公开的透析溶液的供应201和废液管线205。透析可以通过透析机204(也称为循环仪)来促进。透析机可以进一步包括加热器203。透析溶液的流量可以通过流量计202监控。流体计202可以测量并记录循环仪204移出了多少溶液。在一些实施方案中,循环仪204将放入受试者的透析溶液的量与排出的流体的量进行比较。循环仪204可以在受试者入睡时一晚上多次(例如三到五次)填充并清空受试者的腹膜。
血液透析
血液透析是一种从血液中过滤掉废物和水的治疗方法。在血液透析中,使用透析机和称为“人造肾脏”或“透析器”的特殊过滤器来清洁受试者的血液。血液流经位于受试者体外的透析器。图15是血液透析的示例性示意图(来源:https://www.niddk.nih.gov/health-information/kidney-disease/kidney-failure/hemodialysis)。图16概述了血液透析中的过滤过程(来源:https://www.niddk.nih.gov/health-information/kidney-disease/kidney-failure/hemodialysis)。如图15所示,可以通过将两个针头插入受试者的手臂来将正在进行血液透析的患者连接到透析机上。每个针头都连接到与透析机相连的软管上。透析机将血液泵送通过过滤器,然后将血液返回给患者。通过一个针头,血液被抽出以进行透析307。在透析的各个阶段,用动脉压力监测器308、透析器流入压力监测器302和静脉压力监测器304监测未过滤和过滤后的血液。抗凝剂301可用于防止血液凝结。透析机用泵309将血液泵送通过过滤器303(也称为透析器)。透析器303具有两部分,一部分用于血液,另一部分用于称为透析液的洗涤液。薄膜将这两部分分开。一旦血液在过滤器的一端401进入过滤器303,血液就会被迫进入许多非常细的中空纤维402。当血液通过中空纤维时,本文公开的透析溶液404沿相反方向流过纤维的外部。来自血液的废产物进入透析溶液并离开过滤器403。过滤后的血液保留在中空纤维中并返回人体。透析溶液中的一些营养素也可能随着过滤后的血液返回人体。
在一些实施方案中,每周进行约1、2、3、4、5、6或7次血液透析,一次约1、2、3、4、5或6小时,或视需要而定。
实施例
实施例1:癌症治疗过程
向先前确定患有某种类型的癌症的患者提供癌症治疗方案。患者被诊断出患有在原发或转移阶段的实体或液体肿瘤。该方案涉及利用营养改良饮食与用本文公开的组合物进行透析的组合。该方案涉及可以针对每个患者的需求量身定制的代谢干预疗法。如图1所示,可以向诊断为癌症的患者提供代谢癌症疗法。癌症患者接受透析和/或营养饮食治疗,以消耗靶向营养素。
用本文所述的任何食品组合物(即,消耗饮食)将患者引发约3天(“引发阶段”)。在引发阶段,患者的整个饮食包含本文所述的任何食品组合物,但该方案批准的食物和饮料除外。在引发阶段之前和之后,通过靶向lc-ms测定来测量和分析患者的血浆氨基酸水平。
在方案的约第4天,患者继续进食消耗饮食,并开始进行透析治疗,例如血液透析或腹膜透析。患者可以接受单独的血液透析或单独的腹膜透析,也可以在治疗过程中依次或交替进行任一形式的透析。进行血液透析的患者在本文所述的设施处使用本文所述的液体组合物、浓缩组合物或干燥组合物(“透析溶液”)进行透析。患者在白天或晚上接受大约4个小时的透析溶液。患者每周至少接受3次透析治疗,每次透析治疗大约需要4个小时。每次透析治疗后,都要分析患者的血浆氨基酸谱,以监测治疗效果的进展。进行腹膜透析的患者在本文所述的设施、患者家中或方便的位置使用本文所述的液体组合物、浓缩组合物或干燥组合物(“透析溶液”)进行透析。患者每天或每24小时接受大约8-12小时的透析溶液。为了进行连续的腹膜透析,患者需要携带用于施用透析溶液的便携式设备。大约每3天分析患者的血浆氨基酸谱以监测治疗效果的进展。
对于单次/单日清除率为30%或更高的典型透析治疗,根据lc-ms分析,患者的氨基酸谱在不超过约8周后达到治疗消耗水平。此时,患者停止透析治疗,但继续进食消耗饮食,直到完全缓解。一旦患者达到完全缓解,患者将继续进食消耗饮食约2周,以稳定完全缓解,在整个过程中对患者进行测试。
在整个癌症治疗方案中,患者的疾病进展都通过伴随测试进行监测。通过允许患者恢复正常饮食,可以方便地制止或限制出现的任何严重并发症。一旦患者的状况稳定,就会恢复癌症治疗方案。只要不干扰代谢干预治疗,患者就可以继续服用止痛药或其他抗癌药。
实施例2:肥胖症治疗过程
对于相容性引发测试,可以伴有血浆营养素测试一起进行1-4周的饮食干预,以表明在个体患者中的安全性和潜在疗效。如实施例1中所述,在测试期间,患者将仅食用和饮用规定的食品组合物。对于长期使用而言,只要受试者保持肥胖,就可以实施饮食方案。
实施例3:肾脏疾病治疗过程
随着我们透析程序中安全性和清除效率的技术改进,肾脏疾病患者可以通过施用本文所述的干燥组合物、浓缩组合物或液体组合物,仅依靠透析来获得正常的营养养分。遵循如实施例1中所述的透析程序。对于长期使用而言,只要受试者的肾功能仍然受损或丧失,就可以进行透析。
实施例4:癌症治疗过程:仅饮食
对于相容性引发测试,饮食干预可以与伴有癌症进展测试和血浆营养素测试一起进行1-4周,以表明在个体患者中的安全性和潜在疗效。如示例1中所述,在测试过程中,患者只能食用和饮用规定的食物。对于长期使用而言,只要肿瘤没有完全治愈,就可以对患者实施饮食方案。
实施例5:癌症治疗过程:仅透析
随着我们透析程序中安全性和清除效率的技术改进,癌症患者可以通过施用本文所述的干燥组合物、浓缩组合物或液体组合物,仅依靠透析来靶向消耗血浆中的癌症成瘾的营养素,并获得正常的营养素养分。仅透析疗法特别适用于晚期胃肠癌,因为患者通常会失去进食能力,仅依靠营养素输注。对于长期使用而言,只要肿瘤没有完全治愈,就可以对受试者进行透析。
实施例6:透析流体组成
如下所示的表2提供了本文所述的透析流体——干燥组合物、浓缩组合物或液体组合物的示例性配方。
表2:透析流体组成
实施例7:食品组合物
如下所示的表3提供了本文所述的食品组合物的示例性配方。
表3:食品组合物
实施例8:仅饮食对癌症的效果
在结肠癌、乳腺癌、前列腺癌和胰腺癌中测试了营养饮食的效果。给研究中的小鼠安排图2所示的饮食之一。图3示出了用于本公开内容的研究中的饮食组合物的概况,并且实施例14的表5进一步描述了该饮食。在图4至图13b所示的研究中,“完全饮食”是图3的“设计对照”。在图2中,mead201和mead203分别消耗了5种和9种非必需氨基酸。mead202缺少3种非必需氨基酸且1种非必需氨基酸不充足。蛋白质y是天然蛋白质酪蛋白,它是提供蛋白质的常见食品成分。蛋白质z是大豆蛋白。蛋白质x是胶原蛋白(明胶)。
结肠癌
程序。通过皮下注射将hct116细胞植入无胸腺裸鼠。小鼠大约5-6周大。这项研究具有两组:接受完全饮食的小鼠和接受mead202的小鼠。每组有5只小鼠。在第7天给小鼠安排各自的饮食。小鼠自由取食。完全饮食和mead202的组成在实施例14的表5中描述。每周监测肿瘤大小3次。收集肿瘤组织和血浆样品。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。
结果。如图4所示,与用完全饮食治疗的小鼠相比,用mead202治疗的小鼠表现出明显的肿瘤体积减小。在研究过程中,用mead202治疗的小鼠的肿瘤体积始终比完全饮食治疗的小鼠更低。到第25天,mead202小鼠的肿瘤体积比完全饮食的小鼠低25%以上。
三阴性乳腺癌
程序。在图5a中,通过皮下注射向nod-scid小鼠植入mda-mdb-231细胞。小鼠为5-6周大。图5a的研究具有两组:接受完全饮食的小鼠和接受治疗饮食[mead202(第28-45天)和mead203(第45天之后)]的小鼠,并且在第20天给小鼠安排各自的饮食。在图5b中,通过皮下注射将mda-mdb-231细胞植入无胸腺裸鼠。小鼠为5-6周大。图5b的研究具有3组:接受完全饮食的小鼠、接受mead202的小鼠和接受mead203的小鼠,并且在第7天给小鼠安排各自的饮食。每组有5只小鼠。完全饮食和治疗饮食的组成在实施例14的表5中描述。小鼠自由取食。每周监测肿瘤大小3次。收集肿瘤组织和血浆样品。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。
结果。如图5a和图5b所示,与用完全饮食治疗的小鼠相比,用营养饮食治疗的小鼠表现出明显的肿瘤体积减小。在图5a的研究中,用治疗饮食治疗的小鼠始终比用完全饮食治疗的小鼠具有更低的肿瘤体积。到第65天,治疗饮食小鼠的肿瘤体积比完全饮食小鼠低约60%。如图5b的研究中,用mead203和mead202治疗的小鼠的肿瘤体积始终比用完全饮食治疗的小鼠低。到第23天,mead203和mead202小鼠的肿瘤体积比完全饮食小鼠低25%以上。
前列腺癌
程序。通过皮下注射将pc-3细胞植入无胸腺裸鼠。小鼠为5-6周大。该研究具有两组:接受完全饮食的小鼠和接受mead203的小鼠。每组有5只小鼠。在第5天给小鼠安排各自的饮食治疗。小鼠自由取食。完全饮食和mead203的组成在实施例14的表5中描述。每周监测肿瘤大小3次。收集肿瘤组织和血浆样品。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。
结果。如图6所示,与用完全饮食治疗的小鼠相比,用mead203治疗的小鼠表现出明显的肿瘤体积减小。在研究期间,用mead203治疗的小鼠的肿瘤体积始终比用完全饮食治疗的小鼠更低。到第46天,mead203小鼠的肿瘤体积比完全饮食小鼠低约60%。
胰腺癌
程序。通过皮下注射将miapaca-2细胞植入无胸腺裸鼠。小鼠为6-8周大。该研究具有两组:接受完全饮食的小鼠和接受治疗饮食[mead201(第0-24天)、mead202(第25-39天)和mead203(第39天)]的小鼠。每组有5只小鼠。在第0天给小鼠安排各自的饮食。小鼠植入7天后被安排各自的饮食。完全饮食和mead202的组成在实施例14的表5中描述。小鼠自由取食。每周监测肿瘤大小2次。收集肿瘤组织和血浆样品。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。
结果。如图7所示,与用完全饮食治疗的小鼠相比,用治疗饮食治疗的小鼠表现出明显的肿瘤体积减小。在研究期间,平均而言,用治疗饮食治疗的小鼠的肿瘤体积要比用完全饮食治疗的小鼠低。到第50天,治疗饮食小鼠的肿瘤体积比完全饮食的小鼠低40%以上。
实施例9:饮食和透析
在胶质母细胞瘤中测试了营养饮食和透析的效果。给研究中的小鼠安排图2所示的饮食之一并且/或者用图8所示的组合物之一进行透析。在mead102、mead103和mead104中,分别使用了8组分维生素混合物、10组分维生素混合物和10组分维生素混合物。对于mead102,维生素混合物包括:维生素b6、叶酸(维生素b9)、硫胺、核黄素、维生素b12、生物素、胆碱和肌醇。对于mead103,维生素混合物包括mead102混合物、烟酰胺和泛酸钙。下表8中描述了mead101、mead102、mead103和mead104的组成。
表8:透析成分
程序。通过皮下注射将u87mg细胞植入无胸腺裸鼠。小鼠为6-8周大。图9中的研究具有3组:接受完全饮食的小鼠、接受mead203的小鼠,和接受mead203并在多个时间点用mead101、mead102和mead103进行透析的小鼠。每个治疗组有1只小鼠。在第5天给小鼠安排各自的治疗。小鼠植入7天后被安排各自的饮食。小鼠自由取食。为了进行透析,将约2ml的透析溶液注入腹膜腔中,并在约2小时后抽出。每天监测肿瘤大小。箭头指示所使用的透析流体的日期和类型。图10中的研究具有4组:接受完全饮食的小鼠、接受仅饮食的小鼠、接受仅透析的小鼠以及接受饮食和透析的小鼠。每组有6只小鼠。在第1天给小鼠安排各自的治疗。饮食mead203用作治疗饮食。设计的对照用作对照饮食。小鼠植入22天后被安排各自的饮食。小鼠自由取食。使用mead103进行透析。对于每次透析,将约2ml的液体注入腹膜腔,约2小时后抽出。每周进行一次透析。每个工作日对小鼠进行监测。
结果。在图9中,接受mead203饮食和透析的小鼠经历了肿瘤体积减小。在第16天对完全饮食的小鼠实施安乐死,因为连续3次测量肿瘤体积超过2000mm3。另外,由于担心小鼠中有过度溃疡和感染,对小鼠实施安乐死。如图10所示,与接受完全饮食的小鼠和接受仅透析的小鼠相比,接受饮食+透析治疗的小鼠和接受仅饮食治疗的小鼠表现出肿瘤体积的减小。在研究过程中,与其他治疗组相比,饮食+透析小鼠始终具有最低的肿瘤体积。在第12天,与接受完全饮食的小鼠和接受仅透析的小鼠相比,接受饮食+透析治疗的小鼠和接受仅饮食治疗的小鼠白表现出约40%的肿瘤体积减小。
实施例10:体重
程序。在图11a中,通过皮下注射将mda-mdb-231细胞植入无胸腺裸鼠。小鼠为5-6周大。该研究具有4组:接受mead203的小鼠、接受mead202的小鼠、接受完全饮食的小鼠和接受天然食物的小鼠。实施例16描述了天然食物。每组有5只小鼠。在第20天给小鼠安排各自的饮食。完全饮食和治疗饮食的组成在实施例14的表5中描述。小鼠自由取食。每周监测体重3次。收集肿瘤组织和血浆样品,仅分析血浆样品的葡萄糖和β-酮体测量值。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。在图11b中,通过皮下注射将pc-3细胞植入无胸腺裸鼠,通过皮下注射将pc-3细胞植入无胸腺裸鼠。小鼠为5-6周大。该研究具有两组:接受mead203的小鼠和接受完全饮食的小鼠。每组有5只小鼠。在第5天给小鼠安排各自的饮食。小鼠自由取食。完全饮食和mead202的组成在实施例14的表5中描述。每周监测体重3次。收集肿瘤组织和血浆样品,仅分析血浆样品的葡萄糖和β-酮体测量值。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。
结果。如图11所示,与完全饮食的小鼠和天然食物的小鼠相比,接受mead203治疗的小鼠和用mead202治疗的小鼠表现出体重减轻。在第23天,与完全饮食的小鼠和仅透析的小鼠相比,接受mead203的小鼠和用mead202治疗的小鼠体重减轻了约15%。对于各治疗饮食,体重减轻相对稳定。
实施例11:血糖
程序。在图12a中,通过皮下注射将mda-mdb-231细胞植入无胸腺裸鼠。小鼠为5-6周大。该研究具有4组:接受mead203的小鼠、接受mead202的小鼠、接受完全饮食的小鼠和接受天然食物的小鼠。实施例16描述了天然食物。每组有5只小鼠。在第20天,给小鼠安排各自的饮食。完全饮食和治疗饮食的组成在实施例14的表5中描述。小鼠自由取食。在治疗开始之前和治疗完成之后收集血浆样品。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。在图12b中,通过皮下注射将pc-3细胞植入无胸腺裸鼠。小鼠为5-6周大。该研究具有两组:接受mead203的小鼠和接受完全饮食的小鼠。每组有5只小鼠。在第5天,给小鼠安排各自的饮食。小鼠自由取食。完全饮食和mead203的组成在实施例14的表5中描述。在治疗开始之前和治疗完成之后收集血浆样品。收集肿瘤组织和血浆样品,仅分析血浆样品的葡萄糖和β-酮体测量值。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。用novamax葡萄糖试纸测量血浆中的葡萄糖。
结果。如图12a和图12b所示,在治疗组中血糖没有增加。在图12a中,mead202小鼠和med203小鼠的施用后葡萄糖水平与施用前水平相似或更低。在图12b中,mead203小鼠的施用后葡萄糖水平与其施用前水平相似。
实施例12:酮症
程序。在图13a中,通过皮下注射将mda-mdb-231细胞植入无胸腺裸鼠。小鼠为5-6周大。这项研究具有4组:接受mead203的小鼠、接受mead202的小鼠、接受完全饮食的小鼠和接受天然食物的小鼠。实施例16描述了天然食物。每组有5只小鼠。在第20天,给小鼠安排各自的饮食。完全饮食和治疗饮食的组成在实施例14的表5中描述。小鼠自由取食。在治疗开始之前和治疗完成之后收集血浆样品。收集肿瘤组织和血浆样品,仅分析血浆样品的葡萄糖和β-酮体测量值。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。在图13b中,通过皮下注射将pc-3细胞植入无胸腺裸鼠。小鼠为5-6周大。该研究具有两组:接受mead203的小鼠和接受完全饮食的小鼠。每组有5只小鼠。在第5天,给小鼠安排各自的饮食。植入后5天,给小鼠安排各自的饮食。小鼠自由取食。完全饮食和mead203的组成在实施例14的表5中描述。在治疗开始之前和治疗完成之后收集血浆样品。收集肿瘤组织和血浆样品,仅分析血浆样品的葡萄糖和β-酮体测量值。显示了显著性:*为p<0.05,**为p<0.01,***为p<0.001。用novamax酮试纸测定血浆中的β-酮体。
结果。如图13a和图13b所示,治疗饮食不会引发酮症。在图13a中,mead202小鼠和med203小鼠的施用后的β-酮水平与施用前水平相似。在图13b中,mead203小鼠的施用后β-酮水平与其施用前的水平相似。
实施例13:透析流体组成
如下所示的表4提供了本文所述的透析流体——干燥组合物、浓缩组合物或液体组合物的示例性配方。
表4:透析流体组成
实施例14:食品组合物
如下所示的表5提供了本文所述的食品组合物的示例性配方。下面的食品组合物是上面研究中使用的饮食。
表5:食品组合物
实施例15:用谷氨酸和维生素减少半胱氨酸摄取
本公开内容的研究表明,当接受mead治疗饮食时,小鼠血浆谷氨酸增加了约80-100%。血浆谷氨酸的增加可能由于对xct转运蛋白的影响而导致半胱氨酸的更新减少。从理论上讲,这可以使所有细胞吸收半胱氨酸的能力减半。
本公开内容的研究表明,维生素在减少半胱氨酸中具有重要的作用。维生素(尤其是b族维生素)对于本文公开的透析和营养饮食很重要。维生素可以维持正常细胞的适当生理学。维生素对神经健康和新陈代谢很重要。维生素还可以帮助正常细胞合成靶营养素——当这些营养素在饮食中没有提供或通过透析消耗掉时。维生素c不包括在小鼠研究中,因为维生素c(抗坏血酸)不是小鼠的维生素,因为它们可以体内产生。维生素c在治疗人类中有望发挥重要作用。下表6提供了用于本文所述的组合物中的一些示例性维生素。
表6:维生素
实施例16:天然食物组成
表7:天然食物组成
1.配方基于来自最新的成分分析信息的计算数值。由于天然成分的营养组成的变化,以及由于制造过程,将会发生一些营养的损失,分析将会相应地有所不同。
2.营养素以百分数表示,除非另有说明。出于计算目的,水分含量假定为10.0%。
3.ndf=大约纤维素、半纤维素和木质素。
4.adf=大约纤维素和木质素。
5.生理能值(kcal/gm)=蛋白质、脂肪和碳水化合物(使用无氮提取物)的十进制分数分别乘以4、9、4kcal/gm的总和。
1.配方基于来自最新的成分分析信息的计算数值。由于天然成分的营养组成的变化,以及由于制造过程,将会发生一些营养的损失,分析将会相应地有所不同。
2.营养素以百分数表示,除非另有说明。出于计算目的,水分含量假定为10.0%。
3.ndf=大约纤维素、半纤维素和木质素。
4.adf=大约纤维素和木质素。
5.生理能值(kcal/gm)=蛋白质、脂肪和碳水化合物(使用无氮提取物)的十进制分数分别乘以4、9、4kcal/gm的总和。
尽管已经在本文中示出和描述了本发明的优选实施方案,但是对于本领域技术人员而言显而易见的是,这些实施方案仅以示例的方式提供。在不脱离本发明的情况下,本领域技术人员现在将想到许多变型、改变和替代。应当理解,本文所述的本发明的实施方案的各种替代方案可以用于实施本发明。所附权利要求书旨在限定本发明的范围,并且由此涵盖这些权利要求范围内的方法和结构及其等同项。
- 还没有人留言评论。精彩留言会获得点赞!