一种实时荧光解旋酶依赖扩增方法及体系与流程
本发明涉及分子生物学领域。具体而言,涉及一种实时荧光解旋酶依赖扩增方法以及基于该方法的DNA或RNA扩增体系。
背景技术:
PCR技术在科研、疾病诊断、法医鉴定、农业等领域被广泛应用,该技术通过借助热循环仪器,利用温度的循环变化,在体外模拟双链DNA变性成为单链DNA、引物与单链DNA互补配对、DNA聚合酶以单链DNA为模板从引物的3’端开始合成新的DNA链等步骤,使模板DNA被扩增。但是PCR技术依赖热循环仪器,而该仪器成本较高,这使得PCR技术在偏远、贫困地区的应用受到限制,另外,由于在PCR扩增过程中,需要反复升降温,这也使得PCR扩增的时间较长,不利于PCR技术在紧急事件的现场检测。
恒温核酸扩增技术,由于能在恒定温度下体外扩增核酸模板,不需要昂贵的热循环仪器,且省去了反复升降温的时间损耗,加快了扩增的速率。业界常采用的恒温核酸扩增技术包括环介导等温核酸扩增技术(LAMP)和解旋酶依赖扩增(HDA)等。其中,环介导等温核酸扩增技术(LAMP)借助可以回折的特殊引物结构,从而不依赖温度变化即可不断产生可用于扩增的单链DNA模板(Notomi等.(2000),Nucleic acid research 28,doi:10.1093/nar/28.12.e63)。但是LAMP技术需要对核酸模板上的六个区段设计4条引物,引物设计过程复杂,限制因素多;且反应体系中包含的引物种类多、浓度高,限制了LAMP技术同时对多个核酸模板的检测;此外,LAMP扩增的产物复杂,较难通过对产物的分析来区分所得到的产物是否为特异产物。
与LAMP通过特殊结构引物,在扩增过程中不断产生单链DNA模板不同,解旋酶依赖扩增(HDA)(Vincent等.(2004),EMBO reports 5(8):795-800)是通过借助解旋酶(Helicase)的作用,使双链DNA解链成为单链DNA,再借助 单链DNA结合蛋白(Single strand DNA binding protein,SSB)的作用,使单链DNA稳定,或者借助耐热的解旋酶,在没有SSB的情况下,使双链DNA解链成为单链DNA。这使得HDA技术只需要上下游各一条引物即可对核酸模板进行扩增。
更进一步地,现有技术中通过借助双链核酸荧光染料或引物,可以实时监测HDA扩增,但是染料法的实时荧光HDA不能进行识别多重靶标,而引物只能标记FAM、JOE、Alexa Fluor 546三种荧光基团,这也限制了实时荧光HDA的应用。
技术实现要素:
针对现有技术中的不足,本发明解决的技术问题在于提供一种实时荧光解旋酶依赖扩增方法,通过在解旋酶依赖扩增的一侧引物5’端锚定有一发卡结构,并在发卡结构端部标记有在解旋酶依赖扩增反应过程中实时检测产物浓度的荧光物质,从而准确监测HDA反应。
本发明解决的技术问题还在于提供一种实时荧光解旋酶依赖扩增方法,通过在解旋酶依赖扩增的一侧引物5’端锚定有一发卡结构,克服了现有技术的染料法实时荧光HDA不能进行识别多重靶标的问题,并且提高了荧光基团的选择多样性。
为了解决上述技术问题,本发明实施例提供的实时荧光解旋酶依赖扩增方法,其解旋酶依赖扩增的一侧引物5’端锚定有一发卡结构,该发卡结构端部标记有在解旋酶依赖扩增反应过程中实时检测产物浓度的荧光物质。
优选地,所述的发卡结构的5’末端和3’末端互补配对;所述的发卡结构的5’末端和3’末端不与靶标序列互补配对;所述的发卡结构除5’末端和3’末端的序列与所锚定引物延伸后产生的新链互补配对。
优选地,所述发卡结构的5’末端标记了发光基团,3’末端标记了淬灭基团;或者,所述发卡结构的3’末端标记了发光基团,5’末端标记了淬灭基团。
进一步地,发光基团为Pacific Blue、Oregon Green、Bodipy FL-X、FAM、TET、Bodipy R6G-X、JOE、HEX、Cy3、Rhodamine Red-X、TAMRA、Cy3.5、 Texas Red-X、ROX中的任意一种,所述淬灭基团为Dabcyl、BHQ-1、QYS-7、BHQ-2中的任意一种。
优选地,该解旋酶依赖扩增方法中所用解旋酶为耐热的解旋酶。
优选地,该解旋酶依赖扩增方法中所用的解旋酶和DNA聚合酶的选用包含如下选择中的至少一种:
(a)解旋酶为水生栖热菌来源的UvrD
(b)DNA聚合酶为Klentaq DNA聚合酶,或Bst DNA聚合酶大片段,或PyroPhage聚合酶,或DisplaceAce聚合酶,或Vent(exo-)聚合酶。
另外,本发明还提供了一种用于DNA模板扩增的实时荧光解旋酶依赖扩增体系,其包含:5’端锚定了发卡结构的单侧引物,和另一侧引物;该发卡结构端部标记有在解旋酶依赖扩增反应过程中实时检测产物浓度的荧光物质。
该用于DNA模板扩增的实时荧光解旋酶依赖扩增体系还包含:
解旋酶,
ATP,
DNA聚合酶,
dATP,dTTP,dGTP,dCTP,
Tris,
硫酸镁和/或氯化镁,
氯化钠和/或氯化钾。
本发明还提供了一种用于RNA模板扩增的实时荧光解旋酶依赖扩增体系,其包含:5’端锚定了发卡结构的单侧引物,和另一侧引物;该发卡结构端部标记有在解旋酶依赖扩增反应过程中实时检测产物浓度的荧光物质。
该用于RNA模板扩增的实时荧光解旋酶依赖扩增体系还包含:
解旋酶,
ATP,
DNA聚合酶,
逆转录酶,
dATP,dTTP,dGTP,dCTP,
Tris,
硫酸镁和/或氯化镁,
氯化钠和/或氯化钾。
本发明实施例提供的实时荧光解旋酶依赖扩增方法以及基于该方法的DNA或RNA扩增体系,具有如下有益效果:
本发明实施例提供的实时荧光解旋酶依赖扩增方法,通过在解旋酶依赖扩增的一侧引物5’端锚定有一发卡结构,并在发卡结构端部标记有在解旋酶依赖扩增反应过程中实时检测产物浓度的荧光物质,从而准确检测HDA反应。具体而言,该发卡结构的5’末端和3’末端互补配对,发卡结构的5’末端标记了发光基团,3’末端标记了淬灭基团,从而使发光基团与淬灭基团在HDA反应前相互结合,不产生荧光。当模板经过解旋酶作用,由双链DNA解链成为单链DNA时,5’端锚定有该发卡结构一侧引物与单链DNA结合,并在DNA聚合酶的作用下合成互补链,由于发卡结构的5’末端和3’末端不与模板互补配对,而发卡结构除5’末端和3’末端的序列与所锚定引物延伸后产生的新链互补配对,因此,随着DNA聚合反应的发生,标记于发卡结构5’末端的发光基团和3’末端标记了淬灭基团因除5’末端和3’末端的序列与所锚定引物延伸后产生的新链互补配对而分离,发光基团产生荧光,从而实现对HDA反应的准确监测。另外,由于发光基团和淬灭基团分别标记于发卡结构的两端,且发卡结构锚定于5’端HAD反应的一侧引物上,因此,采用本发明的荧光解旋酶依赖扩增方法及体系能够有效地实现多标靶识别,并且能够选择多种发光基团和与之对应的淬灭基团,提高了荧光基团的选择多样性,实现对多模版、多指标HDA反应的实时监测。
附图说明
图1示出了本发明的实时荧光解旋酶依赖扩增方法的原理图。
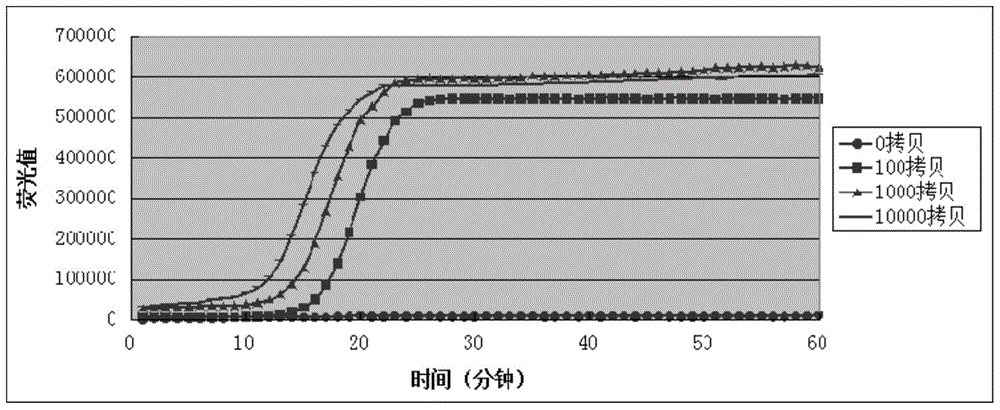
图2示出了实施例1中对含模板的质粒DNA的实时荧光解旋酶依赖扩增图。
图3示出了实施例1中扩增产物的琼脂糖凝胶电泳图。第1个条带为双链 DNA Marker;凝胶上第2至5个条带依次为实施例中的“0拷贝”、“100拷贝”、“1000拷贝”、“10000拷贝”。
图4示出了实施例2中对RNA模板的实时荧光解旋酶依赖扩增图。
具体实施方式
本发明实施例提供的实时荧光解旋酶依赖扩增方法,其解旋酶依赖扩增的一侧引物5’端锚定有一发卡结构,该发卡结构端部标记有在解旋酶依赖扩增反应过程中实时检测产物浓度的荧光物质。
其中,所述的发卡结构的5’末端和3’末端互补配对;所述的发卡结构的5’末端和3’末端不与靶标序列互补配对;所述的发卡结构除5’末端和3’末端的序列与所锚定引物延伸后产生的新链互补配对。
其中,所述发卡结构的5’末端标记了发光基团,3’末端标记了淬灭基团;或者,所述发卡结构的3’末端标记了发光基团,5’末端标记了淬灭基团。
其中,发光基团为Pacific Blue、Oregon Green、Bodipy FL-X、FAM、TET、Bodipy R6G-X、JOE、HEX、Cy3、Rhodamine Red-X、TAMRA、Cy3.5、Texas Red-X、ROX中的任意一种,所述淬灭基团为Dabcyl、BHQ-1、QYS-7、BHQ-2中的任意一种。
其中,该解旋酶依赖扩增方法中所用解旋酶为耐热的解旋酶。
其中,该解旋酶依赖扩增方法中所用的解旋酶和DNA聚合酶的选用包含如下选择中的至少一种:
(a)解旋酶为水生栖热菌来源的UvrD
(b)DNA聚合酶为Klentaq DNA聚合酶,或Bst DNA聚合酶大片段,或PyroPhage聚合酶,或DisplaceAce聚合酶,或Vent(exo-)聚合酶。
另外,本发明实施例提供的一种用于DNA模板扩增的实时荧光解旋酶依赖扩增体系,其包含:5’端锚定了发卡结构的单侧引物,和另一侧引物;该发卡结构端部标记有在解旋酶依赖扩增反应过程中实时检测产物浓度的荧光物质。
该用于DNA模板扩增的实时荧光解旋酶依赖扩增体系还包含:
解旋酶,
ATP,
DNA聚合酶,
dATP,dTTP,dGTP,dCTP,
Tris,
硫酸镁和/或氯化镁,
氯化钠和/或氯化钾。
在这,本发明实施例提供的一种用于RNA模板扩增的实时荧光解旋酶依赖扩增体系,其包含:5’端锚定了发卡结构的单侧引物,和另一侧引物;该发卡结构端部标记有在解旋酶依赖扩增反应过程中实时检测产物浓度的荧光物质。
该用于RNA模板扩增的实时荧光解旋酶依赖扩增体系还包含:
解旋酶,
ATP,
DNA聚合酶,
逆转录酶,
dATP,dTTP,dGTP,dCTP,
Tris,
硫酸镁和/或氯化镁,
氯化钠和/或氯化钾。
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
下面实施例中未注明具体条件的实验方法,通常按照常规条件,例如Sambrook等分子克隆实施手册中所述的条件。
实施例1:使用本发明对DNA模板的扩增。
在本实施例中,使用本发明方法对含金黄色葡萄球菌基因组的FemA基因序列5’-tggtgccttt acagatagca tgccatacag tcatttcacg caaactgttg gccactatga gttaaagctt gctgaaggtt atgaaacaca tttagtggga ataaaaaaca ataataacga ggtcattgca gctt-3’的pMD-18T质粒(购自大连宝生物公司)DNA进行扩增。
(1)引物序列
锚定了发夹结构的上游引物序列:
5’-FAM-tacagaTCATAGTGGCCAACAGAAAGCGAtctgta-Dabcyl-TGGTGCCTTTACAGATAG-3’<SEQ ID NO.1>
下游引物序列:5'-AAGCTGCAATGACCTCGT-3'<SEQ ID NO.2>
发夹结构序列:5’-tacagaTCATAGTGGCCAACAGAAAGCGAtctgta-3’
发卡结构5’端序列:5’-tacaga-3’
发卡结构5’端序列:5’-tctgta-3’
发卡结构中的探针序列:5’-TCATAGTGGCCAACAGAAAGCGA-3’
(2)质粒DNA模板的准备
紫外分光光度法测定质粒的浓度,根据质粒DNA的分子量,计算得每微升溶液中质粒DNA的拷贝数,用TE缓冲液(10mmol/l Tris-HCl,1mmol/l EDTA,pH7.5)稀释至每微升溶液含109拷贝质粒DNA,然后用TE缓冲液10倍梯度稀释,连续稀释7个梯度。
(3)针对DNA模板的实时荧光解旋酶依赖扩增反应体系:
-6mmol/l MgSO4,
-50mmol/l KCl,
-30mmol/l Tris-HCl(pH 8.8),
-0.1%Triton X-100(v/v),
-0.8mmol/l dNTPs,
-10μmol/l引物,
-1.5mmol/l ATP,
-Taq UvrD解旋酶,
-5U Bst DNA聚合酶大片段,
-1μl质粒DNA模板,
-反应液总体积25μl。
(4)针对DNA模板的实时荧光解旋酶依赖扩增
实时荧光解旋酶依赖扩增在ABI StepOne(Life Technologies公司)仪器中进行,反应程序是:65℃,1分钟,60个循环,检测荧光信号,结果如图2所示。
(5)琼脂糖凝胶电泳
1%琼脂糖凝胶于1×TAE缓冲液中,在4v/cm场强条件下对扩增产物进行分析,电泳结束后用4×SYBR GreenⅠ染料染色20分钟,然后观察电泳结果如图3所示。
实施例2:使用本发明对RNA模板的扩增。
在本实施例中,使用本发明方法对含人的甘油醛-3-磷酸脱氢酶基因mRNA序列:5’-gcucccucuu ucuuugcagc aaugccuccu gcaccaccaa cugcuuagca ccccuggcca aggucaucca ugacaacuuu gguaucgugg aaggacu-3’进行扩增。
(1)引物序列
锚定了发夹结构的上游引物序列:
5’-FAM-tacagaAGGGGTGCTAAGCAGTTGGTGtctgta-Dabcyl-GCTCCCTCTTTCTTTGCA-3’<SEQ ID NO.3>
下游引物序列:5'-AGTCCTTCCACGATACCAA-3'<SEQ ID NO.4>
发夹结构序列:5’-tacagaAGGGGTGCTAAGCAGTTGGTGtctgta-3’
发卡结构5’端序列:5’-tacaga-3’
发卡结构5’端序列:5’-tctgta-3’
发卡结构中的探针序列:5’-AGGGGTGCTAAGCAGTTGGTG-3’
(2)样品处理
对口腔上皮细胞或血液取样后,对样品进行RNA提取,所得RNA用于扩增。
(3)针对RNA模板的实时荧光解旋酶依赖扩增反应体系:
-6mmol/l MgSO4,
-50mmol/l KCl,
-30mmol/l Tris-HCl(pH 8.8),
-0.1%Triton X-100(v/v),
-0.8mmol/l dNTPs,
-10μmol/l引物,
-1.5mmol/l ATP,
-1U MMLV逆转录酶,
-5U RNase抑制剂,
-Taq UvrD解旋酶,
-5U Bst DNA聚合酶大片段,
-1μl RNA模板,
反应液总体积25μl。
(4)针对RNA模板的实时荧光解旋酶依赖扩增
实时荧光解旋酶依赖扩增在ABI StepOne(Life Technologies公司)仪器中进行,反应程序是:42℃,15分钟,1个循环;65℃,1分钟,60个循环,检测荧光信号,结果如图4所示。
以上所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种新的多肽——人rna解旋酶9.13和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人核糖核酸解旋酶48.4和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人rna解旋酶10和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人rna解旋酶13和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人rna解旋酶9和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人rna解旋酶12和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人rna解旋酶105和编码这种多肽的多核苷酸的制作方法
- Hcv ns-3丝氨酸蛋白酶抑制剂的制作方法
- 丙型肝炎病毒ns3解旋酶atp结合位点单克隆抗体识别表位的制作方法
- 一个编码冰缘植物冷诱导蛋白的基因及其在抗寒转基因烟草中的应用的制作方法