多重PCR检测脑炎脑膜炎相关病毒用引物组和试剂盒的制作方法
本发明涉及生物技术领域,具体地,涉及多重PCR检测脑炎脑膜炎相关病毒引物组和试剂盒及其检测方法。
背景技术:
病毒感染引起的神经系统损伤己经逐渐成为临床上最常见的中枢神经系统感染性疾病,虫媒病毒类、肠道病毒等多种病毒感染均可以引发不同程度神经系统症状。
目前由于疫苗的推广及传染媒介干预措施得力,使得具有地域性、季节性、流行性的乙脑、森林脑炎脑膜炎等多种传染病发病率明显下降,而由肠道病毒、疱疹病毒、呼吸道病毒等引起的中枢神经系统感染成为了常见病、多发病,严重危害儿童健康,甚至致死、致残。中枢神经系统病毒感染的病原种类繁杂,已经发现130余种病毒可以引起病毒性脑炎脑膜炎,各国病毒性脑炎脑膜炎的病原分布情况各不相同。在世界范围内,最常见的脑炎脑膜炎病原是乙型脑炎脑膜炎病(Japanese encephalitis virus,JEV)、腮腺炎病毒(Mumps virus,MuV)、肠道病毒(Enterovirus,EV)、单纯疱疹病毒(Herpes simplex virus,HSV)、麻疹病毒(Measle virus,MEV)、呼吸道合胞病毒(Respiratory Syncytial Virus,RSV)、西尼罗病毒(West Nile Virus,WNV)、蜱传脑炎脑膜炎病毒(Tickborne Encephalitis Virus)、流感病毒(Influenza viruses,IFV)、腺病毒(Adenovirus,ADV)等。
病毒性脑炎脑膜炎的早期诊断能有效减轻免疫引起的脑组织损伤,降低后遗症发生率及死亡率。目前常用的检测手段有脑脊液病毒分离、免疫学检测、脑电图和影像学检查及PCR等方法。
传统病毒性脑炎脑膜炎病原体检测技术包括脑脊液病毒分离、免疫学检测等,上述检测方法在临床应用中均存在一定局限性,病毒分离培养虽然是诊断金标准,但对实验室条件要求高,所需时间较长,工作量较大,同一时期无法处理大量样本。而免疫学检测中,病毒易变异,不同病毒间存在交叉反应性等因素均有可能影响检测结果。
PCR因具有较高的敏感性和特异性,操作简便、快速,已逐渐应用于多种病毒性疾病的临床诊断。目前国内外均建立了采用PCR技术对传统病毒性脑炎脑膜炎病原体进行快速检测的技术。但多使用单重PCR技术进行检测,多对引物的退火温度和浓度不尽相同,需要多轮PCR反应逐一检测,这种方法操作繁琐,耗费时间和人力,敏感性和特异性差、检出率低和覆盖度差的问题;需要分别做好每个反应体系的质量控制,比如内部质控。
技术实现要素:
本发明的目的在于解决现有脑膜炎相关病毒检测技术中存在的耗时长、敏感性和特异性差、检出率低和覆盖度差的问题,提供一种新的脑膜炎相关病毒检测引物和方法。
为达到以上目的,本发明提供了一种多重PCR检测脑炎相关病毒用引物组,其中,该引物组包括SEQ ID NO.1和3-22所示的引物;所述脑炎相关病毒包括乙型脑炎脑膜炎病毒、腮腺炎病毒、肠道病毒、单纯疱疹病毒、麻疹病毒、呼吸道合胞病毒、西尼罗病毒、蜱传脑炎脑膜炎病毒、流感病毒和腺病毒。
本发明还提供了一种多重PCR检测脑炎相关病毒的检测方法,该方法包括如下步骤:
(1)提取待测样本的总核酸;
(2)对所述总核酸进行逆转录获得PCR模板;用本发明所述的引物组对所述PCR模板进行多重PCR扩增,获得多重PCR扩增后的物料;
(3)对所述多重PCR扩增后的物料进行核酸电泳检测,得到核酸电泳检测的结果;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有581bp的扩增产物,则指示所述待测样本中含有乙型脑炎脑膜炎病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有189bp的扩增产物,则指示所述待测样本中含有腮腺炎病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有221bp的扩增产物,则指示所述待测样本中含有肠道病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有378bp的扩增产物,则指示所述待测样本中含有单纯疱疹病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有330bp的扩增产物,则指示所述待测样本中含有麻疹病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有123bp的扩增产物,则指示所述待测样本中含有呼吸道合胞病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有277bp的扩增产物,则指示所述待测样本中含有西尼罗病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有505bp的扩增产物,则指示所述待测样本中含有蜱传脑炎脑膜炎病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有150bp的扩增产物,则指示所述待测样本中含有流感病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有402bp的扩增产物,则指示所述待测样本中含有腺病毒。
本发明还提供了检测脑炎相关病毒的试剂盒,所述试剂盒包括本发明所述的多重PCR引物组、逆转录酶和DNA聚合酶;所述脑炎相关病毒包括乙型脑炎脑膜炎病毒、腮腺炎病毒、肠道病毒、单纯疱疹病毒、麻疹病毒、呼吸道合胞病毒、西尼罗病毒、蜱传脑炎脑膜炎病毒、流感病毒和腺病毒。
另一方面,本发明还提供了如上所述的引物组在制备检测脑炎相关病毒的试剂盒中的用途;其中,所述脑炎相关病毒包括乙型脑炎脑膜炎病毒、腮腺炎病毒、肠道病毒、单纯疱疹病毒、麻疹病毒、呼吸道合胞病毒、西尼罗病毒、蜱传脑炎脑膜炎病毒、流感病毒和腺病毒。通过上述技术方案本发明建立了常见脑炎相关病毒多重PCR检测引物组和检测方法,能够实现形态学、免疫学以及单重实时荧光检测所无法完成的快速、全面、敏感、特异、自动的结果判定,显著地提高了对脑炎相关病毒同时进行检测的敏感性、特异性和简便性。
本发明建立的常见十种脑炎脑膜炎病毒多重PCR检测方法,能够实现形态学、免疫学以及单重实时荧光检测所无法完成的快速、全面、敏感、特异、自动的结果判定,达到如下的检测效果:
(一)多重检测覆盖全面
本发明所建立的检测方法能够在一次PCR反应中鉴定脑炎脑膜炎相关的十种病毒,即乙型脑炎脑膜炎病毒、腮腺炎病毒、肠道病毒、单纯疱疹病毒、麻疹病毒、呼吸道合胞病毒、西尼罗病毒、蜱传脑炎脑膜炎病毒、流感病毒、腺病毒,快速获得检测结果,节省时间、人力和物力成本。
(二)特异性高
本发明所建立的检测方法特异性主要体现在一整套引物的特异性,以及全自动结果判定的有效性。所有引物都经过blast比对分析,具有高度的保守性和特异性;同时经过特异性实验验证能够很好的区分与检测目标种属相近的病毒,包括偏肺病毒、冠状病毒OC43、冠状病毒NL63、冠状病毒HKU1、冠状病毒229E、鼻病毒、副流感病毒1-4型、埃可病毒、轮状病毒、诺如病毒及札如病毒等,证明检测方法具有高度的特异性,能够将非检测目标准确区分开来。
(三)灵敏度高
本发明所建立的检测方法能够实现10个目标的同时检测,在一个反应体系中每个检测目标的检测灵敏度可达到10拷贝。本发明灵敏度提高的主要原因是本发明针对所有目标基因的特异性引物对序列设计了特定的LHP序列,LHP序列中的同源通用引物能够在第二阶段PCR中提高多重PCR反应的扩增效率,降低多重PCR反应的非特异性扩增和引物二聚体的产生,而LHP中的6个碱基连接序列能够保证同源通用引物扩增不同毒力基因时具有相同的扩增效率,避免多重PCR扩增过程中不同目标基因产量的失衡,从而在总体上提高多重PCR检测的灵敏度。
(四)成本较低
本发明所建立的多重PCR检测方法在操作性上降低了人力成本和时间成本,原来单重检测需要10次人工和10倍时间,现在使用此方法只需要1次人工和1个反应的时间;该多重检测方法同时节省了重复检测同一个样本的试剂消耗,最大可节省50%的试剂成本。
(五)节省时间
传统的两步法的反应,需要先将病毒的RNA模板逆转录为cDNA,再进行PCR反应,耗时较长。本发明采用一步法的RT-PCR体系,包括提取在内的整个实验过程仅需3小时,显著缩短了检测所需的时间。
(六)自动化结果分析以及判定
采用QIaxcel全自动毛细管电泳分析仪作为结果分析的平台。基于qiaxcel的全自动操作和设定的智能化结果分析程序,实现了结果的自动判定分析。
(七)预防假阴性结果
本发明反应体系中添加的阳性内对照,可以有效的提示因为操作失误、PCR抑制物等原因造成的假阴性检测结果。
本发明为脑炎脑膜炎病毒快速筛查提供了整体的解决方案,能实现快速、敏感特异、自动化地检测十种常见脑炎脑膜炎病毒。
本发明的其他特征和优点将在随后的具体实施方式部分予以详细说明。
具体实施方式
以下结合附图对本发明的具体实施方式进行详细说明。应当理解的是,此处所描述的具体实施方式仅用于说明和解释本发明,并不用于限制本发明。
本发明提供了一种多重PCR检测脑炎相关病毒引物组,其中,该引物组包括SEQ ID NO.1和3-22所示的引物;所述脑炎相关病毒包括乙型脑炎脑膜炎病毒(Japanese encephalitis virus,JEV)、腮腺炎病毒(Mumps virus,MuV)、肠道病毒(Entero virus,EV)、单纯疱疹病毒(Herpes simplex virus,HSV)、麻疹病毒(Measle virus,MEV)、呼吸道合胞病毒(Respiratory Syncytial Virus,RSV)、西尼罗病毒(West Nile Virus,WNV)、蜱传脑炎脑膜炎病毒(Tickborne Encephalitis Virus)、流感病毒(Influenza viruses,IFV)及腺病毒(Adenovirus,ADV)。
其中,优选地,所述引物组还包括SEQ ID NO.23-24所示的引物。SEQ ID NO.23-24所示的引物是以pET-28a质粒为模板设计的一对引物,作为阳性内对照。
具体地,脑膜炎相关病毒多重PCR引物组如表1所示。
表1多重PCR引物组汇总表
其中,SEQ ID NO.1是同源通用引物,该引物与连接序列CATTAA相连,构成LHP序列(SEQ ID NO.2,基于连接序列的同源通用引物(based on ligation-sequence homogenous Primer,LHP))。
本发明还提供了脑炎相关病毒的检测方法,该方法包括如下步骤:
(1)提取待测样本的总核酸;
(2)对所述总核酸进行逆转录获得PCR模板;用本发明所述的引物组对所述PCR模板进行多重PCR扩增,获得多重PCR扩增后的物料;
(3)对所述多重PCR扩增后的物料进行核酸电泳检测,得到核酸电泳检测的结果;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有581bp的扩增产物,则指示所述待测样本中含有乙型脑炎脑膜炎病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有189bp的扩增产物,则指示所述待测样本中含有腮腺炎病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有221bp的扩增产物,则指示所述待测样本中含有肠道病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有378bp的扩增产物,则指示所述待测样本中含有单纯疱疹病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有330bp的扩增产物,则指示所述待测样本中含有麻疹病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有123bp的扩增产物,则指示所述待测样本中含有呼吸道合胞病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有277bp的扩增产物,则指示所述待测样本中含有西尼罗病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有505bp的扩增产物,则指示所述待测样本中含有蜱传脑炎脑膜炎病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有150bp的扩增产物,则指示所述待测样本中含有流感病毒;
如果核酸电泳检测的结果显示所述多重PCR扩增后的物料中含有402bp的扩增产物,则指示所述待测样本中含有腺病毒。
其中,优选地,SEQ ID NO.3-22所示的引物的最终使用浓度各自为0.1-0.8μM,SEQ ID NO.1所示的引物的最终使用浓度为0.4-0.8μM。
其中,优选地,步骤(2)的反应条件包括如下a-i的程序:
a:49-51℃,28-32min;
b:94-96℃,13-18min;
c:94-96℃,28-32s,
d:54-56℃,28-32s,
e:71-73℃,58-62s,进行10个c-e的循环;
f:94-96℃,28-32s,
g:49-51℃,28-32s,
h:71-73℃,59-61s,进行30个f-h的循环;
i:71-73℃,5-10min。
其中,在上述程序中,程序a为对总核酸进行逆转录获得PCR模板的过程,逆转录的目的是将总核酸中的RNA逆转录为cDNA,而在逆转录过程中总核酸中的DNA不会受到影响,逆转录过程结束后,逆转录获得的cDNA和总核酸中的DNA共同作为PCR模板进行下一步的多重PCR扩增。
其中,单纯疱疹病毒和腺病毒的检测序列为DNA序列。
在本公开所提供的方法中,反应体系的组成成分包括待测样本的总核酸、多重PCR引物组、逆转录酶、DNA聚合酶、PCR反应缓冲液和dNTP,在同一个反应体系中进行逆转录过程和多重PCR扩增反应。
其中,所述待测样本可以包括但不限于食品、药品、排泄物、呕吐物和体液中的至少一种。优选地,本发明的多重PCR检测脑炎相关病毒的检测方法不用于诊断。或者说,脑炎相关病毒的定性与定量结果与疾病是否发生没有一一对应的相关性不属于诊断结果,但是脑炎相关病毒的定性与定量的检测结果能够作为中间信息,供临床医生参考。
其中,优选地,所述核酸电泳检测包括核酸凝胶电泳和/或核酸毛细管电泳。
在本发明的一种实施方式中,采用QIaxcel全自动毛细管电泳分析仪作为结果分析的平台。基于QIaxcel的全自动操作和设定的智能化结果分析程序,从而实现结果的自动判定分析。
本发明还提供了一种多重PCR检测脑膜炎相关病毒的试剂盒,所述试剂盒包括本发明所述的多重PCR引物组、逆转录酶和DNA聚合酶;所述脑炎相关病毒包括乙型脑炎脑膜炎病毒、腮腺炎病毒、肠道病毒、单纯疱疹病毒、麻疹病毒、呼吸道合胞病毒、西尼罗病毒、蜱传脑炎脑膜炎病毒、流感病毒和腺病毒。
其中,优选地,所述试剂盒还包括PCR反应缓冲液,逆转录酶和dNTP。
另一方面,本发明还提供了如上所述的引物组在制备检测脑炎相关病毒的试剂盒中的用途;其中,所述脑炎相关病毒包括乙型脑炎脑膜炎病毒、腮腺炎病毒、肠道病毒、单纯疱疹病毒、麻疹病毒、呼吸道合胞病毒、西尼罗病毒、蜱传脑炎脑膜炎病毒、流感病毒和腺病毒。
本发明的其他特征和优点将在随后的具体实施方式部分予以详细说明。
附图说明
附图是用来提供对本发明的进一步理解,并且构成说明书的一部分,与下面的具体实施方式一起用于解释本发明,但并不构成对本发明的限制。在附图中:
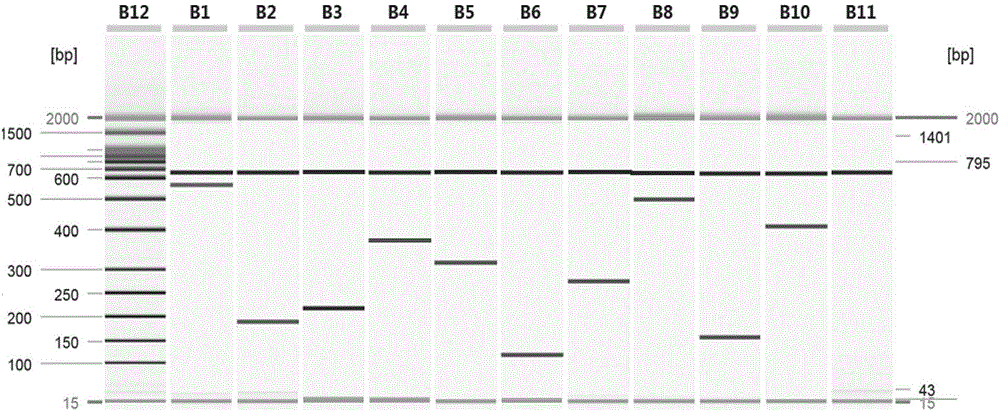
图1为本发明试剂盒实施例1多重体系对单重目标的扩增结果;
B12:100-1500bp Size Marker,
B1:乙型脑炎脑膜炎病毒扩增片段581bp,
B2:腮腺炎病毒扩增片段189bp,
B3:肠道病毒扩增片段221bp,
B4:单纯疱疹病毒扩增片段378bp,
B5:麻疹病毒扩增片段330bp,
B6:呼吸道合胞病毒扩增片段123bp,
B7:西尼罗病毒扩增片段277bp,
B8:蜱传脑炎脑膜炎病毒扩增片段505bp,
B9:流感病毒扩增片段150bp,
B10:腺病毒扩增片段402bp,
B11:空白对照。
图2为本发明试剂盒替换引物多重体系对单重目标的扩增结果;
B12:100-1500bp Size Marker,
B1:乙型脑炎脑膜炎病毒扩增片段180bp,
B2:腮腺炎病毒扩增片段320bp,
B3:肠道病毒扩增片段444bp,
B4:单纯疱疹病毒扩增片段372bp,
B5:麻疹病毒扩增片段496bp,
B6:呼吸道合胞病毒扩增片段560bp,
B7:西尼罗病毒扩增片段378bp,
B8:蜱传脑炎脑膜炎病毒扩增片段670bp,
B9:流感病毒扩增片段229bp,
B10:腺病毒扩增片段280bp,
B11:空白对照。
实施例1
1、引物合成:
按照表1所示的序列,进行SEQ ID NO.1和3-22的引物的合成。
以物质的量为单位,将SEQ ID NO.3-22的引物各取1重量份,与4重量份的SEQ ID NO.1的引物混合,构成本实施例的引物组。
2、试剂盒的组建:
该试剂盒含有2×RT PCR缓冲液、RT-PCR enzyme mix、10×引物混合液、阳性对照、超纯水构成。
试剂盒检测的反应体系为25μL,其配置如下:2×RT PCR缓冲液12.5μL(含IAC模板);RT-PCR enzyme mix 1μL;10×引物混合物2.5μL(包括IAC在内的长引物对浓度各2μM,同源通用引物SEQ ID NO 1浓度为8μM);模板2μL,超纯水7μL。
3、试剂盒的操作和结果判断
(1)病毒基因组的提取
采用商品化提取试剂,从确诊了感染病毒类型的脑脊液或其他临床样本中提取病毒的DNA和RNA核酸。
(2)反应体系的配置
取200μL的PCR管配置25μL的反应体系,其配置如下:2×RT PCR缓冲液12.5μL(含IAC模板);RT-PCR enzyme mix 1μL;10×引物混合物2.5μL;模板2μL,超纯水7μL。
(3)PCR反应
将PCR管放入Bio-Rad C1000型PCR仪中,开启热盖后,按照如下程序进行PCR反应:50℃30min,进行逆转录;95℃15min;95℃30s,55℃30s,72℃60s,10个循环;95℃30s,50℃30s,72℃,60s,30个循环;72℃5min。
(4)QIAxcel全自动毛细管电泳分析仪分析PCR产物
将PCR反应管放入全自动毛细管电泳仪QIAxcel Advanced(凯捷公司),使用高分辨率卡夹,选择15-2000bp的alignment marker,100-1500bp的size marker,自动分析目标条带的大小。
(5)结果判断
具体判定如下:扩增的结果显示,包括空白对照在内的所有泳道均至少有一个条带扩增,空白对照有阳性内对照(670bp)的扩增,其他检测有目标条带和(或)阳性内对照的扩增,表明所有PCR反应均成立,排除假阴性的结果。否则视实验无效,需要重复。根据乙型脑炎脑膜炎病毒581bp,腮腺炎病毒189bp,肠道病毒221bp,单纯疱疹病毒378bp,麻疹病毒189bp,呼吸道合胞病毒123p,西尼罗病毒277bp,蜱传脑炎脑膜炎病毒505bp,流感病毒150bp,腺病毒402bp,判定脑炎脑膜炎病毒种类。
结果如图1所示。
在IAC扩增的基础上,泳道B1还出现1条581bp的PCR扩增产物,是乙型脑炎脑膜炎病毒的扩增条带;泳道B2还出现1条189189bp的PCR扩增产物,是腮腺炎病毒的扩增条带;泳道B3还出现1条221bp的PCR扩增产物,是肠道病毒的扩增条带;泳道B4还出现1条378bp的PCR扩增产物,是单纯疱疹病毒的扩增条带;泳道B5还出现1条330bp的PCR扩增产物,是麻疹病毒的扩增条带;泳道B6还出现1条123bp的PCR扩增产物,是呼吸道合胞病毒的扩增条带;泳道B7还出现1条277bp的PCR扩增产物,是西尼罗病毒的扩增条带;第泳道B8还出现1条505bp的PCR扩增产物,是蜱传脑炎脑膜炎病毒的扩增条带;泳道B8还出现1条150bp的PCR扩增产物,是流感病毒的扩增条带;泳道B10还出现1条402bp的PCR扩增产物,是腺病毒的扩增条带。泳道B11为NTC,仅有IAC扩增条带。
实施例2试剂盒的特异性试验
选择偏肺病毒(源自国家CDC,编号为IVDC 2.2445)、冠状病毒OC43(源自国家CDC,编号为IVDC 2.2339)、冠状病毒NL63(源自国家CDC,编号为IVDC 2.2338)、冠状病毒HKU1(源自国家CDC,编号为IVDC2.2440)、冠状病毒229E(源自国家CDC,编号为IVDC 2.2441)、鼻病毒(源自国家CDC,编号为IVDC 2.2500)、副流感病毒1-4型(源自国家CDC,编号为IVDC 2.2610)、埃可病毒(源自国家CDC,编号为IVDC 2.2333)、轮状病毒(源自国家CDC,编号为IVDC 2.2450)、诺如病毒(源自国家CDC,编号为IVDC 2.2461)、札如病毒(源自国家CDC,编号为IVDC 2.2462)等作为特异性验证模板。
应用本发明试剂盒检测这些待检目标,在阳性对照成立的条件下,待检目标均无非特异性的杂带,表明本发明试剂盒能够有效区分检测目标与非检测目标,具有较好的特异性。
实施例3试剂盒的最低检出限试验
评估用检测样本:用限制性内切酶SpeI和PvuII酶切乙型脑炎脑膜炎病毒、腮腺炎病毒、肠道病毒、麻疹病毒、呼吸道合胞病毒、西尼罗病毒、蜱传脑炎脑膜炎病毒、流感病毒等的标准品质粒,将其线性化并进行体外转录;选取初始浓度为106拷贝/μl转录产物梯度稀释,作为最低检出限评估的模板。因单纯疱疹病毒和腺病毒为DNA病毒,选取初始浓度为106拷贝/μl的含扩增序列的质粒进行梯度稀释,作为最低检出限评估的模板。
按照实施例1的方法进行检测,结果显示试剂盒的最低检出限可达到10拷贝/反应。
实施例4本发明的试剂盒与文献方法的比较
评价本发明试剂盒与文献报道(Development of a GeXP based multiplex RT-PCR assay for simultaneous detection of eight arboviruses related to encephalitis)效果比较,主要从敏感度、特异性和覆盖度三个方面进行比较。
评价用阳性样本:乙型脑炎脑膜炎病毒(源自国家CDC,编号分别为IVDC 2.24421、2.24422、2.24423、2.24424、2.24425、2.24426、2.24427、2.24428、2.24429、2.24430)、腮腺炎病毒(源自国家CDC,编号分别为IVDC2.25311、2.25312、2.25313、2.25314、2.25315、2.25316、2.25317、2.25318、2.25319、2.25320)、肠道病毒(源自国家CDC,编号为IVDC2.22332、2.22332、2.22333、2.22334、2.22335、2.22336、2.22337、2.22338、2.22339、2.22340)、单纯疱疹病毒(源自国家CDC,编号为IVDC 2.21343、2.21344、2.21345、2.21346、2.21347、2.21348、2.21349、2.21350、2.21351、2.21352)、麻疹病毒(源自国家CDC,编号为IVDC 2.21751、2.21752、2.21753、2.21754、2.21755、2.21756、2.21757、2.21758、2.21759、2.21760)、呼吸道合胞病毒(源自国家CDC,编号为IVDC 2.27613、2.27614、2.27615、2.27616、2.27617、2.27618、2.27619、2.27620、2.27621、2.27622)、西尼罗病毒(源自国家CDC,编号为IVDC 2.27801、2.27802、2.27803、2.27804、2.27805、2.27806、2.27807、2.27808、2.27809、2.27810)、蜱传脑炎脑膜炎病毒(源自国家CDC,编号为IVDC 2.27930、2.27931、2.27932、2.27933、2.27934、2.27935、2.27936、2.27937、2.27938、2.27939)、流感病毒(源自国家CDC,编号为IVDC 2.25331、2.25332、2.25333、2.25334、2.25335、2.25336、2.25337、2.25338、2.25339、2.25340)、腺病毒(源自国家CDC,编号为IVDC 2.29512、2.29513、2.29514、2.29515、2.29516、2.29517、2.29518、2.29519、2.29520、2.29521)各10株。
评价用阴性样本:选择实施例2中偏肺病毒、冠状病毒OC43、冠状病毒NL63、冠状病毒HKU1、冠状病毒229E、鼻病毒、副流感病毒1-4型、埃可病毒、轮状病毒、诺如病毒、札如病毒等病毒作为特异性验证模板。将以上菌毒株提取核酸后,等比例混合成一个阴性评估模板。
特异性评估:按照本发明实施例2进行特异性评估操作。
覆盖度评估:采用本发明试剂盒和文献方法分别检测10株评价用阳性样本。
最低检出限评估:用限制性内切酶SpeI和PvuII酶切乙型脑炎脑膜炎病毒、腮腺炎病毒、肠道病毒、麻疹病毒、呼吸道合胞病毒、西尼罗病毒、蜱传脑炎脑膜炎病毒、流感病毒等的标准品质粒,将其线性化并进行体外转录;选取初始浓度为106拷贝/μl转录产物梯度稀释,作为最低检出限评估的模板。因单纯疱疹病毒和腺病毒为DNA病毒,选取初始浓度为106拷贝/μl含扩增片段的质粒进行梯度稀释,作为最低检出限评估的模板。采用本发明试剂盒和文献方法分别检测各脑炎脑膜炎病毒的梯度稀释模板。
比较结果:本发明试剂盒和文献报道方法检测阴性样本结果均为阴性,表明均具有较好的特异性。
本发明试剂盒检测评价用阳性样本,均获得阳性结果,而文献报道方法有2株乙型脑炎脑膜炎病毒和2株呼吸道合胞病毒病毒的漏检。
本发明试剂盒和文献报道方法检测十种脑炎脑膜炎病毒的最低检出限对比如下表2。
表2本发明与文献报道方法的最低检出限对比结果
由上表可知,本发明试剂盒检测10种目标基因的最低检出限均能达到10拷贝/μl的水平,而文献报道方法只有肠道病毒、麻疹病毒、呼吸道合胞病毒、西尼罗病毒能够达到100拷贝/μl的水平,其余只能达到1000拷贝/μl的水平。本发明试剂盒检测的最低检出限显著优于文献报道方法。
对比例1
制备对比引物25-44,见表3。
表3对比引物序列表
按照实施例1的方法进行检测,区别仅在于,将实施例1的引物组中SEQ ID NO.3-4所示的引物替换为SEQ ID NO.25-26所示的引物获得对比引物组1。
将实施例1的引物组中SEQ ID NO.5-6所示的引物替换为SEQ ID NO.27-28所示的引物获得对比引物组2。
将实施例1的引物组中SEQ ID NO.7-8所示的引物替换为SEQ ID NO.29-30所示的引物获得对比引物组3。
将实施例1的引物组中SEQ ID NO.9-10所示的引物替换为SEQ ID NO.31-32所示的引物获得对比引物组4。
将实施例1的引物组中SEQ ID NO.11-12所示的引物替换为SEQ ID NO.33-34所示的引物获得对比引物组5。
将实施例1的引物组中SEQ ID NO.13-14所示的引物替换为SEQ ID NO.35-36所示的引物获得对比引物组6。
将实施例1的引物组中SEQ ID NO.15-16所示的引物替换为SEQ ID NO.37-38所示的引物获得对比引物组7。
将实施例1的引物组中SEQ ID NO.17-18所示的引物替换为SEQ ID NO.39-40所示的引物获得对比引物组8。
实施例1的引物组中SEQ ID NO.19-20所示的引物替换为SEQ ID NO.41-42所示的引物获得对比引物组9。
实施例1的引物组中SEQ ID NO.21-22所示的引物替换为SEQ ID NO.43-44所示的引物获得对比引物组10。
其中,用对比引物组1扩增乙型脑炎脑膜炎病毒标准品质粒样品;
用对比引物组2扩增腮腺炎病毒标准品质粒样品;
用对比引物组3扩增肠道病毒标准品质粒样品;
用对比引物组4扩增单纯疱疹病毒标准品质粒样品;
用对比引物组5扩增麻疹病毒标准品质粒样品;
用对比引物组6扩增呼吸道合胞病毒标准品质粒样品;
用对比引物组7扩增西尼罗病毒标准品质粒样品;
用对比引物组8扩增蜱传脑炎脑膜炎病毒标准品质粒样品;
用对比引物组9扩增流感病毒标准品质粒。
用对比引物组10扩增腺病毒标准品质粒。
分别按照实施例1和2的方法进行特异性和最低检出限试验,结果显示本对比例的引物25-44的特异性、最低检出限和覆盖率均差于实施例1-3的引物(如图2所示)。
图2中第4、7及10泳道除了阳性内质控外没有扩增条带,其余泳道出现目标扩增条带的显示条带颜色较浅,因此最低检出限低于本试剂盒的10拷贝/μL;除此之外,对比例方案的扩增均有不同程度的引物二聚体。
以上结合附图详细描述了本公开的优选实施方式,但是,本公开并不限于上述实施方式中的具体细节,在本公开的技术构思范围内,可以对本公开的技术方案进行多种简单变型,这些简单变型均属于本公开的保护范围。
另外需要说明的是,在上述具体实施方式中所描述的各个具体技术特征,在不矛盾的情况下,可以通过任何合适的方式进行组合,为了避免不必要的重复,本公开对各种可能的组合方式不再另行说明。
此外,本公开的各种不同的实施方式之间也可以进行任意组合,只要其不违背本公开的思想,其同样应当视为本公开所公开的内容。
- 还没有人留言评论。精彩留言会获得点赞!