天山堇菜中具有二聚哌啶类Ⅲ和Ⅳ型骨架的生物碱化合物及制备方法与流程
本发明涉及一种天山堇菜中具有二聚哌啶类ⅲ型和ⅳ型骨架的生物碱化合物及制备方法。
背景技术:
天山堇菜为堇菜科(violaceae)堇菜属(viola)植物天山堇菜(violatianshanica)的干燥全草。《保健药园》中也称比乃非谢吉。分布于我国新疆天山、昆仑山、帕米尔高原,云南、四川、西藏,中亚地区亦有分布,是维吾医药中常用药物。天山堇菜为多年生草本;其形态特征:根茎多粗短,主根圆柱状或倒长圆锥形,黄白或淡棕色;叶基生,叶片卵状或长圆状卵形,先端钝,全缘或具圆齿,具短腺毛;花单生于花梗顶端,花梗稍超出根生叶或等长,花瓣5枚,倒卵形,白色具淡紫色条纹。干燥药材多皱缩;粗短根茎(2-4mm)具环纹及叶柄残基;粗壮主根(0.5-2cm)灰白色至浅黄褐色;花灰蓝色。天山堇菜收录于:《中华本草》、《维吾尔药志》、《中华人民共和国卫生部药品标准·维吾尔药分册》、《维吾尔药材标准》。《中华本草》中记载的功能与主治:生湿生寒,清热解毒,消炎退烧,润肺消肿,润喉止咳,通利二便;主治干热性或胆液质性疾病,如发热发烧,干热性头痛及急性胸膜炎,肺炎,咽干咳嗽,二便不利等。《白色宫殿》中记载用于治疗血液性质头痛、眼病,热性咳嗽,胸膜炎、肺炎,尿少便秘等。《拜地依药书》中记载用于治疗体外热性炎肿,热性胃炎、肝炎,白喉,小儿癫痫,热性头痛,皮肤瘙痒等。
天山堇菜的药理学研究较少,现代药理学研究表明天山堇菜具有抗炎作用,抗氧化活性,抗菌活性。同属的其他植物研究比较多,有抗乙型肝炎活性,免疫抑制活性,抗炎活性,抑制哮喘作用,细胞毒活性,抗饮食性肥胖,抗凝血活性,抗疟原虫活性,杀菌活性,降压降脂活性,肌松弛及镇静催眠活性,胶原酶抑制活性,促胃肠运动及泻下作用,退烧及抗惊厥活性,抗氧化活性,改善慢性失眠作用,酪氨酸酶及胆碱酯酶抑制活性等。
天山堇菜的化学成分研究较少,已报道了4个苯丙素类化合物;同属其他植物的化学成分报道较多,有三萜及其皂苷,倍半萜,香豆素,双香豆素,黄酮,水杨酸衍生物,苯丙素类,醌类,环多肽等。
本发明对天山堇菜的生物碱成分进行的充分的分析分离研究,从中获得了全新的二聚哌啶类的新骨架(ⅲ)及其对应的生物碱化合物1天山堇宁a,化合物2天山堇宁b,以及二聚哌啶类的新骨架(ⅳ)其对应的生物碱化合物3天山堇啶。
技术实现要素:
本发明目的在于,提供一种天山堇菜中具有二聚哌啶类ⅲ和ⅳ型骨架的生物碱化合物及制备方法,该化合物1为天山堇宁a,化合物2为天山堇宁b,化合物3为天山堇啶;该方法采用甲醇溶剂进行提取,通过酸溶碱沉法制得总碱,通过两相溶剂分配法得到上相部位,再利用葡聚糖凝胶色谱法以及正反相色谱法分离得到ⅲ和ⅳ型新骨架生物碱化合物1为天山堇宁a,化合物2为天山堇宁b,化合物3为天山堇啶。
本发明所述的一种天山堇菜中具有二聚哌啶类ⅲ和ⅳ型骨架的化合物,该化合物为天山堇宁a、天山堇宁b和天山堇啶,结构式为:
其中式ⅲ为二聚哌啶类ⅲ型骨架;1为二聚哌啶类骨架ⅲ型所对应的化合物天山堇宁a;2为二聚哌啶类骨架ⅲ型所对应的化合物天山堇宁b;式ⅳ为二聚哌啶类ⅳ型骨架;3为二聚哌啶类骨架ⅳ型所对应的化合物天山堇啶。
所述天山堇菜中具二聚哌啶ⅲ和ⅳ型骨架的化合物的制备方法,按下列步骤进行:
a、将天山堇菜全草粉碎,用无水甲醇溶剂冷浸回流、渗漉、超声或微波提取2-10次,合并提取液并干燥,得到总提取物;
b、将步骤a中的总提取物用氯仿溶解,用水进行萃取,收集氯仿层并干燥得氯仿部位,再将氯仿部位用0.5n的硫酸溶解过滤,收集滤液,滤液用乙酸乙酯萃取以去除非生物碱杂质,去杂质的滤液用饱和碳酸氢钠水溶液调ph至10-14,得到碱化液;
c、将步骤b中的碱化液用二氯甲烷充分萃取并干燥,得到总生物碱;
d、将步骤c中的总生物碱用体积比5:5:5:5-1:5:1:5的正己烷:乙酸乙酯:甲醇:水的两相溶剂系统进行分配,收集上相有机相,干燥得到上相部位,再将上相部位进行正相硅胶柱层析分段分离,以体积比100:0,85:15,70:30,55:45的环己烷:乙酸乙酯为洗脱溶剂进行梯度洗脱,得到4个部位为v100,v85,v70和v55;
e、将步骤d中的v70部位以无水甲醇为溶剂,经葡聚糖凝胶lh-20分离得到v70-1组分,将v70-1组分利用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为34%的乙腈水溶液;流速:4.0ml/min进行分离,分别收集并干燥2.5分钟至6.5分钟的流份(v70-1-1),18.5分钟至19.5分钟的流份(v70-1-6),以及20分钟至21分钟的流份(v70-1-7),再将流份v70-1-1继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为37%的甲醇水溶液;流速:3.1ml/min进行纯化,收集50至53分钟的流份,干燥即得化合物3天山堇啶;将流份v70-1-6继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为59%的甲醇水溶液;流速:2.8ml/min进行纯化,收集21.5至23分钟的流份,干燥即得化合物2天山堇宁b,将流份v70-1-7继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为52.8%的甲醇水溶液;流速:4.0ml/min进行纯化,收集31.5至33.5分钟的流份,干燥即得化合物1天山堇宁a。
本发明所述的天山堇菜中具有二聚哌啶类ⅲ和ⅳ型骨架的生物碱化合物及制备方法,其中具有二聚哌啶类ⅲ型骨架的生物碱化合物1和化合物2的结构鉴定:
化合物1:命名为天山堇宁a;白色无定形粉末,uv(meoh)λmax(logε)305(2.08)nm,200(3.95)nm;hr-esi(+)ms:[m+h]+331.2038;分子式:c19h26n2o3;1h和13c核磁数据见表1;经hmbc相关谱解析确定化合物结构如图1所示。
化合物2:命名为天山堇宁b;白色无定形粉末,uv(meoh)λmax(logε)295(4.28)nm;hr-esi(+)ms:[m+h]+315.2084;分子式:c19h26n2o2;1h和13c核磁数据见表1;经hmbc相关谱解析确定化合物结构如图1所示。
具有二聚哌啶类ⅳ型骨架的生物碱化合物3的结构鉴定:
化合物3:命名为天山堇啶;黄色无定形粉末,uv(meoh)λmax(logε)461(2.20)nm,255(3.56)nm;hr-esi(+)ms:[m+h]+356.2344;分子式:c21h29n3o2;1h和13c核磁数据见表1;经hmbc相关谱解析确定化合物结构如图1所示。
表1.生物碱化合物1,2和3的氢碳核磁数据
附图说明
图1为本发明生物碱化合物1,2和3的hmbc相关解析图;
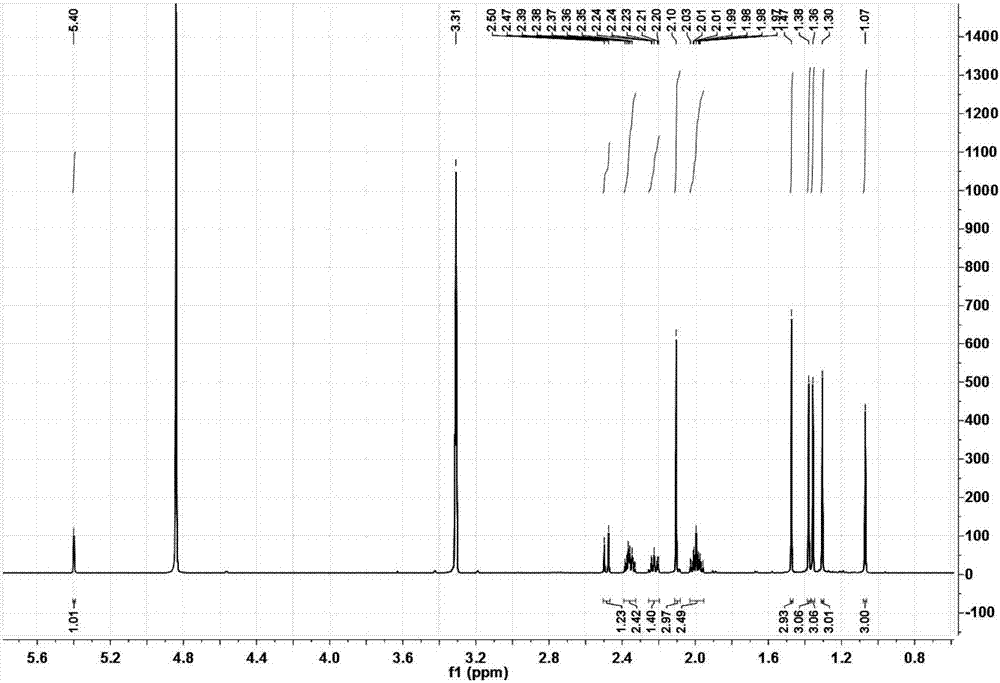
图2为本发明生物碱化合物1的1h-nmr图;
图3为本发明生物碱化合物1的13c-nmr图;
图4为本发明生物碱化合物1的hmbc核磁图;
图5为本发明生物碱化合物1的高分辨质谱图;
图6为本发明生物碱化合物2的1h-nmr图;
图7为本发明生物碱化合物2的13c-nmr图;
图8为本发明生物碱化合物2的hmbc核磁图;
图9为本发明生物碱化合物2的高分辨质谱图;
图10为本发明生物碱化合物3的1h-nmr图;
图11为本发明生物碱化合物3的13c-nmr图。
图12为本发明生物碱化合物3的hmbc核磁图;
图13为本发明生物碱化合物3的高分辨质谱图。
具体实施方式
实施例1
a、将粉碎的天山堇菜全草粉末9.5kg,加入20升无水甲醇溶液室温浸泡24小时,重复提取10次,合并提取液并干燥,得到总提物1.5kg;
b、将步骤a中的总提物用4升氯仿溶解,加入4升水萃取,收集氯仿层并干燥得到氯仿部位,再将氯仿部位用2升0.5n的硫酸溶解,过滤,收集滤液,滤液用乙酸乙酯萃取去除非生物碱杂质,去杂质后的酸水液用饱和碳酸氢钠水溶液调ph10,得到碱化液;
c、将步骤b中的碱化液用二氯甲烷充分萃取并干燥得到总生物碱70克;
d、将步骤c中的总生物碱用体积比3:5:3:5的正己烷:乙酸乙酯:甲醇:水的两相溶剂系统进行分配,收集上相有机相,干燥得到上相部位47克,再将上相部位进行正相硅胶(100-200目)柱层析分段分离,以体积比100:0,85:15,70:30,55:45的环己烷:乙酸乙酯为洗脱溶剂进行梯度洗脱,得到4个部位为v100,v85,v70和v55;
e、将步骤d中的v70部位以无水甲醇为溶剂,经葡聚糖凝胶lh-20分离得到v70-1组分,将v70-1组分利用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为34%的乙腈水溶液;流速:4.0ml/min进行分离,分别收集并干燥2.5分钟至6.5分钟的流份(v70-1-1),18.5分钟至19.5分钟的流份(v70-1-6),以及20分钟至21分钟的流份(v70-1-7),将流份v70-1-1继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为37%的甲醇水溶液;流速:3.1ml/min进行纯化,收集50至53分钟的流份,干燥即得化合物3天山堇啶;将流份v70-1-6继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为59%的甲醇水溶液;流速:2.8ml/min进行纯化,收集21.5至23分钟的流份,干燥既得化合物2天山堇宁b;再将流份v70-1-7继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为52.8%的甲醇水溶液;流速:4.0ml/min进行纯化,收集31.5至33.5分钟的流份,干燥既得化合物1天山堇宁a。
实施例2
a、将粉碎的天山堇菜全草粉末9.5kg,加入20升无水甲醇回流4小时,重复提取6次,合并提取液并干燥,得到总提物2.0kg;
b、将步骤a中的总提物用4升氯仿溶解,加入4升水萃取,收集氯仿层并干燥得到氯仿部位,再将氯仿部位用2升0.5n的硫酸溶解,过滤,收集滤液,滤液用乙酸乙酯萃取去除非生物碱杂质,去杂质后的酸水液用饱和碳酸氢钠水溶液调ph至11,得到碱化液;
c、将步骤b中的碱化液用二氯甲烷充分萃取并干燥得到总生物碱77克;
d、将步骤c中的总生物碱用体积比5:5:5:5的正己烷:乙酸乙酯:甲醇:水的两相溶剂系统进行分配,收集上相有机相,干燥得到上相部位32克,再将上相部位进行正相硅胶(100-200目)柱层析分段分离,以体积比100:0,85:15,70:30,55:45的环己烷:乙酸乙酯为洗脱溶剂进行梯度洗脱,得到4个部位为v100,v85,v70和v55;
e、将步骤d中的v70部位以无水甲醇为溶剂,经葡聚糖凝胶lh-20分离得到v70-1组分,将v70-1组分利用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为34%的乙腈水溶液;流速:4.0ml/min进行分离,分别收集并干燥2.5分钟至6.5分钟的流份(v70-1-1),18.5分钟至19.5分钟的流份(v70-1-6),以及20分钟至21分钟的流份(v70-1-7),将流份v70-1-1继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为37%的甲醇水溶液;流速:3.1ml/min进行纯化,收集50至53分钟的流份,干燥即得化合物3天山堇啶;将流份v70-1-6继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为59%的甲醇水溶液;流速:2.8ml/min进行纯化,收集21.5至23分钟的流份,干燥既得化合物2天山堇宁b;再将流份v70-1-7继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为52.8%的甲醇水溶液;流速:4.0ml/min进行纯化,收集31.5至33.5分钟的流份,干燥既得化合物1天山堇宁a。
实施例3
a、将粉碎的天山堇菜全草粉末9.5kg,加入20升无水甲醇溶液渗漉24小时,重复提取8次,合并提取液并干燥,得到总提物1.7kg;
b、将步骤a中的总提取物用4升氯仿溶解,加入4升水进行萃取,收集氯仿层并干燥得氯仿部位,再将氯仿部位用0.5n的硫酸溶解,过滤,收集滤液,滤液用乙酸乙酯萃取以去除非生物碱杂质,去杂质的滤液用饱和碳酸氢钠水溶液调ph至12,得到碱化液;
c、将步骤b中的碱化液用二氯甲烷充分萃取并干燥,得到总生物碱72克;
d、将步骤c中的总生物碱用体积比1:5:1:5的正己烷:乙酸乙酯:甲醇:水的两相溶剂系统进行分配,收集上相有机相,干燥得到上相部位55克,再将上相部位进行正相硅胶(100-200目)柱层析分段分离,以体积比100:0,85:15,70:30,55:45的环己烷:乙酸乙酯为洗脱溶剂进行梯度洗脱,得到4个部位为v100,v85,v70和v55;
e、将步骤d中的v70部位以无水甲醇为溶剂,经葡聚糖凝胶lh-20分离得到v70-1组分,将v70-1组分利用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为34%的乙腈水溶液;流速:4.0ml/min进行分离,分别收集并干燥2.5分钟至6.5分钟的流份(v70-1-1),18.5分钟至19.5分钟的流份(v70-1-6),以及20分钟至21分钟的流份(v70-1-7),将流份v70-1-1继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为37%的甲醇水溶液;流速:3.1ml/min进行纯化,收集50至53分钟的流份,干燥即得化合物3天山堇啶;将流份v70-1-6继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为59%的甲醇水溶液;流速:2.8ml/min进行纯化,收集21.5至23分钟的流份,干燥既得化合物2天山堇宁b;再将流份v70-1-7继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为52.8%的甲醇水溶液;流速:4.0ml/min进行纯化,收集31.5至33.5分钟的流份,干燥既得化合物1天山堇宁a。
实施例4
a、将粉碎的天山堇菜全草粉末9.5kg,加入20升无水甲醇超声3小时,重复提取4次,合并提取液并干燥,得到总提物1.55kg;
b、将步骤a中的总提取物用4升氯仿溶解,加入4升水进行萃取,收集氯仿层并干燥得氯仿部位,再将氯仿部位用0.5n的硫酸溶解过滤,收集滤液,滤液用乙酸乙酯萃取以去除非生物碱杂质,去杂质的滤液用饱和碳酸氢钠水溶液调ph至13,得到碱化液;
c、将步骤b中的碱化液用二氯甲烷充分萃取并干燥,得到总生物碱64克;
d、将步骤c中的总生物碱用体积比2:5:2:5的正己烷:乙酸乙酯:甲醇:水的两相溶剂系统进行分配,收集上相有机相,干燥得到上相部位49克,再将上相部位进行正相硅胶(100-200目)柱层析分段分离,以体积比100:0,85:15,70:30,55:45的环己烷:乙酸乙酯为洗脱溶剂进行梯度洗脱,得到4个部位为v100,v85,v70和v55;
e、将步骤d中的v70部位以无水甲醇为溶剂,经葡聚糖凝胶lh-20分离得到v70-1组分,将v70-1组分利用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为34%的乙腈水溶液;流速:4.0ml/min进行分离,分别收集并干燥2.5分钟至6.5分钟的流份(v70-1-1),18.5分钟至19.5分钟的流份(v70-1-6),以及20分钟至21分钟的流份(v70-1-7),将流份v70-1-1继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为37%的甲醇水溶液;流速:3.1ml/min进行纯化,收集50至53分钟的流份,干燥即得化合物3天山堇啶;将流份v70-1-6继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为59%的甲醇水溶液;流速:2.8ml/min进行纯化,收集21.5至23分钟的流份,干燥既得化合物2天山堇宁b;再将流份v70-1-7继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为52.8%的甲醇水溶液;流速:4.0ml/min进行纯化,收集31.5至33.5分钟的流份,干燥既得化合物1天山堇宁a。
实施例5
a、将粉碎的天山堇菜全草粉末9.5kg,加入20升无水甲醇微波1小时,重复提取2次,合并提取液并干燥,得到总提物1.1kg;
b、将步骤a中的总提取物用4升氯仿溶解,加入4升水进行萃取,收集氯仿层并干燥得氯仿部位,再将氯仿部位用0.5n的硫酸溶解过滤,收集滤液,滤液用乙酸乙酯萃取以去除非生物碱杂质,去杂质的滤液用饱和碳酸氢钠水溶液调ph至14,得到碱化液;
c、将步骤b中的碱化液用二氯甲烷充分萃取并干燥,得到总生物碱48克;
d、将步骤c中的总生物碱用体积比4:5:4:5的正己烷:乙酸乙酯:甲醇:水的两相溶剂系统进行分配,收集上相有机相,干燥得到上相部位25克,再将上相部位进行正相硅胶(100-200目)柱层析分段分离,以体积比100:0,85:15,70:30,55:45的环己烷:乙酸乙酯为洗脱溶剂进行梯度洗脱,得到4个部位为v100,v85,v70和v55;
e、将步骤d中的v70部位以无水甲醇为溶剂,经葡聚糖凝胶lh-20分离得到v70-1组分,将v70-1组分利用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为34%的乙腈水溶液;流速:4.0ml/min进行分离,分别收集并干燥2.5分钟至6.5分钟的流份(v70-1-1),18.5分钟至19.5分钟的流份(v70-1-6),以及20分钟至21分钟的流份(v70-1-7),将流份v70-1-1继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为37%的甲醇水溶液;流速:3.1ml/min进行纯化,收集50至53分钟的流份,干燥即得化合物3天山堇啶;将流份v70-1-6继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为59%的甲醇水溶液;流速:2.8ml/min进行纯化,收集21.5至23分钟的流份,干燥既得化合物2天山堇宁b;再将流份v70-1-7继续用反相色谱柱:ymcpydrospherec185μm10×250mm;溶剂:浓度为52.8%的甲醇水溶液;流速:4.0ml/min进行纯化,收集31.5至33.5分钟的流份,干燥既得化合物1天山堇宁a。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种光稳定剂中间体2,2,6,6-四甲基-4-哌啶酯类化合物及其制备方法
- 一种2-芳基氟代哌啶衍生物及其制备方法
- N-(4-氟苄基)-n-(1-甲基哌啶-4-基)-n’-(4-(2-甲基丙氧基)苯基甲基)脲酒石酸盐晶型 ...的制作方法
- 3,5-双(芳基亚甲基)-1-取代-4-哌啶酮系列化合物及其在制备抗食管癌药物的应用
- 哌啶脲衍生物的制作方法
- 一种(s)-(+)-1-(2-哌啶苯基)-3-甲基正丁胺的制备方法
- 一种哌啶化合物及其制备方法
- 用作gpr120激动剂的取代的螺哌啶基化合物的制作方法
- 一类膦功能化聚醚哌啶盐离子液体及其在烯烃氢甲酰化反应中的应用
- 一种合成1-(N-Boc-4-哌啶)-4-吡唑硼酸频哪醇酯的方法
- 一种光稳定剂中间体2,2,6,6-四甲基-4-哌啶酯类化合物及其制备方法
- 一种2-芳基氟代哌啶衍生物及其制备方法
- N-(4-氟苄基)-n-(1-甲基哌啶-4-基)-n’-(4-(2-甲基丙氧基)苯基甲基)脲酒石酸盐晶型 ...的制作方法
- 3,5-双(芳基亚甲基)-1-取代-4-哌啶酮系列化合物及其在制备抗食管癌药物的应用
- 哌啶脲衍生物的制作方法
- 一种(s)-(+)-1-(2-哌啶苯基)-3-甲基正丁胺的制备方法
- 一种哌啶化合物及其制备方法
- 用作gpr120激动剂的取代的螺哌啶基化合物的制作方法
- 一类膦功能化聚醚哌啶盐离子液体及其在烯烃氢甲酰化反应中的应用
- 一种合成1-(N-Boc-4-哌啶)-4-吡唑硼酸频哪醇酯的方法