一种棕榈酰化修饰的半胱氨酸多肽的制备方法与流程
本发明涉及多肽领域,尤其涉及棕榈酰化修饰的半胱氨酸多肽的合成方法。
背景技术:
蛋白质在具有生物活性功能之前要经过磷酸化、糖基化、泛素化和脂质化等一系列复杂的修饰过程。蛋白质棕榈酰化修饰的类型及机制,依据其连接方式,分为两种类型:(1)s型。s端通过不稳定的硫酯键连接到cys,可逆,较多见。(2)n型。n端通过稳定的酰胺键连接到cys或gly,不可逆。由于绝大多数棕榈酰化蛋白质都以s型修饰为主,所以棕榈酰化修饰通常指s-棕榈酰化。
蛋白质棕榈酰化修饰是半胱氨酸侧链修饰的结果。蛋白质棕榈酰化修饰通常指16个碳的脂肪酸棕榈酸盐通过不稳定的硫酯键共价结合到蛋白质特定的半胱氨酸残基(cysteineresidues,cys)侧链上;在一定条件下,硫酯键发生水解,棕榈酸盐脱离cys,蛋白质实现去棕榈酰化,因此s-棕榈酰化修饰是一个可逆的过程。s-棕榈酰化修饰是一种最普遍且唯一可逆的翻译后脂质修饰形式,能增加蛋白质的疏水性,对蛋白质的转运、细胞器定位和功能具有重要的作用,赋予蛋白质多样化的生理功能。
100多种蛋白质(包括受体、配体、信号转导子)棕榈酰化修饰后调节蛋白质的活性、稳定性、膜融合及胞内转运、介导蛋白质定位亚细胞器、参与调节多种细胞信号通路、介导蛋白质-蛋白质、蛋白质-脂质互相作用。棕榈酰化蛋白质参与组成各种细胞膜脂质构成域,促进自身或其他蛋白质定位膜脂筏(富含胆固醇,鞘磷脂和gpi微结构域)中;许多棕榈酰化蛋白质与疾病和肿瘤密切相关,参与肿瘤发生发展dhhc蛋白在细胞信号通路中发挥重要作用,因此通过类似物或抑制剂进行干扰,可应用于疾病和肿瘤的治疗。
鉴于半胱氨酸棕榈酰化在蛋白靶向药物开发方向的广阔应用前景,本发明的目的在于解决常规固相合成方法中因巯基活性较低难以实现硫脂连接,以及液相进行棕榈酰化修饰过程中,难以定点修饰,副反应多,且后处理过程中因为硫酯键可发生水解,易于发生连接之后又断裂的情况。
有鉴于上述的缺陷,本设计人,积极加以研究创新,以期创设一种棕榈酰化修饰的半胱氨酸的制备方法,使其更具有产业上的利用价值。
技术实现要素:
为解决上述技术问题,本发明的目的是提供一种棕榈酰化修饰的半胱氨酸多肽的制备方法,该方法操作简单、可对多个位点半胱氨酸棕榈酰化进行定点修饰。
本发明的棕榈酰化修饰的半胱氨酸多肽的制备方法,包括以下步骤:
(1)多肽fmoc-cys-otbu与棕榈酸在第一溶剂中发生酰化反应,得到的中间体fmoc-cys(pal)-otbu,所述中间体去除保护基otbu后,得到氨基酸序列如下的多肽片段:
fmoc-cys(pal)-oh。
其中,去除保护基otbu的试剂为二氯甲烷(dcm)和三氟乙酸(tfa),体积比为1:1。
(2)将wangresin与活化后的氨基酸fmoc-thr(tbu)-oh在第二溶剂中发生反应,得到氨基酸序列如下的多肽片段:
fmoc-thr(tbu)-resin。
(3)脱除步骤(2)中得到的连接有氨基酸的树脂fmoc保护基,得到氨基酸序列如下的多肽片段:
h-thr(tbu)-resin。
(4)将步骤(3)中得到的h-thr(tbu)-resin与合成氨基酸fmoc-cys(pal)-oh在第二溶剂中发生耦合反应,得到氨基酸序列如下的多肽片段:
fmoc-cys(pal)-thr(tbu)-resin。
(5)重复步骤(3)和(4),依次反应下列氨基酸:fmoc-thr(tbu)-oh,fmoc-lys(boc)-oh,fmoc-trp(boc)-oh,fmoc-tyr(tbu)-oh,fmoc-cys(trt)-oh,fmoc-phe-oh,fmoc-lys(boc)-oh,得到氨基酸序列如下的多肽片段:
h-lys(boc)-phe-cys(trt)-tyr(tbu)-trp(boc)-lys(boc)-thr(tbu)-cys(s-pal)-thr(tbu)-resin。
(6)裂解步骤(5)中得到的多肽片段,经纯化,得到氨基酸序列如下的棕榈酰化修饰的半胱氨酸多肽:
h-lys-phe-cys-tyr-trp-lys-thr-cys(s-pal)-thr-oh。
进一步的,步骤(1)中,fmoc-cys-otbu与棕榈酸的摩尔比为1:0.8-1.2,优选1:1。
进一步的,步骤(1)中,所述酰化反应中还加入催化剂,所述催化剂为4-二甲氨基吡啶(dmap)。
催化剂用量相当于约0.2倍fmoc-cys-otbu的摩尔量。
步骤(1)中,所述酰化反应时间为8-12h(搅拌反应过夜)。
步骤(1)中,中间体在50%dcm/tfa中反应3-4h,优选2h。
进一步的,步骤(1)中,所述第一溶剂为二氯甲烷(dcm)、dmf和thf的一种或几种。优选dcm。
进一步的,所述第二溶剂为dmf、dcm和dmso中的一种或几种。优选dmf。
进一步的,步骤(2)中,所述反应中加入用于缩合的的缩合试
剂n,n-二异丙基碳二亚胺(dic)。
其中,dic的用量相当于约3倍wangresin的摩尔量。
进一步的,步骤(2)中,所述反应中还加入有催化剂4-二甲氨基吡啶(dmap)。
其中,dmap的用量相当于约0.1倍wangresin的摩尔量。
进一步的,步骤(3)中,用于脱除fmoc保护基的试剂为哌啶、dmf、1,8-二氮杂二环十一碳-7-烯(dbu)和吗啉中的一种或几种。优选哌啶与dmf的混合液。
其中,哌啶与dmf的体积比为2:8。
进一步的,步骤(4)中,所述合成氨基酸fmoc-cys(pal)-oh的用量相当于约3倍wangresin的摩尔量。
进一步的,步骤(4)中,所述耦合反应中加入缩合剂2-(7-偶氮苯并三氮唑)-四甲基脲六氟磷酸(hbtu)。
其中,hbtu的用量相当于约3倍wangresin的摩尔量。
进一步的,步骤(4)中,所述反应中还加入用于活化氨基酸的活化剂。
进一步的,所述活化剂为n,n-二异丙基乙胺(diea)、n-甲基吗啡啉(nmm)的一种或两种。
其中,diea的用量相当于约10倍wangresin的摩尔量。
进一步的,步骤(6)中,裂解步骤(5)中得到的多肽片段的裂解液为三氟乙酸(tfa)、水、1,2-乙二硫醇(edt)、三异丙基硅烷(tis)、苯甲醚、间甲酚和苯甲硫醚中的一种或几种。
进一步的,所述裂解液包括体积百分数为92-98%的tfa、1-3%的水、1-3%的edt和0.8-1.2%的tis。
所述裂解液优选包括体积百分数为95%的tfa、2%的水、2%的edt和1%的tis。
其中,裂解液用量为10ml/g。
借由上述方案,本发明至少具有以下优点:
1、本发明提供了一种半胱氨酸棕榈酰化修饰多肽的合成工艺方法,操作简单,易于实验室进行,且适用性强;
2、本发明采用先合成棕榈酰化半胱氨酸做为多肽合成的氨基酸原料,即fmoc-cys(pal)-oh,从而解决巯基与棕榈酸发生硫脂反应困难的问题,并且可对多个位点半胱氨酸棕榈酰化进行定点修饰;
3、本发明避免了半胱氨酸棕榈酸化液相修饰过程中的后处理过程,步骤简单,节约时间成本,并且避免了s-棕榈酰不稳定因素。
上述说明仅是本发明技术方案的概述,为了能够更清楚了解本发明的技术手段,并可依照说明书的内容予以实施,以下以本发明的较佳实施例并配合附图详细说明如后。
附图说明
图1是本发明的实施例1中产品高效液相色谱仪检测分析图;
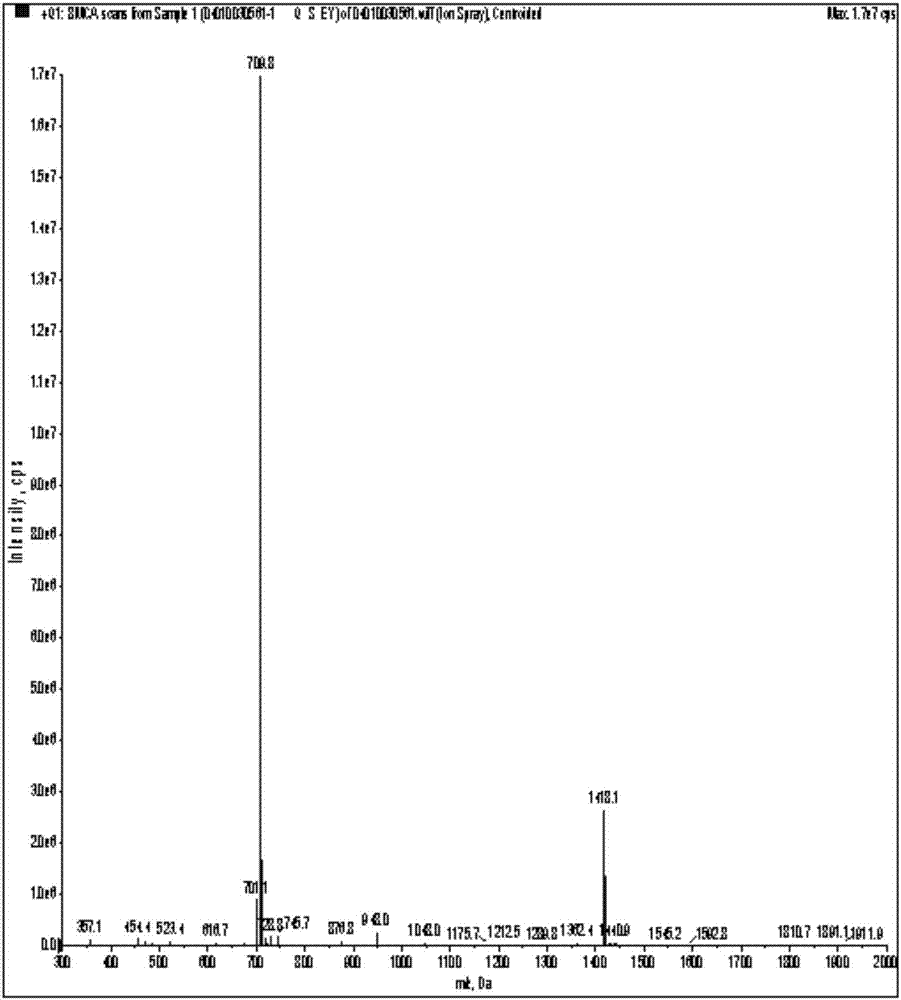
图2是本发明的实施例1中产品电喷雾质谱仪检测分析图。
具体实施方式
下面结合附图和实施例,对本发明的具体实施方式作进一步详细描述。以下实施例用于说明本发明,但不用来限制本发明的范围。
实施例1:
h-lys-phe-cys-tyr-trp-lys-thr-cys(s-pal)-thr-oh的合成,从多肽的c端向n端合成:
一、向250ml三口瓶中依次加入fmoc-cys-otbu(3.39g,1mmol,1.0eq),棕榈酸(2.56g,1mmol,1.0eq),dmap(0.25g,0.2mmol,0.2eq),dcm(150ml)。搅拌,体系澄清。滴加dcc/dcm,搅拌反应过夜。反应体系抽滤,滤液浓缩之干。滤液用dcm溶解,滤液用1nhcl、饱和氯化钠分别洗两次,分液,浓缩至干。固体的500ml单口瓶中加入50%dcm/tfa,反应2h,浓缩至干经硅胶柱纯化得fmoc-cys(pal)-oh,纯度97.23%,收率73%。
二、称量0.6mmol/gwangresin1g(合成规模为0.6mmol)放入反应管中,加dmf(15ml/g),氮气鼓吹30min,使之充分溶胀。
三、连接多肽的第一个氨基酸:通过沙芯抽滤掉溶剂,加入0.35gfmoc-thr(tbu)-oh用适量dmf溶解完全,加入1.8mmoldic,再加入0.06mmoldmap,通氮气反应120min,吡啶:乙酸酐=1:1封头30min。得到fmoc-thr(tbu)-resin
四、脱除fmoc保护基:去掉反应液,加20%哌啶/dmf溶液(15ml/g),5min,抽掉反应液,再加20%哌啶/dmf溶液(15ml/g),10min。抽掉哌啶溶液,dmf洗涤树脂6次,去除脱除保护基试剂的残留。取十几粒树脂,用乙醇洗三次,加入茚三酮,kcn,苯酚溶液各一滴,105℃-110℃加热5min,变深蓝色说明保护基fmoc已脱除,得到h-thr(tbu)-resin。
五、氨基酸耦合反应:加入1.8mmol的合成氨基酸fmoc-cys(pal)-oh用适量dmf溶解完全,再加入1.8mmolhbtu和6mmol的diea,通氮气反应40min,通过沙芯抽滤掉反应溶剂,dmf洗涤树脂5次,去除过量的保护氨基酸。取十几粒树脂,用乙醇洗三次,加入茚三酮,kcn,苯酚溶液各一滴,105℃-110℃加热5min,无色说明反应完全,得到fmoc-cys(pal)-thr(tbu)-resin。
六、按照肽链中的氨基酸顺序,重复步骤四、五,反应下列氨基酸:fmoc-thr(tbu)-oh,fmoc-lys(boc)-oh,fmoc-trp(boc)-oh,fmoc-tyr(tbu)-oh,fmoc-cys(trt)-oh,fmoc-phe-oh,fmoc-lys(boc)-oh,得到h-lys(boc)-phe-cys(trt)-tyr(tbu)-trp(boc)-lys(boc)-thr(tbu)-cys(s-pal)-thr(tbu)-resin。
七、配制裂解液(10ml/g):tfa95%;水2%;edt2%;tis1%,裂解树脂120min,抽滤去除树脂得滤液,冰乙醚析出白色固体,使用离心机离心,白色固体用冰乙醚洗涤6次,烘干得到白色粉末粗肽712mg,即得粗肽h-lys-phe-cys-tyr-trp-lys-thr-cys(s-pal)-thr-oh。
八、将粗肽用水/乙腈溶解,用反向c18色谱柱的高效液相色谱仪进行分离纯化,流动相:a液0.1%tfa的水溶液,b液0.1%的乙腈溶液,检测波长为220nm,将含目标产物溶液冻干,得到纯品308mg,收率46.1%。
纯品用30%乙腈/70%水溶解,浓度1mg/ml,用反向c18色谱柱的高效液相色谱仪检测,如图1所示,表明:根据峰面积归一法,得到纯度较高目标产物,纯度为95.55%;用电喷雾质谱仪检测ms,如图2所示,表明:esi正离子图谱表明产品质谱正确(目标产物理论分子量1417.84)。
以上所述仅是本发明的优选实施方式,并不用于限制本发明,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明技术原理的前提下,还可以做出若干改进和变型,这些改进和变型也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!