一种检测肺炎克雷伯氏菌的实时定量LAMP引物组及试剂盒的制作方法
本发明涉及微生物检测
技术领域:
,具体说是涉及一种快速并且可实时定量检测肺炎克雷伯氏菌的lamp引物组及试剂盒。
背景技术:
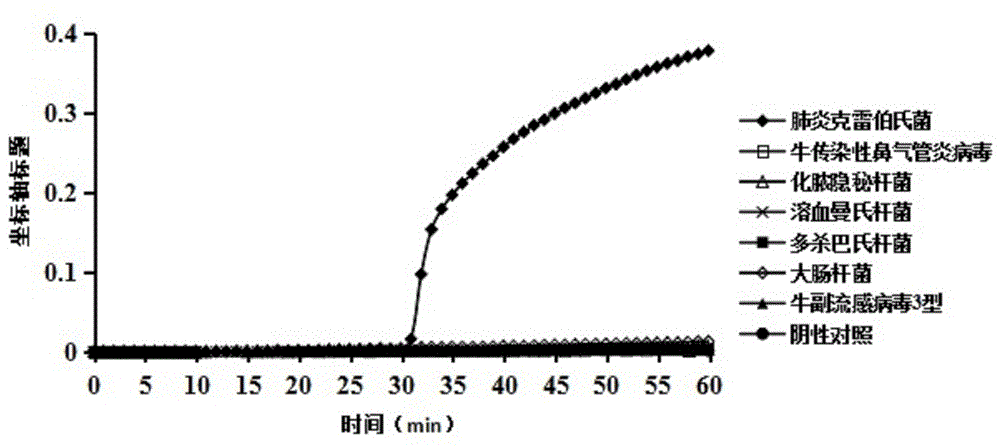
:肺炎克雷伯氏菌(klebsiellapneumonia,kpn)为肠杆菌科克雷伯氏菌属的革兰氏阴性菌。可侵害人和动物的肠道、呼吸道等器官,从而可引起肺炎、肝脓肿、伤口感染和败血症等症状,是一种人兽共患病的病原。同时,牛感染肺炎克雷伯氏菌后,对多杀性巴氏杆菌、溶血性曼氏杆菌以及牛支原体等病原的易感性增加。目前,该病原体在全球范围内均有分布,在中国的分布流行同样十分广泛,造成巨大的经济损失,成为威胁牛养殖业的重要病原之一。专利公布号为cn104328174a公开一种检测鼠肺炎克雷伯氏菌的lamp引物、试剂盒及方法,是通过肺炎克雷伯氏菌tyrb基因序列设计lamp引物,建立适用于临床样品检测、特异性强、灵敏度高的鼠肺炎克雷伯氏菌可视化检测方法;可通过观测绿色荧光的有无快速准确的检测出肺炎克雷伯氏菌的存在,最低检测限为5.6拷贝数/反应。但该方法存在速率不够高,并且不能实时定量检测的问题。综上所述,急需建立一种可以快速、准确检测和鉴定肺炎克雷伯氏菌的方法具有重要的应用价值。技术实现要素:本发明的目的是提供一种快捷准确检测鉴别肺炎克雷伯氏菌的方法,公开一种快速、实时定量检测肺炎克雷伯氏菌的lamp引物组及应用。为实现本发明目的所使用的技术方案为:一种检测肺炎克雷伯氏菌的实时定量lamp引物组,所述的lamp引物组为seqidno:1~5所示的核苷酸序列;所述seqidno:1、seqidno:2为内引物fip和bip;所述seqidno:3、seqidno:4为外引物f3和b3;所述seqidno:5为环引物lf。优选地,所述的lamp引物组具有与seqidno:1~5所示的核苷酸序列中同源性为60%以上的序列。优选地,所述的lamp引物组具有与seqidno:1~5所示的核苷酸序列中进行杂交的序列。优选地,所述的lamp引物组具有与seqidno:1~5所示的核苷酸序列进行转录的序列。优选地,所述的lamp引物组具有与seqidno:1~5所示的核苷酸序列进行优化截短的序列。本发明还提供一种如以上所述的检测肺炎克雷伯氏菌的实时定量lamp试剂盒,包括lamp引物组、2×反应缓冲液、bstdna聚合酶、rnase-freewater和肺炎克雷伯氏菌dna模板。优选地,所述2×反应缓冲液由buffer、dntps、mg2+组成。优选地,所述lamp试剂盒的反应体系为25μl:其中包括12.5μl的2×反应缓冲液,1μl的bstdna聚合酶,5pmol的seqidno:1,5pmol的seqidno:2,40pmol的seqidno:3,40pmol的seqidno:4,25pmol的seqidno:5,2μl的肺炎克雷伯氏菌dna模板,再加入超纯水补足25μl。优选地,所述lamp试剂盒的应程序为:63℃恒温保持60min,扩增结束后85℃灭活5min。本发明的显著进步是:1)特异性强所检测的阴性对照细菌和水对照均无阳性结果出来。2)灵敏度高利用本发明的肺炎克雷伯氏菌lamp扩增引物组建立的lamp检测方法具有高度敏感性,检测限约为1.15×10-2ng/μl。3)迅速得出结果肺炎克雷伯氏菌在血平板上需要20小时以上才长出明显菌落,生化试验通常耗时24-72小时,做出正确的鉴定需要2-4天时间。本发明提供的lamp检测方法在60分钟内即可完成扩增,且扩增结束即可判断结果,不需要再进行琼脂糖凝胶电泳紫外线分析,从样品的基因组dna提取到获得最终结果可在2-3小时内完成。4)准确性高目前建立的大多数lamp方法,在反应结束后打开反应管加入荧光染料进行显色反应,观察是否有显色来判读试验结果,或者通过跑电泳的方法进行结果判定,无法区分特异性扩增与非特异性扩增,因此增加了假阳性诊断结果的几率;而且对于弱阳性反应,通过人为肉眼判读的方式很可能误判为阴性。本方法通过浊度仪实时监控反应管的扩增情况,能够避免上述的缺陷,具有更高的准确性。此外,利用本发明的肺炎克雷伯氏菌lamp扩增引物组建立的lamp检测方法具有高度敏感性,高灵敏度保证了在样品dna含量极低的情况下,使用本发明肺炎克雷伯氏菌的lamp扩增引物也可以扩增出目的dna片段,检测结果更准确。5)不造成污染常规的lamp方法在反应结束后通过凝胶电泳的方法来判读结果,或者开盖加入荧光染料进行判断,凝胶电泳使用的染料对环境也造成污染,且打开反应管容易造成实验室气溶胶污染。本方法通过浊度仪实时监控反应管的扩增情况,反应结束即可获得结果,不需要打开反应管的盖子,能有效避免气溶胶污染。6)可实时定量本发明利用tubidimeterreal-timela-320浊度仪来实时分析lamp反应的结果,不同标准样品浓度的负对数及其对应的浊度值达到0.1所需的时间成线性关系,由此绘制标准曲线,获得标准曲线方程,即可进行定量检测。附图说明图1是本发明lamp扩增引物组的特异性检测结果:只有肺炎克雷伯氏菌的反应管出现浊度的上升曲线,为阳性结果,6个对照菌反应管和水对照反应均无扩增,为阴性结果。图2是本发明lamp扩增引物组的敏感性检测结果,其中a1:1.15×101ng/μl;a2:1.15×100ng/μl;a3:1.15×10-1ng/μl;a4:1.15×10-2ng/μl;a5:1.15×10-3ng/μl;a6:1.15×10-4ng/μl。肺炎克雷伯氏菌dna的起始浓度为1.15×101ng/μl,经10倍倍比稀释后进行lamp,结果显示lamp法检测限约为1.15×10-2ng/μl。图3是本发明定量检测肺炎克雷伯氏菌lamp方法的标准曲线:不同标准样品浓度的负对数及其对应的浊度值达到0.1所需的时间成线性关系,由此绘制标准曲线,获得标准曲线方程,即可进行定量检测。具体实施方式下面结合具体实施例,对本发明作进一步详细的阐述,但本发明的实施方式并不局限于实施例表示的范围。这些实施例仅用于说明本发明,而非用于限制本发明的范围。此外,在阅读本发明的内容后,本领域的技术人员可以对本发明作各种修改,这些等价变化同样落于本发明所附权利要求书所限定的范围。下述实施例中所使用的实验方法如无特殊说明,均为常规方法。下述实施例中所使用的材料、试剂等,如无特殊说明,均可从商业途径得到1、材料的准备肺炎克雷伯氏菌、牛传染性鼻气管炎病毒、化脓隐秘杆菌、溶血曼氏杆菌、多杀巴氏杆菌、大肠杆菌、牛副流感病毒3型,为广西壮族自治区兽医所分离鉴定和保存。bstdna聚合酶购自北京蓝谱生物科技有限公司,细菌基因组dna提取试剂盒购自康为世纪生物科技有限公司。2、lamp引物组的设计与合成根据genbank中的肺炎克雷伯氏菌毒力因子尿素酶urease(urea)的基因序列,进行基因序列比对,选取保守区域,设计特异性lamp引物,其中f3、b3为外引物,fip、bip为内引物,lf为环引物,其中f3gcggcctgaagctcaact(seqidno:1)b3gtccgggaaggtggct(seqidno:2)fipcgcttttgccgtcccgagcggagtccgtggccctgat(seqidno:3)bipctgatggaggaaggccgacatggacctggatatccgggatca(seqidno:4)lfctgacccgcaagcaggtgatg(seqidno:5)。引物组由上海英骏生物有限公司合成。3、病原菌基因组dna提取取适量病原菌培养物至于灭菌离心管中,若为液体培养物,则离心后去上清,取沉淀,再使用细菌基因组dna提取试剂盒提取病原菌基因组dna。4、lamp反应体系建立按25μl体系配置:2×反应缓冲液12.5μlbstdna聚合酶1μlf35pmolb35pmolfip40pmolbip40pmollf25pmol肺炎克雷伯氏菌dna2μl超纯水补足25μl。5、lamp反应程序lamp反应在实时浊度仪(la-320c,日本荣研公司)密闭进行,浊度仪实时监控扩增情况,反应程序为63℃保持60min,反应结束后85℃灭活5min。6、结果判定实时浊度仪实时监测反应扩增情况,仪器通过读取反应管的浊度值绘制浊度曲线,出现浊度上升曲线的为阳性结果,没有出现浊度上升曲线的为阴性结果。反应结束,即可获得结果,避免通过人为肉眼观察的主观判断失误。7、lamp扩增引物组在lamp扩增试剂中的使用7.1标准品制备抽提肺炎克雷伯氏菌纯培养物的基因组dna作为标准样品,测定其浓度,-70℃保存备用。7.2特异性检测分别提取肺炎克雷伯氏菌、牛传染性鼻气管炎病毒、化脓隐秘杆菌、溶血曼氏杆菌、多杀巴氏杆菌、大肠杆菌、牛副流感病毒3型的基因组dna作为lamp反应的模板,检验lamp方法的特异性。7.3敏感性检测取标准样品肺炎克雷伯氏菌基因组dna,测定其起始浓度,用rna-freewater进行连续10倍倍比稀释7个稀释度,取各稀释度2μl作为模板进行lamp扩增,进行敏感性检测。7.4定量检测设置对照:浓度为1:1.15×101ng/μl;2:1.15×100ng/μl;3:1.15×10-1ng/μl;4:1.15×10-2ng/μl;的肺炎克雷伯氏菌基因组dna标准样品各一个,因为标准样品浓度的负对数值与其扩增浊度值为0.1的时间值成线性关系,所以可以将浊度仪捕捉到的值与时间(如表1)做成标准曲线,获得标准曲线方程,即可对未知样品的基因拷贝数进行定量检测。结果:1、lamp扩增引物组的特异性试验结果对1株肺炎克雷伯氏菌、6株阴性对照菌和水对照进行lamp扩增,结果如图1所示,肺炎克雷伯氏菌反应管在30min左右出现浊度的上升曲线,为阳性结果,7株阴性对照菌反应管和水对照反应管曲线均无扩增情况出现,为阴性结果。2、lamp扩增引物组的敏感性试验结果肺炎克雷伯氏菌基因组dna标准样品起始浓度为1.15×101ng/μl,经10倍倍比稀释后进行lamp扩增,结果如图2所示,lamp法检测限约为1.15×10-3ng/μl,是普通pcr方法的10倍。3、绘制定量检测肺炎克雷伯氏菌的标准曲线设置对照:浓度为1.15×101ng/μl、1.15×100ng/μl、1.15×10-1ng/μl、1.15×10-2ng/μl的肺炎克雷伯氏菌基因组dna标准样品各一个,因为标准样品浓度的负对数值与其扩增浊度值为0.1的时间值成线性关系,所以可以将浊度仪捕捉到的值与时间(如表1)做成标准曲线,获得标准曲线方程,y=0.3014x-11.148,如图3所示,相关系数r2=0.9945,呈良好的线性关系。以时间为x值,可求出y值即浓度的负次方数,则浓度为10-y,再乘以基数1.15,即为1.15×10-yng/μl。如某试验样品达到浊度值为0.1的时间为30分钟时,带入所建立的标准曲线方程,从而达到定量的效果。表1标准样品浓度负对数与对应反应管浊度值为0.1的时间时间(min)33.936.939.943.9标准值(-log)-1012以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内所作的任何修改、等同替换、改进等,均应包含在本发明的包含范围之内。序列表<110>广西壮族自治区兽医研究所<120>一种检测肺炎克雷伯氏菌的实时定量lamp引物组及试剂盒<141>2019-02-02<160>5<170>siposequencelisting1.0<210>1<211>18<212>dna<213>人工序列(artificialsequencelatin)<400>1gcggcctgaagctcaact18<210>2<211>16<212>dna<213>人工序列(artificialsequencelatin)<400>2gtccgggaaggtggct16<210>3<211>37<212>dna<213>人工序列(artificialsequencelatin)<400>3cgcttttgccgtcccgagcggagtccgtggccctgat37<210>4<211>42<212>dna<213>人工序列(artificialsequencelatin)<400>4ctgatggaggaaggccgacatggacctggatatccgggatca42<210>5<211>21<212>dna<213>人工序列(artificialsequencelatin)<400>5ctgacccgcaagcaggtgatg21当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1