一种手性醛催化剂及制备方法以及催化不对称亲核加成反应的方法与流程
本发明涉及氨基酸类化合物合成技术领域,具体涉及一种手性醛催化剂及制备方法以及催化不对称亲核加成反应的方法。
背景技术:
氨基酸衍生物在化学,生物等领域具有极其广泛的用途,天然及非天然手性氨基酸化合物的合成一直都是不对称有机合成领域的重要研究课题。手性醛催化氨基酸酯及其类似物的不对称α-官能化反应,直接使用氨基未被保护的简单伯胺氨基酸化合物作为反应底物,减少了目前报道的催化体系在催化这一化学转化时需要对氨基进行保护和去保护的步骤,更加符合化学反应的原子经济性和步骤经济性。因此,该策略有望成为非天然手性氨基酸衍生物合成的最有效的手段,在手性氨基酸合成领域具有较好的应用前景。
目前,氨基酸酯及其类似物的不对称α-官能化反应主要使用氨基酸酯的醛亚胺或者酮亚胺作为反应底物,该转化需要使用当量的醛或者酮作为保护基,这对于原子经济性来说是不利的。另外,这也额外的增加了上保护基和脱保护基的步骤,于步骤经济性也是不利的。
技术实现要素:
为解决以上技术问题,本发明提供一种手性醛催化剂及制备方法以及催化不对称亲核加成反应的方法。
技术方案如下:
一种手性醛催化剂,其关键在于其化学通式如下:
其中当x为h时,ar为苯基或萘基;当x为i时,ar为苯基;当x为br时,ar为h、苯基、萘基、4-tbuc6h4、4-tmsc6h4中的任一种;当x为4-ch3oc6h4、4-cf3c6h4、3,5-2cf3c6h3中的任一种时,ar为苯基。
上述x为br,ar为萘基。
一种手性醛催化剂的制备方法,其关键在于按以下步骤进行:
步骤①:将(s)-1,1’-联二萘酚溶于二氯甲烷中,加入二异丙基乙基胺,冷却至-78℃,加入三氟甲磺酸酐,搅拌后升至室温,反应完全后冰浴下加入饱和nahco3溶液,分液得水相和有机相,干燥有机相后得化合物1,化合物1结构式如附图1所示;
步骤②:
②-1:氮气氛围下,将化合物1和1,2-双(二苯基膦)乙烷二氯化镍溶于四氢呋喃中,滴加现制的芳基格氏试剂,并加热至回流,反应8h后淬灭,用乙酸乙酯萃取水相,无水na2so4干燥有机相后得化合物2,化合物2结构式如附图1所示;
②-2:将步骤①中所得的化合物1溶于乙醇,依次加入pd/c催化剂和二异丙基乙基胺,在h2氛围中室温反应6h,抽滤,干燥液相得化合物18,化合物18的结构式如附图2所示;
步骤③:将化合物2或化合物18溶于干燥的四氢呋喃,在0℃下加入nah并搅拌,然后滴加氯甲基甲醚,移至室温继续反应,反应完全后淬灭,并用乙酸乙酯萃取,干燥有机相,其中化合物2经上述操作得化合物3,化合物3结构式如附图1所示;化合物18经上述操作得化合物3’,其结构式如附图2所示;
步骤④:在氮气氛围下,将化合物3或化合物3’溶于四氢呋喃中,加入四甲基乙二胺,冷却至-78℃,滴加正丁基锂,然后升至室温搅拌5h,再次降温至-78℃,滴加硼酸三甲酯后又升至室温反应24h,反应完毕后于0℃下加入盐酸溶液并搅拌30min,然后用乙酸乙酯萃取,干燥有机相,其中化合物3经上述操作得化合物4,化合物4结构式如附图1所示;化合物3’经上述操作得化合物4’,其结构式如附图2所示;
步骤⑤:将化合物4或化合物4’溶于氯仿冷却至0℃,加入双氧水反应2h,反应完毕后,在0℃下滴入饱和na2so3溶液至无气泡产生,分相,干燥有机相,其中化合物4经上述操作得化合物5,化合物5结构式如附图1所示;化合物4’经上述操作得化合物5’,其结构式如附图2所示;
步骤⑥:将化合物5或化合物5’、k2co3悬浮于丙酮中,室温下加入碘甲烷后回流反应至原料完全消失,抽滤除去固体,干燥滤液,其中化合物5经上述操作得化合物6,化合物6结构式如附图1所示;化合物5’经上述操作得化合物6’,其结构式如附图2所示;
步骤⑦:将化合物6或化合物6’溶于1,4-二氧六环中,加入盐酸溶液并加热,待原料完全消失后冷却至室温,稀释后分相,干燥有机相,其中化合物6经上述操作得化合物7,化合物7结构式如附图1所示;化合物6’经上述操作得化合物7’,其结构式如附图2所示;
步骤⑧:将化合物7或化合物7’溶于二氯甲烷,加入二异丙基乙基胺,冷却至-78℃,滴加三氟甲磺酸酐,搅拌后升至室温,待原料完全消失后淬灭,分相,干燥有机相,其中化合物7经上述操作得化合物8,化合物8结构式如附图1所示;化合物7’经上述操作得化合物8’,其结构式如附图2所示;
步骤⑨:氮气保护下,将化合物8或化合物8’、1,2-双(二苯基膦)乙烷二氯化镍溶于乙醚,在-10℃下滴加甲基溴化镁溶液,回流反应8h,反应完毕后淬灭,并用乙酸乙酯萃取水相,干燥有机相,其中化合物8经上述操作得化合物9,化合物9结构式如附图1所示;化合物8’经上述操作得化合物9’,其结构式如附图2所示;
步骤⑩:将化合物9或化合物9’、n-溴代琥珀酰亚胺及偶氮二异丁腈加入圆底烧瓶中,并加入环己烷,加热至80℃,待原料完全消失后冷却至室温,分相,干燥有机相,其中化合物9经上述操作得化合物10、11的混合物,二者的结构式如附图1所示;而化合物9’经上述操作得化合物10’,其结构式如附图2所示;
步骤
步骤
步骤
步骤
其中化合物16经上述操作后得到的手性醛催化剂的通式中:
x为h,ar为苯基时记为iiia;x为h,ar为萘基时记为iiib;
其中化合物17经上述操作后得到的手性醛催化剂的通式中:
x为br,ar为苯基时记为iiid;x为br,ar为萘基记为iiie;
x为br,ar为4-tbuc6h4记为iiif;x为br,ar为4-tmsc6h4记为iiig;
化合物13’经上述操作后得到的手性醛催化剂的通式中:x为br,ar为h,记为iiic;
当x为4-ch3oc6h4,ar为苯基时记为iiil;当x为4-cf3c6h4,ar为苯基时记为iiim;当x为3,5-2cf3c6h3,ar为苯基时记为iiin。
一种手性醛催化氨基酸衍生物不对称亲核加成反应的方法,其关键在于:将氨基酸酯或氨基酸酯盐酸盐、α,β-不饱和羰基化合物加入反应瓶中,再依次加入上述手性醛催化剂、2,6-二羧基吡啶和1,5,7-三氮杂环[4.4.0]癸-5-烯以及有机溶剂,充分搅拌反应。
上述氨基酸酯或氨基酸酯盐酸盐为2.0当量,α,β-不饱和羰基化合物为1.0当量,手性醛催化剂为0.1当量,2,6-二羧基吡啶为0.25当量,所述1,5,7-三氮杂环[4.4.0]癸-5-烯为1.0当量。
上述有机溶剂为甲苯、四氢呋喃、氯仿、1,2-二氯乙烷、乙酸乙酯、二甲苯、均三甲苯、氯苯、三氟甲基苯中的任一种。
上述α,β-不饱和羰基化合物的化学通式如下:
其中r1和r2分别独自地选自烃基或烷基中的任一种。
上述氨基酸酯或氨基酸酯盐酸盐的化学通式如下:
其中:r3为h或co2r中,而r为烷基或h中的任一种;r4为烷基或h。
有益效果:采用本发明的有益效果是在催化不对称亲核加成反应时的催化体系使用了手性醛作为催化剂,避免了金属离子对产品的污染,该不对称亲核加成反应方法使用范围广泛,对于各种α,β-不饱和酮以及各种甘氨酸酯均能取得良好的效果,产物多样性的合成有利于对其进一步的转化和利用。
附图说明
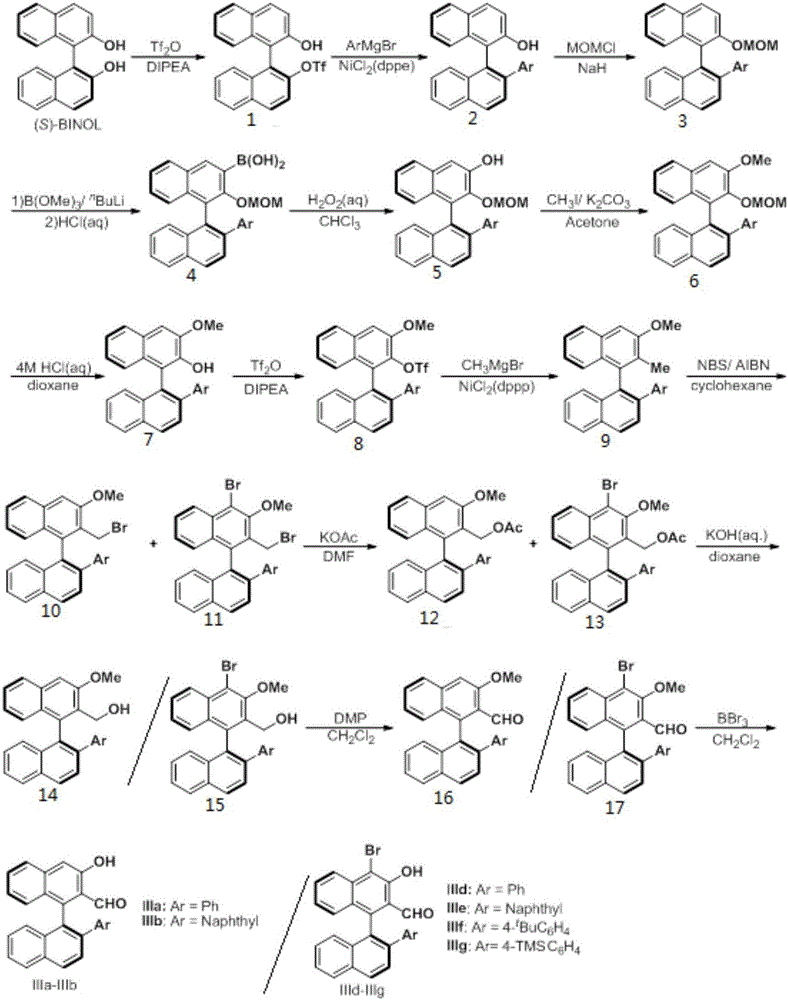
图1为手性醛催化剂iiia、iiib以及iiid-iiig的合成路径图;
图2为手性醛催化剂iiic的合成路径图;
图3为手性醛催化剂iiik的合成路径图;
图4为手性醛催化剂iiil-iiin的合成路径图;
图5为手性醛催化氨基酸衍生物不对称亲核加成反应过程图。
具体实施方式
下面结合实施例和附图对本发明作进一步说明。
实施例1,一种手性醛催化剂,按下列步骤制备:
步骤①:将20mmol(5.72g)的(s)-1,1’-联二萘酚((s)-binol)溶于50ml二氯甲烷中,加入21mmol(3.47ml)的二异丙基乙基胺(dipea),冷却至-78℃,加入21mmol(3.44ml)的三氟甲磺酸酐(tf2o),搅拌10min后升至室温,tlc监测反应,反应完全后冰浴下加入饱和nahco3溶液,分液得水相和有机相,用二氯甲烷萃取水相,将萃取物和分液所得的有机相合并,用无水na2so4干燥有机相后,经柱层析纯化醚(petroleum:acoet=30:1)得化合物1约8.04g,收率达96%;
步骤②:氮气氛围下,将120mmol镁屑(2.88g)加入到干燥的三颈瓶中,并加入5ml重蒸的四氢呋喃及一粒单质碘,室温下慢慢加入50mmol(45ml)相应取代溴苯的四氢呋喃溶液(相应取代溴苯指:与最终制备的手性催化剂的取代基ar相关,如手性催化剂的ar为苯基时为溴苯;手性催化剂的ar为萘基时为2-溴萘;手性催化剂的ar为4-tbuc6h4时为对叔丁基溴苯;手性催化剂的ar为4-tmsc6h4时为对三甲基硅基溴苯),滴加完毕后回流反应6h,制得浓度为1mol/l的现制芳基格氏试剂50ml;
氮气氛围下,将10mmol(4.18g)化合物1和1mmol(528mg)1,2-双(二苯基膦)乙烷二氯化镍溶于14ml重蒸的四氢呋喃中,在-10℃下滴加上述现制芳基格氏试剂50ml,滴加完毕后加热至回流,反应8h后用饱和nh4cl溶液淬灭,用乙酸乙酯萃取水相,无水na2so4干燥有机相后经柱层析(petroleum:acoet=30:1)纯化得化合物2,收率达90-98%,化合物2结构式如附图1所示;
步骤③:将10.73mmol的化合物2溶于干燥的四氢呋喃,在0℃下慢慢加入17.2mmol(687mg,60%)nah并搅拌15min,然后逐滴滴加16.1mmol(1.22ml)氯甲基甲醚(momcl),移至室温继续反应,tlc监测反应进程,反应完全后,0℃下加入饱和nh4cl溶液淬灭,并用乙酸乙酯萃取,合并有机相后用无水na2so4干燥,经柱层析(petroleum:acoet=10:1)纯化的化合物3,收率达82-90%;
步骤④:在氮气氛围下,将8.44mmol化合物3溶于40ml四氢呋喃中,加入12.66mmol(1.89ml)四甲基乙二胺,冷却至-78℃,滴加12.66mmol(7.9ml)正丁基锂(nbuli),该正丁基锂在正己烷中的浓度为1.6mol/l,然后升至室温搅拌5h,再次降温至-78℃,滴加25.32mmol(2.88ml)硼酸三甲酯后又升至室温反应24h,反应完毕后于0℃下加入1mol/l的盐酸溶液10ml并搅拌30min,然后用乙酸乙酯萃取,有机相用无水na2so4干燥后旋干得化合物4的粗产品,该粗产品直接用于下一步反应;
步骤⑤:将步骤④中所得的化合物4的粗产品溶于30ml氯仿冷却至0℃,慢慢加入30%的双氧水6ml,反应2h,反应完毕后,在0℃下慢慢滴入饱和na2so3溶液至无气泡产生,分相,并用二氯甲烷萃取水相,合并有机相后用无水na2so4干燥并旋干,经柱层析(petroleum:acoet=4:1)得化合物5,收率达39-74%;
步骤⑥:将5.87mmol化合物5和17.61mmol(2.43g)k2co3悬浮于26ml丙酮(acetone)中,室温下加入23.47mmol(1.46ml)碘甲烷后回流反应至原料完全消失,抽滤除去固体,滤饼用ch2cl2洗涤,将洗涤液和滤液合并,旋干滤液得化合物6的粗产物,该粗产品可直接用于下一步反应;
步骤⑦:将化合物6的粗产品溶于16ml的1,4-二氧六环(dioxane)中,加入16ml浓度为4mol/l的盐酸溶液并加热至60℃,待原料完全消失后冷却至室温,加入水和乙酸乙酯稀释后分相,水相用乙酸乙酯萃取,有机相用无水na2so4干燥后旋干,经柱层析(petroleum:acoet=10:1)纯化得化合物7,收率达95-98%;
步骤⑧:将5.65mmol化合物7溶于17ml二氯甲烷,加入14.13mmol(2.33ml)二异丙基乙基胺,冷却至-78℃,滴加11.3mmol(1.84ml)三氟甲磺酸酐,搅拌10min后升至室温,待原料完全消失后在冰浴下加入饱和nahco3溶液淬灭,分相,水相用二氯甲烷萃取,有机相经无水na2so4干燥后经柱层析(petroleum:acoet=30:1)纯化得化合物8,收率达80-86%;
步骤⑨:氮气保护下,将4.68mmol化合物8和0.14mmol(76.2mg)1,2-双(二苯基膦)乙烷二氯化镍[nicl2(dppe)]溶于13ml重蒸的乙醚,在-10℃下逐滴滴加3mol/l的甲基溴化镁4.68ml,滴加完毕后回流反应8h,反应完毕后用饱和nh4cl溶液淬灭,并用乙酸乙酯萃取水相,无水na2so4干燥有机相后经柱层析(petroleum:acoet=30:1)纯化得化合物9,收率达90-98%;
步骤⑩:将4.79mmol化合物9、19.16mmol(3.41g)n-溴代琥珀酰亚胺(nbs)及0.48mmol(78.6mg)偶氮二异丁腈(aibn)加入圆底烧瓶中,并加入25ml环己烷(cyclohexane),加热至80℃,tlc监测反应进程,待原料完全消失后冷却至室温,加入饱和nh4cl和乙酸乙酯稀释,分相,并用乙酸乙酯萃取水相,无水na2so4干燥有机相后经柱层析(petroleum:acoet=60:1)分离得化合物10、11的混合物,总收率可达80-89%;
步骤
步骤
步骤
步骤
其中化合物16经上述操作后可得两种手性醛催化剂,分别记为iiia和iiib;
化合物17经上述操作后可得四种手性醛催化剂,分别记为iiid、iiie、iiif和iiig;
将该化合物18经与上述步骤③-步骤
步骤
催化剂iiia-iiib,以及iiid-iiig的合成路径见附图1,其中iiia的x为h,ar为苯基(ph);iiib的x为h,ar为萘基(naphthyl);iiid的x为br,ar为苯基;iiie的x为br,ar为萘基;iiif的x为br,ar为4-tbuc6h4;iiig的x为br,ar为4-tmsc6h4;
催化剂iiic的合成路径见附图2,其中x为br,ar为h;
催化剂iiik的合成路径见附图3,其中x为i,ar为苯基;
催化剂iiil-iiiln的合成路径见附图4,其中iiil的x为4-ch3oc6h4,ar为苯基;iiim的x为4-cf3c6h4,ar为苯基;iiin的x为3,5-2cf3c6h3,ar为苯基。
用核磁共振对制备的手性醛催化剂分别进行表征,结果如下:
催化剂iiia:(s)-3-hydroxy-2'-phenyl-[1,1'-binaphthalene]-2-carbaldehyde
黄色固体;[α]d20=-103.5(c=0.2,ch2cl2);1hnmr(600mhz,cdcl3)δ10.91(s,1h),9.55(s,1h),8.10(d,j=8.4hz,1h),8.00(d,j=8.1hz,1h),7.68(dd,j=26.4,8.4hz,2h),7.50(dt,j=15.2,7.4hz,2h),7.33(t,j=7.7hz,2h),7.27(s,1h),7.16–7.10(m,2h),7.08(d,j=6.7hz,1h),7.05(t,j=7.1hz,2h),6.96(d,j=7.3hz,2h);13cnmr(150mhz,cdcl3)δ197.43,156.48,146.45,140.94,140.85,137.98,133.45,132.46,129.95,129.85,129.41,128.52,128.44,128.14,128.04,127.92,127.88,127.29,127.20,127.00,126.80,126.34,124.50,119.97,112.10;hrms(esi):c27h18nao2(m+na)+:计算值:397.1199,测定值:397.1206.
催化剂iiib:(s)-3-hydroxy-[1,1':2',2”-ternaphthalene]-2-carbaldehyde
黄色固体;1hnmr(600mhz,cdcl3)δ10.82(s,1h),9.61(s,1h),8.13(d,j=8.5hz,1h),8.01(d,j=8.2hz,1h),7.74(d,j=8.5hz,1h),7.68(d,j=8.4hz,1h),7.65(d,j=7.2hz,1h),7.54–7.46(m,5h),7.40(d,j=8.6hz,1h),7.39–7.32(m,3h),7.22(s,1h),7.19–7.12(m,2h),7.03(d,j=8.5hz,1h);13cnmr(150mhz,cdcl3)δ197.32,156.47,146.39,140.79,138.39,138.01,133.54,132.94,132.52,132.19,130.22,129.86,129.46,128.51,128.17,128.13,127.94,127.91,127.89,127.66,127.50,127.35,127.04,126.80,126.41,126.36,126.19,126.11,124.57,120.04,112.19.hrms(esi):c31h20nao2(m+na)+:计算值:447.1356,测定值:447.1358.
催化剂iiic:(r)-4-bromo-3-hydroxy-[1,1'-binaphthalene]-2-carbaldehyde
黄色固体;1hnmr(600mhz,cdcl3)δ11.94(s,1h),9.54(s,1h),8.32(d,j=8.6hz,1h),8.06(d,j=8.3hz,1h),7.99(d,j=8.3hz,1h),7.68–7.62(m,2h),7.55–7.51(m,1h),7.50(dd,j=6.9,0.9hz,1h),7.38–7.34(m,1h),7.27–7.25(m,1h),7.21–7.16(m,2h);13cnmr(150mhz,cdcl3)δ197.35,153.29,147.04,136.46,133.32,131.78,131.48,129.52,129.25,128.48,128.42,128.39,127.32,126.65,126.26,126.00,124.97,120.27,107.39.hrms(esi):c21h13brnao2(m+na)+:计算值:398.9991,测定值:399.0005.
催化剂iiid:(s)-4-bromo-3-hydroxy-2'-phenyl-[1,1'-binaphthalene]-2-carbaldehyde
黄色固体;[α]d20=-119.0(c=0.2,ch2cl2);1hnmr(600mhz,cdcl3)δ11.72(s,1h),9.50(s,1h),8.26(d,j=8.5hz,1h),8.11(d,j=8.3hz,1h),7.99(d,j=8.0hz,1h),7.72–7.61(m,2h),7.56–7.48(m,1h),7.39(d,j=8.4hz,1h),7.32(t,j=7.1hz,1h),7.21(t,j=7.1hz,1h),7.12–7.03(m,4h),6.95(d,j=7.0hz,2h);13cnmr(150mhz,cdcl3)δ196.86,153.28,146.08,141.07,140.60,136.05,133.33,132.44,131.27,129.71,129.15,128.42,128.21,128.19,127.89,127.48,127.38,126.59,126.45,126.40,125.13,119.86,107.28;hrms(esi):c27h17brnao2(m+na)+:计算值:475.0304,测定值475.0314.
催化剂iiie:(s)-4-bromo-3-hydroxy-[1,1':2',2”-ternaphthalene]-2-carbaldehyde
黄色固体;[α]d20=-143.5(c=0.2,ch2cl2);1hnmr(600mhz,cdcl3)δ11.64(s,1h),9.56(s,1h),8.25(d,j=8.6hz,1h),8.14(d,j=8.5hz,1h),8.01(d,j=8.2hz,1h),7.74(d,j=8.5hz,1h),7.70–7.62(m,2h),7.55–7.47(m,5h),7.40–7.32(m,3h),7.26–7.21(m,1h),7.09(d,j=8.5hz,1h),7.01(dd,j=8.5,1.7hz,1h);13cnmr(150mhz,cdcl3)δ196.80,153.28,146.02,140.95,138.16,136.10,133.42,132.94,132.52,132.25,131.29,129.76,129.43,129.22,128.42,128.26,128.15,127.92,127.89,127.84,127.56,126.60,126.54,126.47,126.35,126.26,126.15,125.20,119.93,107.40;hrms(esi):c31h19brnao2(m+na)+:计算值:525.0461,测定值:525.0468.
催化剂iiif:(s)-4-bromo-2'-(4-(tert-butyl)phenyl)-3-hydroxy-[1,1'-binaphthalene]-2-carbaldehyde
黄色固体;[α]d20=-116.0(c=0.2,ch2cl2);1hnmr(600mhz,cdcl3)δ11.77(s,1h),9.49(s,1h),8.28(d,j=8.6hz,1h),8.09(d,j=8.5hz,1h),7.98(d,j=8.2hz,1h),7.65(t,j=8.0hz,2h),7.49(t,j=7.5hz,1h),7.41(d,j=8.5hz,1h),7.30(t,j=7.7hz,1h),7.23–7.20(m,1h),7.08(d,j=8.2hz,2h),7.01(d,j=8.5hz,1h),6.89(d,j=8.2hz,2h),1.20(s,9h);13cnmr(150mhz,cdcl3)δ196.98,153.36,150.28,146.44,140.93,137.50,136.05,133.43,132.35,131.26,129.65,129.34,128.92,128.52,128.20,128.17,127.38,126.58,126.38,126.31,125.20,125.14,119.84,107.18,34.43,31.16;hrms(esi):c31h25brnao2(m+na)+:计算值:531.0930,测定值:531.0934.
催化剂iiig:(s)-4-bromo-3-hydroxy-2'-(4-(trimethylsilyl)phenyl)-[1,1'-binaphthalene]-2-carbaldehyde
黄色固体;[α]d20=-114.0(c=0.2,ch2cl2);1hnmr(600mhz,cdcl3)δ11.77(s,1h),9.50(s,1h),8.28(d,j=8.6hz,1h),8.10(d,j=8.5hz,1h),7.98(d,j=8.2hz,1h),7.68–7.61(m,2h),7.50(t,j=7.5hz,1h),7.41(d,j=8.5hz,1h),7.31(t,j=7.7hz,1h),7.25–7.19(m,3h),7.01(d,j=8.5hz,1h),6.95(d,j=7.8hz,2h),0.17(s,9h);13cnmr(150mhz,cdcl3)δ196.90,153.32,146.21,140.95,140.82,139.60,136.04,133.37,133.23,132.42,131.29,129.71,129.31,128.96,128.48,128.18,128.05,127.72,127.44,126.60,126.43,126.40,125.18,119.84,107.28,-1.23;hrms(esi):c30h25brnao2si(m+na)+:计算值:547.0699,测定值:547.0701.催化剂iiik:(s)-3-hydroxy-4-iodo-2'-phenyl-[1,1'-binaphthalene]-2-carbaldehyde
黄色固体;[α]d20=-113.5(c=0.2,ch2cl2);1hnmr(600mhz,cdcl3)δ12.00(s,1h),9.43(s,1h),8.19(d,j=8.6hz,1h),8.11(d,j=8.5hz,1h),7.99(d,j=8.2hz,1h),7.65(d,j=8.5hz,1h),7.61(t,j=7.7hz,1h),7.51(t,j=7.5hz,1h),7.36(d,j=8.4hz,1h),7.32(t,j=7.6hz,1h),7.22–7.17(m,1h),7.09(t,j=7.3hz,1h),7.05(t,j=7.7hz,3h),6.95(d,j=7.3hz,2h);13cnmr(150mhz,cdcl3)δ196.70,156.07,147.41,140.99,140.60,138.47,133.29,132.44,131.68,131.48,129.71,129.40,129.23,128.59,128.43,128.21,127.91,127.49,127.41,126.64,126.47,125.19,119.41,86.59;hrms(esi):c27h17inao2(m+na)+:计算值:523.0165,测定值:523.0169.
实施例2,一种手性醛催化氨基酸衍生物不对称亲核加成反应的方法,按下述步骤进行:将α,β-不饱和羰基化合物、氨基酸酯或氨基酸酯盐酸盐加入反应瓶中,再依次加入实施例1制备的手性醛催化剂中的任一种、2,6-二羧基吡啶、1,5,7-三氮杂环[4.4.0]癸-5-烯(tbd),再加入0.5ml溶剂,在50℃下充分磁力搅拌,tlc监测,当α,β-不饱和羰基化合物完全消失后,将整个反应体系直接旋干过柱(过柱条件为石油醚:乙酸乙酯=10:1,其中乙酸乙酯为液体纯净物),获得脯氨酸衍生物,该反应中α,β-不饱和羰基化合物的r1和r2的碳原子数均小于等于10、氨基酸酯或氨基酸酯盐酸盐的r3和r4的碳原子数均小于等于6。
下面结合试验例来进一步说明本发明。
根据实施例2所述方法,分别选取不同的α,β-不饱和羰基化合物和氨基酸酯或氨基酸酯盐酸盐进行反应,反应过程如图5所示,具体试验材料如表1所示,其中“反应原料使用量”一栏中按顺序分别依次表示α,β-不饱和羰基化合物、氨基酸酯或氨基酸酯盐酸盐、手性醛催化剂、2,6-二羧基吡啶、tbd的使用当量,反应结束得到的产物——脯氨酸衍生物的收率和ee值见表1。
分别将试验例1-34所获得的脯氨酸衍生物用核磁共振、高分辨质谱进行表征,结果如下。
试验例1:tert-butyl(2s,3r)-3,5-diphenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例2:tert-butyl(2s,3r)-3-(2-fluorophenyl)-5-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例3:tert-butyl(2s,3r)-3-(3-chlorophenyl)-5-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例4:tert-butyl(2s,3r)-3-(3-bromophenyl)-5-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例5:(2s,3r)-5-phenyl-3-(4-(trifluoromethyl)phenyl)-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例6:tert-butyl(2s,3r)-3-(4-nitrophenyl)-5-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例7:tert-butyl(2s,3r)-3-(4-methoxyphenyl)-5-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例8:tert-butyl(2s,3r)-3-(3-methoxyphenyl)-5-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例9:tert-butyl(2s,3r)-3-(4-(tert-butyl)phenyl)-5-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例10:tert-butyl(2s,3r)-3-(naphthalen-2-yl)-5-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例11:tert-butyl(2s,3r)-3-(furan-2-yl)-5-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例12:tert-butyl(2s,3r)-5-phenyl-3-(thiophen-2-yl)-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例13:tert-butyl(2s,3r)-5-phenyl-3-(pyridin-2-yl)-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例14:tert-butyl(2s,3r)-5-phenyl-3-((e)-styryl)-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例15:tert-butyl(2s,3r)-5-(4-chlorophenyl)-3-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式
试验例16:tert-butyl(2s,3r)-5-(4-chlorophenyl)-3-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例17:tert-butyl(2s,3r)-5-(4-bromophenyl)-3-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例18:(2s,3r)-5-(3,5-bis(trifluoromethyl)phenyl)-3-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例19:tert-butyl(2s,3r)-3-phenyl-5-(p-tolyl)-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例20:tert-butyl(2s,3r)-5-(3-methoxyphenyl)-3-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例21:(2s,3r)-5-(4-(dimethylamino)phenyl)-3-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例22:tert-butyl(2s,3r)-5-([1,1'-biphenyl]-4-yl)-3-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例23:tert-butyl(2s,3r)-5-(3,4-dimethoxyphenyl)-3-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例24:tert-butyl(2s,3r)-5-(naphthalen-1-yl)-3-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例25:tert-butyl(2s,3r)-3-phenyl-5-((e)-styryl)-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例26:tert-butyl(2s,3r)-3-methyl-5-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例27:tert-butyl(2s,3r)-3-ethyl-5-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例28:tert-butyl(2s,3r)-3-cyclopropyl-5-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例29:methyl(2s,3r)-3,5-diphenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例30:ethyl(2s,3r)-3,5-diphenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例31:isopropyl(2s,3r)-3,5-diphenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例32:ethyl(2s,3r)-3-(4-fluorophenyl)-5-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例33:ethyl(2s,3r)-5-(2-chlorophenyl)-3-phenyl-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
试验例34:ethyl(2s,3r)-3-phenyl-5-(p-tolyl)-3,4-dihydro-2h-pyrrole-2-carboxylate,结构式及表征如下:
最后需要说明的是,上述描述仅仅为本发明的优选实施例,本领域的普通技术人员在本发明的启示下,在不违背本发明宗旨及权利要求的前提下,可以做出多种类似的表示,这样的变换均落入本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!