用于凝血感测的微流体芯片的制作方法
背景技术:
微流体学是跨包括工程学、物理学、化学、微技术和生物技术的各种学科来应用的技术。微流体学涉及到对少量流体的研究以及对如何在诸如微流体芯片之类的各种微流体系统和设备中操纵、控制和使用这样的少量流体的研究。例如,微流体生物芯片(被称为“片上实验室”)在分子生物学领域中用于整合化验操作,以用于诸如分析酶和dna、检测生物化学毒素和病原体、诊断疾病等目的。
附图说明
图1示出了根据本公开的微流体感测系统的示例。
图2示出了根据本公开的用于凝血感测的微流体芯片的示例的示意图。
图3进一步示出了根据本公开的微流体芯片的示例。
图4示出了根据本公开的、如用微流体芯片检测到的、在凝血级联期间的阻抗变化的图形表示。
具体实施方式
在定点护理测试中可采用微流体芯片来使得能够在与待测试个体相关联的位置处实现化验操作。例如,在微流体测试的各种定点护理方法中,可通过微流体测试设备中的传感器分析样本以(除了其它可能的状况之外)给出对于疾病状态的指示。
活细胞是有机体的基本结构和功能单元。多数动物和植物细胞具有1-100微米范围的尺寸并且包含至关重要的健康信息。基于细胞的诊断法可被用于检测传染疾病、慢性疾病、以及诸如凝血失调之类的各种生物学异常。传统的细胞级别的诊断工具例如可能是昂贵的,涉及到针对操作的专门训练,并且可能无法一直被部署在定点护理环境处。另外,医疗保健正逐渐从集中化的医院迁移开到更分布式和/或家庭中的环境。此转变例如可涉及到提供与在医院中使用复杂机器完成的测试相同的性能水平和功能性、但是以更小和更便携的形式的技术的使用。
一些诊断工具能够测量血液样本的凝血速率。然而,这样的诊断工具要求使用试剂和/或活化剂来将凝血速率加速至可测量的水平。类似地,这样的诊断工具无法确定血液样本可能处于的凝血级联中的具体阶段。相比而言,根据本公开的微流体芯片可包括阻抗传感器来在无需添加试剂和/或活化剂来加速凝血过程的情况下确定凝血级联的阶段。
出于本公开的目的,术语“微流体”指代与具有容积或者携带颗粒的流体相互作用的设备和/或过道,所述容积或颗粒具有处于“微”范围中的尺寸(分别是微升或微米)。出于本公开的目的,术语“颗粒”涵盖任何微小的片、片段或量,包括但不限于:生物细胞或生物细胞的群组。“流体”可包括液体、气体或者它们的混合。此外,“生物样本”指代血液和/或诸如血浆和/或血清之类的血液成分,以及其它成分。
图1示出了根据本公开的微流体感测系统100的示例。如图1中所示,微流体感测系统100包括微流体芯片102、流体储液器104、电子控制器106和计算设备108。一般而言,流体的样本可被放置在流体储液器104中。在一些示例中,流体可具有低至10皮升(pl)和高至1微升(μl)的容积。流体可以是具有颗粒的宿主流体(hostfluid)(例如,血液样本、包含颜料/颗粒的印墨等等)。如在本文进一步论述的那样,在电子控制器106和计算设备108的控制下,可在微流体芯片102上通过微流体学对流体进行处理并使流体接触微流体芯片102中的传感器。微流体芯片102可向电子控制器106提供表示感测到的数据的电输出信号。
电子控制器106可在计算设备108的控制下。例如,计算设备108可以发送数据到电子控制器106,并可以从电子控制器106接收数据,所述数据包括用于控制微流体芯片102的命令信息和从微流体芯片102得到的传感器数据。
计算设备108可包括中央处理单元(cpu)110、各种支持电路112、存储器114、各种输入/输出(i/o)电路116和外部接口118。在一些示例中,可在计算设备108上安装微流体应用。如本文所用,微流体应用指代由处理资源执行的、指导处理资源实行微流体感测测试的指令。例如,如本文进一步描述的那样,微流体应用可包括由电子控制器106和微流体芯片102执行以实行凝血感测的指令。
支持电路112可包括高速缓存、电源、时钟电路、数据寄存器等。存储器114可以包括随机存取存储器、只读存储器、高速缓存存储器、磁性读/写存储器和/或此类存储器设备的任何组合。i/o电路116可以与外部接口118协作以通过通信介质119促进与电子控制器106的通信。通信介质119可以是任何类型的传输路径,包括电气、光学和/或射频(rf)路径。
外部接口118可包括通用串行总线(usb)控制器,其能够通过usb线缆向电子控制器106发送和接收数据,以及通过usb线缆向电子控制器106提供电力。另外,电子控制器106可接收与微流体芯片102耦合的匣盒101。例如,微流体芯片102可被机械地插入到匣盒101中,并且匣盒101(具有与其耦合的微流体芯片102)可被插入到电子控制器106中。
存储器114可存储操作系统(os)109和驱动器111。os109和驱动器111可包括可由cpu11o执行的指令,以用于通过外部接口118控制计算设备108和电子控制器106。驱动器111可提供os109和电子控制器106之间的接口。相应地,计算设备108可包括可编程设备,其包括例如非暂态处理器/计算机可读介质(例如,存储器)上的机器可读指令。
计算设备108还可包括显示器120,os109可以通过显示器120提供用户界面(ui)122。用户可以使用ui122与os109和驱动器111交互以控制计算设备108、电子控制器106和/或微流体芯片102。例如,用户可使用ui122来启动微流体应用并选择要通过使用微流体芯片102在生物样本上执行的测试。如本文所用,用户可指代医疗保健专业人士和/或患者。然而,示例不限于此,并且用户可指代除了医疗保健专业人士和患者之外的用户。
计算设备108也可显示从电子控制器106接收的数据。例如,计算设备108可显示通过微流体芯片102收集、显示和/或分析的数据。在一些示例中,在计算设备108的ui122上显示的数据可包括诊断,诸如凝血障碍的诊断。此外和/或替换地,在计算设备108的ui122上显示的数据可包括描述使用微流体芯片102收集的数据的图、表和/或其它总结。例如,计算设备108的ui122可显示指示血液样本的凝血速率的数据。然而,示例并不限于此,并且计算设备108的ui122可显示用微流体芯片102收集到的、与流体样本的凝血有关的其它形式的数据。在一些示例中,计算设备108可以是诸如“智能电话”、“平板计算机”或其它设备之类的便携式计算设备。
流体储液器104可与微流体芯片102流体连通。在一些示例中,流体储液器104是外部流体储液器,这意味着流体储液器104在微流体芯片102外部。例如,流体储液器104可在匣盒101上,其中匣盒可接收微流体芯片102。然而,示例并不限于此,并且流体储液器104和/或流体储液器104的一部分可位于微流体芯片102自身上(例如,不在匣盒101上)。例如,流体储液器104的下部可位于微流体芯片102上,而流体储液器104的上部可位于匣盒101上。统称地,与匣盒101耦合的微流体芯片102可被称作微流体设备。
在一些示例中,流体储液器104可保持流体成分/样本和/或溶液并向微流体芯片102供应流体成分/样本和/或溶液。微流体芯片102的各种示例在本文被进一步描述并且通常可包括(一个或多个)入口腔/出口腔124、(一个或多个)微流体通道126、(一个或多个)致动器128、(一个或多个)微流体过滤器130、(一个或多个)传感器131、电气接口132和(一个或多个)喷嘴133。在一些示例中,微流体芯片102的结构和组件可使用诸如薄膜沉积、电铸、激光消融、各向异性蚀刻、溅射、干法或湿法蚀刻、光刻、铸造、模塑、冲压、机械加工、旋涂、层压等传统的集成电路微制造技术来制造。另外,微流体芯片102可由多种材料组成。例如,微流体芯片102可包括体硅衬底,体硅衬底被微制造来形成微流体通道126和/或(一个或多个)传感器131。此外,微流体芯片102可包括由诸如su-8之类的感光聚合物组成的微流体通道126。
电子控制器106可被耦合至微流体芯片102并且可使得能够实现计算设备108和微流体芯片102之间的信息和/或电力的传输。在一些示例中,电子控制器106可包括控制器134、i/o电路136和存储器138。另外,电子控制器106可(诸如通过usb线缆)从计算设备108接收电力。然而,示例并不限于此,并且电子控制器可以包括电源142。
存储器138可存储具有指令140的硬件,指令140可包括可由控制器134执行以用于控制微流体芯片102以及与计算设备108通信的指令。例如,具有指令140的硬件可包括可由控制器134执行以用于控制微流体芯片102上的传感器131的指令。相应地,电子控制器106可包括可编程设备,所述可编程设备包括以软件模块的形式存储在例如非暂态处理器/计算机可读介质(例如存储器)上的机器可读指令。可使用可编程逻辑设备(pld)、专用集成电路(asic)等来实现电子控制器106的全部或者一部分。如本文所用,计算模块可包括计算机可执行指令、硬件组件(例如,各种形式的晶体管逻辑、专用集成电路(asic)等等)或者它们的组合。但是计算模块至少包括例如以模块的形式的可由处理资源执行的指令来实行本文更详细描述的特定动作、任务和功能。
在一些示例中,(一个或多个)传感器131可被安置在(一个或多个)通道126中靠近(一个或多个)通道126的(一个或多个)入口处(例如,比(一个或多个)致动器128更接近流体储液器104)。在另一示例中,(一个或多个)传感器131可被安置在(一个或多个)通道126的入口中。(一个或多个)传感器131可以是使用各种半导体形成技术形成的阻抗传感器。(一个或多个)传感器131可随着流体样本中的颗粒通过和/或靠近(一个或多个)传感器131来检测阻抗变化,如本文进一步论述的那样。
另外,(一个或多个)致动器128可被安置于传感器131下游靠近(一个或多个)通道126的闭端。可使用适合于传送流体样本穿过通道126的各种各样的结构来实现(一个或多个)致动器128。例如,(一个或多个)致动器128可以是产生蒸汽泡以在(一个或多个)通道126内产生流体样本的流体位移的(一个或多个)热敏电阻器。致动器128也可以被实现为压电元件(例如,pzt),其电气感应的偏转生成(一个或多个)通道126内的流体位移。通过电气的、磁性的和其它的力激活的其它偏转膜元件也可能用于供实现(一个或多个)致动器128之用。
流体样本(例如,由流体储液器104接收的流体样本)可从微流体芯片102上的(一个或多个)喷嘴133中喷射。喷嘴可指代适用于与(一个或多个)致动器128一起使用的喷射喷嘴。另外,(一个或多个)喷嘴133可被安置在(一个或多个)通道126中或者沿(一个或多个)通道126安置,如在本文中进一步论述的那样。例如,(一个或多个)喷嘴133可与(一个或多个)通道126中的(一个或多个)传感器131相邻。
尽管在图1中示出了以上描述的元件和配置,但本公开并不限于此。相反,如本文所述,更多或更少的组件可被包括在微流体感测系统100中、在微流体芯片102、电子控制器106和计算设备108中,和/或更多或更少的组件可以以各种配置进行布置,如本文中描述的那样。此外,尽管示出了特定数量的元件(例如,单个通道126),但是取决于微流体感测系统100的期望应用,可存在更多(例如,两个或更多个通道126)和/或更少的诸如流体储液器104、(一个或多个)通道126、(一个或多个)致动器128、(一个或多个)过滤器130、电气接口132、(一个或多个)传感器131、喷嘴133等等的各种元件。
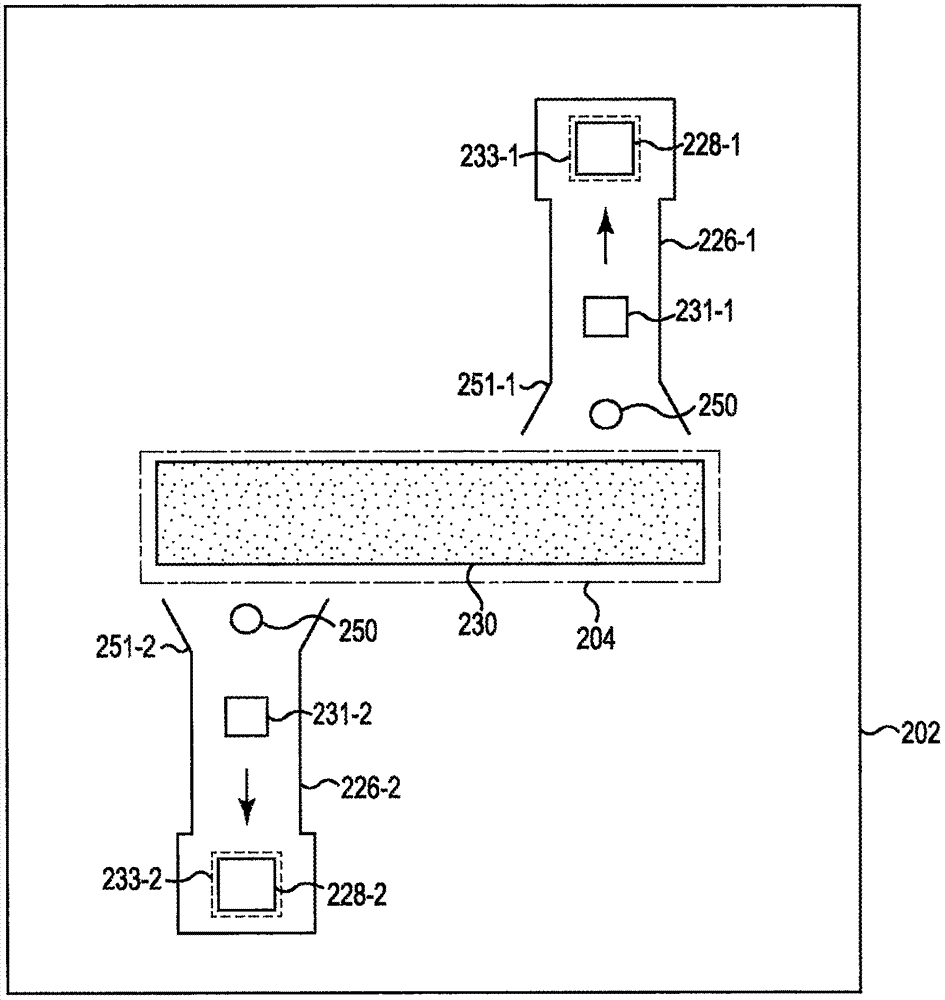
图2示出了根据本公开的用于凝血感测的微流体芯片202的示例的示意图。如图2中所示,微流体芯片202可包括诸如微流体通道之类的多个通道226-1、226-2(统称为通道226),致动器228-1、228-2(统称为致动器228),传感器231-1、231-2(统称为传感器231),用以从流体储液器204接收流体样本250的入口251-1、251-2(统称为入口251),以及喷嘴233-1、233-2(统称为喷嘴233)。如本文所用,喷嘴指的是从通道226的出口和/或开口。此外,如图2中所示,每个喷嘴233可处于微流体通道226的末端。
入口251可提供用于通道226的开口以接收流体样本。在一些示例中,过滤器230可被安置在入口251中。过滤器230可防止流体样本中特定尺寸(取决于过滤器230的尺寸)的颗粒进入通道226。入口251可比通道226具有更大的宽度和容积。就是说,入口251的容积可比通道226的容积更大。入口251可使得流体样本能够从流体储液器204流动到通道226中。
微流体通道226也可包括变窄的部分。变窄的部分可各自是相应微流体通道226中具有比入口251更窄的直径的部分。变窄的部分可相对于入口251在流体储液器204的远端。在一些示例中,微流体通道226的变窄的部分内可包括喷嘴233(例如,出口)。然而示例并不限于此,并且微流体通道226不需要相对于入口251变窄。例如,微流体通道226可以与入口251具有相同的宽度。如本文进一步所述,喷嘴233(例如,出口)可具有空气接口,从而使得喷嘴233被暴露于空气。
另外,微流体芯片202可包括位于每个微流体通道226内的传感器231,诸如阻抗传感器。如本文所用,阻抗传感器可确定阻抗中的改变,例如来确定穿过微流体通道226流至阻抗传感器(例如,传感器231)的血液样本(例如,流体样本250)的凝血级联的阶段。传感器231可在喷嘴233的特定接近度之内。例如,传感器231可距喷嘴233小于100微米(μm)。然而示例并不限于此,并且传感器231可直接在喷嘴233下方。换言之,传感器231-2可位于距入口251-2的一定距离处,该距离等于喷嘴233-2距入口251-2的距离。
如本文所用,凝血级联指代在血凝块的形成中涉及到的一系列阶段。一般地,凝血级联可包括:包括血小板的活化、粘附和聚集以形成软栓子(plug)的第一阶段;包括纤维蛋白丝的形成和蔓延的第二阶段;以及包括全止血栓子的形成的第三阶段。
如本文所用,凝血级联的第一阶段可被称作一期止血。当血细胞被暴露(诸如通过微流体芯片202中的出口228进行暴露)至空气时,可开始血小板粘附。血小板粘附包括诸如血清素、血小板活化因子(paf)、血小板第4因子和血栓素a2以及其它的各种颗粒的释放。这些颗粒的释放可造成血液样本中的血小板形状上的改变以及后续的血小板的粘附。血小板的粘附可接着导致“软栓子”的形成,这标志着凝血级联的第一阶段的结束。
凝血级联的第二阶段可被称作二期止血,并且可导致使在一期止血期间形成的软栓子稳定化。凝血级联的第二阶段可包括纤维蛋白丝的形成和蔓延。纤维蛋白丝指代在血液的凝结中涉及到的纤维状非球状蛋白。纤维蛋白丝的形成包括纤维蛋白原与凝血蛋白酶的聚合。形成的纤维蛋白丝进一步蔓延或倍增,并且聚合的纤维蛋白丝与血小板一起可形成全止血栓子(也被称为血凝块)。如本文所用,全止血栓子的形成指示凝血级联的第三阶段。
如本文进一步所述,传感器231可响应于检测血液样本(例如,流体样本250)处在凝血级联的哪一阶段而检测阻抗中的变化。例如,阻抗传感器(例如,传感器231)可响应于对血液样本中的聚集的血小板的检测而检测阻抗中的变化。在另一示例中,阻抗传感器可响应于对血液样本中的软栓子的检测而检测阻抗中的变化。另外,阻抗传感器可响应于对血液样本中形成的纤维蛋白丝的检测和/或纤维蛋白原的检测而检测阻抗中的变化。此外,阻抗传感器可响应于对血液样本中的全止血栓子的检测而检测阻抗中的变化。
微流体芯片202也可包括被安置于传感器231下游靠近通道226的末端的致动器228。致动器228可以是流体惯性致动器,其可使用各种各样的结构来实现。例如,致动器228可以是泵,诸如产生蒸汽泡以产生通道226内的流体位移的热敏电阻泵。电阻泵(例如,致动器228)可加速流体样本250(诸如,血细胞流)穿过微流体通道226的流动。被移位的流体样本250可从(一个或多个)喷嘴223中喷出。
在一些示例中,传感器231可被安置在通道226中。传感器231可以是使用各种半导体技术形成的阻抗传感器。传感器231可随着流体样本中的颗粒通过传感器231来检测阻抗变化。
如图2中所示,微流体芯片202可包括多个通道226、多个入口251、多个传感器231等等。这样,微流体芯片202可包括多个微流体通道来引导诸如流体样本250之类的血液样本的流动。流体样本250可被向下引导至所述多个通道226中的每一个。尽管图2示出了两个入口251、两个传感器231、两个通道226等等,但示例并不限于此。微流体芯片202可包括比图2中所示更多或更少的特征。
所述多个通道226(例如,微流体通道)中的每一个可在末端处具有出口。流体样本250可从流体储液器204中流动离开并且流向所述多个通道226中的每一个的末端。例如,流体样本250可流入入口251-1,流入通道226-1并流过传感器231-1,并流向通道226-1的末端处的喷嘴233-1。如本文所述,喷嘴233中的每一个可以是通道中的出口,并因此具有空气接口。在一些示例中,每个喷嘴233在直径上的范围可从5至100微米(μm)。另外,通道226中喷嘴233的放置结合喷嘴的空气接口可模拟血液到伤口的流动并且可允许在不使用任何试剂和/或活化剂的情况下检测凝血级联的不同阶段。
在示例中,可在流体储液器204中提供用于过滤所接触的流体样本中的颗粒的过滤器230(例如,网格过滤器)。尽管流体通道226的形状被示出为直的,但这并不意图作为对通道226的形状的限制。因此,通道226的形状可包括其它形状,诸如弯曲的形状、蛇状的形状、具有拐角的形状、它们的组合等等。此外,没有将通道226示为任何特定大小或比例。如在设备上制造的通道226的宽度可不同于此公开的图示中示出的任何大小或比例。在一些示例中,通道226的宽度的范围可以是从500nm至500μm,从而产生用于检测凝血级联的各个阶段的高度灵敏的系统。
此外,微流体通道226内侧或者与微流体通道226紧密邻近的微制造的电阻元件(未在图2中示出)可提供对流体样本的受控加热以加快和/或加速流体样本的流动、迁移、蒸发和/或凝血。电阻元件可通过施加例如在1和30伏特(v)之间的电压来驱动特定的时间段(诸如,1到20微秒(μs))。可借助于热感测电阻器来提供温度反馈。
图3进一步示出了根据本公开的微流体芯片302的示例。具体地,图3示出了微流体芯片302中的传感器331和相关结构的特写视图。
微流体芯片302可包括通道326和传感器331(诸如阻抗传感器)。如本文所述,通道326可包括微流体过道,包括颗粒354的流体可通道该微流体过道。为了此公开的目的,术语“颗粒”涵盖任何微小的片、片段或量,包括但不限于:生物细胞或生物细胞的群组、血液的成分(诸如血小板)、血凝块的成分(诸如纤维蛋白和/或纤维蛋白原)、和/或止血栓子、以及其它。通道326可引导流体和颗粒354流动穿越和/或穿过由传感器331在通道326内形成的电场区域(efr)360(示意性示出)。
传感器331可形成通道326内的efr360。传感器331可包括电接地361和输入电极362,它们协作以形成在通道326的地区内延伸的电场线的区域360。如本文所用,电接地361可包括输入低侧电极,并且输入电极362可包括输入高侧电极。电接地361和输入电极362二者均可以是“本地的”,因为电接地361和输入电极362是由邻近通道326内部或者相对紧密邻近通道326内部(诸如就在通道326的内表面或表层下方或后面)的导电触点提供的。与位于通道326外侧或者远端通道326的远程接地相比,接地361和输入电极362之间的电场区域360的基本大部分(如果不是全部的话)被包含在通道326内部之内。结果,接地361和输入电极362之间的电场线延伸的距离并未长到使信号强度降低或减弱至实质损害阻抗检测的准确度的程度。尽管以上示例描述了接地和电极,但是实施例并不限于此。在一些实施例中,可使用输入高侧电极和输入低侧电极来形成电场线的区域(例如,诸如区域360)。
如图3中所示,输入电极362可位于接近可从其中收集血液的储液器。例如,输入电极362可相对于电接地361位于邻近喷嘴(图2中所示的233-1和/或喷嘴233-2)。类似地,电接地361可相对于输入电极362位于远离喷嘴(图2中所示的233-1和/或喷嘴233-2)。换句话说,传感器(例如,阻抗传感器)可位于邻近喷嘴,并且可至少部分地由于传感器和喷嘴的邻近度而确定血液样本中的凝血阶段。
在一些示例中,电接地361和输入电极362的厚度范围可从100埃(a)至5000a。此外,电接地361和输入电极362之间的距离范围可从2μm至50μm。然而示例并不限于此,并且电极可具有其它厚度并且可比本文所述的距离相隔更大或更小的距离。
当流体通过efr360时,区域360的电场线可至少部分地被流体阻挡,从而使得区域360的电场线可被更改并且行进在流体中的颗粒周围。efr360的电场线由于不得不行进在流体中的颗粒周围而产生的增加的长度可改变(例如,增加)电性阻抗,这可在输入电极362处被检测到。结果,由于流体对efr360的阻挡而产生的阻抗的增加可用作通道中的血液(例如,流体)的凝血阶段的指示符。
在一些示例中,输入电极362和接地361可被置于使得一旦血液开始凝血就可检测到凝血阶段。例如,喷嘴(例如图2中所示的喷嘴233)可位于紧密邻近输入电极362和接地361。当血液(例如,流体)流经通道(例如,图2中所示的通道226)时,喷嘴中的空气接口可使得凝血级联开始。随着血液凝血并且流过输入电极362,接地361和输入电极362之间的电场可改变。例如,粘附的血小板可使得efr360偏转并引起在与粘附的血小板相关联的阈值范围内的阻抗变化。类似地,纤维蛋白丝可使得efr360偏转并引起在与纤维蛋白丝相关联的阈值范围内的阻抗变化。另外,全止血栓子可使得efr360偏转并引起在与全止血栓子相关联的阈值范围内的阻抗变化。
图4示出了根据本公开的、如用微流体芯片检测到的在凝血级联期间阻抗变化的图形表示470。如关于图3所述,随着血液在微流体芯片中的通道内凝血并且流过电极,接地和电极之间的电场可改变。此电场的变化可导致阻抗的变化,这可在一段时间上被监测到。在一些示例中,可基于由传感器检测到的阻抗的变化来确定凝血阶段(例如,凝血级联的阶段)。例如,响应于阻抗在阈值时段(诸如2分钟)期间从第一值变化为不同于(例如,大于)第一值的第二值,可检测到凝血的具体阶段。
例如,在471处,血液样本(例如,图2中所示的流体250)可在微流体芯片(例如,图2中所示的微流体芯片202)内朝向喷嘴(例如,图2中所示的喷嘴233)迁移。随着血液朝向喷嘴迁移,阻抗可维持在未与凝血级联的成分相关联的水平,诸如小于0.4x104欧姆(ω)。换言之,响应于检测到小于0.4x104ω的阻抗水平,传感器可检测到诸如粘附的血小板、聚集的血小板、纤维蛋白丝和/或止血栓子之类的凝血成分的缺失。
在472处,可检测到凝血级联的第一阶段(由图形表示470顶部的罗马数字“i”指示)。例如,靠近喷嘴(例如,图2中所示的喷嘴233)的血小板粘附可产生与血小板粘附相关联的阻抗水平,诸如在0.4x104ω和1.0x104ω之间。在473处,可通过检测到靠近喷嘴的血小板的聚集而进一步确定凝血级联的第一阶段。例如,靠近喷嘴的血小板聚集可产生与聚集的血小板相关联的阻抗水平,诸如在1.0x104ω和1.6x104ω之间。
在474处,可检测到凝血级联的第二阶段(由图形表示470顶部的罗马数字“ii”指示)。例如,靠近喷嘴的纤维蛋白丝的形成和蔓延可产生与形成的纤维蛋白丝相关联的阻抗水平,诸如在1.6x104ω和1.8x104ω之间。
此外,在475处,可检测到凝血级联的第三阶段(由图形表示470顶部的罗马数字“iii”指示)。例如,靠近喷嘴的全止血栓子的形成可产生与形成的止血栓子相关联的阻抗水平,诸如1.8x104ω或更高。尽管本文出于例证的目的提供了阻抗水平,但是本公开的示例并不限于此。凝血级联的每个阶段的阻抗值可大于或小于本文所述的值。
在本公开中,参考附图,附图形成本公开的一部分,并且其中通过图示的方式示出能够如何实践本公开的多个示例。这些示例已经被足够详细地描述,以使本领域技术人员能够实践本公开的示例,并且应当理解,可能能够使用其它示例并且可能能够进行过程、电气和/或结构的改变而不脱离本公开的范围。
本文的附图遵循编号惯例,其中第一位数字对应于附图的编号并且剩余的数字标识附图中的元件或组件。可以能够增加、交换和/或消除在本文的多个附图中示出的元件,以便提供本公开的多种附加示例。此外,在附图中提供的元件的比例和相对大小的目的在于例证本公开的示例,而不应当被认定为具有限制意义。
另外如本文使用的,“一个”或“多个”某一事物可以指代一个或多个这种事物。例如,“多个小工具”可以指一个或多个小工具。此外,如本文所用,“多个”某一事物可指代不止一个这种事物。
上面的说明书、示例和数据提供本公开的方法和应用的描述以及系统和方法的使用。由于可以能够在不脱离本公开的系统和方法的精神和范围的情况下做出多个示例,所以本说明书仅阐述多种可能的示例配置和实现中的一些。
- 还没有人留言评论。精彩留言会获得点赞!