用于搅动至少一种用于HCV测定的液体试剂的设备的制作方法
本公开要求于2013年12月27日提交的PCT/US2013/078036的优先权,其全部内容通过参考的方式并入本文。序列表本申请包括序列表,该序列表已经以ASCII格式通过电子方式提交,并且通过引用将其全部并入本文。所述ASCII副本于2014年12月17日生成,以HCV申请_SL.txt命名,且大小为27字节。
技术领域:
本公开通常涉及流体分析器,更加尤其地涉及用于搅动液体的方法和设备。此外,本公开涉及包括至少两个容器的流体分析器,该容器具有圆角矩形形状且具有容纳液体的空腔,该液体包括至少一种试剂。
背景技术:
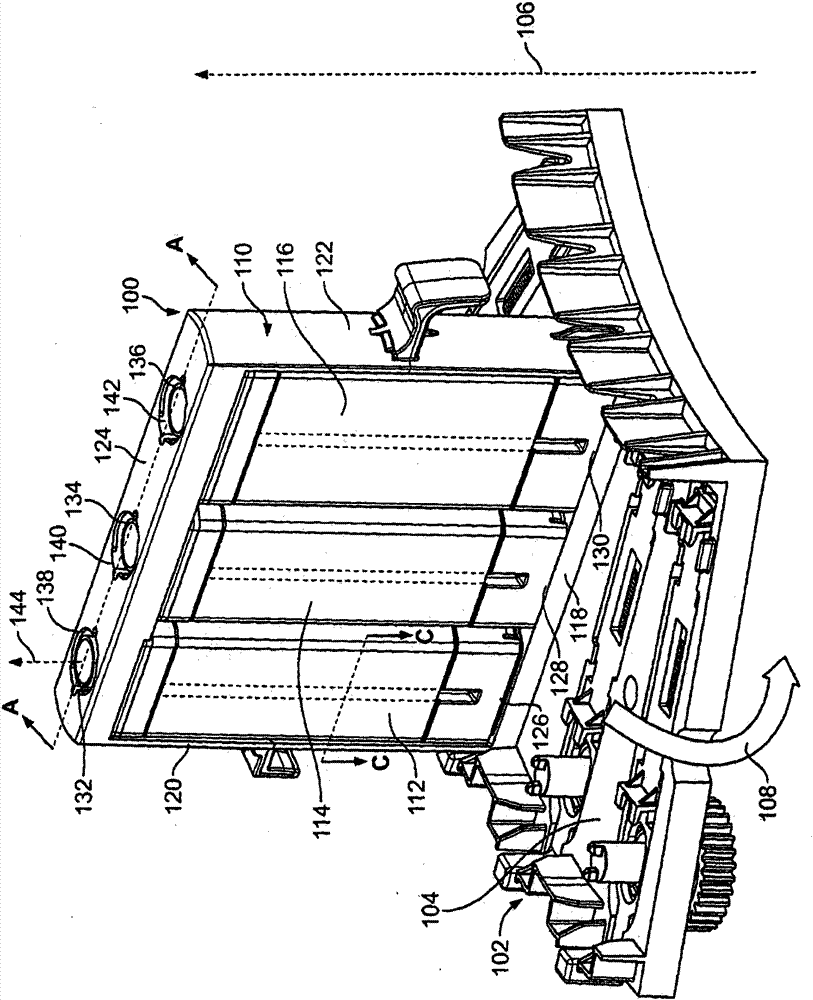
:自动分析器用于分析包括从患者收集的生物材料的样品用于诊断的目的。通常地,样品的分析涉及样品与液体容器中一个或多个试剂发生的反应。一些自动分析器将试剂存储于位于传送带上的容器中。当需要特定试剂时,该传送带进行旋转以将容纳试剂的容器移动至临近的抽吸/分配装置。该传送带通过加速和减速的方式移动,这对试剂施加了旋转力使得微粒分散在试剂中。然而,容器中的部分微粒可能积聚在容器的底部。技术实现要素:定义下列术语与本公开相关:“大约”是指与所述数值大约a+/-10%的变化。我们可以这样理解,所述变化总是包含在本文提供的任何给定数值之内,无论是否对此进行特别说明。“抗体”和“多个抗体”是指单克隆抗体、多特异性抗体、人抗体、人源化抗体(全部或部分人源化)、动物抗体(例如但不限于,鸟(例如,鸭子或鹅)),鲨鱼,鲸鱼,以及哺乳动物,包括非灵长类动物(例如,牛、猪、骆驼、羊驼、马、山羊、兔子、绵羊、仓鼠、豚鼠、猫、狗、大鼠、小鼠,等等)或者非人灵长类动物(例如,猴子、猩猩,等等)、亲和力成熟抗体、重组抗体、嵌合抗体、单链Fv(“scFv”)、单链抗体、单结构域抗体、Fab片段、F(ab’)片段、F(ab’)2片段、二硫键连接的Fv(“sdFv”)、以及抗独特型(“抗Id”)抗体、双结构域抗体、双可变结构域(DVD)或三可变结构域(TVD)抗体(双可变结构域免疫球蛋白以及制备它们的方法描述于Wu,C等人,NatureBiotechnology,25(11):1290-1297(2007)和PCT国际申请2001/058956中,每个文献的内容均通过引用并入本文),和抗体片段,包括以上任意的功能活性的表位结合片段。特别地,抗体包括免疫球蛋白分子和免疫球蛋白分子的免疫活性片段,被称为包含分析物结合位点的分子。免疫球蛋白分子可以是任何类型(例如,IgG、IgE、IgM、IgD、IgA和IgY)、任何类别(例如,IgG1、IgG2、IgG3、IgG4、IgA1和IgA2)或子类。为简单起见,针对分析物的抗体在本文中通常是指或者“抗分析物抗体”或者仅仅是指“分析物抗体”。“亲和力成熟抗体”在本文中是指在一个或多个CDR中具有一个或多个变化的抗体,与不具有所述变化的亲本抗体相比,其产生了抗体对目标抗原的亲和力(例如,KD、kd、或ka)的改进。实例性的亲和力成熟抗体将会具有对于目标抗原的纳摩尔或甚至是皮摩尔的亲和力。本领域已知用于生产亲和力成熟抗体的多种程序,包括已使用生物显示而制备的结合抗体文库的筛选。例如,MARKS等人,BioTechnology,10:779-783(1992)中描述了通过VH和VL结构域替换的亲和力成熟。CDR的随机诱变和/或框架残基描述于Barbas等人,Proc.Nat.Acad.Sci.USA,91:3809-3813(1994)、Schier等人,Gene,169:147-155(1995)、Yelton等人,J.Immunol,155:1994-2004(1995)、Jackson等人,J.Immunol,154(7):3310-3319(1995)、以及Hawkins等人,J.Mol.Biol,226:889-896(1992)中。在选择性诱变位置和与活性增强氨基酸残基接触或高突变位置处的选择性突变描述于美国专利号6,914,128B1中。因此,其亲和力(即KD、kd或ka)已经通过使用生物显示而制备的结合抗体文库的筛选而增加或提高的抗体是指“亲和力成熟抗体”。“抗体片段”、“抗体的抗原活性片段”、以及“多个抗体片段”是指包括抗原结合位点或可变区域的完整抗体的部分。该部分不包括完整抗体的Fc区域的恒定重链结构域(例如,CH2、CH3、或CH4,这取决于抗体同种型)。抗体片段的实例包括,但不限于,Fab片段、Fab’片段、Fab’-SH片段、F(ab’)2片段、Fd片段、Fv片段、双价抗体、单链Fv(scFv)分子、仅包含一个轻链可变结构域的单链多肽、包含轻链可变结构域的三个CDR的单链多肽、仅包含一个重链可变区的单链多肽、以及包含重链可变区的三个CDR的单链多肽。“CDR”在本文中是指在抗体可变序列内的“互补决定区”。在重链和轻链的每个可变区均有三个CDR,其对于每个可变区分别被特定为“CDR1”、“CDR2”和“CDR3”。术语“CDR组”在本文中是指在与抗原结合的单一可变区内发生的一组三个CDR。三个CDR的确切边界已根据不同系统进行不同地定义。由Kabat(Kabat等人,SequencesofProteinsofImmunologicalInterest(NationalInstitutesofHealth,Bethesda,Md.(1987)和(1991)))描述的系统不仅提供了适用于抗体的任何可变区的清晰残基编号系统,还提供了精确的残基边界用于定义三个CDR。所述CDR可以是指“KabatCDR”。Chothia和其同事(Chothia和Lesk,J.Mol.Biol,196:901-917(1987);以及Chothia等人,Nature,342:877-883(1989))发现在KabatCDR内特定的子部分尽管在氨基酸序列的水平上具有很大的不同但却采用了近乎相同的肽骨架构造。所述子部分被特定为“L1”、“L2”和“L3”,或者“H1”、“H2”和“H3”,其中“L”和“H”分别指示轻链和重链区域。所述区域可以被称作“ChothiaCDR”,其边界与KabatCDR重叠。用于定义与KabatCDR重叠的CDR的其他边界描述于由Padlan,FASEBJ.,9:133-139(1995),和MacCallum,J.Mol.Biol.,262(5):732-745(1996)中。还有其他CDR边界定义可能没有严格遵从本文中的任何系统,但其将无疑与KabatCDR重叠,尽管它们可能会根据假设或实验发现而被缩短或加长,所述假设或实验发现是特定残基或残基群或甚至整个CDR没有显著影响抗原结合。尽管特定实施例使用Kabat-或Chothia-定义的CDR,所述方法可利用根据所述这些系统中任意定义的CDR。如本文中所使用的,表达“竞争性测定”是指其中未标记的抗原和标记的抗原竞争与相同的抗体结合的测定。举例,固体支持物上涂覆抗体,所述抗体能特异性地结合标记的抗原或者未标记的抗原。将所述固体支持物、标记的抗原和怀疑包含抗原的患者样品混合在一起。当然,在患者样品中的任何抗原是未标记的。标记的抗原和未标记的抗原竞争位于固体支持物上的抗体位点。仅当标记的抗原附着在位于固体支持物上的抗体时,就会生成信号,这是因为只有标记的抗原能够产生信号。患者样品中的抗原数量与产生的信号数量成反比。本文提供了竞争性测定的其他实例,以及更多的实例是本领域的技术人员所熟知。根据本文描述的方法和本领域中已知的其他方法,“组分”、“多个组分”以及“至少一种成分”,通常是指捕获抗体、检测或缀合抗体、校准物、对照、敏感性实验组、容器、缓冲剂、稀释剂、盐、酶、酶的辅助因子、检测剂、预处理剂/溶液、基质(例如,作为溶液)、停止液以及能够包含在用于实验样品测定的试剂盒中的类似物,如患者尿液、血清或血浆样品。一些组分可以在溶液中或是冻干的用于重构以用于测定。“对照”是指已知不包含目的分析物(“阴性对照”)或包含目的分析物(“阳性对照”)的组合物。阳性对照可包括已知浓度的目的分析物。“对照”、“阳性对照”和“校准物”可在本文中交换地使用以指示包括已知浓度的目的分析物的组合物。“阴性对照”可用于建立测定性能特征,并且它是试剂(例如,分析物)完整性的有用指示器。“由.....编码”是指为多肽序列编码的核酸序列。也包括通过由序列编码成的多肽可进行免疫识别的多肽序列。因此,本文公开的“多肽”、“蛋白”或“氨基酸”序列可以具有与特定的多肽或本文特定的氨基酸序列的至少60%的相似性、至少大约70%的相似性、至少大约80%的相似性、至少大约90%的相似性、至少大约95%的相似性以及至少大约99%的相似性。“表位”、“多个表位”或“目的表位”是指在被识别并能够结合至其特定结合伙伴上的互补位点的任意分子上的位点。该分子和特定结合伙伴是特定结合对的部分。例如,表位可以是多肽、蛋白、半抗原、碳水化合物抗原(如,但不限于,糖脂、糖蛋白或脂多糖)、或多糖。其特定结合伙伴可以是,但不限于,抗体。特定的多肽或蛋白的“片段”是指包括从特定多肽或蛋白衍生出的至少大约5-10、10-20、20-30、30-40、40-50、50-60、60-70、70-80、80-90、100-120、120-150、150-200或200-250个氨基酸的氨基酸序列。“框架”(FR)或“框架序列”在本文中是指可变区减去CDR的序列。因为CDR序列的精确定义可由不同系统确定(例如,参见上面的内容),框架序列的意思受制于相应地不同说明。六个CDR(轻链的CDR-L1、-L2和-L3以及重链的CDR-H1、-H2和-H3)也将在轻链和重链上的框架区域划分为在每个链上的四个子区域(FR1、FR2、FR3和FR4),其中CDR1位于FR1和FR2之间,CDR2位于FR2和FR3之间,并且CDR3位于FR3和FR4之间。在没有将特定子区域指定为FR1、FR2、FR3和FR4的情况下,如由其他指出的框架区域表示在单一、自然发生地免疫球蛋白链的可变区之内组合的FR。如本文中使用的,FR表示四个子区域之一,FR表示构成框架区域的四个子区域中的两个或更多个。本领域已知的人重链和轻链FR序列可被用作重链和轻链“接受者”框架序列(或者简单的说是“接受者”序列)以通过使用本领域已知的技术来人源化非人抗体。在一个实施例中,人重链和轻链接受者序列选自在公众可获得的数据库如V-base(hypertexttransferprotocol://vbase.mrc-cpe.cam.ac.uk/)或国际信息系统((hypertexttransferprotocol://imgt.cines.fr/texts/IMGTrepertoire/LocusGnenes/)列示的框架序列。本文中使用的对于两个或更多个多肽或多核苷酸序列的内容中的“相同”或“同一性”是指该序列具有特定比例的残基在特定区域上是相同的。该比例可通过以下步骤计算得到:以最佳的方式比对两个序列,比较在特定区域上的两个序列,确定在该位置处在两个序列中发生等同的残基的位置的数量以得到匹配位置的数量,将匹配位置的数量除以在特定区域内的位置的总数,并且将结果乘以100以得到序列同一性的百分比。在两个序列具有不同的长度或者比对产生了一个或多个交错末端并且比较的特定区域仅包括单一序列的情况下,那么单一序列的残基包含在计算的分母而非分子中。“分离的”是指材料从其原始环境(例如,如果它是自然发生的,那么就是自然环境)中移除。例如,存在于活的动物中的自然发生的多核苷酸或多肽不是分离的,但是从自然系统中的一些或全部共存材料中分开的相同的多核苷酸或DNA或多肽就是分离的。这样的多核苷酸可以是载体的部分和/或这样的多核苷酸或多肽可以是组合物的部分,并且仍旧被分离,因此所述载体或组合物不是其自然环境的一部分。“标记”和“可检测标记”是指附着至抗体或分析物以使得在抗体和可检测分析物之间的反应可检测的部分,并且这样标记的抗体或分析物是指“可检测标记的”。标记能够产生可通过视觉或有用的装置而可检测的信号。各种标记包括信号生成物质,如色原、荧光化合物、化学发光化合物、放射性化合物等等。标记的代表性实例包括产生光的部分,例如吖啶鎓化合物,和产生荧光的部分,例如荧光素。其他标记在本文中描述。在这点上,部分本身可以不是可检测的,但在与另一部分发生反应而变得可检测。使用术语“可检测标记的”旨在包括所述进行标记。“患者”和“受试者”在本文中可交换地使用以指动物,如鸟(例如,鸭子或鹅),鲨鱼,鲸鱼,以及哺乳动物,包括非灵长类动物(例如,牛、猪、骆驼、羊驼、马、山羊、兔子、绵羊、仓鼠、豚鼠、猫、狗、大鼠和小鼠)和灵长类动物(例如,猴子、猩猩和人)。优选地,患者或受试者是人,如由于疾病或研究条件而怀疑具有目的疾病或病况、诊断具有目的疾病或病况,或正在进行用于目的疾病或病况的预防性或治疗性处理的人。本文中使用的“多核苷酸”是指任何长度的核苷酸的聚合物形式,是核糖核苷酸或脱氧核糖核苷酸。该术语仅仅是指分子的初级结构。因此,该术语包括双链DNA和单链DNA以及双链RNA和单链RNA。它还包括多核苷酸的修饰如甲基化或加帽,以及非修饰形式。“多肽”和“蛋白”在本文中可交换地使用并且表示通过共价键和/或非共价键连接的氨基酸的分子链。该术语不是指产品的特定长度。因此,肽、寡肽和蛋白包含在多肽的定义内。该术语包括多肽的表达后修饰,例如,糖基化、乙酰化、磷酸化等等。此外,片段、类似物、突变的或变体蛋白、融合蛋白等等包含在多肽的意思内。例如,本文中描述的多肽或肽可以具有15至750个氨基酸的长度。“预定的临界”和“预定的水平”通常是指用于通过比较测定结果和预定临界/水平而评估诊断/预后/治疗的功效结果的测定临界值,其中该预定临界/水平已经与各种临床参数(例如,疾病的严重性、进展/非进展/改善,等)相联系或关联。本公开提供了示例性预定水平。然而,我们都知道临界值可根据免疫测定(例如,使用的抗体,等)的性质而变化。它也在本领域的普通技术内以采用本文中的公开用于其他免疫测定,以获得基于本公开的所述其他免疫测定的免疫测定特定临界值。然而,预定临界/水平的精确值可在测定之间发生变化,本文中描述的相关性通常是适用的。在本文描述的诊断性测定中使用的“预处理试剂”,例如,裂解、沉淀和/或增溶试剂是裂解存在于测试样品中的任何细胞和/或增溶存在于测试样品中的任何分析物的试剂。本文还进一步说明,预处理不是对所有样品来说都是必需的。在其他情况下,增溶分析物使得该分析物从存在于样品中的任何内生结合蛋白释放出来。预处理试剂可以是同质的(不需要分离步骤)或者异质的(需要分离步骤)。通过使用同质预处理试剂,在进行测定的下一步骤程序之前,从测试样品中去除任何沉淀的分析物结合蛋白。该预处理试剂任选地包括:(a)一个或多个溶剂和盐;(b)一个或多个溶剂、盐和去垢剂;(c)去垢剂;(d)去垢剂和盐,或(e)适用于细胞裂解和/或分析物增溶的任何试剂或试剂的组合。“纯化的多肽”是指目的多肽或其片段基本上不含细胞组分,即,其包含少于大约50%,优选地少于大约70%,并且更加优选地,少于大约90%的细胞组分,目的多肽与所述细胞组分是自然地相关联的。纯化的方法在本领域是已知的。在本文描述的免疫测定和试剂盒的内容中的“质量控制试剂”包括但不限于校准物、对照和敏感性实验组。典型地,使用“校准物”或“标准”(例如,一个或多个,如很多个)是为了建立校准(标准)曲线用于解释如抗体或分析物的分析物的浓度。任选地,可以使用在预定正/负临界附近的单一校准物。多校准物(例如,多于一个的校准物或可变数量的校准物)可以联合使用以包括“敏感性实验组”。“重组抗体”和“多个重组抗体”是指通过一个或多个步骤制备的抗体,包括通过重组技术将编码一个或多个单克隆抗体的全部或部分的核酸序列克隆如何是的表达载体,并随后在何是的宿主细胞中表达抗体。该术语包括但不限于重组产生的单克隆抗体、嵌合抗体、人源化抗体(全部或部分人源化)、由抗体片段形成的多特性或多价结构、双功能抗体、复共轭对配合物Ab、和本文中描述的其他抗体(双可变结构域免疫球蛋白及其制作方法描述于由Wu,C等人,NatureBiotechnology,25:1290-1297(2007)中)。本文中使用的术语“双功能抗体”是指包括具有用于一个抗原位点的特异性的第一臂和具有用于不同抗原位点特异性的第二臂的抗体,即,该双功能抗体具有双重特异性,。“重组宿主细胞”、“宿主细胞”、“细胞”、“细胞系”、“细胞培养物”和其他表示微生物或作为单细胞实体培养的更高级别真核细胞系的这类术语是指这样的细胞,其能够用作,或已经用作重组载体或其他转染的DNA的接受者,并且包括已转染的原始细胞的原始子代。在本文中交换使用的“重组多肽”或“重组蛋白”描述了这样一种多肽,根据其来源或做作是其与在自然中与其相关联的多肽的全部或部分是不相关的,和/或与除了其在自然中联系的多肽以外的多肽相联系。重组或编码的多肽或蛋白不是非要从设计的核酸序列翻译而来。它还可以以任何形式生成,包括化学合成(合成肽)或重组表达系统的表达。“复制子”是指如质粒、染色体或病毒的任何遗传元件,其表现出如同细胞内多核苷酸复制的自发单元。“样品”、“测试样品”和“患者样品”可以在本文中交换使用。样品,例如尿、血清、血浆、羊水、脑脊髓液、胎盘细胞或组织、内皮细胞、白细胞或单核细胞的样品可以如从患者获得地直接使用,或者可预处理,如通过过滤、稀释、提取、浓缩、离心、对干扰组分进行灭活、增加试剂等等,从而以本文中讨论的或其他本领域已知的一些方式来修饰样品的特性。在本公开的上下文中,样品优选地是血清或血浆,并且最优选地是血清。“固相”或“固体支持物”是指任何不溶的或者可通过后来的反应变得不溶的材料。就其吸引和固定化捕获剂的本身固有的能力而选择固相。任选地,所述固相具有在其上粘附的连接剂,该连接剂具有吸引和固定化捕获剂的能力。例如,连接剂可包括带电物质,其根据捕获剂本身或根据与捕获剂缀合的带电物质而带相反电荷。总之,连接剂可以是任何结合伙伴(优选地异性的),该结合伙伴固定化(附着)在固相上并且具有通过结合反应来固定化捕获剂的能力。连接剂使得捕获剂在性质测定之前或性质测定期间间接地与固相材料结合。固相可以是,例如,塑料、衍生塑料、磁性或非磁性金属、玻璃或硅,包括,例如,试管、微量滴定孔、薄片、珠、微粒、芯片和在本领域的普通技术中已知的其他构造。“特异性结合伙伴”是特异性结合对的成员。特异性结合对包括两个不同的分子,其通过化学或物理方式彼此特异性结合。因此,除了普通免疫测定的抗原和抗体特异性结合对,其他特异性结合对可包括生物素和亲和素(或者链霉亲和素)、碳水化合物和外源凝集素、互补核苷酸序列、效应子和接受子分子、辅酶因子和酶、酶和酶抑制剂,等等。进一步,特异性结合对可包括是原始特异性结合成员的类似物的成员,例如,分析物-类似物。免疫反应特异性结合成员包成员括抗原、抗原片段和抗体,包括单克隆和多克隆抗体,以及复合物和其片段,无论是否分离或重组生成的。在特异性结合对的成员(例如,抗原(或其片段))和抗体(或其抗原反应性片段),以及结合蛋白(或其片段)之间相互作用的内容中的“特异性的”和“特异性”是指相互作用的选择性反应。词组“特别地结合至”和类似物词组是指特异性结合对的第一成员(例如,抗体或其抗原反应片段)与特异性结合对的第二成员(例如,抗原)结合,而不特异性结合其他抗原(或其片段)的能力。本文中使用的“合成肽”是指任何长度的氨基酸的聚合形式,其可通过本领域的技术人员已知的方法进行化学合成。所述合成肽在多种应用中都是有用的。本文中使用的“变体”是指这样的多肽,其通过插入、删除或保守性置换氨基酸而在氨基酸序列方面不同于给定多肽,但保留了已知给定多肽的生物活性。氨基酸的保守性置换,即用相似属性(例如,亲水性以及带电区域的程度以及分布)的不同氨基酸置换一个氨基酸,在本领域中被认为作为一般涉及微小变化。如本领域中熟知的(参见,例如,Kyte等人,J.Mol.Biol.157:105-132(1982)),这些微小变化部分地可通过考虑氨基酸的亲水指数而鉴定。氨基酸的亲水指数基于其亲水性和电荷的考虑。如本领域所熟知的,具有相似亲水指数的氨基酸可进行替换并且仍旧保留蛋白的功能。在一方面,具有亲水指数为±2的氨基酸可进行替换。氨基酸的亲水性也可用于显示产生保留生物功能的蛋白的替换。在涉及肽的内容中考虑氨基酸的亲水性允许计算所述肽的最大当地平均亲水性,已经报道了一种有用的措施以使得抗原性和免疫原性很好的相关联(参见,例如,美国专利号US4,554,101,其通过参考的形式合并于并入本文)。正如本领域已知的,具有相似亲水性的氨基酸的替换得到保留生物学活性的肽,例如免疫原性。在一方面,使用彼此具有亲水值在±2之内的氨基酸进行替换。氨基酸的疏水指数和亲水性值受到所述氨基酸的具体侧链的影响。与观察相一致,生物学功能相容的氨基酸替换理解为取决于氨基酸的相对相似性,并且尤其是所述氨基酸的侧链,这通过疏水性、亲水性、电荷、尺寸和其他特性得以揭示。“变体”也可用来指作抗体的抗原反应性片段,其在氨基酸序列方面不同于抗体的相应片段,但是仍旧是抗原反应性的并且可与抗体的相应片段竞争,该抗体与目的分析物结合。“变体”也可用于描述通过如蛋白水解、磷酸化作用,或其他翻译后修饰而已经进行不同处理,但仍旧保持其抗原反应性的多肽或其片段,。“载体”是复制子,另一多核苷酸部分附着在其上,以产生附着区段的复制和/或表达。设备本文公开的是用于搅动液体,如,例如自动诊断分析器的容器中的液体试剂的方法和设备,所述自动诊断分析器可以是,例如,临床化学分析器、免疫测定分析器、和/或血液分析器。用于自动诊断分析器中的部分试剂包括液体和微粒,其中所述微粒是混合的,并且在一些实施例中,基本上均匀地分散在液体中。自动诊断分析器典型地围绕轴旋转试剂容器或瓶子并且旋转在容器的内含物上施加力以混合所述内含物。传统的试剂瓶是圆柱形的并且包括内部叶片,该叶片用于混合并分散试剂液体中的颗粒。本文公开的实例使用矩形、圆角矩形或基本上呈矩形形状的试剂容器。所述容器具有容纳至少一种液体试剂的空腔。本文公开的实施例获得试剂的均匀混合和分散,如,例如,包括微粒的试剂。所述公开的实施例提供了比很多已知构造在诊断系统中更大的空间利用。因此,使用本文描述的实施例,与很多已知的系统相比,分析器可具有增加的负荷容量和/或更小的尺寸。在一些实施例中,所述容器或瓶子中的一个是大约20毫米(mm)深,大约36mm宽以及大约92mm高。其他实施例可能具有其他尺寸。所述公开实施例的另一优势是实施例瓶子可利用制造技术,如,例如,吹塑技术而生成,这样与很多已知构造的制造技术相比,可减少成本。在本文公开的实施例中,实施例瓶子的平的反面响应瓶子的加速和减速而在瓶子的液体中生成了混合运动。本文公开的实施例瓶以振动的方式在其中心纵轴周围进行旋转。此外,所述瓶子连接至套筒,所述套筒在传送带的转轴周围旋转。如本文所公开的,所述瓶子和帽包括特征,其提供支持物面用于旋转瓶子。所述瓶子可由一种材料或多种材料构成以使得瓶子的一个或多个表面作为舍弃式轴承一样发挥效用。在一些实施例中,所述瓶子可由高密度聚乙烯构成,其具有良好的耐磨特性并且能够经受,例如,30天的机载使用期(例如,在诊断分析器上连续使用),只有微不足道的磨损。加速和减速以及矩形壁在瓶中的液体上施加力以促进瓶中内含物的混合。瓶子内的圆形或曲线型底部也可通过生成由于沉淀而积聚在瓶子底部的颗粒向上的运动来帮助混合,当瓶子处于静止状态时会有沉降的发生。更加特别地,通过瓶子的旋转生成的离心力使得所述沉降的颗粒移出瓶子的底部中心,并且在颗粒随着瓶子底部的轮廓时提升颗粒。在一些实施例中,在大约振动一分钟内从视觉上确认均匀混合。其他混合周期和振动频率可根据所用的试剂、所用的微粒、进行的诊断测试和/或其他因素被使用。本文公开的是包括基座、第一端壁和第二端壁的实施例设备。所述实施例设备还包括第一容器和第二容器,所述第一容器和第二容器具有圆角矩形剖面状并且形成圆角矩形块,例如,具有圆角边缘的条状物体(总体地是指呈圆角矩形形状)。此外,实施例设备包括第一容器支持物用于保持第一容器。所述实施例第一容器支持物包括第一杆用于啮合第一容器的第一边缘从而非旋转地将第一容器连接至基座。同样的,实施例设备还包括第二容器支持物用于保持第二容器。所述实施例第二容器支持物包括用于啮合第二容器的凹槽和圈以及用于啮合第二容器的第二边缘的脊。所述实施例第二容器相对于基座进行选择性旋转。在一些实施例中,实施例设备还包括第三容器支持物用于保持第三容器。所述实施例第三容器支持物包括第二杆用于啮合第三容器的第三边缘从而非旋转地将第三容器连接至基座。在一些实施例中,设备在旋转的第一轴周围进行旋转,同时第二容器相对于基座在旋转的第二轴周围进行旋转。在一些实施例中,第二容器在锁紧位置和非锁紧位置之间移动,在所述锁紧位置处第二容器的第二边缘与脊进行啮合从而非旋转地将第二容器连接至基座,在非锁紧位置处第二容器被提高使得第二边缘与脊脱离,同时凹槽在圈周围旋转。在一些实施例中,所述设备包括具有进入第一容器的第一孔和进入第二容器的第二孔的盖子。同样的,本文公开了包括第一侧壁和基本上平行于第一侧壁的第二侧壁的实施例设备。所述实施例设备还包括连接至第一侧壁和第二侧壁上的顶壁。所述实施例设备还包括与顶壁相对的底壁并且该底壁连接至第一侧壁和第二侧壁上。所述底壁具有第一侧面用于限定容纳液体的空腔。所述实施例设备还包括从底壁的第一侧面朝向顶壁延伸的突出。在一些实施例中,所述突出位于底壁的中心。同样地,在一些实施例中,所述突出位于底壁的旋转轴上。此外,在一些实施例中,所述突出具有沿底壁的旋转轴放置的尖端。在一些实施例中,所述实施例设备包括第三侧壁和与第三侧壁相对的第四侧壁。在这样的实施例中,所述第三侧壁和第四侧壁是弯曲的。在一些实施例中,底壁具有第一弯曲半径,并且突出具有不同于第一弯曲半径的第二弯曲半径。在一些实施例中,第一弯曲半径定向于第一方向并且第二弯曲半径定向于不同于第一方向的第二方向。在一些实施例中,所述第一侧壁包括向第二侧壁延伸的肋。同样地,在一些实施例中,设备包括依靠于底壁的第一侧的杆。在这样的实施例中,所述突出从底壁的第二侧延伸。在一些实施例中,所述杆限定了很多槽口。同样地,在一些实施例中,所述槽口是与旋转装置可啮合的从而在与凹部对齐的旋转轴周围旋转设备,即,与凹部的中心轴共轴。在一些实施例中,第一侧壁包括第一平面部分并且第二侧壁包括第二平面部分。此外,在一些实施例中,所述实施例设备包括第三侧壁和与第三侧壁相对的第四侧壁。在这样的实施例中,第一侧壁、第二侧壁、第三侧壁或第四侧壁的至少两个包括边缘用于啮合载体上的脊从而在非旋转位置容纳所述容器。本文还公开的是实施例方法,该方法包括将第一容器从第一位置提升至第二位置,在所述第一位置中第一容器的边缘与运载器的脊啮合并且第一容器的凹槽与运载器的圈啮合,在所述第二方向中所述边缘从所述脊脱离而所述凹槽与所述圈啮合。所述实施例方法还包括在旋转轴的周围旋转第一容器,并混合第一容器的内含物。在这样的实施例中,所述内含物通过第一容器的第一基本上平的侧壁和第一容器的底部突出而混合。在一些实施例中,所述实施例方法包括非旋转支持运载器上的第二容器同时旋转第一容器。此外,在一些实施例中,所述实施例方法包括降低第一容器至第一位置从而非旋转地将第一容器连接至运载器。试剂本文公开的设备包括至少第一容器和第二容器。任选地,该设备可包括第三容器。每种容器可呈圆角矩形形状。第一和第二容器,以及任选地,如果存在的话,第三容器,各包括容纳液体的空腔。在每个容器中的液体可包含许多试剂。该容器包括用于确定存在于测试样品中的丙型肝炎病毒(HCV)抗体和/或HCV抗原的存在、数量和/或浓度所需的试剂。在本领域中已知的任何合适的测定可用于此方法。实例包括,但不限于,免疫测定,如,例如,单克隆-多克隆或单克隆-单克隆或抗原-抗原、夹心免疫测定、放射性同位素检测测定(放射免疫分析(RIA))和酶检测测定(酶免疫分析(EIA)或酶联免疫吸附测定(ELISA))、竞争抑制免疫测定(例如,正向和反向)、荧光偏振免疫测定(FPIA)、酶倍增免疫测定技术(EMIT)、生物发光共振能量转移测定(BRET)、以及均相化学发光测定等等。在一个实施例中,该液体试剂是一个或多个特异结合伙伴,其中该特异结合伙伴特异地结合包含在测试样品中的任何抗HCV抗体和/或HCV抗原。例如,特异性结合伙伴可以是特异地结合测试样品中的任何HCV抗原的一个或多个抗体和/或,特异性结合伙伴可以是特异地结合测试样品中的任何HCV抗体的一个或多个蛋白、多肽或其片段(如分离的多肽、纯化的多肽、合成肽或重组多肽或重组蛋白)。捕获测试样品中的HCV抗原的特异结合伙伴被称为“捕获剂”,例如“捕获抗体”。捕获测试样品中的抗HCV抗体的特异性结合伙伴被称为“捕获剂”,例如“捕获抗原”。检测测试样品中的HCV抗原的特异性结合伙伴被称为“检测剂”,例如“缀合物”。检测测试样品中的抗HCV抗体的特异性结合伙伴被称为“检测剂”,例如“缀合物”。可用于本发明的一个或多个容器中(如第一容器、第二容器、第三容器等)的一种或多种捕获剂和一种或多种检测剂可衍生在NCBI参考序号M67463获得的HCVI蛋白,下面的表1提供了该序列。表1:全长HCVI蛋白(NCBI参考序列号M67463)下面的表格2提供了上述表1(SEQIDNO:1)中示出的HCVI的各种结构域表2:HCVI结构域NS4ASEQIDNO:1的氨基酸1658-1711NS4BSEQIDNO:1的氨基酸1712-1972NS5ASEQIDNO:1的氨基酸1973-2420NS5BSEQIDNO:1的氨基酸2421-3011在一个实施例中,下面的表3提供了可用于本发明的一个或多个容器中(如第一容器、第二容器、第三容器等)的一种或多种捕获剂和一种或多种检测剂。表3:捕获剂和检测剂确定测试样品中抗HCV抗体和/或HCV抗原的存在、数量或浓度的方法本公开提供了用于确定测试样品中存在的HCV抗体和/或HCV抗原的存在、数量和/或浓度的方法。在本领域中已知的任何合适的测定可用于此方法。实例包括,但不限于,免疫测定,如,例如,单克隆-多克隆或单克隆-单克隆或抗原-抗原、夹心免疫测定、放射性同位素检测测定(放射免疫分析(RIA))和酶检测测定(酶免疫分析(EIA)或酶联免疫吸附测定(ELISA))、竞争抑制免疫测定(例如,正向和反向)、荧光偏振免疫测定(FPIA)、酶倍增免疫测定技术(EMIT)、生物发光共振能量转移测定(BRET)、以及均相化学发光测定等。在SELDI为基础的免疫测定中,捕获剂(试剂)附着在质谱探针的表面上,如预激活蛋白芯片阵列。分析物(例如,抗HCV抗体和/或HCV抗原)然后被特异性地捕获在生物芯片上,并且该捕获(例如,抗HCV抗体和/或HCV抗原)由质谱检测出来。可替代地,抗HCV抗体和/或HCV抗原可从捕获剂中洗脱出来,并且通过传统的MALDI(基质辅助的激光解吸离子化质谱技术)或SELDI进行检测。化学发光微粒免疫测定,特别是使用自动分析器(AbbottLaboratories,ABBOTTPark,IL),是优选的免疫测定的实例,尽管可以使用如本文所述的抗体进行其他测定和工具。临床化学也可用于本公开的内容。临床化学涉及通过利用多种技术来分析体液,如,血液、尿液、脑脊髓液(CSF)、积液,以及粪便,或者任何前述的组分,所述技术包括从简单化学分析技术(例如,肝脏功能和肾脏功能)到使用且测量酶活性,分光光度测定法,以及电泳。临床化学也包括内分泌学、毒理学以及治疗性药物监测。临床化学进一步可包括仅使用单一抗体、浊度测定以及颗粒加强的浊度测定,本领域的技术人员所熟知的其他形式。本领域已知的用于收集、处理和加工体液,如,尿液、血液、血清和血浆等以及其他体液的方法用于本公开的实际操作中,例如,当根据本公开的抗体用作免疫诊断试剂,和/或用在抗HCV抗体和/或HCV抗原的免疫测定的试剂盒中时。测试样品还包括除了目的分析物之外的部分,如抗体、抗原、半抗原、激素、药物、酶、受体、蛋白、肽、多肽、寡核苷酸或多核苷酸。例如,所述样品可以是从受试者获得的全血液样品。必要的或者期望的是,测试样品,尤其是全血,在进行本文描述的免疫测定之前被处理,例如,用预处理试剂处理。即使预处理是不必要的(例如,大多数尿液样品)情况下,仅仅为了方便,可选择进行预处理(例如,关于商业平台的部分规则)。任选地,所述测试样品是血清。预处理试剂可以是适合用于本发明的免疫测定和试剂盒的任何试剂。预处理任选地包括:(a)一种或多种溶剂(例如,甲醇和乙二醇)和盐;(b)一种或多种溶剂、盐和去垢剂;(c)去垢剂,或者(d)去垢剂和盐。预处理试剂在本领域中是已知的,并且可采用这种预处理,例如,如文献中所述的(参见,例如,Yatscoff等人,AbbottTDxMonoclonalAntibodyAssayEvaluatedforMeasuringCyclosporineinWholeBlood,Clin.Chem.36:1969-1973(1990)和Wallemacq等人,EvaluationoftheNewAxSYMCyclosporineAssay:ComparisonwithTDxMonoclonalWholeBloodandEMITCyclosporineAssays,Clin.Chem.45:432-435(1999))用于AbbottTDx,和分析器(Abbott实验室,AbbottPark,IL)的测定,和/或市场上可得到的。此外,可以如Abbott的美国专利号US5,135,875、欧洲专利公开号0471293,以及美国专利US7,993,851、8,329,415和7,883,855(通过引用将其涉及预处理的教导的全部内容并入本文)中描述的进行预处理。预处理试剂可以是异质剂或同质剂。使用异质预处理试剂时,预处理试剂使存在于样品中的分析物结合蛋白沉淀。这样的预处理步骤包括:通过从沉淀的分析物结合蛋白中分离通过向样品中添加预处理试剂而形成混合物的上层清液,而去除任何分析物结合蛋白。在这种测定中,缺少任何结合蛋白的混合物的上层清液用于测定,直接进入抗体捕获步骤。如果使用同质预处理试剂,那么就不存在分离步骤。测试样品的整个混合物和预处理试剂与用于抗HCV抗体和/或HCV抗原的标记的特异性结合伙伴接触。在由第一特异性结合伙伴捕获之前或者期间,这种测定所采用的预处理试剂通常稀释在预处理测试样品混合物中。尽管这样稀释,在捕获期间,一定数量的预处理试剂(例如,在使用有机试剂的情况下,会有5M甲醇和/或0.6M乙二醇)仍然存在(或保留)于测试样品混合物中。在异质形式中,从受试者获得测试样品之后,制备第一混合物。所述混合物包含用于评估抗HCV抗体和/或HCV抗原的测试样品以及一种或多种第一特异性结合伙伴,其中,第一特异性结合伙伴和包含在测试样品中的任何抗HCV抗体和/或HCV抗原形成了第一特异性结合伙伴-抗-HCV抗体复合物和/或第一特异性结合伙伴-HCV抗原复合物。第一特异性结合伙伴可以是特异性地结合测试样品中的任何HCV抗原的抗体和/或,第一特异性结合伙伴可以是特异性地结合测试样品中的任何HCV抗体的蛋白、多肽或其片段(如分离的多肽、纯化的多肽、合成肽或重组多肽或重组蛋白)。添加测试样品和第一特异性结合伙伴以形成混合物的顺序不是关键的。任选地,第一特异性结合伙伴固定化在固相上。用于免疫测定(用于第一特异性结合伙伴和,任选地,第二特异性结合伙伴)的固相可以是本领域中已知的任何固相,如,但不限于,磁性颗粒、珠、试管、微量滴定板、小玻璃管、膜、支架分子、薄膜、滤纸、盘和芯片。在含有第一特异性结合伙伴-抗-HCV抗体复合物和/或第一特异性结合伙伴-HCV抗原复合物的混合物形成之后,使用本领域中已知的任何技术去除任何未结合的抗-HCV抗体和/或HCV抗原。例如,未结合的抗-HCV抗体和/或HCV抗原可通过洗涤被去除。理想地,然而,第一特异性结合伙伴存以过量于测试样品中任何抗-HCV抗体和/或HCV抗原而存着,这样存在于测试样品中的所有抗-HCV抗体和/或HCV抗原被第一特异性结合伙伴结合。在去除任何未结合的抗-HCV抗体和/或HCV抗原之后,将第二特异性结合伙伴添加至混合物以形成第一特异性结合伙伴-抗-HCV抗体-第二特异性结合伙伴复合物和/或第一特异性结合伙伴-HCV抗原-第二特异性结合伙伴复合物。任选地,第二特异性结合伙伴是特异性地结合目的分析物上的表位的抗体,所述表位不同于被第一特异性结合伙伴结合的目的分析物上的表位,和/或第二特异性结合伙伴是特异性地结合样品中的抗-HCV抗体的蛋白、多肽或其片段(如分离的多肽、纯化的多肽、合成肽或重组多肽或重组蛋白)。因此,同样任选地,第二特异性结合伙伴使用上述可检测标记进行标记或包含上述可检测标记。可以使用本领域中已知的任何合适的可检测标记。例如,可检测标记可以是放射性标记(如3H、125I、35S、14C、32P和33P)、酶标记(如生物素、辣根过氧化物酶、碱性磷酸酶、葡萄糖6-磷酸脱氢酶,等等)、化学发光标记(如吖啶鎓醚、硫酯、或者磺胺药物;鲁米诺、异鲁米诺、phenanthridiniumester,等等)、荧光标记(如荧光素(例如,5-荧光素、6-羧基荧光素、3’6-羧基荧光素、5(6)-羧基荧光素、6-六氯-荧光素、6-四氯荧光素、荧光素异硫氰酸盐,等等))、罗丹明、藻胆蛋白、R-藻红素、量子点(例如,锌硫化物加帽的硒化镉)、热标记、或者免疫-聚合酶链反应标记。关于标记、加标记的步骤和标记的检测的介绍可参见Polak和VanNoorden,IntroductiontoImmunocytochemistry,第二编,SpringVerlag,N.Y.(1997)和Haugland,HandbookofFluorescentProbesandResearchChemicals(1996),其是由MolecularProbes,Inc.,Eugene,Oregon出版的合并手册和目录。荧光标记可用于FPIA(参见,例如,美国专利号5,593,896、5,573,904、5,496,925、5,359,093和5,352,803,通过引用将其整体并入本文)。吖啶鎓化合物在均相化学发光测定中可作为可检测标记使用(参见,例如,Adamczyk等人,Bioorg.Med.Chem.Lett.16:1324-1328(2006);Adamczyk等人,Bioorg.Med.Chem.Lett.4:2313-2317(2004);Adamczyk等人,Bioorg.Med.Chem.Lett.14:3917-3921(2004)和Adamczyk等人,Org.Lett.5:3779-3782(2003))。化学发光测定可根据由Adamczyk等人,Anal.Chim.Acta579(1):61-67(2006)中描述的方法进行。当可使用任何合适的测定形式时,微孔板块化学发光计量仪(MithrasLB-940,BertholdTechnologiesU.S.A.,LLC,OakRidge,TN)使得迅速测定小体积的多个样品。化学发光计量仪可通过使用96-孔黑色聚乙烯微孔板(Costar#3792)而装备有多个试剂注射器。每个样品可被添加至分别的孔,接着根据所用测定的类型所确定的,同时添加/按次序添加其他试剂。理想地,在使用吖啶鎓芳基酯的中性或碱性溶液中形成pseudobases是可避免的,如通过酸化。然后通过孔-孔的方式记录化学发光响应。这点上,记录化学发光应答的时间将部分取决于添加试剂和所使用颗粒吖啶鎓之间的延迟。添加测试样品和特异性结合伙伴以形成用于化学发光测定的混合物的顺序不是关键的。如果用吖啶鎓化合物对第一特异性结合伙伴进行可检测地标记,那么形式可检测标记的第一特异性结合伙伴-分析物(抗原或抗体)复合物。可替代地,如果使用第二特异性结合伙伴,并且用吖啶鎓化合物对第二特异性结合伙伴进行可检测地标记,那么形成可检测标记的第一特异性结合伙伴-分析物(抗原或抗体)-第二特异性结合伙伴的复合物。任何未结合的特异性结合伙伴,无论标记的或未标记的,可以通过使用本领域已知的任何技术,如通过洗涤,从混合物中去除。在添加上述吖啶鎓化合物之前、同时、或之后,过氧化氢可在混合物的原位生成或者提供或供应给混合物。过氧化氢可以以对本领域的技术人员来说显而易见的很多方式在原位生成。可替代的,过氧化氢的源可以简单地添加至混合物。例如,过氧化氢的源可以是已知包含有过氧化氢的一种或多种缓冲液或其他溶液。在这点上,可以简单地添加过氧化氢溶液。当向样品中同时或相继添加至少一种碱性溶液时,产生可检测信号,即化学发光信号,指示抗-HCV抗体和/或HCV抗原的存在。碱性溶液包含至少一种碱,并且pH大于或等于10,优选地,大于或等于12。碱性溶液的实例包括,但不限于,氢氧化钠、氢氧化钾、氢氧化钙、氢氧化铵、氢氧化锰、碳酸钠、碳酸氢钠、氢氧化钙、碳酸钙和碳酸氢钙。添加至样品的碱性溶液的量取决于碱性溶液的浓度。根据所用的碱性溶液的浓度,本领域的技术人员可以容易地确定添加至样品中的碱性溶液的量。可通过使用本领域技术人员已知的常规技术检测生成的化学发光信号。根据生成信号的强度,可定量样品中抗-HCV抗体和/或HCV抗原的量。特别地,样品中抗-HCV抗体和/或HCV抗原的量与生成信号的强度成比例。可通过将生成的光的量与抗-HCV抗体和/或HCV抗原的标准曲线比较或与参考标准比较而定量存在的抗-HCV抗体和/或HCV抗原的量。标准曲线可通过质谱、重量分析法和其他本领域已知的其他技术,通过使用抗-HCV抗体和/或HCV抗原的连续稀释或已知浓度的溶液而生成。抗-HCV抗体和/或HCV抗原免疫测定通常可通过使用本领域已知的任何形式来进行,所述形式如,但不限于,夹心形式。特别地,在一种形式中,特异性地结合HCV抗原的抗体用于确定样品中HCV抗原的总量。更加特别地,抗体结合HCV抗原结合形成免疫复合物,这被称为彼此“夹心”。通常地,用于捕获测试样品中的HCV抗原的抗体被称为“捕获剂”,例如“捕获抗体”。用于将可检测和可定量的标记结合在夹心上的抗体被称为“检测剂”,例如“检测抗体”或“缀合物”。在另一形式中,特异性地结合抗-HCV抗体的蛋白、多肽或其片段(如分离的多肽、纯化的多肽、合成肽或重组多肽或重组蛋白)用于确定样品中HCV抗体的总量。更加特别地,蛋白多肽或其片段结合HCV抗体而形成免疫复合物,这被称为彼此“夹心”。通常地,用于捕获测试样品中抗-HCV抗体的蛋白多肽或其片段被称为“捕获剂”,例如“捕获蛋白/肽/多肽”。用于将可检测和可定量的标记与夹心结合的蛋白多肽或其片段被称为“检测剂”,例如“检测蛋白/肽/多肽”或“缀合物”。一般地说,用于(例如,怀疑含有)抗-HCV抗体和/或HCV抗原的在测试样品可与至少一种捕获剂(例如,抗体和/或蛋白多肽或其片段)和至少一种检测剂(例如,分别是抗体和/或蛋白多肽或其片段)同时或者相继并且以任何的顺序相接触。例如,测试样品可以首先接触至少一种捕获剂,然后(相继)接触至少一种检测剂。可替代地,测试样品可以首先接触至少一种检测剂,然后(相继)接触至少一种捕获剂。在另一替代中,测试样品可与捕获剂和检测剂同时接触。在夹心测定的形式中,怀疑含有抗-HCV抗体和/或HCV抗原的样品首先在允许形成捕获剂/抗-HCV抗体复合物和/或捕获剂/HCV抗原复合物的条件下与至少一种捕获剂接触。如果使用了多于一种的捕获剂,那么就会形成多重捕获剂/抗-HCV抗体复合物和/或多重捕获剂/HCV抗原复合物。在夹心测定中,以样品中预期的抗-HCV抗体和/或HCV抗原的最大量的摩尔过量使用捕获剂。例如,可使用每毫升大约5μg至大约1mg捕获剂的缓冲液(例如,微粒涂覆缓冲液)。竞争抑制免疫测定经常用于测量小分析物,这是因为需要仅通过一个抗体的结合,所述竞争抑制免疫测定包括相继和经典形式。在相继的竞争抑制免疫测定中,将针对目的分析物的捕获单克隆抗体和/或捕获蛋白多肽或其片段涂覆或捕获在微量滴定板的孔上。当含有目的分析物的样品被添加至孔中时,目的分析物结合涂覆的或捕获的单克隆抗体和/或捕获的蛋白多肽或其片段结合。洗涤之后,将已知量的标记的(例如,生物素或辣根过氧化物酶(HRP))分析物添加至孔中。用于酶标记的底物是产生信号所必须的。用于HRP的合适底物的实施例是3,3’,5,5’-四甲基联苯胺(TMB)或分子邻苯二胺盐酸盐(OPD)。洗涤之后,测量由标记的分析物生成的信号,并且与样品中分析物的量成反比。在经典的竞争抑制免疫测定中,将针对目的分析物的单克隆抗体和/或蛋白多肽或其片段涂覆或捕获在微量滴定板的孔上。然而,不同于相继竞争抑制免疫测定,同时将样品和标记的分析物添加至孔。样品中的任何分析物与标记的分析物竞争结合捕获的单克隆抗体和/或捕获的蛋白/肽/多肽。洗涤之后,测量由标记的分析物生成的信号,并且该信号与样品中分析物的量成反比。可替代地,捕获剂可与微量结合,其事前被涂覆链酶亲和素或生物素(例如,使用Power-BindTM-SA-MP链酶亲和素涂覆的微量滴定板(Seradyn,Indianapolis,IN))或抗-种类-特异单克隆抗体。如果需要,底物可以被衍生以允许与捕获剂上的各种官能团发生反应。这种衍生需要使用特定的连接剂,其实例包括,但不限于,马来酸酐、N-羟基琥珀酰亚胺和1-乙基-3-(3-二甲氨基丙基)碳化二亚胺。在测试样品用于测定抗-HCV抗体和/或HCV抗原之后,将其与至少一种捕获剂(例如,第一捕获抗体)接触,孵育混合物以使得形成第一捕获(或多重捕获)剂/抗-HCV抗体复合物和/或第一捕获(或多重捕获)剂/HCV抗原复合物。如果将测试样品与多于一个的捕获剂接触,那么会形成多重捕获剂/抗-HCV复合物和/或多重捕获剂/HCV抗原复合物。孵育可在pH为大约4.5至大约10.0,温度为大约2℃至大约45℃,时间为至少大约为一(1)分钟至大约十八(18)分钟,优选地大约1分钟至大约24分钟,最优选地大约4分钟至大约18分钟的条件下进行。本文所述的免疫测定可在一步(是指测试样品、至少一种捕获抗体和至少一种检测抗体和/或测试样品,至少一种捕获蛋白/肽/多肽和至少一种检测蛋白/肽/多肽都被相继或同时添加至反应器中)或多于一步,如2步、3步等进行。在形成(第一或多重)捕获剂/抗-HCV抗体复合物和/或(第一或多重)捕获剂/HCV抗原复合物之后,所述复合物然后与至少一种检测剂接触(在允许形成(第一或多重)捕获剂/抗-HCV抗体/检测剂复合物和/或(第一或多重)捕获剂/HCV抗原/检测剂复合物的条件下)。如果(第一或多重)捕获剂/抗-HCV抗体复合物和/或(第一或多重)捕获剂/HCV抗原复合物与多于一个检测剂相接触,那么然后形成(第一或多重)捕获剂/抗-HCV抗体/多个检测剂复合物和/或(第一或多重)捕获剂/HCV抗原/多个检测剂复合物。由于利用捕获剂,当将至少一种检测剂与(第一或多重)捕获剂/抗-HCV抗体复合物和/或(第一或多重)捕获剂/HCV抗原复合物相接触时,需要在与上述相似的条件下的孵育时间用于形成(第一或多重)捕获剂/抗-HCV抗体/检测剂复合物和/或(第一或多重)捕获剂/HCV抗原检测剂复合物。优选地,至少一种检测剂包含可检测标记。可检测标记可以在形成(第一或多重)捕获剂/抗-HCV抗体/检测剂复合物和/或(第一或多重)捕获剂/HCV抗原/检测剂复合物形成之前、同时或之后与至少一种检测剂结合。可使用本领域已知的任何可检测标记(参见上述讨论,包括Polak和VanNoorden(1997)和Haugland(1996))。可检测标记可直接或通过连接剂结合检测剂。可以使用的连接剂的实例是EDAC(1-乙基-3-(3-二甲氨基丙基)碳化二亚胺、氢氯化物),其可以从Sigma-Aldrich,St.Louis,MO公司商购获得。可以使用的其他连接剂是本领域已知的。用于将可检测标记与检测剂结合的方法在本领域是已知的。此外,许多可检测标记能够买到或合成,其已经含有有助于将可检测标记连接至抗体和/或蛋白多肽或其片段的末端基团,如CPSP-吖啶鎓醚(例如,9-[N-甲苯璜酰基-N-(3-丙羧基)]-10-(3-磺丙基)吖啶鎓羧胺)或者SPSP-吖啶鎓醚(例如,N10-(3-丙羧基)-N-(3-丙羧基)-吖啶鎓-9-羧胺)。捕获剂/抗-HCV抗体/检测剂复合物和/或捕获剂/HCV抗原/检测剂复合物可以是,但不一定是,在标记的定量之前从测试样品的残留物中分离出来。例如,如果至少一种捕获剂结合固体支持物,如,孔或珠,分离可以通过去除与固体支持物接触的(测试样品的)流体而实现。可替代地,如果至少一种捕获剂结合固体支持物,那么它可以同时与测试样品和至少一种检测剂接触以形成捕获剂/抗-HCV抗体//检测剂复合物和/或捕获剂/HCV抗原/检测剂复合物,接下来去除与固体支持物接触的测试样品。如果至少一种捕获剂没有结合固体支持物,然后捕获剂/抗-HCV抗体/检测剂复合物和/或捕获剂/HCV抗原/检测剂复合物不必从测试样品中去除用于定量标记的量。在形成标记的捕获剂/抗-HCV抗体/检测剂复合物和/或标记的捕获剂/HCV抗原/检测剂复合物之后,通过使用本领域已知的技术定量复合物中标记的量。例如,如果使用酶标记,标记的复合物与用于标记的底物发生反应,从而给出定量的反应如颜色的显色。如果所述标记是放射性标记,使用闪烁计数器定量该标记。如果所述标记是荧光标记,通过用一种颜色的光(被称为“激发波长”)刺激标记,并检测响应刺激由标记发射出的另一颜色(被称为“发射波长”)而定量该标记。如果所述标记是化学发光标记,通过检测可视的发射光或通过使用照度计、X-射线胶片、高速摄影胶片、CCD照相机等检测发射光而定量该标记。一旦已经定量复合物中标记的量之后,确定测试样品中抗-HCV抗体和/或HCV抗原的存在和/或浓度。特别地,抗-HCV抗体和/或HCV抗原的浓度可利用标准曲线来确定,该标准曲线通过使用已知浓度的抗-HCV抗体和/或HCV抗原的连续稀释而生成。除了使用连续稀释,标准曲线可以通过质谱和通过本领域已知的其他技术经重量分析地生成。在化学发光微粒测定中使用分析器,缀合物稀释液pH应该在大约6.0+/-0.2,微粒涂覆缓冲液应该被保持在室温下(例如,大约17℃至大约27℃),微粒涂覆缓冲液pH应该在大约6.5+/-0.2,并且微粒稀释液pH应该在大约7.8+/-0.2。固体优选地小于大约0.2%,如小于大约0.15%,小于大约0.14%,小于大约0.13%,小于大约0.12%,或小于大约0.11%,如大约0.10%。在向前的竞争性结合形式中,使用等份的已知浓度的可检测标记的抗-HCV抗体和/或HCV抗原与测试样品中的抗-HCV抗体和/或HCV抗原竞争与捕获剂结合,如,分别特异性地结合HCV抗原和/或抗-HCV抗体的抗-HCV抗体和/或HCV抗原。所述捕获剂可同时或相继与测试样品和标记的抗-HCV抗体和/或HCV抗原相接触。所述捕获剂可以固定化在固体支持物上。如果理想的话,捕获剂可直接固定化在固体支持物上或通过连接剂固定化在固体支持物上。例如,分别特异性地结合HCV抗原和/或抗-HCV抗体的抗体和/或蛋白多肽或其片段可通过与连接剂结合而固定化在固体支持物上,该连接剂固定化在固体支持物上。两种不同类型的复合物可生成—捕获剂-标记的抗-HCV抗体复合物和捕获剂-未标记的抗-HCV抗体复合物和/或捕获剂-标记的HCV抗原复合物和捕获剂-未标记的HCV抗原复合物。所述复合物可以是,但不需要是,在通过与标准曲线比较而定量可检测标记之前分离自测试样品的残留物(例如,从固体支持物上分离测试样品),所述标准曲线例如通过一系列的校准物、通过质谱、重力分析法或其他方式而生成的曲线。在相反的竞争性结合形式中,固定化的抗-HCV抗体和/或HCV抗原可以相继地或同时地与测试样品和标记的特异性结合伙伴,如抗体或蛋白多肽或其片段相接触,该特异性结合伙伴特异性地结合HCV抗原和/或抗-HCV抗体。标记的特异性结合伙伴可以结合存在于测试样品中的固定化的HCV抗原和/或抗-HCV抗体。结合存在于测试样品中的HCV抗原和/或抗-HCV抗体的标记的特异性结合伙伴与测试样品的残留物一起从固定化的HCV抗原和/或抗-HCV抗体中分离出来。然后通过与标准曲线比较而检测和/或定量附着至固定化的HCV抗原和/或抗-HCV抗体的可检测标记的量,所述标准曲线例如通过一系列的校准物、通过质谱、重力分析法或其他方式而生成的曲线。FPIA基于竞争性结合免疫测定原则。当被线式偏振光激活时,荧光标记的化合物将会发射荧光素,该荧光素的偏振度与其旋转速率成反比。当荧光标记的跟踪-捕获剂复合物被线式偏振光激活时,发射的光保持高的偏振,这是因为荧光团被束缚不在光吸收的时间和光发射的时间之间的旋转。当“游离”跟踪化合物(即,没有结合捕获剂的化合物)被线式偏振光激活时,其旋转要比在竞争性结合免疫测定中产生的相应跟踪-捕获剂缀合物更快。FPIA优于RIA,这是因为没有放射性物质需要特殊处理和处置。此外,FPIA是能够简单且快速进行的同质测定。通常地,预定水平可用作参照标准,从而相对于参照标准来评估当就抗-HCV抗体和/或HCV抗原测定测试样品时获得的结果。通常地,在作出所述比较时,通过在合适的条件下运行足够次特定的测定而获得预定水平,从而可以得出分析物存在、量或浓度与疾病、紊乱或病况的特定的阶段或终点或者与特定病征相联系或关联。典型地,预定水平通过测定参考受试者(或受试者群体)而获得。优选的技术方案:1.一种用于搅动至少一种液体的设备,包括:基座;第一端壁;第二端壁;具有圆角矩形形状的第一容器;具有圆角矩形形状的第二容器;用于保持所述第一容器的第一容器支持物,所述第一容器支持物包括用于啮合所述第一容器的第一边缘的第一杆,以非旋转地方式将第一容器连接至所述基座;以及用于保持所述第二容器的第二容器支持物,所述第二容器支持物包括用于啮合所述第二容器凹槽的圈和用于啮合所述第二容器的第二边缘的脊,所述第二容器相对于所述基座是可选择性旋转的;和盖子,具有进入第一容器的第一孔和进入第二容器的第二孔;以及其中所述第一容器和所述第二容器各具有容纳液体的空腔。2.根据项目1所述的用于搅动至少一种液体的设备,还包括用于保持第三容器的第三容器支持物,所述第三容器支持物包括用于啮合所述第三容器的第三边缘的第二杆,以非旋转地方式将所述第三容器连接至所述基座。3.根据项目1所述的用于搅动至少一种液体的设备,其中所述设备在第一旋转轴的周围进行旋转,并且所述第二容器相对于所述基座在第二旋转轴的周围进行旋转。4.根据项目1所述的用于搅动至少一种液体的设备,所述第二容器是在锁紧位置和非锁紧位置之间可移动的,在所述锁紧位置中,所述第二容器的所述第二边缘与所述脊啮合以非旋转地方式将所述第二容器连接至所述基座,并且在所述非锁紧位置中,所述第二容器被提升以使所述第二边缘脱离所述脊,并且所述凹槽在所述圈周围是可旋转的。5.根据项目1所述的用于搅动至少一种液体的设备,其中所述第一容器包括液体,所述液体包括至少下列试剂:a)选自如下的至少一种蛋白或肽:i.HCV的至少一种NS3蛋白;ii.衍生自HCV的NS3的结构域1的至少一种肽;iii.衍生自HCV的核心区域的至少一种肽;iv.衍生自HCV的E1区域的至少一种肽;v.衍生自HCV的E2区域的至少一种肽;vi.衍生自HCV的P7区域的至少一种肽;vii.衍生自HCV的NS2区域的至少一种肽;viii.衍生自HCV的NS4A区域的至少一种肽;ix.衍生自HCV的NS4B区域的肽至少一种;x.衍生自HCV的NS5A区域的至少一种肽;xi.衍生自HCV的NS5B区域的至少一种肽;以及iv.i-xi的任何组合;以及b).结合所述HCV的核心的至少一种抗体或其抗体片段。6.根据项目1所述的用于搅动至少一种液体的设备,其中所述第一容器包括液体,所述液体包括至少下列试剂:a)至少一种固相,在所述固相上涂覆选自如下的至少一种蛋白或肽:i.HCV的至少一种NS3蛋白;ii.衍生自HCV的NS3的结构域1的至少一种肽;iii.衍生自HCV的核心区域的至少一种肽;iv.衍生自HCV的E1区域的至少一种肽;v.衍生自HCV的E2区域的至少一种肽;vi.衍生自HCV的P7区域的至少一种肽;vii.衍生自HCV的NS2区域的至少一种肽;viii.衍生自HCV的NS4A区域的至少一种肽;ix.衍生自HCV的NS4B区域的肽至少一种;x.衍生自HCV的NS5A区域的至少一种肽;xi.衍生自HCV的NS5B区域的至少一种肽;以及iv.i-xi的任何组合;以及b)至少一种固相,在所述固相上涂覆结合所述HCV的核心的至少一种抗体或其抗体片段。7.根据项目5或6所述的设用于搅动至少一种液体的备,其中所述第二容器包括液体,所述液体包括至少下列试剂:a)选自如下的至少一种蛋白或肽:i.与可检测标记缀合的、HCV的至少一种NS3蛋白;ii.与可检测标记缀合的、衍生自HCV的NS3的结构域1的至少一种肽;iii.与可检测标记缀合的、衍生自HCV的核心区域的至少一种肽;以及iv.i-iii的任何组合;以及b)与可检测标记缀合的、结合HCV的核心的免疫决定区的至少一种抗体或其抗体片段。8.根据项目1所述的用于搅动至少一种液体的设备,其中所述第二容器包括液体,所述液体包括至少下列试剂:a)选自如下的至少一种蛋白或肽;i.HCV的至少一种NS3蛋白;ii.衍生自HCV的NS3的结构域1的至少一种肽;iii.衍生自HCV的核心区域的至少一种肽;iv.衍生自HCV的E1区域的至少一种肽;v.衍生自HCV的E2区域的至少一种肽;vi.衍生自HCV的P7区域的至少一种肽;vii.衍生自HCV的NS2区域的至少一种肽;viii.衍生自HCV的NS4A区域的至少一种肽;ix.衍生自HCV的NS4B区域的肽至少一种;x.衍生自HCV的NS5A区域的至少一种肽;xi.衍生自HCV的NS5B区域的至少一种肽;以及iv.i-xi的任何组合;以及b)结合所述HCV的核心的至少一种抗体或其抗体片段。9.根据项目1所述的用于搅动至少一种液体的设备,其中所述第二容器包括液体,所述液体包括至少下列试剂:a)至少一种固相,在所述固相上涂覆选自如下的至少一种蛋白或肽:i.HCV的至少一种NS3蛋白;ii.衍生自HCV的NS3的结构域1的至少一种肽;iii.衍生自HCV的核心区域的至少一种肽;iv.衍生自HCV的E1区域的至少一种肽;v.衍生自HCV的E2区域的至少一种肽;vi.衍生自HCV的P7区域的至少一种肽;vii.衍生自HCV的NS2区域的至少一种肽;viii.衍生自HCV的NS4A区域的至少一种肽;ix.衍生自HCV的NS4B区域的肽至少一种;x.衍生自HCV的NS5A区域的至少一种肽;xi.衍生自HCV的NS5B区域的至少一种肽;以及iv.i-xi的任何组合;以及b)至少一种固相,在所述固相上涂覆结合所述HCV的核心的至少一种抗体或其抗体片段。10.根据项目8或9所述的用于搅动至少一种液体的设备,其中所述第一容器包括液体,所述液体包括至少下列试剂:a)选自如下的至少一种蛋白或肽:i.与可检测标记缀合的、HCV的至少一种NS3蛋白;ii.与可检测标记缀合的、衍生自HCV的NS3的结构域1的至少一种肽;iii.与可检测标记缀合的、衍生自HCV的核心区域的至少一种肽;以及iv.i-iii的任何组合;以及b)与可检测标记缀合的、结合HCV的核心的免疫决定区的至少一种抗体或其抗体片段。11.根据项目6或9中任一项所述的用于搅动至少一种液体的设备,其中所述固相是微粒。12.根据项目5、6、8或9中任一项所述的用于搅动至少一种液体的设备,其中所述蛋白、肽、抗体和/或抗体结合片段与可检测标记缀合。13.根据项目5、6、7、8、9或10中任一项所述的用于搅动至少一种液体的设备,其中所述抗体是多克隆的、单克隆的、人的、人源化的、嵌合抗体、单链抗体、表位结合片段、单链Fv(scFv)、单链抗体、二硫键连接的Fv(sdFv)、包括VL或VH结构域的片段或者由Fab表达文库产生的片段。14.根据项目7、10或12所述的用于搅动至少一种液体的设备,其中所述可检测标记是酶、荧光标记、化学发光标记、生物发光标记、放射性标记、或者任何所述可检测标记中两个或更多个的组合。15.根据项目14所述的用于搅动至少一种液体的设备,其中所述可检测标记是生物素、吖啶鎓或其组合。16.根据项目5或6所述的用于搅动至少一种液体的设备,其中所述第二容器具有容纳液体的空腔,所述液体包括至少一种试剂,其中,所述至少一种试剂是:a.洗涤溶液;b.稀释剂;或者c.其任意组合。17.根据项目1-16任何项所述的用于搅动至少一种液体的设备,还包括具有呈圆角矩形形状的第三容器,所述第三容器具有容纳液体的空腔,所述液体包括至少一种试剂,其中,所述至少一种试剂是:a.洗涤溶液;b.稀释剂;或者c.其任意组合。尽管特定实施例方法、设备和制品已在本文中作出了描述,但是本专利覆盖的范围不仅限于此。相反地,本专利涵盖完全落在本专利权利要求的范围内的所有方法、设备和制品。序列表<110>Luoma,RobertPaulProstko,JohnC.Desai,SureshM.Gutierrez,RobinA.Muerhoff,AnthonyS.<120>用于搅动至少一种用于HIV测定的液体试剂的设备<130>12508USL1附图说明图1A示出了容纳多个实施例容器的实施例套筒,并且所述实施例套筒通过在第一位置的第一容器连接至实施例传送带的部分。图1B示出了在第二位置具有第一容器的图1A的实施例套筒。图2是图1A的A-A截面的剖面图。图3是实施例套筒和脱离传送带并且密封的图1A和2的容器的透视图。图4示出了图1A-3的实施例套筒的实施例容器的多个支座。图5是从实例传送带脱离的图2中的实施例容器和套筒的下部的放大图。图6是实例第一容器的上部和实施例套筒沿图3的B-B截面的透视图、剖面图。图7是图2中第一容器在非锁紧位置的放大图。图8是实例第一容器沿图1A的C-C截面的顶视图、剖面图。图9是从实施例套筒移除的实例第一容器沿图3的D-D截面的剖面图。图10是从实施例套筒移除的实例第一容器沿图3的B-B截面的侧剖面图。图11示出了图6-9中实例第一容器的替代底壁。图12是图11中实例底壁的顶视图。图13是表示本文公开的实例方法的流程图。若干附图或若干附图的部分可能没有按比例绘制。相反地,为了清楚说明多层和区域,可能放大附图中层的厚度。只要有可能,整个附图和附属的书面说明中使用相同的参考数字指示相同或类似的部件。如本专利中所使用的,说明任何部件(例如,层、薄膜、区域、或板块)以任何方式(例如,安置于、位于、放置于、或形成于,等)位于另一部件上,这是指参考部件或者与其他部件相接触,或者参考部件通过位于它们之间的一个或多个中间部件而位于其他部件之上。说明任何部件与另一部件相接触,就是说在两个部件之间没有中间部件。具体实施方式现在转至附图,图1A是连接至诊断分析器的传送带102上的实施例套筒100的透视图。在示出的实施例中,传送带102包括平台104,套筒100支持于其上。套筒100可手动地通过自动装置经由传送装置,和/或经由任何其他装置和/或技术被传送至和/或放置于平台104上。在操作实施例传送带102期间,平台104和因此套筒100在旋转的第一轴106周围沿着由传送带102限定的基本上环形通道108进行旋转。在一些实施例中,多个套筒连接至平台104。在一些实施例中,平台104定期地或不定期地在一个方向上例如,通道108的方向上移动。在其他实施例中,平台104以前后(例如,摆动)的运动形式移动。例如,平台104可重复地在第一方向(例如,顺时针)移动第一距离,然后在与第一方向相反的第二方向(例如,逆时针)移动第二距离。在一些实施例中,第一方向大于第二方向使得位于平台104上的套筒100在第一旋转轴106的周围通过前后的运动方式旋转。在一些实施例中,在平台104在第一方向移动之后,平台104在以第二方向移动之前在给定量的时间段内基本上是静止的。在示出的实施例中,套筒100包括基座或运载器110、第一容器112、第二容器114和第三容器116。在一些实施例中,可能存在其他数量的容器,包括,例如,1、2、4、5、6等等。同样地,在一些实施例中,一个或多个容器可被分割成多个舱以增加运载器上舱的数量。因此,运载器可包括三个容器,并且一个容器可具有三个舱从而在运载器上总共有5个舱。其他组合也是可能的。在示出的实施例中,运载器110被连接至平台104以与平台104一起旋转。实施例运载器110包括支座118、第一端壁120、第二端壁122和盖子124。在示出的实施例中,第一容器112、第二容器114和第三容器116的第一端126、128、130分别连接至支座118上,并且第一容器112、第二容器114和第三容器116的第二端132、134、136分别连接至盖子124上。在示出的实施例中,第一容器112、第二容器114和第三容器116相对于由传送带102限定的环形通道108呈径向排列在运载器110内。在示出的实施例中,第一容器112临近第一端壁120放置,第三容器116临近第二端壁122放置,并且第二容器114放置在第一容器112和第二容器114之间。实施例容器112、114、116具有圆角矩形形状。在其他实施例中,实施例容器112、114、116具有其他形状(例如,矩形、正方形、圆柱形、三角形或其他合适的形状)。每个容器112、114、116可容纳液体。在一些实施例中,所述液体包括待分析的样品,一个或多个试剂和/或固体颗粒(例如,涂覆顺磁性颗粒和/或其他微粒的胶乳)。实施例盖子124包括三个进入容器112、114、116的孔138、140、142。例如,液体可经由各自的孔138、140、142被存放入第一容器112、第二容器114和第三容器116中和/或从其中移除。在一些实施例中,第一容器112、第二容器114和/或第三容器116具有大约相同的液体容量。在其他实施例中,第一容器112、第二容器114和/或第三容器116具有不同的液体容量。第一容器112、第二容器114和/或第三容器116可被充以相同量或不同量的液体。图1B是实施例套筒100在第一容器112相对于运载器110在第二旋转轴144周围进行旋转时的透视图。在示出的实施例中,第一容器112被连接至运载器110上使得第一容器112与运载器110一起在第一旋转轴106的周围并且相对于运载器110在第二旋转轴144的周围进行旋转。在一些实施例中,相对于运载器110的第一容器112的旋转对应于平台104的运动。在示出的实施例中,当套筒100与平台104在第一方向上移动时,第一容器112在第一方向上相对于运载器110旋转了2转。当套筒100与平台104在第二方向上移动时,第一容器112在第二方向上相对于运载器110移动了1转。以这种方式,第一容器112以前后和/或振动的运动方式相对于运载器110移动。第一容器112在第一方向和第二方向上相对于运载器110的上述旋转数量以及方式(例如,前后移动)仅仅是实施例,在所述方式中容器相对于运载器110移动。在其他实施例中,第一容器112相对于运载器110以其他方式、旋转数量、方向等等旋转。在一些实施例中,第一容器112在第二旋转轴144的周围完全旋转,并且在一些实施例中,第一容器112在第二旋转轴144的周围前后摆动。同样地,在一些实施例中,第一容器112在第二旋转轴144的周围移动,同时传送带102相对于第一旋转轴106是静止的。图2是连接至传送带102上的实施例套筒100沿图1A中A-A截面的剖面图。实施例套筒100经由运载器110可拆卸地连接至传送带102。在示出的实施例中,平台104包括第一叉子200和第二叉子202以使在运载器110上啮合相应的结构(例如,孔、插孔连接器等),并且在相对于平台104的位置容纳运载器110。在其他实施例中,套筒100以其他方式(例如,经由一个或多个卡箍、夹子、螺栓、卡位、弹簧加载鞘、和/或其他机械紧固零件)可拆卸地连接至传送带102。在示出的实施例中,第一容器112、第二容器114和第三容器116各包括与盖子124的孔138、140、142之一相通(例如,延伸至)的喉口203、205、206(例如,与容器112、114、116之一流体相通的套管或管子)。在操作实施例传送带102期间,液体可经由喉口203、205、206(例如,经由吸液管)从容器112、114、116中分配(例如,存放)和/或吸取(例如,移除)。在示出的实施例中,第二容器114和第三容器116连接至运载器110,使得在操作传送带102期间(例如,当平台104沿着环形通道108移动套筒100时)第二容器114和第三容器116相对于运载器110基本上是静止的。在示出的实施例中,传送带102包括联轴器210以使第一容器112在第二旋转轴144的周围相对于运载器110旋转。在示出的实施例中,运载器110的支座118限定临近第一容器112的第一端126的第四孔212。在示出的实施例中,联轴器210通过第四孔212以图2的方位从平台104的下方延伸以啮合第一容器112。结合图8更加详细的描述,联轴器210将第一容器112从支座118提升以使得第一容器112在第二旋转轴144的周围相对于运载器110旋转。图2的实施例联轴器210是插头连接器以啮合位于实施例第一容器112的第一端126上的插孔连接器214。在其他实施例中,插头连接器210和插孔连接器214可以掉换。在示出的实施例中,插头联轴器210包括具有突出218的柄216,并且实施例插孔连接器214包括具有槽口222的杆220以接收柄216的突出218。在示出的实施例中,联轴器210通过操作连接至旋转装置224(例如,齿轮)。旋转装置224可操作地连接至传送带102的驱动装置(例如,发动机)(未示出)。在一些实施例中,当传送带102在第一旋转轴106周围旋转平台104时,旋转装置224和联轴器210在第二旋转轴144的周围进行旋转以在第二旋转轴144的周围相对于运载器110旋转第一容器112。因此,在示出的实施例中,联轴器210用于限定第二旋转轴144。在示出的实施例中,第二旋转轴144基本上平行于第一容器112的纵轴。图3是实施例套筒100从图1A-2的传送带102解连接的透视图。在示出的实施例中,运载器110包括第一手柄300和第二手柄302以便于通过人(例如,手动)和/或机器人抓住、容纳、提升、移动和/或传送套筒100。在示出的实施例中,第一帽304连接至第一容器112,第二帽306连接至第二容器114,并且第三帽308连接至第三容器116。帽304、306、308基本上覆盖和/或密封容器112、114、116的喉口203、205、206。在一些实施例中,第一容器112、第二容器114和/或第三容器116在套筒100连接至传送带102之前至少部分被填充液体。因此,实施例帽304、306、308阻止液体流出容器112、114、116,同时套筒100被提升、搬运、移动、传送等。如在下面更详尽的描述,实施例第一帽304可在锁紧位置容纳第一容器112。图4示出了图1A-3中运载器110的实施例支座118。在示出的实施例中,支座118包括支持物表面400、第一容器支持物402、第二容器支持物404和第三容器支持物406。第二容器114和第三容器116分别经由第二容器支持物404和第三容器支持物406连接至支座118上。在示出的实施例中,第二容器支持物404和第三容器支持物406包括第一突出408(例如,脊)和第二突出410(例如,杆)。在示出的实施例中,当第二容器114和第三容器116连接至支座118上时,第二容器114和第三容器116位于支持物表面400上,并且啮合第一突出408和第二突出410。第一突出408和第二突出410保持第二容器114和第三容器116,并且基本上阻止第二容器114和第三容器116相对于运载器110的移动。在其他实施例中,运载器110采用额外的和/或不同的突出,保持成员和/或装置以保持第二容器114和/或第三容器116。实施例第一容器支持物402包括第三突出412(例如,脊)以保持第一容器112和/或基本上阻止当第一容器112在锁紧位置(例如,非旋转位置)(图5)时第一容器112相对于运载器110旋转。在示出的实施例中,第三突出412是具有对应于第一容器112的圆角矩形形状的圆角矩形剖面状的脊。在示出的实施例中,第三突出412被升高到相对于支座118的支持物表面400的第一高度。实施例第一容器支持物402还包括环形脊或圈414。在示出的实施例中,第四孔212由第一容器支持物402限定,并且圈414放置于第四孔212周围的支持物表面400上。实施例圈414在操作实施例定位装置224和实施例传送带102期间,提供了齿轮表面,保持、支持、稳定、对齐和/或定向第一容器112。实施例圈414被升高到相对于支持物表面400的第二高度,且第二高度高于第一高度。结合图7在下文中更详尽的描述,当套筒100放置在平台104上时,传送带102的联轴器210啮合第一容器112,并且相对于运载器110的支持物表面400提升第一容器112至未锁紧位置,在该未锁紧位置中第一容器112经由联轴器210自由旋转。图5是当第一容器112在下部或锁紧位置时,实施例第一容器112的第一端126的剖面图。在示出的实施例中,套筒100从传送带102上解连接(例如,在将套筒100传送至平台104期间)。在锁紧位置上,第一容器112的第一周边外缘或边缘500被支持于运载器110的支持物表面400上。第一容器112的第一边缘500啮合第三突出412,使得第三突出412基本上阻止第一容器112相对于运载器110旋转(例如,第三突出412阻止第一容器112的旋转)。因此,在示出的实施例中,当第一容器112在锁紧位置时,第一容器112非旋转地连接至运载器110上。在一些实施例中,第一容器112的第一边缘500的形状和尺寸基本上符合第三突出412的形状。在示出的实施例中,第一容器112的插孔连接器214放置在由圈414限定的空间(例如,第四孔212),并且圈414在第一容器112的凹槽501中被接收到。实施例第二容器114包括第二边缘502和第二凹槽503。在示出的实施例中,第二边缘502啮合第一突出408和第二容器支持物404的第二突出410以将第二容器114非旋转地连接至运载器110。实施例第三容器116包括第三边缘504和第三凹槽506。在示出的实施例中,第三容器支持物406的第一突出408和第二突出410放置在第三凹槽506中,并且啮合第三容器116的第三边缘504以将第三容器116非旋转地连接至运载器110上。图6是当第一容器112在锁紧位置时,第一容器112的第二端132沿着图3的B-B截面的剖面图。图5的实施例第一帽304延伸至盖子124的第一孔138,并且连接至第一容器112的喉口203。实施例第一帽304包括密封部分600用于盖子124和/或密封第一容器112的喉口203。在示出的实施例中,第一帽304包括连接在密封部分600上的手柄602。手柄602便于操纵第一帽304、连接并且解连接(例如,移除)第一帽304至第一容器112上等。当第一容器112连接至运载器110,并且第一帽304连接至第一容器112时,第一帽304啮合(例如,接触)盖子124以基本上在锁紧位置容纳或保持第一容器112。在示出的实施例中,第四突出606从第一帽304的密封部分延伸。实施例第四突出606从密封部分600的外周表面608径向延伸。实施例运载器110的实施例盖子124包括延伸入第一孔138的部分的棱610。在图6的定向中,第一帽304在第一位置,使得第四突出606放置在棱610的下面。因此,当第一帽304在第一位置时,第四突出606啮合棱610以基本上阻止第一容器112相对于运载器110平行于第二旋转轴144的移动。例如,第四突出606可接触棱610以阻止第一容器112在第三突出412之上被提升(图5)。因此,在示出的实施例中,第一帽304容纳与第三突出412啮合的第一容器112,借以保持第一容器112位于锁紧位置。移除实施例第一帽304使得第一容器112从下降的或锁紧位置(图5)移动至升高的或未锁紧位置(图7),其中第一容器112可相对于运载器110旋转。为了从第一容器112移除图6的实施例第一帽304,第一帽304进行旋转直至第四突出606在盖子124的棱610的第一孔138的槽口或空间612(例如,与第一孔138相通的狭槽)中对齐。第一帽304然后可从第一容器112(例如,经由手柄602)中移除。如下面详尽的描述,当第一容器112位于未锁紧位置时,第一容器112可从支持物表面400处被提升以使得第一容器112相对于运载器110旋转。第二帽306和第三帽308进行相似地操作以分别确保第二容器114和第三容器116并且确保盖子124的位置。图7示出了位于未锁紧位置的实施例第一容器112。在示出的实施例中,套筒100连接至传送带102上,并且第一帽304从第一容器112中移除。运载器110的实施例联轴器210通过第四孔212延伸并且沿着第二旋转轴144移动(例如,提升或升高)第一容器112。在示出的实施例中,联轴器210将第一容器112移动到第三高度,该第三高度大于第三突出412(图4和5)的第一高度且小于圈414的第二高度。当实施例第一容器112被提升至第三高度时,第一容器112的第一边缘500脱离第三突出412。因此,第一容器112在第二旋转轴144的周围自由旋转(例如,第三孔412没有阻止第一容器112的旋转)。在示出的实施例中,当第一容器112被移动至未锁紧位置时,插孔连接器214保持在由圈414限定的空间内。在一些实施例中,当第一容器112相对于运载器110旋转时,第一容器112的插孔连接器214和圈414作为齿轮发挥效用。图8是图1A-7的实施例第一容器112沿图1A的C-C截面的剖面图。在示出的实施例中,第一容器112包括第一侧壁800、第二侧壁802、第三侧壁804和第四侧壁804。第一侧壁800位于第二侧壁802的对侧。在示出的实施例中,第一侧壁800包括向第二侧壁802延伸的第一肋808。实施例第二侧壁802包括向第一侧壁800延伸的第二肋810。实施例第一肋808和实施例第二肋810分别沿着第一侧壁800和第二侧壁802延伸,基本上平行于第二旋转轴144。在示出的实施例中,第一肋808和第二肋810各放置在与第三侧壁804和第四侧壁806几乎等距的位置。图8中示出的第一肋808和第二肋810仅仅是实施例。因此,第一肋808和/或第二肋810在其他实施例中可具有其他定向、形状、尺寸等。在一些实施例中,第一侧壁800和/或第二侧壁802可包括其他数量的肋(例如,0、2、3等)。此外,在一些实施例中,一个或多个肋可仅以相对于第二旋转轴144的角度定向和/或比其他更接近于端壁804、806之一而向壁下部分延伸。实施例第一容器112呈圆角矩形形状。在示出的实施例中,第一侧壁800基本上与第二侧壁802平行。实施例第一侧壁800包括第一平的或平面的部分812,并且实施例第二侧壁802包括平行于第一平面部分812的第二平的或平面的部分814。在示出的实施例中,第三侧壁804在第四侧壁806的对侧,并且第三侧壁804和第四侧壁806是弯曲的。在示出的实施例中,第三侧壁804和第四侧壁806相对于第一容器112的纵轴向外弯曲。在示出的实施例中,在第一侧壁800和第二侧壁802之间的第一距离小于在第三侧壁804和第四侧壁806之间的第二距离。在其他实施例中,第一距离大于或等于第二距离。在一些实施例中,第一容器112的深度为大约20毫米(例如,从第一侧壁800的最外面的点到第二侧壁802上最外面点的距离),且宽度为大约36毫米(例如,从第三侧壁804上最外面点到第四侧壁806上最外面点的距离)。其他实施例具有其他尺寸。在其他实施例中,第一容器112具有其他形状,如,例如,矩形、正方形、圆柱形、三角形和/或其他合适的形状或形状的组合。图9是图1A-8中实施例第一容器112沿图3的D-D截面且从套筒100移除的剖面图。图10是实施例第一容器112沿图3中B-B截面的剖面图,其相似于图6,但是显示的是第一容器112的全长。参考图9,实施例第一容器112包括底壁900和在底壁900对侧的顶壁902。实施例顶壁902连接至第一侧壁800、第二侧壁802、第三侧壁804和第四侧壁806。在示出的实施例中,顶壁902基本上是平面的。喉口203在图9的定向中从实施例顶壁902开始向上延伸。在示出的实施例中,除去喉口203和第一帽304的第一容器112的高度(例如,从第一边缘500的最外面的点到顶壁902上最外面点)是大约94毫米。其他实施例可能包括其他高度。图9中实施例底壁900连接至第一侧壁800、第二侧壁802、第三侧壁804和第四侧壁806。在示出的实施例中,底壁900是通过第一侧壁800和第二侧壁802在第一轴的周围从顶壁902拱起的或者弯曲。因此,当从容器112的外侧观察时(例如,从容器112的外部的底部),底壁900是凸的,或者当从容器112的内侧观察时是凹的。实施例底壁900也是通过第三侧壁804和第四侧壁806在第二轴的周围从顶壁902拱起的或者弯曲。因此,实施例底壁900形成弓形结构。在一些实施例中,第一容器112至少部分充满包括固体颗粒的试剂(例如,涂覆顺磁性颗粒的胶乳)。液体中的一些颗粒可以沉降并且停留在底壁900上(例如,在将套筒100传送至传送带102期间)。在操作传送带102期间,第一容器112在第一旋转轴106(例如,以前后的方式运动)和第二旋转轴144的周围移动以搅动液体和/或将颗粒分散在液体中。例如,当第一容器112经由传送带102移动时,底壁900的弯曲指引液体和/或位于底壁900上或附近的颗粒向顶壁902方向移动(例如,流动),从而搅动液体并且分散颗粒。进一步地,侧壁800、802、804、806,第一肋808和/或第二肋810与和/或相对于液体的运动使得搅动液体并且分散颗粒。在一些实施例中,第一容器112搅动液体使得在操作传送带102期间,液体基本上均匀地分散在液体内。图11-12示出了本文公开的具有替代底壁1100的第一容器112。图11是第一容器112下部的透视图、剖面图,该图示出了实施例底壁1100。在示出的实施例中,侧壁800、802、804、806,顶壁902和底壁1100限定了空腔1101用以接收且容纳液体。在示出的实施例中,底壁1100包括从第一侧壁800延伸至第二侧壁802,且从第三侧壁804延伸至第四侧壁806的洼或凹部1102(当从容器112内侧观察时)。实施例凹部1102从顶壁902在第一轴1104和第二轴1106的周围向外拱起(例如,垂直于第二旋转轴144并且彼此相互垂直的斧状物)。在一些实施例中,凹部1102是类似于弓形的或半球形的结构。实施例底壁1100还包括从底壁1100的第一侧1110向顶壁902延伸的凸出或突出1108(例如,延伸至空腔1101)。在示出的实施例中,插孔连接器214的杆220与突出1108对齐,并且依靠于底壁1100的第二侧1112,其在第一侧1110的对侧。在示出的实施例中,突出1108是具有顶或尖1114的凸面(例如,圆形的或弯曲的突出或凸出)。因此,图11的实施例底壁1100包括凹部1102和凸部(例如,实施例突出1108)。在其他实施例中,突出1108具有其他形状(例如,锥形的、角锥形的、等等)。图12的实施例突出1108具有第一弯曲半径,并且实施例凹部1102具有第二弯曲半径。在示出的实施例中,第一弯曲半径小于第二弯曲半径。同样地,在示出的实施例中,第一弯曲半径和第二弯曲半径置于相对的方向。图12是图11的实施例底壁1100的顶视图。在示出的实施例中,突出1108具有置于底壁1100的中心1202上的基本上呈圆形的基座1200。在示出的实施例中,底壁1100的中心1202沿着第二旋转轴144。因此,当实施例第一容器112在第二旋转轴144周围旋转时,底壁1100在第二旋转轴144周围旋转。实施例突出1108的尖1114也放置于底壁1100的中心1202上,并且,因此,在示出的实施例中,尖1114沿着第二旋转轴144放置。因此,突出1108从第二旋转轴144向下倾斜。当实施例第一容器112在第二旋转轴144周围旋转时,置于第一容器112中液体的颗粒沿着第二旋转轴144可能感受到小的离心力或感受不到离心力。因此,这些颗粒可能沉降在底壁1100的突出1108之上或附近。在示出的实施例中,当颗粒沉降在底壁1100的突出1108之上时,颗粒在突出1108上以远离尖1114的方向滑动和/或滚动。因此,颗粒向侧壁800、802、804、806移动,其中离心力便于液体中颗粒均匀的分散。图13示出了的代表实施例方法的流程图。尽管对实施例过程参照图13示出的流程图进行了描述,但是很多其他的方法可以是替代使用的。例如,执行方框的顺序可以改变,和/或所描述的一些方框可以改变、消除,或合并。图13的方法通过将第一容器112下降至第一位置在方框1302处开始,用以将第一容器112非旋转地连接至运载器110。例如,图1A-12中第一容器112可被下降至运载器110的支座118的第一容器支持物402之上。在一些这样的实施例中,第一容器112啮合在第一位置的运载器110的第一部分和运载器110的第二部分。例如,第一边缘500啮合第三突出412,并且插孔连接器214啮合圈414。在一些实施例中,第一帽304连接至第一容器112以容纳或保持第一容器112在第一位置。在方框1304,第二容器114非旋转地支持于运载器110上。在一些实施例中,第二容器114经由第二容器支持物404的第一突出408和第二突出410非旋转地连接至第二容器支持物404。在一些实施例中,第三容器116经由第三容器支持物406的第一突出408和第二突出410也非旋转地支持在运载器110上。在方框1306,第一容器112从第一位置被提升至第二位置,其中第一容器112从运载器110的第一部分脱离,同时保持与运载器110的第二部分的啮合。例如,第一容器112可以通过传送带102的实施例联轴器210从支持物表面提升至第三高度。当套筒100连接至传送带102时,联轴器210延伸至第四孔212中,并且将第一容器112提升至第三高度。当第一容器112被提升至第三高度时,第一边缘500脱离第三突出412,并且插孔连接器214被放置于由圈414限定的空间内。在方框1308,第一容器112在旋转轴周围旋转(例如,摆动和/或旋转)。在一些实施例中,第一容器112在第一旋转轴106的周围与平台104一起旋转,并且经由联轴器210在第二旋转轴144的周围旋转。在方框1310,混合第一容器112中的内含物。例如,通过第一侧壁800和/或第二侧壁802的平面部分搅动容器中的液体和/或颗粒。在一些实施例中,同样地通过容器的底部突出,如,例如,图11和12的底壁1100的突出1108混合第一容器112的内含物。在一些实施例中,混合第一容器112的内含物,使得颗粒基本上均匀地分散在第一容器112的液体中。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1