一种时间分辨荧光免疫层析法定量测定降钙素原的试剂盒的制作方法
本发明涉及一种定量检测用于降钙素原(PCT)的试剂盒(时间分辨荧光免疫层析法)。
背景技术:
细菌或病毒等经由创面、呼吸道、泌尿道、消化道入侵,在严重创伤,全身抵抗力下降,体内正常菌群失调,细菌移位等时,均可引起机体出现严重的感染症状,是引起临床各种并发症,如脓毒症、败血症休克,多器官功能障碍症(multiple organ dysfunction syndrome,MODS),乃至死亡的主要原因。据美国2001年统计资料显示,该年仅重度脓血症就有75.1万例,平均死亡率高达28.5%,这意味着该年死亡的人数是爱滋病(acquired immunodeficiency syndrome,AIDS)的近三倍。对感染性疾病及其并发症的早期诊断和及时治疗,能有效的降低死亡率。而目前常规使用的诊断指标(如白细胞分类和计数,C-反应蛋白,血常规检查等),是非特异性的,易引起误诊或漏诊。
1990年发现的降钙素原(procalcitonin,PCT)经证实其在血清中浓度的增高与感染的发生有密切关系,能为疾病的诊断、鉴别,治疗方案的选择,预后判断等提供新的实验室标准。在正常及健康的个体中,其血清浓度极低,仅为10-50pg/ml,一般方法检测不到。在全身性细菌、真菌及寄生虫感染,系统炎症反应综合症、败血症、急慢性肺炎、急性胰腺炎、活动性肝炎、创伤等患者的血清PCT水平异常增高,其浓度比正常水平大几倍甚至上万倍;其在病毒感染,自身免疫性疾病,器官移植排除反应等患者血清中的浓度不增高或轻微增高。这现象决定了PCT的高度特异性,因此可用于此类疾病的鉴别诊断,在全身性细菌感染和脓毒症辅助鉴别诊断、预后判断、疗效观察等方面有很高的临床价值,可广泛用于ICU病房、血液科、外科、内科、器官移植科、治疗实验室等。
目前PCT在医院和血液系统广泛使用标记免疫分析技术的检测方法,此技术具有灵敏度高、特异性强等优点,已被广泛应用于PCT的基础研究和临床各个领域的应用研究。最常用的标记免疫分析技术是放射免疫分析(RIA)和酶免疫分析(EIA),但在实际应用中存在以下缺陷:RIA的放射性核素污染、标记物的货架期短;EIA酶的活性容易失活,导致其灵敏度不高,酶的大分子标记容易影响被标记物的空间结构,使得EIA灵敏度的提高受到限制。
免疫层析(Lateral Flow Immunoassay,LFIA)技术是近几年来国内外兴起的一种快速诊断技术。LFIA以硝酸纤维素膜(NC膜)为载体,先将特异的抗体(抗原)固定于NC膜的某 一区带,当膜条一端滴加样品(尿液或血清)后,由于毛细管作用,样品将沿着该膜向前移动,当移动至固定有抗体(抗原)的区域时,样品中相应的抗原(抗体)即与该抗体发生特异性结合,用免疫胶体金等染色可使该区域显示一定的颜色,从而实现特异性的免疫诊断。
目前的LFIA快速检测试剂盒多以胶体金、彩色乳胶颗粒或者荧光素作为标记物。基于胶体金标记技术开发的快速检测产品,存在灵敏度低、主要应用于定性或者半定量、批间差异较大等问题;基于彩色乳胶颗粒虽然批间差异有所改善,但灵敏度依然较低,也只能定性或半定量;基于荧光素标记技术的免疫层析灵敏度得到很大提高,能进行定量检测,但是由于样本中含有较高的荧光本底信号,且stock位移较小,会对检测产生较大的影响。
时间分辨荧光(Time-resolved Fluorescence,TRF)是一种非同位素荧光标记物,与普通荧光相比,具有stock位移大,荧光寿命长等特点,可以有效的避免样品中的本底荧光,以及激发光等杂散光的影响,因此相比普通的荧光具有更高的灵敏度和抗干扰能力。
本发明集合了时间分辨免疫荧光微球标记技术与免疫层析技术的各自优点,两大技术相结合得到一种新的方法,时间分辨荧光免疫层析法,开发出能精确定量的快速免疫层析检测试剂盒。
技术实现要素:
本发明的目的是提供一种新型的、快速定量检测降钙素原(PCT)的时间分辨荧光免疫层析定量检测试剂盒。
为了实现本发明,我们采用了以下技术方案:
1)根据和对照同类进口试剂盒进行临床测值比较:
为了实现本发明,需要对试剂盒所使用的原料进行筛选,从而确定最佳的原料,这一筛选过程包括反应模式、定标品与质控品、原料的组合配对、硝酸纤维素膜、试剂参数优化及性能评估等;
2)确定试剂盒的组分;
本发明提供的一种时间分辨免疫荧光层析法定量测定降钙素原试剂盒,包括:定标品、质控品、说明书、铝膜袋、干燥剂及其包装这些试剂瓶、试纸卡的包装盒。
根据本发明一个优选的实施方案,采用双抗体夹心法对人血清(浆)中的PCT进行检测。试剂含有被事先固定于NC膜上的测试区(T)的PCT特异性的单克隆抗体2和质控区(C)的羊抗鼠IgG,时间分辨荧光微球标记的PCT特异性单克隆抗体1。测试时,样本滴加入加样孔,随之在毛细效应下向观察窗方向层析,并引发时间分辨荧光微球标记抗体的释放,样本中的PCT、时间分辨荧光微球标记的单克隆抗体PCT1以及固定于NC膜测试区的PCT特异 性单克隆抗体2形成双抗体夹心结构,无论样本中有没有PCT存在,质控区羊抗鼠IgG都会与时间分辨荧光微球标记的PCT特异性单克隆抗体1结合,时间分辨荧光微球在特定波长的激发光作用下发射出特定波长的发射光,检测区发射光信号的强弱与样本中PCT的含量成正比。
根据本发明一个优选的实施方案,将浓度为100ng/ml的定值PCT血清用1.5%标准品稀释液配制成定标品A-F,其浓度依次为:A:0ng/mL、B:0.5ng/mL、C:2ng/mL、D:10ng/mL、E:20ng/mL、F:40ng/mL。将浓度为100ng/ml的定值PCT血清用PCT阴性血清配制成浓度为0ng/mL、2ng/mL以及10ng/mL的质控品。1.5%标准品稀释液为50mmol/L Tris-HCl缓冲液(pH7.8),含0.9%NaCl、0.1%NaN3、0.01%Tween-20、1.5%BSA,2-8℃保存。
根据本发明一个优选的实施方案,选择MJG03作为标记原料,购自杭州启泰生物,16B5作为包被原料,购自Hytest。
根据本发明一个优选的实施方案,选择MDI公司的70CNPH-N-SS40作为实验用硝酸纤维素膜。
根据本发明一个优选的实施方案,最终选择微球标记抗体用稀释液稀释为0.1mg/ml、喷量为0.1μl/mm,稀释液主要组分为7.5%的BSA,使用时终浓度为0.1%。
根据本发明一个优选的实施方案,最终选择检测线抗体16B5用15mM PBS(pH 7.4)包被缓冲液稀释至4.2mg/ml及质控线羊抗鼠IgG用10mM PBS(pH 7.4)包被缓冲液稀释至1mg/ml,分别以0.08μl/mm划线,稀释液组分分别为:15mM PBS包被缓冲液(1L),取Na2HPO4·12H2O 5.37g,NaN31g,NaCl 8.77g和海藻糖30g,加适量纯化水充分溶解,调节pH至7.4,再用纯化水稀释至1000ml;10mM PBS包被缓冲液(1L):取Na2HPO4·12H2O 3.58g,NaN31g,NaCl 8.77g和海藻糖30g,加适量纯化水充分溶解,调节pH至7.4,再用纯化水稀释至1000ml。
本发明的试剂盒采用样本类型为人血清或血浆标本。
利用本发明的试剂盒进行检测,具有快速、操作简单、可定量、无放射性污染等特点,非常适用于临床检测。
附图说明
图1为本试剂盒的反应模式示意图。
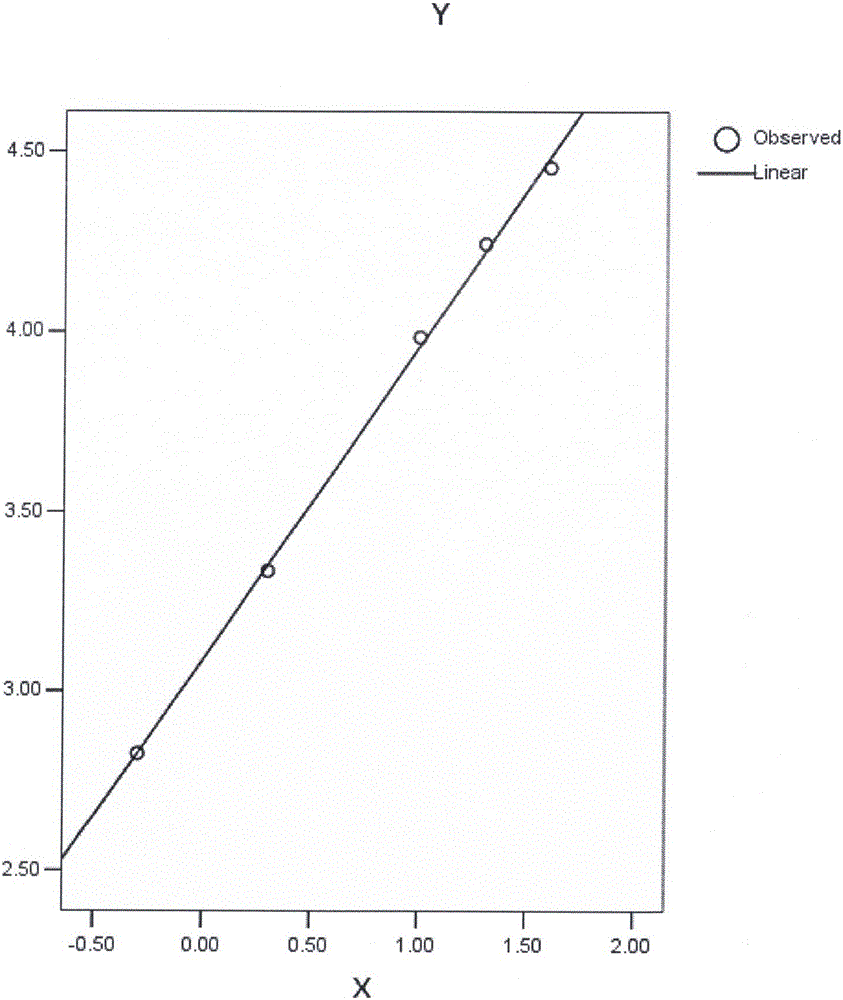
图2为本试剂盒剂量-反应曲线图。
图3为本试剂盒与Elecsys BRAHMS PCT试剂盒234例临床血清样本分析结果图。
具体实施方式
实施例1试剂盒的组成
1)定标品,1套,分别编号A-F
2)质控品,1套,分别编号C1-C3
3)铝膜袋,1个/人份
4)干燥剂,1个/人份
5)说明书,1份
实施例2试剂盒的使用方法
步骤1:
试剂的准备:将试剂以及样本平衡至室温(指20-25℃范围,下同)。
步骤2:
1)试剂的准备
试验前,所有试剂及样品均需平衡至室温(指20-25℃范围,下同)。
2)每孔加入40μl样本。
3)室温层析,充分反应15min-30min。
4)测定各试剂卡荧光值。以定标品浓度的对数为横坐标,荧光值的对数为纵坐标,参见附图1。根据各待测样本的CPS值在相应剂量-反应曲线上拟合出该样本中PCT的浓度。
实施例3反应体系的建立与优化
硝酸纤维素膜的优化:在反应其它条件不变的情况下,我们将Millipore公司的HF 125、HF 150和MDI公司的70CNPH-N-SS40作为层析实验用膜备选膜,通过一系列实验对其性能进行研究,综合考虑阳性荧光值、阴性本底以及检测线与质控线的均匀性效果,最终选择MDI公司的70CNPH-N-SS40。
配对抗体原料的优化:在反应其它条件不变的情况下,对MJG03与16B5组合、138与118组合以及118与138组合分别进行如下3组时间分辨免疫荧光检测实验,并将结果统计如下,根据软件SPSS 13.0以定标品浓度的对数为横坐标,荧光值的对数为纵坐标,由双对数数学模型Log-Log函数处理,计算剂量-反应曲线相关系数(r),同时辅以时间分辨免疫荧光法方法学的评判标准,选择TRF1A检测中效果最好的一组,综合以上结果,最终选择MJG03作为标记原料,16B5作为包被原料。TRFIA法筛选结果见表1。
表1抗体筛选结果
划线量的优化:在反应其它组分不变的情况下,以不同包被量包被于NC膜上,具体如下:
组合一:将检测线抗体16B5用15mM PBS(pH 7.4)包被缓冲液稀释至4.2mg/ml及质控线羊抗鼠IgG用10mM PBS(pH 7.4)包被缓冲液稀释至1mg/ml,分别以0.08μl/mm划线,制成检测线T及质控线C,划线结束后在湿度低于40%的条件下,20~37℃干燥。
组合二:将检测线抗体16B5用15mM PBS(pH 7.4)包被缓冲液稀释至4.2mg/ml及质控线羊抗鼠IgG用10mM PBS(pH 7.4)包被缓冲液稀释至1mg/ml,分别以0.12μl/mm以及0.08μl/mm划线,制成检测线T及质控线C,划线结束后在湿度低于40%的条件下,20~37℃干燥。
将干燥后的时间分辨荧光微球标记抗体结合垫,NC膜以及其它辅料进行组装并切条,通过下一步的性能检测,最终选择检测线抗体16B5用15mM PBS(pH 7.4)包被缓冲液稀释至4.2mg/ml及质控线羊抗鼠IgG用10mM PBS(pH 7.4)包被缓冲液稀释至1mg/ml,分别以0.08μl/mm划线。检测结果如下表:
表2标记抗体使用量
实施例4试剂盒的实验室性能
对实施例1的试剂盒进行实验室性能分析,结果如下:
1)最低检测量
0.08ng/ml。
2)准确性
取高值PCT血样一份,德国Roche Diagnstics Gmbu公司生产的降钙素原检测试剂盒(电化学发光法)测得其浓度为62.8ng/ml,用PCT阴性血清对其进行倍比稀释作为样品,在自制试剂盒上测定,计算其理论值及实测值的比值。各设3个平行实验,计算回收率。见表3。实测浓度与期望浓度测值的比值在0.90-1.13之间,回收率在90%-113%之间。
表3准确度检测结果
3)剂量-反应曲线的线性
按试剂盒操作步骤测定定标品A-F(A:0ng/mL、B:0.5ng/mL、C:2ng/mL、D:10ng/mL、E:20ng/mL、F:40ng/mL)。在定标品B(0.5ng/mL)与定标品F(40ng/mL)之间的浓度范围内,以定标品浓度的对数为横坐标,荧光值的对数为纵坐标,由双对数数学模型Log-Log函数处理,线性回归方程为Y=0.872X+3.088,计算剂量-反应曲线线性相关系数,r=0.9994。试剂盒的剂量-反应曲线图见附图2。
4)精密度(CV%)
测定低、中、高3个质控品(质控品I、II、III),分析内精密度实验设5个试剂条,分析间精密度实验设同一批次试剂,3个不同人独立操作,得到各质控品检测值的均数、标准差及变异系数(CV)。结果分析内变异系数为5.4%-7.7%,分析间变异系数为5.7%-13.4%。
5)特异性
将CRP、IL-6、人降钙素、人抗钙素以定标品稀释液分别稀释至50ng/mL、1IU/mL、60ng/mL及30ng/mL作为样本,用配套仪器测定,结果均小于0.08ng/mL。结果表明本试剂盒与CRP、IL-6、人降钙素和人抗钙素无交叉反应。
实施例6试剂盒同国外试剂盒临床血样测值比较
采用盲法对照的临床试验设计,用本试剂盒与罗氏Elecsys BRAHMS PCT试剂盒共同检测临床样本,共检测样本234例次,其中临床确诊为PCT阳性样本151例,阴性样本83例。使用统计软件SPSS 13.0,对数据进行分析,Y=0.898X+0.750,相关系数R=0.977,R2=0.955,P<0.0001,研究结果表明待考核试剂可靠、准确、安全、简便、稳定,具有较高的临床应用价值。
- 还没有人留言评论。精彩留言会获得点赞!
- 基于量子点的CA15‑3免疫层析试纸条的制备方法与制造工艺
- 肌红蛋白荧光免疫层析试纸条用活化荧光乳胶微球及应用的制造方法与工艺
- 铁蛋白荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 全程C‑反应蛋白荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 一种微流控芯片上基于荧光量子点磁性富集并分离结核分枝杆菌TB的方法及装置与制造工艺
- 25‑羟基维生素D荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 25‑羟基维生素D3荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 降钙素原荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 一种改变量子点荧光色的方法与制造工艺
- 一种基于荧光免疫层析技术的定量检测计算方法与制造工艺
- 基于量子点的CA15‑3免疫层析试纸条的制备方法与制造工艺
- 肌红蛋白荧光免疫层析试纸条用活化荧光乳胶微球及应用的制造方法与工艺
- 铁蛋白荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 全程C‑反应蛋白荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 一种微流控芯片上基于荧光量子点磁性富集并分离结核分枝杆菌TB的方法及装置与制造工艺
- 25‑羟基维生素D荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 25‑羟基维生素D3荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 降钙素原荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 一种改变量子点荧光色的方法与制造工艺
- 一种基于荧光免疫层析技术的定量检测计算方法与制造工艺