铜‑铁普鲁士蓝纳米材料修饰电极、制备方法及其应用与流程
本发明属于电化学分析检测技术领域,具体涉及一种纳米材料铜-铁普鲁士蓝纳米材料修饰电极、制备方法及其对卡托普利的检测应用。
背景技术:
卡托普利(captopril,cap)化学名称为1-[(2s)-2-甲基-3-巯基-1-氧代丙基]-l-脯氨酸,化学式c9h15no3s。因为含有硫巯基,因此可以作为血管紧缩肽转化酶(ace)的抑制剂,已广泛应用于高血压和充血性心力衰竭的临床治疗。并且能够作为生物系统内自由基的清除剂,卡普托利经代谢转化成二硫化物,并且能够和未被吸收利用的卡普托利(40%~60%)一起通过尿液排出体外。因此,从生理角度和用量控制这两方面来说,对尿液中卡普托利进行有效且灵敏的检测是非常有意义的。
现有多种方法检测卡托普利,例如采用高效液相色谱法测定金宝肾片中的卡托普利含量,但缺陷在于仪器设备要求高,分析成本高,液相色谱仪价格高及日常维护费用贵,分析时间一般较长。又例如采用电聚合的方法,在玻碳电极表面沉积均匀分布的铁氰化铜/nafion复合物,再利用循环伏安法研究药物分子卡托普利在该修饰电极上的电化学行为,但是该铁氰化铜/nafion复合物作为修饰电极检测时具有检测浓度范围较窄、稳定性差、可重复性不高等缺点。
技术实现要素:
本发明的目的在于提供一种原位电化学合成铜-铁普鲁士蓝纳米材料修饰电极及其制备方法,并将该修饰电极应用于检测卡托普利。
实现本发明目的的技术方案是:一种纳米材料铜-铁普鲁士蓝纳米材料修饰电极,所述修饰电极是以ito玻璃电极为基底,所述基底表面依次沉积cu纳米粒子和cuhcf纳米粒子。
上述铜-铁普鲁士蓝纳米材料修饰电极的制备方法,包括如下步骤:
1)以cucl2和kcl混合溶液为电解液,以洁净的ito玻璃电极为工作电极,采用电流-时间曲线法进行电化学沉积,20s后取出沉积cu纳米粒子的ito玻璃电极,清洗、干燥;
2)以k3[fe(cn)6]和kcl混合溶液为电解液,以沉积cu纳米粒子的ito玻璃电极为工作电极,采用电流-时间曲线法进行电化学沉积,10800s后取出沉积cuhcf的ito玻璃电极(ito/cuhcf),清洗、干燥。
进一步的,步骤1)中,cucl2和kcl混合溶液中cucl2和kcl的浓度均为0.1m。
进一步的,步骤1)中,所述电化学沉积选用三电极体系,以饱和甘汞电极为参比电极,以铂电极为对电极,电化学沉积的参数如下:初始电流-0.1v,取样间隔1s,实验时间20s,静置时间1s。
进一步的,步骤2)中,k3[fe(cn)6]和kcl混合溶液中k3[fe(cn)6]的浓度为10mm,kcl的浓度为0.1m。
进一步的,步骤2)中,所述电化学沉积选用三电极体系,以饱和甘汞电极为参比电极,以铂电极为对电极,电化学沉积的参数如下:初始电流0.4v,取样间隔0.1s,实验时间10800s,静置时间1s。
上述cuhcf修饰ito电极对卡托普利的检测方法,所述方法包括下列步骤:
采用循环伏安法,在-0.3~1.2v,10mv/s条件下,将ito/cuhcf修饰电极浸入0.1mhcl和0.1mkcl混合溶液中,静置一段时间后,共加入30µl溶液cap(2.344mm)。检测修饰电极对cap的电化学响应。
与现有技术相比,本发明的显著优点是:
(1)本发明通过连续电化学沉积法将活性cuhcf修饰在已羟基化的ito电极表面,表面的羟基化为ito电极提供了活性氢氧根,这使得在电化学沉积过程中强化了铜离子的亲和性,并且能够作为cu2+/[fe(cn)6]3+纳米分子生长的固定位点,所述方法简单快速,重复性好,制备得到的电极环境稳定性好。
(2)本发明合成的cuhcf修饰在电极上具有良好的氧化还原性,对卡托普利具有强烈的催化效果,在cv和安培时间响应曲线上有强的电流响应,具有更大的线性催化范围和更低的检测限(~0.43µm),所述检测方法快速而准确、成本低廉。
附图说明
附图1为实施例1制备的ito/cuhcf修饰电极的扫描电子显微镜表征图片。
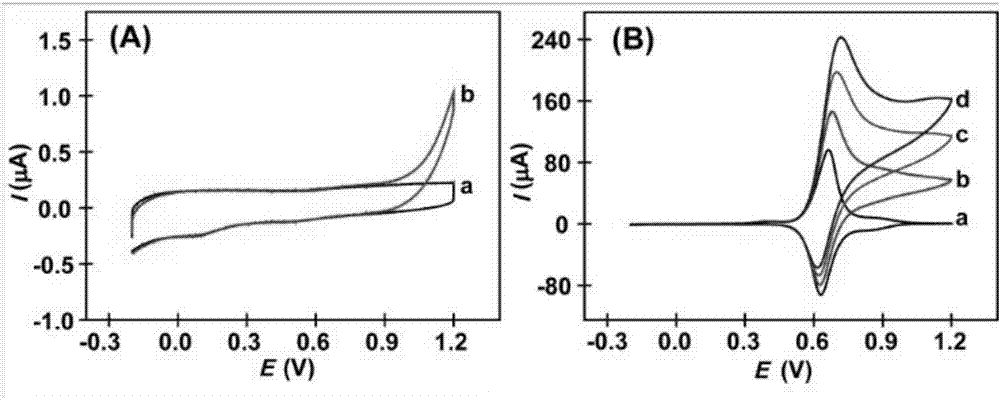
附图2为实施例1制备的不同修饰电极(a)裸露ito,(b)ito/cuhcf在没有底物cap和有cap时不同的电流响应循环伏安曲线图。
附图3为实施例ito/cuhcf电极对不同浓度的cap的安培时间相应曲线图(其中,插图为电流和cap浓度的线性关系图)。
具体实施方式
下面结合附图和具体实施例对本发明作进一步详细描述。
实施例1
如图1,本发明ito/cuhcf修饰电极的制备过程如下:
(1)取合适大小的干净的ito玻璃放入烧杯中,按照28%nh3·h2o:30%h2o2:h2o=1:1:6(体积比)配制40ml混合溶液,将其倒入装有ito玻璃的烧杯中,完成ito的羟基化过程;之后取出用去离子水冲洗,n2吹干备用。
(2)取10ml,0.1mcucl2和0.1mkcl混合溶液置于电解槽中,将三个电极插入电解槽,ito玻璃电极一端全部浸入电解液中。打开电化学工作站。选用电流-时间曲线法,设置实验参数:初始电流-0.1v,取样间隔1s,实验时间20s,静置时间1s。20s后取出ito玻璃电极先后用乙醇,去离子水冲洗,n2吹干并保存,得到ito/cunps修饰电极。
(3)取10ml,10mmk3[fe(cn)6]和0.1mkcl混合溶液置于电解槽中,将(2)得到的ito/cunps电极浸入电解槽中,选用电流-时间曲线法,设置参数:初始电流0.4v,取样间隔0.1s,实验时间10800s,静置时间1s。10800s后取出ito玻璃电极,先后用乙醇,去离子水冲洗,n2吹干并保存。制得ito/cuhcf电极。
将原位电化学合成的ito/cuhcf电极用扫描电子显微镜进行形貌表征,在ito/cuhcf表面有许多规则的立方型微晶生成。其中最大的晶体边缘可达200nm。如图1所示。
实施例2
ito/cuhcf修饰电极的应用
我们通过循环伏安法利用裸露ito电极对不含cap的0.1mkcl和0.1mhcl的溶液进行检测,发现没有催化响应;向溶液中加入0.794mmcap,发现其在1.2v的电势下能进行电催化反应(图2a,裸露ito,a:0mm,b:0.794mm)。将裸露ito电极替换为ito/cuhcf电极(图2b,a:0mm,b:0.794,c:1.575mm,d:2.344mm),我们发现随着cap浓度的增加,相同实验条件下氧化峰电流强度也相应的增加。并且,cap加入浓度按照一定倍数加入,氧化峰电流峰值也类似按照一定倍数增加。同时,将a,b两个曲线图对比可以看出当溶液中cap浓度为0.794mm时,裸露ito电极催化电流峰值在1.2µa左右,而ito/cuhcf电极对其的催化氧化电流峰值在100µa左右,所以在卡托普利的催化实验中,可以忽略裸露ito玻璃电极对其的催化效果。
实施例3
ito/cuhcf修饰电极的应用
如图3所示,当向溶液中分别加入0mm、0.794mm、1.575mm、2.344mm卡托普利时,观察到电流响应值几乎跟随浓度按照一定比例稳定上升。因此利用电流-时间曲线法,在持续外加0.65v电势的0.1mkcl和0.1mhcl溶液中,每100s注入等分卡普托利的试样,对得到的扫描数据进行整理分析,得出ito/cuhcf电极对卡托普利检测的标准曲线y=0.428+65.86x(如图3插图所示),线性相关系数为0.9986,线性范围从6.0×10-7m到5.3×10-4m,并且在s/n=3的基础上检测限为0.43μm。说明cuhcf修饰电极对于卡托普利的电化学检测检测下限低,检测范围广,有很好的应用价值。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种基于碳点检测ATP的修饰电极及其制备方法与流程
- 一种电极修饰材料复合物ImCoPc/RGO的制备方法和应用与流程
- 一种检测氯霉素的SnSe/SWNT修饰电极光致电化学传感器制备方法及应用与流程
- 一种采用三维多孔材料修饰电极检测多灵菌的方法与流程
- 一种复合材料修饰的工作电极检测微量砷及痕量砷和重金属的电化学方法与流程
- 一种碳材料修饰的工作电极检测微量及痕量砷和重金属的电化学方法与流程
- 碳纳米管/金纳米复合材料修饰电极在日落黄的检测中的应用的制造方法与工艺
- 一种基于三聚氰胺纳米银复合材料修饰电极速测硫化物的方法与流程
- 一种表面修饰LATO的LNMO电极材料及制备方法与流程
- 分子印迹过氧化聚吡咯/聚对氨基苯磺酸修饰电极的制备的制造方法与工艺