一种海参口服液快速鉴定试剂盒的制作方法
本发明涉及食品检测领域,具体来说涉及一种海参口服液快速鉴定试剂盒。
背景技术:
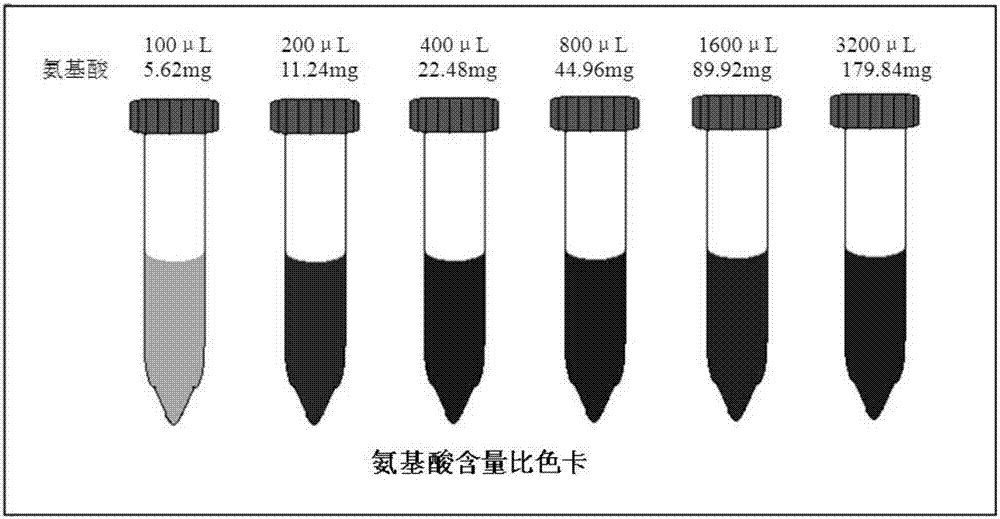
:海参,属海参纲(holothuroidea),海参属,大多生活在海岸线八千米范围内,主要以藻类植物和浮游生物为食。其全身布满肉刺,广泛分布于世界各海洋。我国渤海、东海、南海均有分布,且东南海处海参品种尤为丰富,约有二十多种可食用类海参,海参营养价值丰富,不仅是珍贵的食品,更是名贵中药材。研究表明海参具有提高记忆力、促进器官新陈代谢、治疗高尿酸血症、软化血管以及抑制肿瘤生长等多种疗效。海参口服液也称之为液体海参,可细分为浓缩型、精华型、高活性型等,其本质都是海参口服液。口服液的优点在于降低营养物质分子结构的复杂度,使其更加有利于人体对蛋白、多肽、多糖、皂苷等的直接吸收利用。如果原料质量有保证,且提取技术水平过关,这是一种真正方便、科学、有效地解决吃海参的好办法。海参口服液的制作工艺通常是,先将海参搅碎,然后加酶水解,脱色,再加稳定剂并对风味进行调配,最后杀菌灌装。这种技术因为高度有效地保留了海参最有价值的活性成分,可以使海参多糖彻底分离而被人体吸收,将海参的吸收效率从鲜海参不足20%的利用率或仅为4%的干海参吸收率提高到至少98%以上。一支海参口服液甚至不须消化,无论男女老少服用后都能直接吸收,尤其适用于重病患者、术后恢复期患者以及消化功紊乱的患者。因此海参口服液的质量至关重要:产品是否无糖(以适用于糖尿病患者)、是否添加防腐剂、海参多糖含量是否达到200μg/ml、氨基酸含量是否达到100mg/ml等也是重要判别标准。许多产品徒有华丽包装,但营养价值却与其高昂的价格不相符,甚至有虚报营养物含量的现象。近年来,海参口服液、海参胶囊等以海参为原料的保健品层出不穷,许多既无专利产权,也缺乏高端的生产技术设备的小厂家、小品牌擅自仿照拥有专利产权的生产厂家的技术生产各种海参制品,但因为技术不达标,产品质量无法得到保证,服用这类产品甚至可能带来健康隐患,而普通百姓又难以分辨。目前海参口服液的检测多是其中某一具体成分指标的测定,如曹惠丽等“海参口服液中海参多糖的测定”、杜增鹏“海参活性肽口服液蛋白含量检测技术研究”,往往进行海参口服液的检测需要大型设备和繁琐实验过程,目前市面上尚未有可家用的海参口服液快速检测试剂盒。技术实现要素:针对现有技术存在的上述问题,结合目前现有主要海参口服液开发的现状,本发明针对所需开发一种可家用的海参口服液快速检测试剂盒。本发明的目的之一在于提供一种海参口服液快速鉴伪试剂盒。本发明的目的之二在于提供一种海参口服液快速鉴伪方法。针对上述发明目的,具体的,本发明提供以下技术方案:一种海参口服液快速鉴伪试剂盒,所述试剂盒包括如下试剂:a试剂:茚三酮溶液;b试剂:硫酸铜溶液;c试剂:十六烷基三甲基溴化铵(ctab)溶液;d试剂:标准海参口服液。优选的,a试剂为1%-5%茚三酮溶液,更优选的,a试剂为1%茚三酮溶液取0.2g茚三酮,加蒸馏水20ml超声加热溶解。优选的,b试剂为0.5%-3%硫酸铜溶液,更优选的,b试剂为0.5%硫酸铜溶液,取0.1g硫酸铜,加蒸馏水20ml超声加热溶解;优选的,c试剂为0.1%-2%ctab溶液,更优选的,c试剂为0.5%十六烷基三甲基溴化铵(ctab)溶液:取0.1gctab,加蒸馏水20ml超声加热溶解;优选的,d试剂为标准海参口服液5-15ml。海参标准口服液是指由海参加工而成的正品口服液,而非伪品。更为优选的,海参标准口服液通过如下制备方法获得:海参用清水洗净,刨肠称重100g,切碎后加两倍质量的超纯水,组织匀浆机匀浆10min,得海参匀浆液;加入匀浆液三倍体积pbs缓冲液以及相当于海参质量1%的胃蛋白酶在50℃恒温水浴锅中酶解5h并持续搅拌,保持ph在2-3.5之间,再调整ph至6.8-7.2,加入海参质量1%胰蛋白酶在50℃水浴锅中持续搅拌5h;终止酶解时将水浴锅温度迅速升到90℃以上维持5min;将此浓缩液于3800rpm条件下离心25min,取上清液,悬蒸浓缩至100ml,即为海参标准口服液。优选的,所述试剂盒还包括试剂盒耗材:试管4支,滴管4支。本发明还公开了一种海参口服液快速鉴伪方法,所述方法包括:取标准海参口服液和待测海参口服液各1-2ml分别加入两支试管中,然后每支试管再加入1-2mla试剂,将两支试管沸水浴10-15min后,标准海参口服液管变蓝紫色或者紫黑色(现象ⅰ);再分别向两支试管中分别加入1-2mlb试剂,静置20-30min,标准海参口服液管分层,上层为橘红色澄清透明(现象ⅱ),下层为蓝黑色沉淀(现象ⅲ);分别取上清液1-2ml加入新的试管中,然后在新试管中分别加入1-2mlc试剂,静置5-10min,标准海参口服液管变浑浊或者产生微量沉淀(现象ⅳ);如果待测海参口服液在检测中现象ⅰ-ⅳ中有一个及以上没有出现则说明待测海参口服液为非真品。本发明上述技术方案取得了以下有益效果:(1)针对现有存在的市场难题,本发明提供了一种简便易行的海参口服液鉴伪试剂盒,通过现象明显的反应可以判断海参口服液的多糖及氨基酸大体含量,从而判断海参口服液真伪,无需大型设备和繁琐实验过程,普通消费者即可实现,简便快速,性价比较高。(2)本发明中所用主要试剂茚三酮、硫酸铜、ctab等均为无毒产品,适合普通消费者操作。附图说明图1实施例1方案一实验现象图2实施例1氨基酸含量比色卡图3实施例1多糖含量对比图图4实施例1海参口服液检测结果图5海参提取物与海带提取物的鉴伪,图5a:试管中加入海参提取液和海带提取液各1ml,左为海参提取液,右为海带提取液;图5b:试管中加入茚三酮溶液1ml,沸水浴加热10min后,海参提取液颜色较深,左为海参提取液,右为海带提取液;图5c:沸水浴冷却后,加入硫酸铜溶液1ml,静置20min后,海参提取液产生较多沉淀,左为海参提取液,右为海带提取液;图5d:取滤液,加入ctab溶液后,海带提取液产生少量沉淀,左为海参提取液,右为海带提取液。具体实施方式应该指出,以下详细说明都是示例性的,旨在对本发明提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本发明所属
技术领域:
的普通技术人员通常理解的相同含义。需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本发明的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作和/或它们的组合。正如
背景技术:
所介绍的,市面上尚未有可家用的海参口服液快速检测试剂盒。基于此,本发明提出了一种海参口服液快速鉴伪试剂盒及鉴伪方法。本发明的一个实施方式公开了一种海参口服液快速鉴伪试剂盒,所述试剂盒包括如下试剂:a试剂:茚三酮溶液;b试剂:硫酸铜溶液;c试剂:十六烷基三甲基溴化铵(ctab)溶液;d试剂:标准海参口服液。由于海参的营养价值主要在于其丰富蛋白质、氨基酸及海参多糖的含量,而真假海参口服液的差距也主要体现在蛋白质、氨基酸和海参多糖的含量差异上,因此本试剂盒主要通过检测海参口服液中蛋白质、氨基酸与海参多糖含量来判断海参口服液的品质。然而对于普通消费者来说,缺乏大型的检测设备及手段,常常无法鉴别真伪,服用虚假产品可能带来极大健康隐患。因此,简单高效的鉴伪手段,对于普通消费者来说是必要的。海参口服液中的主要成分包括蛋白质、氨基酸和多糖,本发明首先用a试剂,即茚三酮,通过氨基酸的茚三酮显色反应检测海参口服液中氨基酸含量,颜色越深说明氨基酸含量越高;然后加入b试剂,即硫酸铜溶液,通过铜离子沉淀海参口服液中的蛋白质,同时溶液颜色发生变化,检测海参口服液中蛋白质含量,沉淀越多说明蛋白质越多;最后在上清液中加入c试剂,即ctab溶液,通过ctab和酸性多糖的沉淀反应检测海参口服液中多糖的含量。本发明通过常规检测试剂的选择和顺序组合,实现了仅通过现象明显的反应就可以判断海参口服液的多糖及氨基酸大体含量,从而判断海参口服液真伪,具有操作简单,性价比高的特点。本发明中针对海参多糖的检测采用ctab和酸性多糖的沉淀反应检测的手段,本发明前期研究中发现,海参多糖中以岩藻多糖为主(岩藻多糖含量较高),而检测岩藻多糖需采用浓硫酸和半胱氨酸盐酸盐的紫外分光光度法检测,采用紫外分光光度法检测对于普通大众无法获及,若不利用紫外分光光度法,一是现象不明显,二是过程中采用浓硫酸对于实际推广应用中存在风险(浓硫酸操作不当易引发伤害)。相较海参中岩藻多糖的检测,海参中酸性多糖的检测更适合于本发明简单现象的反应。本发明中试剂盒的检测试剂加入顺序也是关键因素之一,本发明预实验中根据茚三酮颜色反应、ctab沉淀反应为基本反应原理,制备了可用于定量检测氨基酸与多糖含量的试剂盒,过程中发现虽然同时加入茚三酮与ctab更简便易行,但此时则无氨基酸与茚三酮的显色反应,分析其原因可能是高离子浓度下ctab不仅可与酸性多糖反应,还可与氨基酸发生反应,从而影响颜色变化,因此选择先加入茚三酮,对比颜色再加入ctab。另外ctab具有同时沉淀蛋白质和酸性多糖的作用,因此为了排除样品中蛋白质对酸性多糖沉淀的影响,本发明在加入ctab之前先用硫酸铜沉淀样品中蛋白质,既检测了样品中蛋白质含量又排除了蛋白质对酸性多糖检测的影响。优选的实施方案中,a试剂为1%-5%茚三酮溶液,例如茚三酮溶液的浓度(质量百分数)为1%、2%、3%、4%、5%;更优选的,a试剂为1%茚三酮溶液取0.2g茚三酮,加蒸馏水20ml超声加热溶解。优选的实施方案中,b试剂为0.5%-3%硫酸铜溶液,更优选的,b试剂为0.5%硫酸铜溶液,取0.1g硫酸铜,加蒸馏水20ml超声加热溶解;优选的实施方案中,c试剂为0.1%-2%ctab溶液,更优选的,c试剂为0.5%十六烷基三甲基溴化铵(ctab)溶液:取0.1gctab,加蒸馏水20ml超声加热溶解;优选的,d试剂为标准海参口服液5-15ml。海参标准口服液是指由海参加工而成的正品口服液,而非伪品。更为优选的,海参标准口服液通过如下制备方法获得:海参用清水洗净,刨肠称重100g,切碎后加两倍质量的超纯水,组织匀浆机匀浆10min,得海参匀浆液;加入匀浆液三倍体积pbs缓冲液以及相当于海参质量1%的胃蛋白酶在50℃恒温水浴锅中酶解5h并持续搅拌,保持ph在2-3.5之间,再调整ph至6.8-7.2,加入海参质量1%胰蛋白酶在50℃水浴锅中持续搅拌5h;终止酶解时将水浴锅温度迅速升到90℃以上维持5min;将此浓缩液于3800rpm条件下离心25min,取上清液,悬蒸浓缩至100ml,即为海参标准口服液。更为优选的实施方案中,a试剂:1%茚三酮溶液;b试剂:0.5%硫酸铜溶液;c试剂:0.5%十六烷基三甲基溴化铵(ctab)溶液。本浓度条件下,检测试剂加入前后,试剂之间不存在相互干扰现象,且现象反应更为明显。优选的,所述试剂盒还包括试剂盒耗材:试管4支,滴管4支。本发明还公开了一种海参口服液快速鉴伪方法,所述方法包括:取标准海参口服液和待测海参口服液各1-2ml分别加入两支试管中,然后每支试管再加入1-2mla试剂,将两支试管沸水浴10-15min后,标准海参口服液管变蓝紫色或者紫黑色(现象ⅰ);再分别向两支试管中分别加入1-2mlb试剂,静置20-30min,标准海参口服液管分层,上层为橘红色澄清透明(现象ⅱ),下层为蓝黑色沉淀(现象ⅲ);分别取上清液1-2ml加入新的试管中,然后在新试管中分别加入1-2mlc试剂,静置5-10min,标准海参口服液管变浑浊或者产生微量沉淀(现象ⅳ);如果待测海参口服液在检测中现象ⅰ-ⅳ中有一个及以上没有出现则说明待测海参口服液为非真品。具体的,本发明是通过以下技术方案实现的:试剂盒试剂:a试剂:1%茚三酮溶液:取0.2g茚三酮,加蒸馏水20ml超声加热溶解。b试剂:0.5%硫酸铜溶液:取0.1g硫酸铜,加蒸馏水20ml超声加热溶解。c试剂:0.5%十六烷基三甲基溴化铵(ctab)溶液:取0.1gctab,加蒸馏水20ml超声加热溶解。d试剂:标准海参口服液5ml。试剂盒耗材:试管4支,滴管4支。实验流程:取标准海参口服液和待测海参口服液各1ml分别加入两支试管中,然后每支试管再加入1mla试剂,将两支试管沸水浴10min后,标准海参口服液管变蓝紫色或者紫黑色(现象ⅰ),再分别向两支试管中分别加入1mlb试剂,静置20min,标准海参口服液管分层,上层为橘红色澄清透明(现象ⅱ),下层为蓝黑色沉淀(现象ⅲ),分别取上清液1ml加入新的试管中,然后在新试管中分别加入1mlc试剂,静置5min,标准海参口服液管变浑浊或者产生微量沉淀(现象ⅳ)。实验结果:如果待测海参口服液在检测中依次出现现象ⅰ、ⅱ、ⅲ、ⅳ,则说明待测海参口服液相对为真品,但如果待测海参口服液在检测中有一个及以上现象没有出现则说明待测海参口服液为非真品。海参口服液中的主要成分包括蛋白质、氨基酸和多糖,本发明首先用a试剂,即茚三酮,通过氨基酸的茚三酮显色反应检测海参口服液中氨基酸含量,颜色越深说明氨基酸含量越高;然后加入b试剂,即硫酸铜溶液,通过铜离子沉淀海参口服液中的蛋白质,同时溶液颜色发生变化,检测海参口服液中蛋白质含量,沉淀越多说明蛋白质越多;最后在上清液中加入c试剂,即ctab溶液,通过ctab和酸性多糖的沉淀反应检测海参口服液中多糖的含量。本发明中所用主要试剂茚三酮、硫酸铜、ctab等均为无毒产品,适合普通消费者操作。下面结合实施例对本发明作进一步的说明。实施例1茚三酮-ctab检测海参口服液1.1海参浓缩液的制备海参选自威海刺参,用清水洗净,刨肠称重,切碎后加两倍质量的超纯水,组织匀浆机匀浆10min,得海参匀浆液。加入匀浆液三倍体积pbs缓冲液以及相当于海参质量1%的胃蛋白酶在50℃恒温水浴锅中酶解5h并持续搅拌,保持ph在2-3.5之间,再调整ph至6.8-7.2,加入海参质量1%胰蛋白酶在50℃水浴锅中持续搅拌5h。终止酶解时将水浴锅温度迅速升到90℃以上维持5分钟。将此浓缩液于3800r/min条件下离心25分钟,取上清液,悬蒸浓缩至50ml。1.2海参浓缩液氨基酸含量测定(1)1%茚三酮溶液配制:称取茚三酮1.0000g于盛有100ml纯水的烧杯中使其充分溶解,静置过夜,离心后取其上清液备用。(2)氨基酸标准溶液配制:量取谷氨酸纯品0.2000g,为增加谷氨酸溶解速度,可以先浸泡溶胀后加20ml左右纯水溶解,转入50ml容量瓶中,再用少量纯水冲洗烧杯2到3次,倒入容量瓶中,补充纯水到刻度线处,摇匀,得到4mg/ml的谷氨酸标准溶液。(3)谷氨酸—茚三酮标准曲线绘制:准确吸取4mg/ml的氨基酸标准溶液0.0、0.5、1.0、1.5、2.0、2.5、3.0ml(此时溶液中氨基酸含量为0、2、4、6、8、10、12mg),分别倒入15ml试管中,各加纯水补至4ml,然后加入1%茚三酮溶液2ml,摇匀,在37度条件下水浴加热30分钟,取出后冷却至室温。静置10到15min后,在570nm波长下,以无氨基酸的试剂为空白对照测定其余各浓度标准品溶液的吸光度a。以氨基酸质量为横坐标,吸光度a为纵坐标,绘制标准曲线。样品测定:吸取海参浓缩液100μl,加水补至4ml,加1%茚三酮溶液2ml,与标准品共同放入37℃水浴锅中加热30min,冷却后测定吸光度a值,将a值代入标准曲线中求得样品的氨基酸含量。1.3海参浓缩液多糖含量测定岩藻聚糖硫酸酯标准溶液:称取岩藻聚糖硫酸酯0.0100g于烧杯中,先用20ml水溶解后,转入100ml容量瓶中,用少量纯水洗涤烧杯2到3次,再补充纯水到标线,摇匀,此为0.1mg/ml岩藻聚糖硫酸酯标准溶液。87%浓硫酸配制:量取88.78ml98%浓硫酸,边缓慢加水边搅拌,至补足溶液为100ml。3%半胱氨酸盐酸盐溶液:称取0.3000g半胱氨酸盐酸盐倒入烧杯中,加纯水补至10ml,摇匀。岩藻聚糖硫酸酯—半胱氨酸盐酸盐标准曲线绘制:准确吸取0.1mg/ml的岩藻聚糖硫酸酯标准溶液0、40、80、150、300、450、600、750、850μl(相当于0、4、8、15、30、45、60、75、85μg多糖),分别加到10ml试管中,并加水补充至1ml,冰水浴中加入87%浓硫酸4.5ml,混合均匀,1min后于沸水浴加热10min,取出迅速冷却至室温,加3%半胱氨酸盐酸盐溶液0.1ml,静置90min后,分别在427nm和396nm的波长处测定吸光度,以多糖质量为横坐标,吸光度之差为纵坐标,制成标准曲线。样品多糖含量测定:吸取海参浓缩液上清液10μl,加水补至1ml,按标准曲线制作步骤,与标准品共同沸水浴加热10min,冷却后加3%半胱氨酸盐酸盐0.1ml,静置90min,测定吸光度a,测得的a值代入标准曲线求得样品中多糖含量。1.4茚三酮-ctab试剂盒制备(1)方案一:取海参粗提液200μl加入螺口尿沉渣试管中,补充纯水至4ml,先加1%茚三酮溶液2ml,混匀,静置30min→1h→2h→3h,观察颜色变化,再加入0.5%ctab溶液3ml,静置至沉淀完全沉入试管底端,观察沉淀现象。(2)方案二:取海参粗提液200μl加入螺口尿沉渣试管中,补充纯水至4ml,先加入0.5%ctab溶液3ml,静置至沉淀完全沉入试管底端,观察沉淀现象,再加入1%茚三酮溶液2ml,静置适当时间观察溶液颜色与沉淀变化。(3)方案三:取海参粗提液200μl加入螺口尿沉渣试管中,补充纯水至4ml,同时加入1%茚三酮溶液2ml和0.5%ctab溶液3ml,静置适当时间至溶液现象稳定不再变化,观察颜色与沉淀现象。(4)试剂盒制备:经(1)、(2)、(3)的比对得出试剂加入最佳顺序,取海参粗提液100、200、400、800、1600、3200μl加入螺口尿沉渣试管中,加纯水补至4ml,以最佳顺序加入鉴定试剂,观察记录颜色及沉淀体积(高度)差别与变化。1.5海参口服液鉴定:取市面购买海参口服液若干品牌,倒入螺口尿沉渣试管中,倒入a试剂,混匀,再加入b试剂,静置适当时间至溶液性质稳定后观察现象,经与比色卡比对和沉淀体积读数,辨别口服液真伪。2实验结果2.1海参浓缩液的制备:称取鲜海参111.3g,刨肠清洗并绞碎,经匀浆、酶解、灭活、离心、悬蒸浓缩处理得到50ml棕色液体。2.2谷氨酸-茚三酮标准曲线:标准曲线的数据如表1所示,以490nm处吸光度(a)对氨基酸质量做线性回归,得到标准曲线:a=0.00003c-0.0096,r2=0.9917表1氨基酸标准曲线数据图a570(100μl)=0.159代入标准曲线得c=5620μg/100μl50ml浓缩液中共含氨基酸5620/100*50=2810mg即2810mg/111.3g=25.24mg/g(2.52%)2.3岩藻聚糖硫酸酯-半胱氨酸盐酸盐标准曲线:标准曲线的数据如表2所示,分别在427nm和396nm的波长处测定吸光度,以吸光度之差为纵坐标(a),以多糖质量为横坐标,得到标准曲线:a=0.0143c-0.0344,r2=0.9958表2多糖标准曲线数据图a(10μl)=0.675代入标准曲线得c=49.608μg/10μl50ml浓缩液中共含多糖49.608/10*50=248.04mg即248.04mg/111.3g=2.228mg/g(0.2228%)2.4试剂盒制备方案一实验现象:加入1%茚三酮溶液2ml的试管30分钟后颜色变化不太明显,再过1.5h后样品呈蓝紫色,再静置1h后溶液颜色无明显变化,加入0.5%ctab溶液3ml,迅速生成蓝紫色絮状沉淀,静置1h后,沉淀沉积于试管底部,溶液明显有褪色(如图1所示)。方案二实验现象:加入0.5%ctab溶液3ml后,立即产生白色絮状沉淀,静置1h后,沉淀基本沉积于试管底部,再加入1%茚三酮试剂2ml,静置2h,溶液颜色无明显变化,沉淀颜色也无变化,无法观测比较氨基酸含量。方案三实验现象:同时加入2ml1%茚三酮溶液和3ml0.5%ctab溶液,样品变浑浊,但静置1h后无絮状沉淀沉积,再补加1ml0.5%ctab溶液,产生白色絮状沉淀,静置1h后沉淀沉积,但2h内溶液及沉淀均无颜色变化。比色卡制备:方案一现象明显易辨别且操作简便。取海参粗提液100、200、400、800、1600、3200μl,加纯水补至4ml,先加2ml1%茚三酮溶液,静置2h后观察颜色变化,拍下照片制作比色卡,再加入3ml0.5%ctab静置1h,观察沉淀体积,拍照记录,绘制比色卡。2.5试剂盒的使用方法:市面购买海参口服液a、b、c三款品牌,分别取100μl、500μl、1000μl、2000μl倒入试剂盒中,加水补足4ml,加入a试剂(即1%茚三酮溶液2ml),静置2h后将试管颜色与氨基酸含量比色卡作对比。再加入b试剂(0.5%ctab溶液3ml)静置1h后观察沉淀体积,将沉淀体积读数与多糖标准卡比较辨别口服液真伪。结果如图4所示:从检测结果我们可以看出,品牌a、b、c均含有氨基酸类成分,但是品牌b不含酸性多糖成分,品牌a、c均含有酸性多糖成分,因此我们初步可以推测品牌a、c相对较真,品牌b有可能不是海参口服液。实施例2茚三酮-硫酸铜-ctab检测海参口服液1、海参标准口服液的制备海参用清水洗净,刨肠称重100g,切碎后加两倍质量的超纯水,组织匀浆机匀浆10min,得海参匀浆液。加入匀浆液三倍体积pbs缓冲液以及相当于海参质量1%的胃蛋白酶(市售)在50℃恒温水浴锅中酶解5h并持续搅拌,保持ph在2-3.5之间,再调整ph至6.8-7.2,加入海参质量1%胰蛋白酶在50℃水浴锅中持续搅拌5h。终止酶解时将水浴锅温度迅速升到90℃以上维持5min。将此浓缩液于3800rpm条件下离心25min,取上清液,悬蒸浓缩至100ml,即为海参标准口服液。试剂盒试剂:a试剂:1%茚三酮溶液:取0.2g茚三酮,加蒸馏水20ml超声加热溶解。b试剂:0.5%硫酸铜溶液:取0.1g硫酸铜,加蒸馏水20ml超声加热溶解。c试剂:0.5%十六烷基三甲基溴化铵(ctab)溶液:取0.1gctab,加蒸馏水20ml超声加热溶解。d试剂:标准海参口服液5ml。试剂盒耗材:试管4支,滴管4支。2、市售海参口服液的检测购买市售海参口服液a、b、c三款品牌,分别取1ml加入到试管中,同时步骤1中的海参标准口服液1ml加入到另外一支试管中,加入a试剂(即1%茚三酮溶液2ml),将四支试管沸水浴10min后,标准海参口服液管变蓝紫色或者紫黑色(现象ⅰ),再分别向四支试管中分别加入1mlb试剂(即0.5%硫酸铜溶液),静置20min,标准海参口服液管分层,上层为橘红色澄清透明(现象ⅱ),下层为蓝黑色沉淀(现象ⅲ),分别取各试管上清液1ml加入新的试管中,然后在新试管中分别加入1mlc试剂(即0.5%ctab溶液),静置5min,标准海参口服液管变浑浊或者产生微量沉淀(现象ⅳ)。市售海参口服液a、b、c的现象见表3。表3市售三种海参口服液的试剂盒检测结果海参口服液现象ⅰ现象ⅱ现象ⅲ现象ⅳ综合评价海参标准口服液出现出现出现出现真品品牌a出现出现出现出现真品品牌b出现出现未出现未出现非真品品牌c出现未出现未出现出现非真品同时,我们同时用茚三酮法、考马斯亮蓝法和半胱氨酸盐酸盐法检测了海参标准口服液和以上三个品牌中的氨基酸含量、蛋白质含量和海参多糖的含量,结果见表4。表4市售三种海参口服液的氨基酸、蛋白质和海参多糖含量测定结果海参口服液氨基酸含量蛋白质含量海参多糖含量综合评价海参标准口服液2.42%1.23%0.25%真品品牌a1.85%1.53%0.15%真品品牌b1.25%1.06%未检出非真品品牌c0.38%未检出0.56%非真品从以上结果可以看出本发明的试剂盒可以检测判定海参口服液的真伪,而且与口服液中氨基酸、蛋白质、海参多糖含量基本相符,具有操作简单,使用方便的特点,具有极高的推广价值。实施例3海参提取物与海带提取物的鉴伪试剂配置:1%茚三酮溶液:取0.2g茚三酮,加蒸馏水20ml超声加热溶解。0.5%ctab溶液:取0.1gctab,加蒸馏水20ml超声加热溶解。0.5%硫酸铜溶液:取0.1g硫酸铜,加蒸馏水20ml超声加热溶解。实验加入试剂及反应过程如下表5所示。表5海参提取液与海带提取液加入试剂情况取样液1ml加入试管中,加入1ml茚三酮溶液,沸水浴10min,再加入硫酸铜溶液1ml,静置20min,使沉淀沉降,观察沉淀数量。溶液过滤或取上清液,继续加入1mlctab溶液,静置5min,观察沉淀数量。实验结果:1.加入茚三酮水浴之后,两者均变为紫色,海参提取液颜色明显较深,如图5b;2.加入硫酸铜静置后,两者均变色为橘红色,其中海参提取液产生较多絮状沉淀,海带提取液无明显沉淀,或产生较少沉淀,如图5c;3.取滤液加入ctab后,海参提取液有微量沉淀产生,海带提取液产生微量沉淀,如图5d。上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1