一种基于混合抗体的α1-AT免疫比浊法检测试剂盒及其制备使用方法与流程
本发明涉及基因工程及免疫学测定分析领域,尤其涉及一种基于混合抗体的α1-at免疫比浊法检测试剂盒及其制备使用方法。
背景技术:
α1抗胰蛋白酶(α1-at)是一种糖蛋白,含糖10%-20%,主要由肝脏合成,广泛分布于正常人血清和体液中。α1抗胰蛋白酶是血清中最主要的蛋白酶抑制剂,对凝血酶、尿激酶等其他酶也有抑制作用。α1抗胰蛋白酶也是一种急性时相反应蛋白,在炎症性疾患时,α1抗胰蛋白酶可透过毛细血管进入组织液,在炎症局部往往浓度很高,对急性炎性疾病有一定限制作用。
目前,检测α1-at的方法主要有抗原抗体反应和酶速率法两种。其中,酶速率法检测灵敏度不够,临床检测出现较大偏差,且重复性和稳定性较差,临床难以推广应用。二十世纪九十年代,免疫比浊法作为一种均相测定方法开始用于α1-at测定的常规研究,该方法可于生化仪自动化检测,便于临床检验使用。
单克隆抗体是由单一b细胞克隆产生的高度均一、仅针对某一特定抗原表位的抗体。单克隆抗体的制备,是利用特定抗原处理过的b淋巴细胞与骨髓瘤细胞通过细胞融合的方法得到杂交瘤细胞,经hat培养基筛选、elisa检测效价后就得到阳性克隆株,最后进行细胞培养获将细胞注入到动物腹腔中腹水培养,收集上清液/腹水纯化后就得到单克隆抗体。
由多种抗原决定簇刺激机体,相应地就产生各种各样的单克隆抗体,这些单克隆抗体混杂在一起就是多克隆抗体。多克隆抗体的制备,是将抗原直接注入到动物体内进行免疫,经过3-4次免疫,elisa检测其效价合格后,收集血液离心得到上清液,纯化后即得到多克隆抗体。
目前临床中应用的α1-at的免疫比浊法检测试剂盒,从抗体使用角度,又可分为“多克隆抗体”试剂盒和“单克隆抗体”试剂盒两大类。实际应用发现,多克隆抗体类试剂存在检测特异度较差的问题,而单克隆抗体类试剂存在灵敏度较差的问题。其中,单克隆抗体特异性较高,它能专一性的识别某一特定抗原表位,但它对抗原检测具有低的灵敏度。而多克隆抗体,则正好能与单克隆抗体进行互补,其高灵敏度能够弥补单克隆抗体的低灵敏度问题,但却存在检测特异度差的问题。
据此,目前急需一种同时采用高特异性的单克隆抗体与高敏度的多克隆抗体的基于混合抗体的α1-at免疫比浊法检测试剂盒及其制备使用方法,从而提高对试剂盒样本检测的特异性以及灵敏度。
技术实现要素:
本发明所要解决的技术问题在于提供一种同时采用高特异性的单克隆抗体与高敏度的多克隆抗体的基于混合抗体的α1-at免疫比浊法检测试剂盒及其制备使用方法。
本发明采用以下技术方案解决上述技术问题:
一种基于混合抗体的α1-at免疫比浊法检测试剂盒,包括彼此独立的试剂r1和试剂r2双液体组分;
所述试剂r1包括的成分及相应含量为:hepes20-30g/l,naoh0.2-0.8g/l,nacl5-10g/l,edta-na21-1.2g/l,peg-600010-20g/l,peg-80005-10g/l,吐温200.1-0.6%,nan30.01g/l,其溶剂为纯化水;
所述试剂r2包括的成分及相应含量为:nah2po4·2h2o1-2g/l,na2hpo4·12h2o6-10g/l,nacl5-10g/l,edta-na21-1.2g/l,bsa1-5g/l,抗α1-at混合抗体1-20%,nan30.01g/l,其溶剂为纯化水;
其中,所述抗α1-at混合抗体由抗α1-at单克隆抗体i、抗α1-at单克隆抗体ii以及抗α1-at多克隆抗体iii混合而成。
作为本发明的优选方式之一,所述抗α1-at混合抗体中,抗α1-at单克隆抗体i的含量为0.5-2mg/ml,抗α1-at单克隆抗体ii的含量为0.1-1mg/ml,抗α1-at多克隆抗体iii的浓度为0.1-1mg/ml。
作为本发明的优选方式之一,所述试剂r1包括的成分及相应含量具体为:hepes23.83g/l,naoh0.4g/l,nacl9.0g/l,edta-na21.1g/l,peg-600015g/l,peg-80008g/l,吐温200.5%,nan30.01g/l,其溶剂为纯化水。
作为本发明的优选方式之一,所述试剂r2包括的成分及相应含量具体为:nah2po4·2h2o1.48g/l,na2hpo4·12h2o9.71g/l,nacl9.0g/l,edta-na21.1g/l,bsa2.4g/l,抗α1-at混合抗体10%,nan30.01g/l,其溶剂为纯化水。
作为本发明的优选方式之一,还包括α1-at校准品;所述α1-at校准品包括的成分及相应含量为:nah2po4·2h2o1-2g/l,na2hpo4·12h2o6-10g/l,bsa5-10g/l,海藻糖0.4-4g/l,α1-at蛋白0.1-20g/l,nan30.01g/l,甘油5-15%,其溶剂为纯化水。
作为本发明的优选方式之一,所述α1-at校准品包括的成分及相应含量具体为:nah2po4·2h2o1.48g/l,na2hpo4·12h2o9.71g/l,bsa8g/l,海藻糖2g/l,α1-at蛋白10g/l,nan30.01g/l,甘油10%,其溶剂为纯化水。
作为本发明的优选方式之一,所述抗α1-at混合抗体中的抗α1-at单克隆抗体i、抗α1-at单克隆抗体ii、抗α1-at多克隆抗体iii以及α1-at校准品中的α1-at蛋白均为本领域内可直接购买得到的常规产品。其中,抗α1-at单克隆抗体i与抗α1-at单克隆抗体ii,只要是能与α1-at特异性结合的单克隆抗体,即可。抗α1-at多克隆抗体iii则优选为兔抗α1-at多克隆抗体。
一种上述基于混合抗体的α1-at免疫比浊法检测试剂盒的制备方法,包括如下步骤:
(1)抗α1-at混合抗体的制备
准备两株抗α1-at的单克隆抗体与一株抗α1-at多克隆抗体,即抗α1-at单克隆抗体i、抗α1-at单克隆抗体ii以及抗α1-at多克隆抗体iii;
将所述抗α1-at单克隆抗体i、抗α1-at单克隆抗体ii以及抗α1-at多克隆抗体iii进行混合制成抗α1-at混合抗体,并使得所述抗α1-at混合抗体中,抗α1-at单克隆抗体i的含量为0.5-2mg/ml,抗α1-at单克隆抗体ii的含量为0.1-1mg/ml,抗α1-at多克隆抗体iii的含量为0.1-1mg/ml;
(2)α1-at免疫比浊法试剂盒校准品的制备
①配制试剂r1:
按照试剂r1的组分含量,将各组分物质于同一容器中混合,混合均匀后,制得试剂r1;
②配制试剂r2:
按照试剂r2的组分含量,将步骤(1)制得的抗α1-at混合抗体以及余下的其他组分物质于同一容器中混合,混合均匀后,制得试剂r2;
③配制α1-at校准品:
α1-at校准品的相应成分及相应含量为:nah2po4·2h2o1-2g/l,na2hpo4·12h2o6-10g/l,bsa5-10g/l,海藻糖0.4-4g/l,α1-at蛋白0.1-20g/l,nan30.01g/l,甘油5-15%,其溶剂为纯化水;
按照上述α1-at校准品的组分含量,将各组分物质于同一容器中混合,混合均匀后,制得α1-at校准品。
一种上述基于混合抗体的α1-at免疫比浊法检测试剂盒的使用方法,包括如下具体步骤:
(1)吸取3μl样本,加入240μl试剂r1,37℃孵育3-5min;
(2)再加入60μl试剂r2进行混合,并使其充分反应;
(3)1min后读取吸光值a1,5min后读取吸光值a2,计算δa;
(4)定标方法为6点定标,采用全自动生化分析仪进行检测,并设置校准品浓度分别为:0g/l、0.18g/l、0.37g/l、0.74g/l、1.47g/l和2.94g/l;依据定标值,根据δa测算样本中α1-at含量。
本发明相比现有技术的优点在于:
(1)相比其他方法,本发明利用免疫比浊法测定α1-at,并采用高特异性的单克隆抗体混合高灵敏度的多克隆抗体混合制备获得抗α1-at混合抗体,提高了对样本检测的特异性以及灵敏度;
(2)本发明在试剂r1中采用了peg-6000和peg-8000混合使用,提高了试剂反应的吸光度值,提升了试剂检测的灵敏度;
(3)本发明利用在校准液中添加一定量的甘油和海藻糖,保证了校准液的稳定性,提升了试剂盒检测的准确度。
附图说明
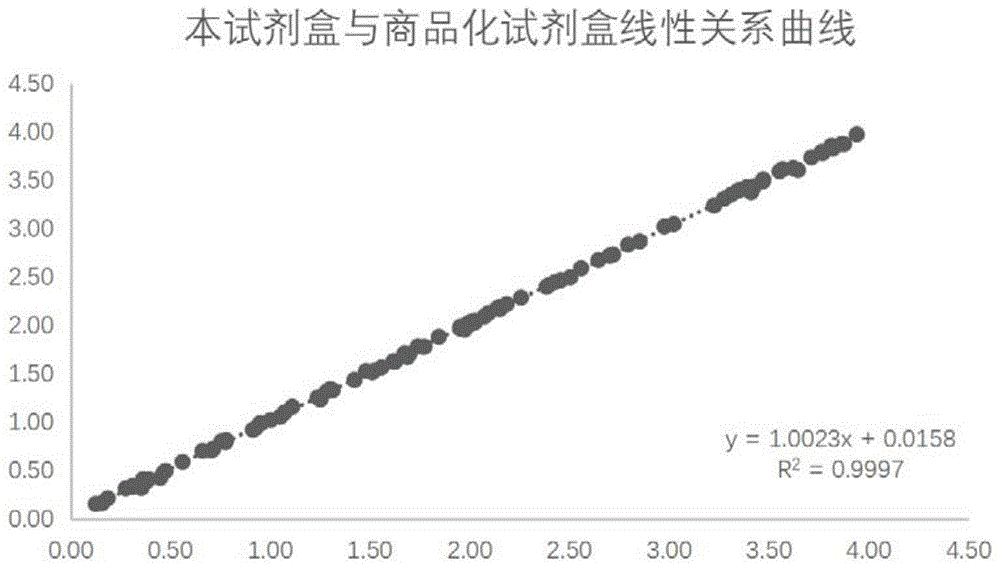
图1是实施例6中本发明试剂盒与商品化α1-at检测试剂盒线性关系曲线图;
图2是实施例6中本发明试剂盒线性范围线性回归图。
具体实施方式
下面对本发明的实施例作详细说明,本实施例在以本发明技术方案为前提下进行实施,给出了详细的实施方式和具体的操作过程,但本发明的保护范围不限于下述的实施例。
实施例1
本实施例的一种基于混合抗体的α1-at免疫比浊法检测试剂盒,包括彼此独立的试剂r1和试剂r2双液体组分。
所述试剂r1包括的成分及相应含量为:hepes20g/l,naoh0.2g/l,nacl5g/l,edta-na21g/l,peg-600010g/l,peg-80005g/l,吐温200.1%,nan30.01g/l,其溶剂为纯化水。
所述试剂r2包括的成分及相应含量为:nah2po4·2h2o1g/l,na2hpo4·12h2o6g/l,nacl5g/l,edta-na21g/l,bsa1g/l,抗α1-at混合抗体1%,nan30.01g/l,其溶剂为纯化水。其中,抗α1-at混合抗体由抗α1-at单克隆抗体i、抗α1-at单克隆抗体ii以及兔抗α1-at多克隆抗体iii混合而成。
进一步地,上述抗α1-at混合抗体中,抗α1-at单克隆抗体i的含量为0.5mg/ml,抗α1-at单克隆抗体ii的含量为0.1mg/ml,兔抗α1-at多克隆抗体iii的浓度为0.1mg/ml。
此外,所述基于混合抗体的α1-at免疫比浊法检测试剂盒还包括α1-at校准品;α1-at校准品包括的成分及相应含量为:nah2po4·2h2o1g/l,na2hpo4·12h2o6g/l,bsa5g/l,海藻糖0.4g/l,α1-at蛋白0.1g/l,nan30.01g/l,甘油5%,其溶剂为纯化水。
实施例2
本实施例的一种基于混合抗体的α1-at免疫比浊法检测试剂盒,包括彼此独立的试剂r1和试剂r2双液体组分。
所述试剂r1包括的成分及相应含量为:hepes30g/l,naoh0.8g/l,nacl10g/l,edta-na21.2g/l,peg-600020g/l,peg-800010g/l,吐温200.6%,nan30.01g/l,其溶剂为纯化水。
所述试剂r2包括的成分及相应含量为:nah2po4·2h2o2g/l,na2hpo4·12h2o10g/l,nacl10g/l,edta-na21.2g/l,bsa5g/l,抗α1-at混合抗体20%,nan30.01g/l,其溶剂为纯化水。其中,抗α1-at混合抗体由抗α1-at单克隆抗体i、抗α1-at单克隆抗体ii以及兔抗α1-at多克隆抗体iii混合而成。
进一步地,上述抗α1-at混合抗体中,抗α1-at单克隆抗体i的含量为2mg/ml,抗α1-at单克隆抗体ii的含量为1mg/ml,兔抗α1-at多克隆抗体iii的浓度为1mg/ml。
此外,所述基于混合抗体的α1-at免疫比浊法检测试剂盒还包括α1-at校准品;α1-at校准品包括的成分及相应含量为:nah2po4·2h2o2g/l,na2hpo4·12h2o10g/l,bsa10g/l,海藻糖4g/l,α1-at蛋白20g/l,nan30.01g/l,甘油15%,其溶剂为纯化水。
实施例3
本实施例的一种基于混合抗体的α1-at免疫比浊法检测试剂盒,包括彼此独立的试剂r1和试剂r2双液体组分。
所述试剂r1包括的成分及相应含量为:hepes23.83g/l,naoh0.4g/l,nacl9.0g/l,edta-na21.1g/l,peg-600015g/l,peg-80008g/l,吐温200.5%,nan30.01g/l,其溶剂为纯化水。
所述试剂r2包括的成分及相应含量为:nah2po4·2h2o1.48g/l,na2hpo4·12h2o9.71g/l,nacl9.0g/l,edta-na21.1g/l,bsa2.4g/l,抗α1-at混合抗体10%,nan30.01g/l,其溶剂为纯化水。其中,抗α1-at混合抗体由抗α1-at单克隆抗体i、抗α1-at单克隆抗体ii以及兔抗α1-at多克隆抗体iii混合而成。
进一步地,上述抗α1-at混合抗体中,抗α1-at单克隆抗体i的含量为1.5mg/ml,抗α1-at单克隆抗体ii的含量为0.5mg/ml,兔抗α1-at多克隆抗体iii的浓度为0.5mg/ml。
此外,所述基于混合抗体的α1-at免疫比浊法检测试剂盒还包括α1-at校准品;α1-at校准品包括的成分及相应含量为:nah2po4·2h2o1.48g/l,na2hpo4·12h2o9.71g/l,bsa8g/l,海藻糖2g/l,α1-at蛋白10g/l,nan30.01g/l,甘油10%,其溶剂为纯化水。
实施例4
本实施例的一种上述实施例1-3中基于混合抗体的α1-at免疫比浊法检测试剂盒的制备方法,包括如下步骤:
(1)抗α1-at混合抗体的制备
准备两株抗α1-at的单克隆抗体与一株抗α1-at多克隆抗体,即抗α1-at单克隆抗体i、抗α1-at单克隆抗体ii以及抗α1-at多克隆抗体iii;
将所述抗α1-at单克隆抗体i、抗α1-at单克隆抗体ii以及抗α1-at多克隆抗体iii进行混合制成抗α1-at混合抗体,并使得抗α1-at混合抗体中抗α1-at单克隆抗体i、抗α1-at单克隆抗体ii与抗α1-at多克隆抗体iii的含量分别对应上述实施例;
(2)α1-at免疫比浊法试剂盒校准品的制备
①配制试剂r1:
按照试剂r1的组分含量,将各组分物质于同一容器中混合,混合均匀后,制得试剂r1;
②配制试剂r2:
按照试剂r2的组分含量,将步骤(1)制得的抗α1-at混合抗体以及余下的其他组分物质于同一容器中混合,混合均匀后,制得试剂r2;
③配制α1-at校准品:
按照α1-at校准品的组分含量,将各组分物质于同一容器中混合,混合均匀后,制得α1-at校准品。
实施例5
本实施例的一种上述实施例1-3中基于混合抗体的α1-at免疫比浊法检测试剂盒的测试使用方法。
分析方法:两点终点法;
反应方向:上升反应;
校准方式:logit-log(4p)或spline处理;
测定波长:340nm;
测定温度:37℃;
样本:试剂r1:试剂r2=3:240:60(μl)
测试步骤:吸取3μl样本,加入240μl试剂r1,37℃孵育3-5min,加入60μl试剂r2,1min后读取吸光值a1,5min后读取吸光值a2,计算δa。
定标方法:6点定标,采用日立7180全自动生化分析仪(或其他品牌型号),进行检测,设置校准品浓度分别为:0、0.18、0.37、0.74、1.47和2.94g/l。
依据定标值根据δa测算样本中α1-at含量。
实施例6
本实施例用以评价上述实施例中基于混合抗体的α1-at免疫比浊法检测试剂盒:
(1)线性相关性验证:
利用实施例3配方配制试剂,与国家食品药品监督管理总局认可的某上市公司的α1-at检测试剂盒进行对照检测,检测100份临床血清样本,检测结果如下表1,获得了本发明试剂盒与上市某公司在售α1-at检测试剂的相关性曲线(见图1;图1中,横坐标代表上市某公司在售α1-at检测试剂的检测结果值,单位g/l;纵坐标代表本发明试剂盒的检测结果值,单位g/l),通过检测结果显示,两试剂盒的线性相关曲线为y=1.0087-0.0653x,相关系数r2=0.9897,说明两者较大的相关性。
表1本发明试剂盒与某上市公司在售α1-at检测试剂盒线性相关性比对值
(2)线性范围验证
使用重组α1-at和生理盐水配制成浓度4.0g/l、2.0g/l、1.0g/l、0.5g/l和0g/l(生理盐水对照)的测试品,使用本发明试剂盒测定各测试品浓度,以稀释浓度为自变量,以测定结果为因变量求出线性回归方程(见图2;图2中,横坐标代表稀释浓度,单位g/l;纵坐标代表测定浓度,单位g/l),计算测定结果的相对偏差。检测与计算结果如表2所示,结果显示,测定结果与稀释浓度之间的线性回归方程为y=0.9575+0.0318x,相关系数r2=0.9999,说明线性关系良好,线性范围可达4g/l。
表2本发明试剂盒线性范围验证
(3)准确度验证
取具有溯源性高值血清质控和低值血清质控各一份,使用所述试剂盒检测10次,取均值,与质控靶值进行比对。结果表明检测值较靶值相对偏差较小,准确度较高,见表3。
表3所述试剂盒准确度验证结果
(4)精密度验证
取经在售试剂盒检测的临床血清样本高值和低值各一份,使用所述试剂盒对同一份血清样本连续检测10次,计算所述试剂盒的变异系数。精密度检测数据如下表4,检测结果表明所述试剂盒在检测高值和低值样本时的变异系数较小分别为0.34%和1.73%,精密度较好。
表4所述试剂盒精密度验证结果
(5)灵敏度及特异度验证
采用进口间接elisa法α1-at检测试剂盒检测筛选50份阳性血清50份阴性血清,选择市售采用抗α1-at多克隆抗体制备的免疫比浊法试剂盒、市售采用抗单克隆抗体制备的免疫比浊法试剂盒与所述试剂盒同步检测此100份血清样本,按各试剂盒判定标准设高于参考标准为阳性,低于参考标准为阴性,以进口间接elisa法检测试剂盒为金标准计算各试剂盒的灵敏度和特异度,结果见表5。结果表明,所述试剂盒较市售两款试剂盒有较高的灵敏度及特异度。本发明的突出优点是较单克隆抗体制备试剂盒有更高的灵敏度且较多克隆抗体制备的试剂盒有更高的特异度,从而大大地提高临床检测的准确性满足临床检测的需求。
表5所述试剂盒灵敏度及特异度与市售试剂盒比较
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!