miR‑135b抑制剂在治疗骨肉瘤肺转移和复发的药物中的用途的制作方法
本发明涉及一种miR-135b抑制剂在治疗骨肉瘤肺转移和复发的药物中的用途。
背景技术:
骨肉瘤是致残率和致死率较高的、主要发生在10-25岁年龄段的原发性恶性骨肿瘤。上世纪80年代初,骨肉瘤患者的5年生存率已达到60%-70%,但近30年没有得到进一步提升。导致骨肉瘤治疗失败的主要原因是转移和复发。据报告,骨肉瘤患者一旦发生转移或复发其生存率仅为20-30%。肺转移是骨肉瘤转移的主要方式。在初诊患者中有20%的患者出现远处转移,其中90%为肺转移;接受正规治疗的患者中有50%的患者出现复发,其中80%为肺转移型复发,提示解决骨肉瘤肺转移和复发可以进一步提高骨肉瘤患者的5年生存率。但目前还没有方法可以有效的治疗骨肉瘤的肺转移和复发。
随着分子生物学技术的发展,人们对肿瘤的发生发展机制有了更深入的了解,并依据肿瘤发生发展中涉及的异常分子和基因,设计和研制针对特定分子和基因靶点的药物,选择性杀伤肿瘤细胞,这种方法叫肿瘤分子靶向治疗。今年来,肿瘤分子靶向治疗已经成为肿瘤治疗的发展方向,肿瘤分子靶向药物的研究和临床应用使肿瘤治疗水平提高到一个新的高度。
肿瘤干细胞是指肿瘤中具有自我更新能力并产生异质性肿瘤细胞的细胞群,导致肿瘤的耐药、转移和复发,是肿瘤靶向治疗的一个重要靶点。肿瘤干细胞由很多因素来调控;miRNA是其中一个调控因素。miRNA是指由19-22个核苷酸组成的、非编码蛋白的RNA,通过对目标基因信使RNA的降解和翻译抑制对细胞生长、发育、分化、死亡等生物过程起着重要的作用。研究表明,人类基因中有1/3的基因直接收到miRNA的调控,更重要的是最近研究表明包括骨肉瘤在内的大部分肿瘤中存在miRNA的异常表达,而且异常表达的miRNA与肿瘤的发生、发展和患者的预后密切相关。更重要的是靶向此类异常表达的miRNA可以有效的抑制肿瘤的进展。
miR-135b是一种已知道的微小RNA,其相关基本信息为:Accession No:MIMAT0000758,基本序列为5`-UAUGGCUUUUCAUUCCUAUGUGA-3`。已有研究报告表明miR-135b在前列腺癌,肺癌,直肠癌,肝癌和骨肉瘤中异常表达,且起促癌的作用。然而,其对骨肉瘤的肺转移和复发中的影响还未见报道。本发明首次发现miR-135b可以作为治疗骨肉瘤肺转移和复发的靶点,miR-135b的抑制剂可用于治疗骨肉瘤。
已有大量实体瘤相关研究显示,肿瘤原发灶与转移灶之间在组织特点、蛋白质组表达、细胞生物学行为等多个方面存在较多区别。利用免疫组化和基因测序技术对骨肉瘤患者原发病灶组织与转移灶组织进行检测对比,分析发现,患者原发病灶与骨转移病灶之间的生物学信息以及基因表达具有相似性。但部分转移灶,特别是肺转移灶在组织学和基因表达上与原发病灶具有较大差异。因此在治疗时,极有可能出现对原发病灶有效,而转移病灶无效的情况,反之亦然。在JAFFE等的研究中以阿霉素、顺铂、甲氨蝶呤、异环磷酰胺(ADM,DDP,MTX,IFO)为主大剂量化疗对骨肉瘤原发疾病取得了74%的5年生存率,但在转移或复发患者中明显疗效更低。这也从侧面证明了对原发灶与转移灶的治疗需要进一步的区分、细化,才能获得最佳效果。
技术实现要素:
本发明的目的在于解决目前骨肉瘤肺转移和复发治疗困难的问题,提供了一种miR-135b抑制剂在治疗骨肉瘤肺转移和复发的药物中的用途,所述用途以促进骨肉瘤肺转移和复发的miR-135b作为治疗靶点,利用miR-135b的抑制剂来治疗骨肉瘤肺转移和复发,其中miR-135b抑制剂包括miR-135b的antisense或antagomiR或表达miR-135b antisense的质粒。miRNA antagomiR是经过特殊化学修饰的miRNA抑制剂,与普通的miRNA抑制剂(antisense)相比,antagomiR在动物体内具有更高的稳定性,其作用时间可长达数周。
本发明利用转染阴性对照核苷酸链和miR-135b antisense的骨肉瘤肿瘤干细胞建立了负瘤动物模型,并观察了miR-135b抑制剂对肿瘤干细胞致瘤的影响。实验结果表明miR-135b抑制剂可以有效抑制肿瘤干细胞的肿瘤形成。
本发明还利用具有强转移能力的骨肉瘤细胞系建立了低表达miR-135b的稳定细胞系,并利用此细胞株建立了骨肉瘤肺转移模型。通过尾静脉注射建立骨肉瘤肺转移模型4周以后,将小鼠处死,取出肺观察了肺表面形成的肿瘤,并通过制作石蜡切片和H&E染色在显微镜下评估了骨肉瘤的肺转移程度。实验结果表明miR-135b的抑制可以显著的抑制骨肉瘤细胞的肺转移。
此外,本发明还利用骨肉瘤肿瘤干细胞建立了负瘤模型,并腹腔注射的方式处理了顺铂和对照antagomiR或miR-135b antagomiR。18天以后停止药物处理,并继续观察了肿瘤大小的变化。实验结果显示,停药后经过一定时间后顺铂和对照组antagomiR的处理组肿瘤从新开始生长(复发),但在顺铂和miR-135b antagomiR处理组并没有发现此种现象。
本发明还涉及miR135b抑制剂在制备治疗骨肉瘤转移和复发的药物中的用途,所述的miR-135b抑制剂包括单链RNA和表达此单链RNA的质粒,单链RNA的具体序列为5`-UCACAUAGGAAUGAAAAGCCAUA-3`,所述RNA可以是经过修饰的RNA。
其中所述药物除包含miR-135b抑制剂,还可以包含药物学上常见的药物载体,其中所述载体是注射溶媒、等渗调节剂、pH调节剂、稳定剂、保护剂等。
所述药物可以制备成常见的剂型,例如注射剂、颗粒剂、片剂、胶囊、气雾剂等,所述注射剂可以是溶液型、混选型、或乳剂型,可以通过皮下注射、肌肉注射、静脉注射或静脉滴注的方式给药。
注射溶媒选自注射用水、注射用油、乙醇、甘油、聚乙二醇等;所述等渗调节剂选自氯化钠、氯化钾、葡萄糖、碳酸氢钠、乳酸钠、甘油等,氯化钠浓度范围一般为0.5-0.9%,葡萄糖浓度范围一般为4-5%,甘油浓度范围一般为2.25%左右;所述的pH调节剂选自乳酸、柠檬酸、磷酸氢二钠、磷酸二氢钠、磷酸、碳酸钠、碳酸氢钠等,乳酸的浓度范围一般为0.1%左右,柠檬酸的浓度一般为0.5%左右,磷酸氢二钠和磷酸二氢钠的浓度一般为1.7%和0.71%左右,碳酸钠、碳酸氢钠的浓度一般为0.06%和0.005%左右;所述稳定剂选自肌酐、甘氨酸、肌酐的浓度一般为0.5-0.8%,甘氨酸的浓度一般为1.5-2.25%;所述保护剂选自乳糖、蔗糖、麦芽糖、人血白蛋白,乳糖的浓度一般为2-5%,蔗糖的浓度一般为2-5%,麦芽糖的浓度一般为2-5%,人血白蛋白浓度一般为0.2-2%。
附图说明
通过阅读参照以下附图所作的对非限制性实施例所作的详细描述,本发明的其它特征、目的和优点将会变得更明显:
图1.把转染阴性对照核苷酸链和miR-135b抑制剂(miR-135b antisense)的骨肉瘤肿瘤干细胞接种到裸鼠背部皮下以后,观察其是否成瘤。结果显示,转染阴性对照核苷酸链的肿瘤干细胞在裸鼠体内形成了肿瘤,但转染miR-135bantisense的肿瘤干细胞没有形成肿瘤。
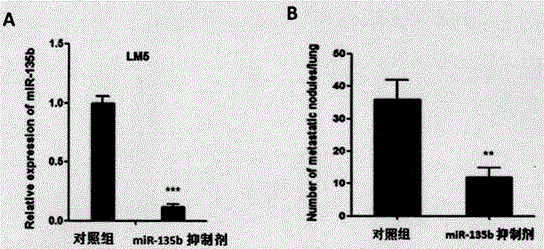
图2.通过尾静脉注射的方式利用稳定表达miR-135bantisense的骨肉瘤细胞及其对照组细胞建立骨肉瘤肺癌转移模型。注射细胞4周以后,处死实验动物取肺,观察肺表面形成的肿瘤。其中,图2A显示骨肉瘤细胞中的miR-135b表达。图2B显示,抑制miR-135b可以明显抑制骨肉瘤细胞的肺转移。
图3.从骨肉瘤肺转移动物模型中取出肺,进行固定,H&E染色,可见处理抑制miR-135b可以明显抑制骨肉瘤的肺转移。
图4.利用肿瘤干细胞建立骨肉瘤的裸鼠负瘤模型,并通过腹腔注射的方式处理了磷酸缓冲盐溶液(untreated)或顺铂和阴性对照antogomiR(CDDP)或顺铂和miR-135b antagomiR(CDDP-miR-135b-in)。18天以后,停止药物处理并观察了24天。结果显示,磷酸缓冲盐溶液处理组的肿瘤在整个实验期内处于生长状态;顺铂加miR-135b antagomiR处理组的肿瘤生长在药物处理期内处于负生长状态、在停药后处于停止生长状态;顺铂加对照antagomiR的处理组的肿瘤在停药12天以后开始从新生长。
图5.从裸鼠负荷瘤模型中取出肿瘤以后,为了观察抑制miR-135b对肿瘤细胞增殖的影响,利用Ki67抗体进行了免疫组化。结果显示,抑制miR-135b可以明显抑制肿瘤的增殖。
附图中相同或相似的附图标记代表相同或相似的部件。
具体实施方式
下文的公开提供了许多不同的实施例或例子用来实现本发明的不同结构。为了简化本发明的公开,下文中对特定例子的部件和设置进行描述。此外,本发明可以在不同例子中重复参考数字和/或字母。这种重复是为了简化和清楚的目的,其本身不指示所讨论各种实施例和/或设置之间的关系。应当注意,在附图中所图示的部件不一定按比例绘制。本发明省略了对公知组件和处理技术及工艺的描述以避免不必要地限制本发明。
实施例1:miR-135b antisense的处理显著抑制骨肉瘤肿瘤干细胞在动物中的肿瘤形成
(1)利用肿瘤干细胞标志蛋白CD133的抗体,通过流式的方法从骨肉瘤细胞Saos-2中筛选CD133高表达的肿瘤干细胞。
(2)上述筛选的CD133高表达的肿瘤干细胞分为两个组,其中一组细胞转染阴性对照核苷酸链(对照组);另一组细胞转染miR-135b antisense(处理组)。
(3)转染12小时以后,把被转染的细胞接种到5只6周龄的母裸鼠背部皮下(1×105个细胞/只小鼠)。对照细胞接种到裸鼠的背部右侧;处理组细胞接种到裸鼠背部的左侧,并观察了2个月。接种细胞两个月以后发现对照组(右侧)全部形成了肿瘤,但转染miR-135b antisense的细胞没有形成肿瘤(左侧)(图1)。
实施例2:miR-135b antisense显著抑制骨肉瘤的肺转移
(1)为了构建骨肉瘤肺转移动物模型首先建立了低表达miR-135b的稳定骨肉瘤细胞系。
在六孔板中以1×106细胞/孔的密度接种LM5骨肉瘤细胞。细胞铺板第二天,把表达miR-135b antisense的质粒或表达非特异性核苷酸单链的对照组质粒转染到细胞中。转染48小时以后开始稳定细胞的筛选。细胞用2ug/ml嘌呤霉素每三天处理一次,共处理3次。筛选第十二天,收部分细胞,提RNA检测miR-135b的表达量。确定miR-135b低表达以后(图2A),利用此系稳定细胞建立骨肉瘤肺转移动物模型。
(2)建立骨肉瘤肺转移模型。将4×105个低表达miR-135b的LM5骨肉瘤稳定细胞系及其对照组细胞通过尾静脉注射到6周玲母裸鼠体内(8只裸鼠/组);4周以后把裸鼠处死,取肺,在显微镜下数肺表面形成的肿瘤数,并固定、切片、H&E染色。结果显示,抑制miR-135b显著的减少了骨肉瘤的肺转移(图2B和图3)。
实施例3:miR-135b antagomiR显著抑制肿瘤干细胞引起的骨肉瘤复发。建立裸鼠负荷瘤模型:利用肿瘤干细胞标志蛋白CD133的抗体通过流式的方法从Saos-2骨肉瘤细胞中选出CD133高表达的肿瘤干细胞,并把此细胞接种到18只6周龄母裸鼠背部皮下(1×105个细胞/只小鼠)。两周以后按照肿瘤大小把裸鼠分为三个处理组,并通过腹腔注射的方法处理药物。第一组注射了磷酸缓冲盐溶液(100ul)(untreated);第二组动物注射了顺铂(5mg/Kg体重)和10uM阴性对照核苷酸链(CDDP);处理组动物注射了顺铂和10uM miR-135b antagomiR(CDDP-miR-135b-in)。药物处理每三天一次,共处理了6次;肿瘤大小每三天测量一次。药物处理结束以后再观察了24天。实验结果显示,药物处理结束12天后,处理对照核苷酸链和顺铂的对照组动物的肿瘤开始重新生长,但处理miR-135bantagomiR和顺铂的处理组动物的肿瘤仍处于停止生长状态(图4)。近一步,细胞增殖标志物蛋白Ki67的免疫组化结果显示miR-135antagomiR处理显著的抑制了肿瘤细胞的增殖(图5)。免疫组化的具体方法如下:
免疫组化:药物处理4次以后,从每个处理组选3只动物处死,取出肿瘤组织用多聚甲醛固定做石蜡切片、免疫组化。(将石蜡切片放于60℃的烘烤箱中烘烤2-3个小时;二甲苯浸泡10分钟;二甲苯浸泡10分钟;二甲苯浸泡10分钟;90%乙醇浸泡10分钟;80%乙醇浸泡10分钟;自来水洗2分钟;蒸馏水洗1分钟;3%的H2O2中孵育10分钟;PBS清洗2次,5分钟/次;擦干玻片,滴加一抗,于4℃冰箱过夜;第二天取出,PBS清洗2次,5分钟/次;滴加二抗,37℃孵育25-30分钟;PBS清洗2次,5分钟/次;滴加DAB显色;充分水洗,终止显色;苏木素显色液体中浸泡1分钟,并冲洗;盐酸酒精冲洗;饱和碳酸锂冲洗;95%酒精1分钟;无水酒精1分钟;无水酒精2分钟;取出片子吹干;滴加封片油封片。
虽然关于示例实施例及其优点已经详细说明,应当理解在不脱离本发明的精神和所附权利要求限定的保护范围的情况下,可以对这些实施例进行各种变化、替换和修改。对于其他例子,本领域的普通技术人员应当容易理解在保持本发明保护范围内的同时,工艺步骤的次序可以变化。
此外,本发明的应用范围不局限于说明书中描述的特定实施例的工艺、机构、制造、物质组成、手段、方法及步骤。从本发明的公开内容,作为本领域的普通技术人员将容易地理解,对于目前已存在或者以后即将开发出的工艺、机构、制造、物质组成、手段、方法或步骤,其中它们执行与本发明描述的对应实施例大体相同的功能或者获得大体相同的结果,依照本发明可以对它们进行应用。因此,本发明所附权利要求旨在将这些工艺、机构、制造、物质组成、手段、方法或步骤包含在其保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!