一种增强免疫力的药物组合物及其应用的制作方法
本发明属于药物组合物技术领域,具体的说,涉及一种增强免疫力的药物组合物及其应用。
背景技术:
中医药用于养生治病已有二千多年的历史。伴随着社会的进步、竞争的激烈,如今的人们工作压力更大,导致人体体质下降,人体的疫力也同样的下降,处于一种亚健康状态,因此人们对提高机体免疫力的产品需求量与日俱增。而增强机体免疫力的产品已经不满足于生化类产品,更多地青睐于植物和中药提取物的产品。
技术实现要素:
为解决以上技术问题,本发明的目的在于提供一种增强免疫力的药物组合物及其应用,产品具有增强人体免疫力的功效。
本发明目的是这样实现的:一种增强免疫力的药物组合物,其关键在于由以下重量份数的原料组成:
天麻340~360份、
灵芝340~360份、
酸枣仁600~650份、
柏子仁250~300份。
上述原料中还添加有辅料,该辅料由150~155份乳糖、58~62份甘露醇、58~62份微晶纤维素、22~27份羧甲基淀粉钠和2~3份硬脂酸镁组成,所述原料和辅料混合最终制成片剂。
上述原料由350份天麻、350份灵芝、625份酸枣仁、275份柏子仁组成,所述辅料由152.5份乳糖、60份甘露醇、60份微晶纤维素、25份羧甲基淀粉钠和2.5份硬脂酸镁组成。
上述的一种增强免疫力的药物组合物的制片方法由以下步骤组成:先将天麻切片,并将酸枣仁炒制,然后将天麻、灵芝、酸枣仁和柏子仁按重量份数混合,并加入10倍原料总重量的水,并熬煮提取两次,两次的滤液浓缩至相对密度为1.2~1.3后,于65~75℃下真空干燥成干浸膏,粉碎成浸膏粉,按重量份数将辅料与浸膏粉混合均匀后,制粒干燥,最后压片得到片剂。
一种增强免疫力的药物组合物在制备用于增强免疫力的药物中的应用。
一、本发明原料公知的药理作用如下:
1、天麻:块茎入药,味甘性平,归肝经,天麻的化学成分包括酚性化合物及其苷类(天麻苷)、甾醇和有机酸类(琥珀酸、β-谷甾醇、柠檬酸、棕榈酸等)、多糖类及其他成分;具有息风止痉,平肝阳,祛风通络的功效。
2、灵芝:真菌的干燥子实体入药,味淡性温,归心、肺、肝、肾经,灵芝的主要生理活性成分有灵芝多糖、三萜类化合物、蛋白质、多肽、核苷类、呋喃类、甾醇、生物碱和氨基酸等。而其中的灵芝多糖、三萜类化合物和蛋白质是灵芝的主要活性成分;具有益气血、安心神、健脾胃的功效。
3、酸枣仁:成熟种子入药,味甘、酸,性平,归肝胆心经,酸枣仁的化学成分主要包括脂肪酸类、皂苷类、黄酮类、生物碱以及氨基酸等;具有补肝、宁心、敛汗、生津的功效。
4、柏子仁:成熟种子入药,味甘性平,归心肝脾经,柏子仁含大量脂肪油并含少量的挥发油、皂苷、植物甾醇、维生素A、蛋白质等。具有养心安神、敛汗、润肠通便的功效。
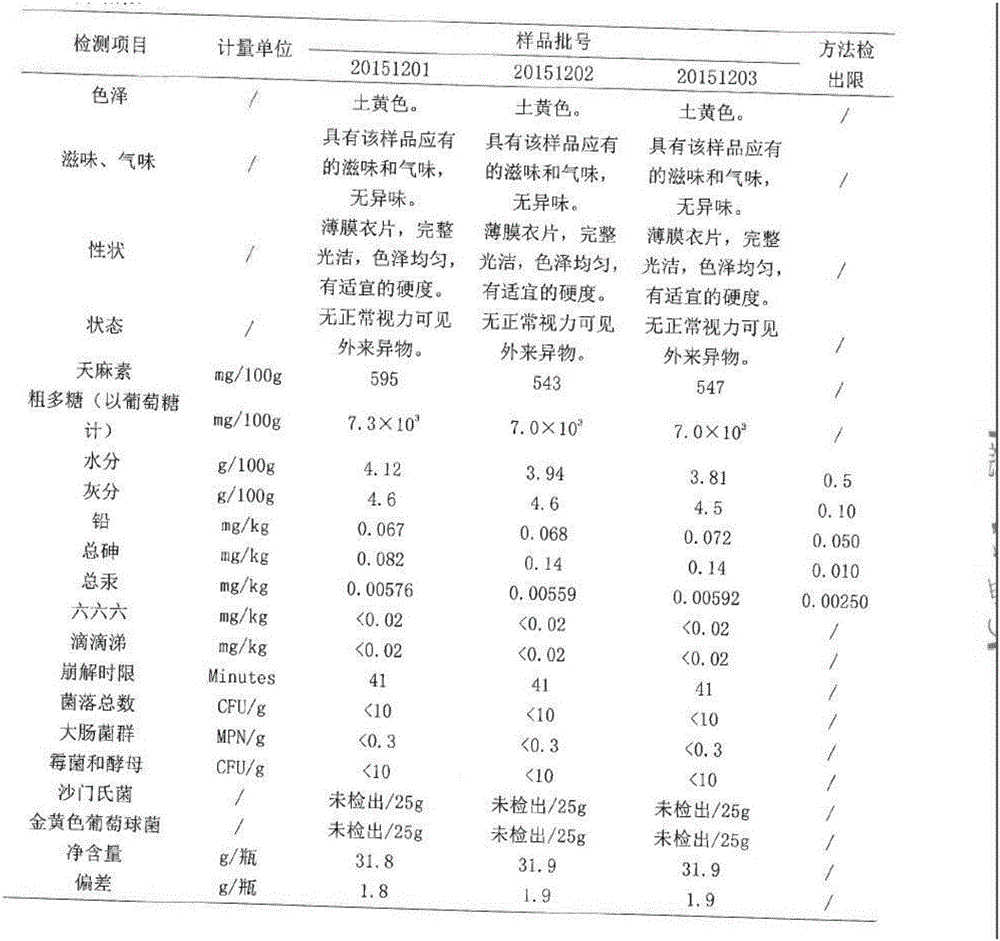
二、样品放置条件:温度37±0.2℃,相对湿度75±0.2%,密闭保存0天、l个月、2个月、3个月各测1次,共测4次。结果分别如图1和2和3和4所示:由图1~4可见,本申请制备的片剂于密闭、阴凉干燥处放置,保质期为24个月,色、味、形状和状态等均正常。
三、天麻、灵芝、酸枣仁和柏子仁配伍具有增强人体免疫力的作用。
1、材料和方法:
1.1样品:本申请制片方法得到的片剂,样品核准净含量为0.5g/片×60片/瓶。人体推荐剂量为:每日2.0/60kgBW,去包衣颗粒推荐剂量为:每日1.94g/60kgBW。以下使用的样品均为本申请片剂去3%包衣分的颗粒。
1.2实验动物:动物选用16~18g清洁级雌性小鼠192只,共分为四批进行试验,每批分四组,每组12只,试验一批进行脏器/体重比值测定、迟发型变态反应实验、半数溶血值(HC50)的测定和抗体生成细胞数的测定;试验二批进行碳廊清试验;试验三批进行小鼠腹腔巨噬细胞吞噬鸡红细胞实验;试验四批进行ConA诱导的小鼠淋巴细胞转化实验和NK细胞活性测定。
1.3剂量:本申请片剂的推荐剂量为成人每日1.94g,相当于0.0323g/kgBW/d,实验设人体推荐量的5倍、10倍、30倍,即每日0.16g/kgBW、0.32g/kgBW、0.97g/kgBW为低、中、高剂量组。受试物配制:称取5.82g样品加无菌水至60mL为高剂量受试物;称取1.92g样品加无菌水至60mL为中剂量受试物;称取0.96g样品加无菌水至60mL为低剂量受试物;受试物每日一次经口给予,连续灌胃31天后,测各项指标。小鼠灌胃体积为10mL/kgBW。同时设一空白对照组0g/kgBW,用无菌水代替受试物,每日灌胃体积与各受试物组相同。各剂量组均给予维持饲料。
1.4试验方法:
1.4.1脏器体重比值的测定
小鼠称重后颈椎脱臼处死,取脾脏和胸腺,去尽筋膜,用滤纸吸干脏器表面血污,称重,计算脾脏体重比值和胸腺体重比值。
1.4.2迟发型变态反应(DTH)试验(足跖增厚法)
取羊血,生理盐水洗涤3次,每只小鼠经腹腔注射2%(v/v,用生理盐水配制)SRBC悬液(2000r/min,10min)0.2mL,致敏后4天,测量左后足跖部厚度,然后在测量部位皮下注射20%(v/v,用生理盐水配制)SRBC悬液20μL,于注射后24h测量左后足跖部厚度,以上两次测量均为同一部位测量三次,取平均值,以攻击前后足跖厚度的差值来表示DTH的程度,受试样品组的撤职显著高于对照组的差值,可判定该项实验结果阳性。
1.4.3ConA诱导的小鼠淋巴细胞转化实验(MTT法)
无菌取脾,置于盛有适量无菌Hank’s液洗2次,每次离心5min(1000r/min),然后将细胞悬浮于1mL的完全培养液中镜检计数,调整细胞浓度为3×106个/mL,再将脾细胞悬液分两孔加入24孔培养板中,没空1.0mL,在其中一孔加75μL ConA液(相当于7.5μg/mL),另一孔作为对照,置二氧化碳培养箱中5%二氧化碳,37℃培养72h。培养结束前4h,每孔轻轻吸去上清液0.7mL不含小牛血清的RPMII640培养液,同时加入MTT 50μL/孔,继续培养4h,培养结束后,每孔加入1mL酸性异丙醇,吹打混匀,使紫色结晶完全溶解,然后将此液体移入比色杯中,在分光光度计上比色测定,波长570nm,淋巴细胞的增殖能力用加ConA孔的光密度值减去不加ConA孔的光密度值差值表示,受试样品组的光密度差值显著高于对照组的光密度差值,可判定该项实验结果阳性。
1.4.4抗体生成细胞数的测定
取羊血,生理盐水洗涤3次,每只小鼠经腹腔注射2%(v/v,用生理盐水配制)SRBC悬液0.2mL,将SRBC免疫5天后的小鼠颈椎脱臼处死,取出脾脏,轻轻磨碎脾脏,制成细胞悬液,离心5min,用Hank’s液洗2遍,最后将细胞悬浮在8mL Hank’s液中,将琼脂糖加热溶解后,与等量双倍Hank’s液混合,分装小试管,每管0.5mL,再向管内加10%(v/v,用SA液配制)SRBC悬液μL、脾细胞悬液8μL,迅速混匀后,倾倒于已刷琼脂糖薄层的玻片上,作平行片,待琼脂凝固后,将玻片水平扣放于片架上,放入二氧化碳培养箱中37℃温育1h,然后用SA缓冲液稀释的补体)(1:8)加入到玻片架凹槽内,继续温育1.5h后,计数溶血空斑数。可反映抗体生成细胞数用空斑数/全脾细胞来表示。受试样品组的空斑数显著高于对照组的空斑数,可判定该项实验结果阳性。
1.4.5半数溶血值的测定
取羊血,生理盐水洗涤3次,每只小鼠经腹腔注射2%(v/v,用生理盐水配制)SRBC悬液0.2mL,将SRBC免疫5天后摘除眼球取血于离心管内,放置约1h,将凝固血于管壁剥离,使血清充分析出,离心收集血清,SA缓冲液稀释血清300倍,取1.0mL置试管内,依次加入10%(v/v,用生理盐水配制)SRBC悬液0.5mL,补体1.0mL,另设不加血清的对照管,置37℃恒温水浴中保温15min后,冰浴终止反应。离心取上清1mL,加Hb稀释液3.0mL,同时取10%(v/v,用SA缓冲液配制)的SRBC悬液0.25mL,加Hb稀释液至4mL,于另一试管中,充分混匀,放置10min后,于540nm处以对照管作空白,分别测定各管光密度值,溶血素的量以半数溶血值表示,按下式计算:
样品半数溶血值=样品光密度值/SRBC半数溶血时的光密度值×稀释倍数
受试样品组的HC50显著高于对照组的HC50,可判定该项实验结果阳性。
1.4.6小鼠碳廊清实验
按体重从小鼠尾静脉注射稀释4倍的印度墨汁,待墨汁注入,立即计时,注入墨汁后10min,分别从内呲静丛取血20μL,并将其加到2.0mL 0.1%Na2CO3溶液中,用分光光度计在600nm波长处测定光密度值,以0.1%Na2CO3溶液作为空白对照,将小鼠处死,取肝脏和脾脏称重,以吞噬指数(a)表示小鼠碳廊清的能力按下式计算a:其中k=(lgOD1-lgOD2)/(t2-t1);a=体重+(肝重+脾重)×k1/3。受试样品组的吞噬指数显著高于对照组的吞噬指数,可判定该项实验结果阳性。
1.4.7小鼠腹腔巨噬细胞吞噬鸡红细胞实验
小鼠腹腔注射20%(v/v,用生理盐水配制)鸡红细胞悬液1mL,间隔30min,颈椎脱臼处死,经处理后,取腹腔巨噬细胞洗液1mL,分别于2片载玻片上,放入垫有湿纱布的搪瓷盒内,移置37℃温育30min,漂洗,去除未贴片细胞,晾干,以1:1丙酮甲醇溶液固定,染色,再用蒸馏水漂洗晾干,油镜下计数,每片计数100个巨噬细胞,按下式计算吞噬率和吞噬指数:
吞噬百分率(%)=吞噬鸡红细胞的巨噬细胞数/计数的巨噬细胞数×100%
吞噬指数=被图示的鸡红细胞总数/计数的巨噬细胞数
得出的吞噬百分率再按下式进行数据转换,式中P为吞噬百分率,用小数表示,所得数据为计量资料,受试样品组的吞噬百分率和吞噬指数均显著高于对照组的吞噬百分率和吞噬指数,可判定该项实验结果阳性。
1.4.8NK细胞活性的测定
通过乳酸脱氢酶LDH测定法测定,计算NK细胞活性:实验前3天将靶细胞YAC-1进行传代培养,应用前以Hank’s液洗3次,用含10%小牛血清的RPMII640完全培养液调整细胞浓度为4×105个/mL,受试小鼠颈椎脱臼处死,无菌取脾,制成脾细胞悬液,清洗2次后,离心,弃上清液将细胞浆弹起,加入0.5mL灭菌20秒,裂解红细胞后再加入0.5mL双倍Hank’s液及8.0mLHank’s液,离心10min,用1mL含含10%小牛血清的RPMII640完全培养液重悬,镜检计数,用RPMII640完全培养液调整细胞浓度为2×107个/mL,使效应细胞与靶细胞比为50:1。取靶细胞和效应细胞各100μL,加入U形96孔培养吧中,靶细胞自然四方孔加靶细胞和培养液各100μL,靶细胞最大稀释孔加靶细胞和1%NP40各100μL,上述各项均设三个平行孔,置二氧化碳培养箱中5%二氧化碳,37℃培养4h,将96孔板离心,吸取每孔上清100μL,置平底96孔培养板中,加入LDH基质液100μL,反应3~10min,然后每孔加入1mol/L HCl溶液30μL,终止反应,在酶标仪490nm处测光密度值,计算NK细胞活性:
NK细胞活性(%)=(反应孔OD-自然释放孔OD)/(最大四释放孔OD-自然释放孔OD)×100%
得出的NK细胞活性按下式剂型数据转换,式中P为NK细胞活性,用小数表示,所得数据为计量资料,受试样品组的NK细胞活性显著高于对照组的NK细胞活性,可判定该项实验结果阳性。
2、实验结果:
2.1本申请原料制得的片剂对小鼠体重的影响
表1各组小鼠的初始体重
由表1可见,小鼠的初始体重在四批实验动物各剂量组与0g/kgBW组间比较,差异均无显著性(P>0.05)。即小鼠的初始体重在各组间较为均衡。
表2对小鼠体重的影响
由表2可见,经口给予小鼠不同剂量的本申请片剂去包衣颗粒31天后后,小鼠的体重在四批各剂量组与0g/kgBW组间比较,差异均无显著性(P>0.05)。即本申请原料制成的片剂对小鼠体重无不良影响。
2.2本申请原料制得的片剂对小鼠脏器/体重比值的影响
表3对小鼠脾脏/体重比值的影响
由表3可见,经口给予小鼠不同剂量的本申请片剂去包衣颗粒31天后,各剂量组小鼠脾脏/体重比值与0g/kgBW组比较,差异均无显著性(P>0.05),即本申请片剂对小鼠的脾脏/体重比值无影响。
表4对小鼠胸腺/体重比值的影响
由表3可见,经口给予小鼠不同剂量的本申请片剂去包衣颗粒31天后,各剂量组小鼠胸腺/体重比值与0g/kgBW组比较,差异均无显著性(P>0.05),即本申请片剂对小鼠的胸腺/体重比值无影响。
2.3本申请原料制得的片剂对小鼠细胞免疫功能的影响
表5对小鼠迟发型变态反应的影响
由表5可见,经口给予小鼠不同剂量的本申请片剂去包衣颗粒31天后,各剂量组小鼠足跖肿胀度与0g/kgBW组比较,差异均无显著性(P>0.05),即本申请片剂对小鼠迟发型变态反应程度无影响。
表6对小鼠淋巴细胞转化实验的影响
由表6可见,经口给予小鼠不同剂量的本申请片剂去包衣颗粒31天后,各剂量组小鼠淋巴细胞增殖能力与0g/kgBW组比较,差异均无显著性(P>0.05),即本申请片剂对小鼠淋巴细胞增殖能力无影响。
2.4本申请原料制得的片剂对小鼠体液免疫的影响
表7对小鼠抗体生成细胞数的影响
由表7可见,经口给予小鼠不同剂量的本申请片剂去包衣颗粒31天后,与0g/kgBW组比较,0.97g/kgBW小鼠溶血空斑数提高,有显著性差异(P<0.05),即本申请片剂在高剂量组能提高小鼠抗体生产细胞数。
表8对小鼠半数溶血值的影响
由表7可见,经口给予小鼠不同剂量的本申请片剂去包衣颗粒31天后,与0g/kgBW组比较,0.97g/kgBW小鼠溶血值提高,有显著性差异(P<0.05),即本申请片剂在高剂量组能提高小鼠半数溶血值。
2.5本申请原料制得的片剂对小鼠单核-巨噬细胞吞噬功能的影响
表9对小鼠碳廊清能的影响
由表9可见,经口给予小鼠不同剂量的本申请片剂去包衣颗粒31天后,与0g/kgBW组比较,差异均无显著性(P>0.05),即本申请片剂对小鼠的碳廊清能力无影响。
表10对小鼠巨噬细胞吞噬鸡红细胞吞噬率的影响
由表10可见,经口给予小鼠不同剂量的本申请片剂去包衣颗粒31天后,与0g/kgBW组比较,0.32g/kgBW组小鼠巨噬细胞吞噬鸡红细胞吞噬率提高,有显著性差异(P<0.05),0.97g/kgBW小鼠巨噬细胞吞噬鸡红细胞吞噬率提高,有显著性差异(P<0.01),即本申请片剂在高剂量组能提高小鼠巨噬细胞吞噬鸡红细胞吞噬率。
表11对小鼠巨噬细胞吞噬鸡红细胞吞噬指数的影响
由表11可见,经口给予小鼠不同剂量的本申请片剂去包衣颗粒31天后,与0g/kgBW组比较,0.32g/kgBW组小鼠巨噬细胞吞噬鸡红细胞吞噬指数提高,有显著性差异(P<0.01),0.97g/kgBW小鼠巨噬细胞吞噬鸡红细胞吞噬指数提高,有显著性差异(P<0.01),即本申请片剂在高剂量组能提高小鼠巨噬细胞吞噬鸡红细胞吞噬指数。
2.6本申请原料制得的片剂对小鼠NK细胞活性的影响
表12对小鼠NK细胞活性的影响
由表12可见,经口给予小鼠不同剂量的本申请片剂去包衣颗粒31天后,与0g/kgBW组比较,差异均无显著性(P>0.05),即本申请片剂对小鼠NK细胞活性无影响。
综上所述,经口给予小鼠不同剂量的本申请片剂去包衣颗粒31天后,与0g/kgBW组比较,该受试物在0.32g/kgBW组能提高小鼠巨噬细胞吞噬鸡红细胞吞噬率和吞噬指数;在0.97g/kgBW组能提高小鼠抗体生成细胞数、提高小鼠半数溶血值、提高小鼠巨噬细胞吞噬鸡红细胞吞噬率和吞噬指数。受试物对小鼠体重增长无不良影响。根据《保健食品检验与评价技术规范》对增强免疫力保健食品的判定标准可知,本申请原料制得的片剂具有增强免疫力的功能。
有益效果:
本发明一种增强免疫力的药物组合物及其应用,产品具有增强人体免疫力的功效。
附图说明
图1为放置0天的检测结果;
图2为放置1个月的检测结果;
图3为放置2个月的检测结果;
图4为放置3个月的检测结果。
具体实施方式
下面结合实施例对本发明作进一步说明。
实施例1:
一种增强免疫力的药物组合物,称取原料:350g天麻、350g灵芝、625g酸枣仁、275g柏子仁。称取辅料:152.5g乳糖、60g甘露醇、60g微晶纤维素、25g羧甲基淀粉钠、2.5g硬脂酸镁。
将天麻切片,并将酸枣仁炒制,然后将天麻、灵芝、酸枣仁和柏子仁按重量份数混合,并加入10倍原料总重量的水,并熬煮提取两次,两次的滤液浓缩至相对密度为1.2~1.3后,于65~75℃下真空干燥成干浸膏,粉碎成浸膏粉,按重量份数将辅料与浸膏粉混合均匀后,制粒干燥,最后压片得到片剂。
上述药物组合得到的产品具有增强人体免疫力的功效。
实施例2:
一种增强免疫力的药物组合物,称取原料:340g天麻、340g灵芝、600~650g酸枣仁、250g柏子仁。称取辅料:150g乳糖、58g甘露醇、58g微晶纤维素、22g羧甲基淀粉钠、2g硬脂酸镁。
将天麻切片,并将酸枣仁炒制,然后将天麻、灵芝、酸枣仁和柏子仁按重量份数混合,并加入10倍原料总重量的水,并熬煮提取两次,两次的滤液浓缩至相对密度为1.2~1.3后,于65~75℃下真空干燥成干浸膏,粉碎成浸膏粉,按重量份数将辅料与浸膏粉混合均匀后,制粒干燥,最后压片得到片剂。
上述药物组合得到的产品具有增强人体免疫力的功效。
实施例3:
一种增强免疫力的药物组合物,称取原料:360g天麻、360g灵芝、650g酸枣仁、300g柏子仁。称取辅料:155g乳糖、62g甘露醇、62g微晶纤维素、27g羧甲基淀粉钠、3g硬脂酸镁。
将天麻切片,并将酸枣仁炒制,然后将天麻、灵芝、酸枣仁和柏子仁按重量份数混合,并加入10倍原料总重量的水,并熬煮提取两次,两次的滤液浓缩至相对密度为1.2~1.3后,于65~75℃下真空干燥成干浸膏,粉碎成浸膏粉,按重量份数将辅料与浸膏粉混合均匀后,制粒干燥,最后压片得到片剂。
上述药物组合得到的产品具有增强人体免疫力的功效。
最后需要说明的是,上述描述仅仅为本发明的优选实施例,本领域的普通技术人员在本发明的启示下,在不违背本发明宗旨及权利要求的前提下,可以做出多种类似的表示,这样的变换均落入本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!