甲状腺激素及其药学上可接受的盐或前药在制备治疗和/或预防皮肤疾病的药物中的应用的制作方法
本发明涉及甲状腺激素及其药学上可接受的盐或前药的一种新用途,具体涉及一种甲状腺激素及其药学上可接受的盐或前药在制备治疗和/或预防皮肤疾病的药物中的应用。
背景技术:
硬皮病(scleroderma)是一种以局限性或弥漫性皮肤增厚和纤维化为特征,可累及心、肺、肾、消化道等多个系统的全身性自身免疫病,依据其皮肤病变的程度及病变累及的部位,可分为局限性和系统性两型。局限性硬皮病主要表现为皮肤硬化;系统性硬皮病,又称为系统性硬化症。病变特点为皮肤纤维增生及血管洋葱皮样改变,最终导致皮肤硬化、血管缺血,除皮肤受累外,它也可影响内脏(心、肺和消化道等器官)。基本的病理变化是结缔组织的纤维化、萎缩及血管闭塞性血管炎等。
硬皮病的病因不明,可能与遗传、免疫、环境、血管病变及胶原代谢改变等综合因素相关。尽管部分硬皮病病例通过治疗可停止发展或缓解,但目前没有特效治疗方法。因此,亟待研发硬皮病防治新方法。
激素衍生物是在多种基本代谢转化中扮演重要生物角色的一类化合物。在所述化合物中,甲状腺激素例如甲状腺素((s)-2-氨基-3-[4-(4-羟基-3,5-二碘苯氧基)-3,5-二碘苯基]丙酸,经常简写为t4),和三碘甲状腺原氨酸(简写为t3),代表重要的关键分子,涉及在体内控制多种代谢过程的速率。甲状腺激素被广泛用于涉及甲状腺障碍的数种病变的治疗。然而,迄今为止尚未见有关甲状腺激素及其药学上可接受的盐或前药用于治疗和/或预防皮肤疾病的报道。
技术实现要素:
为解决上述问题,本发明提供了一种甲状腺激素及其药学上可接受的盐或前药的新用途,即在制备治疗和/或预防皮肤疾病的药物中的应用。
本发明第一方面提供了甲状腺激素及其药学上可接受的盐或前药在制备治疗和/或预防皮肤疾病的药物中的应用。
其中,所述皮肤疾病包括硬皮病。
其中,所述皮肤疾病包括硬斑病、线状硬皮病伴颜面偏侧萎缩、cres综合征、肢端硬皮病、嗜酸性筋膜炎、慢性放射性皮炎、淋巴水肿性硬化、新生儿硬化症、静脉曲张综合征、硬化性粘液水肿、硬化性萎缩苔藓、硬化萎缩综合征和纤维化型基底细胞癌中的至少一种。
其中,所述甲状腺激素及其药学上可接受的盐或前药包括甲状腺激素t3和/或t4及其药学上可接受的盐或前药。
其中,所述甲状腺激素及其药学上可接受的盐或前药作为单一活性成分或与其他药学上可接受的活性成分构成组合物以制备所述药物。
其中,所述药物与其他活性药剂联合使用,所述其他活性药剂包括尼达尼布。
其中,所述药物的给药方式包括局部给药、消化道给药或非消化道给药。
其中,所述药物的给药方式包括表皮给药。
其中,所述甲状腺激素及其药学上可接受的盐或前药的用量为每天0.1-5000微克/公斤体重。
本发明实施例提供了甲状腺激素及其药学上可接受的盐或前药的一种新用途,甲状腺激素及其药学上可接受的盐或前药可以有效地保护上皮细胞,调节上皮细胞表面蛋白合成、储存和分布,促进上皮细胞成熟、分化和细胞完整性,促进上皮细胞内受损线粒体恢复,增强线粒体生物合成,从而有利于受损皮肤组织修复,阻止和逆转皮肤纤维化,调节免疫反应,达到治疗硬皮病的效果。
本发明第二方面提供了一种试剂盒,包括说明书和如上述第一方面所述的药物。
附图说明
图1为本发明试验设计流程图;
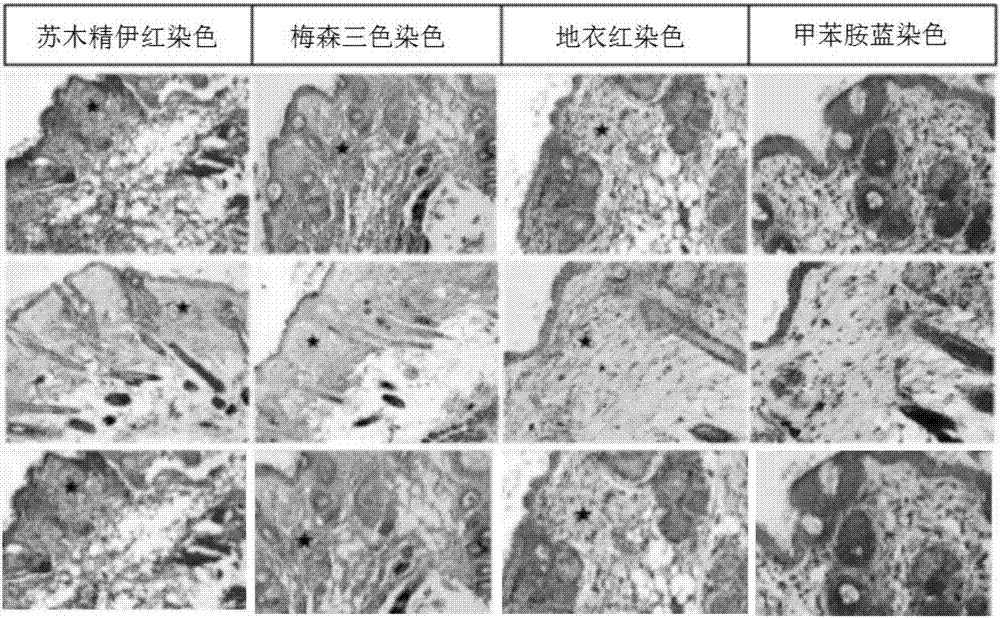
图2为不同处理条件下小鼠的组织切片图;
图3为甲状腺素对博来霉素诱导的皮肤纤维化的治疗后col1a1相对表达强度对比图;
图4为甲状腺素对博来霉素诱导的皮肤纤维化的治疗后的表皮厚度、真皮厚度和血管数量直方图;
图5为不同处理条件下的(a)梅森三色(masson)染色皮肤组织代表图;(b)皮肤羟脯氨酸相对含量直方图;(c)皮肤厚度相对变化直方图;(d)胶原蛋白i基因表达水平相对变化直方图。(n=16,***p<0.0001)。
具体实施方式
以下所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也视为本发明的保护范围。
除非特殊声明,所有本文中的技术性和科学名词在该发明中和普遍使用的含义相同。尽管有些方法和材料的叙述可以用于本发明的描述。
本文中,“一”用于指一个或多于一个(比如至少一个)。举例说明,“一种成分”的含义是一种成分或多于一种成分。
本文中,测量值表达方法,比如数量,持续时间,而类似是指包括±20%或±10%的变量,或者更为精确的±5%或者±1%,更精确能在某些特定数值达到±0.1%,这些变量更适合文章所描述的方法。
疾病或者紊乱“减轻”指的是患者该问题症状的严重程度,发病频率有所下降,或两者都有。
“共同给与”一方面的含义是同时给与实验者试验药物或者盐水对照(参照组)跟另外一种药物一起治疗,本文中,共同给与实际操作时候是分开给药的,只是在该治疗中药物为联合使用。共同给与的药物可以是各种形态或混合物,比如固体、液体、凝胶或者溶液。
本文中,“组合”或者“药物组合”指的是本发明中所使用的一种以上药物的混合,使用药物学上可接受的载体。药物组合帮助药物更容易到达病人或实验动物病灶。条款中描述多种技术包括,并不局限于,静脉给药、口服、气雾吸入、肠胃外、眼部、鼻腔、肺部和局部给药。
本文中“疾病”指的是实验动物的健康状态不能维持稳态,所以在本文中疾病不改善,动物的健康状态持续恶化。
本文中“紊乱”指的是实验动物的健康状态能够维持稳态,但是如果实验动物的健康状态比没有“紊乱”的动物要差。如果不予以治疗,“紊乱”并不一定会导致实验动物发展成疾病状态。
本文中“有效剂量”,“药物学有效剂量”和“治疗有效剂量”指非毒理性但足够剂量能够引起所需的生物学结果。这些结果包括减少或减轻疾病的特征,症状,疾病的原因,或者其它生物学系统的良好方向发展。针对个体合适的治疗剂量可根据常规实验数据正常范围得出。
本文中,“硬皮病”或者“皮肤纤维化”指的是特征为在皮肤形成或逐渐发展成过多纤维结缔组织(纤维化)的一组疾病。硬皮病患者的皮肤出现变硬、变厚和萎缩的改变,依据其皮肤病变的程度及病变累及的部位,可分为局限性和系统性两型。局限性硬皮病按皮损形态及分布又可分为:滴状硬皮病、片状硬皮病、带状硬皮病以及泛发性硬皮病。系统性硬皮病按受累范围、程度、进展速度及预后等,又可分为:肢端型硬皮病及弥漫性硬皮病。
本文中“病人”,“实验对象”,“个体”可以相互转化使用,对于实验动物和实验细胞而言也是如此,体内和体外都一样。在没有限制的实施例中,病人,实验对象和个体指的是人。
本文中,“药物学可接受的”指的是一种材料,比如载体或者稀释剂,他们本身不影响药物的生物学活性,而且相对是无毒的,比如该材料可以注入个体体内而不会引起不好的生物学反应或和其携带的药物发生严重的反应。
本文中,“药物学可接受的载体”指的是药学上可接受的材料,组织和或者载体,比如液体,固体填料,稳定剂,分散剂,悬浮剂,稀释剂,赋形剂,增稠剂,溶剂或包封材料,他们的作用是运输本发明中的有效成分,使其在患者体能发挥应有的作用。一般而言,运输是从一个器官,或者身体的某一部分到达另外一个器官或者身体的另外一个部分。每一个载体必须和各个配方成分相兼容,包括发明中的有效成分,使其对患者不产生负面影响。这些材料在药物学上可接受的载体包括:糖类,比如乳糖,葡萄糖和蔗糖;淀粉,例如玉米淀粉和马铃薯淀粉;纤维素,以及其药学上可接受的盐或前药,比如羧甲基纤维素钠,乙基纤维素和乙酸纤维素;粉末黄蓍胶;麦芽;明胶;滑石;赋形剂,例如可可脂和栓剂蜡;油,例如花生油,棉籽油,红花油,芝麻油,橄榄油,玉米油和大豆油;二醇,例如丙二醇;多元醇,例如甘油,山梨醇,甘露醇和聚乙二醇;酯,例如油酸乙酯和月桂酸乙酯;琼脂;缓冲剂,例如氢氧化镁和氢氧化铝;表面活性剂;藻酸;无热原水;等渗盐水;林格氏溶液;乙醇;磷酸盐缓冲溶液;以及其它无毒在药物学上配方相容物质。
本文中,“药物学上可接受的载体”也包括所有的表面涂料,抗菌和抗真菌制剂,吸收延迟剂,和与本发明中有用的化合物的活性相容的类似物,这些在生理学上能被病人所接受。
补充的活性化合物也可以掺入有效成分组合中。
“药物学上可接受的载体”也可以进一步包括发明中在药物学上可接受的有效盐成分。其它成分也包括制药学上的成分组成,在条例中描述和使用的该项发明,比如在remington制药学科学((genaro,ed.,mackpublishingco.,1985,easton,pa),在此引用作为参考。
本文中,词语“药物学上可接受的盐”指的是由药物学上可接受的无毒酸制备的化合物的盐,可给与病人,包括无机酸,有机酸,溶剂化物,水合物或笼形物。
本文中,“预防”含义为在给与了药物后未发病的实验者能避免或者延迟和疾病或状况相关的症状发生。
本文中,“t3”指的是(s)-三碘甲状腺原氨酸,碘甲腺氨酸,(s)-2-氨基-3-[4-(4-羟基-3-碘苯氧基)-3,5-二碘苯基]丙酸或其盐或溶剂合物。具体地,t3的化学式如下式(ⅰ)所示。
本文中,“t4”(s)-甲状腺素,(s)-2-氨基-3-[4-(4-羟基-3,5-二碘苯氧基)-3,5-二碘苯基]丙酸或其盐或溶剂合物。具体地,t4的化学式如下式(ⅱ)所示。
“治疗上的”指的是对于已经显现出了病变特征的实验个体进行的治疗,为了达到减轻或者消除症状的目的。
本文中“治疗”或者“治疗过程”定义为使用治疗上的药物,比如本发明中的化合物(单独使用或者跟其它药物联合使用),用在病人,或者用在病人身体提取分离的组织或者细胞系(比如为了诊断和体外培养)。该病人其具有本文考虑的病症,病症的症状或能发展成本文考虑的病症的可能性,为了治愈,治疗,减轻,改变,减弱,提高或者影响本文考虑的病症和或者发展出该病症状的可能性。这些治疗可以根据不同药物基因组学的最新知识在适当情况下量体裁衣。
贯穿于本发明文件,本发明的各个方面可以以一定范围的格式呈现。值得注意的是,范围格式中的描述仅为了方便和简洁,并不是本发明应用范围不灵活的限制。相应的,范围描述应被认为已经详细公开了全部可能的子范围和范围内的单个数值。例如,诸如1至6的范围的描述应当被认为已经具体公开了子范围,例如1至3,1至4,1至5,2至4,2至6,从3到6等,以及在该范围内的单个数字,例如1,2,2.7,3,4,5,5.1,5.3,5.5和6。这适用于该范围的宽度。
本发明实施方式第一方面提供了一种甲状腺激素及其药学上可接受的盐或前药在制备治疗和/或预防皮肤疾病的药物中的应用。
本发明实施方式中,所述皮肤疾病包括硬皮病。具体地,所述皮肤疾病包括硬斑病、线状硬皮病伴颜面偏侧萎缩、cres综合征、肢端硬皮病、嗜酸性筋膜炎、慢性放射性皮炎、淋巴水肿性硬化、新生儿硬化症、静脉曲张综合征、硬化性粘液水肿、硬化性萎缩苔藓、硬化萎缩综合征和纤维化型基底细胞癌中的至少一种。
本发明实施方式中,所述甲状腺激素及其药学上可接受的盐或前药包括甲状腺激素t3和/或t4及其药学上可接受的盐或前药。可选地,所述甲状腺激素及其药学上可接受的盐或前药包括甲状腺激素t3和/或t4的钠盐。具体地,所述甲状腺激素及其药学上可接受的盐或前药包括甲状腺素钠。
本发明实施方式中,所述甲状腺激素及其药学上可接受的盐或前药作为单一活性成分或与其他药学上可接受的活性成分构成组合物以制备所述药物。
本发明实施方式中,所述甲状腺激素及其药学上可接受的盐或前药可与药物学上可接受的载体构成组合物以制备所述药物。在一个实施例中,本发明的药物组成使用包括本发明中药物的有效治疗剂量和一个药学上的合理载体。载体可以是含有例如水,乙醇,多元醇(例如甘油,丙二醇和液体聚乙二醇等),其合适的混合物和植物油的溶剂或分散介质。可通过使用如卵磷脂包裹,通过在分散体的情况下维持所需的粒度和通过使用表面活性剂来保持适当的流动性。防止微生物的作用可以通过各种抗菌剂和抗真菌剂,例如对羟基苯甲酸酯,氯丁醇,苯酚,抗坏血酸,硫柳汞等实现。在许多情况下,优选在组合物中包含等渗物质,例如糖,氯化钠或多元醇如甘露醇和山梨醇。
本发明实施方式中,所述甲状腺激素及其药学上可接受的盐或前药与油脂性基质构成组合物以制备所述软膏状药物,所述甲状腺激素及其药学上可接受的盐或前药以固体状态或油状分散在所述油脂性基质中。可选地,所述油脂性基质选自烃类、脂肪酸酯类和动植物油中的至少一种。进一步可选地,烃类例如可以举出凝胶化烃(含有分子量3500以上的聚乙烯的液体石蜡,优选含有分子量3500-35000的聚乙烯2-8%的液体石蜡)、重质液体石蜡、轻质液体石蜡、白凡士林、黄凡士林、角鲨烯等,脂肪酸酯类例如可以举出中链脂肪酸甘油三酸酯、硬化脂等的合成油、橄榄油、大豆油、花生油、红花油、米糠油、芝麻油、山茶油、玉米油、棉籽油、椰子油等植物油、猪油、牛脂等动物油及这些的硬化油等,蜡类例如可以举出蜂蜡、巴西棕榈蜡等天然蜡、石蜡、微晶蜡等石油蜡、褐煤蜡等矿物蜡、合成蜡等。另外还可以将这些物质中的几种混合使用。具体地,所述油脂性基质选自白色凡士林、白色凡士林与轻质液体石蜡的组合、白色凡士林和液体石蜡的组合、白色凡士林和石蜡的组合、白色凡士林和角鲨烷组合、白色凡士林和甲基聚硅氧烷的组合中的至少一种。可选地,所述软膏状药物中甲状腺激素及其药学上可接受的盐或前药的含量为20μg/ml-60μg/ml,可选地为40μg/ml。
另外,为了提高软膏与皮肤的亲和性,本发明的软膏剂中也可以含有表面活性剂。表面活性剂例如可以举出非离子型表面活性剂及/或阴离子型表面活性剂。非离子型表面活性剂例如可以举出聚氧乙烯聚氧丙烯二醇类、脂肪醇类、甘油脂肪酸酯类、聚氧乙烯山梨糖醇酐脂肪酸酯类等,阴离子型表面活性剂例如可以举出脂肪酸类、硫酸酯类、聚丙烯酸酯类、羧乙烯聚合物类、纤维素衍生物类及其碱盐等,优选非离子型表面活性剂,使用表面活性剂的情况下,其含量通常为软膏剂中的50%以下,优选30%以下,通常例如为2-50%,优选5-30%。
除含有表面活性剂之外还可以进一步含有水形成乳液。乳液的形态既可以是w/o型,也可以是o/w型,但油脂性基剂优选容易与皮肤接触的w/o型。在使用水的情况下,水的含量通常为软膏剂中的50%以下,优选30%以下,通常例如为5-50%,优选10-30%。
本发明的软膏剂中也可以加入其他的添加剂如苯酚类等抗氧化剂,苯甲酸类等防腐剂。在加入这些添加剂的情况下,添加剂的含量通常为软膏剂中的0.01-1%。
本发明的软膏剂可以直接涂于患部,也可以制成涂布有软膏剂的泥敷剂、膏药剂等贴剂。
本发明的油脂性软膏剂可以利用常法调制。即,将甲状腺激素及其药学上可接受的盐或前药混和到上述油脂性基剂以及根据需要加入的表面活性剂、水以及其他的添加剂中,使之均匀分散,在粘度很高的情况下加热。在使用水的情况下最后加入水混合。甲状腺激素及其药学上可接受的盐或前药可以在混合之前粉碎,也可以在混合分散工序中粉碎。当甲状腺激素及其药学上可接受的盐或前药的粒度较大时,也可以与液态烃类一起粉碎后混合。利用显微镜对软膏剂中的甲状腺激素及其药学上可接受的盐或前药的粒度进行粒径测定,平均粒径为60μm以下,优选30μm以下,优选其粒子数的至少80%在1-100μm的范围内,特别优选在2-50μm的范围内。
在一个实施例中,本发明的药物直接和药物学组成包装在了一起,包括一个含有治疗有效剂量药物的容器,单独使用或者和另外一个药物学物质共同使用;本发明在的说明描述了用药物治疗,预防或者减轻疾病或紊乱的症状的使用方法。
制剂可以与常规赋形剂,即适合于本领域已知的任何合适的给药方式的药物学上合适的有机或无机载体物质的混合物使用。药物学准备工作可无菌处理,如果需要可与辅助剂混合,例如润滑剂,防腐剂,稳定剂,润湿剂,乳化剂,影响渗透压缓冲剂的盐,着色剂,调味剂和/或芳香物质等。也可以根据需要与其它活性成分组合使用,例如止痛剂。
本发明实施方式中,本发明中的药物联合至少一种其它药物对于治疗和预防硬皮病效果更好。其它药物可能是发明中所包含的,或者比如可以买到的,已知的可以预防或减轻纤维性皮肤病症状的药物。可选地,所述药物与其他活性药剂联合使用,所述其他活性药剂包括尼达尼布。
本发明实施方式中,所述药物的给药方式包括局部给药、消化道给药或非消化道给药。局部给药是指直接用药于要影响的身体部位,如表皮给药(即为患处涂抹)。消化道给药,包括口服。非消化道给药包括经动脉注射、静脉注射、肌肉注射、心内注射、皮下注射、或透皮给药。可选地,所述药物的给药方式包括患处涂抹、口服或注射。
本发明的药物制剂可以使用已知的方法准备。这样的制剂可以直接给与于实验对象,用于例如该材料适合某一实验对象。每一种制剂中还可以包含一种或多种分散剂或润湿剂,悬浮剂和防腐剂。制剂成分还可以包括另外的赋形剂,例如填充剂和甜味剂,调味剂或着色剂。
给药方案可以影响有效量的组成成分。本发明治疗制剂可以在发病前或者发病后给与实验对象。此外,几次分开的剂量以及交错剂量可以每日或顺序给药,或者剂量可以连续输注,或者可以是推注。还有,治疗制剂的剂量可根据治疗或预防情况的紧急情况按比例地增加或减少。可以通过调整剂量方案以提供最佳治疗效果。
向患者,优选哺乳动物,更优选人施用本发明中的药物可以使用已知的给药程序,用本发明中陈述的疾病或紊乱的剂量和治疗时间给与执行。本研究中有效治疗剂量需要根据不同因素来调整,包括病人疾病和紊乱的发展阶段,年龄,性别,体重;还有治疗药物的活性。比如,可以每天施用几个分开的剂量,或者可以按照治疗情况的紧急情况按比例减少剂量。其中一个非限制性示例为本发明的治疗药物有效剂量范围约为每天0.1-5000微克/公斤体重。
研究人员将能够研究相关因素并且在不进行过度实验的情况下确定治疗药物的有效剂量。实际应用中本发明的有效成分的含量,给与方法可能根据每一个患者而不同,因为每个患者对药物的反映,对药物毒性的阈值各不相同。
本发明中治疗的有效剂量和给与病人的剂量要根据病人的年龄,性别和体重,已经目前用药情况以及疾病的发展情况进行调整。医生,比如内科医生或者兽医,有能力做出病人所需有效成分的处方决定权。比如内科医生或者兽医可使用比推荐剂量较低的剂量开始治疗,然后逐渐增加已达到所期待的治疗效果。
本发明中合适的剂量范围可以是每天0.1μg到5000μg,或者1μg到500μg,或者5μg到250μg。这个剂量可以一次给与,或者分多次给与,可以一天给与1到4次。当多次给药时,每次的剂量可以相同也可以不同。比如,每天1μg的剂量可以分两次0.5μg间隔12小时给与。
某些实施例中,本发明的用药量为1μg到5000μg。某些实施例中,本发明的用药含量少于1000μg,或少于500μg,或少于200μg,或少于50μg。同样的,在某些实施例中,本发明中额外药物的剂量少于1000μg,或少于800μg,或少于600μg,或少于500μg,或少于400μg或少于300μg,或少于200μg,或少于100μg,或少于50μg,或少于40μg,或少于30μg,或少于25μg,或少于20μg,或少于15μg,或少于10μg,或少于5μg,或少于2μg,或少于1μg,或少于0.5μg,或者是其中任何一个中间值。
在其中一个实施例中,本研究的药物给与病人的频率为一天一次到五次以上。在另一实施例中,本研究药物给药频率可以是但并不局限于每天一次,每两天一次,每三天一次,直到每周一次,每两周一次。很明显的是,目前给药多种组合的频率不尽相同,取决于但不局限于年龄,疾病和紊乱是否进行过治疗,性别,健康状况以及其它因素。因此,本发明不应被理解为限于任何特定的剂量方案,并且给与任何患者的精确剂量和组合物,要通过考虑到患者的所有其他因素而进行物理确定后来决定。
可以理解的是每天给与的药物可以但并不局限于每天一次,每两天一次,每三天一次,每四天一次,每五天一次。比如说,针对每两天给与的频率,一天给与5μg,可以由周一开始给与第一个5μg,然后周三5μg,周五5μg,依次进行下去。
在患者状态改善的情况下,根据医生的判断,可以连续给与本发明的药物;或者,所施用的药物的剂量暂时减少或暂时中止一段时间(比如“药物假期”)。药物假期的长短可以从2天到1年,包括2天,3天,4天,5天,6天,7天,10天,12天,15天,20天,28天,35天,50天,70天,100天,120天,150天,180天,200天,250天,280天,300天,320天,350天或者365天。药物假期中剂量减少范围是10%-100%,可包括10%,15%,20%,25%,30%,35%,40%,45%,50%,55%,60%,65%,70%,75%,80%,85%,90%,95%,或者100%。
一旦病人出现症状改善,维持治疗的剂量可以给与。另外,也可以将剂量或频率,或者两者都降低,如果患者的身体功能在疾病和紊乱情况下都有所改善。在其中一个实施例中,病人需要长期间断性的智力,因为症状的反复出现和/或感染。
本发明中药物使用方法可制成每单位剂量的方式。术语“单位剂量方式”指的是适于作为接受治疗的患者的单位剂量的物理上不连续单位,其中每个单位含有提前计算好的活性物质,经计算产生所需的治疗效果的剂量,也可以联合适宜的制药载体使用。单位剂量方式可以一天一次,也可以一天多次(比如1天一次到四次)。当每天给与多次剂量时,单位剂量可以每次相同或不同。
毒性和治疗效果的测定是可选择进行的,结果来自细胞学实验和动物实验,包括但不并局限于,ld50(让实验群体50%的致死剂量)和ed50(让实验群体50%的有效剂量)。毒性和有效性的比值为治疗指数,为ld50和ed50的比值。可根据细胞学和动物学获得的数据来推断出用于人体的剂量范围。每个药物的剂量最好是体循环中接近ed50并且毒性最小。剂量根据这个范围可根据给与方式和使用途径改变。
本发明实施例提供了甲状腺激素及其药学上可接受的盐或前药的一种新用途,甲状腺激素及其药学上可接受的盐或前药可以有效地保护上皮细胞,调节上皮细胞表面蛋白合成、储存和分布,促进上皮细胞成熟、分化和细胞完整性,促进上皮细胞内受损线粒体恢复,增强线粒体生物合成,从而有利于受损皮肤组织修复,阻止和逆转皮肤纤维化,调节免疫反应,达到治疗硬皮病的效果。
本发明实施方式第二方面提供了一种试剂盒,包括说明书和如上述第一方面所述的药物。
本发明实施方式中,所述说明书描述了治疗和/或预防皮肤疾病的说明,给药途径,频率等。
实施例1:
甲状腺素软膏的制备:
取甲状腺激素或其钠盐与凡士林混合均匀,形成甲状腺激素或其钠盐浓度为40μg/ml的甲状腺激素软膏。
下面结合附图来说明本发明具体实施情况。
图1为试验设计流程图,c57bl小鼠经2.5u/kg博来霉素皮下注射诱导皮肤纤维化,四周后分组分别用甲状腺激素(30ng/kg)和凡士林(对照)涂抹患处,每天三次。在四周后,采集皮肤样品,进行硬皮病指标检测。其中每个星期收获一组进行胶原蛋白表达测试。其中,图中的数字“48”和“510”代表样品数量。
图2为组织切片的纤维观察。分别显示皮肤纤维化(hes),胶原蛋白积聚,弹性纤维和核酸分布状况。第一行,博来霉素处理前,第二行,博来霉素处理后,第三行,博来霉素诱导纤维化后,用甲状腺激素t3处理4个星期后的结果。从图中可以看出与正常对照相比,博来霉素处理可诱导皮肤纤维化,表现为皮肤变薄,正常乳头状浸润程度下降,出现纤维化病灶,胶原积累增加。
图3表明甲状腺素对博来霉素诱导的皮肤纤维化的治疗作用。c57bl小鼠经2.5u/kg博来霉素皮下注射,诱导产生皮肤纤维化四周后,涂搽甲状腺激素软膏(40μg/ml),每天三次,每周采集皮肤样品,进行纤维化分析。从图中可以看出博来霉素处理可诱导i型胶原基因表达,mrna水平显著增加,而甲状腺素t3处理则可抑制该基因的表达,减缓和逆转皮肤纤维化进程,从而起到治疗作用。
图4表明甲状腺素对博来霉素诱导的皮肤纤维化的治疗作用。c57bl小鼠经2.5u/kg博来霉素皮下注射,诱导产生皮肤纤维化四周后,涂搽甲状腺激素软膏(40μg/ml),每天三次,四周后采集皮肤样品,进行纤维化分析。从图中可以看出博来霉素可诱导表皮变薄,真皮层加厚,血管数减少,而甲状腺素t3处理则可增加皮下血管数量,有利于损伤修复。
图5表明甲状腺素可防止和治疗博来霉素诱导的硬皮症。a代表梅森三色染色皮肤组织代表图;b代表皮肤羟脯氨酸相对含量直方图;c代表皮肤厚度相对变化直方图;d代表胶原蛋白i基因表达水平相对变化直方图。(n=16,***p<0.0001),a组为盐水对照组,b组为给与博来霉素(2.5u/kg)组,c组为给与博来霉素(2.5u/kg)和尼达尼布(给与量为50mg/kg)组,d组为给与博来霉素(2.5u/kg)和t4(给与量为40mg/kg)组,e组为给与博来霉素(2.5u/kg)和t3(给与量为40μg/kg)组。从图中可以看出甲状腺素处理可抑制博来霉素诱导的胶原蛋白积累,减少羟脯氨酸的积累,抑制胶原蛋白基因表达,促进皮肤损伤修复,恢复原生结构。
研究显示缺少甲状腺激素会加剧皮肤纤维化,局部涂抹甲状腺激素软膏可减轻皮肤损伤和纤维化动物模型中的疾病进程。这些结果给与甲状腺激素有可能有效治疗皮肤损伤和硬皮病的病人。结果显示,靶向在受损皮肤中给与甲状腺激素及其药学上可接受的盐或前药可以有效减轻或完全阻止纤维化过程。
如本文所报道的,动物学研究包括在博来霉素引起的小鼠皮肤损伤模型中,在疾病发展的不同时间点多次给予t4或t3至受损皮肤组织有利于疾病治愈。在预防实验中,t4在博来霉素诱导后第3天到第7天后给药可有效抑制皮肤纤维化,促进伤口愈合。在治疗实验中,t4和t3在博来霉素诱导硬皮病后(28天开始给药),每天给药,在两个星期后取样检测,发现对硬皮病有显著疗效。跟fda批准药尼达尼布相比,甲状腺激素具有更好的疗效,尤其是t3。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!