一种循环肿瘤细胞的体内富集装置的制作方法
本发明涉及医疗器械领域,更具体地涉及一种循环肿瘤细胞的体内富集装置。
背景技术:
随着对恶性肿瘤精确诊治要求的不断提高,以循环肿瘤细胞(circulatingtumorcells,ctc)和循环肿瘤dna(ctdna)为代表的液态活检(liquidbiopsy)技术近年来成为国内外研究热点。ctc指来源于原发肿瘤或转移瘤,脱离基底膜后的并进入血管的肿瘤细胞。ctc在血液循环中可单个存在,也可堆积成团,黏附其他血细胞簇,形成循环肿瘤微栓子(circulatingtumormicroembli,ctm),其增殖与转移潜能更强,是恶性肿瘤患者出现术后复发和远处转移的重要原因。国内外多项研究证实ctc在肺癌的诊断、危险分级、早期转移预测、疗效评价及治疗方面发挥了积极作用。由于其具有获取简便、微创、易于连续监测的特点,有望成为精准医疗时代极具发展潜力的早期肺癌无创诊断和实时疗效监测的新型肿瘤标志物,具有很广阔的应用前景。
ctc作为完整的肿瘤细胞或细胞团,不但携带更完整的基因信息,同时也携带完整的肿瘤蛋白表达信息,因此ctc相关的研究仍然是国内外研究者关注的焦点。然而,体内ctc的数量很少,在进展期肿瘤患者中,大概每100万血细胞(1ml血液)中混杂1个肿瘤细胞,而在早期患者中,该数目更低。因此,进行ctc研究的首要步骤必须先进行富集以获取足够多的ctc,该步骤也是现阶段限制ctcs领域发展的重要瓶颈。
分离和富集方法通常基于ctcs物理性质(密度和大小)或生物免疫学特征(分子特征),前者主要包括密度梯度离心技术和膜过滤技术,后者主要包括免疫磁珠分选技术以及微流体芯片技术。但是,目前ctc富集检测主要在体外进行,抽取7-30ml不等的血液样本,采用特定的技术将ctc与血细胞分离,浓集后再进行后续分析。这种方法在一次检测中采血量有限(通常在30ml以内,占全血容量的比例不足1%),而且后续的处理操作过程还会造成循环肿瘤细胞的进一步丢失,造成有效循环肿瘤细胞数量的减少,甚至造成分析鉴定无法进行的致命缺陷。
技术实现要素:
本发明的目的是提供一种循环肿瘤细胞的体内富集装置,从而解决现有技术中对循环肿瘤细胞的体外捕获低效低质的问题。
为了解决上述技术问题,本发明采用以下技术方案:
提供一种循环肿瘤细胞的体内富集装置,所述体内富集装置包括:一可经外周静脉穿刺到达中心静脉的导管本体,所述导管本体的管壁上分布有若干筛孔,所述导管本体内填充有靶向循环肿瘤细胞的捕获粒子,所述导管本体的前端为盲端。
所述捕获粒子的表面预先组装有对所述循环肿瘤细胞特异性靶向结合的亲水性药物或特异性抗体。
所述特异性抗体包括:epcam抗体、hea抗体、esa抗体、或者ck7抗体等等。应当理解,此处并未穷举所有的特异性抗体,针对各种不同的恶性肿瘤患者,其循环肿瘤细胞上的抗原也各不相同或者各有差异,只要捕获粒子上预先组装针对该循环肿瘤细胞的亲水性药物或特异性抗体,即可实现该特异性靶向,对ctc进行高效高质地捕获。有关该不同肿瘤表面的抗原以及相应的特异性抗体的选择具体可参考文献“卵巢癌外周血循环肿瘤细胞检测及分子表型分析”(陆松梅,重庆医科大学,2015)。
所述捕获粒子是一种介孔粒子,包括无机介孔粒子和有机介孔粒子。
根据本发明的一个优选实施例,所述介孔粒子可由氧化硅材料制成,但是应当理解的是,该材料不局限于氧化硅,可应用其他具有生物相容性的无机或有机材料来合成捕获粒子,比如聚酰胺等。例如,文献(nanobiotechnology,2015;13:9,1-13)就公开了一种采用聚酰胺(pamam)大分子完全羧化后偶联抗epcam抗体,捕获ctc。
所述筛孔的孔径小于所述捕获粒子的孔径,以保证捕获粒子持续保持在导管本体内部,不会进入血液,导致潜在毒性。
ctc的直径一般为10~30μm,大多数为10~20μm,因此,为了使较多的ctc进入导管本体内,导管本体1管壁上的筛孔2的直径优选设计为20~25μm,捕获粒子的直径优选设计为30~35μm。
根据静脉的平均管径尺寸,头静脉大约为6mm,贵要静脉大约为8mm,导管本体的外径优选为4.5~5.0mm。
所述导管本体沿其长度方向具有均匀的管径,也称“均匀构型”。
所述导管本体沿其长度方向具有不均匀的管径。
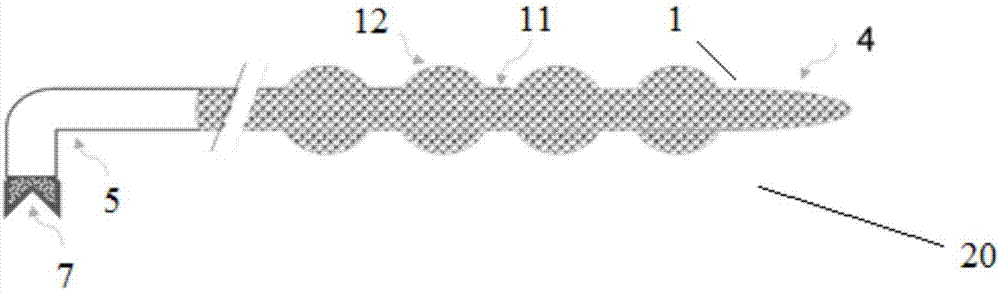
优选地,所述导管本体沿其长度方向具有多个通过圆柱状部分彼此间隔开的球状突起部分,所述球状突起部分的管径始终大于所述圆柱状部分的管径。该结构也称“球样扩张型”。
相比“均匀构型”,“球样扩张型”的优点即在于可以增加与粒子接触的血液体积,由于循环肿瘤细胞与肿瘤分期密切相关,因此若临床分期较早,血管管径合适,则理论上优先选用“球样扩张型”。但是,其存在的缺点则是“球样扩张型”的导管结构明显比“均匀构型”复杂,工艺设计也相应比“均匀构型”复杂。
所述导管本体的前端为盲端,防止捕获粒子漏出。
所述导管本体的前端采用钝化处理,减小导管本体的前端对血管及组织的损伤。
首先,根据本发明提供的循环肿瘤细胞的体内富集装置,采用了类似picc导管的设计,但是又与picc导管的结构有所不同。
所谓“picc导管”,即经外周静脉穿刺中心静脉置管,是利用导管从外周手臂的静脉进行穿刺,导管直达靠近心脏的大静脉,避免化疗药物与手臂静脉的直接接触,加上大静脉的血流速度很快,可以迅速冲稀化疗药物,防止药物对血管的刺激,因此能够有效保护上肢静脉,减少静脉炎的发生,减轻患者的疼痛,提高患者的生命质量。
根据本发明提供的循环肿瘤细胞的体内富集装置,与picc导管的结构相比主要具有以下几个不同点:1)体内富集装置的导管本体的管壁上分布有若干筛孔,导管本体内还填充有靶向ctc的捕获粒子,而picc导管的管壁既没有筛孔,管内也不填充粒子;2)体内富集装置的导管本体除了具有均匀管径的结构之外,还可以具有不均匀管径的结构,而picc导管仅具有均匀的管径;3)体内富集装置的导管本体的前端为盲端,防止捕获粒子漏出,而picc导管前端为敞开端,便于药物的输送;4)导管盲端采用圆钝化处理,减小对血管及组织的损伤。
本发明的发明人通过对制作导管的材质进行反复测试,为了使导管的稳定性达到最优,包括:导管的韧性,导管壁内筛孔孔径制作的均匀性以及在血流内长期留置后的筛孔完整性,使筛孔不被血液内组分填塞封闭,优选的导管材质为硅胶和医用聚氨酯,最优选的导管材质为医用聚氨酯。
医用聚氨酯的优点即在于其具有优良的生物相容性、可黏合性和抗血栓性,同时还具有优良的力学性能,在医用生物材料中扮演了十分重要的角色。
其次,根据本发明提供的循环肿瘤细胞的体内富集装置,其工作原理如下:捕获粒子采用介孔材料制成,粒子内核部分的介孔孔道具有一定疏水性而外层介孔孔道具有亲水性,此种结构的空腔或内核部分呈现和有机乳液的相似性,即相当于有机乳液中的疏水部分,介孔壳层相当于有机乳液中的亲水端,可以组装亲水性药物或特异性抗体,从而实现特异性靶向结合,受结合的循环肿瘤细胞被滞留在导管内,形成富集。
介孔粒子的稳定性包括:1)粒子本身的稳定性以保持粒子大小在体内始终大于导管孔径,故而不致漏出导管;2)粒子表面修饰的抗体的稳定性以保证有足够的靶点与ctc结合;3)粒子-ctc结合产物的稳定性能够满足带至体外进行ctc收集分析。
根据本发明提供的循环肿瘤细胞的体内富集装置,其体内捕获实施方式类似于经外周中心静脉穿刺操作,具体为:在无菌条件下,按照标准操作规程将该装置经贵要静脉、头静脉或肘正中静脉(首选贵要静脉)穿刺置入并固定,置入48-96小时后,将导管取出并进行下一步ctc分析鉴定工作。
根据本发明提供的一种循环肿瘤细胞的体内富集装置,相对现有技术具有以下优点:
1)在体捕获:无需抽取血样,而是将所设计的导管本体经贵要静脉、头静脉或者肘正中静脉置入血管内约20cm。导管本体漂浮于血流内,实时捕捉血流内的ctc目标,这样可以彻底克服现有技术受采血量所限获得ctc过少难于分析的弊端。
2)长时捕捉:根据本发明提供的装置可以长时留置于体内(维持48~96小时),以保证血液内的ctc与导管内靶向ctc的捕获粒子的充分接触、暴露和结合。这对于血内ctc丰度较低的早期肿瘤尤其重要,鉴于此,本装置较既往系统更适于开展对早期肺癌,包括同时性多原发性肺癌的检测和分析。
3)结合滞留:根据本发明提供的装置的导管壁上密布若干筛孔,以保证血液(包括血细胞和ctc)进入导管内;导管内注入含有靶向ctc的捕获粒子,捕获粒子直径大于筛孔的孔径,以保证捕获粒子始终停留在导管内,不会进入血液,导致潜在毒性。粒子表面通过抗体修饰靶向结合ctc,受结合的ctc被滞留于导管内,形成富集。
4)诊断与治疗同步进行:根据本发明提供的装置的导管可以作为picc使用,对于正在接受治疗的患者尤为方便。在进行静脉化疗前或后,可导入ctc捕获液(含有可针对ctc特异性靶向结合的亲水性药物或特异性抗体,比如epcam抗体的靶向粒子)实时评估血内的ctc数量,及时了解体内肿瘤的负荷和对治疗的反映。
根据本发明提供的体内富集装置,该装置具有体内使用、高效捕捉和临床便捷应用的特点,为各种肿瘤(肺癌、乳腺癌等)的早期诊断、靶向治疗、复发转移检测、疗效评估等提供基于循环肿瘤细胞的分子基因诊断信息,利用有效的ctc检测技术,优化肿瘤治疗流程,因此具有十分广阔的应用前景。总之,本发明提供了一种能够在体捕获、长时捕捉、结合滞留、诊断与治疗同步进行的循环肿瘤细胞的体内富集装置。
附图说明
图1是根据本发明的一个优选实施例的体内富集装置的结构示意图;
图2是根据本发明的另一优选实施例的体内富集装置的结构示意图;
图3是填充在体内富集装置中的捕获粒子对ctc的特异性靶向结合的示意图。
具体实施方式
以下结合具体实施例,对本发明做进一步说明。应理解,以下实施例仅用于说明本发明而非用于限制本发明的范围。
实施例1
如图1所示,是根据本发明的一个优选实施例的体内富集装置10。该装置包括:一可经外周静脉穿刺到达中心静脉的导管本体1,导管本体1的管壁上分布有若干筛孔2,导管本体1内填充有靶向ctc的捕获粒子3。捕获粒子3的表面预先组装有对ctc6特异性靶向结合的亲水性药物或特异性抗体31。筛孔2的孔径小于捕获粒子3的孔径,防止捕获粒子3从导管本体1中漏出。从图1中可见,该导管本体1沿其长度方向具有均匀的管径。
导管本体1的前端4为盲端,防止捕获粒子漏出。
导管本体1的前端大约10mm的长度部分采用钝化处理,减小导管本体1的前端对血管及组织的损伤。
根据该优选实施例,导管本体1的末端5不设置筛孔2。由于导管本体1的末端为体外部分,为了安全考虑,防止发生气体栓塞或者感染,该部分必须为无孔。
根据该优选实施例,导管本体1的末端5还连接有一导管接口7,通过该导管接口7实现与减压套筒的连接,进而通过减压套筒对导管本体1起到保护作用。
ctc的直径一般为10~20μm,当ctc经筛孔2进入导管本体1内,即被捕获粒子3捕获。
根据该优选实施例,为了使较多的ctc进入导管本体1内,该导管本体1管壁上的筛孔2的直径为20μm,捕获粒子3的直径为30μm,导管本体1的外径大约为4.5mm。
实施例2
如图2所示,是根据本发明的另一优选实施例的体内富集装置20。该装置20与前一实施例的装置10的结构大致相似,唯一区别仅在于导管本体1沿其长度方向具有不均匀的管径。根据该特别优选的实施例,导管本体1沿其长度方向具有多个通过圆柱状部分11彼此间隔开的球状突起部分12,所述球状突起部分12的管径始终大于所述圆柱状部分11的管径。该结构也称“球样扩张型”。该“球样扩张型”的优点在于可以增加与捕获粒子3接触的血液体积,若临床分期较早,血管管径合适,则理论上优先选用这种“球样扩张型”,以便于高效高质地收集ctc。
根据上述实施例1提供的体内富集装置10,其工作原理如图3所示,其中,针对肺癌患者,ctc6表面具有特异性的epcam抗原61以及其他抗原62,捕获粒子3的表面预先组装有epcam抗体31。因此,当该体内富集装置10穿刺进入体内并固定好之后,血液(包括血细胞和ctc)经过筛孔2进入导管本体1内时,捕获粒子3的表面以epcam抗体31修饰靶向结合ctc6,受结合的ctc6则被滞留于导管本体1内,从而形成富集,实现对体内ctc的高效高质收集。
实施例3
根据该实施例,本发明还提供了上述体内富集装置10的一种可选的操作规程,具体如下:
1)该装置应由受过医学专业培训的人员使用,始终遵守常规卫生要求。
2)摆体位,使患者术肢与躯体呈90度。
3)在穿刺肢体下方垫防水垫巾、一次性垫巾,放置止血带。
4)选择穿刺部位,静脉选择原则为:首选贵要静脉,依次是正中静脉,再次是头静脉。
5)从预穿刺点沿静脉走向至右胸锁关节,将实测数值减去2-5cm即为导管置入长度。
6)穿无菌隔离衣(助手协助),戴无菌手套。
7)铺无菌台:①助手取肝素盐水250ml,2/3倒于治疗碗内,1/3给术者冲洗无菌手套并擦干;②将10ml注射器、输液贴、输液接头打开放入无菌区,将无纺布纱球放入弯盘内备用;③打开该体内富集装置的外包装,将其放入无菌区内。
8)预冲,检查导管、连接器、输液接头并用肝素盐水浸泡导管,用10ml注射器抽取肝素盐水备用。
9)注入ctc捕获液:用20ml注射器将ctc捕获液体(含epcam抗体修饰的捕获粒子的生理盐水)缓慢注入导管内,备用。
10)穿刺点消毒:以穿刺点为中心,用2%碘酒消毒一遍,75%酒精脱碘两遍,消毒范围上下直径为20cm,两侧至臂缘。
11)铺孔巾及治疗巾,覆盖术肢,暴露穿刺点。
12)助手位于对侧,在预穿刺部位上方扎止血带,嘱病人握拳。
13)将导管、穿刺针置于术者右侧无菌区内,注射器、无菌剪刀、输液贴、无菌纱球、无菌方纱(1块)置于术者左侧无菌区内。穿刺:①以15~30度角进行静脉穿刺;②见回血后,放平穿刺针继续推进1~2mm,送插管鞘,鞘内可见回血;③左手食指按压插管鞘前端止血,拇指固定穿刺鞘,嘱病人松拳,助手协助松止血带,右手撤出穿刺针。
14)送管:固定好插管鞘,将导管自插管鞘内缓慢、匀速送入,同时嘱病人向穿刺侧转头并将下颌贴肩以防止导管误入颈静脉。
15)拔出插管鞘:送管至预定长度后,在鞘的末端处压迫止血并固定导管,然后拔出插管鞘。
16)修剪导管长度:体外保留导管5~7cm,用无菌剪刀垂直剪断导管(注意不要剪出斜面或毛碴)。
17)安装减压套筒及连接器并贴膜固定。
18)拔管:导管置入48~96小时后,揭去固定敷料,穿刺点消毒,铺无菌巾,操作者戴无菌手套,距穿刺点2厘米处捏住导管,平行静脉走行方向直线缓慢拉出导管,穿刺伤口处可根据常规静脉抽血处理方法进行处理。导管取出后,应立即用肝素钠盐水浸泡冲洗导管,完毕剪开导管盲端,用注射器抽取生理盐水缓慢注入导管内,将导管内粒子冲出并进行下一步分离鉴定工作。使用完毕的导管按照规定进行医疗废弃物处理。
19)在整个置管过程中,患者有任何不适均应停止操作并进行相应处理。
以上所述的,仅为本发明的较佳实施例,并非用以限定本发明的范围,本发明的上述实施例还可以做出各种变化。即凡是依据本发明申请的权利要求书及说明书内容所作的简单、等效变化与修饰,皆落入本发明专利的权利要求保护范围。本发明未详尽描述的均为常规技术内容。
- 还没有人留言评论。精彩留言会获得点赞!