增强骨诱导的植入物表面的制作方法
本申请要求2016年8月3日提交的美国临时专利申请号62/370,459的优先权,其内容通过引用结合在本文中。本发明总体涉及骨科植入物领域。特别地,本发明涉及用于骨科植入物的金属表面,其在植入体内时刺激间充质干细胞分化成前成骨细胞,并刺激前成骨细胞成熟为成骨细胞,从而促进新骨生长。通过添加制造工艺和二次加工的组合制备表面。
背景技术:
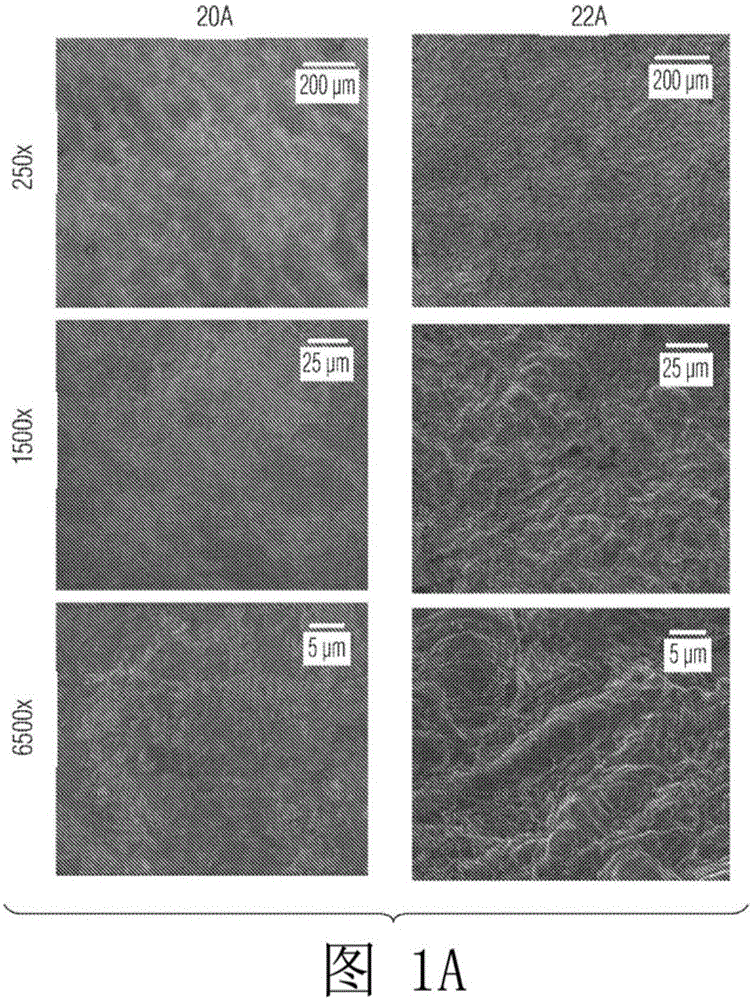
:在整个说明书中引用了各种出版物,包括专利、公开的申请、科技文章和学术文章。这些引用的出版物中的每一个都通过引用整体并且出于所有目的并入本文。各种骨科植入物用于矫正骨骼缺陷。在许多情况下,需要将植入物与相邻骨骼整合,但不容易实现。例如,已知通常用于骨科植入物的某些聚合物材料如聚醚醚酮(peek)不能与骨结合。即使对于能够与骨结合的钛合金等金属,光滑的表面也能提供缓慢和差的集成。此外,骨科植入物上的整合表面装饰有牙齿、尖刺、凹槽和其他突出表面实际上可以阻止或避免骨整合。在需要整合的地方,整合率直接关系到患者的整体健康状况。整合越快,手术修复区愈合的速度越快,患者恢复生活方式的速度越快,以前受到需要骨科干预的条件的阻碍。因此,非常希望在骨科植入物和相邻骨之间发生整合。因此,本领域仍然需要能够实现快速和高质量骨整合的整合表面。技术实现要素:为了满足这个和其他需要,并且鉴于其目的,本发明的特征在于骨科植入物的骨诱导表面,包括骨接触和自由表面。这些骨诱导表面根据包括添加制造具有一个或多个自由表面并且具有一个或多个适于与骨接触的骨接触表面的骨科植入物的方法生产,然后机械地,化学地,或者机械地和化学地侵蚀一个或多个骨接触表面并且任选地,机械地,化学地,或机械地和化学地侵蚀一个或多个自由表面中的一个或多个,以将包括微尺度结构和纳米级结构的骨诱导粗糙度赋予机械、化学或机械和化学侵蚀的表面。一个或多个骨接触和自由表面中的一个或多个可包括宏观粗糙度。在优选方面,在添加制造之后,该方法包括机械侵蚀然后化学侵蚀一个或多个骨接触表面,并且任选地,机械地,化学地,或机械地和化学地侵蚀一个或多个自由表面中的一个或多个以赋予骨诱导粗糙度。因此,在一个或多个自由表面中的一个或多个被侵蚀的一些优选方面中,一些自由表面被侵蚀并且一些自由表面不被侵蚀。根据该方法产生的骨接触表面和自由表面显著增强、促进和/或上调,包括其速率和程度,骨诱导、成骨、碱性磷酸酶的间充质干细胞表达、osterix的前成骨细胞表达和骨钙素的成骨细胞表达中的一种或多种。当这些表面与骨接触或与间充质干细胞接触时,会发生这种增强、促进和/或上调。这种接触可以是体外、体内或原位接触。当这些其他类型的表面与骨接触或与间充质干细胞接触(这种接触可以是体外、体内或原位接触)时,由根据该方法产生的表面获得的骨诱导、成骨、碱性磷酸酶的间充质干细胞表达、osterix的前成骨细胞表达和骨钙素的成骨细胞表达中的一种或多种的增强显著大于骨科植入物的骨诱导、成骨、间充质干细胞碱性磷酸酶表达、成骨细胞前成骨细胞表达和/或骨钙素成骨细胞表达。在一些方面,这样的其他类型的表面没有包括微尺度结构和纳米级结构的骨诱导粗糙度,例如,未经机械和/或化学侵蚀处理的表面,以赋予包括微尺度结构和纳米级结构的骨诱导粗糙度。在一些方面,根据该方法产生的一个或多个骨接触表面,当与骨接触时,相对于来自比较骨接触表面的骨诱导显著增强骨诱导,所述比较骨接触表面包括宏观粗糙度并且包括骨诱导粗糙度,所述骨诱导粗糙度包括通过机械和化学侵蚀体基底产生的微尺度结构和纳米级结构,当比较表面与骨接触时。在一些方面,根据该方法产生的一个或多个骨接触表面,当与骨接触时,相对于来自比较骨接触表面的成骨显著增强成骨,所述比较骨接触表面包括宏观粗糙度并且包括骨诱导粗糙度,所述骨诱导粗糙度包括通过机械和化学侵蚀体基底产生的微尺度结构和纳米级结构,当比较表面与骨接触时。在一些方面,根据该方法产生的一个或多个骨接触表面,当与骨接触时,相对于来自比较骨接触表面的间充质干细胞的碱性磷酸酶的表达水平显著增强间充质干细胞的碱性磷酸酶的表达水平,所述比较骨接触表面包括宏观粗糙度并且包括骨诱导粗糙度,所述骨诱导粗糙度包括通过机械和化学侵蚀体基底而产生的微尺度结构和纳米级结构,当比较表面与骨接触时。在一些方面,根据该方法产生的一个或多个骨接触表面,当与骨接触时,相对于来自比较骨接触表面的前成骨细胞的osterix表达水平显著增强前成骨细胞的osterix表达水平,所述比较骨接触表面包括宏观粗糙度并且包括骨诱导粗糙度,所述骨诱导粗糙度包括通过机械和化学侵蚀体基底而产生的微尺度结构和纳米级结构,当比较表面与骨接触时。在一些方面,根据该方法产生的一个或多个骨接触表面,当与骨接触时,相对于来自比较骨接触表面的成骨细胞的骨钙素表达水平显著增强成骨细胞的骨钙素表达水平,所述比较骨接触表面包括宏观粗糙度并且包括骨诱导粗糙度,所述骨诱导粗糙度包括通过机械和化学侵蚀体基底而产生的微尺度结构和纳米级结构,当比较表面与骨接触时。添加制造骨科植入物的步骤可包括用电子束熔化(ebm)附加地制造骨科植入物。添加制造骨科植入物的步骤可包括通过选择性激光烧结附加地制造骨科植入物,包括例如直接金属激光烧结(dmls)。添加制造骨科植入物的步骤可包括用选择性激光熔化附加地制造骨科植入物,包括例如lasercusingtm。添加制造骨科植入物的步骤可包括使用熔融沉积成型(fdm)、直接金属沉积、激光工程网成型(lens)、基于线的定向能量沉积,或使用能源进行熔化的任何其他方法附加地制造骨科植入物。在添加制造骨科植入物的步骤之后,添加制造方法可以进一步包括热等静压(hip)或对骨科植入物进行应力消除。骨科植入物优选包括金属或陶瓷。金属可包括钴铬合金、钛合金,钛、铝和钒的合金,钛和镍的合金、镍钛合金或不锈钢。本发明的特征还在于骨科植入物,该植入物包括一个或多个骨接触表面和一个或多个自由表面,所述自由表面根据本文件中描述或举例说明的任何方法制备。由机械侵蚀、化学侵蚀或机械和化学侵蚀加工而成的这些植入物上的表面包括骨诱导粗糙度,其包括微尺度结构和纳米级结构,其显着增强、促进和/或上调骨诱导,包括其速率和程度,当这些表面与骨接触或与间充质干细胞接触时,例如,在将植入物植入体内之后。应理解,前面的一般性描述和以下的详细描述都是本发明的示例性而非限制性的。附图说明当结合附图阅读时,从以下详细描述中可以最好地理解本发明。附图中包括几个数字,如下所述。图1a显示了添加制造的表面的扫描电子显微镜(sem)图像,包括表面20a和表面22a,表面20a是一种直接金属激光烧结(dmls)产生的表面,其经受应力消除但没有侵蚀,表面22a是dmls产生的表面,其经受应力消除和机械和化学侵蚀;图1b显示了添加制造表面的sem图像,包括表面20b和表面22b,表面20b是ebm生产的表面,其经受热等静压(hip)但没有侵蚀,表面22b是ebm生产的表面,受到hip和机械和化学侵蚀;图1c显示了添加制造的表面的sem图像,包括表面20c和表面22c,表面20c是dmls产生的表面,其经受hip但没有侵蚀,表面22c是dmls产生的表面,受到hip和机械和化学侵蚀;图1d显示了添加制造的表面的sem图像,包括表面16e和表面16f,表面16e是激光产生的表面,其经受热等静压和使用碳酸氢钠鼓风的机械侵蚀,表面16f是激光产生的表面,使用钛爆炸经受热等静压和机械侵蚀;图1e显示了添加制造的表面29d的sem图像,该表面是激光产生的表面,具有内部宏观纹理,经受热等静压和机械和化学侵蚀;图2a显示了在添加制造的表面20a-20c和22a-22c上培养的mg63细胞表达的碱性磷酸酶(alp)水平(表面20a-20c和22a-22c是与图1a至1c中所述相同的表面);图2b显示了在添加制造的表面20a-20c和22a-22c上培养的mg63细胞表达的骨桥蛋白水平(表面20a-20c和22a-22c是与图1a至1c中所述相同的表面);图2c显示了在添加制造的表面20a-20c和22a-22c上培养的mg63细胞表达的runx2的水平(表面20a-20c和22a-22c是与图1a至1c中所述相同的表面);图3a显示在添加制造的表面20a-20c和22a-22c上培养的saos-2细胞表达的碱性磷酸酶水平(表面20a-20c和22a-22c是与图1a至1c中所述相同的表面);图3b显示在添加制造的表面20a-20c和22a-22c上培养的saos-2细胞表达的osterix水平(表面20a-20c和22a-22c是与图1a至1c中所述相同的表面);图3c显示在添加制造的表面20a-20c和22a-22c上培养的saos-2细胞表达的骨钙素水平(表面20a-20c和22a-22c是与图1a至1c中所述相同的表面);图3d显示分别在添加制造的表面16e、16f和29d上培养的saos-2细胞表达的碱性磷酸酶(最左边的条)、osterix(中心条)和骨钙素(最右边的条)的水平(表面16e、16f和29d是与图1d和1e中所述相同的表面);以及图4显示了机械侵蚀以及机械和化学侵蚀的组合如何从添加剂构造中去除未烧结或部分烧结的粉末。具体实施方式在整个说明书和权利要求中使用与本发明的方面有关的各种术语。除非另有说明,否则这些术语将在本领域中给出它们的普通含义。其他具体定义的术语应以与本文件中提供的定义一致的方式解释。如在本文件中所使用的,单数形式“一”、“一个”和“该”包括复数指示物,除非另有明确说明。术语“受试者”或“患者”可互换使用。受试者可以是任何动物,包括哺乳动物,例如伴侣动物、实验动物和非人灵长类动物。人类是首选。“垂直地”添加制造骨科植入物意味着在添加制造过程中,构建开始于植入物的不接触骨的表面(例如,自由表面),这样,骨接触表面由叠加层的一个或多个边缘产生。作为示例,但不限于此,如果骨科植入物的顶部或底部表面旨在接触骨骼但是植入物的侧面不打算接触骨骼,那么构建从植入物的一侧开始,并且随着层的沉积,产生与骨接触的顶部和底部表面。垂直添加制造与更传统的水平添加制造工艺形成对比,其中构造始于骨接触表面。作为示例,但不限于此,如果骨科植入物的顶部或底部表面旨在接触骨骼但是植入物的侧面不打算接触骨骼,则通过水平添加制造,构建开始于接触骨骼的顶层或底层中的任一个。如本文件中所使用的,“大块基底”是指骨科植入物,或骨科植入物的前体,范例或原型,例如预成型坯、坯料、实心、金属铸件、锻造金属、金属块、金属锭或大量金属,其制造时不需要任何添加制造。如本文件中所使用的,“骨诱导”和“骨诱导”是指诱导或引发成骨,并且包括将未成熟的间充质干细胞募集到加工的(例如,机械和/或化学侵蚀)骨接触表面和/或骨科植入物的加工的(例如,机械和/或化学侵蚀)自由表面,随后是这些干细胞向前成骨细胞的表型进展和分化以及前成骨细胞向成骨细胞的进一步表型进展和分化。这种表型进展和分化的特征在于通过间充质干细胞上调碱性磷酸酶表达,随后当间充质干细胞分化成前成骨细胞时上调卵巢,随后随着前成骨细胞成熟为成骨细胞而上调骨钙素。“成骨”包括骨基质的形成和发展。如本文件中所使用的,“自由表面”是骨科植入物的表面,其在植入物植入体内时不直接接触骨。然而,经过加工以赋予骨诱导粗糙度的自由表面包括微米级和纳米级结构,该自由表面可以刺激从头骨生长,使得在植入后一段时间和伴随的骨从自由表面生长出来后,自由表面接触骨。在一些方面,例如,当植入物植入体内时,骨科植入物的一个或多个自由表面可接触骨移植成材料(例如,合成、同种异体移植物或自体移植物材料)。从业者可以将骨移植物材料放置成与一个或多个自由表面接触。根据本发明已经观察到,骨科植入物的添加制造随后是添加制造的表面的机械和化学侵蚀的组合导致这样的表面能够刺激前成骨细胞成熟为成骨细胞,并且刺激前成骨细胞和成骨细胞以上调促进和支持成骨的蛋白质的表达。发现这些表面至少显著增强了这些蛋白质的量,并且据信这些蛋白质的表达速率也得到了提高。据信这些表面还能够刺激间充质干细胞分化成前成骨细胞,并上调促进和支持成骨的蛋白质的表达。当骨科植入物与相邻骨的整合(例如,骨整合)是期望的结果时,这种蛋白质的上调意味着体内(例如,在这些表面和相邻骨之间)的整合过程将快速且稳健地进行。因此,本发明的特征在于骨诱导骨接触表面用于骨科植入物,其根据从添加制造骨科植入物开始的方法生产,然后处理添加产生的植入物的表面,该表面旨在利用产生和/或增强表面的骨诱导结构特征的侵蚀技术促进新骨生长。一般来说,用于产生促进骨诱导的骨接触表面的方法包括首先添加制造骨科植入物,例如,植入物本体具有所需的基本形状、构造和结构取向,用于植入植入物的身体内的特定位置,以及用于植入物的特定矫正应用,然后处理植入物的一个或多个表面(例如,骨接触和自由表面中的任一个或两个)以产生增强骨生长的生物活性表面形貌。在一些优选的方面,通过顺序添加制造和减成蚀刻工艺产生的一个或多个骨接触表面包括重叠的宏观尺度粗糙度、微尺度粗糙度和纳米级粗糙度。在一些优选的方面,通过顺序添加制造和减成蚀刻工艺产生的一个或多个自由表面包括重叠的微尺度粗糙度和纳米级粗糙度。每个粗糙度可包括规则的、不规则的或规则和不规则结构特征的组合,例如宏观粗糙度、微观粗糙度,并且就表面的结构布置而言,纳米级粗糙度可以独立地是规则的、不规则的,或者规则的和不规则的。添加制造工艺产生的表面通常在微观上是光滑的。因此,优选用于生产骨科植入物的添加制造技术至少在骨接触表面上赋予宏观粗糙度,尽管通过添加过程产生的自由表面可以是粗糙的或光滑的触摸。宏观尺度粗糙度包括宏观结构特征,其用于抓住骨并且一旦植入体内就抑制植入物的移动。宏观尺度特征的形状、配置、取向、尺寸、设计和布局可以编程到添加制造软件中。因此,在一些方面,骨科植入物的添加制造包括通过添加制造来管理和设计植入物本体的几何形状、尺寸和结构特征。植入物本体可包括任何合适的形状或几何形状,以及任何合适数量的侧面和表面-包括骨接触表面并包括自由表面-这可能取决于例如体内植入部位的特定形状和位置。植入物可包括平坦的、圆形的、规则的和/或不规则的表面。作为示例,但不限于此,骨科植入物可以包括关节置换(例如,臀部、膝盖、肩部、肘部、踝部、腕部、颌部等),长骨或短骨(或其部分)置换,颅骨或颌骨置换,用于诱导单独骨骼融合或物理连接的植入物(例如,手指关节、踝关节、椎骨或脊柱运动节段),用于将另一个植入物固定到骨头上的植入物(例如,骨螺钉、椎弓根螺钉和固定元件),以促进骨折反复的植入物,包括骨螺钉、髓内钉、杆和板等,或任何植入物,以替换、修复、支撑或补充体内的任何骨骼。在一些方面,植入物包括用于替换椎间盘或用于替换脊柱运动节段的植入物。在高度优选的方面,植入物旨在与周围骨骼整合。植入工程和设计可以是计算机辅助的。此外,添加制造还包括工程和设计宏观结构特征的几何形状、尺寸和结构特征或要赋予植入物的骨接触表面的粗糙度。该工程可以源自通过积极酸蚀刻大块衬底产生的表面的宏观粗糙度的成像/光学扫描,其中成像信息输入到添加制造程序模型中。宏观尺度粗糙度的工程可以考虑由国际标准化组织(iso)(例如iso468:1982)建立的一个或多个粗糙度参数的特定值的合理设计。这些参数包括但不限于rp(最大高度轮廓)、rv(最大轮廓谷深度)、rz(轮廓的最大高度)、rc(轮廓的平均高度)、rt(轮廓的总高度)、ra(轮廓的算术平均偏差)、rq(轮廓的均方根偏差)、rsk(轮廓的偏斜度)、rku(轮廓的峰度)、rsm(轮廓的平均宽度)、rδq(轮廓的均方根斜率)、rmr(轮廓的材料比)、rδc(轮廓截面高度差)、lp(采样长度-主要轮廓)、lw(采样长度-波纹轮廓)、lr(采样长度-粗糙度轮廓)、ln(评估长度)、z(x)(纵坐标值)、dz/dx(局部斜率)、zp(轮廓峰值高度)、zv(轮廓谷深度)、zt(轮廓元素高度)、xs(轮廓元素宽度)和mi(轮廓的材料长度)。其他参数可包括rsa(表面积增加)、rpc(峰值计数)、h(swedish高度)、iso平坦度(面积平坦度偏差)、ptiso(峰谷曲率高度)、rtm(平均峰谷粗糙度)、rv(最低值)、rvm(平均谷形深度)、ry(最大峰谷粗糙度)、rpm(平均峰面高度)、s(局部峰值之间的平均间距)、sm(平均线峰值之间的平均间距)、峰数、峰密度、峰间距、谷数、谷密度和谷间距。此外,预期添加制造还可包括微尺度粗糙度的几何形状、尺寸和结构特征的工程和设计,和/或纳米级粗糙度赋予植入物的骨接触或自由表面,特别是随着添加制造设备的能力的发展,允许更加精细和细致入微的细节添加制造。骨科植入物可以由任何合适的材料添加地制造,包括金属、陶瓷、骨或其任何组合或复合物。金属是非常优选的。金属可包括合金。优选的金属包括钛和钛合金,例如镍-钛合金(例如,镍钛合金),以及铝和钒(例如6-4)钛合金、钴铬合金、以及外科级钢(例如不锈钢)。骨科植入物优选地不由诸如聚醚醚酮(peek)的聚合物制成。添加制造可以包括通过将固体材料沉积到基底上,然后将沉积的固体材料烧结或熔化成骨科植入物层,然后将更多的固体材料沉积到前一层上,然后烧结或熔化新沉积的层,使其与前一层熔合并建立下一层来连续分层,并重复这些步骤,直到完成注入。沉积的固体材料可以是线、粉末、颗粒、微粒、碎片或其组合的形式,其通过能量源烧结或熔化。粉末、颗粒、微粒、碎片或其组合优选基本上为球形。优选粉末、颗粒、微粒、碎片或其组合不包括不规则形状或边缘或锯齿状边缘。球体可以包括不同的尺寸,或者可以具有基本相同的尺寸。添加制造可包括粉末、颗粒、微粒、线、碎片或其组合的烧结和/或熔化。烧结和/或熔化优选实现粉末、颗粒、微粒、碎片或其组合的基本上完全熔化,使得沉积的层由基本上完全熔融的材料组成,该材料优选为金属。合适的添加制造技术包括但不限于选择性激光烧结,包括例如直接金属激光烧结(dmls)(是eosgmbh的服务标志)、选择性激光熔化,包括例如lasercusingtm(conceptlaserschutzrechtsverwaltungsgmbh)、电子束熔化(ebm)、熔融沉积建模(fdm)、直接金属沉积、激光工程网成型(lens)和基于线的定向能量沉积。因此,能量源可以包括激光器或电子束,但是可以使用任何合适的熔化材料的技术。沉积和/或烧结或熔化可以在惰性环境中进行,例如,用低氧和/或在氮气和/或氩气存在下进行。在一些方面,在连续层沉积在其上之前,先前层(刚刚形成)基本上没有固化。在一些方面,前一层(刚刚形成)在连续层沉积在其上之前至少部分固化。在一些方面,植入物是垂直添加制造的。垂直添加制造开始于形成一层,该层将构成除正在制造的植入物的骨接触表面之外的表面(例如,自由表面),其中连续的层被沉积和烧结或熔化直到完成相对的面。因此,骨接触表面由以垂直构建方案铺设的层的边缘产生。在通过添加过程完成植入物本体的构建之后,植入物本体可以经受应力消除处理,包括对形成的植入物本体的再加热。应力消除可以在真空和/或惰性气体下进行。加热可以在引起金属内扩散的温度下进行,然后进行冷却步骤。在一些方面,再加热也可伴有压力。压力可以是单轴的(例如,从一个方向施加;热单轴压制或hup)或等静压(例如,从所有方向均匀地施加)。热等静压(hip)是非常优选的。通过将植入物本体置于密封容器中来进行hip,该容器可通过添加和移除气体来加热和压力控制。通常,一旦将植入物本体放置在密封容器中,就将容器抽空以除去任何污染气体。然后加热容器,同时将惰性气体(例如氩气)引入腔室中以增加压力。然后将容器在升高的温度和压力下保持一段时间,之后将容器快速冷却并减压。hip在低于制造植入物本体的材料的熔点的温度下进行,但是在足够高的温度下进行,其中植入体的扩散和塑性变形发生。温度通常低于熔化温度的80%。例如,对于含有6%铝和4%钒的钛合金,根据astm标准规范f3001,可以将植入物本体加热至895℃(1643°f)至955℃(1751°f)±15℃(59°f)的温度,压力至少为100mpa(14,504psi),持续180±60分钟,然后冷却至425℃(797°f)以下。对于其他材料,本领域普通技术人员已知类似的规范,例如来自astm的其他标准。据信hip导致植入物本体的变化。例如,温度和压力的组合导致植入物体内存在的任何内含物的塌陷。在一些方面,植入物本体的密度在hip之后可以基本上接近或等于100%,这意味着植入物可以基本上没有包含体(内部孔)。去除层间边界并去除夹杂物改善了植入物本体的机械强度并降低了植入后失效的可能性。金属扩散还可以减少或消除由上述添加制造工艺产生的金属层之间的边界。此外,来自hip的升高的温度和压力促使金属扩散穿过晶界,导致晶粒结构、晶粒尺寸、晶粒组成、晶粒分布或其任何组合的细化。在一些方面,hip可以至少增加晶粒尺寸,特别是当耦合到电子束熔融添加构造时。hip可以改变植入物表面上的晶粒结构和晶间边界。在添加制造步骤之后,并且进一步进行减压、hup或hip处理,如果在该方法中采用这种处理,该方法还包括侵蚀骨接触表面、自由表面、或者附加地产生的骨接触表面和自由表面,以将骨诱导结构特征赋予这些表面。骨诱导结构特征包括微尺度结构和促进或增强骨诱导的纳米级结构。添加制造的植入物的一个或多个骨接触表面被机械地、化学地或机械地和化学地侵蚀,以将包括微尺度结构和纳米级结构的骨诱导粗糙度赋予骨接触表面。在一些方面,添加制造的植入物的一个或多个自由表面被机械地、化学地或机械地和化学地侵蚀,以将包括微尺度结构和纳米级结构的骨诱导粗糙度赋予自由表面。因此,可以加工添加制造的植入物的骨接触表面和自由表面中的任一个或两者,以包括骨诱导微尺度和纳米级结构。有效地,这种处理可以建立与侵蚀产生的微尺度和纳米级结构相加地制造的宏观尺度结构的重叠。机械和/或化学处理用作减成法,例如侵蚀或蚀刻。机械侵蚀包括但不限于将骨科植入物的骨接触表面暴露于光蚀刻、能量轰击、等离子体蚀刻、激光蚀刻、电化学蚀刻、加工、钻孔、研磨、喷丸、喷砂(例如,砂或喷砂,包括用铝或氧化钛颗粒喷砂),或这些方法的任何组合。化学侵蚀可包括,例如,将选择表面或整个植入物暴露于化学物质如酸或碱,其中酸或碱蚀刻与酸或碱接触的骨接触表面。化学侵蚀可包括但不限于化学、电化学、光化学、光电化学或其他类型的化学研磨,蚀刻或用于去除部分基板的其他处理。蚀刻剂可以是湿的或干的,以及任何状态:液体、气体或固体。在优选的方面,在添加制造之后连续使用机械侵蚀和化学(例如酸)侵蚀。机械侵蚀优选在化学侵蚀之前。优选地,机械侵蚀和化学侵蚀都不会将孔引入骨接触表面。在用于将骨诱导特征赋予这些表面的植入物表面的侵蚀之前,可以通过掩蔽来保护植入物的其他表面,其不是用于骨诱导或以其他方式诱导骨生长,或者已经被添加地制造成光滑的。在一些方面,可以通过掩蔽来保护自由表面。然后可以机械地和化学地侵蚀植入物的暴露的非掩蔽表面。优选通过使用颗粒喷射来实现机械侵蚀。颗粒可包括有机或无机介质。合适的颗粒包括例如氧化铝颗粒和/或氧化钛颗粒和/或玻璃珠颗粒和/或浮石颗粒和/或碳化硅颗粒和/或羟基磷灰石颗粒,或其他合适的金属颗粒,或陶瓷颗粒。有机颗粒如核桃壳或可溶解颗粒如碳酸氢钠也是合适的。优选使用酸实现化学侵蚀,但是可以使用能够侵蚀植入物材料的骨接触表面的任何化学品。优选的酸是强酸,例如hf、hno3、h2so4、hcl、hbr、hi、hclo4、柠檬酸及其任何组合,但所用的特定酸并不重要。据信,酸以增强骨接触或自由表面的骨诱导增强特性的方式蚀刻晶粒结构和晶界。非常优选化学侵蚀在机械侵蚀之后。化学侵蚀可以在单一化学处理中完成,尽管可以采用多种处理以增加或增强骨接触表面上的纳米级结构。控制化学侵蚀的强度、侵蚀发生的温度以及分配给侵蚀过程的时间允许精细控制由侵蚀产生的所得表面。更一般地,机械侵蚀、化学侵蚀以及机械和化学侵蚀的组合可以从植入物表面去除不需要的污染物(或碎片)。图4显示了机械侵蚀以及机械和化学侵蚀的组合如何从添加构造中去除未烧结或部分烧结的粉末。图4显示了放大250倍(顶行)和放大1500倍(底行)的烧结钛合金表面的sem图像。左列图像显示了机器的放大表面(加法构建),没有任何后续侵蚀处理。中心柱图像显示添加构建后机械侵蚀后的放大表面。右列图像显示了添加构建后顺序机械侵蚀和化学侵蚀后的放大表面。除了赋予微尺度结构特征之外,机械侵蚀还可以从植入物表面移除或减少碎屑。除了将纳米级结构特征赋予植入物表面之外,酸侵蚀还可以从植入物表面除去或减少碎屑。碎片可能包括外部碎片,如灰尘或其他处理工件。外部碎片还可以包括来自机械侵蚀/爆破步骤的介质的颗粒或组分,这些颗粒可能已经嵌入植入物表面。碎片还可以包括固有碎片,例如添加构建过程的伪影,例如在添加构建期间未完全熔化或完全烧结的粉末、颗粒、微粒等。例如,图4显示了由添加构建产生的钛表面的sem图像,左列中的图像(在两个不同的放大率下)说明一些颗粒未从添加构建中完全整合。因此,存在植入物上的这种颗粒在植入后可能脱落的风险,并且在局部或全身对患者产生负面影响。因此,侵蚀过程可用于从表面除去未烧结/未熔化或未完全烧结或熔化的颗粒,从而降低颗粒移位的风险。如图4的中心柱所示,机械侵蚀可以显着减少来自附加构建结构表面的未整合或部分整合的颗粒的量。并且如图4的右栏所示,化学侵蚀的添加(在机械侵蚀之后)可以进一步减少来自添加构建结构的表面的未整合或部分整合的颗粒的量。在侵蚀过程步骤之后,可以从植入物移除任何保护性掩蔽,并且可以清洁侵蚀和未侵蚀的表面。表面也可以钝化,例如,使用包含硝酸的水溶液。可以清洁表面并用水冲洗。在优选的方面,没有材料添加、浸渍、嵌入、涂覆、喷涂或以其他方式放置在骨接触表面上。在优选的方面,没有材料添加、浸渍、嵌入、涂覆、喷涂或以其他方式放置在自由表面上。(事实上,侵蚀过程可用于去除不需要的污染物。)通过添加制造,随后机械侵蚀、化学侵蚀或机械和化学侵蚀产生的骨接触表面和自由表面包括骨诱导粗糙度,其包括宏观尺度、微尺度和纳米级结构的组合。添加制造工艺优选主要产生宏观尺度特征,其特别设计到在制造期间产生的骨接触表面中,并且由添加制造工艺产生的自由表面基本上是光滑的并且没有这些宏观尺度结构。然而,在一些方面,一个或多个自由表面可以包括宏观尺度特征,特别是但不是必须的,当这些表面在植入时与骨移植材料接触时。机械和化学侵蚀分别将微尺度和纳米级结构添加到加工的骨接触表面和加工的自由表面。在优选的方面,机械侵蚀主要将微尺度结构赋予加工表面,并且机械侵蚀之后的化学侵蚀主要赋予纳米级结构。因此,由添加制造和机械和/或化学侵蚀产生的骨接触表面和自由表面包括宏观粗糙度、微观粗糙度和纳米级粗糙度,其可以至少部分重叠,或者可以基本上重叠,或者可以完全重叠。总的来说,这三种结构特征尺度显着增强了干细胞分化、成骨细胞成熟、成骨细胞发育、骨诱导和成骨中的一种或多种。宏观尺度的结构特征包括相对大的尺寸,例如,以毫米(mm)为单位测量的尺寸,例如1mm或更大。微尺度结构特征包括以微米(μm)为单位测量的尺寸,例如1微米或更大,但小于1毫米。纳米结构特征包括以纳米(nm)测量的尺寸,例如1纳米或更大,但小于1微米。宏观结构特征、微结构特征和/或纳米结构特征的图案可以以规则和/或重复图案组织,并且可选地可以彼此重叠,或者这些特征可以是不规则或随机的图案,或重复的不规则图案(例如,不规则图案的网格)。可以调整该文件中描述的添加制造和机械和化学侵蚀步骤以产生适合于特定植入物应用的深度、高度、长度、宽度、直径、特征尺寸和其他几何形状的混合。还可以调整特征图案的方向。这种柔韧性是合乎需要的,特别是因为骨诱导增强表面的最终图案可以与植入时可能施加在植入物上的生物力和植入方向相反。宏观结构特征、微尺度结构特征和纳米级结构特征不同于齿、钉、脊和其他抓骨的超宏观尺度结构,这些结构通常存在于骨接触植入物的表面上。这种齿、钉和脊旨在挖掘或耙骨。相反,骨接触表面包括本文件中描述或举例说明的宏观结构,其通过添加制造产生,不像齿、钉、脊和其他抓骨的超宏观结构那样损坏或挖掘骨骼。相反,本发明的骨接触表面支撑骨表面的摩擦型抓握并且一旦植入体内就抑制植入物的移动。在骨接触表面上和在添加制造之后由机械侵蚀和化学侵蚀产生的自由表面上的骨诱导微尺度和纳米级结构增强和/或促进骨诱导。添加制造随后是机械侵蚀、化学侵蚀,或机械和化学侵蚀两者产生或赋予骨接触和自由表面的骨诱导粗糙度,这些表面经过这种侵蚀处理。骨诱导粗糙度包括微尺度结构和纳米级结构,其结合以促进、增强或促进骨诱导的速率和/或量。从这种骨诱导粗糙度,新骨生长起源于骨科植入物的这种加工表面并在其上生长。骨科植入物的骨接触表面上的宏观结构抓住骨骼并抑制植入物在体内的移动,反过来,这进一步促进、增强或加速骨诱导的速率和/或量,因为随着新骨生长的进行,运动抑制限制了初期骨组织的破裂。(例如,非预期的运动可以通过破坏新形成的骨基质和组织来破坏骨生长过程)。来自通过添加制造,然后通过机械侵蚀、化学侵蚀或机械和化学侵蚀两者以赋予骨诱导粗糙度的骨接触表面和自由表面的增强和/或促进显着大于骨诱导或通过表面获得的骨诱导的增强和/或促进水平。没有受到机械和化学侵蚀之一或两者的影响。未经受机械和化学侵蚀之一或两者的骨接触和/或自由表面可以没有包括微尺度结构和纳米级结构的骨诱导粗糙度。在一些方面,根据该方法(添加制造,随后是机械和/或化学侵蚀)生产的一个或多个骨接触表面,当与骨接触时,相对于骨诱导、成骨、间充质干细胞的碱性磷酸酶表达,前成骨细胞的osterix表达和/或来自未处理的骨接触表面(未用机械和/或化学侵蚀处理)的成骨细胞的骨钙素表达,通过间充质干细胞显着增强骨诱导、成骨、碱性磷酸酶表达、成骨细胞表达的osterix和成骨细胞表达骨钙素中的一种或多种,当未处理的表面与骨接触时。来自通过添加制造,然后通过机械侵蚀、化学侵蚀或机械和化学侵蚀两者以赋予骨诱导粗糙度的骨接触表面和自由表面的增强和/或促进显着大于通过包含骨诱导粗糙度的比较表面实现的骨诱导或骨诱导的增强和/或促进水平,所述粗糙度包括微尺度结构和通过机械侵蚀、化学侵蚀或者大块基底(即,不是通过添加制造生产的基底)的机械和化学侵蚀两者产生的纳米级结构。因此,在植入物被添加制造并且其表面被加工/侵蚀并且其中比较植入物由大块基底制造并且其表面被加工/侵蚀的情况下,与加工的大块基底的骨诱导相比,来自加工的附加制造的植入物的骨诱导可以显着增强。据信,表面不会显着增强骨诱导,不是骨诱导的,和/或相对于通过添加制造随后机械侵蚀、化学侵蚀或机械和化学侵蚀产生的骨科植入物表面的骨诱导能力较差,以赋予本发明的骨诱导粗糙度,所述表面是平滑的,或者包括未加工/侵蚀的齿、脊、凹槽和超宏观结构,或包括已经冷喷涂、热喷涂或用粘合剂固定的颗粒、纤维或粉末,或者没有机械侵蚀、化学侵蚀,或机械和化学侵蚀两者,以赋予包括微尺度结构和纳米级结构的骨诱导粗糙度,或者缺少包括微尺度结构和纳米级结构的骨诱导粗糙度。相关地,骨科植入物表面不显着增强骨诱导,不是骨诱导的,和/或相对于通过机械侵蚀、化学侵蚀或者大块基底的机械和化学侵蚀产生的骨科植入物表面其骨诱导能力较差,所述骨科植入物表面是平滑的,或者包括未加工/侵蚀的齿、脊、凹槽和超宏观结构,或包括已经冷喷涂、热喷涂或用粘合剂固定的颗粒、纤维或粉末,或者没有机械侵蚀、化学侵蚀,或机械和化学侵蚀两者,以赋予包括微尺度结构和纳米级结构的骨诱导粗糙度,或者缺少包括微尺度结构和纳米级结构的骨诱导粗糙度。在骨接触表面上和在添加制造之后由机械侵蚀和化学侵蚀产生的自由表面上的骨诱导微尺度和纳米级结构增强和/或促进成骨。添加制造随后是机械侵蚀、化学侵蚀,或机械和化学侵蚀两者产生或赋予骨接触和自由表面的骨诱导粗糙度,这些表面经过这种侵蚀处理。骨诱导粗糙度包括微尺度结构和纳米级结构,其结合以促进、增强或加速成骨的速率和/或量。从这种骨诱导粗糙度,新骨生长起源于骨科植入物的这种加工表面并在其上生长。骨科植入物的骨接触表面上的宏观结构抓住骨骼并抑制植入物在体内的移动,而这反过来又进一步促进、增强或加速成骨的速率和/或量,因为随着新骨生长的进行,运动抑制限制了初期骨组织的破裂(例如,非预期的运动可以通过破坏新形成的骨基质和组织来破坏骨生长过程)。来自通过添加制造,然后通过机械侵蚀、化学侵蚀或机械和化学侵蚀两者以赋予骨诱导粗糙度的骨接触表面和自由表面的增强和/或促进显着大于通过包括骨诱导粗糙度的比较表面获得的成骨或增强和/或促进成骨的水平,所述骨诱导粗糙度包括微尺度结构和通过机械侵蚀、化学侵蚀或者大块基底的机械和化学侵蚀产生的纳米级结构。因此,在植入物被添加制造并且其表面被加工/侵蚀并且其中比较植入物由大块基底制造并且其表面被加工/侵蚀的情况下,来自加工的添加制造的植入物的成骨作用将比加工的大块基底的成骨显着增强。据信,骨科植入物表面不会显着增强成骨,不是成骨的,和/或相对于通过添加制造随后机械侵蚀、化学侵蚀或机械和化学侵蚀产生的骨科植入物表面的成骨能力较差,以赋予本发明的骨诱导粗糙度,所述骨科植入物表面是平滑的,或者包括未加工/侵蚀的齿、脊、凹槽和超宏观结构,或包括已经冷喷涂、热喷涂或用粘合剂固定的颗粒、纤维或粉末,或者没有机械侵蚀、化学侵蚀,或机械和化学侵蚀两者,以赋予包括微尺度结构和纳米级结构的骨诱导粗糙度,或者缺少包括微尺度结构和纳米级结构的骨诱导粗糙度。相关地,骨科植入物表面不会显着增强成骨,不是成骨的,和/或相对于通过机械侵蚀、化学侵蚀或者大块基底的机械和化学侵蚀产生的骨科植入物表面,它们的成骨能力较差,所述骨科植入物表面是平滑的,或者包括未加工/侵蚀的齿、脊、凹槽和超宏观结构,或包括已经冷喷涂、热喷涂或用粘合剂固定的颗粒、纤维或粉末,或者没有机械侵蚀、化学侵蚀,或机械和化学侵蚀两者,以赋予包括微尺度结构和纳米级结构的骨诱导粗糙度,或者缺少包括微尺度结构和纳米级结构的骨诱导粗糙度。可以测量骨诱导作为碱性磷酸酶(alp)表达、osterix(osx)表达和骨钙素(oxn)表达中的一种或多种的水平的函数。这些标志物证实了证实骨诱导正在发生的表型进展。alp代表干细胞分化成前成骨细胞的早期标志物。osterix代表第一个骨特异性转录因子表达(runx2通常认为是表达为成骨细胞分化过程的一部分的第一个转录因子,尽管该转录因子不是骨特异性并影响细胞内的其他生化过程)。骨钙素代表成熟的成骨细胞标记物。在优选方面,由添加制造、机械侵蚀和化学侵蚀引起的骨接触表面和自由表面显着增强和/或促进alp表达,然后是osterix表达,然后是干细胞的骨钙素表达,因为它分化成前成骨细胞并成熟为成骨细胞。因此,在植入物被添加制造并且其表面被加工/侵蚀并且其中比较植入物由大块基底制造并且其表面被加工/侵蚀的情况下,分别来自间充质干细胞、前成骨细胞和成骨细胞的alp、osx和ocn中的一种或多种的表达,它们与经过加工的加工制造的植入物表面接触,与来自已处理的大块基底表面接触的间充质干细胞、前成骨细胞和成骨细胞中的一种或多种alp,osx和ocn的表达相比将显着增强。据信,其表面不具有骨诱导粗糙度的骨科植入物,包括微尺度结构和由机械侵蚀,化学侵蚀或机械和化学侵蚀产生的纳米级结构,分别从间充质干细胞、前成骨细胞和成骨细胞中诱导一种或多种alp、osx和ocn的最小表达,或者不诱导分别从间充质干细胞、前成骨细胞和成骨细胞中一种或多种alp、osx和ocn的表达。因此,骨科植入物表面不能显着增强分别来自间充质干细胞、前成骨细胞和成骨细胞的alp、osx和ocn中的一种或多种的表达,不诱导分别来自间充质干细胞、前成骨细胞和成骨细胞中的alp、osx和ocn中的一种或多种的表达,和/或相对于通过添加制造,随后是机械侵蚀、化学侵蚀,或机械和化学侵蚀两者产生的骨科植入物表面,分别从间充质干细胞、前成骨细胞和成骨细胞中诱导alp、osx和ocn中一种或多种表达的能力较差,以赋予本发明的骨诱导粗糙度,所述骨科植入物表面是平滑的,或者包括未加工/侵蚀的齿、脊、凹槽和超宏观结构,或包括已经冷喷涂、热喷涂或用粘合剂固定的颗粒、纤维或粉末,或者没有机械侵蚀、化学侵蚀,或机械和化学侵蚀两者,以赋予包括微尺度结构和纳米级结构的骨诱导粗糙度,或者缺少包括微尺度结构和纳米级结构的骨诱导粗糙度。相关地,骨科植入物表面不能显着增强分别来自间充质干细胞、前成骨细胞和成骨细胞的alp、osx和ocn中的一种或多种的表达,不诱导分别来自间充质干细胞、前成骨细胞和成骨细胞中的alp、osx和ocn中的一种或多种的表达,和/或相对于通过大块基底的机械侵蚀、化学侵蚀,或机械和化学侵蚀两者产生的骨科植入物表面,分别从间充质干细胞、前成骨细胞和成骨细胞中诱导alp、osx和ocn中一种或多种表达的能力较差,所述骨科植入物表面是平滑的,或者包括未加工/侵蚀的齿、脊、凹槽和超宏观结构,或包括已经冷喷涂、热喷涂或用粘合剂固定的颗粒、纤维或粉末,或者没有机械侵蚀、化学侵蚀,或机械和化学侵蚀两者,以赋予包括微尺度结构和纳米级结构的骨诱导粗糙度,或者缺少包括微尺度结构和纳米级结构的骨诱导粗糙度。包括以下示例以更清楚地说明本发明的总体性质。这些示例是本发明的示例性而非限制性的。示例1添加制造钛表面的sem图像使用激光熔化/烧结(例如,直接金属激光烧结(dmls))或电子束熔化(ebm)来添加制造钛盘。然后对这些盘进行应力消除或热等静压,并进行机械和化学侵蚀,如表1所示。获得了盘的扫描电子显微镜(sem)图像,并显示在图1a、1b、1c、1d和1e中。(sem是一种电子显微镜,其中样品的表面被反射形成图像的电子束扫描。)表面20a是dmls产生的表面,其经受应力消除但没有侵蚀。表面20b是ebm生产的表面,其经受热等静压,但没有侵蚀。表面20c是dmls生产的表面,其经受热等静压,但没有侵蚀。表面22a是dmls产生的表面,其经受应力消除和机械和化学侵蚀。表面22b是ebm生产的表面,其经受热等静压和机械和化学侵蚀。表面22c是dmls生产的表面,其经受热等静压和机械和化学侵蚀。表面16e是激光产生的表面,其使用碳酸氢钠喷射进行热等静压和机械侵蚀。表面16f是激光产生的表面,其使用钛爆炸进行热等静压和机械侵蚀。表面29d是激光产生的表面,具有内置的宏观纹理,经受热等静压和机械和化学侵蚀。图1a、1b、1c、1d和1e的sem图像显示了如何通过添加制造的表面的连续机械和化学侵蚀将微米级和纳米级结构赋予钛表面。表1.添加制造表面#,制造后添加制造处理20a,只有dmls消除应力20b,只有ebmhip20c,只有dmlship22a,dmls,然后是机械和化学侵蚀消除应力22b,ebm,然后是机械和化学侵蚀hip22cdmls,然后是机械和化学侵蚀hip16e,激光产生,然后是机械侵蚀hip16f,激光产生,然后是机械侵蚀hip29d,激光产生,然后是机械和化学侵蚀hip示例2碱性磷酸酶、osterix和骨钙素作为成骨细胞发育和骨诱导的公认标志物成骨分化是一个连续过程,其特征在于几种蛋白质的上升和下降。本文件中分析的蛋白质表征早期(alp)、中期(osx)和晚期(ocn)成骨细胞标记物。成骨细胞分化的过程开始于间充质干细胞发展成能够经历成骨或软骨形成并表达alp的中间祖细胞。致力于成骨谱系的这些中间祖细胞(现称为前成骨细胞)增加alp的表达。随着前成骨细胞进展为成骨细胞,osx的表达增加,并且最终,一旦前成骨细胞变成成骨细胞,ocn的表达增加。成骨细胞最终将进一步成熟并开始转变为骨细胞或经历细胞凋亡。成熟的成骨细胞状态的特征在于alp降低,一旦成骨细胞分化为骨细胞,osx和ocn的表达也降低(baekw-yetal.,j.boneminer.res.24:1055–65(2009);zhangc.,j.orthopaedicsurg.andres.5:1(2010);andtuqetal.,tissueeng’g1:2431–40(2007))。体内评估显示在骨折愈合期间存在alp和ocn。在这些评估中,alp和ocn产生在骨折后8周愈合骨折中最高(leungksetal.,bone&jointjournal75:288–92(1993);andherrmannm.etal.,clin.chemistry48:2263–66(2002))。此外,alp和ocn已用于体外评估合成材料促进体内骨形成的可能性。已经进一步证明,体外增加的alp和ocn与体内合成移植物成功相关(bordenm.etal.,j.biomed.mater.res.61:421–29(2002);bordenm.etal.,biomaterials.23:551–59(2002);andbordenm.etal.,j.bonejointsurg.br.86:1200–08(2004))。使用钛网的类似评估已经将体外alp和骨桥蛋白(分化早于分离的基质蛋白比ocn)与体内成功相关联(dattan.,biomaterials.26:971–77(2005);bancroftg.n.,proc.natl.acad.sci.u.s.a.99:12600–05(2002);andsikavitsasvietal.,j.biomed.mater.67a:944–51(2003))。示例3骨诱导表面生长的mg63细胞成骨标志物的评估mg63细胞是前成骨细胞系。将mg63细胞接种到10,000个细胞/cm2的盘上,在含有10%fbs、1%青霉素/链霉素、50μg/ml抗坏血酸和10mmβ-甘油磷酸的emem中培养。培养7天后,用含有蛋白酶抑制剂的piercemammalianproteinextractionreagent裂解细胞,并且评估裂解物的碱性磷酸酶(alp)、骨桥蛋白(opn)和runx2的表达。碱性磷酸酶(alp),一种早期成骨细胞分化标志物,通过酶测定法测定,依赖于在alp存在下将对硝基苯基磷酸酯转化为对硝基苯酚,然后测量对硝基苯酚的吸光度。将alp标准化为样品中存在的dna量。用标准picogreen测定法测量dna。骨桥蛋白(opn),一种由成骨细胞在整个分化过程中表达的蛋白质,通过定量western印迹测量并归一化为微管蛋白。结果显示在图2a、2b和2c中。图2a-2c的表面键如表1所示。图2a显示了在添加制造的表面20a、20b和20c以及22a、22b和22c上培养的mg63细胞表达的碱性磷酸酶的水平。图2b显示了在添加制造的表面20a、20b和20c以及22a、22b和22c上培养的mg63细胞表达的骨桥蛋白水平。图2c显示了在添加制造的表面20a、20b和20c以及22a、22b和22c上培养的mg63细胞表达的runx2的水平。表面20a、20b和20c以及22a、22b和22c是与图1a、1b和1c中所述相同的表面。如图所示,在alp、runx2和opn表达方面,添加制造的(dmls和ebm)和加工(机械和化学侵蚀)表面明显优于加成制造但未加工的表面。示例4骨诱导表面生长的saos2细胞成骨标志物的评估saos-2细胞获自atcc(manassas,va);picogreenassays,mccoy的5a培养基和青霉素/链霉素均来自lifetechnologies(carlsbad,ca);胎牛血清获自atlantabiologicals(atlanta,ga);碱性磷酸酶测定法获自bio-rad(hercules,ca);osterixelisa获自lifespanbiosciences(seattle,wa)和osteocalcinelsia获自r&dsystems(minneapolis,mn)。将saos-2细胞维持在由补充有15%fbs和1%青霉素/链霉素的mccoy's5a组成的基础生长培养基中。一旦在培养物中达到适当数量的细胞,将saos-2细胞以10,000细胞/cm2的密度接种在钛盘表面(表1)上。在每种表面类型上培养saos-2细胞7天,并且每两天更换培养基。在第7天,将培养基冷冻用于进一步分析,并将saos-2细胞在ripa缓冲液中裂解(150mm氯化钠,1%v/vtritonx-100非离子表面活性剂,0.5%w/v脱氧胆酸钠,0.1%w/v十二烷基硫酸钠,50mmtrizma碱,ph8.0)。按照制造商的方案,使用picogreenassay定量细胞dna。根据制造商的方案,通过alp催化的对硝基苯磷酸转化为对硝基苯酚来测定碱性磷酸酶(alp)。使用elisa测定并遵循制造商的方案定量osterix(osx)和骨钙素(ocn)。还测定了runx2和opn,但未显示任何实质趋势或显着数据(数据未显示);这些都是非常早期的成骨细胞标志物。结果显示在图3a、3b、3c和3d中。图3a-3d的表面键如表1所示。图3a显示了在添加制造的表面20a、20b和20c以及22a、22b和22c上培养的saos-2细胞表达的碱性磷酸酶的水平。图3b显示了在添加制造的表面20a、20b和20c以及22a、22b和22c上培养的saos-2细胞表达的osterix水平。图3c显示了在添加制造的表面20a、20b和20c以及22a、22b和22c上培养的saos-2细胞表达的骨钙素水平。图3d显示分别在添加制造的表面16e、16f和29d上培养的saos-2细胞表达的碱性磷酸酶(最左边的条)、osterix(中心条)和骨钙素(最右边的条)的水平。表面20a、20b、20c、22a、22b、22c、16e、16f和29d是与图1a、1b、1c、1d和1e中所述相同的表面。如图3a、3b和3c所示,所有添加制造和加工(机械和化学侵蚀)表面相对于未经加工(机械和化学侵蚀)添加制造的表面,表现出alp、osx和ocn标记的改善的表达。如alp、osx和ocn标记所证明的,相对于没有侵蚀的添加制造表面,添加制造的表面的处理显着增强了成骨细胞分化。如图3d所示,相对于表面16e和16f,添加制造和加工(机械和化学侵蚀)表面29d表现出改善的alp、osx和ocn标记物的表达,所述表面16e和16f是仅通过机械但非化学侵蚀添加制造和加工的。尽管以上参考某些特定实施例和示例进行了说明和描述,但是本发明并不旨在限于所示的细节。而是,在不脱离本发明的精神的情况下,可以在权利要求的等同物的范围和范围内对细节进行各种修改。例如,明确地旨在本文件中广泛叙述的所有范围在其范围内包括落入更宽范围内的所有较窄范围。除非特别说明,否则还明确地指出,制造上述各种装置的过程的步骤不限于任何特定顺序。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1