一种产生NO的pH敏感脂质体及其制备方法与流程
本发明属于生物医用材料技术领域,具体涉及一种产生no的ph敏感脂质体及其制备方法。
背景技术:
肿瘤细胞多药耐药性的产生是肿瘤治疗失败的重要原因。关于肿瘤细胞的耐药机制,目前比较流行的观点是p-糖蛋白(p-gp)介导的药物外排。no是一种气体分子信使,其在各种生理过程中起着关键作用。更重要的是,no可以下调p-gp的表达水平,从而起到逆转肿瘤多药耐药性的作用。据报道,no供体在肿瘤细胞内可通过酶、酸性、氧化还原、光等刺激产生no,但是no供体存在生理稳定性差、缺乏靶向性和组织特异性、药物作用时间过短等问题,从而限制了其作为p-gp抑制剂的应用。
脂质体是一种由磷脂组成的双分子层结构囊泡,其具有良好的生物相容性和生物利用度,可以同时包载脂溶性和水溶性的药物小分子。ph敏感性脂质体可在肿瘤组织或肿瘤细胞的酸性ph条件下促发药物释放。本发明结合具有肿瘤微环境(ph=6.5)ph敏感的聚合物peg-pll-dma和no供体可自发产生no的特点,构建可产生no的ph敏感脂质体,使其具有在肿瘤组织微环境中可发生电荷翻转并自发产生no的特性,提高疗效。
技术实现要素:
本发明的目的在于提供一种产生no的ph敏感脂质体,该脂质体在肿瘤组织微环境可发生电荷翻转以促进肿瘤细胞对脂质体的摄取,并可同时产生no,以抑制p-gp介导的药物外排,逆转肿瘤多药耐药性。
为实现上述目的,本发明采用如下技术方案:
一种产生no的ph敏感脂质体,该脂质体的磷脂层中包含了胆固醇(chol)、氢化大豆卵磷脂(hspc)、1,2-二硬脂酸-3-磷脂酰乙醇胺-聚乙二醇2000(dspe-peg2000)、(2,3-二油酰基-丙基)-三甲胺(dotap)和疏水性抗肿瘤药物,内水相中包载了亲水性no供体,并通过静电作用将ph敏感性聚合物聚乙二醇-聚赖氨酸-二甲基马来酸酐(peg-pll-dma)包覆在脂质体表面。
其中,hspc、chol、dspe-peg2000、dotap和疏水性抗肿瘤药物的摩尔比为12:1:1:(0.3~10):(0.1~5)。所述疏水性抗肿瘤药物为紫杉醇、多烯紫杉醇、喜树碱和长春新碱中的任意一种。
hspc、dotap及dspe-peg2000的质量之和与所用亲水性no供体的质量之比为10:1~120:1。所述亲水性no供体为二亚乙基三胺no亲核复合体(detanonoate)、聚壬二酐no亲核试剂(papanonoate)和精胺氮氧化加合物(sperminenonoate)中的任意一种。
hspc、dotap及dspe-peg2000的质量之和与所用peg-pll-dma的质量之比为1:1~1:30。
所述产生no的ph敏感脂质体的制备方法包括以下步骤:
(1)将hspc、chol、dspe-peg2000、dotap和疏水性抗肿瘤药物溶解于氯仿溶液中;
(2)通过旋转蒸发法除去氯仿溶液,得到均匀的膜状材料;
(3)用ph=8.0含0.5~3mm亲水性no供体的pbs缓冲溶液洗脱后,再采用超声波细胞破碎仪,在功率为100~400w的条件下超声处理5-20min,以形成包载有no供体和抗肿瘤药物的脂质体;
(4)加入peg-pll-dma,室温搅拌5min~8h,即得所述产生no的ph敏感脂质体。
本发明的显著优点在于:本发明采用ph敏感性聚合物peg-pll-dma包覆共载有抗肿瘤药物与no供体的阳离子脂质体,使所得ph敏感脂质体在肿瘤组织微环境中可发生电荷翻转,以利于肿瘤细胞对脂质体的摄取;当到达肿瘤细胞后,包载于脂质体内水相的no供体可自发产生no,既可抑制p-gp介导的药物外排,又可提高脂质体膜的通透性,增强包载于脂质体磷脂双分子层间的抗肿瘤药物在肿瘤细胞的富集,提高疗效。
附图说明
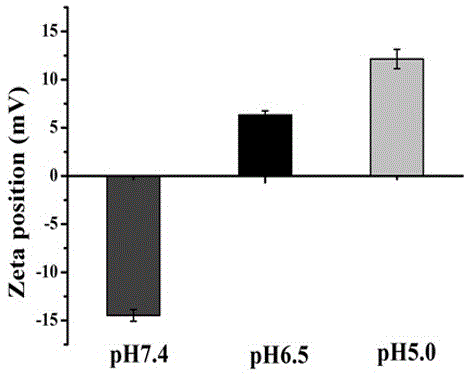
图1为实施例1制备的产生no的ph敏感脂质体在不同ph值的pbs中的电位图。
具体实施方式
为了使本发明所述的内容更加便于理解,下面结合具体实施方式对本发明所述的技术方案做进一步的说明,但是本发明不仅限于此。
实施例1:一种产生no的ph敏感脂质体的制备方法
(1)将chol2.01mg、hspc47.03mg、dspe-peg200013.75mg、dotap7.0mg和紫杉醇4.05mg溶解于30ml氯仿溶液中;
(2)利用旋转蒸发仪,在室温下以100r/min的转速旋蒸4h,得到均匀的膜状材料;
(3)用6.78ml、ph=8.0含2.2mmdetanonoate的pbs缓冲溶液洗脱后,利用超声波细胞破碎仪在功率为300w的条件下超声处理10min,以形成包载有no供体和抗肿瘤药物的脂质体;
(4)以hspc、dotap及dspe-peg2000的质量之和与peg-pll-dma的质量之比为1:6加入peg-pll-dma,室温搅拌1h,即得产生no的ph敏感脂质体。
实施例2:一种产生no的ph敏感脂质体的制备方法
(1)将chol2.01mg、hspc47.03mg、dspe-peg200013.75mg、dotap15.05mg和紫杉醇4.05mg溶解于30ml氯仿溶液中;
(2)利用旋转蒸发仪,在室温下以100r/min的转速旋蒸4h,得到均匀的膜状材料;
(3)用7.58ml、ph=8.0的含1.375mmdetanonoate的pbs缓冲溶液洗脱后,利用超声波细胞破碎仪在功率为300w的条件下超声处理10min,以形成包载有no供体和抗肿瘤药物的脂质体;
(4)以hspc、dotap及dspe-peg2000的质量之和与peg-pll-dma的质量之比为1:30加入peg-pll-dma,室温搅拌1h,即得产生no的ph敏感脂质体。
实施例3:产生no的ph敏感脂质体的电位测定
分别采用ph=7.4、6.5和5.0的pbs溶液将实施例1制备的产生no的ph敏感脂质体稀释至浓度为400µg/ml,用马尔文激光粒度仪测定其zeta电位,其结果见图1。
由图1可知,在ph=7.4的pbs溶液中,脂质体的zeta电位为负电荷;在ph=6.5和5.0的pbs溶液中,脂质体发生电荷翻转变为正电荷,说明所制备的脂质体具有ph敏感性。
实施例4:产生no的ph敏感脂质体的体外释放实验
在满足漏槽条件的情况下,将275ml实施例1制备的脂质体用ph=8.0的pbs溶液稀释至1ml,然后分别浸入40mlph=7.4、6.5、5.0的pbs溶液,37℃、100r/min条件下进行释放;分别于预先设定的时间点(1、2、4、8、12、24、48、72、96、120h)取出0.5ml释放液,同时补充等量的新鲜pbs溶液;取出的释放液用适量乙腈稀释后利用hplc于227nm波长处检测药物释放量,计算紫杉醇的累积释放率。
实验结果显示,释放120h时,在ph=7.4的溶液中,产生no的ph敏感脂质体和未包载no的脂质体中紫杉醇的释放量都在30%左右;在ph=6.5的溶液中,产生no的ph敏感脂质体中紫杉醇的释放量增至70%,而未包载no的脂质体中紫杉醇的释放量仍低于53%;在ph=5.0的溶液中,产生no的ph敏感脂质体中紫杉醇的释放量高达90%,未包载no的脂质体中紫杉醇的释放量约70%,以上结果进一步证明脂质体中包载的no供体在酸性条件下产生的no可明显促进脂质体中紫杉醇的释放。
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
- 还没有人留言评论。精彩留言会获得点赞!