一种复合神经修复导管及其制备方法与流程
本发明属于医用生物材料、医疗器械领域,具体涉及一种复合神经修复导管及其制备方法和应用。
背景技术:
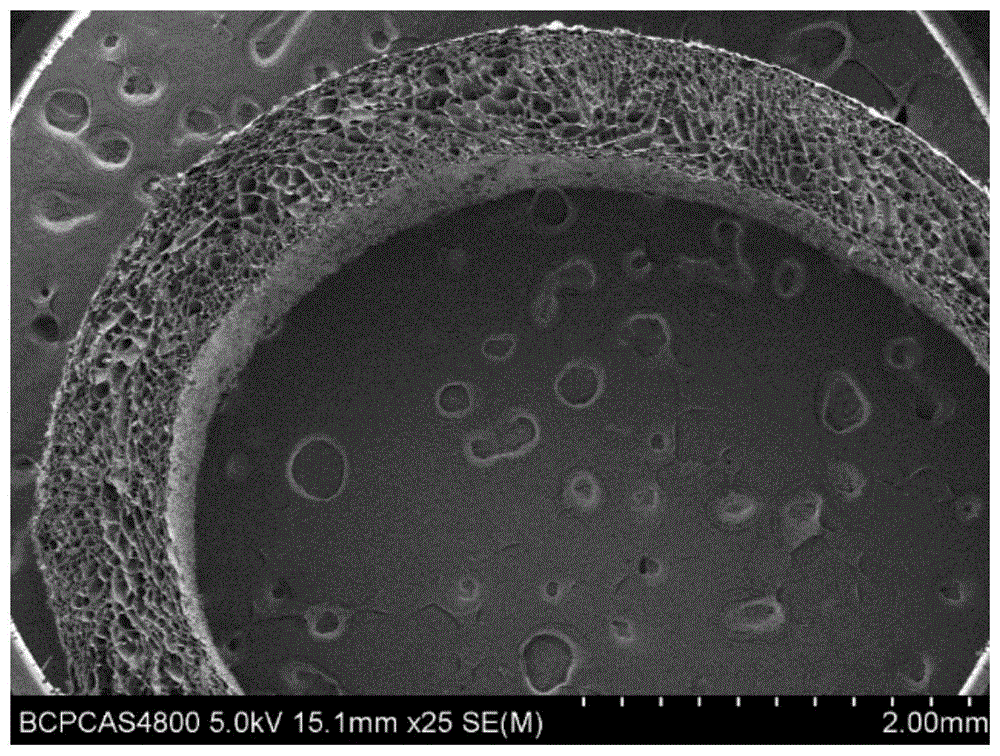
:神经导管是利用组织工程学的原理和方法,用天然和/或合成可降解高分子材料制备的可以在周围神经损伤断端建立神经桥接的中空管状结构,能够为损伤的神经提供适宜的神经再生微环境。常用的天然材料包括胶原、明胶、壳聚糖、丝素蛋白等,均具有良好的生物相容性、低免疫原性;合成可降解高分子材料包括聚乳酸、聚羟基丁酸戊酸共聚酯、聚(d,l-乳酸-co-乙醇酸)等,具有良好的力学强度、可降解性特点。神经修复过程是一个复杂的生物学问题,导管除了具有良好的生物相容性、无毒、低免疫原性性外,适宜的导管构型及力学强度对神经修复同样起到重要作用。目前,通过研究不同管壁结构,无论单层、双层还是多层结构仍存在一些问题,不能完全仿制出具有天然神经结构的支架。已经上市的天然高分子材料的神经导管,虽然具有良好的生物相容性、低免疫原性,但缺陷在于力学强度不足,降解过快,在实际临床应用过程中耐撕裂能力差,容易出现中空导管崩塌现象而阻碍神经修复过程。合成可降解高分子材料的神经导管虽然具有相对更好的力学强度、较慢的降解性能,但其仍然具有聚酯自身的疏水性及相对较差的生物相容性的缺点,不利于细胞的附着和迁移并容易引起排异反应。因此,制备出具有完整三维结构、良好生物相容性、优良的力学强度、适宜的生物降解性,并能够引导神经再生的神经导管具有重要意义。目前,同时兼具良好生物相容性、定向引导神经再生、可降解并能够良好的支撑导管结构的神经导管仍然处于研究探索阶段,许多专利技术均提出各种的制备神经导管的方法,步骤相对较繁琐,可操作性差。因此提供一种简单、可行、易于工业化的神经导管制作方法对于临床应用具有重要意义。技术实现要素:为解决现有技术中存在的缺陷,本发明提供了一种复合神经修复导管及其制备方法和应用。一方面,本发明提供了一种复合神经修复导管,所述复合神经修复导管包括中空的天然高分子导管以及包覆在天然高分子导管外面的静电纺丝纤维层;所述天然高分子导管由质量体积浓度为4%-7%的胶原浆液制成,所述静电纺丝纤维层由包含聚乳酸和壳聚糖的纺丝溶液制成,所述聚乳酸和壳聚糖的质量比例为(6-9.5):(0.5-4)。进一步的,所述天然高分子导管优选由质量体积浓度为6%的胶原浆液制成;优选的,所述胶原为i型胶原。在一个实施方式中,所述胶原浆液是将胶原蛋白与酸溶液混合后制备得到胶原浆液。所述聚乳酸和壳聚糖的质量比例为(7-9.5):(0.5-3),优选,(8-9.5):(0.5-2),更优选,(9-9.5):(0.5-1),更优选,7:3、8:2、9:1或9.5:0.5。所述纺丝溶液是将聚乳酸和壳聚糖溶于三氟乙酸中制备得到。进一步的,所述天然高分子导管孔径为50-220μm,壁厚0.4±0.3mm,所述静电纺丝纤维层的厚度为0.05-0.15mm,纤维直径为300-700nm。另一方面,本发明提供了复合神经修复导管的制备方法,所述方法包括中空的天然高分子导管的制备以及包覆静电纺丝纤维层的步骤;在制备天然高分子导管时选择合适质量体积浓度的胶原浆液,注入模具中,冷冻干燥,高温固定成型;然后将中空的天然高分子导管通过静电纺丝方法包覆静电纺丝纤维层得到复合神经修复导管。在其他的实施方式中,复合神经修复导管的制备方法还包括复合修复导管干燥、包装、灭菌等步骤。优选的,所述干燥方法为真空干燥,条件为:30-60℃真空干燥12-48h或室温风干48-96h,优选40℃真空干燥24h。优选的,灭菌方式为环氧乙烷气体灭菌或者钴60辐照灭菌,优选环氧乙烷气体灭菌。在一个实施方式中,所述中空的天然高分子导管的制备包括如下步骤:(1)提取i型胶原蛋白,将胶原蛋白研磨粉碎后在0.4-0.8m冰醋酸中酸化120-240min,得到均匀浆液;(2)将上述浆液进行离心,温度控制在5-20℃,转数3000-5000rpm,时间40-100min,灌装至模具中;(3)将模具固定后,为沿轴向方向缓慢进样,进行梯度冷冻成型,匀速升降机速度为5-15转/min,角度调节5-10,时间间隔1-10s,温度降至-60℃后停止下降,维持20-50min,并在冷冻室解冻1-5h;(4)将成型产品取出中轴后进行冷冻干燥,高温真空固定。所述浆液中胶原蛋白浓度为4-10%(质量体积比);优选6-7%(质量体积比);所述冰醋酸的摩尔浓度优选0.5-0.6m;浆液离心的温度优选12℃,转数优选4000rpm,时间优选80min。由上述方法制备获得的导管孔径为50-220μm,内径2-5mm,壁厚0.4±0.3mm。优选导管长15cm,内径4mm,壁厚0.5mm。在一个实施方式中,所述静电纺丝过程如下:将聚乳酸、壳聚糖以三氟乙酸作为溶剂混合为均匀的静电纺丝溶液,静电纺丝溶液中聚乳酸:壳聚糖(质量比)=(7-9.5):(0.5-3);优选聚乳酸:壳聚糖(质量比)=7:3;优选聚乳酸:壳聚糖(质量比)=8:2;优选聚乳酸:壳聚糖(质量比)=9:1;优选聚乳酸:壳聚糖(质量比)=9.5:0.5。单轴静电纺丝,静电高压15-30kv,推进速度0.8-2.4ml/h,接收距离15-30cm,纺丝时间60-120min。优选静电高压20kv,推进速度1.8ml/h,接收距离20cm,纺丝时间90min。本发明还提供了使用本发明所述方法制备获得的复合神经修复导管。本发明还提供了所述复合神经修复导管在神经修复临床手术中的应用。尤其适用于各种原因的创伤和肿瘤切除造成的周围神经缺损,修复缺损长度1.5cm。另一方面,本发明还提供了复合神经修复导管在制备抗拉伸和耐降解的神经修复材料中的应用;优选的,所述降解为蛋白酶降解、酸降解或碱降解中的一种或多种。进一步的,所述抗拉伸为使用med-01医药包装性能测试仪,设定条件为10mm/min,对材料进行拉伸测试,材料的平均最大拉力不低于29n,优选,不低于34n,更优选,不低于42n,更优选,不低于48n,更优选,不低于50n。本发明的有益效果是:1、本发明通过胶原导管的冷冻干燥技术结合一步静电纺丝方法,获得更适宜于神经修复过程的复合神经修复导管;在保持胶原导管特性的基础上,明显改善了胶原导管的力学强度,在神经修复过程中维持良好的三维结构,避免出现导管崩塌现象;该制作工艺简单,材料来源丰富低廉,易于工业化。2、冷冻干燥获得具有定向多孔的天然高分子胶原导管,具有良好的生物相容性且孔隙连通并沿着导管方向排列,能够引导神经细胞定向生长,促进神经再生;外层包覆无序的静电纺丝纤维,由于聚乳酸和壳聚糖的不相容性,在静电纺丝过程中随着纺丝溶剂的挥发而发生相分离,聚阳离子壳聚糖向外游离,从而直接形成核壳结构;由于静电纺丝技术自身的高孔隙率、大比表面特点能够模拟人体细胞外基质结构,有利于细胞附着、迁移和生长,此外,该纤维膜成分选择为内层是合成可降解聚乳酸和外层是天然高分子壳聚糖,聚乳酸具有良好的可纺性从而确保纤维膜优良的力学强度,外层壳聚糖改善了聚乳酸的生物相容性和亲水性;在神经修复过程中不仅能够为轴突生长提供导向作用,而且无序的核壳结构静电纺丝纤维的包覆能够提供各向同性的优良的力学强度,提高导管在外科手术使用中的耐撕裂能力以及由内而外梯度逐层降解能够确保在神经再生过程中保持神经导管三维结构的完整性和可塑性。附图说明此处所说明的附图用来提供对本申请的进一步理解,构成本申请的一部分,本申请的示意性实施例及其说明用于解释本申请,并不构成对本申请的不当限定。在附图中:图1为本发明制备所得的复合神经导管内层横切面的扫描电子显微镜(sem)图;图2为本发明制备所得的复合神经修复导管内层侧切面的扫描电子显微镜(sem)图;图3为本发明制备所得的复合经修复导管外层纺丝纤维的扫描电子显微镜(sem)图;图4为本发明制备所得的复合神经修复导管外层纺丝纤维的透射电子显微镜(tem)图;图5为本发明制备所得的复合神经修复导管外层纺丝纤维用异硫氰酸荧光素标记后激光扫描共聚焦显微镜(clsm)图;图6为本发明制备所得的复合神经修复导管横截面外观照片;图7为本发明制备所得的复合神经修复导管整体外观照片;图8为酶降解20min时实施例1胶原管在降解液中的状态;图9为酶降解20min时实施例2复合修复管在降解液中的状态;图10为酶降解40min时实施例1胶原管在降解液中的状态;图11为酶降解40min时实施例2复合修复管在降解液中的状态;图12为酶降解60min时实施例1胶原管在降解液中的状态;图13为酶降解60min时实施例2复合修复管在降解液中的状态;图14为酶降解60min时实施例2复合修复管在降解液中的纵面图;图15为120min时复合修复管在降解液中的状态;图16为酸降解0min时实施例1胶原管缩小状态;图17为酸降解180min时实施例2复合修复管状态;图18为酸降解60min时实施例2复合修复管拉伸观察;图19为碱降解过程中实施例2复合修复导管状态。具体实施方式为了更清楚的阐释本申请的整体构思,下面以实施例的方式进行详细说明。在下文的描述中,给出了大量具体的细节以便提供对本申请更为彻底的理解。然而,对于本领域技术人员来说显而易见的是,本申请可以无需一个或多个这些细节而得以实施。在其他的例子中,为了避免与本申请发生混淆,对于本领域公知的一些技术特征未进行描述。实施例1:复合神经修复导管内层胶原导管的制备以内层胶原导管用6%浓度胶原浆液制备为例,内层导管制备步骤如下:(1)按照0.6g研磨粉碎后的i型胶原蛋白:10ml(0.6m醋酸溶液)的比例混合,酸化200min得到浓度为6%(质量体积比)的均匀胶原浆液;(2)将步骤(1)胶原浆液离心:温度控制在10±2℃,转数4000rpm,时间60min;(3)离心后装至模具:取直径为6mm,长度为30mm的中空不锈钢圆柱状模具,注入胶原浆液,中轴直径为4mm,插入模具;(4)冷冻干燥:梯度冷冻:模具置于升降机中,下降速度为10转/min,角度调节为9,时间间隔1.5s,温度降至-60℃关闭升降机,在-80℃~-60℃维持40min,在冷冻室-20℃~-30℃条件下解冻2h,打开模具两端的固定帽,取出中轴,其中,冻干干燥程序如下:(5)高温真空固定:压力为-0.09mpa,温度为105±2℃,固定时间为24h。以下实施例2-6制备复合神经修复导管所用的内层胶原导管均采用实施例1相同的方法。实施例2:复合神经修复导管外层制备方法一(1)静电纺丝过程:将0.95g聚乳酸和0.05g壳聚糖溶解于三氟乙酸中,形成均匀的壳聚糖质量含量为5%的纺丝溶液,聚乳酸:壳聚糖=9.5:0.5(质量比);将实施例1制备的胶原导管置于静电场中,静电高压20kv,接收距离20cm,推进速度1.8ml/h,纺丝时间90min;(2)40℃真空干燥24h;(3)初包装后环氧乙烷气体灭菌。实施例3:复合神经修复导管外层制备方法二(1)静电纺丝过程:将0.9g聚乳酸和0.1g壳聚糖溶解于三氟乙酸中,形成均匀的壳聚糖质量10%的纺丝溶液,聚乳酸:壳聚糖=9:1(质量比);将实施例1制备的胶原导管置于静电场中,静电高压20kv,接收距离20cm,推进速度1.8ml/h,纺丝时间90min;(2)40℃真空干燥24h;(3)初包装后环氧乙烷气体灭菌。实施例4:复合神经修复导管外层制备方法三(1)静电纺丝过程:将0.8g聚乳酸和0.2g壳聚糖溶解于三氟乙酸中,形成均匀的壳聚糖质量含量为20%的纺丝溶液,聚乳酸:壳聚糖=8:2(质量比);将实施例1制备的胶原导管置于静电场中,静电高压22kv,接收距离25cm,推进速度1.5ml/h,纺丝时间90min;(2)40℃真空干燥24h;(3)初包装后环氧乙烷气体灭菌。实施例5:复合神经修复导管外层制备方法四(1)静电纺丝过程:将0.7g聚乳酸和0.3g壳聚糖溶解于三氟乙酸中,形成均匀的纺丝溶液,壳聚糖质量含量为30%,聚乳酸:壳聚糖=7:3(质量比);将实施例1制备的胶原导管置于静电场中,静电高压20kv,接收距离22cm,推进速度1.8ml/h,纺丝时间90min;(2)40℃真空干燥24h;(3)初包装后环氧乙烷气体灭菌。实施例6:复合神经修复导管外层制备方法五(1)静电纺丝过程:将0.6g聚乳酸和0.4g壳聚糖溶解于三氟乙酸中,形成均匀的纺丝溶液,壳聚糖质量含量为40%,聚乳酸:壳聚糖=6:4(质量比);将实施例1制备的胶原导管置于静电场中,静电高压22kv,接收距离20cm,推进速度1.5ml/h,纺丝时间90min;(2)40℃真空干燥24h;(3)初包装后环氧乙烷气体灭菌。实施例7:复合神经修复导管外层制备方法六实施例1中胶原浓度为4%,其他条件不变:(1)静电纺丝过程:将0.9g聚乳酸和0.1g壳聚糖溶解于三氟乙酸中,形成均匀的壳聚糖质量10%的纺丝溶液,聚乳酸:壳聚糖=9:1(质量比);采用实施例1的方法,用4%(质量体积比)的均匀胶原浆液制备4%胶原导管,然后将4%胶原导管置于静电场中,静电高压20kv,接收距离20cm,推进速度1.8ml/h,纺丝时间90min;(2)40℃真空干燥24h;(3)初包装后环氧乙烷气体灭菌。实施例8:复合神经修复导管外层制备方法七实施例1中胶原浓度为10%,其他条件不变:(1)静电纺丝过程:将0.9g聚乳酸和0.1g壳聚糖溶解于三氟乙酸中,形成均匀的壳聚糖质量10%的纺丝溶液,聚乳酸:壳聚糖=9:1(质量比)。采用实施例1的方法,用10%(质量体积比)的均匀胶原浆液制备10%胶原导管,然后将10%胶原导管置于静电场中,静电高压20kv,接收距离20cm,推进速度1.8ml/h,纺丝时间90min;(2)40℃真空干燥24h;(3)初包装后环氧乙烷气体灭菌。本发明为了更加直观形象地说明外层静电纺丝纤维的核壳结构,内层主要成分为聚乳酸外层主要成分为壳聚糖,采用异硫氰酸荧光素标记壳聚糖的方法进行表征,在纤维表面显示出明显的黄绿的荧光,如图5外层静电纺丝纤维的荧光染色的clsm图所示。实施例9:复合神经修复导管效果比较1、拉伸强度分析使用med-01医药包装性能测试仪,设定条件为10mm/min,对材料进行拉伸实验,实验结果如下:2、酶降解分析每个肖特瓶中加入100ml纯化水,0.833ml浓盐酸,1g胃蛋白酶,在摇床中混合10分钟后37℃水浴预热30min,加入试验样品,摇床温度设定为37℃,转速为150r/min,震荡观察降解情况。3、酸降解分析配置6m盐酸,分别放入实验品,于60℃烘箱中静置,不同时间进行观察。降解时间6%胶原导管(实施例1)实施例20min迅速缩小,变形迅速缩小,变形5min体积减小体积逐渐缩小,保持管状结构10min完全降解,溶液澄清体积逐渐缩小,保持管状结构60min-体积逐渐缩小,保持管状结构180min-体积逐渐缩小,仍可见管状结构在60min时,对实施例2的导管进行拉伸,仍具有较好的力学性能。4、碱降解分析配置2.5%氢氧化钠溶液,分别放入实验品,于60℃烘箱中静置,不同时间进行观察。降解时间6%胶原导管(实施例1)实施例20min无明显变化迅速缩小,变形5min体积减小体积减小15min完全降解体积减小,溶液有絮状纤维20min-体积减小,溶液有絮状纤维50min-完全降解,溶液浑浊综上比较可发现,内层6%胶原导管,外层聚乳酸与壳聚糖质量比为9.5:0.5,纺丝条件:静电高压20kv,接收距离20cm,推进速度1.8ml/h,纺丝时间90min的条件下可获得较理想的复合神经胶原导管。复合神经胶原导管相比于胶原导管在一定时间内能更好地保持结构的完整性和可塑性,将更有利于神经修复。以上所述仅为本申请的实施例而已,并不用于限制本申请。对于本领域技术人员来说,本申请可以有各种更改和变化。凡在本申请的精神和原理之内所作的任何修改、等同替换、改进等,均应包含在本申请的权利要求范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1