桑树叶水提物粉末,其制备,自由基清除作用及应用的制作方法
本发明涉及一种制备鲜桑树叶水提物粉末的方法,涉及由该方法制得的鲜桑树叶水提物粉末在制备自由基清除药物中的应用。本发明属于生物医药领域。
背景技术:
大量统计数据说明,自由基堆积造成的损伤包括氮自由基及羟自由基堆积造成的损伤与衰老,人体免疫功能低下,动脉粥样硬化,缺血再灌注及癌症发病有密切关系。有效地预防氮自由基及羟自由基堆积造成的损伤已经成为全球关注的健康问题。虽然有些维生素和中药具有氮自由基及羟自由基清除作用,但作为预防药物长期服用仍然存在不确定性。发现无任何毒副作用可用于预防氮自由基及羟自由基堆积造成的损伤的药物,是药物研究的重要方向。这样一来,开发无毒副作用的清除氮自由基及羟自由基的药物便越来越受到重视。虽然已经付出了巨大努力,可是一直取得没有实质性进展。
桑树叶通常在春季枝叶茂盛时采摘,晒干或新鲜食用。例如晒干的桑树叶可以泡茶,鲜嫩的桑树叶可以炖汤或凉拌。民间认为桑树叶具有疏散风热,清肺润燥及清肝明目功效。
发明人长期从事鲜桑树叶水提物粉末的化学成分及治疗作用研究。发明人对鲜桑树叶水提物粉末的化学组分进行质谱分析,发现了23种未见报道的组分,主要包括桂皮酰奎尼酸和多取代懈皮素。虽然报道过鲜桑树叶水提物粉末单一组分的生物活性,但是全组分联合的生物活性并不知情。通过反复研究发明人发现,这23种组分联合可清除氮自由基及羟自由基。与所有桑树叶的已知发明相比,本发明的鲜桑树叶水提物粉末可清除自由基的发明达到了一个全新高度。根据这些认识,发明人提出了本发明。
技术实现要素:
本发明所要解决的技术问题是提供一种制备鲜桑树叶水提物粉末的方法以及由该方法制备得到的鲜桑树叶水提物粉末,实验证明,由本发明制备得到的鲜桑树叶水提物粉末具有免疫增强作用。为了达到所述目的,本发明采用了以下四方面的技术手段。
第一方面的技术手段是提供了一种鲜桑树叶水提物粉末,分析鲜桑树叶水提物粉末的质谱总离子流图谱及对应的质谱峰的23种组分认定这种鲜桑树叶水提物粉末中含有11种奎尼酸类化合物及12种懈皮素类化合物;其中,所述的11种奎尼酸类化合物为3-o-[e-2-羧基正戊羰氧-3-羟基正丁酰氧-4-羧基正丙酰氧-5-羟基-6-(4-羧基-1-正丁烯羰氧)桂皮酰]奎尼酸,3-o-[e-2-羧基正丙烯羰氧-3-羟基-4-羟基正丙羰氧-5-羧基乙酰氧-6-(6-羟基-1,3-己二烯羰氧)桂皮酰]奎尼酸,3-o-[e-2-羟基乙酰氧-3-(5-羧基-1-正戊烯羰氧)-4,5,6-三(4-羧基-1-正丁烯羰氧)桂皮酰]奎尼酸,3-o-[e-2-羟基-3-羧基乙酰氧-4-羧基正丙烯羰氧-5,6-二(4-羧基正丁羰氧)桂皮酰]奎尼酸,3-o-[e-2-甲氧-3-羟基正丁烯酰氧-4-羧基正丁烯酰氧-5-(4-羧基-1-正丁烯羰氧)-6-(6-羟基-1-正己烯羰氧)桂皮酰]奎尼酸,3-o-[e-2-羟基正丙烯酰氧-3,4-二羧基正丙酰氧-5-(6-羟基-1,3,5-正己三烯羰氧)-6-(5-羟基-1,3-正戊二烯羰氧)桂皮酰]奎尼酸,3-o-[e-2,5-二(5-羧基-1,3-正戊二烯羰氧)-3-(6-羧基-1,3,5-正己三烯羰氧)-4-(4-羧基-1,3-正丁二烯羰氧)-6-(8-羟基-1,3,5,7-正辛四烯羰氧)桂皮酰]奎尼酸,3-o-[e-2,3,6-三(3-羧基-1-正丙烯羰氧)-4-(4-羧基-1,3-正丁二烯羰氧)-5-(4-羟基-1,3-正丁二烯羰氧)桂皮酰]奎尼酸,3-o-[e-2,5-二羟基正丙烯酰氧-3-羧基正丙烯酰氧)-4-(3-羧基-1-正丙烯羰氧)-6-羧基正丙羰氧桂皮酰]奎尼酸,3-o-[e-2,5-二甲氧-3-(4-羧基正丁羰氧)-4-(6-羟基-1-正己烯羰氧)-6-(5-羧基正戊羰氧)桂皮酰]奎尼酸和3-o-[e-2,5-二甲氧-3-羧基正丙羰氧-4,5-二(5-羧基正戊羰氧)桂皮酰]奎尼酸;其中,所述的12种懈皮素类化合物为3-o-葡萄糖苷-2’,3’-二甲氧-4’,5’-二(3-羧基-1-正丙烯羰氧)-6’-(6-羟基-1,3-正己二烯羰氧)懈皮素,3-o-葡萄糖苷-2’-羟基-3’-(6-羧基正己羰氧)-4’-(4-羧基-1-正丁烯羰氧)-5’-(3-羧基正丁羰氧)-6’-(5-羧基正戊羰氧)懈皮素,3-o-葡萄糖苷-2’-羟基-3’-(4-羟基正丁羰氧)-4’-(5-羟基正戊羰氧)-5’-羧基乙酰氧-6’-羟基乙酰氧懈皮素,3-o-葡萄糖苷-2’,6’-二甲氧基-3’-(4-羟基-1,3-正丁二烯羰氧)-4’,5’-二(4-羟基-1-正丁烯羰氧)懈皮素,3-o-葡萄糖苷-2’-甲氧基-3’-(4-羟基-1,3-正丁二烯羰氧)-4’-(4-羧基-1,3-正丁二烯羰氧)-5’-(3-羧基-1-正丙烯羰氧)-6’-甲酰氧懈皮素,3-o-葡萄糖苷-2’-羟基-3’-(4-羧基-1,3-正丁二烯羰氧)-4’-(4-羧基-1,3-正丁二烯羰氧)-5’,6’-二(3-羧基正丙羰氧)懈皮素,3-o-葡萄糖苷-2’-甲酰氧-3’-(3-羟基正丙羰氧)-4’-(3-羧基正丙羰氧)-5’-羧基正丙酰氧-6’-羟甲氧懈皮素,3-o-葡萄糖苷-2’-甲氧基-3’-(6-羧基-1,3,5-正己三烯羰氧)-4’,5’-二(3-羧基-1-正丁烯羰氧)-6’-甲酰氧懈皮素,3-o-葡萄糖苷-2’,3’,6’-三甲氧基-4’-羟甲基-5’-(6-羟基正己羰氧)懈皮素,3-o-葡萄糖苷-2’-羟基-3’-(3-羧基-1-正丙烯羰氧)-4’-(3-羟基正丙羰氧)-5’,6’-二羟基正丙酰氧懈皮素,3-o-葡萄糖苷-2’,3’-二甲氧基-4’-羟甲基-5’-(6-羟基正己羰氧)-6’-(3-羟基正丙羰氧)懈皮素和3-o-葡萄糖苷-2’-甲酰氧-3’,4’-二羧基乙酰氧基-5’-(7-羧基-1,3,5-正庚三烯羰氧)-6’-(9-羧基-1,3,5-正壬三烯羰氧)懈皮素。
第二方面的技术手段是提出一种制备所述的鲜桑树叶水提物粉末的方法,使鲜桑树叶水提物粉末可以这样制得:鲜桑树叶用自来水洗净,在蒸馏水中于60℃-90℃加热0.5-4小时,过滤,残饼用蒸馏水洗,合并的滤液减压浓缩,得到的粉末即为鲜桑树叶水提物粉末。
第三方面的技术手段是提出一种制备所述的鲜桑树叶水提物粉末的优选方法,其特征在于取鲜桑树叶,用自来水洗净,在蒸馏水中于70℃加热2小时,过滤,残饼用蒸馏水洗,合并的滤液减压浓缩,得到的粉末即为鲜桑树叶水提物粉末。
第四方面的技术手段是提出了鲜桑树叶水提物粉末在制备自由基清除药物中的应用。
附图说明
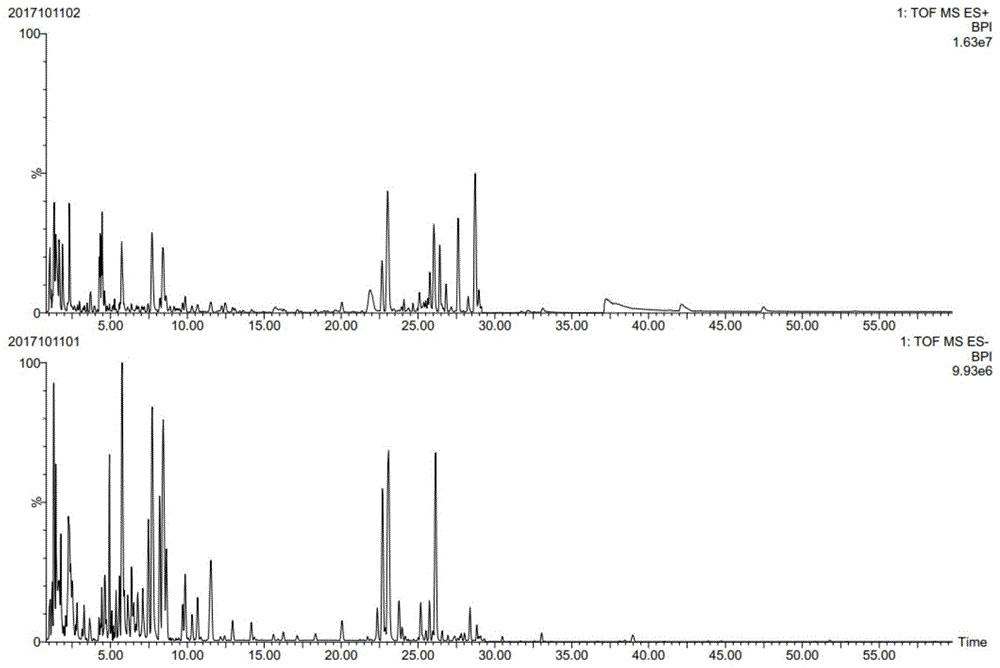
图1.鲜桑叶水提物粉末的uplc-质谱总离子流图谱。
图2.鲜桑叶水提物粉末中的3-o-[e-2-羧基正戊羰氧-3-羟基正丁酰氧-4-羧基正丙酰氧-5-羟基-6-(4-羧基-1-正丁烯羰氧)桂皮酰]奎尼酸及裂解产物。
图3.鲜桑叶水提物粉末中的3-o-[e-2-羧基正丙烯羰氧-3-羟基-4-羟基正丙羰氧-5-羧基乙酰氧-6-(6-羟基-1,3-己二烯羰氧)桂皮酰]奎尼酸及裂解产物。
图4.鲜桑叶水提物粉末中的3-o-[e-2-羟基乙酰氧-3-(5-羧基-1-正戊烯羰氧)-4,5,6-三(4-羧基-1-正丁烯羰氧)桂皮酰]奎尼酸及裂解产物。
图5.鲜桑叶水提物粉末中的3-o-[e-2-羟基-3-羧基乙酰氧-4-羧基正丙烯羰氧-5,6-二(4-羧基正丁羰氧)桂皮酰]奎尼酸及裂解产物。
图6.鲜桑叶水提物粉末中的3-o-[e-2-甲氧-3-羟基正丁烯酰氧-4-羧基正丁烯酰氧-5-(4-羧基-1-正丁烯羰氧)-6-(6-羟基-1-正己烯羰氧)桂皮酰]奎尼酸及裂解产物。
图7.鲜桑叶水提物粉末中的3-o-[e-2-羟基正丙烯酰氧-3,4-二羧基正丙酰氧-5-(6-羟基-1,3,5-正己三烯羰氧)-6-(5-羟基-1,3-正戊二烯羰氧)桂皮酰]奎尼酸及裂解产物。
图8.鲜桑叶水提物粉末中的3-o-[e-2,5-二(5-羧基-1,3-正戊二烯羰氧)-3-(6-羧基-1,3,5-正己三烯羰氧)-4-(4-羧基-1,3-正丁二烯羰氧)-6-(8-羟基-1,3,5,7-正辛四烯羰氧)桂皮酰]奎尼酸及裂解产物。
图9.鲜桑叶水提物粉末中的3-o-[e-2,3,6-三(3-羧基-1-正丙烯羰氧)-4-(4-羧基-1,3-正丁二烯羰氧)-5-(4-羟基-1,3-正丁二烯羰氧)桂皮酰]奎尼酸及裂解产物。
图10.鲜桑叶水提物粉末中的3-o-[e-2,5-二羟基正丙烯酰氧-3-羧基正丙烯酰氧)-4-(3-羧基-1-正丙烯羰氧)-6-羧基正丙羰氧桂皮酰]奎尼酸及裂解产物。
图11.鲜桑叶水提物粉末中的3-o-[e-2,5-二甲氧-3-(4-羧基正丁羰氧)-4-(6-羟基-1-正己烯羰氧)-6-(5-羧基正戊羰氧)桂皮酰]奎尼酸及裂解产物。
图12.鲜桑叶水提物粉末中的3-o-[e-2,5-二甲氧-3-羧基正丙羰氧-4,5-二(5-羧基正戊羰氧)桂皮酰]奎尼酸及裂解产物。
图13.鲜桑叶水提物粉末中的3-o-葡萄糖苷-2’,3’-二甲氧-4’,5’-二(3-羧基-1-正丙烯羰氧)-6’-(6-羟基-1,3-正己二烯羰氧)懈皮素及裂解产物。
图14.鲜桑叶水提物粉末中的3-o-葡萄糖苷-2’-羟基-3’-(6-羧基正己羰氧)-4’-(4-羧基-1-正丁烯羰氧)-5’-(3-羧基正丁羰氧)-6’-(5-羧基正戊羰氧)懈皮素及裂解产物。
图15.鲜桑叶水提物粉末中的3-o-葡萄糖苷-2’-羟基-3’-(4-羟基正丁羰氧)-4’-(5-羟基正戊羰氧)-5’-羧基乙酰氧-6’-羟基乙酰氧懈皮素及裂解产物。
图16.鲜桑叶水提物粉末中的3-o-葡萄糖苷-2’,6’-二甲氧基-3’-(4-羟基-1,3-正丁二烯羰氧)-4’,5’-二(4-羟基-1-正丁烯羰氧)懈皮素及裂解产物。
图17.鲜桑叶水提物粉末中的3-o-葡萄糖苷-2’-甲氧基-3’-(4-羟基-1,3-正丁二烯羰氧)-4’-(4-羧基-1,3-正丁二烯羰氧)-5’-(3-羧基-1-正丙烯羰氧)-6’-甲酰氧懈皮素及裂解产物。
图18.鲜桑叶水提物粉末中的3-o-葡萄糖苷-2’-羟基-3’-(4-羧基-1,3-正丁二烯羰氧)-4’-(4-羧基-1,3-正丁二烯羰氧)-5’,6’-二(3-羧基正丙羰氧)懈皮素及裂解产物。
图19.鲜桑叶水提物粉末中的3-o-葡萄糖苷-2’-甲酰氧-3’-(3-羟基正丙羰氧)-4’-(3-羧基正丙羰氧)-5’-羧基正丙酰氧-6’-羟甲氧懈皮素及裂解产物。
图20.鲜桑叶水提物粉末中的3-o-葡萄糖苷-2’-甲氧基-3’-(6-羧基-1,3,5-正己三烯羰氧)-4’,5’-二(3-羧基-1-正丁烯羰氧)-6’-甲酰氧懈皮素及裂解产物。
图21.鲜桑叶水提物粉末中的3-o-葡萄糖苷-2’,3’,6’-三甲氧基-4’-羟甲基-5’-(6-羟基正己羰氧)懈皮素及裂解产物。
图22.鲜桑叶水提物粉末中的3-o-葡萄糖苷-2’-羟基-3’-(3-羧基-1-正丙烯羰氧)-4’-(3-羟基正丙羰氧)-5’,6’-二羟基正丙酰氧懈皮素及裂解产物。
图23.鲜桑叶水提物粉末中的3-o-葡萄糖苷-2’,3’-二甲氧基-4’-羟甲基-5’-(6-羟基正己羰氧)-6’-(3-羟基正丙羰氧)懈皮素及裂解产物。
图24.鲜桑叶水提物粉末中的3-o-葡萄糖苷-2’-甲酰氧-3’,4’-二羧基乙酰氧基-5’-(7-羧基-1,3,5-正庚三烯羰氧)-6’-(9-羧基-1,3,5-正壬三烯羰氧)懈皮素及裂解产物。
图25.鲜桑树叶水提物粉末浓度依赖地抑制氮自由基峰强度。
图26.鲜桑树叶水提物粉末浓度依赖地抑制羟自由基峰强度。
具体实施方式
为了进一步阐述本发明,下面给出一系列实施例。这些实施例完全是例证性的,它们仅用来对本发明进行具体描述,不应当理解为对本发明的限制。
实施例1制备鲜桑树叶水提物粉末
鲜桑树叶用自来水洗净,取100g洗净的鲜桑树叶在900ml蒸馏水中于60℃-90℃加热0.5-4小时,优选为70℃加热2小时,过滤,残饼用蒸馏水洗,合并的滤液减压浓缩,得到的7.3g粉末即为鲜桑树叶水提物粉末。
实施例2测定鲜桑树叶水提物粉末的色谱和质谱离子流谱
2-1.样品溶液的制备(10mg/ml)
称取26.7mg鲜桑树叶水提物粉末,用2.67ml超纯水中将粉末溶解。得到的溶液经超声震荡1分钟,之后再于13000r/min离心10分钟。取上清液,过0.22μm滤膜,置于样品瓶中供色谱和质谱测定用。
2-2.色谱条件
色谱条件
色谱柱:waters,acquity
进样体积:2μl;
流动相:水(0.1%甲酸),乙腈;
按照表1的梯度用流动相洗色谱柱。
表1流动相梯度表
2-3.测定色谱图
按照上面的色谱测定条件测定并记录鲜桑树叶水提物粉末的uplc色谱图(见图1)。
2-4.测定离子流谱和质谱的条件
电喷雾离子化模式为正(pi)及负(ni)模式。离子模式参数:毛细管电压为1000v,去溶剂气流速为800l/h,温度450℃,源温度为120℃,锥孔气流速为50l/h,喷雾气压为6bar,碎裂电压为20-45v,取样锥电压为6v,采集模式为msecontinuum分辨率模式,带电粒子的质量数与电荷数之比(m/z)数据采集范围为100-1500,低能量通道trap碎裂电压为6v,高能量通道trap碎裂电压选择梯度电压为20-60v,选取le(亮氨酸脑啡肽)为质量锁采集m/z,范围为100-1500。
实施例3指定鲜桑树叶水提物粉末中23种组分的结构
将实施例2的uplc色谱与质谱联接,测定鲜桑树叶水提物粉末的uplc-质谱。质谱条件是电喷雾离子化的正离子和负离子两种模式。离子模式参数:毛细管电压为1000v,去溶剂气流速为800l/h,温度450℃,源温度为120℃,锥孔气流速为50l/h,喷雾气压为6bar,碎裂电压为20-45v,取样锥电压为6v,采集模式为msecontinuum分辨率模式,带电粒子的质量数与电荷数之比(m/z)数据采集范围为100-1500,低能量通道trap碎裂电压为6v,高能量通道trap碎裂电压选择梯度电压为20-60v,选取le(亮氨酸脑啡肽)为质量锁采集m/z,范围为100-1500。在45分钟内分出23个独立峰。根据质谱裂解规律,这些峰(按照总离子流图谱从左到右的峰顺序)的指定见表2。这23种组分在质谱条件下的裂解产物见说明书附图2-24。
表2总离子流图谱中峰对应组分保留时间,负离子质量数,结构及名称
实施例4评价鲜桑树叶水提物粉末清除氮自由基的作用
为考察鲜桑树叶水提物粉末清除氮自由基的作用,本发明按照标准方法在顺磁共振仪上测定了在不同浓度下桑树叶水提物粉末的水溶液清除氮自由基,即清除1,1-二苯基-2-(2,4,6-三硝基苯基)肼自由基(1,1-diphenyl-2-picrylhydrazylradical,dpph)的活性。具体操作包括制备dpph的二氧六环溶液(0.8g/ml)和鲜桑树叶水提物粉末的超纯水溶液(0.31mg/ml,0.62mg/ml,1.25mg/ml,2.5mg/ml,5mg/ml及10mg/ml)。向0.5mlep管中加10μldpph的二氧六环溶液及10μl超纯水,涡旋混匀得待测样品。用毛细管吸取样品加入顺磁管中,封口胶封口,避光室温孵育10分钟,见光室温孵育10分钟,在顺磁共振仪上重复6次得鲜桑树叶水提物粉末的超纯水溶液浓度为零的氮自由基谱。向0.5mlep管中加10μldpph的二氧六环溶液及10μl鲜桑树叶水提物粉末的超纯水溶液(0.31mg/ml,0.62mg/ml,1.25mg/ml,2.5mg/ml,5mg/ml及10mg/ml),涡旋混匀得待测样品。用毛细管吸取样品加入顺磁管中,封口胶封口,避光室温孵育10分钟,见光室温孵育10分钟,在顺磁共振仪上重复6次得浓度为0.31mg/ml,0.62mg/ml,1.25mg/ml,2.5mg/ml,5mg/ml及10mg/ml的鲜桑树叶水提物粉末的超纯水溶液的氮自由基谱。图25的结果说明,鲜桑树叶水提物粉末的水溶液浓度依赖地降低氮自由基峰强度。鲜桑树叶水提物粉末具有优秀的氮自由基清除作用。
实施例5评价鲜桑树叶水提物粉末清除羟自由基的作用
为考察鲜桑树叶水提物粉末的羟自由基的清除作用,本发明按照标准方法在顺磁共振仪上测定了在不同浓度下鲜桑树叶水提物粉末的水溶液清除羟自由基的活性。具体操作包括将5μlfeso4·7h2o水溶液(2.78mg/ml),5μl5,5-二甲基-1-氧化吡咯啉
(5,5-dimethyl-1-pyridine-n-oxide,dmpo)水溶液(11.316mg/ml)及5μlh2o2水溶液(1%)在ep管中涡旋混匀。用毛细管吸取样品加入顺磁管中,封口胶封口,避光室温孵育10分钟,见光室温孵育10分钟,在顺磁共振仪上重复6次得鲜桑树叶水提物粉末的超纯水溶液浓度为零的羟自由基谱。将5μlfeso4·7h2o水溶液(2.78mg/ml),5μldmpo水溶液(11.316mg/ml),5μl鲜桑树叶水提物粉末的水溶液(0.16mg/ml,0.31mg/ml,0.62mg/ml,1.25mg/ml,2.5mg/ml及5mg/ml)及5μlh2o2水溶液(1%)在ep管中涡旋混匀。用毛细管吸取样品加入顺磁管中,封口胶封口,避光室温孵育10分钟,见光室温孵育10分钟,在顺磁共振仪上重复6次得浓度为0.16mg/ml,0.31mg/ml,0.62mg/ml,1.25mg/ml,2.5mg/ml及5mg/ml的鲜桑树叶水提物粉末的超纯水溶液的羟自由基谱。图26的结果说明,鲜桑树叶水提物粉末的超纯水溶液浓度依赖地降低羟自由基峰强度。鲜桑树叶水提物粉末具有优秀的羟自由基清除作用。
- 还没有人留言评论。精彩留言会获得点赞!