活性药物递送装置及其使用方法与流程
政府的权利
本发明专利获得了政府的支持,其中,美国国立卫生研究院的资助项目为r44ey028495。政府拥有本发明的某些权利。
相关专利申请的交叉引用
根据《美国法典》第35章第119节(e)项规定本专利申请案主张于2018年7月6日提交的编号为62/694,794的美国临时专利申请案以及于2018年8月29日提交的编号为62/724,535的美国临时专利申请案提交日期的优先权;这些专利中的内容以引用方式并入本文中。
介绍
对于在住院和非卧床护理环境中所行的许多常见手术而言,疼痛是主要的限制因素。此类手术的简短清单包括皮肤活检、细针抽吸活检、静脉插管、疫苗接种、注射(包括麻醉剂和气体注射)、抽血、中心导管置入以及手指和足跟采血以进行血液分析(血糖测定)。药物麻醉是一种主要的疼痛缓解方法,但局部麻醉药物的递送通常需要经历令人不快的注射过程。
眼球表面是可以向其递送治疗药物的组织表面。通过玻璃体内注射疗法(ivt)将药物直接递送至眼内的技能改变了以往发生的许多致盲性疾病(包括黄斑变性和糖尿病性视网膜病变)的治疗前景。这些疗法在预防失明方面取得的成功使得所进行的玻璃体内注射的数量急剧增加,仅2013年,美国便进行了约410万次玻璃体内注射。ivt的适应证数目持续增加,使得这种疗法的使用率每年都显著提高。ivt的主要局限性在于:患者感到不适、眼球表面出血、角膜毒性以及对需要接受这种疗法的大量患者进行治疗的时间限制。这些缺点与难以向高度血管化的眼球表面递送眼部麻醉药物相关。
为了进行眼部注射,医师首先采用多种方法中的一种或更多种来进行眼球表面麻醉,所述多种方法包括以下方法:局部施用麻醉剂滴剂;结膜下注射利多卡因;将浸泡在利多卡因中的棉签(通常称为“拭子”)放在计划的注射部位上;施用局部麻醉凝胶,或这些方法的一些组合。眼部麻醉后,医师或助手通过给眼周区域涂抹必妥碘或类似杀菌剂进行消毒灭菌。任选地,放置开睑器,而后医师使用对针头的放置进行导引的卡钳来标记注射位置。再次对眼球表面进行消毒灭菌,然后由医生进行注射。目前的局部麻醉方法具有独特的缺点,而且患者在眼内注射期间以及之后经常感到不适。
技术实现要素:
本发明提供了活性药物递送装置。所述装置的方面包括未经表面灭菌的注射器、包括无菌组织接触表面的头端以及与所述注射器和所述头端可操作地耦合的针头。本发明还提供了所述装置的使用方法。
简要附图说明
图1提供了根据本发明的实施例的手持式活性药物递送装置的视图。
图2提供了图1所示装置的远端的近摄图。
图3a和3b提供了根据本发明的实施例的头端的视图。
图4a和4b提供了根据本发明的实施例的载药注射器的视图。
图5提供了根据本发明的实施例的对接站的视图。
图6a至6i显示了根据本发明的实施例的活性药物施用方案。
图7a和7b提供了根据本发明的两个不同实施例的套件的视图。
定义
本文中使用的术语“组织”是指受试者(例如,生物体,例如哺乳动物,例如人)中具有相似功能和结构的一个或更多个细胞聚集体或多个不同类型的此类聚集体。组织可以包括,例如,器官组织、肌肉组织(例如,心肌;平滑肌;和/或骨骼肌)、结缔组织、眼结膜组织、神经组织和/或上皮组织。
在本发明中,术语“受试者”与术语“患者”可互换使用。在某些实施例中,受试者为“哺乳动物”,此术语被广泛地用于描述属于哺乳动物类的生物体,包括食肉动物(例如狗和猫)、啮齿类动物(例如小鼠、豚鼠和大鼠)以及灵长类动物(例如人、黑猩猩和猴子)。在一些实施例中,受试者是人类。术语“人类”可以包括任何发育阶段(例如,胎儿、新生儿、婴儿、少年、青少年、成人)的男性和女性受试者,其中在某些实施例中,所述人类受试者是少年、青少年或成人。虽然本文所述的装置和方法适于对人类受试者进行手术,但是应当理解,标的装置和方法还可以用于对其他受试者(即,“非人类受试者”)进行手术。
依照常规含义,术语“无菌”是指无活菌或其他微生物。“无菌区”是指手术室/诊所内只能使用无菌设备的区域,只有经过外科擦洗和更衣的人员才能进入该区域。
在一些情况下,所述装置或其部分可以被视为具有近端和远端。术语“近端的”是指在使用过程中朝向操作员的方向,或者是指在使用过程中(例如,在组织穿刺装置进入组织时)更靠近操作员(例如,远离受试者或其组织)的位置(例如,空间位置)。类似地,术语“远端的”是指在使用过程中朝向远离操作员的方向,或者是指在使用过程中(例如,在组织穿刺装置进入组织时)远离操作员(例如,更靠近受试者或其组织)的位置(例如,空间位置)。因此,短语“近端”是指装置在使用过程中最靠近操作员的一端,而短语“远端”是指装置在使用过程中与操作员相距最远的一端。
模块由一个或更多个功能块组成,这些功能块协同作业以执行特定功能——模块的目的。给定模块可以硬件、软件或其组合的形式实现。在一些情况下,模块可以包括电路元件,例如集成电路。集成电路(如有)可以包括多个不同的功能块,其中所述功能块全部存在于管腔内支架上的单个集成电路中。单个集成电路是指包括所有不同功能块的单个电路结构。因此,所述集成电路是单片集成电路(也称为ic、微电路、微芯片、硅片、计算机芯片或芯片),即,在半导体材料制薄基板表面上制造的微型电子电路(可以包括半导体器件和无源元件)。
此外,在本发明的一个或更多个(例如,一个、两个、三个或四个等)部分(例如,下文所述的“描述”、“装置”、“方法”和/或“套件”部分)中提供的定义和描述同样适用于其他部分所述的装置、方法和方面。
实施方式
本发明提供了活性药物递送装置。所述装置的方面包括未经表面灭菌的注射器、包括无菌组织接触表面的头端以及与所述注射器和所述头端可操作地耦合的针头。本发明还提供了所述装置的使用方法。
在更加详细地描述本发明之前,应当理解,本发明不限于所描述的特定实施例,因为在实际实施中一定会存在差异。还应当理解,本文中使用的术语仅用于描述特定实施例,而无意限制本发明构思,本发明的范围将仅由所附权利要求书限定。
在提供数值范围的情况下,应当理解,该范围的上限和下限之间的每个中间值以及在该范围内的任何其他规定值或中间值都包含在本发明的范围内。除非上下文另有明确规定,否则每个中间值应低至下限单位的十分之一。这些较小范围的上限和下限可独立地包括在较小范围内,并且也包括在本发明内,需遵守所述范围内任何特别排除的限值的要求。在所述范围包括一个或两个限值的条件下,排除了那些所包括限值中的任一个或两个的范围也包括在本发明内。
本文中提出的某些范围在数值前带有术语“大约”。本文中使用术语“大约”的目的是为其后的精确数字以及与该术语之后数字接近或近似的数字提供文字支持。在确定某一数字是否接近或近似于具体列举的数字时,接近或近似的未列举数字在其出现的上下文中可以是基本上等同于所具体列举数字的数字。
除非另有定义,否则本文所用的所有技术和科学术语的含义与本发明所属领域的普通技术人员通常理解的含义相同。尽管与本文所描述的方法和材料类似或等同的方法和材料也可用于本发明的实施或测试中,但下文描述了具有代表性的示例性方法和材料。
在本说明书中引用的所有出版物和专利通过引用方式并入本文中,犹如每一单独出版物或专利被具体地和单独地表明通过引用方式并入,且通过引用并入本文的目的是公开和描述与引用的出版物相关的方法和/或材料。任何出版物的引用均是针对其在申请日之前公开的内容,并且不应将其解释为承认由于之前的发明使得本发明无权早于此类出版物。此外,所提供的出版日期可能与实际出版日期不同,可能需要单独确认。
需要注意的是,如本文和所附权利要求书中所使用的,单数形式的“一”、“一个”和“所述/该”包括复数指代对象,除非上下文另有明确说明。还应注意,可以起草权利要求以排除任何可选要素。因此,该陈述旨在作为使用诸如“单独”、“仅”等与陈述权利要求要素有关的专用术语或使用“否定”限制的前置基础。
在阅读本发明后,以下内容对所属领域的技术人员来说是显而易见的,本文所描述和列出的每个单独的实施例都具有分层的组分和特征,这些组分和特征可在不脱离本发明的范围和精神的情况下与其他几个实施例中任一实施例的特征进行快速分解或合并。可按陈述的事件顺序或逻辑上可能的任何其他顺序实施任何陈述的方法。
尽管为了语法的流畅性已经或将要描述该设备和方法,并进行功能上的说明,但应明确理解,除非《美国法典》第35章有明确规定,否则任何情况下都不得将权利要求解释为必须受“方式”或“步骤”的限制,而应按照等效物的司法原则与权利要求中所述定义的含义和等效物的完整范围相符,当明确按照《美国法典》第35章第112节的规定编写权利要求时,权利要求应与《美国法典》第35章第112节中的法定等效物完全相符。
装置
如上所述,本发明提供了活性药物递送装置。由于所述装置是活性药物递送装置,因此其被配置成通过诸如受试者的目标递送部位将一定量(例如,剂量)的活性药物(例如,治疗药物)递送至靶组织。所述活性药物可以处于任何合适的状态,例如液态、固态或半固态(例如,凝胶)或气态,下文将对此作更为详细的探讨。在一些情况下,所述装置将液体活性药物组合物递送至靶组织。虽然通过所述装置递送至靶组织的液体活性药物组合物的剂量可能会有所不同,但是在一些情况下,所述剂量范围为5μl至100μl,例如10μl至50μl。在其他情况下,所述剂量可以更大,而且在一些实施例中,所述剂量范围为100μl至5000μl。
如上所述,所述装置的方面包括未经表面灭菌且包括所述活性药物的液体组合物的注射器;包括无菌组织接触表面的头端;以及与所述注射器和所述头端可操作地耦合的针头。现在将对这些组件中的每一项作更为详细的探讨。
依照常规含义,术语“注射器”是指用于注入流体的装置。在一些情况下,注射器包括主体,例如管状主体,例如,标刻度的圆柱形筒状物(其可由玻璃或塑料制成),其在第一端或近端具有柱塞,且在第二端或远端具有孔口,例如,可使所述活性药物组合物从所述注射器内部进入与所述容器的远端可操作地接合的针头内。所述注射器被配置成容纳所需量的活性药物组合物。虽然所述注射器的容积可能会有所不同,但是在一些情况下,所述容积范围为0.1至5.0ml,例如0.1至1.50ml,包括0.1至1.0ml,例如0.70至0.80ml。在一些情况下,所述注射器的容积足以容纳量超过在所述装置使用期间被递送至靶组织递送部位的量的活性药物组合物。虽然所述过量幅度可能会有所不同,但是在一些情况下,所述幅度范围为所述递送量的110%至500%,例如120%至150%。当所述活性药物组合物为非气态组合物时,所述储器(和所述活性药物递送系统的其他组件)中任何气体(例如空气)的量可能最少,其中在一些情况下,所述量为10μl或更少,例如5μl或更少、3μl或更少、2μl或更少或1μl或更少。如上所述,虽然通过所述装置递送至靶组织的液体活性药物组合物的剂量可能会有所不同,但是在一些情况下,所述剂量范围为5μl至100μl,例如10μl至50μl。在一些情况下,所述注射器可以包括剂量标记,例如,指示所递送的活性药物组合物剂量的光学可识别标识。所述剂量标记指示的剂量可能会有所不同,在一些情况下,所述剂量范围为10至100μl,例如50μl。在其他情况下,所述注射器可以不包括剂量标记,例如,在所述装置未被配置成手动操作且所述电机被配置成致动所述注射器以递送准确、所需的剂量的情况下。所述注射器可以由任何合适的材料制成,包括玻璃(例如1类)、塑料(这样,所述容器为聚合物容器,例如,环烯烃聚合物(cop)和环烯烃共聚物(coc))等。合适的材料包括但不限于以下已发布的出版物中所述的材料:第wo2013/178771、wo2015/173260、wo2017/087798和wo2017/085253号pct申请出版物;这些出版物中的内容以引用方式并入本文。
如上所述,在一些实施例中,所述注射器未经表面灭菌。由于这些实施例的注射器未经表面灭菌,因此所述注射器的外表面为非无菌表面。非无菌是指任何必须被视为非无菌或无法将其视为无菌的物质,例如,由于所述表面的相关处理过程所致,例如所述表面的处理/加工过程(例如,依据标准医疗程序确定)。在一些情况下,所述非无菌表面是指未经使其无活菌或其他微生物的处理的表面(例如,表面未经灭菌程序,例如热灭菌程序(例如蒸汽暴露)或化学灭菌程序(例如暴露于环氧乙烷气体、暴露于过氧化氢气体等离子体、过乙酸浸泡、臭氧暴露等))。在一些情况下,未经灭菌的表面上存在至少一种活菌或其他微生物。虽然所述注射器的外表面为非无菌表面,但是所述注射器的内部以及其中的内容物(例如液体活性药物组合物)是无菌的。在其他实施例中,所述注射器可以是表面已灭菌的注射器。
任何所需的活性药物组合物可存在于所述注射器的容器(即,储器)或药物容器中,包括容纳固体植入物的套筒,其中活性药物组合物可根据需要包括单一活性药物或两种或更多种不同活性药物的组合。活性药物是在疾病的诊断、治愈、缓解、治疗或预防中发挥药理活性或其他直接作用,或者影响人或动物身体的结构或任何功能的任何组分,并且可以是液体、凝胶或固体。可存在于给定活性药物组合物中的一种活性药物是治疗药物,其是可用于治疗、医治或治愈病症或疾病的药物。活性药剂可能会有所不同,其中活性药剂的示例包括但不限于小分子活性药物、多肽活性药物,例如,抗体及其结合片段、融合蛋白等、核酸活性药物、细胞活性药物等。可存在的治疗性活性药物的示例包括但不限于:类固醇,例如可的松、地塞米松、氟轻松、氯替泼诺、二氟泼尼酯、氟米龙、泼尼松龙、甲羟孕酮、去炎松、倍他米松、氟扎可特、氢化可的松、利美索龙及其衍生物;非甾体抗炎药,例如水杨酸、吲哚基乙酸、芳基乙酸、芳基丙酸和烯醇酸衍生物,包括溴芬酸、双氯芬酸、氟比洛芬、酮咯酸氨丁三醇和奈帕芬胺;抗生素,例如杆菌肽、贝西沙星、左氧氟沙星、莫西沙星、磺胺醋酰、妥布霉素、头孢唑啉、头孢拉啶、头孢克洛、头孢匹林、头孢唑肟、头孢哌酮、头孢替坦、头孢呋辛、头孢噻肟、头孢羟氨苄、头孢他啶、头孢氨苄、头孢噻吩、头孢羟唑、头孢西丁、头孢尼西、头孢拉尼、头孢拉尼、头孢曲松、头孢羟氨苄、头孢拉啶、头孢呋辛、环孢菌素、氨苄青霉素、阿莫西林、环青霉素、氨苄青霉素、青霉素g、青霉素v钾、哌拉西林、苯唑西林、巴氨西林、氯洒西林、替卡西林、阿洛西林、羧苄西林、甲氧西林、萘夫西林、红霉素、四环素、强力霉素、米诺环素、氨曲南、氯霉素、环丙沙星、克林霉素、甲硝哒唑、庆大霉素、林可霉素、妥布霉素、万古霉素、多黏菌素b硫酸盐、甲磺酸粘菌素、粘菌素、阿奇霉素、安灭菌、磺胺甲恶唑、甲氧苄氨嘧啶、加替沙星、氧氟沙星及其衍生物;血管内皮生长因子(vegf)调节剂,例如,vegf抑制剂或拮抗剂,例如酪氨酸激酶抑制剂、vegf特异性结合剂,例如,vegf抗体或其结合片段、vegf结合融合蛋白等;血小板衍化生长因子(pdgf)调节剂,例如,pdgf抑制剂或拮抗剂,例如pdgf特异性结合剂,例如pdgf抗体或其结合片段、pdgf结合融合蛋白等;血管生成素(ang)调节剂,例如ang2调节剂,例如,ang2抑制剂或拮抗剂,例如ang2特异性结合剂,例如ang2抗体或其结合片段、ang2结合融合蛋白等;ang2和vegf组合抑制剂;含有vegf抑制剂的抗体生物聚合物共轭物;含有苹果酸舒尼替尼的聚-丙交酯-共聚-乙交酯酸(plga)颗粒;胎盘生长因子(plgf)调节剂,例如,plgf抑制剂或拮抗剂,例如plgf特异性结合剂,例如,plgf抗体或其结合片段、plgf结合融合蛋白等;组织坏死因子(tnf)调节剂,例如,抗tnfα药物,例如针对tnf-α的抗体、针对tnf-α的抗体片段和tnf结合融合蛋白,包括英夫利昔单抗、依那西普、阿达木单抗、赛妥珠单抗和戈利木单抗;mtor抑制剂,例如西罗莫司、西罗莫司类似物、依维莫司、替西罗莫司和mtor激酶抑制剂;细胞,例如间充质细胞(例如,间充质干细胞),或被转染以产生治疗性化合物的细胞;神经保护剂,例如抗氧化剂、钙调神经蛋白抑制剂、nos抑制剂、σ-1调节剂、ampa拮抗剂、钙通道阻滞剂和组蛋白去乙酰酶抑制剂;抗高血压剂或眼内压降低剂,例如前列腺素类似物、rok抑制剂、β阻断剂、α激动剂和碳酸酐酶抑制剂;多特异性调节剂,例如,双特异性调节剂,例如双特异性结合剂,例如,双特异性抗体或其结合片段,包括与vegf和ang2特异性结合的药物;氨基甾醇,例如角鲨胺;抗组胺药,例如h1-受体拮抗剂和组胺h2-受体拮抗剂,例如,氯雷他定、羟嗪、苯海拉明、氯苯那敏、溴苯那敏、赛庚啶、特非那定、氯马斯汀、曲普利啶、卡比沙明、二苯拉林、苯茚胺、阿扎他定、曲吡那敏、右旋氯苯那敏、右旋溴苯那敏、甲地拉嗪和异丁嗪抗敏安、苯那敏、嘧啶胺、氯环嗪、松齐拉敏及其衍生物;酪氨酸激酶抑制剂,包括受体酪氨酸激酶抑制剂;基于核酸的治疗药物,例如基因载体,例如,质粒、rnai药物,例如,sirna、shrna;补体系统调节剂,例如,补体系统抑制剂,包括替代补体途径抑制剂(例如因子d、备解素、因子b、因子ba和因子bb)和经典补体途径抑制剂(例如c3a、c5、c5a、c5b、c6、c7、c8、c9和c5b-9);化疗药物,例如,阿霉素、环磷酰胺、放线菌素、博莱霉素、道诺霉素、多柔比星、表柔比星、丝裂霉素、甲氨蝶呤、氟尿嘧啶、卡铂、卡莫司汀(bcnu)、甲基-ccnu、顺铂、依托泊苷、干扰素、喜树碱及其衍生物、苯芥胆留醇、紫杉醇及其衍生物、泰索帝及其衍生物、长春碱、长春新碱、他莫昔芬、依托泊苷、哌泊舒凡、环磷酰胺和氟他胺及其衍生物;葡萄糖调节剂,例如胰岛素;免疫调节剂等。
活性药物以治疗有效量存在于活性药物组合物中。活性药物组合物中给定活性药物的量可能会有所不同,例如,这取决于特定活性药物、目标条件等,其中在一些情况下,给定活性药物量的范围为0.0005至10000mg/ml,例如10至500mg/ml,包括25至200mg/ml。
除所述活性药物外,给定活性药物组合物包括药学上可接受的递送载体,例如,药学上可接受的水性载体。对于药学上可接受的水性载体,除水之外,所述水性递送载体可以包括多种不同组分,包括但不限于:盐类、缓冲剂、防腐剂、溶解度增强剂、粘度调节剂、着色剂等。合适的水性载体包括无菌蒸馏水或纯净水、等渗溶液(例如等渗氯化钠或硼酸溶液)、磷酸盐缓冲生理盐水(pbs)、丙二醇和丁二醇。其他合适的载体成分包括硝酸苯汞、硫酸钠、亚硫酸钠、磷酸钠和磷酸一钠。其他合适的载体成分的其他示例包括醇类、脂肪和油类、聚合物、表面活性剂、脂肪酸、粘度调节剂、乳化剂和稳定剂、抗微生物剂、ph调节剂。给定活性药物组合物的粘度可能会有所不同。在一些情况下,所述粘度范围为0.005至5000厘泊,例如1至500厘泊,包括0.5至400厘泊。
根据本发明的实施例可以递送的活性药物组合物请参阅以下出版物:于2018年8月24日提交的申请序列号为62/722,447、标题为“粘性活性药物递送装置及其使用方法”的美国临时专利申请案;于2018年8月24日提交的申请序列号为62/722,454、标题为“固体活性药物制剂递送装置及其使用方法”的美国临时专利申请案以及于2018年8月24日提交的申请序列号为62/722,657、标题为“皮下给药装置及其使用方法”的美国临时专利申请案;这些专利申请案中的内容以引用方式并入本文。
给定注射器可以在其容器或储器中包括单一活性药物组合物或两种或更多种不同的活性药物组合物。所述两种或更多种活性药物组合物在活性药剂、递送载体、粘度等方面可以彼此有所不同。在给定注射器包括两种或更多种不同的活性药物组合物的情况下,所述不同的活性药物组合物可以通过屏障(例如易碎屏障)彼此隔开,使得每种不同的活性药物组合物存在于所述注射器的相应腔室内。在此类情况下,所述注射器可以具有两个或更多个腔室,例如,其中每个不同的活性药物组合物容器对应一个腔室。在递送过程中,可以破坏所述屏障以混合所述活性药物组合物。例如,在两个腔室因易碎屏障而彼此隔开的情况下,在活性药物组合物递送期间移动柱塞可以破坏所述易碎屏障,以便混合所述两种或更多种活性药物组合物。如有需要,可以采用屏障破坏机构,例如屏障穿刺机构等。
给定装置可以包括填充有一种或更多种活性药物组合物(例如,如上所述)的单支注射器,或者包括两支或更多支注射器(每支注射器填充有一种或更多种活性药物组合物),例如,包括两支注射器(每支注射器填充有不同的活性药物组合物)的装置。当装置包括两支或更多支注射器(每支注射器填充有不同的活性药物组合物)时,所述不同的活性药物组合物在活性药物、递送载体、粘度等方面可以彼此有所不同。在这些实施例中,所述装置可被配置成将所述不同注射器中含有的所述活性药物组合物作为单独的组合物递送至所述靶组织中,或者其可被配置成在递送至靶组织之前将所述不同注射器中的所述活性药物组合物混合。在实施例中,当所述装置被配置成将所述不同注射器中含有的所述活性药物组合物作为单独的组合物递送至所述靶组织中时,在活性药物组合物递送期间,每支注射器可与其自己的针头可操作地耦合。或者,每支注射器可与单个具有适用于每个注射器的内容物的不同内腔或通道的针头可操作地耦合,例如,具有中央分隔件的针头,所述中央分隔件定义了两条彼此流体隔离且与双注射器系统的一支注射器可操作地耦合的通道。在实施例中,当所述装置被配置成在递送至靶组织之前将所述不同注射器中的所述活性药物组合物混合时,所述注射器可以在递送期间与具有单条通道的单个针头可操作地耦合,使得所述不同注射器的内容物在通过所述针头时混合。如有需要,可以在所述装置中提供混合元件,例如在所述注射器与所述针头的交接处。
本发明的装置还包括具有无菌组织接触表面的头端。由于所述头端的组织接触表面是无菌的,因此至少在所述装置使用过程中接触组织的表面部分无活菌或其他微生物。在一些情况下,所述组织接触头端的尺寸使得所述组织接触头端被置于所述眼球表面时,针头进入发生在与所述角膜缘相距预定距离处(其中距离可以如上所述),其中此类构造可以消除在(玻璃体内、眼房内等)手术之前对安全注射距离进行手动测量的任何需求。因此,所述组织接触头端可被配置成防止与靶组织递送部位附近的组织结构接触,例如,眼晶状体或眼视网膜(所述靶组织递送部位为眼组织递送部位)。例如,所述组织接触头端可被配置成仅延伸一定的限制距离,所述距离超过所述组织递送组件主体的靶组织接触端。虽然所述限制距离可能会有所不同,但是在一些情况下,所述限制距离的范围为0.5至8mm,例如3至4mm。虽然所述组织接触表面可以具有任何合适的构造,但是在一些情况下,所述表面是平坦的。所述组织接触表面的形状可能会有所不同,其中某些实施例的形状包括圆形、椭圆形、三角形、矩形,包括正方形、六边形、八边形等。所述组织接触表面的面积也可能会有所不同,其中在一些情况下,所述面积范围为0.5至50mm2。
本发明的装置还包括与所述注射器和所述头端可操作地耦合的针头。所述针头被配置成通过诸如靶组织递送部位所述活性药物组合物从注射器输送至靶组织。所述针头可以具有任何合适的尺寸,并且在一些情况下,其规格范围为20号至35号,例如23号至35号、27号至35号、30号至33号,例如29、291/2、30、31、32、33和34号。根据需要,所述针头可以包括单个内腔或位于同一芯内的两个或更多个单独的内腔容器,例如,其中所述针头包括同一芯内含有的两个单独的内腔,且其规格范围为23至30号。所述针头可以由任何合适的材料制成,例如,不锈钢等。所述针头的近端可以是用于与所述注射器可操作地耦合的接头。可以存在任何合适的接头,其中可以存在接头,例如鲁尔接头,例如,鲁尔滑动件或鲁尔锁定接头。
如上所述,所述针头与所述注射器和所述头端可操作地耦合。所述针头的近端可与所述注射器的远端可操作地接合,使得所述注射器内部的液体组合物通过所述注射器的远端开口并进入所述针头内部(即,孔)。所述针头的近端可以利用任何合适的构造与所述注射器的远端可操作地接合。合适构造的示例包括但不限于压配合构造、鲁尔接头构造,例如,鲁尔滑动件或鲁尔锁等。
除了与所述注射器可操作地耦合之外,所述针头还可以与包括所述无菌组织接触表面的头端可操作地耦合。在一些情况下,所述头端是具有近端和远端的结构,其近端通过诸如合适接头等附接于所述针头,而其远端延伸至超过所述针头的远端一定距离,例如,所述距离的范围为2至20mm,其中所述远端包括所述无菌组织接触表面。所述头端可由单个组件或两个或更多个彼此可操作地连接的组件组成。例如,头端可以包括第一近端组件和第二远端组件,其中所述远端组件包括所述无菌组织接触表面,而所述近端组件包括用于与所述针头可操作地耦合的接头。所述近端组件可以进一步容纳所述针头或其部分,使得所述近端组件可被视为是针罩。所述近端组件和远端组件可被配置成在使用期间相对于彼此移动。所述两个组件相对于彼此移动的距离可能会有所不同,其中在一些情况下,所述距离的范围为1至20mm,例如2至10mm。在一些情况下,锁定机构在致动之前相对于所述组织接触头端的远端固定所述针头的远端。当所述组织接触头端相对于所述针头运动时(例如所述组织接触头端围绕所述针头的中心纵向旋转运动),所述锁定机构是是可释放的。例如,可以相对于所述相关针头转动组织接触头端,例如转动四分之一圈,这可以移除锁定且可以相对于所述组织接触头端的远端移动所述针头。所述头端的远端(即,组织接触端)可以包括开口,所述开口的尺寸适合让所述针头的远端在活性药物递送期间穿过所述接触头端,从而使所述针头与靶组织直接接触。在致动时,所述针头的远端相对于所述组织接触头端的远端移动。在致动和活性药物递送期间,所述针头的远端延伸至超过所述组织接触头端的远端及其无菌表面的距离可能会有所不同,并且在一些情况下,所述距离的范围为0.1至5mm,例如0.5至4.0mm。虽然所述开口(如有)的尺寸可能会有所不同,但是在一些情况下,所述开口的直径适于具有一定规格(例如,如上所述)的针头穿过。在一些情况下,所述组织接触头端的远端可由导热材料制成,例如,金属或其合金,例如,在所述组织接触头端的远端与所述致动器组件冷却系统的冷却元件的远端可操作地接合的情况下,例如,详见下文。还可以采用其他合适的材料,例如聚合材料。给定头端可被配置成与单个针头,或者两个或更多个针头可操作地耦合。例如,给定头端可被配置成与两个针头可操作地耦合,例如,在装置包括两支注射器(例如,如上所述)的情况下。
在一些情况下,所述组织接触头端可以包括一个或更多个过滤器。所述过滤器可被配置成在递送到靶组织递送部位之前,去除所述活性药物组合物中存在的颗粒或其他不需要的组分。此类过滤器可被配置成抑制粒径大于一定孔径(孔径范围为>0.1μm至>50μm,例如>5m)的颗粒通过。所述一个或更多个过滤器可以位于所述治疗药物递送系统内任何合适的位置,例如,位于从所述容器进入所述注射器的出口处、位于沿所述注射器的某一点、位于所述注射器的远端等。
如有需要,所述远端(即,组织接触表面)可以包括活动盖,例如,在所述装置用于将治疗药物递送至目标递送部位之前一直存在的活动盖。所述盖可被配置成释放衬垫或类似结构,使其可在使用前被轻易移除。根据需要,所述盖可以是无菌的或经过消毒的,并且由任何合适的材料制成,例如塑料等。所述盖还可以采用无菌剥离型包装、无菌盒等形式。
如有需要,所述装置可以包括抗微生物元件。所述抗微生物元件可以是任何合适的具有抗微生物特性的元件,并且可以位于所述治疗药物递送系统内的一个或更多个位置。例如,所述抗微生物元件可以位于所述主体的远端(即,组织接触端),以便至少在所述装置与所述靶组织递送部位接触期间提供无菌条件;对所述靶组织递送部位进行消毒等。所述抗微生物元件可以包括抗微生物剂,其可以存在于支承物中,例如基质材料、储器等。如同所述治疗药物一般,所述抗微生物剂(如有)可以各种不同的物理形态(包括液态、固态、半固态和气态)存在于组合物中。目的抗微生物剂包括但不限于:聚维酮碘化物(必妥碘)、氯己定(诺尔瓦森)、乙醇、二氧化氯及其衍生物、其他醇类等。
如有需要,所述活性药物递送系统可以包括镇痛剂/麻醉剂。所述镇痛剂/麻醉剂(如有)可以任何合适的方式存在,所述存在方式适于在所述装置使用期间将所述镇痛剂/麻醉剂递送至所述靶组织递送部位。例如,所述镇痛剂/麻醉剂可以位于所述头端的远端(即,组织接触端),以便至少在所述装置与所述靶组织递送部位接触期间提供无菌条件。所述镇痛剂/麻醉剂可以存在于支承物中,例如基质材料、储器等。如同所述治疗药物一般,所述镇痛剂/麻醉剂(如有)可以各种不同的物理形态(包括液态、固态、半固态和气态)存在于组合物中。目的镇痛剂/麻醉剂包括但不限于:利多卡因、苯佐卡因、丙胺卡因、利多卡因、杜比卡因、甲哌卡因、布比卡因等;天然衍生品,例如蛤蚌毒素、新蛤蚌毒素、河豚毒素、薄荷醇、丁香酚和可卡因等。
本发明的活性药物递送装置可被配置成用于将活性药物递送至各种靶组织和/或其递送部位。靶组织的示例包括外部和内部部位,其中内部递送部位包括位于体腔内的部位。外部部位可以包括角质化部位,以及以皮肤膜、粘膜和皮肤粘膜区组织为特征的部位。在一些情况下,所述靶组织是通过眼组织递送部位接触的组织,其中目的眼组织递送部位包括从角膜缘开始,一直延伸至任何距离所述角膜缘后部1mm至10mm、所述角膜缘后部2mm至8mm以上的位置(例如距离所述角膜缘3mm至6mm、距离所述角膜缘3mm至4mm)的区域,例如,以便经由平坦部或皱摺部进行眼内注射。眼组织递送部位可以包括所述眼睛的角膜、结膜、巩膜外层和巩膜。目的眼组织递送部位包括接受玻璃体内注射疗法(ivt)、眼球后注射疗法、筋膜下注射疗法、视网膜下注射疗法、脉络膜上腔注射疗法、结膜下注射疗法、眼房内注射疗法等的部位。
在一些情况下,给定活性药物递送装置仅包括注射器以及与所述组织接触头端可操作地耦合的针头,例如,如上所述。例如,所述装置可被配置成手动致动,使得使用者(例如保健医生)可以将所述头端的无菌组织接触表面置于目标位置(例如眼睛表面的位置),相对于所述远端头端移动针罩,使所述针头穿过眼睛表面进入眼内,然后压下所述注射器的柱塞,以便将所述注射器内一定剂量的活性药物组合物经由所述针头移至眼内。
在其他情况下,所述装置可以包括致动器,所述致动器被配置成在使用期间移动所述注射器的柱塞。在这些情况下,所述注射器和所述组织接触头端(统称为活性药物递送系统)可被配置成可操作地,并且在一些情况下可释放地接合于所述装置的致动器组件的接收空间内。在这些情况下,所述活性药物递送系统可以包括锁定元件的组件,可用于将所述活性药物递送系统可释放地接合于所述装置的致动器组件的接收空间内。可以采用任何合适的锁定机构,例如但不限于:压配合件、可移动闩锁等。存在于所述活性药物递送组件上的锁定元件的锁定元件组件可能会根据需要而有所不同,并且基于存在于所述致动器上的配对元件加以选择。
因此,活性药物递送装置的实施例包括活性药物递送系统和致动器组件,其中所述活性药物递送系统存在于所述致动器组件的接收空间内(例如注射器接收空间),并且所述致动器组件包括活性药物递送系统致动器。在一些情况下,所述活性药物递送系统可释放地接合于所述致动器组件的接收空间内。因此,在此类情况下,所述活性药物递送系统被配置成易于与所述致动器组件的接收空间分离,且不会以任何方式损害所述致动器组件的功能,以便在所述致动器组件的接收空间内安置另一活性药物递送系统。因此,本发明的装置被配置成使得所述致动器组件可以依次用于多个不同的活性药物递送系统。受关注的是如下构造,即,所述活性药物递送系统可以手动可操作地安置于所述致动器组件单元的接收空间内,且无需使用任何工具。在一些情况下,所述装置进一步包括锁定元件,其可用于将所述活性药物递送系统可释放地接合于所述装置的致动器组件的接收空间内。可以采用任何合适的锁定机构,例如但不限于:压配合件、可移动闩锁等。
在给定装置包括活性药物递送系统和致动器组件的情况下,所述活性药物递送系统可以进一步包括一种或更多种标识。此类标识(如有)可以存在于所述活性药物递送系统的一个或更多个组件上,例如注射器、头端等。在一些情况下,存在于所述活性药物递送系统上的标识是被配置成由所述装置致动器组件的标识读取器读取的标识,例如,如下所述。虽然此类读取器兼容的标识可能会有所不同,但是在一些情况下,所述标识是条形码,例如线性条形码或矩阵条形码,例如二维码。在一些情况下,所述读取器兼容的标识是射频识别(rfid)标签,例如近场通信(nfc)标签,其中rfid标签可以是无源的或有源的。所述标识中包括的信息可以包括但不限于所述治疗药物的名称(品牌名和/或通用名)、生产日期、有效期至、生产来源、剂量、药物浓度、预期给药途径、处理和储存信息、递送量、适用证、批号等。
除了读取器兼容的标识之外,所述治疗药物递送系统可以包括被配置成由保健医生读取的视觉标识。视觉标识是指人在看到所述标识时可以轻易理解、无需对其进行计算机处理的标识。此类标识的示例包括但不限于文字标识、颜色编码标识、通常理解的符号、识别性商标、徽标等。由所述视觉标识传达的信息可能会根据需要而有所不同,其中由所述视觉标识传达的信息的示例包括但不限于:有关所述活性药物递送系统或其中存在的活性药物的信息,例如所述治疗药物的名称(品牌名和/或通用名)、生产日期、有效期至、生产来源、剂量、药物浓度、预期给药途径、处理和储存信息、递送量、适用证、批号等。
如上所述,所述致动器组件被配置成与活性药物递送系统(例如,如上所述)可操作地接合,以形成本发明的活性药物递送装置。根据本发明的实施例的致动器组件的方面包括具有近端和远端的主体、活性药物递送系统接收空间,所述接收空间被配置成与活性药物递送系统(例如,如上所述)可操作地,并且在一些情况下可释放地接合。所述致动器组件的其他方面包括被配置成致动活性药物递送系统的活性药物递送系统致动器。所述致动器可以进一步包括被配置成缓解靶组织递送部位疼痛的疼痛缓解系统的一个或更多个组件,并且在一些情况下,所述致动器可以包括疼痛缓解系统的全部组件。
所述致动器是被配置成致动所述活性药物递送系统以便将活性药物递送至靶组织递送部位的元件或子系统。所述活性药物递送系统致动器的性质可能会有所不同,例如,这取决于所述活性药物递送系统的性质。例如,所述活性药物递送系统致动器可被配置成控制所述针头的角位置、线性位置、速度和加速度中的一项或更多项。在一些情况下,单独使用或与所述活性药物递送系统的导引元件结合使用的所述致动器被配置成使所述针头与所述活性药物递送系统的远端(即,组织接触端)成一定角度,所述角度范围为0°至90°,例如75°至90°。在一些实施例中,所述活性药物递送系统以预定角度存在于所述装置中,例如,当所述冷头端适用于生物组织时,相对于所述生物组织成90度,以便在所述装置头端置于眼睛上(邻接角膜缘的位置,且使得所述头端周围的眼球表面全部(360度)出现极轻微的凹陷)时,所述针头头端可重复地以确定的、安全的角度插入眼中(即,眼睛角膜缘后部),以免出现碰触视网膜、小带或晶状体的危险。在一些情况下,所述致动器可以一定速度将所述注射器引入靶组织递送部位,所述速度范围为0.1至100mm/s,例如1至10mm/s,包括3.5至9mm/s。所述活性药物递送系统致动器可被配置成控制所述注射器中活性药物组合物的释放。所述致动器可被配置成以受控方式从所述靶组织递送部位取出所述针头。在一些这样的情况下,所述致动器可被配置成以一定速度从靶组织递送部位抽出所述针头,所述速度范围为0.1至100mm/s,例如1至10mm/s,包括3.5至9mm/s。在一些情况下,所述致动器被配置成灌注所述组织注射器,例如,在所述活性药物递送系统包括一定量的气体,例如空气(例如以气泡的形式)的情况下,所述致动器可移除所述系统中的气体,例如,使所述气体经由所述针头从所述系统中排出。在一些情况下,所述致动器被配置成在第一灌注运动和第二注射运动中依次移动所述药物容器。在一些情况下,所述致动器进一步被配置成在注射所述活性药物组合物之后将所述针头收回所述装置中。
所述致动器可能会根据需要而有所不同。可以在本发明的实施例中使用且存在于所述致动器组件中的致动器的示例包括但不限于:电动致动器(包括那些包括诸如步进电机、dc电机、有刷电机或无刷电机等微型电机的致动器),以及非电动致动器,例如,气动致动器、液压动力致动器、弹簧加压致动器、手动操作致动器,例如包含致动器的柱塞等。根据需要,所述致动器的功能可以由一个或更多个模块控制。所述致动器可被配置成改变药物注射的速度和深度。
除了致动器之外,所述致动器组件可以包括疼痛缓解系统的一个或更多个组件,包括全部组件。所述致动器可以缓解疼痛,这使得所述致动器被配置成缓解与通过所述装置将活性药物递送至靶组织递送部位相关联的疼痛。虽然疼痛缓解的幅度可能会有所不同,但是在一些情况下,与合适的对照(例如,无疼痛缓解的相同递送)相比,所述疼痛缓解的幅度为5%或更多,例如10%或更多,包括20%或更多。如上所述,疼痛缓解系统是在向目标递送部位递送活性药物期间缓解疼痛的系统。所述疼痛缓解系统可能会根据需要而有所不同,其中在本发明的装置中使用的疼痛缓解系统包括麻醉产生系统(即,例如,通过阻断所述靶组织递送部位中的所有感觉,使得所述靶组织递送部位至少出现一定程度的(若非完全的)感觉丧失的系统)和镇痛产生系统(即,使得所述靶组织递送部位的疼痛有所减轻且感觉未完全丧失的系统)。
在一些情况下,麻醉产生系统是冷却系统,即,使所述靶组织递送部位的温度降低一定量以便在所述靶组织递送部位产生所需麻醉作用的系统。所述冷却系统可能会有所不同,并且在一些情况下,所述冷却系统是使冷元件(例如,冷头端或冷组织接合件(例如组织接触头端,例如,详见下文))与所述靶组织递送部位接触的系统。所述冷却系统的冷元件(其可以是组织接合件的组件,例如,详见下文)可能会有所不同,并且在一些情况下,所述冷元件被配置成在与所述靶组织递送部位接触时,使温度维持在-80℃至+5℃之间,例如-20℃至0℃、-20℃至-5℃,包括-15℃至-5℃。在实施给定递送方法期间,根据需要,组织接合件可以保持恒定温度或者在一个或更多个不同的温度范围内循环。例如,组织接合件可被配置成具有落入第一范围(例如,如上所述)内的温度,以在治疗药物递送期间发挥所需的冷冻麻醉作用,然后在移除所述装置之前循环至第二更暖温度,例如温度范围为0至-5℃,例如0至-2.5℃,包括0至-1℃。在另一实施例中,所述冷却可以是无源的,所述温度基于诸如所述装置未附接至所述冷却基站的时间量、所述装置头端抵靠生物组织放置的时间量以及所述生物组织的温度等因素而升高。在所述靶组织递送部位是眼组织递送部位(例如,如别处所述)的情况下,进行冷却以引起快速血管收缩能够减少眼球表面出血的发生,并且可以防止出现重复血管损伤和长期循环损害。
可用于麻醉产生疼痛缓解系统的目的特定冷却系统可能会有所不同,其中目的冷却系统包括但不限于:热电冷却系统、液体蒸发冷却系统、固体升华冷却系统、焦耳-汤姆逊冷却系统、热力循环冷却系统、吸热反应冷却系统、低温物质冷却系统等。
在一些情况下,所述疼痛缓解麻醉产生系统是热电冷却系统,例如,包括热电(珀耳帖)装置或单元中的一项或组合的系统。虽然在本发明的装置的实施例中采用的热电冷却系统可能会有所不同,但是在一些情况下,所述热电冷却系统包括被配置成与靶组织递送部位接触的冷头端(因此也被称为组织接合件);以及电源、控制器、冷却能集中器、一个或更多个珀耳帖单元模块和散热器(其可以是固体材料或者在容器中包括一种流体相,例如液相)中的一项或更多项。应当理解,在一些实施例中,给定热电冷却系统可以包括加热元件(未示出),所述加热元件与冷却元件一起运作,以精确地保持所述的温度和/或热通量。有关在本发明的装置中使用的热电冷却系统的实施例的更多详情请参阅第9,956,355号美国专利;该专利中的内容以引用方式并入本文。
在其他情况下,所述冷却系统可以包括熔化温度为0℃或更低的物质,例如相变材料,例如plusicee-11或e-15相变材料(pcmproductsltd.)。如上所述,可以采用其他非热电冷却疼痛缓解系统,例如但不限于:液体蒸发冷却系统、固体升华冷却系统、焦耳-汤姆逊冷却系统、热力循环冷却系统、吸热反应冷却系统和低温物质冷却系统。
除冷却系统之外,其他类型的麻醉产生系统可以用作疼痛缓解系统。此类麻醉系统包括但不限于:递送麻醉剂的系统,例如但不限于:钠通道阻滞剂,例如,氨基酰胺或氨基酯(例如丙美卡因、丁卡因或利多卡因滴剂、凝胶或乳膏);天然衍生品,例如蛤蚌毒素、新蛤蚌毒素、河豚毒素、薄荷醇、丁香酚和可卡因;等等。
同样受人关注的疼痛缓解系统是镇痛产生系统,例如,如上所述。在本发明的装置的实施例中使用的镇痛产生系统的示例包括施用上述被视为是局部麻醉剂的药物。其还可以包括但不限于其他技术,例如电刺激(campbell和taub,神经病学档案,1973;28(5):347-350)等。
如上所述,在一些情况下,所述致动器组件可以包括锁定元件的组件,其可用于将所述活性药物递送系统可释放地接合于所述装置的致动器组件的接收空间内。如上所述,可以采用任何合适的锁定机构,例如但不限于:压配合件或卡扣等。存在于所述致动器组件上的锁定元件的锁定元件组件可能会根据需要而有所不同,并且基于存在于所述致动器上的配对元件加以选择。
在一些情况下,所述致动器组件包括用于读取与所述致动器组件可释放地接合的活性药物递送系统的标识的标识读取器。所述标识读取器可能会根据需要而有所不同,这取决于与所述治疗药物递送组件相关联的标识的性质。例如,在标识是条形码的情况下,所述致动器的标识读取器可以是任何合适的条形码或二维码扫描仪。同样地,在标识是射频标识的情况下,所述致动器的标识读取器可以是任何合适的rfid或nfc读取器。所述标识读取器(如有)在所述致动器上的位置使得其能够读取治疗药物递送组件(在与所述致动器可释放地接合时)的标识。
如果所述致动器组件包括标识读取器,则在一些情况下,所述致动器被配置成仅当所述标识读取器检测到可接受的标识时才处于激活状态。可接受的标识可以是传达一种或更多种据此判断可接受性的信息的标识,例如但不限于:活性药物递送系统是否填充正确的活性药物;活性药物递送组分是否已过期;活性药物递送组分是否由可接受的、可信赖的制造商制造;活性药物递送组分之前是否被登记为丢失等。在此类情况下,在可接受标识由所述标识读取器读取时,所述读取器可与仅启用一个或更多个致动器组件(例如治疗药物递送系统致动器、疼痛缓解系统等)的致动器控制元件耦合。因此,在不可接受的标识由所述读取器读取时,所述读取器可以向所述控制器发送禁用一个或更多个致动器组件的信号。或者,在不可接受的标识由所述读取器读取时,所述读取器可以向所述控制器发送不得启用一个或更多个致动器组件的信号。
本发明的致动器组件可以进一步包括通信模块,所述模块与所述致动器的一个或更多个组件可操作地耦合,且可由此向另一组件(例如,外部设备等)进行数据传输。所述通信模块可被配置成根据需要以有线或无线模式进行数据传输。例如,所述通信模块可被配置成在使用时利用诸如联网设备以无线方式传输数据,然后在对接站对接时使用有线配置来传输数据,例如,如下所述。所述致动器的通信模块可以,例如,通过硬件和/或软件实现被配置成执行所需的通信功能,例如,接收来自致动器元件的数据;传输数据,例如,传输至用于有线通信的usb端口或用于无线通信的无线发射器等。所述通信模块(以及本文所述的任何其他模块,例如致动器控制器模块等)由一个或更多个功能块组成,这些功能块协同作业以执行特定功能——所述模块的目的。给定通信模块可以硬件、软件或其组合的形式实现。在一些情况下,所述通信模块可以包括电路元件,例如集成电路。集成电路(如有)可以包括多个不同的功能块,即,模块,其中所述功能块全部存在于管腔内支架上的单个集成电路中。单个集成电路是指包括所有不同功能块的单个电路结构。因此,所述集成电路是单片集成电路(也称为ic、微电路、微芯片、硅片、计算机芯片或芯片),即,在半导体材料制薄基板表面上制造的微型电子电路(可以包括半导体器件和无源元件)。
如有需要,致动器组件可以包括以某种方式向所述致动器组件提供工作功率的各种不同类型的电源。所述电源的性质可能会有所不同,并且可以包括也可以不包括电源管理电路。在一些情况下,所述电源可以包括蓄电池。所述蓄电池(如有)可以是一次性蓄电池或可充电蓄电池。对于可充电蓄电池,可以使用任何合适的方案对所述蓄电池进行充电。在一些应用中,所述致动器的蓄电池使用寿命范围为0.1至100小时,例如0.5至10小时或1小时至5小时。
在某些情况下,本发明的致动器包括可更新的控制模块,这意味着所述致动器被配置成可更新所述致动器的一种或更多种控制算法。更新可以通过任何合适的方案来实现,例如,通过有线连接(例如,经由所述装置上的usb端口)或无线通信协议将已更新的算法数据传输至所述控制模块。所述更新内容可能会有所不同。在一些情况下,更新致动器组件,以将所述单元配置成与特定治疗药物递送组件结合使用。在这种情况下,相同的致动器组件可与两个或更多个不同的治疗药物递送组件结合使用,所述递送组件可以在一个或更多个方面彼此有所不同,例如,治疗药物的标识、治疗药物递送组件的制造商等。所述更新信息还可以包括一般功能更新,使得所述致动器组件可以在任何所需时间内进行更新,以包括一种或更多种附加软件功能和/或修改所述装置的一个或更多个现有程序。所述更新信息可以通过任何来源提供,例如,特定的细长构件、互联网等。
所述致动器组件可以包括一个或更多个安全机构,例如,包括如上所述的标识/读取器兼容性机构。在一些实施例中,所述治疗药物递送系统致动器仅在注射过程中持续按下开关的情况下提供致动。在一些实施例中,设有停止注射的安全机制。
在一些情况下,所述致动器组件可以包括显示器。显示器是指视觉显示单元,其可以包括以图像、亮色和/或文本形式向使用者展示视觉数据的屏幕。所述屏幕可能会有所不同,其中目的屏幕类型是lcd屏幕。所述显示器(如有)可与所述致动器组件集成。因此,所述显示器可以是具有所述致动器组件的集成结构,这使得其无法在不以某种方式损坏显示屏的情况下与所述致动器组件分离。所述显示器(如有)的尺寸足以与所述致动器结合使用,其中目的屏幕尺寸可以包括100cm2或更小,例如20cm2或更小等。所述显示器可被配置成向使用者展示各种不同类型的信息,其中此类信息可以包括装置设置,包括头端温度、冷却应用时间、治疗药物标识和治疗药物到期日期等。在一些情况下,所述致动器组件可以包括基于led的灯光系统,以告知使用者所述装置的状态,包括冷却参数、注射器位置、注射状态和蓄电池指示器。
整个活性药物递送装置可被配置成适于单次使用,使得整个活性药物递送装置为一次性用品。或者,所述活性药物递送装置的一个或更多个组件可重复使用。例如,所述致动器组件可重复使用,而所述活性药物递送系统及其组件(例如,注射器、针头、组织接触头端等)只能使用一次。
本发明的各种装置组件可以使用任何合适的材料或其组合来制造,包括但不限于:金属材料,例如钨、铜、不锈钢合金、铂或其合金、钛或其合金、钼或其合金、镍或其合金等;聚合材料,例如聚四氟乙烯、聚酰亚胺、peek等;陶瓷,例如氧化铝(例如,steatitetm氧化铝、maecortm氧化铝)等。所述药物储器可以由塑料制成,例如聚丙烯或聚苯乙烯,或者由通常用于注射器等的任何材料制成。其也可以由玻璃制成,包括通常用于长期储存药物和生物制品的1类玻璃。或者,其可以由用于长期储存药物或生物制品的不可浸出的塑料材料制成,例如环烯烃共聚物(crystalzenith)等。
本文所述的活性药物递送装置可以是手持式装置。在此类实施例中,由于所述装置是手持式装置,因此其被配置成方便成人握在手中。因此,所述装置可以具有适合成人手抓握的构造。所述装置的重量可能会有所不同,并且在一些情况下,所述重量范围为0.05至3,例如0.1磅至1磅。本发明的手持式装置可以具有任何合适的构造,其中合适的手柄构造的示例详见下文。
具体实施例
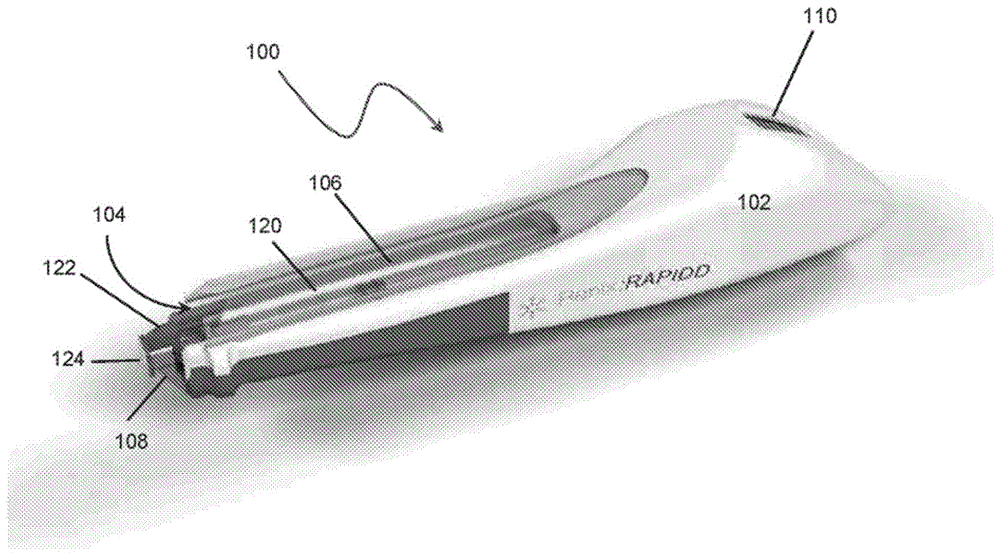
图1提供了根据本发明的实施例的手持式治疗药物递送装置的视图。如图1所示,装置100包括致动器组件102(其包括活性药物递送系统接收空间104)和适用于接收空间106的透明盖。还示出了致动器组件102的疼痛缓解系统的冷却头端108。致动器组件102还包括led110。接收空间104中存在活性药物递送系统120,其包括具有无菌、平坦组织接触表面124的头端122。
图2提供了图1所示装置100的远端的近摄图。如图2所示,致动器100的远端包括与致动器100的疼痛缓解系统的冷却臂108可操作地接合的头端122。头端122的组织接触表面124是无菌的,而冷却臂108是非无菌的。
图3a提供了头端组件130的近摄图,所述头端组件包括与针头可操作地耦合的头端122。如图3a所示,头端组件130由两个不同的组件组成,即,远端组件131和近端组件132。远端组件131包括无菌组织接触表面124,可以被称为组织接触组件。近端组件132容纳所述针头,也可以被称为针罩。如图所示,针罩132与远端组件130成滑动关系,这通过远端组件132的导轨136实现。所述距离x可能会有所不同,并且在一些实施例中,所述距离范围为1至20mm,例如2至10mm。还示出了存在于所述针罩中的针头的鲁尔接头134,其中鲁尔接头134被配置成与注射器可操作地接合。在使用过程中,针罩132和远端组件131一同移动,使得所述距离x减小至5mm或更小,例如2mm或更小,其中在一些情况下,x变为0mm,且所述针头的远端延伸至穿过无菌组织接触表面124的通道。如有需要,在使用前,头端组件122可以安置在密封外壳中,如图3b所示。如图3b所示,头端组件130存在于由容器142和盖帽144组成的头端组件外罩140中。容器142和盖帽144可以通过任何合适的方法装配在一起,例如卡扣配合、螺纹配合等,且可以提供用于容纳所述头端的无菌外罩。
图4a提供了装置100的注射器的视图。如图4a所示,注射器150由透明材料制成,例如,玻璃或塑料,并且其近端包括柱塞152,而远端154被配置成与图3a所示的头端122的近端组件132可操作地耦合。外表面156是非无菌的,而含有活性药物组合物的内部158是无菌的。在使用之前,注射器150的远端可以用盖帽160密封,例如,以保持所述注射器内部的无菌性,例如,如图4b所示。
对接站和包括对接站的系统
本发明的方面包括被配置成对接致动器组件的对接站,以及包括对接站和致动器组件的系统。对接站是被配置成与致动器组件接合的基础单元或类似器件,例如,如上所述。与致动器组件接合时,所述对接站可以执行一项或更多项功能,所述功能可以包括但不限于:使疼痛缓解系统保持在所需状态(例如,将冷却系统保持在所需温度);在所述致动器组件与外部设备之间传输数据;对致动器组件的远端进行消毒;对致动器组件的电源进行充电;与计算机、服务器或数据库等进行通信。所述对接站可以包括单个致动器组件对接点(即,被配置成以接合方式接收致动器的场所或位置),或者两个或更多个致动器组件对接点,使得在一些情况下,对接站中的致动器对接点的数量范围为1至6个,例如2至4个。本发明的对接站可以具有任何合适的配置。对接站可以根据需要被配置成桌面装置、壁挂式装置、落地式装置等。所述组件对接点可被配置成仅容纳冷却能集中器,当另一冷却能集中器不再处于所需温度时,所述集中器可以与所述装置可操作地耦合。所述对接站可以具有多个端口来同时对多个器件进行充电,并且可被配置成冷却利用相同冷却机制或不同冷却机制的不同器件。在一实施例中,所述基站可以冷却独立冷却单元,所述冷却单元可以夹在所述装置中。
为了提供不同的所需功能,所述对接站可以包括多个不同的子系统或组件。例如,对接站可以包括冷却系统,例如,其被配置成使所对接的致动器和/或治疗药物递送组件的温度保持在所需范围内。合适的冷却系统的示例包括但不限于上述冷却系统。所述对接站可以包括通信模块,例如,用于调节在所对接的致动器和/或治疗药物递送组件与所述对接站的模块和/或外部设备之间进行的数据传输。所述对接站可以包括电源模块,例如,用于对所对接的致动器的电源进行充电。所述对接站可以包括检测器,例如,用于检测所对接的致动器和/或治疗药物递送组件。所述对接站可以包括标识读取器,例如,用于读取所对接的致动器和/或治疗药物递送组件上的标识,例如,如上所述的标识读取器。如有需要,所述对接站可以包括诸如如上所述的标识。
除了对接站(例如,如上所述)之外,本发明的方面进一步包括对接系统。对接系统包括具有与其对接的一个或更多个致动器组件的对接站。
图5提供了根据本发明的实施例的对接站的视图。如图5所示,对接站160包括用于可操作地接合装置100的致动器组件102的接收空间162。关于对接站组件的更多详细信息请参阅申请序列号为pct/us2018/037157的pct专利申请案;该申请案中的内容以引用方式并入本文。
智能装置配置
如上所述,在一些情况下,所述活性药物递送系统包括标识,并且所述致动器组件包括标识读取器(例如,如上所述),使得所述装置可被视为“智能”装置。在此类实施例中,各种不同类型的信息均可以存储在标识上。标识读取器读取标识时(例如,在所述治疗药物递送组件与所述致动器组件可释放地接合时),可将所述信息传送至所述致动器组件。
在一些情况下,所述标识包括活性药物递送组分信息。活性药物递送组分信息是关于所述活性药物递送组分本身的信息或数据。此类信息可以包括活性药物递送组分的历史记录信息。历史记录信息是关于所述活性药物递送组分的性质和/或所述活性药物递送组分过往经历的一起或更多起事件的信息。历史记录信息包括但不限于:活性药物标识(例如,活性药物递送组分中含有的治疗药物(或其代替物)的名称);活性药物和/或活性药物递送组分的生产批号;活性药物递送组分处理信息(例如,关于活性药物递送组分通过的供应通道的信息);活性药物递送组分剂量、浓度和/或体积;以及活性药物递送组分到期日期、监管链信息(例如,包括时间和地理信息的货物跟踪信息,以及随时间变化的温度信息,例如可能已发生的任何储存温度偏移等)等。因此,历史记录信息可以包括关于活性药物递送组分中含有的特定活性药物的信息。此类信息可以包括但不限于所述活性药物的名称(品牌名和/或通用名)、生产日期、有效期至、生产来源、剂量、药物浓度、预期给药途径、处理和储存信息、递送量、适用证、批号等。
在一些情况下,所述标识包括活性药物递送组分信息,即,活性药物递送组分使用信息。活性药物递送组分使用信息是关于活性药物递送组分的实际使用的信息或数据,例如,实际使用活性药物递送组分,以向目标递送部位递送活性药物。此类信息可能会有所不同,并且可以包括使用日期信息(即,关于组分使用数据、时间等的信息);施用信息,例如,确认已实际递送至受试者体内;施用所述治疗药物的受试者的身份;施用所述治疗药物的受试者的身体状况等。
本领域技术人员应当理解,所述信息可以直接存储在标识上,或者可以使用标识信息在链接的数据库中查找。
智能装置实施例(例如,如上所述)考虑到一种或更多种所需的功能,包括但不限于库存管理功能、增强治疗功能、病历历史记录功能、数据分析功能等。例如,智能装置实施例提供了各种不同的库存管理功能,包括使用者对治疗药物递送组分进行自动重新排序(例如,依据使用者的预设偏好)、对单一治疗药物递送组分进行跟踪(例如,管理丢失、被盗或过期的商品组分)等。智能装置实施例提供了各种不同的增强治疗功能,包括自动生成手术记录、与现有电子病历通信以集成至患者图表中、发送关于药物/剂量/给药途径的数据以便记录和/或记账、汇总关于药物/剂量/给药途径的数据以用于市场研究和分析且便于记录报销等。由智能装置实施例提供的功能的示例(例如,如本文所述)详情请参阅已发布的第20160030683、20170098058、20170119969、20170124284和20170124285号美国专利申请出版物;这些出版物中的功能相关内容以引用方式并入本文。
由智能装置实施例提供的功能的示例(例如,如本文所述)详情请参阅申请序列号为pct/us2018/037157的pct专利申请案;该申请案中的内容以引用方式并入本文。
方法
本发明的方面进一步包括诸如通过使用本发明的活性药物递送装置将活性药物递送至受试者的靶组织递送部位的方法。所述方法的方面可以包括:使活性药物递送装置的无菌组织接触头端(例如,如上所述)接触所述靶组织递送部位;以及致动所述活性药物递送系统,以将一定剂量的活性药物组合物递送至所述靶组织递送部位。
如上所述,所述靶组织递送部位可能会有所不同。靶组织递送部位的示例包括外部和内部递送部位,其中内部递送部位包括位于体腔内的部位。外部部位包括角质化部位,以及以皮肤膜、粘膜和皮肤粘膜区组织为特征的部位。在一些情况下,所述靶组织递送部位是眼睛部位,其中目的眼睛部位包括从角膜缘开始,一直延伸至任何距离所述角膜缘后部1mm至10mm(例如距离所述角膜缘后部2mm至8mm以上)的位置的区域。在一些情况下,目的区域包括角膜和角膜缘。
为了使所述装置的远端与所述靶组织部位接触,可以操纵所述装置,使得所述装置的远端与所述靶组织部位接触。如有需要,所述远端与所述靶组织递送部位接触可以通过用适度的力将所述远端推靠在所述靶组织递送部位上来维持。
如上所述,装置的实施例可以包括疼痛缓解系统。可以致动所述疼痛缓解系统(如有)以缓解所述靶组织递送部位的疼痛。依据所述疼痛缓解系统的性质,所述疼痛缓解系统可以在所述装置的远端与所述靶组织递送部位接触之前或之后启用。例如,在所述疼痛缓解系统是冷却系统的情况下,可以启用所述疼痛缓解系统,使得所述无菌组织接触表面在与所述靶组织递送部位接触之前处于所需温度。或者,在所述疼痛缓解系统通过另一种机制(例如电刺激)缓解疼痛的情况下,所述疼痛缓解系统可以在所述无菌组织接触表面与所述靶组织递送部位接触之后启用。
在所述无菌组织接触表面与所述靶组织递送部位接触并致动疼痛缓解系统(如有)之后,致动所述活性药物递送系统,以将一定量(例如,剂量)的活性药物递送至所述靶组织递送部位。在所述活性药物递送系统的致动引起治疗药物自动递送的情况下,所述装置的抓握方式使得所述无菌组织接触表面在所述活性药物递送期间始终与所述靶组织递送部位接触。在活性药物递送完成之后,所述活性药物递送装置的针头可以从所述靶组织递送部位中抽出,例如,使用受控的回缩轮廓实现。
所述装置可用于将活性药物递送至各种不同类型的受试者的靶组织递送部位。在一些情况下,此类受试者为“哺乳动物”,此术语被广泛地用于描述属于哺乳动物类的生物体,包括食肉动物(例如狗和猫)、啮齿类动物(例如小鼠、豚鼠和大鼠)以及灵长类动物(例如人、黑猩猩和猴子)。在某些实施例中,所述受试者是人类。所述方法可以是诊断和/或治疗方法。
在一些情况下,所述方法包括组装活性药物递送装置,例如,通过将活性药物递送系统可操作地接合于致动器组件的接收空间中,以形成完整的装置,例如,如上所述。在一些情况下,所述方法包括从对接站中移除所述致动器组件,例如,如上所述。在一些情况下,所述方法进一步包括从所述致动器组件的接收空间中移除所述活性药物递送系统。所述移除可以包括处置所述治疗药物递送系统。在一些情况下,所述方法进一步包括将所述致动器组件对接于所述对接站中。
本发明的方面包括将活性药物递送至受试者眼内的方法。在此类实施例中,所述方法可以包括打开包装,例如,如下所述,所述包装包括预先填充有活性药物的注射器。如上所述,所述注射器可以具有无菌内部,而且其中存在的活性药物可以是无菌的。所述注射器还可以包括非无菌外表面,例如,所述主体的外表面的至少一部分是非无菌的,例如,如上所述。所述方法可以包括将无菌针头与所述注射器可操作地耦合,例如,通过诸如鲁尔接头将无菌针头接口耦合至所述注射器的孔口上。在某些实施例中,所述非无菌外表面可以接触一个或更多个表面,例如但不限于无菌区、无菌手套、患者的眼球表面、针头或接口表面等,这使得所述表面处于非无菌状态,例如,如上所述。随后,可以将所述活性药物施用于眼内,例如,通过压下注射器的柱塞实现。
图6a至6i显示了根据本发明的实施例的活性药物施用方案。在图6a至6i所示的方案中,所述方案首先提供存在于外罩中的头端以及在远端具有可移除盖帽或塞子的载药注射器。载药注射器未经表面灭菌,因此可在所述无菌区外进行操作。在图6b所示的步骤中,取下所述远端塞子,使得所述注射器准备好与所述头端进行可操作地接合。取下所述塞子可以露出接头,例如,用于与所述针头可操作地耦合的接头,其中所述接头可以是鲁尔接头,例如鲁尔滑动件或鲁尔锁。在图6c中,取下所述头端外罩的盖帽,露出所述头端的近端。在图6d中,所述头端的近端与所述注射器的远端耦合,例如,通过压配合运动实现,从而使得所述注射器的内部与所述头端的针头以流体连通方式耦合,并且所述注射器内的液体活性药物可以流入所述针头。在图6e中,取下所述头端的头端容器,使得活性药物递送系统准备好被安置于致动器的接收空间内,以形成活性药物递送装置100。在图6f中,所述组装好的装置100以直立位置安置,以便通过所述致动器的自动灌注活动来灌注所述装置。在所述装置灌注完成后,所述装置的无菌组织接触表面与眼睛接触,并保持足够长的时间,以便所述冷却系统给予所需的疼痛缓解,具体如图6g所示。如图6h中,所述致动器被激活以将所述针头移动至眼睛中,例如,其中致动包括移动所述针头,使其穿过所述无菌组织接触表面的通道,从而将所述针头的远端置于所述靶组织处。在将所述针头的远端置于所述靶组织处之后,所述致动器会移动所述注射器的柱塞,以便将所述注射器中所需剂量的活性药物组合物通过所述针头移至眼内。在一些情况下,所述注射器在致动过程中不在无菌区。使用后,从所述致动器中取出所述活性药物递送系统,并将所述致动器置于所述对接站中,例如,如图6i所示。
效用
本发明的装置(例如,如上所述)可用于将各种不同类型的活性药物递送至靶组织递送部位,以治疗各种不同类型的病症。本发明的活性药物递送装置可用于将活性药物递送至各种靶组织递送部位。靶组织递送部位的示例包括外部和内部递送部位,其中内部递送部位包括位于体腔内的部位。外部部位可以包括角质化部位,以及以皮肤膜、粘膜和皮肤粘膜区组织为特征的部位。在一些情况下,所述靶组织递送部位是眼组织递送部位,其中目的眼组织递送部位包括从角膜缘开始,一直延伸至任何距离所述角膜缘后部2mm至8mm以上的位置(例如距离所述角膜缘3mm至6mm、距离所述角膜缘3mm至4mm)的区域,例如,以便经由平坦部或皱摺部进行眼内注射。眼组织递送部位可以包括所述眼睛的结膜、巩膜外层和巩膜。在一些情况下,标的装置用于玻璃体内注射疗法(ivt)、眼球后注射疗法、筋膜下注射疗法、视网膜下注射疗法、脉络膜上腔注射疗法、结膜下注射疗法、眼房内注射疗法等。
所述装置及其使用方法可用于递送各种不同类型的活性药物。如上所述,可以递送任何所需的活性药物组合物,其中给定活性药物组合物可以包括单一活性药物或两种或更多种不同活性药物的组合。如上所述,活性药剂是在疾病的诊断、治愈、缓解、治疗或预防中发挥药理活性或其他直接作用,或者影响人或动物身体的结构或任何功能的任何组分。活性药物可能会有所不同,其中活性药剂的示例包括但不限于小分子活性药物、多肽活性药物,例如,抗体及其结合片段、融合蛋白等、核酸活性药物、细胞活性药物等。可存在的治疗性活性药物的示例包括但不限于:类固醇,例如可的松、地塞米松、氟轻松、氯替泼诺、二氟泼尼酯、氟米龙、泼尼松龙、甲羟孕酮、去炎松、倍他米松、氟扎可特、氢化可的松、利美索龙及其衍生物;非甾体抗炎药,例如水杨酸、吲哚基乙酸、芳基乙酸、芳基丙酸和烯醇酸衍生物,包括溴芬酸、双氯芬酸、氟比洛芬、酮咯酸氨丁三醇和奈帕芬胺;抗生素,例如杆菌肽、贝西沙星、左氧氟沙星、莫西沙星、磺胺醋酰、妥布霉素、头孢唑啉、头孢拉啶、头孢克洛、头孢匹林、头孢唑肟、头孢哌酮、头孢替坦、头孢呋辛、头孢噻肟、头孢羟氨苄、头孢他啶、头孢氨苄、头孢噻吩、头孢羟唑、头孢西丁、头孢尼西、头孢拉尼、头孢拉尼、头孢曲松、头孢羟氨苄、头孢拉啶、头孢呋辛、环孢菌素、氨苄青霉素、阿莫西林、环青霉素、氨苄青霉素、青霉素g、青霉素v钾、哌拉西林、苯唑西林、巴氨西林、氯洒西林、替卡西林、阿洛西林、羧苄西林、甲氧西林、萘夫西林、红霉素、四环素、强力霉素、米诺环素、氨曲南、氯霉素、环丙沙星、克林霉素、甲硝哒唑、庆大霉素、林可霉素、妥布霉素、万古霉素、多黏菌素b硫酸盐、甲磺酸粘菌素、粘菌素、阿奇霉素、安灭菌、磺胺甲恶唑、甲氧苄氨嘧啶、加替沙星、氧氟沙星及其衍生物;血管内皮生长因子(vegf)调节剂,例如,vegf抑制剂或拮抗剂,例如酪氨酸激酶抑制剂、vegf特异性结合剂,例如,vegf抗体或其结合片段、vegf结合融合蛋白等;血小板衍化生长因子(pdgf)调节剂,例如,pdgf抑制剂或拮抗剂,例如pdgf特异性结合剂,例如pdgf抗体或其结合片段、pdgf结合融合蛋白等;血管生成素(ang)调节剂,例如ang2调节剂,例如,ang2抑制剂或拮抗剂,例如ang2特异性结合剂,例如ang2抗体或其结合片段、ang2结合融合蛋白等;ang2和vegf组合抑制剂;含有vegf抑制剂的抗体生物聚合物共轭物;含有苹果酸舒尼替尼的聚-丙交酯-共聚-乙交酯酸(plga)颗粒;胎盘生长因子(plgf)调节剂,例如,plgf抑制剂或拮抗剂,例如plgf特异性结合剂,例如,plgf抗体或其结合片段、plgf结合融合蛋白等;组织坏死因子(tnf)调节剂,例如,抗tnfα药物,例如针对tnf-α的抗体、针对tnf-α的抗体片段和tnf结合融合蛋白,包括英夫利昔单抗、依那西普、阿达木单抗、赛妥珠单抗和戈利木单抗;mtor抑制剂,例如西罗莫司、西罗莫司类似物、依维莫司、替西罗莫司和mtor激酶抑制剂;细胞,例如间充质细胞(例如,间充质干细胞),或被转染以产生治疗性化合物的细胞;神经保护剂,例如抗氧化剂、钙调神经蛋白抑制剂、nos抑制剂、σ-1调节剂、ampa拮抗剂、钙通道阻滞剂和组蛋白去乙酰酶抑制剂;抗高血压剂或眼内压降低剂,例如前列腺素类似物、rok抑制剂、β阻断剂、α激动剂和碳酸酐酶抑制剂;多特异性调节剂,例如,双特异性调节剂,例如双特异性结合剂,例如,双特异性抗体或其结合片段,包括与vegf和ang2特异性结合的药物;氨基甾醇,例如角鲨胺;抗组胺药,例如h1-受体拮抗剂和组胺h2-受体拮抗剂,例如,氯雷他定、羟嗪、苯海拉明、氯苯那敏、溴苯那敏、赛庚啶、特非那定、氯马斯汀、曲普利啶、卡比沙明、二苯拉林、苯茚胺、阿扎他定、曲吡那敏、右旋氯苯那敏、右旋溴苯那敏、甲地拉嗪和异丁嗪抗敏安、苯那敏、嘧啶胺、氯环嗪、松齐拉敏及其衍生物;酪氨酸激酶抑制剂,包括受体酪氨酸激酶抑制剂;基于核酸的治疗药物,例如基因载体,例如,质粒、rnai药物,例如,sirna、shrna;补体系统调节剂,例如,补体系统抑制剂,包括替代补体途径抑制剂(例如因子d、备解素、因子b、因子ba和因子bb)和经典补体途径抑制剂(例如c3a、c5、c5a、c5b、c6、c7、c8、c9和c5b-9);化疗药物,例如,阿霉素、环磷酰胺、放线菌素、博莱霉素、道诺霉素、多柔比星、表柔比星、丝裂霉素、甲氨蝶呤、氟尿嘧啶、卡铂、卡莫司汀(bcnu)、甲基-ccnu、顺铂、依托泊苷、干扰素、喜树碱及其衍生物、苯芥胆留醇、紫杉醇及其衍生物、泰索帝及其衍生物、长春碱、长春新碱、他莫昔芬、依托泊苷、哌泊舒凡、环磷酰胺和氟他胺及其衍生物;胰岛素等。
所述装置可用于递送治疗药物以治疗各种不同的病症。目的病症包括但不限于眼部疾病,例如眼部病症、眼内新生血管病症。“眼内新生血管疾病”是一种以眼内新生血管形成为特征的疾病。眼内新血管疾病的示例包括,例如,增生性视网膜病变、脉络膜新生血管形成(cnv)、年龄相关性黄斑变性(amd)、地图样萎缩(ga)、糖尿病和其他缺血相关性视网膜病变、糖尿病性黄斑水肿、病理性近视、冯·希佩尔-林道病、眼组织胞浆菌病、视网膜中央静脉阻塞(crvo)、视网膜分支静脉阻塞(brvo)、翼状胬肉、角膜新生血管形成和视网膜新生血管形成。术语“年龄相关性黄斑变性”是指通常影响老年人且由于视网膜损伤而导致视野中心(黄斑)视力丧失的病症。这些病症中的一些或全部均可以通过玻璃体内注射vegf-拮抗剂来治疗,例如,如上所述。根据本发明的方面可以治疗的其他眼部疾病包括但不限于:视网膜脱离(气动视网膜固定术——通过使用本发明的装置将气体注射至眼内进行治疗),其中所述装置可以将注射深度控制为所需/最佳深度。目的病症还包括中心性浆液性脉络膜视网膜病变和葡萄膜炎,包括前葡萄膜炎、睫状体平坦部炎、中间葡萄膜炎和后葡萄膜炎。
套件
本发明还提供了包括至少一种或更多种治疗药物递送组件(例如,如上所述)的套件。例如,套件可以包括针头和组织接触头端(例如,如上所述)和/或预先填充有活性药物组合物的注射器,其中这些组件可以彼此隔开或彼此可操作地接合为复合结构。例如,套件可以包括头端组件(其包括与针头接合且存在于外罩中的头端,例如,如图3b所示)和如图4b所示的载药注射器。如有需要,套件可以进一步包括致动器组件、对接站等。套件组件可以存在于包装中,根据需要,所述包装可以是无菌的,也可以是非无菌的。例如,在所述套件包括载药注射器(例如,如上所述)的情况下,在将所述注射器置于所述包装中之后,不对所述包装进行灭菌处理。
图7a和7b提供了根据两个不同实施例的套件的视图。在图7a中,套件180包括第一包装组件182(其中存在头端组件,如图3b所示)和第二包装组件184(其中存在载药注射器,如图4b所示)。在图7b中,所述套件包括单个包装组件186,其中存在所述头端组件和所述载药注射器。
所述套件中还可能有所述套件组件的使用说明。所述说明书可以记录在合适的记录媒体上。例如,所述说明书可以印在基材上,例如,纸或塑料等。因此,所述套件中的说明书可以包装说明书、所述套件或其组成部分的容器(即,与包装或分包装有关)上的标签等的形式存在。在其他实施例中,所述说明书可以作为载于合适的计算机可读存储介质(例如,便携式闪存驱动器、dvd-rom或cd-rom等)上的电子存储数据文件存在。所述说明书可以采用任何形式,包括有关如何使用所述装置的完整说明书,或发布在万维网上、载有说明书的可访问网址。
虽然本文附有权利要求书,但本发明的范围还受以下条款限定:
1.一种活性药物递送装置,所述装置包含:
(a)未经表面灭菌且包含所述活性药物的液体组合物的注射器;
(b)包含无菌组织接触表面的头端;以及
(c)与所述注射器和所述头端可操作地耦合的针头。
2.根据条款1所述的装置,其中所述注射器的容积范围为0.1至5.0ml。
3.根据条款2所述的装置,其中所述注射器的容积范围为0.1至1.50ml。
4.根据条款3所述的装置,其中所述注射器的容积范围为0.1至1.0ml。
5.根据前述条款中任一项所述的装置,其中所述装置被配置成递送体积范围为5μl至100μl的药剂。
6.根据条款5所述的装置,其中所述装置被配置成递送体积范围为10μl至50μl的药剂。
7.根据前述条款中任一项所述的装置,其中所述注射器包含剂量标记。
8.根据条款7所述的装置,其中所述剂量标记指示递送剂量小于所述注射器的容积。
9.根据条款7或8所述的装置,其中所述剂量标记范围为5至100μl。
10.根据条款9所述的装置,其中所述剂量标记为50μl。
11.根据条款1至6中任一项所述的装置,其中所述注射器不包括剂量标记。
12.根据前述条款中任一项所述的装置,其中所述注射器包含一个或更多个腔室。
13.根据前述条款中任一项所述的装置,其中所述注射器包含玻璃制品。
14.根据条款1至12中任一项所述的装置,其中所述注射器包含塑料制品。
15.根据条款14所述的装置,其中所述塑料选自由环烯烃聚合物(cop)和环烯烃共聚物(coc)组成的群组。
16.根据前述条款中任一项所述的装置,其中所述无菌组织接触表面为平面。
17.根据前述条款中任一项所述的装置,其中所述无菌组织接触表面的组织接触表面面积范围为0.5至50mm2。
18.根据前述条款中任一项所述的装置,其中所述无菌组织接触表面包含大小适合让所述针头穿过其中的通道。
19.根据前述条款中任一项所述的递送装置,其中所述针头的规格范围为23至35号。
20.根据条款19所述的递送装置,其中所述针头的规格范围为30至33号。
21.根据条款19所述的递送装置,其中所述针头的规格范围为23至30号。
22.根据条款19至21中任一项所述的装置,其中所述针头包含两个或更多个内腔。
23.根据条款22所述的装置,其中所述针头包含两个内腔。
24.根据前述条款中任一项所述的装置,其中所述针头的远端相对于所述无菌组织接触表面是可移动的。
25.根据前述条款中任一项所述的装置,其中所述针头存在于针罩内。
26.根据条款25所述的装置,其中所述头端与所述针罩的远端可操作地耦合,且所述注射器的远端与所述针罩的近端可操作地耦合。
27.根据条款26所述的装置,其中所述注射器的远端通过接头与所述针罩的近端可操作地耦合。
28.根据条款27所述的装置,其中所述接头为鲁尔接头。
29.根据条款28所述的装置,其中所述鲁尔接头包含鲁尔滑动件。
30.根据条款28所述的装置,其中所述鲁尔接头包含鲁尔锁。
31.根据前述条款中任一项所述的装置,其中所述头端与两个或更多个针头可操作地耦合。
32.根据前述条款中任一项所述的装置,其中所述装置进一步包含致动器组件,所述组件包含被配置成移动所述液体组合物使其通过所述针头的致动器。
33.根据条款32所述的装置,其中所述致动器包含电机。
34.根据条款32所述的装置,其中所述致动器包含弹簧。
35.根据条款32所述的装置,其中所述致动器包含手动致动器。
36.根据条款32至35中任一项所述的装置,其中所述致动器被配置成依次执行第一灌注运动和第二注射运动。
37.根据条款36所述的装置,其中所述致动器进一步被配置成在所述第二注射运动后抽回所述针头。
38.根据条款32至37中任一项所述的装置,其中所述致动器组件进一步包含注射器接收空间,所述空间包含注射器。
39.根据条款32至38中任一项所述的装置,其中所述致动器组件进一步包含与所述头端可操作地耦合的疼痛缓解系统。
40.根据条款39所述的装置,其中所述疼痛缓解系统包含麻醉产生系统。
41.根据条款40所述的装置,其中所述麻醉产生系统包含冷却系统。
42.根据条款41所述的装置,其中所述冷却系统选自由以下各项组成的群组:热电冷却系统、液体蒸发冷却系统、固体升华冷却系统、固体熔化冷却系统、焦耳-汤姆逊冷却系统、热力循环冷却系统、吸热反应冷却系统和低温物质冷却系统。
43.根据条款42所述的装置,其中所述冷却系统包含热电冷却系统。
44.根据条款43所述的装置,其中所述热电冷却系统包含珀耳帖单元、将所述珀耳帖单元与所述组织接触表面耦合的导体以及与所述珀耳帖单元耦合的散热器。
45.根据条款42所述的装置,其中所述冷却系统包含低温物质冷却系统。
46.根据条款45所述的装置,其中所述低温物质冷却系统包含液体或凝胶。
47.根据前述条款中任一项所述的装置,其中所述液体组合物包含vegf调节剂。
48.根据条款47所述的装置,其中所述vegf调节剂包含抗体、双特异性抗体或其结合片段。
49.根据前述条款中任一项所述的装置,其中所述液体组合物包含补体系统调节剂。
50.根据条款49所述的装置,其中所述补体系统调节剂包含小分子、抗体或其结合片段。
51.根据前述条款中任一项所述的装置,其中所述液体组合物包含眼内压降低剂。
52.根据条款51所述的装置,其中所述眼内压降低剂选自由前列腺素类似物、rok抑制剂、β阻断剂、碳酸酐酶抑制剂、α激动剂、酪氨酸激酶抑制剂、血管生成素抑制剂、胎盘生长因子抑制剂、核酸试剂及其组合组成的群组。
53.根据前述条款中任一项所述的装置,其中所述液体组合物包含两种或更多种活性药物。
54.根据条款53所述的装置,其中所述液体组合物包含vegf调节剂和补体系统调节剂。
55.根据条款54所述的装置,其中所述液体组合物包含双特异性抗体和补体系统调节剂。
56.根据前述条款中任一项所述的装置,其中所述注射器包含两个或更多个腔室,每个腔室均含有不同的液体组合物。
57.根据条款56所述的装置,其中所述不同的液体组合物具有不同的粘度。
58.根据条款1至55中任一项所述的装置,其中所述装置包含两支或更多支注射器,每支注射器均含有不同的液体组合物。
59.根据条款58所述的装置,其中所述不同的液体组合物具有不同的粘度。
60.根据前述条款中任一项所述的装置,其中所述装置为手持式装置。
61.根据前述条款中任一项所述的装置,其中所述装置被配置成将所述液体组合物递送至眼组织递送部位。
62.一种用于活性药物递送装置的头端组件,所述头端组件包含:
包含无菌组织接触表面的头端;以及
与所述头端可操作地耦合的针头。
63.根据条款62所述的头端组件,其中所述无菌组织接触表面为平面。
64.根据条款62和63中任一项所述的头端组件,其中所述无菌组织接触表面的组织接触表面面积范围为0.5至50mm2。
65.根据条款62至64中任一项所述的头端组件,其中所述无菌组织接触表面包含大小适合让所述针头穿过其中的通道。
66.根据条款62至65中任一项所述的头端组件,其中所述针头的规格范围为23至35号。
67.根据条款66所述的头端组件,其中所述针头的规格范围为30至33号。
68.根据条款66所述的头端组件,其中所述针头的规格范围为23至30号。
69.根据条款66至68中任一项所述的头端组件,其中所述针头包含两个或更多个内腔。
70.根据条款69所述的头端组件,其中所述针头包含两个内腔。
71.根据条款62至70中任一项所述的头端组件,其中所述针头的远端相对于所述无菌组织接触表面是可移动的。
72.根据条款62至71中任一项所述的头端组件,其中所述针头存在于针罩内。
73.根据条款72所述的头端组件,其中所述头端与所述针罩的远端可操作地耦合。
74.根据条款73所述的头端组件,其中所述针罩的近端包含接头。
75.根据条款74所述的头端组件,其中所述接头为鲁尔接头。
76.根据条款75所述的头端组件,其中所述鲁尔接头包含鲁尔滑动件。
77.根据条款75所述的头端组件,其中所述鲁尔接头包含鲁尔锁。
78.根据条款62至77中任一项所述的头端组件,其中所述头端组件存在于密封罩内。
79.根据条款78所述的头端组件,其中所述密封罩包含无菌内部和非无菌外部。
80.根据条款78和79中任一项所述的头端组件,其中所述外罩包含头端组件容器和盖帽。
81.根据条款62至80中任一项所述的头端组件,其中所述头端与两个或更多个针头可操作地耦合。
82.一种未经表面灭菌且包含无菌液体组合物的注射器,所述无菌液体组合物包含活性药物。
83.根据条款82所述的注射器,其中所述注射器的容积范围为0.1至5.0ml。
84.根据条款83所述的注射器,其中所述注射器的容积范围为0.1至1.50ml。
85.根据条款84所述的注射器,其中所述注射器的容积范围为0.1至1.0ml。
86.根据条款82至85中任一项所述的注射器,其中所述注射器被配置成递送体积范围为5μl至100μl的药剂。
87.根据条款86所述的注射器,其中所述注射器被配置成递送体积范围为10μl至50μl的药剂。
88.根据条款82至87中任一项所述的注射器,其中所述注射器包含剂量标记。
89.根据条款88所述的注射器,其中所述剂量标记指示递送剂量小于所述注射器的容积。
90.根据条款88或89所述的注射器,其中所述剂量标记范围为10至100μl。
91.根据条款90所述的注射器,其中所述剂量标记为50μl。
92.根据条款82至87中任一项所述的注射器,其中所述注射器不包括剂量标记。
93.根据条款82至92中任一项所述的注射器,其中所述液体组合物包含vegf调节剂。
94.根据条款93所述的注射器,其中所述vegf调节剂包含抗体、双特异性抗体或其结合片段。
95.根据条款82至94中任一项所述的注射器,其中所述液体组合物包含补体系统调节剂。
96.根据条款95所述的注射器,其中所述补体系统调节剂包含小分子、抗体或其结合片段。
97.根据条款82至96中任一项所述的注射器,其中所述液体组合物包含眼内压降低剂。
98.根据条款97所述的注射器,其中所述眼内压降低剂选自由前列腺素类似物、rok抑制剂、β阻断剂、碳酸酐酶抑制剂、α激动剂、酪氨酸激酶抑制剂、血管生成素抑制剂、胎盘生长因子抑制剂、核酸试剂及其组合组成的群组。
99.根据条款82至98中任一项所述的注射器,其中所述液体组合物包含两种或更多种活性药物。
100.根据条款99所述的注射器,其中所述液体组合物包含vegf调节剂和补体系统调节剂。
101.根据条款100所述的注射器,其中所述液体组合物包含双特异性抗体和补体系统调节剂。
102.根据条款82至101中任一项所述的注射器,其中所述注射器包含两个或更多个腔室,每个腔室均含有不同的液体组合物。
103.根据条款102所述的注射器,其中所述不同的液体组合物具有不同的粘度。
104.根据条款82至103中任一项所述的注射器,其中所述注射器包含远端可移除盖帽。
105.根据条款104所述的注射器,其中取下所述可移除盖帽会露出接头。
106.根据条款105所述的注射器,其中所述接头包含鲁尔接头。
107.根据条款106所述的注射器,其中所述鲁尔接头包含鲁尔滑动件。
108.根据条款106所述的注射器,其中所述鲁尔接头包含鲁尔锁。
109.根据条款82至108中任一项所述的注射器,其中所述注射器包含一个或更多个腔室。
110.根据条款82至109中任一项所述的注射器,其中所述注射器包含玻璃制品。
111.根据条款82至109中任一项所述的注射器,其中所述注射器包含塑料制品。
112.根据条款111所述的注射器,其中所述塑料选自由环烯烃聚合物(cop)和环烯烃共聚物(coc)组成的群组。
113.一种用于活性药物递送装置的致动器组件,所述活性药物递送装置包含未经表面灭菌且包含所述活性药物的液体组合物的注射器;可操作地包含无菌组织接触表面的头端;以及与所述注射器和所述头端可操作地耦合的针头,所述致动器组件包含:
被配置成移动所述液体组合物使其通过所述针头的致动器。
114.根据条款113所述的致动器组件,其中所述致动器包含电机。
115.根据条款113所述的致动器组件,其中所述致动器包含弹簧。
116.根据条款113所述的致动器组件,其中所述致动器包含手动致动器。
117.根据条款113至116中任一项所述的致动器组件,其中所述致动器被配置成依次执行第一灌注运动和第二注射运动。
118.根据条款117所述的致动器组件,其中所述致动器进一步被配置成在所述第二注射运动后抽回所述针头。
119.根据条款113至118中任一项所述的致动器组件,其中所述致动器组件进一步包含注射器接收空间,所述空间被配置成接收所述注射器。
120.根据条款113至119中任一项所述的致动器组件,其中所述致动器组件进一步包含与所述头端可操作地耦合的疼痛缓解系统。
121.根据条款120所述的致动器组件,其中所述疼痛缓解系统包含麻醉产生系统。
122.根据条款121所述的致动器组件,其中所述麻醉产生系统包含冷却系统。
123.根据条款122所述的致动器,其中所述冷却系统选自由以下各项组成的群组:热电冷却系统、液体蒸发冷却系统、固体升华冷却系统、固体熔化冷却系统、焦耳-汤姆逊冷却系统、热力循环冷却系统、吸热反应冷却系统和低温物质冷却系统。
124.根据条款123所述的致动器,其中所述冷却系统包含热电冷却系统。
125.根据条款124所述的致动器,其中所述热电冷却系统包含珀耳帖单元、将所述珀耳帖单元与所述组织接触表面耦合的导体以及与所述珀耳帖单元耦合的散热器。
126.根据条款123所述的致动器,其中所述冷却系统包含低温物质冷却系统。
127.根据条款126所述的致动器,其中所述低温物质冷却系统包含液体或凝胶。
128.根据条款113至127中任一项所述的致动器组件,其中所述致动器组件存在于对接站中。
129.一种向靶组织递送一种或更多种活性药物的方法,所述方法包含:
(a)将活性药物递送装置的无菌组织接触表面与所述靶组织的靶组织递送位点接触,所述装置包含:
(i)未经表面灭菌且包含所述一种或更多种活性药物的液体组合物的注射器;
(ii)包含所述无菌组织接触表面的头端;以及
(iii)与所述注射器和所述头端可操作地耦合的针头;
(b)致动所述注射器,以移动所述注射器内一定剂量的所述液体组合物使其通过针头,从而将所述活性药物递送至所述靶组织。
130.根据条款129所述的方法,其中致动包含移动所述针头,使其穿过所述无菌组织接触表面的通道,从而将所述针头的远端置于所述靶组织处。
131.根据条款129至130中任一项所述的方法,其中所述方法进一步包含灌注所述装置。
132.根据条款129至131中任一项所述的方法,其中方法进一步包含组装所述装置。
133.根据条款132所述的方法,其中组装所述装置包含将所述注射器与包含所述头端和所述针头的头端组件可操作地耦合,以形成组装好的注射器和针头。
134.根据条款129至133中任一项所述的方法,其中所述致动包含手动致动。
135.根据条款134所述的方法,其中所述手动致动包含先相对于所述头端移动所述针头,然后压下所述注射器的柱塞。
136.根据条款135所述的方法,其中所述方法进一步包含将所述组装好的注射器和针头与致动器耦合。
137.根据条款136所述的方法,其中所述致动器进一步包含疼痛缓解系统,且所述方法进一步包含致动疼痛缓解系统。
138.根据条款129至137中任一项所述的方法,其中所述液体组合物包含vegf调节剂。
139.根据条款138所述的方法,其中所述vegf调节剂包含抗体、双特异性抗体或其结合片段。
140.根据条款129至139中任一项所述的方法,其中所述液体组合物包含补体系统调节剂。
141.根据条款140所述的方法,其中所述补体系统调节剂包含小分子、抗体或其结合片段。
142.根据条款129至141中任一项所述的方法,其中所述液体组合物包含眼内压降低剂。
143.根据条款142所述的方法,其中所述眼内压降低剂选自由前列腺素类似物、rok抑制剂、β阻断剂、碳酸酐酶抑制剂、α激动剂、酪氨酸激酶抑制剂、血管生成素抑制剂、胎盘生长因子抑制剂、核酸试剂及其组合组成的群组。
144.根据条款129至143中任一项所述的方法,其中所述液体组合物包含两种或更多种活性药物。
145.根据条款144所述的方法,其中所述液体组合物包含vegf调节剂和补体系统调节剂。
146.根据条款144所述的方法,其中所述液体组合物包含双特异性抗体和补体系统调节剂。
147.根据条款129至146中任一项所述的方法,其中所述注射器包含两个或更多个腔室,每个腔室均含有不同的液体组合物。
148.根据条款147所述的方法,其中所述不同的液体组合物具有不同的粘度。
149.根据条款129至148中任一项所述的方法,其中所述注射器在接触和致动期间不在所述无菌区内。
150.根据条款149所述的方法,其中所述方法包含以非无菌方式处理所述注射器。
151.根据条款129至150中任一项所述的方法,其中所述靶组织递送部位包含眼组织递送部位。
152.根据条款151所述的方法,其中所述眼组织递送部位位于所述角膜缘0.5mm至4mm范围内。
153.根据条款152所述的方法,其中所述方法包含通过所述角膜将所述液体组合物递送至所述前眼房。
154.根据条款129至153中任一项所述的方法,其中所述方法是用于治疗受试者的眼病的方法。
155.一种将活性药物组合物递送至受试者眼内的方法,所述方法包含:
(a)打开含有载药注射器的包装,所述注射器包含:
(i)包含所述活性药物组合物的无菌内部;以及
(ii)非无菌外表面;
(b)将无菌针头的无菌接头与所述注射器可操作地耦合;
(c)使所述非无菌外表面与第二表面接触,使得所述第二表面在所述接触后变为非无菌状态;以及
(d)用所述注射器将所述活性药物组合物施用于受试者眼内。
156.根据条款155所述的方法,其中所述方法是用于治疗受试者的眼病的方法。
157.根据条款156所述的方法,其中所述活性药物组合物包含vegf调节剂。
158.根据条款156所述的方法,其中所述vegf调节剂包含抗体、双特异性抗体或其结合片段。
159.根据条款156所述的方法,其中所述活性药物包含补体系统调节剂。
160.根据条款159所述的方法,其中所述补体系统调节剂包含小分子、抗体或其结合片段。
161.根据条款156所述的方法,其中所述活性药物包含眼内压降低剂。
162.根据条款161所述的方法,其中所述眼内压降低剂选自由前列腺素类似物、rok抑制剂、β阻断剂、碳酸酐酶抑制剂、α激动剂、酪氨酸激酶抑制剂、血管生成素抑制剂、胎盘生长因子抑制剂、核酸试剂及其组合组成的群组。
163.根据条款155至162中任一项所述的方法,其中所述活性药物组合物包含两种或更多种活性药物。
164.根据条款163所述的方法,其中所述活性药物组合物包含vegf调节剂和补体系统调节剂。
165.根据条款163所述的方法,其中所述活性药物组合物包含双特异性抗体和补体系统调节剂。
166.根据条款155至165中任一项所述的方法,其中所述注射器包含两个或更多个腔室,每个腔室均含有不同的活性药物组合物。
167.根据条款166所述的方法,其中所述不同的液体组合物具有不同的粘度。
168.根据条款155至167中任一项所述的方法,其中所述针头的规格范围为23至35号。
169.根据条款168所述的方法装置,其中所述针头的规格范围为29至33号。
170.根据条款155至169中任一项所述的方法,其中所述第二表面包含无菌区。
171.根据条款155至170中任一项所述的方法,其中所述第二表面包含无菌手套。
172.根据条款155至171中任一项所述的方法,其中所述第二表面包含眼球表面。
173.根据条款155至172中任一项所述的方法,其中所述第二表面包含所述针头或针头接口表面。
174.一种套件,其包含:
(a)活性药物递送装置头端组件,其包含:
(i)包含无菌组织接触表面的头端;以及
(c)与所述头端可操作地耦合的针头;
其中所述头端组件存在于密封罩内,所述密封罩包含无菌内部和非无菌外部;以及
(b)未经表面灭菌且包含液体组合物(包含活性药物)的注射器。
175.根据条款174所述的套件,其中所述针头是无菌的。
176.根据条款174至175中任一项所述的套件,其中所述无菌组织接触表面为平面。
177.根据条款174至176中任一项所述的套件,其中所述无菌组织接触表面的组织接触表面面积范围为0.5至50mm2。
178.根据条款174至177中任一项所述的套件,其中所述无菌组织接触表面包含大小适合让所述针头穿过其中的通道。
179.根据条款174至178中任一项所述的套件,其中所述针头的规格范围为23至35号。
180.根据条款179所述的套件,其中所述针头的规格范围为30至33号。
181.根据条款180所述的套件,其中所述针头的规格范围为23至30号。
182.根据条款174至181中任一项所述的套件,其中所述针头包含两个或更多个内腔。
183.根据条款182所述的套件,其中所述针头包含两个内腔。
184.根据条款174至183中任一项所述的套件,其中所述针头的远端相对于所述无菌组织接触表面是可移动的。
185.根据条款174至184中任一项所述的套件,其中所述针头存在于针罩内。
186.根据条款185所述的套件,其中所述头端与所述针罩的远端可操作地耦合。
187.根据条款186所述的套件,其中所述针罩的近端包含接头。
188.根据条款187所述的套件,其中所述接头为鲁尔接头。
189.根据条款188所述的套件,其中所述鲁尔接头包含鲁尔滑动件。
190.根据条款188所述的套件,其中所述鲁尔接头包含鲁尔锁。
191.根据条款184至190中任一项所述的套件,其中所述外罩包含头端组件容器和盖帽。
192.根据条款174至191中任一项所述的套件,其中所述注射器的容积范围为0.1至5.0ml。
193.根据条款192所述的套件,其中所述注射器的容积范围为0.1至1.50ml。
194.根据条款193所述的套件,其中所述注射器的容积范围为0.1至1.0ml。
195.根据条款174至194中任一项所述的套件,其中所述注射器被配置成递送体积范围为5μl至100μl的药剂。
196.根据条款195所述的套件,其中所述注射器被配置成递送体积范围为10μl至50μl的药剂。
197.根据条款174至196中任一项所述的套件,其中所述注射器包含剂量标记。
198.根据条款197所述的套件,其中所述剂量标记指示递送剂量小于所述注射器的容积。
199.根据条款197至198中任一项所述的套件,其中所述剂量标记范围为10至100μl。
200.根据条款199所述的套件,其中所述剂量标记为50μl。
201.根据条款174至196中任一项所述的套件,其中所述套件不包括剂量标记。
202.根据条款174至201中任一项所述的套件,其中所述液体组合物包含vegf调节剂。
203.根据条款202所述的套件,其中所述vegf调节剂包含抗体、双特异性抗体或其结合片段。
204.根据条款174至203中任一项所述的套件,其中所述液体组合物包含补体系统调节剂。
205.根据条款204所述的套件,其中所述补体系统调节剂包含小分子、抗体或其结合片段。
206.根据条款174至205中任一项所述的套件,其中所述液体组合物包含眼内压降低剂。
207.根据条款206所述的套件,其中所述眼内压降低剂选自由前列腺素类似物、rok抑制剂、β阻断剂、碳酸酐酶抑制剂、α激动剂、酪氨酸激酶抑制剂、血管生成素抑制剂、胎盘生长因子抑制剂、核酸试剂及其组合组成的群组。
208.根据条款174至207中任一项所述的套件,其中所述液体组合物包含两种或更多种活性药物。
209.根据条款208所述的套件,其中所述液体组合物包含vegf调节剂和补体系统调节剂。
210.根据条款208所述的套件,其中所述液体组合物包含双特异性抗体和补体系统调节剂。
211.根据条款174至210中任一项所述的套件,其中所述注射器包含两个或更多个腔室,每个腔室均含有不同的液体组合物。
212.根据条款211所述的套件,其中所述不同的液体组合物具有不同的粘度。
213.根据条款174至212中任一项所述的套件,其中所述注射器包含远端可移除盖帽。
214.根据条款213所述的套件,其中取下所述可移除盖帽会露出接头。
215.根据条款214所述的套件,其中所述接头包含鲁尔接头。
216.根据条款215所述的套件,其中所述鲁尔接头包含鲁尔滑动件。
217.根据条款215所述的套件,其中所述鲁尔接头包含鲁尔锁。
218.一种套件,其包含:
(a)注射器,其包含:
(i)具有非无菌外表面且定义包含活性药物组合物的无菌内部空间的主体;
(ii)位于所述主体第一端的柱塞;
(iii)位于所述主体第二端的孔口;以及
(iv)密封所述孔口的可移除盖帽;以及
(b)含有所述注射器的非无菌包装。
219.根据条款218所述的套件,其中所述非无菌包装在将所述注射器置于所述包装中之后未对其进行灭菌处理。
220.根据条款218至219中任一项所述的套件,其中所述注射器的容积范围为0.1至5.0ml。
221.根据条款220所述的套件,其中所述注射器的容积范围为0.1至1.50ml。
222.根据条款221所述的套件,其中所述注射器的容积范围为0.1至1.0ml。
223.根据条款218至222中任一项所述的套件,其中所述注射器被配置成递送体积范围为5μl至100μl的药剂。
224.根据条款223所述的套件,其中所述注射器被配置成递送体积范围为10μl至50μl的药剂。
225.根据条款218至224中任一项所述的套件,其中所述注射器包含剂量标记。
226.根据条款225所述的套件,其中所述剂量标记指示递送剂量小于所述注射器的容积。
227.根据条款225至226所述的套件,其中所述剂量标记范围为10至100μl。
228.根据条款227所述的套件,其中所述剂量标记为50μl。
229.根据条款218至224中任一项所述的套件,其中所述注射器不包括剂量标记。
230.根据条款218至229中任一项所述的套件,其中所述活性药物组合物包含vegf调节剂。
231.根据条款230所述的套件,其中所述vegf调节剂包含抗体、双特异性抗体或其结合片段。
232.根据条款218至229中任一项所述的套件,其中所述活性药物组合物包含补体系统调节剂。
233.根据条款232所述的套件,其中所述补体系统调节剂包含小分子、抗体或其结合片段。
234.根据条款218至229中任一项所述的套件,其中所述活性药物组合物包含眼内压降低剂。
235.根据条款234所述的套件,其中所述眼内压降低剂选自由前列腺素类似物、rok抑制剂、β阻断剂、碳酸酐酶抑制剂、α激动剂、
酪氨酸激酶抑制剂、血管生成素抑制剂、胎盘生长因子抑制剂、核酸试剂及其组合组成的群组。
236.根据条款218至235中任一项所述的套件,其中所述液体组合物包含两种或更多种活性药物。
237.根据条款236所述的套件,其中所述液体组合物包含vegf调节剂和补体系统调节剂。
238.根据条款236所述的套件,其中所述液体组合物包含双特异性抗体和补体系统调节剂。
239.根据条款218至238中任一项所述的套件,其中所述注射器包含两个或更多个腔室,每个腔室均含有不同的液体组合物。
240.根据条款239所述的套件,其中所述不同的液体组合物具有不同的粘度。
241.根据条款218至240中任一项所述的套件,其中取下所述可移除盖帽会露出接头。
242.根据条款241所述的套件,其中所述接头包含鲁尔接头。
243.根据条款242所述的套件,其中所述鲁尔接头包含鲁尔滑动件或鲁尔锁。
244.根据条款218至243中任一项所述的套件,其中所述注射器主体由玻璃制成。
245.根据条款218至243中任一项所述的套件,其中所述注射器由塑料制成。
在至少一些前述实施例中,一实施例中使用的一个或更多个元件可以在另一实施例中互换使用,除非这种替换在技术上不可行。本领域技术人员应当理解,在不脱离所主张的标的的情况下,可对上述方法和结构进行各种其他省略、添加和修改。所有这些修改和变更内容都旨在被所附权利要求书中定义的标的范围覆盖。
本领域技术人员应当理解,一般而言,本文使用的术语,特别是所附权利要求书中(例如,在所附权利要求书的主体部分中)使用的术语,通常应理解为“开放”术语(例如,术语“包括”应解释为“包括但不限于”,术语“具有”应解释为“至少具有”等)。本领域技术人员还应理解,如果意在所引入的权利要求中标明具体数目,则这种意图将在该权利要求中明确指出,而在无这种明确标明的情况下,则视为不存在这种意图。例如,为帮助理解,所附权利要求可能使用了引导短语“至少一个”和“一个或更多个”来引入权利要求中的特征。然而,这种短语的使用不应被解释为暗示着由不定冠词“一”或“一个”引入的权利要求特征将含有该特征的任意特定权利要求限制为仅含有一个该特征的实施例,即便是该权利要求既包括引导短语“一个或更多个”或“至少一个”又包括不定冠词如“一”或“一个”(例如,“一”和/或“一个”应当被解释为意指“至少一个”或“一个或更多个”);在使用定冠词来引入权利要求中的特征时,同样如此。另外,即使明确指出了所引入权利要求特征的具体数目,本领域技术人员应当认识到,这种列举应解释为意指至少是所列数目(例如,不存在其他修饰语的短语“两个特征”意指至少两个该特征,或者两个或更多该特征)。另外,在使用类似于“a、b和c等中至少一个”这样的表述的情况下,一般来说应该按照本领域技术人员通常理解该表述的含义来予以解释(例如,“具有a、b和c中至少一个的系统”应包括但不限于单独具有a、单独具有b、单独具有c、具有a和b、具有a和c、具有b和c和/或具有a、b和c的系统等)。在使用类似于“a、b或c等中至少一个”这样的表述的情况下,一般来说应该按照本领域技术人员通常理解该表述的含义来予以解释(例如,“具有a、b或c中至少一个的系统”应包括但不限于单独具有a、单独具有b、单独具有c、具有a和b、具有a和c、具有b和c和/或具有a、b和c的系统等)。本领域技术人员还应当理解,实质上任意表示两个或更多可选项目的转折连词和/或短语,无论是在说明书、权利要求书还是附图中,都应被理解为给出了包括这些项目之一、这些项目任一方或两个项目的可能性。例如,短语“a或b”应当被理解为包括“a”或“b”或“a和b”的可能性。
另外,在以马库什组描述本发明的特征或方面的情况下,本领域技术人员应当认识到,本发明因此也是以该马库什组中的任意单独成员或成员子组来描述的。
本领域技术人员应当理解,出于任意和所有目的,例如为了提供书面说明,本文所揭示的所有范围也包含任意及全部可能的子范围及其子范围的组合。任意列出的范围可以被容易地看作充分描述且实现了将该范围至少进行二等分、三等分、四等分、五等分、十等分等。作为非限制性示例,在此所讨论的每一范围可以容易地分成下三分之一、中三分之一和上三分之一等。本领域技术人员应当理解,所有诸如“直至”、“至少”、“大于”、“小于”之类的语言包括所列数字,并且指代了随后可以如上所述被分成子范围的范围。最后,本领域技术人员应当理解,范围包括每一单独数字。因此,例如具有1-3个单元的组是指具有1、2或3个单元的组。类似地,具有1-5个单元的组是指具有1、2、3、4或5个单元的组,以此类推。
尽管为了达到清晰理解的目的采用图示和示例的方式详细描述了前述发明,但是鉴于本发明的教学意义,对于本领域普通技术人员显而易见的是,在不脱离所附权利要求书的精神或范围的情况下,可对其进行特定的变更和修改。
因此,前述内容仅说明了本发明的原理。应当理解,本领域技术人员将能够设计出各种结构,尽管这里没有明确表述或示出,但这些设计反应了本发明的原理,未超出本发明的精神和范围。此外,本文列举的所有示例和条件语言主要为了帮助读者理解本发明的原理和发明人为进一步拓展本领域所提供的构想,并且应解释为不受这些具体列举的示例和条件的限制。而且,本文中引用本发明的原理、方面和实施例及其特定示例的所有陈述旨在涵盖其在结构和功能上的等同物。此外,所述等同物拟包括目前已知的等同物和日后待开发的等同物,即,开发出的任何功能相同的原件且与结构无关。而且,无论在权利要求书中是否明确叙述了本发明的公开内容,都不会向公众披露其中的任何内容。
因此,本发明的范围并不限于本文中显示和描述的示例性实施例。相反,本发明的范围和精神通过所附权利要求书体现。在权利要求书中,只有当权利要求书的限制内容开头明确使用短语“用于……的手段”或“用于……的步骤”时,《美国法典》第35章第112节(f)或《美国法典》第35章第112节(6)明确定义为被援引;如果权利要求书的限制内容中未使用所述短语,则《美国法典》第35章第112节(f)或《美国法典》第35章第112节(6)未被援引。
- 还没有人留言评论。精彩留言会获得点赞!