由硫化铼制造高铼酸水溶液的方法与流程
本发明涉及由硫化铼制造高铼酸水溶液的方法。特别是本发明涉及由硫化铼经由高铼酸而制造高铼酸铵的方法。
背景技术:
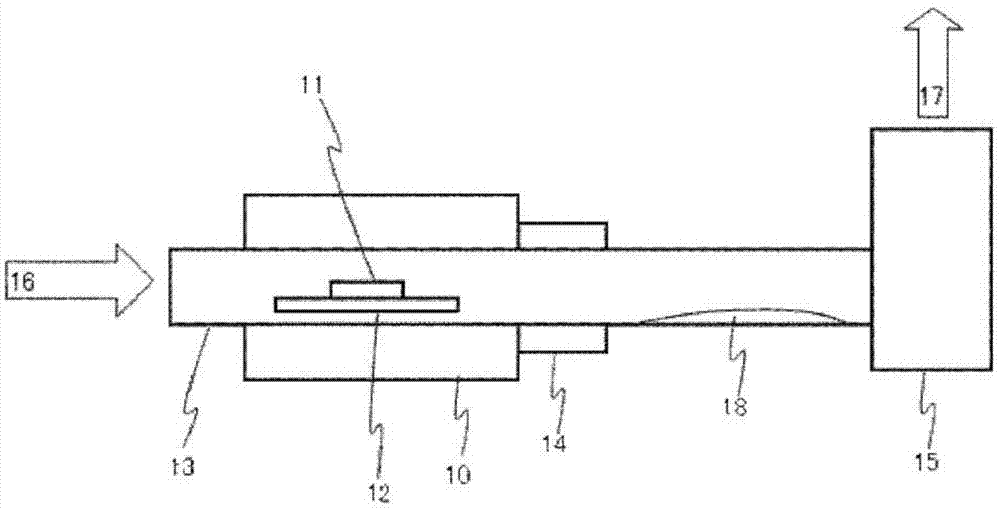
铼是仅伴随钼原矿的辉钼矿和铜矿石的稀有金属,是用于催化剂的添加元素、热电偶和超耐热合金用添加元素、高真空电子管材料等的重要的金属。作为用于工业上回收铼的有前景的原料之一,有粗硫化铼。作为粗硫化铼中的杂质,代表性的是锌、铋等。目前,已知有以日本特开昭62-148327号公报(专利文献1)中记载的方式,由粗硫化铼制造高铼酸钾的方法。在该文献中,使用过氧化氢等氧化剂氧化浸出粗硫化铼,在浸出后液中添加硫化氢,由此在后液中得到纯度高的高铼酸后,添加氢氧化钾而制造高铼酸钾。由高铼酸钾开始,以日本特开平2-20575号公报(专利文献2)中记载的方式,通过在与阳离子交换树脂接触后由氨水中和并过滤的方法等,能够制造高铼酸铵。高铼酸铵作为有价物质可以商业交易,是附加价值高的形态。另外,在日本特开昭47-21323号公报(专利文献3)中记载有一种铼的制造方法,其特征在于,焙烧含铼的钼原矿石并以水萃取,在该萃取液中添加氯化钾,将此时所得到的沉淀溶解在浓硫酸中,将硫酸浓度调节至1~3摩尔以后,使用含有高分子量有机叔胺浓度在0.02摩尔以上的有机溶剂进行萃取,接着用苛性钾水溶液对于该萃取液进行逆萃取,对于该萃取液进行浓缩还原处理。而且,在专利文献3中记载着如下内容,铼以硫化铼的形态含有,通过焙烧,硫化铼被氧化而变成氧化铼(re2o7),在150℃以上的温度下气化而积蓄在烟尘中。还记载若以水萃取烟尘,则氧化铼(re2o7)被吸收到水溶液中,以及由于该水溶液含有大量的二氧化硫和三氧化硫,所以显示出强酸性。现有技术文献专利文献专利文献1:日本特开昭62-148327号公报专利文献2:日本特开平2-20575号公报专利文献3:日本特开昭47-21323号公报发明所要解决的课题按照专利文献1,已知有通过湿式工艺由粗硫化铼制造高铼酸的方法,但也期望提供通过干式工艺由粗硫化铼制造高铼酸的方法。这一点,虽然在专利文献3中记载有:通过焙烧,硫化铼被氧化而变成氧化铼,以及氧化铼在150℃以上的温度下气化,而积蓄在烟尘中,但关于杂质的除去还留有改善的余地。技术实现要素:因此,本发明的课题在于提供一种能够使用干式工艺由硫化铼制造高纯度的高铼酸的方法。本发明人为了解决上述课题而进行深入研究的结果发现,对硫化铼进行两段焙烧的方法是有效的。即,利用第一段焙烧使硫等杂质气化而排出,将铼、锌和铋等作为不挥发成分残留于残渣侧。在第二段的焙烧中,边将锌、铋等不挥发成分作为残渣进行分离,边将铼作为气化后的氧化铼抽出。由此回收的氧化铼的纯度上升。若将得到的氧化铼溶于水中,则可以得到高纯度的高铼酸水溶液。可以理解为本发明除了以包含杂质的硫化铼为对象之外,还能够以实质上不含杂质的高纯度的硫化铼为对象。即,在第一段焙烧中由硫化铼产生硫氧化物,但仅进行一段的焙烧时,该硫氧化物成为杂质混入氧化铼中。但是,通过进行第二段的焙烧能够进一步除去杂质,因此与仅进行一段的焙烧时相比,可以得到硫分少的高纯度的氧化铼。因此,本发明在一方面,是包括如下工序的高铼酸水溶液的制造方法:1)在含氧气体的存在下对硫化铼进行第一焙烧,生成氧化铼和硫氧化物,硫氧化物气化而排出,从而得到氧化铼作为焙烧残渣的工序;2)在含氧气体的存在下对所述焙烧残渣进行第二焙烧,并回收气化后的氧化铼的工序;3)将气化后的氧化铼冷却固化的工序、或者通过一边用水冷却气化后的氧化铼,一边使其溶解于水中,从而得到高铼酸水溶液的工序;4)在将氧化铼固化后的情况下,通过使固化后的氧化铼溶解于水中、或者将固化后的氧化铼加热而气化后溶解于水中,从而得到高铼酸水溶液的工序。本发明在另一方面,是包括如下工序的高铼酸水溶液的制造方法:1)在含氧气体的存在下对含有锌和铋中的至少一种的硫化铼进行第一焙烧,生成氧化铼和硫氧化物,硫氧化物气化而排出,从而得到氧化铼与锌和铋中的至少一种共同作为焙烧残渣的工序;2)在含氧气体的存在下对所述焙烧残渣进行第二焙烧,将锌和铋中的至少一种作为焙烧残渣进行分离,并回收气化后的氧化铼的工序;3)将气化后的氧化铼冷却固化的工序、或者通过一边用水冷却气化后的氧化铼,一边使其溶解于水中,从而得到高铼酸水溶液的工序;4)在将氧化铼固化后的情况下,通过使固化后的氧化铼溶解于水中、或者将固化后的氧化铼加热而气化后溶解于水中,从而得到高铼酸水溶液的工序。在本发明的高铼酸水溶液的制造方法的一个实施方式中,当焙烧残渣中的s品位在0.5~20质量%的范围内时结束第一焙烧。在本发明的高铼酸水溶液的制造方法的另一实施方式中,第一焙烧在100~350℃的炉内气氛温度下进行。在本发明的高铼酸水溶液的制造方法的又一实施方式中,第二焙烧在200~600℃的炉内气氛温度下进行。在本发明的高铼酸水溶液的制造方法的又一实施方式中,在第一焙烧和第二焙烧中,含氧气体被预热到100℃以上。在本发明的高铼酸水溶液的制造方法的又一实施方式中,将气化后的氧化铼冷却固化的工序在伴随的硫氧化物保持在气体状态的条件下进行,从而硫氧化物被固气分离。在本发明的高铼酸水溶液的制造方法的又一实施方式中,在将气化后的氧化铼冷却固化的工序中,固化后的氧化铼被回收到铼酸不溶性的材料上。本发明在另一方面,是将通过本发明的高铼酸水溶液的制造方法得到的高铼酸水溶液作为原料,制造高铼酸钾的方法。本发明在另一方面,是将通过本发明的高铼酸水溶液的制造方法得到的高铼酸水溶液作为原料,制造高铼酸铵的方法。本发明在另一方面,是将通过本发明的高铼酸水溶液的制造方法得到的高铼酸水溶液作为原料,制造铼金属的方法。发明效果根据本发明,提供一种能够由硫化铼制造高纯度的高铼酸的干式工艺。本发明能够归入由硫化铼制造高铼酸铵的方法中。附图说明图1是在实施例的第二段焙烧中使用的焙烧设备的示意图。具体实施方式在本发明的高铼酸水溶液的制造方法的一个实施方式中,包括如下工序:1)在含氧气体的存在下对硫化铼进行第一焙烧,生成氧化铼和硫氧化物,硫氧化物气化而排出,从而得到氧化铼作为焙烧残渣的工序;2)在含氧气体的存在下对所述焙烧残渣进行第二焙烧,并回收气化后的氧化铼的工序;3)将气化后的氧化铼冷却固化的工序、或者通过一边用水冷却气化后的氧化铼,一边使其溶解于水中,从而得到高铼酸水溶液的工序;4)在将氧化铼固化后的情况下,通过使固化后的氧化铼溶解于水中、或者将固化后的氧化铼加热而气化后溶解于水中,从而得到高铼酸水溶液的工序。在本发明的高铼酸水溶液的制造方法的另一实施方式中,包括如下工序:1)在含氧气体的存在下对含有锌和铋中的至少一种的硫化铼进行第一焙烧,生成氧化铼和硫氧化物,硫氧化物气化而排出,从而得到氧化铼与锌和铋中的至少一种共同作为焙烧残渣的工序;2)在含氧气体的存在下对所述焙烧残渣进行第二焙烧,将锌和铋中的至少一种作为焙烧残渣进行分离,并回收气化后的氧化铼的工序;3)将气化后的氧化铼冷却固化的工序、或者通过一边用水冷却气化后的氧化铼,一边使其溶解于水中,从而得到高铼酸水溶液的工序;4)在将氧化铼固化后的情况下,通过使固化后的氧化铼溶解于水中,或者将固化后的氧化铼加热而气化后溶解于水中,从而得到高铼酸水溶液的工序。(硫化铼)本发明中,作为处理对象的硫化铼可以是不含杂质的硫化铼,也可以是含有杂质的粗硫化铼。代表性的是含有锌和铋的至少一种的粗硫化铼,更具代表性的是含有两种的粗硫化铼。在本发明中,所谓“硫化铼”是指含有杂质的粗硫化铼和实质上不含杂质的硫化铼的两者。粗硫化铼的来源不受限制,作为典型例可以列举来源于以下的粗硫化铼。在对于从铜等有色金属的冶炼工序中产生的二氧化硫进行水清洗而得到的废酸中,原矿石中所含的铼与杂质一起混入。在这样的废酸中,通常包含铼、铋、锌、汞、砷、铁、铜等。废酸中的铼以铼酸(hreo4)的形态存在。通过使废酸中的铼与硫化氢反应生成硫化铼,因此能够通过固液分离作为粉体回收。此时,因为锌和铋与硫化氢不发生反应,所以能够分离到液体侧。为了成为杂质少的硫化铼,也可以通过以下这样的方法除去杂质。例如,可以在螯合树脂和强碱性阴离子交换树脂这样的对于汞的吸附力强的树脂中通过废酸,由此进行脱汞。另外,使脱汞后的废酸在阴离子交换树脂中流通,使该树脂选择性地吸附废酸中的铼和铋,从而能够除去未吸附于树脂的砷、铁和铜。在吸附有铼和铋的阴离子交换树脂中流通盐酸等洗脱液,能够使铼和铋从阴离子交换树脂中洗脱。从铼中分离铋可以由色谱法进行。在代表性的实施方式中,根据化学分析(汞以外通过icp-oes进行分析,汞通过还原气化吸光光度法进行分析。),在粗硫化铼中含有铼:30~62质量%、硫:20~38质量%、锌:0.01~1.0质量%、铋:0.01~1.0质量%、汞:0.01~1.0质量%,在更具代表性的实施方式中,在粗硫化铼中,含有铼:35~50质量%、硫:25~32质量%、锌:0.01~0.5质量%、铋:0.01~0.7质量%、汞:0.01~0.7质量%。铼也有一部分作为氧化铼存在的情况。(工序1)在工序1中,在含氧气体的存在下对硫化铼进行第一焙烧,生成氧化铼和硫氧化物,硫氧化物气化而排出,从而得到氧化铼作为焙烧残渣。另外,在硫化铼中包含锌和铋中的至少一种的情况下,优选将这些与氧化铼同时回收于焙烧残渣中。作为用于实施焙烧的炉的种类没有特别限制,可列举窑炉、流动床炉、管状炉等,但由于有基于旋转的搅拌作用且与氧的反应效率高,因而更优选窑炉。可以认为在第一焙烧中,硫化铼遵循以下的反应式转换为氧化铼。re2s7(s)+21/2o2→re2o7(s)+7so2(g)···(式1)so2(g)+1/2o2(g)→so3(g)在第一焙烧中,由于以使生成的硫氧化物气化、并从氧化铼中分离为目的,因此从杂质的除去效率和铼回收效率的观点出发,优选一边使硫氧化物气化用气体管道等排出到炉外,一边在不使氧化铼气化而留在炉内的条件下实施焙烧。即,若加热温度变得过高,则由于气化而损失的氧化铼的比率变高,另一方面,若加热温度过低,则副生成的硫氧化物的除去率降低。需要说明的是,在硫化铼中作为杂质含有汞、砷的情况下,这些也可以同样地利用第一焙烧进行除去处理。根据本发明人的讨论结果,通过在焙烧残渣中的s品位优选为0.5~20质量%的范围时,更优选为0.5~10质量%的范围时,进一步优选为0.5~5质量%时结束第一焙烧,能够边有效地除去杂质边得到高的铼回收率。为了将这样的焙烧残渣中的s品位收入上述范围内,优选将焙烧炉的气氛温度设为100~350℃进行第一焙烧,更优选将焙烧炉的气氛温度设为200~350℃进行第一焙烧。另外,作为焙烧时间,与焙烧炉的规模和结构也相关,若过长则铼的气化进一步发生,另一方面,若过短则氧化反应不会充分发生,因此例如可以设为30~240分钟,优选设为120~180分钟。另外,为了在气氛温度急剧上升时抑制反应,优选预先能够向炉内供给氮、氩等不活泼气体。作为含氧气体,可列举氧、空气、氧与不活泼气体的混合物等,但由于成本升高,所以优选为空气。在此所说的含氧气体中,除了最初以气体存在的含氧气体以外,还包括通过使用在加热时会产生氧这样的固体和液体(例如,氯酸钾、高氯酸铵)而产生的含氧气体。从反应效率的观点出发,优选含氧气体供给上述(式1)所需要的理论当量以上的氧,例如可以为1.2以上,更优选为1.8以上。优选在将含氧气体供给至焙烧炉前进行预热。通过预热含氧气体,能够低温设定焙烧炉的内壁温度,能降低氧化铼的气化率。即,在不预热含氧气体的情况下,由于热传递的问题,必须预先提高为了在含氧气体与硫化铼的界面达到氧化反应充分进行的温度所需要的焙烧炉的内壁温度的设定值。这是焙烧炉的内壁温度变成氧化反应中本来需要的以上的温度,而内壁附近的氧化铼发生气化。另一方面,通过预热含氧气体,无需过度地提高焙烧炉的内壁温度,能够抑制氧化铼的气化。从上述的观点来看,优选将含氧气体预热到与炉内气氛温度相同的温度。但是,若过度地进行预热则造成能量的损耗。(工序2)在工序2中,在含氧气体的存在下对工序1中得到的焙烧残渣进行第二焙烧,并回收气化后的氧化铼。在焙烧残渣中包含锌和铋中的至少一种的情况下,优选将这些作为焙烧残渣从氧化铼分离。用于实施第二焙烧的炉的种类与第一焙烧同样没有特别限制,可列举窑炉、流动床炉、管状炉等,但出于减少残渣的飞散造成的回收时的污染和费用的理由,优选管状炉。可以将焙烧残渣从第一焙烧中使用的炉中暂时取出,用其它焙烧炉实施第二焙烧,也可以使用与第一焙烧同样的焙烧炉。从抑制污染的观点出发,优选使用其它焙烧炉。在使用同一焙烧炉的情况下,在得到高纯度的氧化铼方面,优选通过将反应管等反应容器装入炉内,在第一焙烧结束后,冷却至室温而取出残渣并转移至其它反应容器,然后返回炉内实施第二焙烧,从而防止污染。由于在第二焙烧中具有使氧化铼积极地气化的目的,通常将焙烧炉的炉内气氛温度设定为比第一焙烧更高的温度来实施。但是,若设定为过高的温度,则有可能锌分、铋分也气化,因此优选将焙烧炉的气氛温度设为200~600℃进行第二焙烧,更优选设为300~550℃进行第二焙烧,进一步优选将焙烧炉的气氛温度设为350~500℃进行第二焙烧。另外,作为焙烧时间,与焙烧炉的规模和结构有关,若过长则能量损耗变大,另外方面,若过短则未挥发部分变多,因此优选设为例如30~240分钟,更优选设为120~180分钟。若在第一焙烧中硫化铼的氧化反应和硫氧化物的除去充分完成,则第二焙烧中所需要的气氛气体只要能发挥作为用于输送气化后的氧化铼的载气的作用就已充分。但是,第一焙烧中的硫化铼的氧化反应和硫氧化物的除去还有不完全的可能性,因此在本发明中的第二焙烧中也使用含氧气体。在第二焙烧中,也优选将含氧气体在供给至焙烧炉前进行预热。通过预热含氧气体,能够得到炉内反应的均匀化的优点。气化后的氧化铼的输送使用气体管道即可。另外,在使用同样焙烧炉的情况下,从防止杂质的混入的观点出发,优选将利用与第一焙烧时的气体管道不同的气体管道气化后的氧化铼回收。优选气体管道保温,防止氧化铼在输送途中粘着于管道内壁。若保温时的管道内温度过低,则氧化铼有可能发生固化,因此优选为300℃以上,从能量消耗的观点出发,也不需要过度地提高温度,因此代表性的是在500℃以下,更有代表性的是400℃以下。(工序3)然后,可以将气化后的氧化铼冷却使其固化。此时,在提高氧化铼的纯度的方面,优选通过一边使伴随气化后的氧化铼的硫氧化物保持气体状态,一边将氧化铼冷却固化,由此将硫氧化物固气分离。在提高作业效率方面优选在规定的冷却场所(可以在管道内,也可以在有出入口的容器内。)进行冷却而使其固化。此时,伴随的硫氧化物由于沸点差异,保持该状态作为气体穿过冷却场所,因此通过固气分离,氧化铼的纯度提高。从防止污染的观点出发,优选固化后的氧化铼回收到铼酸不溶性的材料、石英或玻璃上,能够回收到内壁的材质为石英的管道内和容器内。固气分离时,为了提高铼的回收率,也可以设置过滤器。冷却可列举自然放冷、基于热交换的方法等,但出于装置的简略化的理由,优选实施自然放冷的方法。通过冷却到100℃以下,优选冷却到80℃以下,能够使氧化铼完全地固化。若过于低温,则有可能连同与氧化铼一起从焙烧炉中流出的硫氧化物也都液化或固化而被回收,因此,为了将硫氧化物完全除去,优选冷却至so3的沸点即50℃以上的温度,通常来说,产生的硫氧化物的形态为so2,因此也可以冷却至作为so2的沸点以上的常温(例:5~30℃)。作为其他方法,还可以通过边用水冷却气化后的氧化铼边使其溶解于水中,从而直接获得高铼酸水溶液。此时的反应式与工序4中说明的相同。作为边用水冷却边溶解于水中的方法,可列举用湿式洗涤器收集从焙烧炉排出的气化后的氧化铼的方法、利用湿式过滤、湿式电集尘机的方法。在使用湿式洗涤器的情况下,为了增大气液接触面积优选装入颗粒状、筒状或蜂窝状等的填充物。该方法不经过将氧化铼固化的工序因此是简便性高的方法,因为连同与氧化铼一起的硫氧化物也溶解在水中,所以从纯度的观点出发,比将氧化铼固化的方法差。举例来说,使氧化铼溶解到水中的方法与使氧化铼固化的方法相比,高铼酸水溶液中的s品位增加5~10倍左右。(工序4)在使氧化铼固化的情况下,在工序4中,通过使固化后的氧化铼溶解于水中、或者将固化后的氧化铼加热而气化后溶解于水中,得到高铼酸水溶液。可以认为氧化铼遵循以下的反应式转换成高铼酸。re2o7(s或g)+h2o(1)→2hreo4(1)···(式2)氧化铼容易溶解于水,但若水溶液中的浓度过高,则认为反应效率降低。另一方面,若浓度过低,则水使用量增加,操作时的操作性劣化,其后需要浓缩工序。因此,优选氧化铼向水中的投入量为50~500g/l,更优选为150~250g/l。通过使固化后的氧化铼进行固液接触而溶解在水中的方法是简便的方法,也可以是将固化后的氧化铼加热而再度气化后,用洗涤器等进行气液接触而溶解在水中的方法。但是,因为这一方法会发生未回收损失,所以更优选前者的方法。由高铼酸水溶液出发,通过公知的任意的方法,能够制造高铼酸钾,此外还能够制造高铼酸铵。例如,能够在高铼酸水溶液中添加氢氧化钾,将ph调整到11~13左右,使高铼酸钾析出,通过固液分离将其回收。另外,因为高铼酸钾重,容易沉淀,所以优选将容易上浮的杂质分离之后再进行固液分离。另外,也能够通过淘洗等提高纯度。通过用氢等还原高铼酸钾,能够制造金属铼(例如,参照日本特开昭62-124240号公报)。另外,还能够在高铼酸水溶液中添加氨水,将ph调整到7~12左右,使高铼酸铵析出,通过固液分离制造高铼酸铵。通过反复提纯,可以使纯度进一步提高。作为提纯方法,可列举例如进行向纯水的再溶解和结晶析出的方法。中和后,优选在固液分离之前加热至90~105℃进行浓缩。通过以氢等还原高铼酸铵,能够制造金属铼(例如,参照日本特开昭62-146227号公报)。实施例以下,说明本发明的实施例,但实施例是例示为目的,并不意在限定发明。(第一焙烧带来的效果的验证)准备具有表1中记载的分析值的粗硫化铼。各成分的含有率通过化学分析(由icp-oes进行分析。)进行测定。【表1】对于该粗硫化铼500g,以各种窑炉气氛温度条件进行120~140分钟第一焙烧,随后炉冷至室温。作为焙烧炉使用窑炉,作为含氧气体使用空气。任何一例的氧当量均为1.9~2.2的范围。另外,可知将空气预热而达到规定温度(在此为140℃。)之后供给到窑炉的话,炉内气氛温度稳定,硫的挥发率有上升的倾向。测定试验后的残渣的重量,并实施该残渣的化学分析。根据残渣的重量和各元素分析结果,求得各元素的含量(g),由试验前后的含量(g)的差求得气化率。焙烧时间是窑炉内的气氛温度到达规定的温度之后至开始冷却的时间。氧当量是将粗硫化铼所含的铼和硫假定为re2s7或以氧化物以外的形态存在,至全部的铼反应至re2o7、以及全部的硫反应至so3的理论氧当量作为1进行计算。其结果是,窑炉气氛温度为100℃以上且低于200℃时,re的气化率为10%以上且低于20%左右,窑炉气氛温度为200℃以上时,re的气化率为20%以上,若窑炉气氛温度超过350℃,则re的气化率超过40%。对于s的气化率而言,窑炉气氛温度为100℃以上时为10%以上,在300℃以上时为80%以上。需要说明的是,对于zn和bi的气化率而言,在窑炉气氛温度低于600℃时,实质上为0%。(两段焙烧带来效果的验证:将气化后的氧化铼固化后制造高铼酸水溶液的情况)准备具有表3中记载的分析值的粗硫化铼。各成分的含有率通过化学分析(通过icp-oes进行分析。)进行测定。【表2】对于该粗硫化铼150g,在表3-1中记载的条件下进行第一焙烧,随后炉冷至室温。作为焙烧炉使用管状炉,作为含氧气体使用空气。与上述的例子同样地,求出s气化率、焙烧残渣中的s品位、re气化率、zn气化率、bi气化率。结果示于表3-2中。【表3-1】【表3-2】接着,对于第一焙烧中得到的残渣133g,在表4-1中记载的条件下使用图1中的焙烧设备进行第二焙烧。作为焙烧炉使用与第一焙烧不同的管状炉10,以1.5l/min的流量供给空气16。含有气化后的氧化铼的成分在保温于300℃的管状炉外部反应管保温部14中,以气化的状态输送一定距离后,在内壁为石英制的反应管13的未保温的部分被冷却,作为固体状的氧化铼18析出。需要说明的是,气体温度是在从保温部到洗涤器的途中冷却至室温(约30℃)的状态。从反应管出来的气体在洗涤器15吸收硫氧化物,从而使气体无害化而排出。取下有氧化铼18析出的反应管13,使常温的水在反应管13内流通而溶解氧化铼,得到高铼酸水溶液。通过化学分析(通过icp-oes进行分析。)测定所得到的高铼酸水溶液中的各成分浓度,求出以第二焙烧前的残渣为基准(100%)时的各成分的回收率。结果示于表4-2和表4-3中。【表4-1】【表4-2】s回收率re回收率zn回收率bi回收率1.6%80.4%0.3%0%【表4-3】对于得到的高铼酸水溶液,添加氨水使ph达到9而进行中和,随后通过固液分离得到高铼酸铵(apr)的粉末。高铼酸铵的分析结果示于表5中。分析通过gdms进行。可知能够得到高纯度的高铼酸铵。【表5】(比较例)准备具有表6中记载的分析值的粗硫化铼。通过化学分析(通过icp-oes进行分析。)测定各成分的含有率。【表6】对于该粗硫化铼531g,以表7-1中记载的条件使用图1中记载的焙烧设备进地焙烧。随后炉冷至室温。作为焙烧炉使用管状炉10,作为含氧气体,以1.5l/min的流量供给空气16。与上述的例子同样,求出s气化率、焙烧残渣中的s品位、re气化率、zn气化率、bi气化率。结果示于表7-2中。【表7-1】【表7-2】接着,含有气化后的氧化铼的成分在保温于300℃的管状炉外部反应管保温部14中,以气化的状态输送一定距离后,在内壁为石英制的反应管13的不保温的部分被冷却,作为固体状的氧化铼18析出。还有,气体温度从保温部至洗涤器的途中成为被冷却至室温(约30℃)的状态。从反应管出来的气体由洗涤器15吸收硫氧化物,使气体无害化地排出。取下有氧化铼18析出的反应管13,使常温的水在反应管13内流通而溶解氧化铼,得到高铼酸水溶液。通过化学分析(由icp-oes进行分析。)测定所得到的高铼酸水溶液中的各成分浓度,求得以粗硫化铼中的浓度为基准(100%)时的各成分的回收率。结果示于表8-1和表8-2中。【表8-1】s回收率re回收率低于1%70%以上【表8-2】对于得到的高铼酸水溶液,添加氨水使ph达到9而进行中和,随后通过固液分离得到高铼酸铵(apr)的粉末。高铼酸铵的分析结果示于表9中。分析通过gdms进行。【表9】符号说明10管状炉11试样12试样放置处13反应管14反应管保温部15洗涤器16空气17排气18氧化铼当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1