一种提高恩拉霉素B组分产量的发酵培养基及发酵方法与流程
本发明涉及微生物发酵领域,具体地说,涉及一种提高恩拉霉素B组分产量的发酵培养基及发酵方法。
背景技术:
恩拉霉素为多肽类抗生素,它可以阻止黏肽的合成,使细胞壁缺损,导致细胞内渗透压升高,细胞外液渗入菌体,使细菌变形、肿大、破裂而死亡。恩拉霉素对革兰氏阳性菌有很强的活性,特别是对肠道内的有害梭菌有很强的抑杀作用,还可通过抑制肠道中有害细菌的生长繁殖来改变肠道内的菌群平衡。长期使用恩拉霉素,细菌对其不易产生耐药性,与其他抗生素之间也不产生明显交叉耐药。恩拉霉素在饲料中稳定性很高,在室温条件下长期储藏也很少降解,制成颗粒料稳定性更高,与饲料混合后在室温下长期储藏效价下降甚微。最为重要的是,恩拉霉素在消化道内不被各种酶类降解,能保持原有的抗菌活性。恩拉霉素由不同种类的氨基酸和不饱和脂肪酸分子组成,其中氨基酸分子构成环状多肽结构,脂肪酸位于多肽结构末端。根据其末端脂肪酸种类不同,分为恩拉霉素A(C107H138C12N26O31)和恩拉霉素B(C108H140C12N26O31),恩拉霉素则是由这两种成分组成的混合物。
然而,现有技术中恩拉霉素的产量较低,因此,需要一种能够提高恩拉霉素产量的发酵培养基。
技术实现要素:
为了解决现有技术中存在的问题,本发明的目的是提供一种提高恩拉霉素B组分产量的发酵培养基及发酵方法。
为了实现本发明目的,本发明首先提供一种提高恩拉霉素B组分产量的发酵方法,利用杀真菌素链霉菌在发酵培养基中发酵生产恩拉 霉素,所述发酵培养基中添加有复合维生素。
所述复合维生素为市售可得的产品,在本发明的具体实施方式中,所述复合维生素使用颐康金维牌多维元素片(昆明制药集团股份有限公司生产)。
进一步地,所述复合维生素的含量为0.5-1g/L。
更进一步地,所述发酵培养基包括以下含量的成分:8-10g/L的玉米淀粉,10-13g/L的葡萄糖,0.2-0.3g/L的磷酸氢二钾,1-1.5g/L的七水硫酸镁,12-15g/L的氯化钠,2-2.2g/L的碳酸钙。
所述发酵培养基的pH为7.2。
本发明还提供了一种提高恩拉霉素B组分产量的发酵培养基,所述发酵培养基包括以下含量的成分:8-10g/L的玉米淀粉,10-13g/L的葡萄糖,0.2-0.3g/L的磷酸氢二钾,1-1.5g/L的七水硫酸镁,12-15g/L的氯化钠,2-2.2g/L的碳酸钙,0.5-1g/L的复合维生素。
进一步地,所述发酵培养基的制备方法为:
将玉米淀粉、葡萄糖、磷酸氢二钾、七水硫酸镁、氯化钠碳酸钙和复合维生素溶解于蒸馏水中,得到含量分别为10g/L玉米淀粉,13g/L葡萄糖,0.2g/L磷酸氢二钾,1g/L七水硫酸镁,15g/L氯化钠,2.2g/L碳酸钙,0.5-1g/L复合维生素的培养基;pH值为7.2,棉塞封口后再用牛皮纸包扎,121℃灭菌30min。
本发明的有益效果在于:
本发明通过在培养基中添加适量的复合维生素,显著提高了杀真菌素链霉菌发酵产生的恩拉霉素B组分的产量。
附图说明
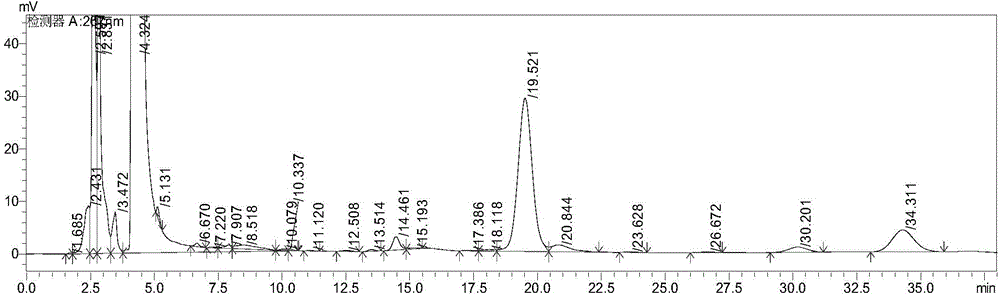
图1为本发明实施例3所述的高效液相色谱图;
图2为本发明对比例1所述的高效液相色谱图。
具体实施方式
以下实施例用于说明本发明,但不用来限制本发明的范围。
实施例1培养基的制备
1、原料
10g玉米淀粉,13g葡萄糖,0.3g磷酸氢二钾,1.5g七水硫酸镁,15g氯化钠,2.2g碳酸钙,1g复合维生素(颐康金维牌多维元素片,昆明制药集团股份有限公司生产),蒸馏水。
2、制备方法
将玉米淀粉、葡萄糖、磷酸氢二钾、七水硫酸镁、氯化钠碳酸钙和复合维生素溶解于蒸馏水中,得到各成分含量如下的培养基:10g/L玉米淀粉,13g/L葡萄糖,0.2g/L磷酸氢二钾,1g/L七水硫酸镁,15g/L氯化钠,2.2g/L碳酸钙,0.5-1g/L复合维生素。调节pH值为7.2,棉塞封口后再用牛皮纸包扎,121℃灭菌30min。
实施例2培养基的制备
1、原料
8g玉米淀粉,10g葡萄糖,0.2g磷酸氢二钾,1g七水硫酸镁,12g氯化钠,2g碳酸钙,0.5g复合维生素。
2、制备方法
将玉米淀粉、葡萄糖、磷酸氢二钾、七水硫酸镁、氯化钠碳酸钙和复合维生素溶解于蒸馏水中,得到各成分含量如下的培养基:8g/L玉米淀粉,10g/L葡萄糖,0.2g/L磷酸氢二钾,1g/L七水硫酸镁,12g/L氯化钠,2g/L碳酸钙,0.5g/L复合维生素。调节pH值为7.2,棉塞封口后再用牛皮纸包扎,121℃灭菌30min。
实施例3发酵生产恩拉霉素
1、杀真菌素链霉菌的培养
杀真菌素链霉菌(Streptomyces fungicidius)BJX002,其保藏号为CGMCC No.6026,以10%的接种量接种于装有实施例1所述培养基的发酵瓶中,在28℃、200r/min条件下培养200h,然后获得发酵浸提液,进行下一步提取。
2、发酵生产恩拉霉素B
2.1提取方法如下:
(1)发酵结束后取2ml发酵液,加入盛有9ml甲醇的10ml磨口比色管中,超声波超声20min,以4000rpm的速度离心10min,取上清溶液,共得到9.2-9.4ml上清。
(2)取1ml上清,以0.45μm的有机相微孔滤膜过滤,获得发酵浸提液,待测。
2.2HPLC分析:
采用岛津LC-10A型高效液相色谱仪,250mm×4.6mm(i d)不锈钢柱,内填Reliasil Cl8型号为Wondasil的C18反相柱,柱温35℃,取步骤(2)的发酵浸提液,进样量20μl;以磷酸缓冲盐(pH8.2):乙腈(体积比为7:3)为流动相进行分离,流速为1ml/min,利用UV检测器在波长267nm处检测并自动形成分离图谱。
色谱结果如图1所示。
对比例1
本对比例实验方法同实施例3,区别在于,本对比例所使用的发酵培养基未添加复合维生素。
色谱结果如图2所示。
通过比较图1和图2可以看出,色谱结果显示在19.5min左右出现的峰值为恩拉霉素A组分,且添加复合维生素对其合成几乎没有影响,含量均约为4650mg/mL。但在34.4min左右出现的峰值有所增加,发酵滤液中恩拉霉素B组分保留时间为34.311min左右,根据洗脱峰面积,计算未加复合维生素时恩拉霉素B组分的含量为4986mg/mL。加有复合维生素时恩拉霉素B组分的含量为5630mg/mL。
可见,与实施例3相比,添加了复合维生素的培养基发酵生产的恩拉霉素B组分的产量提高了13%,虽对A组分的产量未产生明显影响,但恩拉霉素的总量由于B组分的提高,明显得到了显著的提高。
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!