用于生产4‑叠氮基磺酰基邻苯二甲酸酐的方法与流程
背景技术:
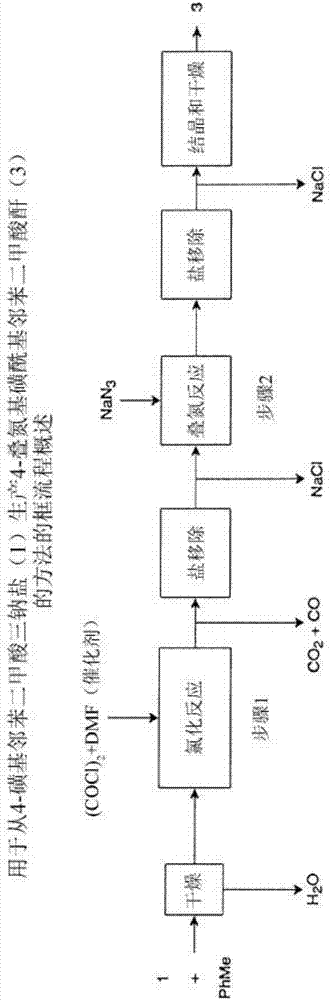
:与叠氮基磺酰基邻苯二甲酸酐(aspa)接枝的聚烯烃已知为用于粘结层应用的有效组合物。然而,aspa的商业供应受到限制、不可靠并且难以获得。因此,本领域认识到对于aspa的可靠的、一致的、高效的和经济生产-并且特别是aspa的商业规模生产的额外来源和/或额外合成程序的需要。技术实现要素:本发明提供用于生产4-叠氮基磺酰基邻苯二甲酸酐或aspa的独特合成路径。本文公开的方法特别有利于aspa的商业生产,这是因为由此提供的效率(即,就能量、成本、时间、生产率、设备和/或可易于获得的起始反应剂而言的效率)。供应可靠的aspa有利地简化由与aspa接枝的聚烯烃制成的粘结层的生产。本发明提供一种用于生产4-叠氮基磺酰基邻苯二甲酸酐的方法。在实施例中,提供方法且该方法包括在溶剂反应条件下使4-磺基邻苯二甲酸三钠盐(1)氯化,以形成溶解的4-氯磺酰基邻苯二甲酸酐(2)和不可溶的氯化钠。方法包括从溶解的4-氯磺酰基邻苯二甲酸酐中第一移除不可溶的氯化钠,以形成经分离的4-氯磺酰基邻苯二甲酸酐。方法包括在溶剂反应条件下使经分离的4-氯磺酰基邻苯二甲酸酐与叠氮化钠反应,以形成溶解的4-叠氮基磺酰基邻苯二甲酸酐和不可溶的氯化钠。方法包括从溶解的4-叠氮基磺酰基邻苯二甲酸酐中第二移除不可溶的氯化钠,以形成经分离的4-叠氮基磺酰基邻苯二甲酸酐。方法包括从经分离的4-叠氮基磺酰基邻苯二甲酸酐中获取固体4-叠氮基磺酰基邻苯二甲酸酐(3)。本发明的优点是用于大规模生产或商业规模生产aspa的方法。本发明的优点是aspa的简单的、有时效的和/或有成本效益的生产方法。附图说明图1是根据本发明的实施例的方法的反应流程。图2是根据本发明的实施例的方法的框流程图。图3是根据本发明的实施例的4-氯磺酰基邻苯二甲酸酐的1hnmr谱图。图4是根据本发明的实施例的4-叠氮基磺酰基邻苯二甲酸酐的1hnmr谱图。图5是根据本发明的实施例的4-叠氮基磺酰基邻苯二甲酸酐的1hnmr谱图。图6是根据本发明的实施例的4-叠氮基磺酰基邻苯二甲酸酐的13cnmr谱图。定义本文中对元素周期表的所有提及应指的是由crc出版公司(crcpress,inc.)2003年出版并且版权所有的元素周期表。另外,对一个或多个族的任何提及应是使用编号族的iupac系统的在此元素周期表中反映的一个或多个族。除非规定为相反、由上下文暗示或本领域惯用,否则所有份数以及百分比均按重量计。出于美国专利实务的目的,本文中所提及的任何专利、专利申请案或公开案的内容都以全文引用的方式并入(或其等效美国版本如此以引用的方式并入),尤其在本领域中的合成技术、定义(在不与本文中提供的任何定义不一致的程度上)和常识的公开内容方面。本文公开的数值范围包括从下限值至上限值所有值并且包括下限值和上限值。对于含有确切值的范围(例如1或2,或3到5或,6或7),任何两个确切值之间的任何子范围都包括在内(例如1到2;2到6;5到7;3到7;5到6等)。如本文所用,术语“组合物”包括包含该组合物的材料的混合物以及由组合物的材料形成的反应产物和分解产物。术语“包含”、“包括”、“具有”和其衍生词并非旨在排除任何额外组分、步骤或程序的存在,无论是否具体地公开。为了避免任何疑问,除非相反说明,否则通过使用术语“包含”所要求的所有组合物都可包括任何额外添加剂、佐剂或化合物,无论聚合或以其它方式。相比之下,术语“基本上由……组成”从任何随后叙述的范围中排除任何其它组分、步骤或程序,除了对可操作性来说不是必不可少的那些之外。术语“由……组成”排除未具体界定或列举的任何组分、步骤或程序。如本文所用,术语“乙烯类聚合物”是包含大多数重量百分比聚合的乙烯单体(以可聚合单体的总量计)并且任选地可包含至少一种聚合的共聚单体的聚合物。术语“聚合物”是通过聚合相同或不同类型的单体而制备的大分子化合物。“聚合物”包括均聚物、共聚物、三元共聚物、互聚物等。术语“互聚物”意指通过聚合至少两种类型的单体或共聚单体而制备的聚合物。其包括但不限于共聚物(其通常是指由两种不同类型的单体或共聚单体制备的聚合物)、三元共聚物(其通常是指由三种不同类型的单体或共聚单体制备的聚合物)、四元共聚物(其通常是指由四种不同类型的单体或共聚单体制备的聚合物)等。术语“聚烯烃”是以聚合物的总重量计含有呈聚合形式大多数重量百分比的烯烃(例如乙烯或丙烯)的聚合物。聚烯烃的非限制性实例包括乙烯类聚合物和丙烯类聚合物。如本文所用,术语“丙烯类聚合物”是包含大多数重量百分比聚合的丙烯单体(以可聚合单体的总量计)并且任选地可包含至少一种聚合的共聚单体的聚合物。具体实施方式本发明涉及4-叠氮基磺酰基邻苯二甲酸酐(或“aspa”)的生产。发现aspa是用于粘结层的烯烃类树脂中的有效接枝组分。本文公开的方法有利地为aspa提供经济的(时间、能量、生产率和/或起始试剂经济)、简化的、可扩展的合成途径与对其商业/工业应用上可接受的产率。aspa的可靠生产相应地促进与aspa接枝的烯烃类聚合物(用作粘结层的组合物)的可靠和经济生产。本发明提供方法。在实施例中,提供方法且该方法包括在溶剂反应条件下使4-磺基邻苯二甲酸三钠盐(1)氯化,以形成溶解的4-氯磺酰基邻苯二甲酸酐(2)和不可溶的氯化钠。如本文所用,“溶剂反应条件”是温度、压力、反应物浓度、溶剂选择、反应物混合/添加参数,和/或在反应容器内促进反应剂之间的反应和所得产品的形成的其它条件。反应处于液相中。将不可溶的氯化钠从溶解的4-氯磺酰基邻苯二甲酸酐中移除,以形成经分离的4-氯磺酰基邻苯二甲酸酐。方法包括在溶剂反应条件下使溶解的4-氯磺酰基邻苯二甲酸酐(2)与叠氮化钠反应,以形成反应产物,即溶解的4-叠氮基磺酰基邻苯二甲酸酐(3)和不可溶的氯化钠。方法包括从溶解的4-叠氮基磺酰基邻苯二甲酸酐中(第二)移除不可溶的氯化钠,以形成经分离的4-叠氮基磺酰基邻苯二甲酸酐(3)。方法包括从溶解的4-叠氮基磺酰基邻苯二甲酸酐中获取固体4-叠氮基磺酰基邻苯二甲酸酐(3)。方法的示意性表示示出在图1和2中。方法利用4-磺基邻苯二甲酸三钠盐(1)作为起始材料。4-磺基邻苯二甲酸三钠盐(1)的结构示出在图1中。在实施例中,在氯化之前,方法包括获得(或另外提供)4-磺基邻苯二甲酸三钠盐和三钠盐异构体的混合物。方法包括从4-磺基邻苯二甲酸三钠盐和三钠盐异构体的混合物中移除残余水。水通过使4-磺基邻苯二甲酸三钠盐和三钠盐异构体进行干燥(或预干燥)步骤来移除,以形成4-磺基邻苯二甲酸三钠盐(1)。可替代地,将4-磺基邻苯二甲酸三钠盐和三钠盐异构体添加至甲苯和水溶液,并且进行移除残余水的共沸共蒸馏,以形成4-磺基邻苯二甲酸三钠盐(1)。方法包括在溶剂反应条件下使4-磺基邻苯二甲酸三钠盐(1)氯化,以形成溶解的4-氯磺酰基邻苯二甲酸酐(2)和不可溶的氯化钠。4-氯磺酰基邻苯二甲酸酐(2)的结构示出在图1中。术语“使氯化”或“氯化”是指将氯引入到有机化合物中。通过与氯化剂反应发生氯化。合适的氯化剂的非限制性实例包括乙二酰氯[(cocl)2]、亚硫酰二氯(socl2)、五氯化磷(pcl5)、三氯化磷(pcl3)和磷酰氯(pocl3)。在实施例中,氯化通过在甲苯溶剂中并且在催化n,n-二甲基甲酰胺(dmf)存在下使4-磺基邻苯二甲酸三钠盐与乙二酰氯(cocl)2反应来实现。氯化还形成氯化钠作为在甲苯溶剂中不可溶的沉淀。在甲苯溶剂中,4-氯磺酰基邻苯二甲酸酐(2)保持可溶,或以其他方式溶解。在实施例中,4-磺基邻苯二甲酸三钠盐的氯化在20℃、或50℃到60℃、或80℃、或100℃、或110℃的温度下进行,其中在0.5小时(h)、或1h、或1.5h到2h、或3h的持续时间内连续添加氯化剂。一旦氯化剂的添加完成,就任选地使反应再继续进行6h、或8h、或10h、或12h、或14h到16h、或18h、或20h、或22h、或24h。方法包括从溶解的4-氯磺酰基邻苯二甲酸酐中移除(或“第一移除”)不可溶的氯化钠(沉淀),以形成经分离的4-氯磺酰基邻苯二甲酸酐。经分离的4-氯磺酰基邻苯二甲酸酐保持溶解在溶剂甲苯中。在实施例中,第一移除步骤包括从溶解的4-氯磺酰基邻苯二甲酸酐中过滤氯化钠。过滤程序可包括少量甲苯溶剂的后续蒸发,以便从经分离的4-氯磺酰基邻苯二甲酸酐中移除过量的氯化剂。在实施例中,第一移除步骤包括从溶解的4-氯磺酰基邻苯二甲酸酐中过滤不可溶的氯化钠,并且随后用小份的水洗涤经分离的4-氯磺酰基邻苯二甲酸酐以移除残余dmf。洗涤程序可包括少量甲苯溶剂的后续蒸发,以便从经分离的4-氯磺酰基邻苯二甲酸酐中移除残余水。在实施例中,第一移除步骤包括将水添加至包括甲苯溶剂、溶解的4-氯磺酰基邻苯二甲酸酐和不可溶的氯化钠的反应混合物。水添加在反应混合物中形成液体水相。液体水相分解或以其他方式溶解不可溶的氯化钠。甲苯溶剂形成液体非水相,其中4-氯磺酰基邻苯二甲酸酐保持溶解。方法包括从液体非水相中分离液体水相,以从溶解的4-氯磺酰基邻苯二甲酸酐中移除不可溶的氯。换句话说,通过液体(水)-液体(非水)相分离来将在液体水相中溶解的氯化钠从液体非水相中经分离的4-氯磺酰基邻苯二甲酸酐中移除。在实施例中,分离步骤包括洗涤程序,其中少量甲苯溶剂的后续蒸发从经分离的4-氯磺酰基邻苯二甲酸酐中移除残余水。方法包括在溶剂反应条件下使经分离的4-氯磺酰基邻苯二甲酸酐(2)与叠氮化钠(nan3)反应,以形成4-叠氮基磺酰基邻苯二甲酸酐(aspa)(3)。aspa(3)的结构示出在图1中。溶剂是甲苯,并且4-叠氮基磺酰基邻苯二甲酸酐反应产物溶解(或以其他方式可溶)在甲苯中。不可溶的氯化钠作为沉淀也形成为副产物。在实施例中,4-氯磺酰基邻苯二甲酸酐与叠氮化钠的反应在0℃、或15℃到20℃、或30℃、或40℃、或50℃的温度下进行,其中在1分钟(min)、或3min、或5min到7min、或9min、或10min的持续时间内连续添加叠氮化钠在水中的溶液。一旦nan3的含水溶液的添加完成,就任选地使反应再继续进行1h到2h。在实施例中,将叠氮化钠直接添加至含有溶解在甲苯中的经分离的4-氯磺酰基邻苯二甲酸酐的反应容器。换句话说,在从反应容器中移除不可溶的氯化钠与将叠氮化钠添加至反应容器之间不发生中间方法步骤(例如,无纯化、无分离、无洗涤)。用于氯化步骤的甲苯溶剂也用作用于叠氮化钠反应的溶剂,并且使得能够在无进一步纯化的情况下使用经分离的4-氯磺酰基邻苯二甲酸酐。以此方式,本方法有利地减少方法步骤并且减少生产aspa最终产物必需的生产设备的量。在实施例中,叠氮化钠作为含水叠氮化钠溶液添加。含水叠氮化钠溶液含有5wt%、或10wt%、或20wt%、或25wt%到30wt%、或40wt%、或50wt%、或60wt%的叠氮化钠。重量百分比以含水叠氮化钠溶液的总重量计。申请人发现将叠氮化钠在水中的溶液添加至其中甲苯作为反应溶剂的经分离的4-氯磺酰基邻苯二甲酸酐有利地避免对于相转移催化剂的需要。方法包括从溶解的4-叠氮基磺酰基邻苯二甲酸酐中移除(或“第二移除”)不可溶的氯化钠(沉淀),以形成经分离的4-叠氮基磺酰基邻苯二甲酸酐。经分离的4-叠氮基磺酰基邻苯二甲酸酐保持溶解在甲苯中。在实施例中,第二移除步骤包括从溶解的4-叠氮基磺酰基邻苯二甲酸酐中过滤氯化钠。过滤程序还包括任何未反应叠氮化钠的移除。方法包括获取呈固体状的经分离的4-叠氮基磺酰基邻苯二甲酸酐。通常,在第二移除步骤之后存在小的盐水层。小的盐水层通过相分离来移除。在实施例中,方法包括使粗固体(3)再结晶,以形成纯化的固体的4-叠氮基磺酰基邻苯二甲酸酐(3)。溶解在甲苯中的经分离的4-叠氮基磺酰基邻苯二甲酸酐(3)在真空下浓缩成粗固体。粗固体从乙酸乙酯/庚烷中再结晶,以提供纯化的且固体的4-叠氮基磺酰基邻苯二甲酸酐(3)。在实施例中,纯化的且固体的4-叠氮基磺酰基邻苯二甲酸酐(3)具有92wt%、或93wt%、或94wt%、或95wt%、或96wt%、或97wt%到98wt%、或99wt%、或99.9wt%的纯度。在实施例中,方法在单个反应容器中执行。氯化、第一移除、反应、第二移除和分离步骤全部在单个反应容器中执行。在单个反应容器中执行本方法的能力通过减少生产4--叠氮基磺酰基邻苯二甲酸酐(3)必需的设备的量来有利地改善生产效率。以举例的方式而非限制,提供本发明的实例。实例1.材料在实例中使用的材料提供于以下表1中。表1材料cas编号来源4-磺基邻苯二甲酸三钠盐3325-08-4西格玛-奥德里奇公司(sigma-aldrich)n,n-二甲基甲酰胺(dmf)68-12-2费舍尔公司(fisher)或西格马-奥德里奇公司乙二酰氯79-37-8西格玛-奥德里奇公司叠氮化钠(nan3)26628-22-8西格玛-奥德里奇公司甲苯108-88-3费舍尔公司乙酸乙酯141-78-6费舍尔公司庚烷142-82-5费舍尔公司2.测试方法在装备有b-acs60-样品转换器和具有z-梯度的5mmpabbo宽频带探针的brukerultrashieldplus400mhz光谱仪上记录1h-和13cnmr波谱。1hnmr光谱数据参考当在丙酮-d6中收集时的残余溶剂峰(中心线2.05ppm)。当在氧化氘(d2o)中收集时,1hnmr光谱数据参考3-(三甲基硅烷基)-1-丙磺酸钠盐(dss钠盐)[(ch3)3sich2-ch2ch2so3na,0.00ppm]的三甲基硅烷基质子共振。13cnmr数据还参考当在丙酮-d6中收集时的残余溶剂峰(中心线29.84ppm)。以下形式用于报告1hnmr共振:化学位移(δ,以ppm为单位)[多重性,以hz为单位的一或多个耦合常数,积分值]。釜中产率和最终产物纯度通过用1,4-双(三甲基硅烷基)苯(1,4-btmsb)作为内标物的1hnmr分析来确定。通常将已知量的样品(例如,粗反应的最终干燥产物)和1,4-btmsb使用精确分析天平称量到30-ml的闪烁瓶中。将混合物溶解在丙酮-d6中,穿过0.45μm的尼龙注射过滤器(如果需要移除不可溶的材料),并且收集所得混合物的1hnmr波谱(16次扫描,20秒的弛豫延迟时间)。然后,wt%纯度从对应于最终产物的共振的平均面积/h积分与1,4-双(三甲基硅烷基)苯(1,4-btmsb)的共振的平均面积/h积分的比率来确定[丙酮-d6:δ0.25(s,18h)和7.52(s,4h)]。4-磺基邻苯二甲酸三钠盐(1)的纯度通过用在d2o中的dss钠盐的1hnmr分析来确定。wt%纯度以如以上所述的相同方式通过对应于(1)的共振相对于dss钠盐的共振的相对积分来确定{δ0.00[s,9h,(ch3)3sich2ch2ch2so3na],0.63[dd,j=8.8,8.8hz,2h,(ch3)3sich2ch2ch2so3na],1.76[m,2h,(ch3)3sich2ch2ch2so3na]和2.91[dd,j=7.6,7.6hz,2h,(ch3)3sich2ch2ch2so3na}。3.从4-磺基邻苯二甲酸三钠盐(1)制备4-氯磺酰基邻苯二甲酸酐(2)反应在具有底部排放口的3-l的有夹套玻璃反应器中执行,该反应器装备有塔顶机械搅拌器、往下泵送的两层45°倾斜的4-叶片叶轮(d=75mm,15mm叶片宽度,75mm层间距)、氮气入口、热套管、dean-stark分水器,以及具有teflon内管的水冷凝器,其排出至含有经机械搅拌的10%含水氢氧化钠溶液的洗涤器。温度使用80:20的dowfrost/水用neslabrte10循环浴来控制。反应器装有4-磺基邻苯二甲酸三钠盐(1)(与3-异构体的4:1混合物)(350.0g,0.992mol,1.0当量,通过用dss钠盐的1hnmr分析确定的88.5wt%纯度)和甲苯(2600ml),以生产灰白色浆液。然后,将混合物加热用于共沸干燥步骤。在109℃(热传递流体浴温=115℃)的大致内部温度下收集馏出物。塔顶收集总共650ml馏出物。使所得混合物冷却至50℃,并且将dean-stark分水器替换为水冷凝器/洗涤器系统。添加无水dmf(14.62g,0.198mol,20mol%),并且使反应混合物升温至50℃。将乙二酰氯(322.6g,2.531mol,2.5当量)逐份装载至60-ml的teflon注射器,并且经由注射泵在3.5小时内通过teflon线装至反应混合物。注意到在整个乙二酰氯的添加中1℃至2℃的轻微放热。反应混合物在50℃下搅拌过夜,并且然后冷却至室温。混合物通过底部排放口移除,并且无机盐由通过真空过滤通过粗糙的-多孔性烧结玻璃料漏斗来收集。反应器用穿过无机盐湿滤饼的新鲜甲苯冲洗。甲苯滤液通过旋转蒸发来部分浓缩,并且存在的细小白色不溶物通过过滤来移除,以提供1423.1g甲苯滤液。将甲苯滤液的样品(1.0164g)移除、蒸发至干并且与1,4-btmsb(37.0mg,0.1658mmol)合并。所得混合物溶解在丙酮-d6(~4ml)中。此样品利用1hnmr的分析指示(2)(与3-异构体的4:1混合物)的浓度为11.0wt%,其对应于64%(0.635mol)的釜中产率。用1,4-btmsb作为内标物的经分离的4-氯磺酰基邻苯二甲酸酐(2,与3-氯磺酰基邻苯二甲酸酐的4:1混合物)的1hnmr波谱(400mhz,丙酮-d6)示出在图3中。1hnmr(400mhz,丙酮-d6):δ8.42(dd,j=8.0,8.0hz,1h,3-异构体),8.51(dd,j=1.0,8.0hz,1h,4-异构体),8.59(dd,j=1.0,8.0hz,1h,3-异构体),8.64(dd,j=1.0,8.0hz,1h,3-异构体),8.76(dd,j=1.0,2.0hz,1h,4-异构体)和8.78(dd,j=2.0,8.0hz,1h,4-异构体)。4.4-氯磺酰基邻苯二甲酸酐(2)至4-叠氮基-磺酰基邻苯二甲酸酐(3)的转化此反应在有夹套的5-l的底部排放口玻璃反应器(150mm直径,~2.5:1深度/宽度比)中进行,该反应器装备有塔顶搅拌器马达、往下泵送的两层45°倾斜的4-叶片叶轮(d=75mm,15mm叶片宽度,75mm层间距)、热套管和热电偶、氮气入口、玻璃水冷凝器和装配有带螺纹聚四氟乙烯(ptfe)栓塞的次级底部排放口。温度控制由通过反应器夹套的dowfrost(50:50丙二醇/水)热传递流体的再循环来实现。所有液体反应剂通过用ptfe隔膜泵(cole-parmer型号#7553-70)和masterflex速度控制器(cole-parmer型号#7553-71)进料的汲取管引入。在5-l反应器下方的是3-l中等孔隙率玻璃料过滤器,其排放到4-l塑料涂覆的玻璃爱伦美氏过滤器烧瓶中。过滤器烧瓶连接至皮带驱动的真空泵和干冰(-78℃)真空分水器。将4-氯磺酰基邻苯二甲酸酐(2)在甲苯中的溶液(与3-氯磺酰基-邻苯二甲酸酐的~5:1混合物)(1270g,0.696mol,1.0当量,14.1wt%活性)和新鲜甲苯(2215g)经由ptfe隔膜泵相继引入到5-l反应器中。启动搅动(150rpm至200rpm)。打开热传递流体浴并且将设定点调节至20℃。叠氮化钠(90.6g,1.392mol,2.0当量)在去离子水(272g)中的溶液在塑料涂覆的琥珀色玻璃瓶中制备,并且然后在7min的时间段内经由ptfe隔膜泵将溶液添加至5-l反应器。含有含水叠氮化钠的瓶相继用去离子水(30ml)和新鲜甲苯(30ml)洗涤。两种冲洗液经由ptfe隔膜泵转移至5-l反应器。在含水叠氮化钠添加的过程中,反应混合物的内部温度从19.5℃增至22.3℃。另外,白色不溶物(氯化钠)的外观在~30秒内观测到。在已搅拌1h18min之后,移除~2ml等分试样的反应器浆液。使等分试样穿过0.45μmptfe注射过滤器,并且滤液通过旋转蒸发来浓缩。残留物利用1hnmr(丙酮-d6)的分析显示已经消耗起始材料。一旦nmr分析完成,反应混合物就通过反应器底部排放口排放,并且盐通过真空过滤通过3-l中等孔隙率玻璃料来移除。5-l反应器和盐滤饼用新鲜甲苯洗涤。将甲苯滤液逐份转移至分液漏斗,并且分离剩余的少量含水盐水。有机相用极少量的去离子水洗涤,并且分离水相。有机相通过旋转蒸发来部分浓缩至1264.1g的质量。将此溶液的样品移除(1.0717g)、蒸发至干并且与1,4-btmsb(33.3mg,0.1492mmol)合并。所得混合物溶解在丙酮-d6(~4ml)中。此样品利用1hnmr的分析指示(3)的浓度为4.5wt%,其对应于32%的釜中产率。图4示出用1,4-btmsb作为内标物的粗4-叠氮基磺酰基邻苯二甲酸酐(3)的1hnmr波谱(400mhz,丙酮-d6)。甲苯溶液通过旋转蒸发来进一步浓缩以留下黄色固体(108.7g)。将粗固体装入装配有teflon搅拌棒和氮气入口的1-l圆底烧瓶。添加乙酸乙酯(349g),并且所得混合物搅拌过夜。均匀的黄色溶液用正庚烷(362g)处理,这引发浑浊度的形成。所得混合物(838g)通过旋转蒸发(在大约50mmhg下25℃至30℃)来浓缩,直到塔顶取出~2/3的总质量(剩余279g浆液)。形成的固体通过真空过滤在中等孔隙率玻璃料上来回收,得到160g的母液。湿滤饼用2:1(v/v)的正庚烷/乙酸乙酯(2×150ml)洗涤,得到238.2g的合并洗涤液。湿滤饼(66.3g)在40℃至50℃下的真空烘箱中干燥,得到为淡黄色固体的4-叠氮基磺酰基邻苯二甲酸酐(3)(51.2g,29%产率,0.202mol)。(3)的样品(192.1mg)与1,4-btmsb(55.2mg,0.2474mmol)合并,并且将所得混合物溶解在丙酮-d6(~4ml)中。此样品利用1hnmr的分析指示(3)以高纯度(>99wt%)的状态分离。图5示出用1,4-btmsb作为内标物的4-叠氮基磺酰基邻苯二甲酸酐(3)的1hnmr波谱(400mhz,丙酮-d6)。1hnmr(400mhz,丙酮-d6):δ8.45(dd,j=2.0,7.0hz,1h),8.64(dd,j=2.0,2.0hz,1h)和8.65(dd,j=2.0,6.0hz,1h)。13cnmr(100mhz,丙酮-d6):δ125.2,128.0,133.9,135.7,137.3,146.1,162.1和162.4。图6示出4-叠氮基磺酰基邻苯二甲酸酐的13cnmr波谱。尤其期望的是,本发明不限于本文中所含有的实施例和说明,而是包括那些实施例的修改形式,该修改形式包括在所附权利要求书范围内出现的实施例的部分和不同实施例的要素的组合。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1