大肠癌纺锤体组装检验点检测用试剂体系和试剂盒及应用的制作方法
本发明涉及基因工程领域,具体涉及一种用于大肠癌纺锤体组装检验点靶点基因检测的试剂体系和试剂盒以及其应用。
背景技术:
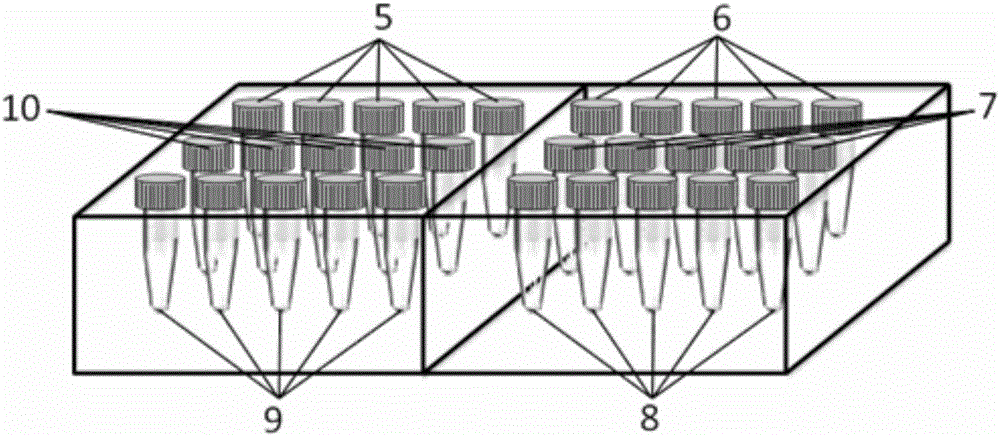
:大肠癌是在直肠和乙状结肠交界处发生的消化道恶性肿瘤,是世界范围内最为普遍的恶性肿瘤之一,尤其是大部分只能在晚期才得到确诊。一直以来大肠癌是一个巨大的公共健康问题,每年在世界范围内有超过130万人的新确诊案例,以40-50岁年龄组发病最高。同时,大肠癌也是既乳腺癌之后第二大女性常见癌症和第三男性高风险癌症,每年约有70万人因大肠癌不幸离世。大肠癌的主要早期表现为消化不良、腹胀、便前腹痛、便血等症状,由于肿瘤溃烂感染还会导致贫血、乏力、消瘦等中毒症状,如不及时治疗会出现黄疸、腹腔积液、水肿等恶性症状。但目前针对晚期大肠癌的治疗依旧停留在手术切除和术后辅助化疗阶段,其副作用和抗性成为最大的缺点。在大部分晚期大肠癌患者中,约有90%是与体细胞染色体异常有关。因此寻找新的肿瘤靶点和对应的治疗方案迫在眉睫。最近,纺锤体组装检验点(SAC)的一项监控机制备受瞩目,其中对所有染色体进行分裂末期抑制直至退回至分裂中期这一功能可令SAC成为抗击肿瘤的新靶点。正常人的粪便每天大约可排泄近1010个大肠上皮细胞,对脱落到粪便里的黏膜细胞进行检测是大肠癌的一种理想筛查手段。大肠癌患者中普遍存在SAC基因表达异常。在有丝分裂中,一旦染色体没有和纺锤微管有效结合,SAC就会终止有丝分裂末期,进而防止发生更大的错误。大肠癌患者中都不同程度的出现SAC活性降低,这极容易导致染色体错配和染色体异常,进而引发体细胞癌变。因此染色体不稳定是大肠癌发生的重要诱因之一,而导致SAC活性异常的根本是调控其活性的基因发生表达异常。调控SAC活性的核心异常表达基因包括:BubR1:位于17号染色体,在调控SAC的基因中其过度表达已经得到证实,其在大肠癌细胞中会中断SAC的维持染色体稳定的功能,因此BubR1是由溃疡性肠炎至癌变的重要的靶点之一。Mad1:位于7号染色体,其过表达会通过引发非整倍体和染色体不稳定导致SAC功能性削弱,并与Ⅱ期和Ⅲ期大肠癌紧密相关。Mad2:位于10号染色体,是SAC活性的关键基因,Mad2还与BubR1共表达,并与肿瘤抑制因子APC的生殖系突变有关。Mad2的过表达参与肠道细胞癌变并且预后差。AURKB:位于17号染色体,靶点是调控有丝分裂在细胞质中正常进行的苏氨酸激酶。AURKB的过度表达会增加大肠癌中染色体不稳定的情况出现,因此AURKB可以作为诊断大肠癌和晚期大肠癌的分子靶点。PlK1:位于16号染色体,是一个调控有丝分裂进程的丝氨酸激酶,在中心体成熟、纺锤体组装和动力微管结合上有重要作用。PLK1的表达可以提高SAC组分和着丝粒的结合,强化纺锤体组装检验点的活性。同样在大肠癌样本中,PlK1也出现过表达。PlK1的过表达会诱导肿瘤恶化并对肿瘤病人的预后有不利影响。尤其在已经手术切除病灶的大肠癌患者中,PlK1的过度表达常常会在放疗后依旧致使大肠癌高风险复发。Cdc20:位于1号染色体,是SAC的关键靶点,在大肠癌样本中发现其有过度表达现象。其过表达与不理想预后和晚期临床阶段有关。此外,TP53是人类大肠癌中最易突变的基因,而BubR1、Mad2、AURKB、PlK1和Cdc20都与TP53的表达有关。因此,SAC相关组分的表达异常是大肠癌最新的重要诊断分子靶点。但目前针对大肠癌的基因检测仅限于寻找发生突变的易感基因和肠道菌群的DNA检测,本专利针对调控癌细胞有丝分裂的纺锤体组装检验点相关的6个靶点的过表达检测将为大肠癌早期诊断和病程发展提供全新的方向和重要参考,填补了SAC相关基因的大肠癌检测空白,也为大肠癌SAC靶点的抑制疗法提供了理论基础。技术实现要素:本发明解决的技术问题是:现有的大肠癌基因检测仅限于寻找发生突变的易感基因和肠道菌群的DNA检测,普遍存在灵敏度低、准确率不高,还费时费力的缺点,其应用受到一定限制。为了解决上述的问题,本发明提供了一种用于大肠癌纺锤体组装检验点靶点基因检测的试剂体系和试剂盒以及其应用。具体来说,针对现有技术的不足,本发明提供了如下技术方案:一方面,本发明提供了一种大肠癌纺锤体组装检验点用试剂体系,所述试剂体系包括用于BubR1基因检测的试剂,用于Mad1基因检测的试剂,用于Mad2基因检测的试剂,用于AURKB基因检测的试剂,用于PlK1基因检测的试剂和用于Cdc20基因检测的试剂。优选地,所述用于BubR1基因检测的试剂包括用于BubR1检测的DNA探针,其序列如SEQIDNO.7所示;所述用于Mad1基因检测的试剂包括用于Mad1检测的DNA探针,其序列如SEQIDNO.8所示;所述用于Mad2基因检测的试剂包括用于Mad2检测的DNA探针,其序列如SEQIDNO.9所示;所述用于AURKB基因检测的试剂包括用于AURKB检测的DNA探针,其序列如SEQIDNO.10所示;所述用于PlK1基因检测的试剂包括用于PlK1检测的DNA探针,其序列如SEQIDNO.11所示;所述用于Cdc20基因检测的试剂包括用于Cdc20检测的DNA探针,其序列如SEQIDNO.12所示。优选地,所述用于BubR1基因检测的试剂包括扩增引物序列SEQIDNO.1a和SEQIDNO.1b;所述用于Mad1基因检测的试剂包括扩增引物序列SEQIDNO.2a和SEQIDNO.2b;所述用于Mad2基因检测的试剂包括扩增引物序列SEQIDNO.3a和SEQIDNO.3b;所述用于AURKB基因检测的试剂包括扩增引物序列SEQIDNO.4a和SEQIDNO.4b;所述用于PlK1基因检测的试剂包括扩增引物序列SEQIDNO.5a和SEQIDNO.5b;所述用于Cdc20基因检测的试剂包括扩增引物序列SEQIDNO.6a和SEQIDNO.6b。另一方面,本发明提供了一种用于大肠癌纺锤体组装检验点靶点基因检测的试剂盒,所述试剂盒包括用于BubR1基因检测的试剂,用于Mad1基因检测的试剂,用于Mad2基因检测的试剂,用于AURKB基因检测的试剂,用于PlK1基因检测的试剂和用于Cdc20基因检测的试剂。优选地,所述用于BubR1基因检测的试剂包括用于BubR1检测的DNA探针,其序列如SEQIDNO.7所示;所述用于Mad1基因检测的试剂包括用于Mad1检测的DNA探针,其序列如SEQIDNO.8所示;所述用于Mad2基因检测的试剂包括用于Mad2检测的DNA探针,其序列如SEQIDNO.9所示;所述用于AURKB基因检测的试剂包括用于AURKB检测的DNA探针,其序列如SEQIDNO.10所示;所述用于PlK1基因检测的试剂包括用于PlK1检测的DNA探针,其序列如SEQIDNO.11所示;所述用于Cdc20基因检测的试剂包括用于Cdc20检测的DNA探针,其序列如SEQIDNO.12所示。优选地,用于BubR1基因的扩增引物序列为SEQIDNO.1a和SEQIDNO.1b;用于Mad1基因的扩增引物序列为SEQIDNO.2a和SEQIDNO.2b;用于Mad2基因的扩增引物序列为SEQIDNO.3a和SEQIDNO.3b;用于AURKB基因的扩增引物序列为SEQIDNO.4a和SEQIDNO.4b;用于PlK1基因的扩增引物序列为SEQIDNO.5a和SEQIDNO.5b;用于Cdc20基因的扩增引物序列为SEQIDNO.6a和SEQIDNO.6b。优选地,所述试剂盒中的试剂包括样品DNA提取组件、PCR扩增组件、PCR产物纯化组件和DNA测序反应组件。优选地,所述PCR产物纯化组件包括ddH2O、SAP酶和ExoI酶。优选地,所述试剂盒中DNA测序反应组件包括ddH2O、EDTA溶液、乙醇溶液、去离子甲酰胺溶液和BigDyemix试剂。优选地,所述试剂盒中的样品DNA提取组件包括粪便裂解液、硅胶膜结合液、硅胶膜洗涤液和蛋白沉淀液。优选地,所述粪便裂解液包括:30-100mmol/LTris-Cl、3-10mmol/LEDTA、0.6-5mmol/LNaCl和0.1-1.0%(W/V)十二烷基硫酸钠。优选地,所述硅胶膜结合液包括3-10mol/L盐酸胍。优选地,所述硅胶膜洗涤液包括:1-5mmol/LTris-Cl、0.5-2mmol/LEDTA、1-5mmol/LNaCl和体积含量为30-50%的乙醇。优选地,所述蛋白沉淀液包括:0.5-2mol/L乙酸钾和体积含量为5-20%冰乙酸。在又一方面,本发明提供了用于BubR1基因检测的试剂,用于Mad1基因检测的试剂,用于Mad2基因检测的试剂,用于AURKB基因检测的试剂,用于PlK1基因检测的试剂和用于Cdc20基因检测的试剂在制备检测大肠癌纺锤体组装检验点的试剂体系和试剂盒中的应用。优选地,所述试剂包括PCR扩增用试剂、限制性内切酶酶切用试剂、PCR产物纯化用试剂。优选地,所述试剂的作用对象为粪便。与现有技术相比,本发明的效果和益处在于:本发明填补了纺锤体组装检验点相关基因的大肠癌检测空白,可同时检测6种相关基因,检测结果全面可靠,而且快速、高效、准确、便捷、灵敏度高、特异性强,误诊率低。本发明提供的检测方法为大肠癌的早期诊断和病程发展提供全新的方向和重要参考。附图说明图1为本发明试剂盒的上层部分,用于获取粪便样本的DNA保存液,其中,1为粪便裂解液,2为硅胶膜结合液,3为硅胶膜洗涤液,4为蛋白沉淀液。图2为本发明试剂盒的下层部分,包含各基因检测用试剂,5为BubR1检测用试剂,6为Mad1检测用试剂,7为Mad2检测用试剂,8为PlK1检测用试剂,9为AURKB检测用试剂,10为Cdc20检测用试剂。每组5个PE管中分别含有相应基因对应的DNA扩增引物、PCR反应组件、TaqDNA聚合酶、PCR产物纯化组件和DNA探针测序反应组件。图3为试剂盒的外包装盒。具体实施方式如上所述,本发明的目的在于:提供一种大肠癌纺锤体组装检验点检测用的试剂体系、试剂盒和应用。本发明的基本原理是通过粪便裂解液、硅胶膜结合液、硅胶膜洗涤液、蛋白沉淀液等试剂的处理这一低成本、低风险和高采集率的细胞样本方法,获得在粪便中数量充足的脱落大肠上皮黏膜细胞,之后利用靶多核苷酸的特异性引物和靶多核苷酸的特异性探针,在耐热DNA聚合酶(Taq酶)、高质量脱氧核糖核苷三磷酸(dNTPs)以及PCR反应缓冲液中,一次性对有丝分裂过程末期纺锤体组装检验点相关六个基因的表达状态进行检测,确定其是否过表达,达到在早期及时对大肠癌的发生和发展进行精准诊断的目的。本发明提供了一种大肠癌纺锤体组装检验点检测用的试剂体系和试剂盒,所述试剂包括用于BubR1基因检测的试剂,用于Mad1基因检测的试剂,用于Mad2基因检测的试剂,用于AURKB基因检测的试剂,用于PlK1基因检测的试剂和用于Cdc20基因检测的试剂。所述试剂盒中的试剂分装到管中,供单人次检测用,保存温度为-20℃。在优选实施方式中,用于BubR1基因检测的试剂包括扩增引物序列SEQIDNO.1a和SEQIDNO.1b,以及用于BubR1检测的DNA探针SEQIDNO.7;用于Mad1基因检测的试剂包括扩增引物序列SEQIDNO.2a和SEQIDNO.2b,以及用于Mad1检测的DNA探针SEQIDNO.8;用于Mad2基因检测的试剂包括扩增引物序列SEQIDNO.3a和SEQIDNO.3b,以及用于Mad2检测的DNA探针SEQIDNO.9;用于AURKB基因检测的试剂包括扩增引物序列SEQIDNO.4a和SEQIDNO.4,以及用于AURKB检测的DNA探针SEQIDNO.10;用于PlK1基因检测的试剂包括扩增引物序列SEQIDNO.5a和SEQIDNO.5b,以及用于PlK1检测的DNA探针SEQIDNO.11;用于Cdc20基因检测的试剂包括扩增引物序列SEQIDNO.6a和SEQIDNO.6b,以及用于Cdc20检测的DNA探针SEQIDNO.12。本发明利用粪便裂解液、硅胶膜结合液、硅胶膜洗涤液以及蛋白沉淀液处理粪便样本,获取粪便样本DNA保存液。然后,利用引物扩增BubR1、Mad1、Mad2、AURKB、PlK1和Cdc20六个基因片段,通过试剂盒中的PCR产物纯化组件进行反应、纯化;在检测用的DNA探针的作用下,扩增PCR纯化产物,扩增结束后,处理PCR产物并放入DNA测序仪中进行测序。以下结合具体实施例对本发明做进一步的说明。其中,实施例中所用的试剂和仪器信息如下:PCR仪,厂家:ABI,型号:ABI-2720PCR,美国;DNA测序仪,厂家:Illumina,型号:HiSeqXTen;dNTPs,厂家:TAKARA,型号:dNTPMixture4030,日本;TaqDNA聚合酶,厂家:TAKARA,型号:ExTaqDRR001A,日本;ExoI酶,厂家:TAKARA,日本;SAP酶,厂家:赛默飞世尔科技有限公司,型号:EF0511;EDTA,厂家:丽水博瑞特化工有限公司,型号:60-00-4;去离子甲酰胺,厂家:上海酶联生物科技有限公司,型号:75-12-7RT;Tris-CL缓冲液,牛血清蛋白,厂家:南京奥多福尼生物科技有限公司,型号:9048-46-8,25g。蛋白酶K,厂家:上海翊圣生物科技有限公司型号:10401ES60,100mg;盐酸胍,厂家:烟台三鼎化工有限公司,型号:50-01-1;如图1所示,试剂盒上层部分设有用于获取粪便样本的DNA保存液,其中,所用试剂的各组分比例不同,但均能获取粪便样本DNA。以下通过具体实施例进一步说明本发明试剂体系和试剂盒的制备和应用。实施例一获取粪便样本DNA保存液的步骤包括:1.采集暴露小于24小时受试者的粪便样本,用无菌刀片挑取170-180mg的样本于冰上。2.在样本中加入3.0ml的粪便裂解液,充分裂解后离心分离,取上清液加入250mg牛血清蛋白,离心得到上清液,在上清液中加入30μl的蛋白酶K置于60℃条件下消化反应2h,得到消化液。粪便裂解液的组成为:30mmol/LTris-Cl、3mmol/LEDTA、0.6mmol/LNaCl和0.1%(W/V)十二烷基硫酸钠。3.将上述所得到的消化液冷却至室温,加入300μl蛋白沉淀液,沉淀蛋白,充分混匀后经离心分离去除蛋白杂质,得到上清液即DNA抽提液。蛋白沉淀液由0.5mol/L乙酸钾和体积含量为5%的冰乙酸配制而成。4.向已经去除蛋白杂质的DNA抽提液中加入硅胶膜结合液(3mmol/L盐酸胍),充分结合DNA,DNA抽提液与硅胶膜结合液的体积比为1:2.5,然后经硅胶膜吸附,离心分离,得到沉淀物,在沉淀物中加入800-1000μl硅胶膜洗涤液洗涤,重复洗涤两次,然后离心分离脱去硅胶膜中残存的硅胶膜洗涤液后,加入80μlTE缓冲液溶解洗脱DNA,离心分离得到离心后的上清液,该上清液为含长度大于20kb的样本DNA保存液。硅胶膜洗涤液的组成为:1mmol/LTris-Cl、0.5mmol/LEDTA、1mmol/LNaCl和体积含量为30%的乙醇。实施例二获取粪便样本DNA保存液的步骤包括:1.采集暴露小于24小时的粪便样本,用无菌刀片挑取200-220mg的样本于冰上。2.在样本中加入0.5ml的粪便裂解液,充分裂解后离心分离,取上清液加入250mg牛血清蛋白,离心得到上清液,在上清液中加入30μl的蛋白酶K置于60℃条件下消化反应2h,得到消化液。粪便裂解液的组成为:100mmol/LTris-Cl、10mmol/LEDTA、5mmol/LNaCl和1.0%(W/V)十二烷基硫酸钠。3.将上述所得到的消化液冷却至室温,加入300μl蛋白沉淀液,沉淀蛋白,充分混匀后经离心分离去除蛋白杂质,得到上清液即DNA抽提液。蛋白沉淀液由2mol/L乙酸钾和体积含量为20%的冰乙酸配制而成。4.向已经去除蛋白杂质的DNA抽提液中加入硅胶膜结合液(10mmol/L的盐酸胍),充分结合DNA,DNA抽提液与硅胶膜结合液的体积比为1:3.0,然后经硅胶膜吸附,离心分离,得到沉淀物,在沉淀物中加入800μl硅胶膜洗涤液洗涤,重复洗涤两次,然后离心分离脱去硅胶膜中残存的硅胶膜洗涤液后,加入100μlTE缓冲液溶解洗脱DNA,离心分离得到离心后的上清液,该上清液为含长度大于20kb的样本DNA保存液。硅胶膜洗涤液的组成为:5mmol/LTris-Cl、2mmol/LEDTA、5mmol/LNaCl和体积含量为50%的乙醇。实施例三制备得到的试剂盒如附图1-3所示,除外包装盒外,主要包括上层和下层两个部分。上层部分用于获取粪便样本的DNA保存液,其中,1装有粪便裂解液,2装有硅胶膜结合液,3装有硅胶膜洗涤液,4装有蛋白沉淀液。下层部分包含各基因检测用试剂,其中,5为BubR1检测用试剂,6为Mad1检测用试剂,7为Mad2检测用试剂,8为PlK1检测用试剂,9为AURKB检测用试剂,10为Cdc20检测用试剂。每组5个PE管中分别含有六种基因对应DNA扩增引物、PCR反应组件、TaqDNA聚合酶、PCR产物纯化组件和DNA探针测序反应组件。利用试剂盒检测出样品各基因的DNA序列后,在NCBI库中查找各基因正常表达的DNA序列,通过序列比对,确定样品中基因表达是否正常,从而判断样品提供者是否患有大肠癌。实施例四以下通过具体实施例说明大肠癌纺锤体组装检验点(SAC)6种靶点基因检测用的试剂及试剂盒的制备方法。其主要包括如下:(1)获取粪便样本DNA保存液1.采集暴露小于24小时的大肠癌患者粪便样本,用无菌刀片挑取180-200mg的样本于冰上。2.在样本中加入1.5ml的粪便裂解液,充分裂解后离心分离,取上清液加入250mg牛血清蛋白,离心得到上清液,在上清液中加入30μl的蛋白酶K置于60℃条件下消化反应2h,得到消化液。粪便裂解液的组成为:50mmol/LTris-Cl、5mmol/LEDTA、1mmol/LNaCl和0.1%(W/V)十二烷基硫酸钠。3.将上述所得到的消化液冷却至室温,加入300μl蛋白沉淀液,沉淀蛋白,充分混匀后经离心分离去除蛋白杂质,得到上清液即DNA抽提液。蛋白沉淀液由2mol/L乙酸钾和体积含量为11.5%的冰乙酸配制而成。4.向已经去除蛋白杂质的DNA抽提液中加入硅胶膜结合液(3mol/L盐酸胍),充分结合DNA,DNA抽提液与硅胶膜结合液的体积比为1:1.5,然后经硅胶膜吸附,离心分离,得到沉淀物,在沉淀物中加入800μl硅胶膜洗涤液洗涤,重复洗涤两次,然后离心分离脱去硅胶膜中残存的硅胶膜洗涤液后,加入100μlTE缓冲液溶解洗脱DNA,离心分离得到离心后的上清液,该上清液为含长度大于20kb的样本DNA保存液。硅胶膜洗涤液的组成为2mmol/LTris-Cl、1mmol/LEDTA、5mmol/LNaCl和体积含量为50%的乙醇。(2)靶点基因扩增利用表1中的PCR反应体系进行PCR扩增BubR1、Mad1、Mad2、AURKB、PlK1和Cdc20六个基因。表1PCR反应体系组成体积(μl)基因组DNA1(30μg/ml)10×TaqBuffer2.5dNTP0.3(30mM,each)TaqDNA聚合酶0.25(6U/μl)上游引物0.25(25μM)下游引物0.25(25μM)ddH2O15.45μl总体积20μlPCR反应参数为:其中,用于BubR1、Mad1、Mad2、AURKB、PlK1和Cdc20基因扩增的引物序列如下:BubR1上游引物,SEQIDNO.1a:TGGCTGTAGTGTTGAATA下游引物,SEQIDNO.1b:CCTACTGGTTCTACCTTCMad1上游引物,SEQIDNO.2a:TCAGGTTGTTAAGTCCAG下游引物,SEQIDNO.2b:CTCGTTTCCATATTCTCTTCMad2上游引物,SEQIDNO.3a:AGGGATAATGAATTTTCTGTAA下游引物,SEQIDNO.3b:CGAGTAAAGGTTTCAGATGAURKB上游引物,SEQIDNO.4a:GGGTTTAGGGATGAGAAG下游引物,SEQIDNO.4b:GCACTTACGTTAAGATGTCPlK1上游引物,SEQIDNO.5a:CTCAGGTGTGGAGTAGGA下游引物,SEQIDNO.5b:CATGGTAAGGTCAGTCTTTCCdc20上游引物,SEQIDNO.6a:AGGGAGGTGTTGATTTTC下游引物,SEQIDNO.6b:GCTGTAGAGTACTTTCAGTC利用以上引物扩增的BubR1基因序列在NCBI中的序列号为NG_016338.1;利用以上引物扩增的Mad1基因序列在NCBI中的序列号为NG_011518.1;利用以上引物扩增的Mad2基因序列在NCBI中的序列号为NC_000004.12;利用以上引物扩增的AURKB基因序列在NCBI中的序列号为NC_000017.11;利用以上引物扩增的PlK1基因序列在NCBI中的序列号为NC_000016.10;利用以上引物扩增的Cdc20基因序列在NCBI中的序列号为NC_000001.11。(3)PCR产物纯化使用检测试剂盒中的PCR产物纯化组件对(2)中扩增得到的PCR产物进行纯化,反应体系如表2:表2PCR产物纯化体系组分体积(μl)PCR产物20SAP酶0.75(1U/μl)ExoI酶0.375(10U/μl)ddH2O3.875Totalvolume25在PCR扩增仪上进行反应,反应条件为37℃、15min,72℃、20min。(4)检测反应设计特异性DNA探针,检测(3)纯化得到的PCR产物,并放入测序仪进行测序。反应体系见表3。表3检测反应体系组分体积(μl)PCR纯化产物1(200ng/μl)DNA测序探针1(3pmol/μl)ddH2O2Totalvolume5利用检测反应体系在PCR扩增仪上进行反应,反应条件为:反应结束后,加入1μl浓度为125mM的EDTA溶液和浓度为100%的乙醇溶液15μl,于室温下沉淀15min;在4℃、3600rpm/min的转速离心30min,轻轻倒去上清液;加入70%乙醇溶液30μl,3600rpm/min离心15min,轻轻倒去上清液;室温放置20min后加入去离子甲酰胺溶液8μl,放入测序仪中。设计的DNA探针序列如下:用于BubR1检测的DNA探针序列SEQIDNO.7:TCAACCACTTATCATCATCTCCACTGT用于Mad1检测的DNA探针序列SEQIDNO.8:TCTCCTCCTCCCGTCTCTGC用于Mad2检测的DNA探针序列SEQIDNO.9:TCGTAAGCCGTAGTTGACGTAA用于AURKB检测的DNA探针序列SEQIDNO.10:CCACTGCTATTCTCCATCACCTTCT用于PlK1检测的DNA探针序列SEQIDNO.11:CTGTCCTTCAATCCGTGGTTCCAATGC用于Cdc20检测的DNA探针序列SEQIDNO.12:ACTCCGTTGCCACAGGTTATCAGAADNA测序仪测得的序列结果如下:测得的BubR1基因序列如SEQIDNO.13所示:TGGCTGTAGTGTTGAATACACTAAAGGCAGCAAAGGATGGAAGCAAGGGACACCAGTTAAGAGATTATTGAAATAATTCAGCTCAAAAGTGAGTTGAGCCAGGTGGAAAACAGTGGAGATGATGATAAGTGGTTGATTTCTGTATATATTTTGAAGGGAGAACCAGTAGG测得的Mad1基因序列如SEQIDNO.14所示:CTCGTTTCCATATTCTCTTCCTCTCCTCCTCCCGTCTTTGCCCAGCCCCTGGCTTCCCTCTAAAAAGATGCTGTTCCTAAGGGTCTGCAATGAATTTTCCTTCTTTCAGAGAAAGACTTCCAAGTTGTGTGCCCCGGGAATGAAATGGAATAAGAGAACGAGGTGGAGTAGGGCAAGAGTCCCTGGACTTAACAACCTGA测得的Mad2基因序列如SEQIDNO.15所示:CGAGTAAAGGTTTCAGATGGATATATGCCACGCTGATATAAAATGCTGTTGATGACGAATGCTGCAAGCAAAAGAAATGTTACAGAAAATTCATTATCCCT测得的AURKB基因序列如SEQIDNO.16所示:GCACTTACGTTAAGATGTCGGGTGTCCCACTGCTATTCTCCATCACCTTCTGGCCAAGGGCAGCTAAGGAGAGAACAGGTAGGTTGAATGCGAACAGGGATGACCTTCTCATCCCTAAACCC测得的PlK1基因序列如SEQIDNO.17所示:CTCAGGTGTGGAGTAGGACAGGCCTCTGTCCTTCAATCCGTGGTTCCAATGCCCATCTGCTTCTCGGCCCTTCCAGGAAAGACTGACCTTACCATG测得的Cdc20基因序列如SEQIDNO.18所示:AGGGAGGTGTTGATTTTCCCAGCGTCTAGACTCACTCCGTTACCACAGGTTATCAGAACAGACTGAAAGTACTCTACAGC(5)序列比对BubR1基因正常表达的碱基序列如SEQIDNO.19所示:TGGCTGTAGTGTTGAATACACTAAAGGCAGCAAAGGATGGAAGCAAGGGACACCAGTTAAGAGGTTATTGAAATAATTCAGCTCAAAAGTGAGTTGAGCCAGGTGGAAAACAGTGGAGATGATGATAAGTGGTTGATTTCTGTATATATTTTGAAGGTAGAACCAGTAGGMad1基因正常表达的碱基序列如SEQIDNO.20所示:CTCGTTTCCATATTCTCTTCCTCTCCTCCTCCCGTCTCTGCCCAGCCCCTGGCTTCCCTCTAAGAAGATGCTGTTCCTAAGGGTCTGCAATGAATTTTCCTTCTTTCAGAGAAAGACTTCCAAGTTGTGTGCCCCGGGAATGAAATGGAATAAGAGAACGAGGTGGAGTAGGGCAAGAGTCCCTGGACTTAACAACCTGAMad2基因正常表达的碱基序列如SEQIDNO.21所示:CGAGTAAAGGTTTCAGATGGATATATGCCACGCTGATATAAAATGCTGTTGATGCCGAATGCTGCAAGCAAAAGAAATGTTACAGAAAATTCATTATCCCTAURKB基因正常表达的碱基序列如SEQIDNO.22所示:GCACTTACGTTAAGATGTCGGGTGTCCCACTGCTATTCTCCATCACCTTCTGGCCAGGGGCAGCTAAGGAGAGAACAGGTAGGTTGAATGCGAACAGGGATGACCTTCTCATCCCTAAACCCPlK1基因正常表达的碱基序列如SEQIDNO.23所示:CTCAGGTGTGGAGTAGGACAGGCCTCTGTCCTTCAATCCGTGGTTCCAATGCCCATCTGCTTCTCGGCCCTGCCAGGAAAGACTGACCTTACCATGCdc20基因正常表达的碱基序列如SEQIDNO.24所示:AGGGAGGTGTTGATTTTCCCAGCGTCTAGACTCACTCCGTTGCCACAGGTTATCAGAACAGACTGAAAGTACTCTACAGC将测序仪测得的样本基因序列和正常表达的基因序列比对,结果可以看到,样本BubR1基因序列与正常表达的BubR1基因序列的区别在于样本基因第64位碱基由G突变成A,第158位碱基由T突变成G;样本Mad1基因序列与正常表达的Mad1基因序列的区别在于样本第38位碱基由C突变成T,第64位碱基由G突变成A;样本Mad2基因序列与正常表达的Mad2基因序列的区别在于样本第55位碱基由C突变成A;样本AURKB基因序列与正常表达的AURKB基因序列的区别在于样本第57位碱基由G突变成A;样本PlK1基因序列与正常表达的PlK1基因序列的区别在于样本第72位碱基由G突变成T;样本Cdc20基因序列与正常表达的Cdc20基因序列的区别在于样本第42位碱基由G突变成A。样本基因组中与纺锤体组装检验点相关的6种基因表达均存在异常,说明样本供体很可能为大肠癌患者或潜伏者,而所取粪便样本确实来自大肠癌患者,验证了本发明试剂盒检测的准确度。实施例五本实施例中的粪便样本来自10名受试者,其中5名为大肠癌患者,5名为健康受试者。对粪便样本编号1-10,试验者并不清楚粪便样本的来源,对每个粪便样本使用3种方法检测:方法1:检测1种SAC相关基因;方法2:检测3种SAC相关基因;方法3:采用本发明试剂盒来同时检测6种SAC相关基因。通过检测结果判断粪便样本提供者是否为大肠癌患者,检测结果见表4。其中,“+”表示基因正常表达;“-”表示基因异常表达;“/”表示没有检测。若各基因表达均异常,则大肠癌检测结果为阳性;若大肠癌各基因表达均正常,则大肠癌检测结果为阴性;若各基因检测结果为大部分正常/异常,小部分异常/正常,则大肠癌检测结果可能出现弱阴性或弱阳性。表4受试者的基因检测结果从表4的结果可以看到,编号1、5和7的粪便样本在仅检测其中一种SAC相关基因的时候,出现假阴性的结果,编号8的粪便样本在仅检测其中一种SAC相关基因的时候,出现假阳性的结果,说明仅检测一种SAC相关基因的表达情况,准确率低,并不足以判断粪便的供体是否为大肠癌患者或为大肠癌潜伏期患者。当检测编号5和8的粪便样本中的3种基因时,编号5的BubR1基因检测结果不准确,编号8的Mad1基因检测结果不准确,分别得出弱阳性和弱阴性的结果;而使用本发明的试剂盒,同时检测6种SAC相关基因得到的结果为编号1、3、5、6和7呈阳性,推断其粪便样本来自大肠癌患者;编号2、4、8、9和10呈阴性,推断其粪便样本来自健康的受试者。粪便样本搜集人员告知,编号为1、3、5、6和7的粪便样本来自大肠癌患者,其粪便检测结果理论上为阳性;编号2、4、8、9和10的粪便样本来自健康的受试者,其粪便检测结果理论上为阴性。综上所述,本试剂盒检测得到的结果与粪便的实际来源相符,说明本发明的试剂盒检测结果准确,而且同时检测6种基因,非常便捷。以上所述仅为本发明较佳实施例,并不用于局限本发明,凡在本发明的精神和原则之内所做的修改、等同替换和改进等,均需要包含在发明的保护范围之内。SEQUENCELISTING<110>刘鹏飞<120>大肠癌纺锤体组装检验点检测用试剂体系和试剂盒及应用<130>OICN160078<160>30<170>PatentInversion3.5<210>1<211>18<212>DNA<213>人工序列<400>1tggctgtagtgttgaata18<210>2<211>18<212>DNA<213>人工序列<400>2cctactggttctaccttc18<210>3<211>18<212>DNA<213>人工序列<400>3tcaggttgttaagtccag18<210>4<211>20<212>DNA<213>人工序列<400>4ctcgtttccatattctcttc20<210>5<211>22<212>DNA<213>人工序列<400>5agggataatgaattttctgtaa22<210>6<211>19<212>DNA<213>人工序列<400>6cgagtaaaggtttcagatg19<210>7<211>18<212>DNA<213>人工序列<400>7gggtttagggatgagaag18<210>8<211>19<212>DNA<213>人工序列<400>8gcacttacgttaagatgtc19<210>9<211>18<212>DNA<213>人工序列<400>9ctcaggtgtggagtagga18<210>10<211>20<212>DNA<213>人工序列<400>10catggtaaggtcagtctttc20<210>11<211>18<212>DNA<213>人工序列<400>11agggaggtgttgattttc18<210>12<211>20<212>DNA<213>人工序列<400>12gctgtagagtactttcagtc20<210>13<211>27<212>DNA<213>人工序列<400>13tcaaccacttatcatcatctccactgt27<210>14<211>20<212>DNA<213>人工序列<400>14tctcctcctcccgtctctgc20<210>15<211>22<212>DNA<213>人工序列<400>15tcgtaagccgtagttgacgtaa22<210>16<211>25<212>DNA<213>人工序列<400>16ccactgctattctccatcaccttct25<210>17<211>27<212>DNA<213>人工序列<400>17ctgtccttcaatccgtggttccaatgc27<210>18<211>25<212>DNA<213>人工序列<400>18actccgttgccacaggttatcagaa25<210>19<211>170<212>DNA<213>测序仪测得的BubR1序列<400>19tggctgtagtgttgaatacactaaaggcagcaaaggatggaagcaagggacaccagttaa60gagattattgaaataattcagctcaaaagtgagttgagccaggtggaaaacagtggagat120gatgataagtggttgatttctgtatatattttgaagggagaaccagtagg170<210>20<211>200<212>DNA<213>测序仪测得的Mad1序列<400>20ctcgtttccatattctcttcctctcctcctcccgtctttgcccagcccctggcttccctc60taaaaagatgctgttcctaagggtctgcaatgaattttccttctttcagagaaagacttc120caagttgtgtgccccgggaatgaaatggaataagagaacgaggtggagtagggcaagagt180ccctggacttaacaacctga200<210>21<211>101<212>DNA<213>测序仪测得的Mad2序列<400>21cgagtaaaggtttcagatggatatatgccacgctgatataaaatgctgttgatgacgaat60gctgcaagcaaaagaaatgttacagaaaattcattatccct101<210>22<211>122<212>DNA<213>测序仪测得的AURKB序列<400>22gcacttacgttaagatgtcgggtgtcccactgctattctccatcaccttctggccaaggg60cagctaaggagagaacaggtaggttgaatgcgaacagggatgaccttctcatccctaaac120cc122<210>23<211>96<212>DNA<213>测序仪测得的Plk1序列<400>23ctcaggtgtggagtaggacaggcctctgtccttcaatccgtggttccaatgcccatctgc60ttctcggcccttccaggaaagactgaccttaccatg96<210>24<211>80<212>DNA<213>测序仪测得的Cdc20序列<400>24agggaggtgttgattttcccagcgtctagactcactccgttaccacaggttatcagaaca60gactgaaagtactctacagc80<210>25<211>170<212>DNA<213>BubR1正常表达序列<400>25tggctgtagtgttgaatacactaaaggcagcaaaggatggaagcaagggacaccagttaa60gaggttattgaaataattcagctcaaaagtgagttgagccaggtggaaaacagtggagat120gatgataagtggttgatttctgtatatattttgaaggtagaaccagtagg170<210>26<211>200<212>DNA<213>Mad1正常表达的序列<400>26ctcgtttccatattctcttcctctcctcctcccgtctctgcccagcccctggcttccctc60taagaagatgctgttcctaagggtctgcaatgaattttccttctttcagagaaagacttc120caagttgtgtgccccgggaatgaaatggaataagagaacgaggtggagtagggcaagagt180ccctggacttaacaacctga200<210>27<211>101<212>DNA<213>Mad2正常表达的序列<400>27cgagtaaaggtttcagatggatatatgccacgctgatataaaatgctgttgatgccgaat60gctgcaagcaaaagaaatgttacagaaaattcattatccct101<210>28<211>122<212>DNA<213>AURKB正常表达的序列<400>28gcacttacgttaagatgtcgggtgtcccactgctattctccatcaccttctggccagggg60cagctaaggagagaacaggtaggttgaatgcgaacagggatgaccttctcatccctaaac120cc122<210>29<211>96<212>DNA<213>Plk正常表达的序列<400>29ctcaggtgtggagtaggacaggcctctgtccttcaatccgtggttccaatgcccatctgc60ttctcggccctgccaggaaagactgaccttaccatg96<210>30<211>80<212>DNA<213>Cdc20正常表达的序列<400>30agggaggtgttgattttcccagcgtctagactcactccgttgccacaggttatcagaaca60gactgaaagtactctacagc80当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1