一种功能化杀菌微球及其制备方法和应用与流程
本发明涉及杀菌领域,尤其涉及一种功能化杀菌微球及其制备方法和应用。
背景技术:
目前常用的饮用水及饮料常用的杀菌方法分别为:热杀菌和非热杀菌。其中,热杀菌主要有:湿热杀菌、干热杀菌、微波杀菌、电热杀菌和电场杀菌等;非热杀菌主要有:化学与生物杀菌、辐照杀菌、紫外线杀菌、脉冲杀菌、超高静压杀菌、脉冲电场(pef)杀菌以及振动磁场杀菌等。热杀菌又可分为高热杀菌和低热杀菌。高热杀菌是利用高温使微生物蛋白质变性以达到杀菌的目的。虽然高热杀菌的杀菌速度较快,杀菌也较为彻底,但往往会破坏液体饮料的营养及品质。低热杀菌最常见的是巴氏杀菌,也是目前最常用的液体食品杀菌技术,简单方便。但其设备较为庞大,而且相比常温杀菌还是需要较多的能耗。化学杀菌是非热杀菌中最常见的方法,也是目前饮用水杀菌的常规方法,其多利用氧化型杀菌剂产生的次氯酸、原子态氧等,使微生物体内一些与代谢有密切关系的酶发生氧化作用而杀灭微生物。但氧化性杀菌剂有它不可克服的缺点:当水源中有机物含量稍高,氯气杀菌将产生氯代有机物,可致癌;稳定性欠佳,易分解,运输贮藏成本高,并存在爆炸等潜在威胁。如果能开发一种价格经济、使用简单、高效、安全的新型杀菌剂,不破坏营养成分的同时,无有害物质残留,而且无需过多专业知识即会使用,非但能改善现做饮料的卫生状况,还可以提高罐装水和饮料的安全,成为提高水质的关键技术之一。
技术实现要素:
本发明提供一种功能化杀菌微球及其制备方法和应用,用来解决现有技术中可溶性杀菌剂残留水体的问题。
为了解决上述技术问题,本发明提供以下技术方案:
(1)将氯球置于反应溶剂dmf中,直至氯球充分溶涨;
(2)在步骤(1)的所得物中加入5-巯基-1-甲基四唑和一定量催化剂金属钠,在氮气保护条件下,保持85-95℃温度搅拌反应11-13小时;
(3)过滤步骤(2)的所得物,得到微球,用反应溶剂浸泡洗涤直至洗涤液无色或微球表面无明显附着物,用蒸馏水洗涤后,用naoh水溶液浸泡,水洗,再依次用无水乙醇、丙酮、乙醚反复洗涤后,过滤微球置于50℃下真空干燥;
(4)在氮气保护条件下,将步骤(3)的所得物置于环氧丙烷中,其中氯球与环氧丙烷的质量体积比为2mg:0.5-1.5ml,于18-22℃下搅拌反应5-8小时,再加入苄氯,氯球与苄氯的质量体积比为1mg∶1-1.5ml。在常温下搅拌反应5-8小时后滤出,用无水乙醇和蒸馏水反复洗涤至表面无环氧丙烷残留,过滤后将微球置于50℃下真空干燥,即得到不溶的固定化杀菌微球。
其反应路线如下:
步骤(1)中,所述氯球与反应溶剂dmf的质量体积比为3mg:1-3ml。
步骤(2)中,5-巯基-1-甲基四唑与氯球的摩尔比为2-5:1,催化剂金属钠加入量为氯球加入量的5%。
本发明的杀菌微球在饮用水或饮料杀菌中的应用。能有效地杀灭饮用水中的微生物,避免水溶性杀菌剂带来的“二次污染”和水体残留问题。
本发明中所用的氯球是交联度为8%dvb,含氮量19.15%,比表面43m2·g‐1的大孔型交联氯甲基化聚苯乙烯珠体,购于南开大学化工厂,是一种极易改性修饰的高分子树脂。
本发明相对于现有技术,具有以下优点:
1.本发明所用的原材料是一种极易改性修饰的树脂氯球,它有较高的机械强度和物理稳定性,具有耐溶胀,耐氧化,耐磨损,耐温度变化,不易碎裂,再生方便等优点,来源广泛,价格低廉,同时由于其有较高的化学反应活性基团氯甲基(–ch2cl),能固定更多不同类型的杀菌功能基,性能稳定,固载量大,杀菌效果也能够更高。本发明创造性地选用多元含氮杂环作为氯球固载的功能基因子,属杂环季铵盐。与目前常见的长链季铵盐杀菌剂相比,不仅具有功能基不易从母体上脱落,不会造成杀菌剂失效和“二次污染”的优点,而且还可以有效地克服直链季铵盐长期使用后会产生抗性影响其性能的缺点,具有明显的经济效益。
2.本发明提供的新型固定化杀菌剂的反应路线简单,合成方法操作方便,只需要母体接枝功能基试剂和接枝后季铵化两步反应即可完成,条件容易实现,两步反应只需要在85-95℃和室温下在三颈瓶中进行即可,无需大型仪器设备,所以容易实现批量生产及自动化控制,具有良好的应用前景。
3.本发明提供的新型杀菌微球主要有以下三点性能优势:1)作用时间短,杀菌效率高,实际自来水杀菌应用中可在1小时之内达到100%杀菌,且在杀菌过程中具有持续时间久,基团不易从载体中脱落,投放量少等优点,比小分子杀菌剂有更好的杀菌性能;2)杀菌微球较难进入动植物体内,可以有效避免由杀菌剂本身造成的“二次污染”;3)本发明提供的杀菌微球是水不溶性的,可有效克服可溶性杀菌剂残留水体的问题,且微球可回收,可重复使用,能够提高资源的利用率。
附图说明
图1是微球合成装置搭建示意图;
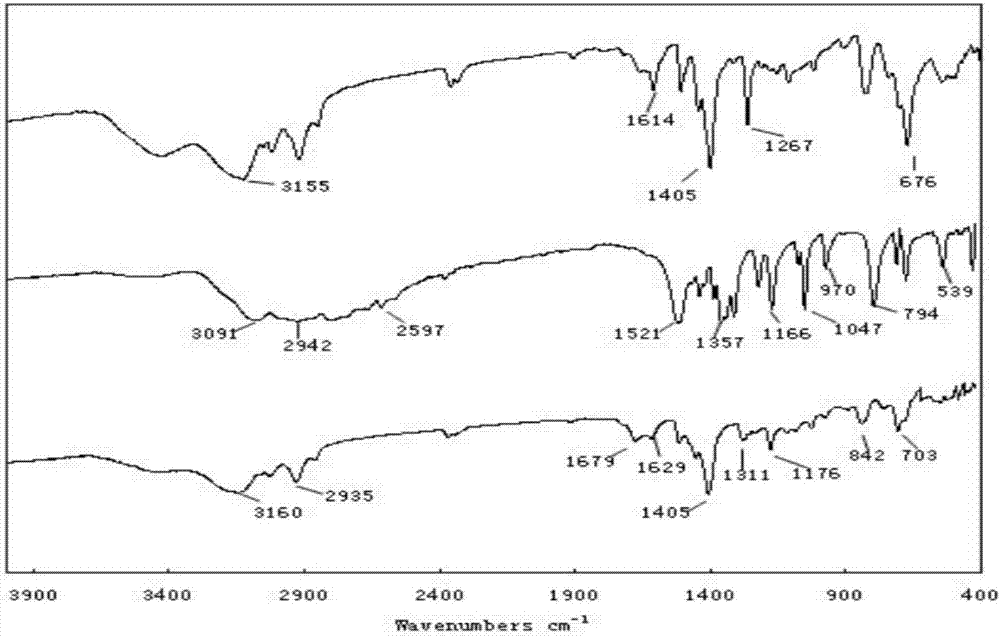
图2所示为氯球、mmt、mmtr的红外光谱图;
图3所示为不同转化率的mmtr对大肠杆菌的杀菌率的对比图;
图4所示为不同转换率的mmtr对金黄色葡萄球菌的杀菌率的对比图;
图5所示为浓度为mbc的mmtr重复使用对大肠杆菌的杀菌率的对比图;
图6所示为浓度为mbc的mmtr重复使用对金黄色葡萄球菌的杀菌率的对比图;
图7所示为浓度为mbc的mmtr在自来水中杀菌率变化曲线;
图1中,1-三颈瓶,2-冷凝管,3-搅拌棒,4-温度计,5-氮气管道。
具体实施方式
下面结合附图和具体实施方式对本发明作进一步详细的说明。
实施例1
量取40ml反应溶剂至容积为100ml的三颈烧瓶中,并加入60.0mg母体(氯球)浸泡过夜。母体充分溶胀后,向三颈烧瓶内加入一定摩尔比的5-巯基-1-甲基四唑和催化剂金属钠,在一定的温度下搅拌反应,并且反应全程通氮气保护。反应12h后,将三颈烧瓶内微球滤出,然后用反应溶剂浸泡洗涤直至洗涤液无色或微球表面无明显附着物,用蒸馏水洗涤后,再用naoh水溶液浸泡,水洗,再依次用无水乙醇、丙酮、乙醚反复洗涤数次后,过滤微球置于50℃下真空干燥备用。
合成微球的季铵化:将按上述过程的所得物放入250ml的三颈烧瓶内,用氮气将瓶内空气排尽后加入30ml的环氧丙烷,20℃下搅拌反应6h后,留向瓶内加入75ml的苄氯,常温下搅拌反应6h后滤出,并用无水乙醇和蒸馏水反复洗涤数次至表面无环氧丙烷残留,过滤后将微球置于50℃下真空干燥,即得到不溶的固定化杀菌微球(以下简称mmtr)。
本发明用傅里叶红外光谱仪对所合成的新化合物mmtr进行了结构表征:如图2所示,原来氯球中676cm-1、1265cm-1的c-cl强吸收峰消失,说明季铵化时,主要为氯苄基发生了反应。配体5-巯基1-甲基四唑的图谱中2597cm-1处-sh特征峰消失,说明其发生了反应,而在新化合物mmtr中出现了842-1176cm-1谱带可能为s-c伸缩振动峰,说明功能基试剂与载体通过巯基与氯球的氯苄基进行接枝反应。而且配体中1047-1521cm-1的四唑谱带减弱,新化合物mmtr中出现了为1405-1629cm-1谱带,表明了芳杂环的存在;而且增加了1679cm-1处c=n伸缩振动吸收峰,1311cm-1处c-n的伸缩振动峰,表明功能基试剂已经成功接枝于载体。
通过以上分析可推断出本发明制备的功能化杀菌微球,其结构式如下:
实施例2
(1)将氯球置于反应溶剂dmf中,直至氯球充分溶涨;步骤(1)中,所述氯球与反应溶剂的质量体积比为3mg:2ml。
(2)在步骤(1)的所得物中加入5-巯基-1-甲基四唑和一定量催化剂金属钠,在氮气保护条件下,保持90℃温度搅拌反应12小时,其中,5-巯基-1-甲基四唑与氯球的摩尔比为2~5:1;
(3)过滤步骤(2)的所得物,得到微球,用反应溶剂浸泡洗涤直至洗涤液无色或微球表面无明显附着物,用蒸馏水洗涤后,用naoh水溶液浸泡,水洗,再依次用无水乙醇、丙酮、乙醚反复洗涤后,过滤微球置于50℃下真空干燥;
(4)在氮气保护条件下,将步骤(3)的所得物置于环氧丙烷中,其中氯球与环氧丙烷的质量体积比为2mg:1ml,于20℃下搅拌反应6小时,再加入苄氯,氯球与苄氯的质量体积比为1mg∶1.25ml。在常温下搅拌反应6小时后滤出,用无水乙醇和蒸馏水反复洗涤至表面无环氧丙烷残留,过滤后将微球置于50℃下真空干燥,即得到不溶的固定化杀菌微球。
实施例3
本发明的杀菌微球的制备方法,包括以下步骤:
(1)将氯球置于反应溶剂dmf中,直至氯球充分溶涨;所述氯球与反应溶剂dmf的质量体积比为3mg:1ml。
(2)在步骤(1)的所得物中加入5-巯基-1-甲基四唑和一定量的催化剂金属钠,在氮气保护条件下,保持85℃温度搅拌反应13小时;5-巯基-1-甲基四唑与氯球的摩尔比为2:1。
(3)过滤步骤(2)的所得物,得到微球,用反应溶剂浸泡洗涤直至洗涤液无色或微球表面无明显附着物,用蒸馏水洗涤后,用naoh水溶液浸泡,水洗,再依次用无水乙醇、丙酮、乙醚反复洗涤后,过滤微球置于50℃下真空干燥;
(4)在氮气保护条件下,将步骤(3)的所得物置于环氧丙烷中,其中氯球与环氧丙烷的质量体积比为2mg:0.5ml,于18℃下搅拌反应8小时,再加入苄氯,氯球与苄氯的质量体积比为1mg∶1ml。在常温下搅拌反应5小时后滤出,用无水乙醇和蒸馏水反复洗涤至表面无环氧丙烷残留,过滤后将微球置于50℃下真空干燥,即得到不溶的固定化杀菌微球。
实施例4
本发明的杀菌微球的制备方法,包括以下步骤:
(1)将氯球置于反应溶剂dmf中,直至氯球充分溶涨;步骤(1)中,所述氯球与反应溶剂dmf的质量体积比为3mg:1-3ml。
(2)在步骤(1)的所得物中加入5-巯基-1-甲基四唑和一定量的催化剂金属钠,在氮气保护条件下,保持95℃温度搅拌反应11小时;步骤(2)中,5-巯基-1-甲基四唑与氯球的摩尔比为2-5:1。
(3)过滤步骤(2)的所得物,得到微球,用反应溶剂浸泡洗涤直至洗涤液无色或微球表面无明显附着物,用蒸馏水洗涤后,用naoh水溶液浸泡,水洗,再依次用无水乙醇、丙酮、乙醚反复洗涤后,过滤微球置于50℃下真空干燥;
(4)在氮气保护条件下,将步骤(3)的所得物置于环氧丙烷中,其中氯球与环氧丙烷的质量体积比为2mg:1.5ml,于22℃下搅拌反应5小时,再加入苄氯,氯球与苄氯的质量体积比为1mg∶1.5ml。在常温下搅拌反应8小时后滤出,用无水乙醇和蒸馏水反复洗涤至表面无环氧丙烷残留,过滤后将微球置于50℃下真空干燥,即得到不溶的固定化杀菌微球。
对比例1
将实施例1中的反应溶剂、反应温度、搅拌转速及反应摩尔比根据下表对应组合进行对比实验,从而获得不同转化率的mmtr。
表1不同转化率的mmtr合成条件
由表1可知,mmtr的最佳反应条件为:反应溶剂为dmf,反应温度为90℃,母体与配体的反应摩尔比为1∶5,mmtr的转化率为91.3%。
对比例2
将实施例一中的反应溶剂改为甲苯或水,其余按实施例一操作,得到以下结果:
表2不同反应试剂对mmtr转化率的影响
由表2可得:在dmf作反应溶剂时,mmtr的含氮量含硫量最高,因此,mmtr的最佳反应溶剂为dmf。
对比例3
将实施例一的配体5-巯基-1-甲基四唑(mmt)改为3-氨基-5-巯基-1,2,4-三氮唑(att),腺嘌呤(at),其余按实施例一操作,得到以下结果:
表3不同配体的转化率
由表3可得:mmt作配体时,杀菌微球的合成率最高。
实验1:杀菌实验
本实验以革兰氏阴性代表细菌大肠杆菌(e.coli)cicc21524和革兰氏阳性代表细菌金黄色葡萄球菌(s.aureus)cicc10384作为受试菌,这两种菌种均购于中国工业微生物菌种保藏管理中心。具体实验操作步骤及评价方法如下:
所有菌株均作为储备培养物辅以15%(v/v)甘油的营养肉体培养基中,保持于-20℃储存。菌株置于在lb培养基内,37℃恒温振荡器中培养18小时;活化后用移液枪取出一定量菌液,在4000rmp下离心洗涤。将所得菌斑用0.85%的生理盐水通过十倍稀释法稀释成浓度约为106cfu/ml的菌悬液备用。
杀菌活性测试
取若干无菌的100ml摇瓶,加入50ml上述制备的菌悬液;在样品组中加入一定量充分溶胀的杀菌微球mmtr、attr、atr,对照组不加入杀菌微球;振荡各混合液,接触不同时间后,根据gb/t4789.3-2010提供的方法,将不同接触时间上清液分别逐级稀释,稀释至适宜浓度后用玻璃涂布棒涂匀,倒置平板于37℃下培养进行平板活菌计数。通过以下公式计算微球杀菌率:
为提高杀菌率的准确性,杀菌率由同一时间点对照组和样品组取样进行平板计数后结果根据公式计算得到。
表4所示为杀菌微球mmtr、attr、atr对e.coli,s.aureus的最低杀菌浓度(mbc),其中,杀菌时间均为3小时,atr为以腺嘌呤为功能基试剂得到的杀菌微球,attr为以3-氨基-5-巯基-1,2,4-三氮唑为功能基试剂得到的杀菌微球。
表4杀菌微球mmtr、attr、atr对e.coli,s.aureus的最低杀菌浓度(mbc)
由表4可知,atr对两种受试菌均无杀灭效果,而attr对两种受试菌的杀菌效果不及mmtr。
此外,图3所示为不同转化率的mmtr对大肠杆菌的杀菌率的对比图;图4所示为不同转换率的mmtr对金黄色葡萄球菌的杀菌率的对比图。由图3可知,mmtr的转化率越高,大肠杆菌的杀菌率越高;由图4可知,mmtr的转化率越高,金黄色葡萄球菌的杀菌率越高。
实验2:杀菌微球的重复使用
将杀菌后的微球过滤晾干,置于摇瓶中,加入hcl与etoh以1:8(v/v)的混合溶液30ml,振荡2.5h后,用蒸馏水和生理盐水冲洗3~5遍后重新用于杀菌,杀菌时间与再生前相同,为3h。
图5所示为浓度为mbc的mmtr重复使用对大肠杆菌的杀菌率的对比图;图6所示为浓度为mbc的mmtr重复使用对金黄色葡萄球菌的杀菌率的对比图。由图5及图6可知,本发明较佳实施例提供的杀菌微球的重复使用后对大肠杆菌及金黄色葡萄球菌的杀菌率影响不大。换言之,本发明较佳实施例提供的杀菌微球的重复使用效果好。
实验3:mmtr在自来水中的实际应用
自取的自来水经过平板计数法测定,其中菌落总数约为85cfu·ml-1,符合城市自来水的国家标准(gb5749-2006)。取若干无菌的100ml摇瓶,加入50.0ml的自来水;样品组中加入一定量充分溶胀的杀菌微球,对照组不加入杀菌微球;振荡各混合液,接触不同时间后,将不同接触时间上清液分别逐级稀释,进行平板活菌计数。仍然以公式计算杀菌率。
通过上述实验测得mmtr作用于自来水时的最低杀菌浓度(mbc)为0.3mg·ml-1,由图7中mmtr在自来水中杀菌率与时间的关系曲线可以显示杀菌微球可在250min后将自来水的菌全部杀死,虽然自来水中总菌数不多,但自来水中含有许多无机盐、金属离子或其他小分子物质。金属离子及部分无机离子可能易被mmtr的含氮杂环吸附,证明其具有良好的广谱抗菌性和应用前景。
上述实施例不以任何方式限制本发明,凡是采用等同替换或等效变换的方式获得的技术方案均落在本发明的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!