一种琥珀酸美托洛尔晶型及其制备方法与流程
本申请是申请号为cn201210208496.2、申请日为2012年06月25日、发明名称为“一种琥珀酸美托洛尔晶型及其制备方法”的发明专利申请的分案申请。
本发明属于抗高血压药物领域,具体涉及琥珀酸美托洛尔晶型及其制备方法。
背景技术:
美托洛尔是β1-选择性(心选择性)肾上腺素受体阻断剂,即心脏选择性药物。其在临床上广泛用于高血压和缺血性心脏病、慢性稳定性心力衰竭、心律失常等多种心血管疾病患者的治疗,系近年来世界高血压治疗的首选药,也是我国的基本药物。
1975年,阿斯利康公司以其酒石酸盐形式上市,商品名“倍他乐克”。由于酒石酸美托洛尔的溶解度很大(>700mg/ml),为了获得更为缓慢而持久释放美托洛尔的目的,阿斯利康公司又开发了商品名为“toprol-xl”的琥珀酸美托洛尔,其在37℃水中的溶解度(270mg/ml)显著低于酒石酸美托洛尔,并于1992年获美国fda批准用于治疗高血压和心绞痛。目前国内广泛使用酒石酸美托洛尔,国内尚无琥珀酸美托洛尔原料上市。
琥珀酸美托洛尔(metroprololsuccinate,结构式如式1所示),化学名为1-异丙氨基-3-[对-(2-甲氧乙基)苯氧基]-2-丙醇琥珀酸盐,该药具有较低的溶解度,适合制备缓控释制剂,副作用小,用药安全性高,可作为高血压患者的长期用药。
关于琥珀酸美托洛尔,现有技术中公开如下:
中国专利cn102295569公开了一种(s)-琥珀酸美托洛尔的制备方法,采用乙醇、丙酮、异丙醇结晶,但没有对晶型进行研究。
wo2007141593公开了一种琥珀酸美托洛尔的晶型,其晶型的x-射线粉末衍射在2θ为7.1、11.5、12.2、13.1、14.1、14.4、14.9、17.2、20.1、22.8、23.1、24.3、24.6、25.8、26.2、27.2、30.1、31.9、33.4处有峰,结晶溶剂为异丙醇。
鉴于琥珀酸美托洛尔的药用价值,仍需对其晶型进行研究,提供具有含量(或纯度)高、杂质含量低、质量稳定、适用于制成药物制剂的琥珀酸美托洛尔的晶型。
技术实现要素:
出人意料的,本发明人发现了一种新的琥珀酸美托洛尔晶型,含量(或纯度)高、杂质含量低、质量稳定,为琥珀酸美托洛尔药品的临床应用提供了安全保障。
一种琥珀酸美托洛尔晶型,其特征在于,使用cu-kα辐射,以2θ角度(°)表示的x-射线衍射在以下位置有峰:7.4±0.2、14.4±0.2、20.4±0.2、21.5±0.2、24.4±0.2。
一种新的琥珀酸美托洛尔的晶型,其特征在于,使用cu-kα辐射,以2θ角度(°)表示的x-射线衍射在7.4±0.2、14.4±0.2、20.4±0.2、21.5±0.2、24.4±0.2位置有峰,还在以下位置有峰:
(1)14.7±0.2、23.4±0.2、26.5±0.2;或者
(2)11.8±0.2、14.7±0.2、15.2±0.2、17.5±0.2、23.4±0.2、26.5±0.2、27.4±0.2、32.2±0.2;或者
(3)11.2±0.2、11.8±0.2、12.5±0.2、13.4±0.2、14.7±0.2、15.2±0.2、17.5±0.2、19.2±0.2、23.4±0.2、25.5±0.2、26.5±0.2、27.4±0.2、30.4±0.2、32.2±0.2、33.1±0.2、34.9±0.2、35.6±0.2、36.5±0.2、37.6±0.2、37.9±0.2、38.5±0.2、39.8±0.2、40.6±0.2、47.1±0.2、48.5±0.2、50.4±0.2;
一种新的琥珀酸美托洛尔的晶型,其特征在于,使用cu-kα辐射,以2θ角度(°)表示的x-射线衍射在7.4±0.2、14.4±0.2、20.4±0.2、21.5±0.2、24.4±0.2位置有峰,还在以下位置有峰:
(1)14.1±0.2;或者
(3)14.1±0.2、14.7±0.2;或者
(4)14.1±0.2、14.7±0.2、21.2±0.2、23.0±0.2、23.4±0.2、26.5±0.2、27.4±0.2、40.0±0.2;
上述的琥珀酸美托洛尔的晶型,熔点为136.0~138.0℃。
上述的琥珀酸美托洛尔的晶型,采用差示扫描量热(dsc)技术,以10℃/分钟升温速率进行测定,吸热最大值在136.0~138.0℃,该吸热过程在dsc谱图上表现在为一尖锐的吸热峰;该吸热峰为dsc谱图上唯一显著的吸热峰,谱图中没有明显放热峰。
本发明的另一方面还提供了一种包含本发明琥珀酸美托洛尔晶型固体物质的原料药,所述原料药用于制备抗高血压的药物。
本发明的另一方面还提供了一种包含本发明琥珀酸美托洛尔晶型固体物质的药物组合物。该药物组合物还可以包含一种或更多种药学上可接受载体,不具体限定药学上可接受载体的种类,只要它们适于药用并不会显著影响本发明琥珀酸美托洛尔晶型的药效即可。
本发明的另一方面还提供了一种包含本发明琥珀酸美托洛尔晶型固体物质的剂型,不具体限制剂型的种类,可以为片剂、胶囊、缓释制剂、控释制剂等不同的药物制剂形式,优选为琥珀酸美托洛尔缓释制剂。
本发明的另一方面还提供本发明所述的琥珀酸美托洛尔晶型固体物质的制备方法:将琥珀酸美托洛尔粗品加入无水乙醇中,加热回流至溶解,降温至-10~10℃,析出晶体为琥珀酸美托洛尔晶型样品。
一种琥珀酸美托洛尔晶型的制备方法:将琥珀酸美托洛尔粗品加入无水乙醇中,加热回流至溶解,降温至40~60℃,保温搅拌0.5~3.0小时,降温至-10~10℃,保温静置2~10小时,析出晶体为琥珀酸美托洛尔晶型样品。
其中,
琥珀酸美托洛尔粗品与无水乙醇的重量-体积比可为1:2~10,优选为1:3~8。
所述的降温至40~60℃,为0.5~2小时降温至40~60℃。
所述的保温搅拌,搅拌转速为100~300转/分。
所述的降温至-10~10℃,为1.0~3.0小时降温至-10~10℃。
一种琥珀酸美托洛尔晶型的制备方法:将琥珀酸美托洛尔粗品加入无水乙醇中,加热回流至溶解,降温至-10~10℃,保温搅拌5~15小时,析出晶体为琥珀酸美托洛尔晶型样品。
其中,
琥珀酸美托洛尔粗品与无水乙醇的重量-体积比可为1:2~10,优选为1:3~8。
所述的降温至-10~0℃,为3.0~5.0小时降温至-10~0℃。
所述的保温搅拌,搅拌转速为20~80转/分。
所述的琥珀酸美托洛尔粗品可参照cn1128786c及cn102295569所公开的方法进行制备,上述文献内容在此引入作为参考。
所述的美托洛尔粗品可以按照以下方法制备:
本发明所得的琥珀酸美托洛尔晶型,质量稳定性好,含量高,杂质含量低,更适于贮存和作为原料药开发。
附图说明
粉末x-射线衍射谱附图的检测条件如下:
仪器:xrdd8advance,由德国bruker制造
革巴:cu-kα辐射
阶跃角:0.02°
管压:40kv
管流:50ma
计算时间:0.3秒。
图1a:实施例1所得琥珀酸美托洛尔晶型样品的粉末x-射线衍射图。纵坐标轴表示衍射强度(cps),横坐标轴表示衍射角(2θ),2θ=5-60°。
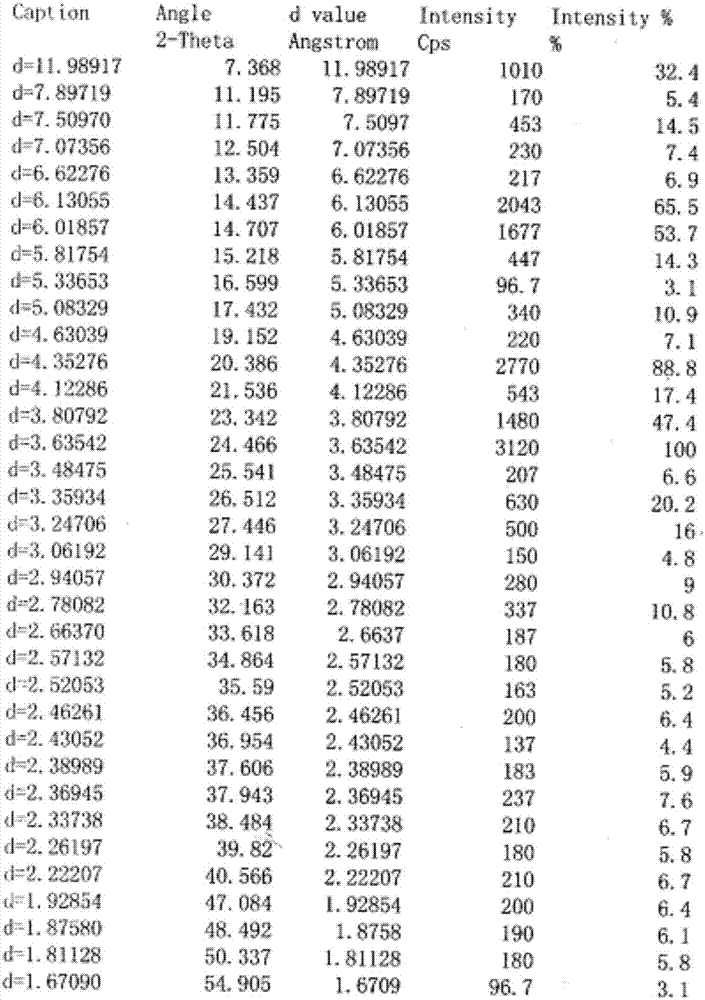
图1b:图1a图谱数据。
图2:实施例1所得琥珀酸美托洛尔晶型样品的dsc图谱。
图3a:实施例8所得琥珀酸美托洛尔晶型样品的粉末x-射线衍射图。纵坐标轴表示衍射强度(cps),横坐标轴表示衍射角(2θ),2θ=5-60°。
图3b:图3a图谱数据。
图4:实施例8所得琥珀酸美托洛尔晶型样品的dsc图谱。
具体实施方式
实施例1:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇565ml,加热回流至产品溶解,1.5小时内降温至45℃,搅拌转速为150转/分,保温搅拌1.0小时,2.0小时内降温至0℃,保温静置5.0小时,析出晶体,抽滤,真空干燥后,得白色固体131.05g,重量收率为93.6%,熔点为136.6~137.4℃。
实施例2:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇280ml,加热回流至产品溶解,0.5小时内降温至55℃,搅拌转速为100转/分,保温搅拌0.5小时,1.5小时内降温至5℃,保温静置5.0小时,析出晶体,抽滤,真空干燥后,得白色固体70.14g,重量收率为50.1%,熔点为136.1~136.7℃。
实施例3:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇420ml,加热回流至产品溶解,1.5小时内降温至47℃,搅拌转速为150转/分,保温搅拌1.0小时,2.0小时内降温至-5℃,保温静置2.0小时,析出晶体,抽滤,真空干燥后,得白色固体133.42g,重量收率为95.3%,熔点为136.2~136.8℃。
实施例4:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇700ml,加热回流至产品溶解,2.0小时内降温至40℃,搅拌转速为250转/分,保温搅拌2.5小时,2.5小时内降温至-5℃,保温静置7.0小时,析出晶体,抽滤,真空干燥后,得白色固体132.58g,重量收率为94.7%,熔点为136.9~137.7℃。
实施例5:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇840ml,加热回流至产品溶解,0.5小时内降温至60℃,搅拌转速为300转/分,保温搅拌2.0小时,3.0小时内降温至-10℃,保温静置6.0小时,析出晶体,抽滤,真空干燥后,得白色固体133.42g,重量收率为95.3%,熔点为137.2~137.8℃。
实施例6:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇980ml,加热回流至产品溶解,1.0小时内降温至50℃,搅拌转速为200转/分,保温搅拌1.5小时,1.0小时内降温至10℃,保温静置10.0小时,析出晶体,抽滤,真空干燥后,得白色固体126.14g,重量收率为90.1%,熔点为136.5~137.2℃。
实施例7:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇1400ml,加热回流至产品溶解,1.0小时内降温至52℃,搅拌转速为200转/分,保温搅拌3.0小时,2.0小时内降温至0℃,保温静置4小时,析出晶体,抽滤,真空干燥后,得白色固体119.28g,重量收率为85.2%,熔点为136.8~137.4℃。
实施例8:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇560ml,加热回流至产品溶解,4.0小时内降温至0℃,搅拌转速为70转/分,保温搅拌9.0小时,析出晶体,抽滤,真空干燥后,得白色固体129.92g,重量收率为92.8%,熔点为137.1~137.8℃。
实施例9:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇280ml,加热回流至产品溶解,3.0小时内降温至10℃,搅拌转速为60转/分,保温搅拌10.0小时,析出晶体,抽滤,真空干燥后,得白色固体77.28g,重量收率为55.2%,熔点为136.6~137.4℃。
实施例10:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇420ml,加热回流至产品溶解,4.5小时内降温至-5℃,搅拌转速为50转/分,保温搅拌12.0小时,析出晶体,抽滤,真空干燥后,得白色固体131.32g,重量收率为93.8%,熔点为136.5~137.1℃
实施例11:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇700ml,加热回流至产品溶解,3.5小时内降温至5℃,搅拌转速为40转/分,保温搅拌5.0小时,析出晶体,抽滤,真空干燥后,得白色固体130.06g,重量收率为92.9%,熔点为137.2~137.8℃
实施例12:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇840ml,加热回流至产品溶解,5.0小时内降温至-10℃,搅拌转速为30转/分,保温搅拌8.0小时,析出晶体,抽滤,真空干燥后,得白色固体131.74g,重量收率为94.1%,熔点为136.4~137.1℃
实施例13:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇980ml,加热回流至产品溶解,3.5小时内降温至3℃,搅拌转速为20转/分,保温搅拌15.0小时,析出晶体,抽滤,真空干燥后,得白色固体127.68g,重量收率为91.2%,熔点为136.3~137.0℃
实施例14:琥珀酸美托洛尔晶型的制备
将琥珀酸美托洛尔粗品140g,加无水乙醇1400ml,加热回流至产品溶解,4.5小时内降温至-8℃,搅拌转速为80转/分,保温搅拌13.0小时,析出晶体,抽滤,真空干燥后,得白色固体114.1g,重量收率为81.5%,熔点为136.9~137.7℃。
将实施例1~14得到的琥珀酸美托洛尔晶型样品进行将x-射线衍射分析(简称:xrd),所得的x-射线衍射数据如表1-1、表1-2所示。
表1-1实施例1~7晶型样品x-射线衍射数据
表1-2实施例8~14晶型样品x-射线衍射数据
由表1-1、表1-2可以看出:实施例1~14所得的晶型样品x-射线衍射在反射角2θ为7.4±0.2、14.4±0.2、20.4±0.2、21.5±0.2、24.4±0.2处有峰,为同一晶型。
由表1-1可以看出:实施例1~7所得的晶型样品特征峰的峰位、峰型几乎完全一致,是同一晶型。
由表1-2可以看出:实施例8~14所得晶型样品特征峰的峰位、峰型几乎完全一致,是同一晶型。
本发明研究人员长期致力于琥珀酸美托洛尔原料药的研究,为了获得质量稳定的琥珀酸美托洛尔的新晶型,发明人对本发明的晶型进行了稳定性试验。
实施例15:琥珀酸美托洛尔晶型稳定性试验
1、加速试验
根据(中国药典2010年版二部附录xixc)相关规定进行本品的加速试验。
取各实施例样品适量,模拟上市包装,在温度40℃±2℃、相对湿度为75%±5%条件下放置6个月,分别于第1、2、3、6个月末取样,比较外观后测试其它考察指标,结果与0月数据比较。将加速6个月后的样品进行x-射线衍射分析(简称:xrd),观察与0月晶型是否一致,加速试验结果见表2-1、表2-2。
表2-1实施例1~7晶型样品加速试验稳定性结果表
表2-2实施例8~14晶型样品加速试验稳定性结果表
加速试验结果表明:在模拟上市包装条件下,各实施例样品在温度40℃±2℃、相对湿度为75%±5%条件下放置6个月,各项检测指标均无显著性变化,符合规定。
x-射线衍射分析结果表明:本发明琥珀酸美托洛尔的晶型加速6个月后的x-射线衍射图谱与0月图谱完全一致,表明本发明的晶型在加速条件放置6个月,稳定性良好。
2、长期实验
根据(中国药典2010年版二部附录ⅺxc)相关规定进行本品的长期试验。
取各实施例样品适量,模拟上市包装,在温度25℃±2℃、相对湿度为60%±10%条件下放置,于第3、6、9、12月各取样一次,比较外观后测试其它考察指标,结果与0月数据比较。将长期12个月后的样品进行x-射线衍射分析(简称:xrd),观察与0月晶型是否一致,长期试验结果见表3-1、表3-2。
表3-1实施例1~7晶型样品长期试验稳定性结果表
表3-2实施例8~14晶型样品长期试验稳定性结果表
长期试验结果表明:各实施例样品在模拟上市包装条件下,在25℃±2℃、相对湿度为60%±10%的环境中放置了12个月,各月的检测数据与0月数据比较,各项指标均无显著性变化。试验结果表明:本品在长期试验条件下比较稳定。
x-射线衍射分析结果表明:本发明琥珀酸美托洛尔的晶型,长期12个月后的x-射线衍射图谱与0月图谱完全一致,表明本发明的晶型在长期条件放置12个月,稳定性良好。
以上结果表明:本发明琥珀酸美托洛尔的晶型,含量高、杂质含量低、质量稳定、晶型稳定,可以作为原料药使用。
- 还没有人留言评论。精彩留言会获得点赞!