苯基桥联的三芳胺及二茂铁端基化合物及其制备方法和应用与流程
本发明涉及光电材料
技术领域:
,特别涉及一种苯基桥联的三芳胺及二茂铁端基化合物及其制备方法和应用。
背景技术:
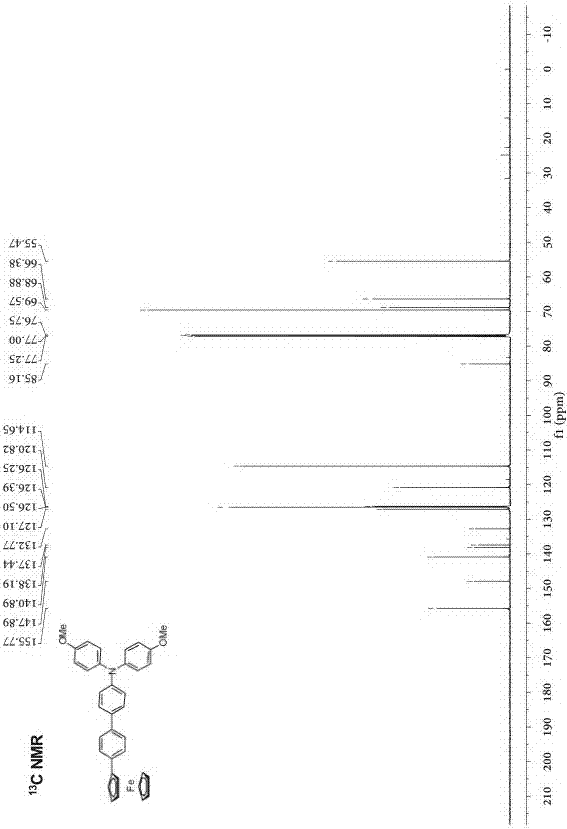
:二茂铁是茂金属化合物,可与有机共轭分子构成金属有机化合物,如二茂铁乙炔类化合物。三芳胺及其衍生物是一类重要的有机分子,在医药中间体、农药、染料化工、有机材料等领域有着广泛的应用,因其有着优秀的电荷传输性能,也常被作为有机光电材料来研究。从已公开的文献中可以知道,二茂铁及三芳胺均具有优良的电化学活性以及稳定性。近年来,已经有不少数量的文献公开了共轭配体桥联的双二茂铁或双三芳胺化合物的合成方法及其电子耦合性质研究和在分子电子器件中的应用。若能够以二茂铁及三芳胺分别作为氧化还原活性端基共轭桥联合成有机-无机混杂的分子导线模型,将为新型分子导线的设计与合成提供了另外一条新途径,令人遗憾的是,至今仍还未见到与此相关的任何报道。技术实现要素:本发明要解决的技术问题是提供一种苯基桥联的三芳胺及二茂铁端基化合物。进一步,本发明还提供上述化合物的制备方法以及其在分子导线方面的应用。为了解决上述技术问题,本发明采用如下技术方案:苯基桥联的三芳胺及二茂铁端基化合物,其结构式为:;其中r为h或ch3或och3;中间苯环连接点分别处在各自苯环的间位(m)或对位(p)。作为本发明的另一方面,制备上述苯基桥联的三芳胺及二茂铁端基化合物的方法包括以下步骤:往反应容器中加入硼酸酯取代的三芳胺,单溴代苯基二茂铁,碳酸钾,四(三苯基膦)钯,甲苯,乙醇及水,在搅拌回流下反应12~24小时后冷却,混合体系用ch2cl2溶剂萃取,所得有机相用饱和nacl溶液洗涤,然后用无水na2so4干燥,过滤后得滤液,脱除滤液中的溶剂并分离出其它杂质后得到橙红色固体,即为苯基桥联的三芳胺及二茂铁端基化合物。其中,所述碳酸钾按浓度为2mol/l配成溶液并按每毫摩尔硼酸酯取代的三芳胺或单溴代苯基二茂铁加4-5ml的配比添加。其中,所述四(三苯基膦)钯按硼酸酯取代的三芳胺或单溴代苯基二茂铁质量的5%-10%添加。其中,所述硼酸酯取代的三芳胺与单溴代苯基二茂铁的质量比为1:1-1.1:1。其中,所述甲苯按每毫摩尔硼酸酯取代的三芳胺或单溴代苯基二茂铁加20-25ml的配比进行添加,所述乙醇和水按每毫摩尔硼酸酯取代的三芳胺或单溴代苯基二茂铁各加4-5ml的配比进行添加。其中,所述滤液中的溶剂在压强为0.005-0.01kpa、温度为30-35℃条件下,用旋转蒸发仪旋转蒸发脱除;所述其它杂质采用柱色谱分离,所柱色谱分离采用乙酸乙酯和石油醚配制而成的洗脱剂,所述洗脱剂中乙酸乙酯和石油醚的体积比为1:10-1:5。作为本发明的另一方面,上述苯基桥联的三芳胺及二茂铁端基化合物的应用包括将其作为分子导线材料。本发明取得的有益效果在于:本发明选择二茂铁及三芳胺分别作为氧化还原活性端基,通过共轭的苯环桥联合成了有机-无机混杂的分子导线模型,得到了一种具有全新结构的化合物,经电化学方法测试发现该化合物端基之间具有较强的电子相互作用,可以以该化合物为基础开发出新的分子导线材料,该全新结构的化合物可为后续新型分子导线的设计与合成开辟一条新的途径。附图说明:图1为实施例1所得化合物的核磁共振氢谱图;图2为实施例1所得化合物的核磁共振碳谱图;图3为实施例2所得化合物的核磁共振氢谱图;图4为实施例2所得化合物的核磁共振碳谱图;图5为实施例3所得化合物的核磁共振氢谱图;图6为实施例3所得化合物的核磁共振碳谱图;图7为实施例4所得化合物的核磁共振氢谱图;图8为实施例4所得化合物的核磁共振碳谱图。具体实施方式为了便于本领域技术人员的理解,下面结合4个实施例对本发明作进一步的说明,实施例提及的内容并非对本发明的限定。一、制备新化合物。需要提前说明的是,下述实施例仅列举了r基团为och3的制备过程与测试结果,本领域技术人员应当明白,当r基团为h或ch3时,其制备过程及测试结果与以下实施例近似,为简化表述,就不再一一说明。实施例1:制备苯基桥联的三芳胺及二茂铁端基化合物:在圆底烧瓶中加入硼酸酯取代的三芳胺0.2g(0.464mmol)、单溴代苯基二茂铁0.143g(0.420mmol)、浓度为2mol/l的碳酸钾溶液2ml、2ml乙醇及10ml甲苯,混合体系搅拌下加热回流24h,冷却,混合体系用ch2cl2溶剂萃取,所得有机相用饱和nacl溶液洗涤,然后用无水na2so4干燥,过滤,在压强为0.01kpa,温度为30℃下,用旋转蒸发仪旋干滤液,经柱色谱分离(洗脱剂:乙酸乙酯/石油醚(v/v=1:8),得橙红色固体182mg,产率:77%。。元素分析(c36h31feno2):理论值:c,76.46;h,5.53。测定值:c,76.55;h,5.38。结构数据:1hnmr(500mhz,cdcl3):δ3.78(s,6h,-och3),4.05(s,5h,fc-h),4.31(s,2h,fc-h),4.65(s,2h,fc-h),6.84(d,j(hh)=5.0hz,4h),6.99(d,j(hh)=10.0hz,2h),7.08(d,j(hh)=5.0hz,4h),7.44(d,j(hh)=10.0hz,2h),7.49(dd,j(hh)=10.0hz,4h).13cnmr(125mhz,cdcl3):δ55.47(och3),66.38,68.88,69.57,85.16,114.65,120.82,126.25,126.39,126.50,127.10,132.77,137.44,138.19,140.89,147.89,155.77.实施例2:制备苯基桥联的三芳胺及二茂铁端基化合物:在圆底烧瓶中加入硼酸酯取代的三芳胺0.2g(0.464mmol)、单溴代苯基二茂铁0.143g(0.420mmol)、浓度为2mol/l的碳酸钾溶液2ml、2ml乙醇及10ml甲苯,混合体系搅拌下加热回流24h,冷却,混合体系用ch2cl2溶剂萃取,所得有机相用饱和nacl溶液洗涤,然后用无水na2so4干燥,过滤,在压强为0.01kpa,温度为30℃下,用旋转蒸发仪旋干滤液,经柱色谱分离(洗脱剂:乙酸乙酯/石油醚(v/v=1:8),得橙红色固体160mg,产率:67%。元素分析(c36h31feno2):理论值:c,76.46;h,5.53。测定值:c,76.41;h,5.60。结构数据:1hnmr(500mhz,cdcl3):δ3.80(s,6h,-och3),4.05(s,5h,fc-h),4.31(s,2h,fc-h),4.67(s,2h,fc-h),6.85(d,j(hh)=10.0hz,4h),7.01(d,j(hh)=5.0hz,2h),7.10(d,j(hh)=5.0hz,4h),7.31(t,j(hh)=5.0hz,1h),7.36(d,j(hh)=5.0hz,1h),7.40(d,j(hh)=5.0hz,1h),7.44(d,j(hh)=5.0hz,2h),7.64(s,1h).13cnmr(125mhz,cdcl3):δ55.47(och3),66.60,68.87,69.59,85.59,114.68,120.71,124.25,124.31,124.49,126.58,127.54,128.62,133.12,139.58,140.84,140.89,148.16,155.85.实施例3:制备苯基桥联的三芳胺及二茂铁端基化合物:在圆底烧瓶中加入硼酸酯取代的三芳胺0.4g(0.928mmol)、单溴代苯基二茂铁0.286g(0.840mmol)、浓度为2mol/l的碳酸钾溶液5ml、5ml乙醇及20ml甲苯,混合体系搅拌下加热回流24h,冷却,混合体系用ch2cl2溶剂萃取,所得有机相用饱和nacl溶液洗涤,然后用无水na2so4干燥,过滤,在压强为0.01kpa,温度为30℃下,用旋转蒸发仪旋干滤液,经柱色谱分离(洗脱剂:乙酸乙酯/石油醚(v/v=1:8),得橙红色固体266mg,产率:56%。。元素分析(c36h31feno2):理论值:c,76.46;h,5.53。测定值:c,76.39;h,5.62。结构数据:1hnmr(500mhz,cdcl3):δ3.77(s,6h,-och3),4.01(s,5h,fc-h),4.30(s,2h,fc-h),4.62(s,2h,fc-h),6.84(d,j(hh)=10.0hz,4h),6.93(d,j(hh)=10.0hz,1h),7.11(d,j(hh)=10.0hz,5h),7.19(s,1h),7.23-7.30(m,3h),7.39(d,j(hh)=5.0hz,1h),7.57(s,1h).13cnmr(125mhz,cdcl3):δ55.43(och3),66.64,68.86,69.56,85.49,114.68,119.22,119.33,119.49,124.76,125.00,125.12,126.58,128.52,129.25,139.58,140.95,141.23,142.04,149.22,155.80.实施例4:制备苯基桥联的三芳胺及二茂铁端基化合物:在圆底烧瓶中加入硼酸酯取代的三芳胺0.2g(0.464mmol)、单溴代苯基二茂铁0.143g(0.420mmol)、浓度为2mol/l的碳酸钾溶液2ml、2ml乙醇及10ml甲苯,混合体系搅拌下加热回流24h,冷却,混合体系用ch2cl2溶剂萃取,所得有机相用饱和nacl溶液洗涤,然后用无水na2so4干燥,过滤,在压强为0.01kpa,温度为30℃下,用旋转蒸发仪旋干滤液,经柱色谱分离(洗脱剂:乙酸乙酯/石油醚(v/v=1:8),得橙红色固体140mg,产率:59%。。元素分析(c36h31feno2):理论值:c,76.46;h,5.53。测定值:c,76.57;h,5.44。结构数据:1hnmr(500mhz,cdcl3):δ3.77(s,6h,-och3),4.01(s,5h,fc-h),4.29(s,2h,fc-h),4.62(s,2h,fc-h),6.84(d,j(hh)=10.0hz,4h),6.93(d,j(hh)=10.0hz,1h),7.11(d,j(hh)=5.0hz,5h),7.19(t,j(hh)=5.0hz,1h),7.23(d,j(hh)=5.0hz,1h),7.27-7.29(m,2h),7.39(d,j(hh)=5.0hz,1h),7.58(s,1h).13cnmr(125mhz,cdcl3):δ55.43(och3),66.64,68.86,69.56,85.49,114.68,119.22,119.33,119.49,124.75,125.00,125.12,126.57,128.52,129.26,139.59,140.95,141.23,142.04,149.22,155.80.在上述4个实施例中,硼酸酯取代的三芳胺、单溴代苯基二茂铁为反应物,碳酸钾溶液作为催化剂,当然也可以采用四(三苯基膦)钯或者包含碳酸钾和四(三苯基膦)钯的复合型催化剂,甲苯、乙醇及水为反应所需溶剂。上述4个实施例所得化合物结构不同的原因在于所采用的硼酸酯取代的三芳胺、单溴代苯基二茂铁结构不同(即反应物分子式相同,但结构不同),从而导致了虽然原料配比及反应条件相近,但最终所得苯基桥联的三芳胺及二茂铁端基化合物结构不同的情况。二、测试上述4个实施例所得苯基桥联的三芳胺及二茂铁端基化合物端基之间的电子耦合性能。测量方法:电化学测量采用的是电化学工作站chi660c(chinstrumentscompany,usa)。以玻碳电极作为工作电极,铂电极作对电极,ag+|ag电极为参比电极。以0.001moll-1n-bu4npf6的ch2cl2溶液为电解液,被测底物的浓度0.001moll-1。循环伏安通常以扫描速率为100mvs-1测得,方波伏安在f=10hz条件下测得。通过电化学方法对苯基桥联的三芳胺及二茂铁端基化合物进行循环伏安及方波伏安测试,得到了两次氧化还原的电位差值(δe)以及平衡常数kc值,相应结果如表1所示。表1化合物e1/2(1)(v)e1/2(2)(v)δe(mv)bkcc实施例10.4900.7302401.14×104实施例20.4930.6911982.22×103实施例30.4960.7332371.00×104实施例40.5020.7092073.15×103由上表数据可知,该苯基桥联的三芳胺及二茂铁端基化合物属于无机-有机混合氧化还原端基化合物,其在电化学上呈现了两次连续的单电子氧化还原过程,δe结果显示通过苯环桥联的二茂铁及三芳胺端基也表现出较强的电子相互作用(耦合),这将为混合氧化还原活性端基分子导线及分子电子的研究提供新的研究思路。上述实施例为本发明较佳的实现方案,除此之外,本发明还可以其它方式实现,在不脱离本技术方案构思的前提下任何显而易见的替换均在本发明的保护范围之内。最后,应该强调的是,为了让本领域普通技术人员更方便地理解本发明相对于现有技术的改进之处,本发明的一些描述已经被简化,并且为了清楚起见,本申请文件还省略了一些其它元素,本领域技术人员应该意识到这些省略的元素也可构成本发明的内容。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1