四羟基修饰的双脲类化合物及其凝胶和基于凝胶检测汞离子的方法与流程
本发明属于汞离子检测技术领域,具体涉及一种四羟基修饰的双脲类化合物,以及采用该化合物制备的可逆共价键分子凝胶和基于该凝胶检测汞离子的方法。
背景技术:
有毒的金属离子对人类的健康和环境有着非常严重的影响,因此,检测水生态系统中这些污染物成为人们关注的焦点。汞是环境中最有害的有毒金属离子之一,一般通过煤的燃烧、电厂、海洋、火山喷发、金矿和固体垃圾的焚烧等途径产生。汞离子(hg2+)最稳定的形式是形成无机汞,它具有腐蚀性和致癌性等高细胞毒性,它能够使大脑、神经系统、肾脏以及内分泌系统受到严重损害,长期接触无机汞会引起自身免疫系统的疾病。因此,对环境和生物样品中汞离子进行高灵敏度和高选择性的检测有着非常重要意义。目前,常用的检测hg2+的方法主要有原子吸收光谱法(atomicabsorptionspectrometry,aas),原子荧光光谱法(atomicfluorescencespectrometry,afs),电感耦合等离子体质谱法(inductivelyoupledplasmamassspectrometry,icpms)和高效液相色谱法(high-performanceliquidchromatography,hplc)等。虽然这些方法有很多优点,但是,它们通常需要昂贵的仪器设备,样品的制备过程繁琐,需要对样品进行分离和富集,从而需要大量的时间。因此,建立一种高灵敏度、高选择性、耗时短、成本低的测定hg2+的方法成为当今研究的热点。光学传感器不需要特殊的仪器,还可以对hg2+进行可视化检测,引起人们的广泛关注。如今,提出了基于有机发色团和荧光基团、共轭聚合物、核酸、dna酶、蛋白、薄膜以及纳米粒子的hg2+传感器。虽然这些光学传感器要比传统方法简单很多,但大多数的灵敏度和选择性低,探针材料的合成步骤繁杂,或不适合实际样品的检验,使其应用受到了很大的限制。因此,设计一种不仅灵敏度和选择性高,而且简单、经济、实用的检测hg2+的方法仍然是目前研究的前沿热点。
技术实现要素:
本发明所要解决的技术问题在于提供一种四羟基修饰的双脲类化合物,以及基于该化合物的可逆共价键分子凝胶和以该凝胶为基质检测汞离子的方法。
解决上述技术问题所采用的四羟基修饰的双脲类化合物的结构式如下所示:
式中r代表
上述四羟基修饰的双脲类化合物的制备方法为:将2-氨基-1,3-丙二醇溶于甲醇中,将式i所示的二异氰酸酯的二氯甲烷溶液逐滴加入上述溶液中,其中2-氨基-1,3-丙二醇与二异氰酸酯的摩尔比为2:1;甲醇与二氯甲烷的体积比为1:75,常温搅拌反应16小时,过滤,用乙酸乙酯洗涤,干燥,得到四羟基修饰的双脲类化合物,具体合成路线如下:
本发明的可逆共价键分子凝胶是由上述的四羟基修饰的双脲类化合物与硼酸盐在二甲亚砜与水的混合溶剂中通过可逆硼氧键和脲基之间的氢键形成,其中硼酸盐为硼酸锂、硼酸钠、四丁基硼酸铵中的任意一种,所述的硼酸盐是由硼酸和氢氧化物反应生成,其中所述的氢氧化物为氢氧化锂、氢氧化钠或四丁基氢氧化铵。
上述可逆共价键分子凝胶的制备方法为:将四羟基修饰的双脲类化合物和硼酸完全溶解于二甲亚砜中,然后加入氢氧化物的水溶液,混合均匀,所得混合液常温静置10~20分钟,得到可逆共价键分子凝胶。
上述可逆共价键分子凝胶的制备方法中,所述的四羟基修饰的双脲类化合物、硼酸、氢氧化物的摩尔比为1:1:1,且混合液中四羟基修饰的双脲类化合物的浓度为0.018~0.050g/ml;所述的二甲亚砜与水的体积比为7:3~9:1。
基于本发明可逆共价键分子凝胶检测汞离子的方法由下述步骤组成:
1、将四羟基修饰的双脲类化合物和硼酸完全溶解于二甲亚砜中,然后加入含氢氧化物和氯金酸的水溶液,混合均匀,常温避光静置10~20分钟,得到含有氯金酸的无色凝胶。
2、在含有氯金酸的无色凝胶上加入水合肼的无水乙醇溶液,在密封条件下避光放置12~48小时,得到含有纳米金颗粒的凝胶。
3、在含有纳米金颗粒的凝胶上加入超纯水将凝胶破坏,然后加入二甲亚砜使溶液澄清透明,得到凝胶和纳米金的复合溶液,采用紫外-可见分光光度计测定该复合溶液的表面等离子共振吸收峰λ0,再加入不同浓度的汞离子标准样品溶液,采用紫外-可见分光光度计测定不同浓度汞离子对应体系的表面等离子共振吸收峰λ,并绘制δλ随汞离子浓度变化的标准曲线,其中δλ=λ0-λ。
4、按照上述步骤3的方法用紫外-可见分光光度计测量待测样品对应体系的表面等离子共振吸收峰λ,根据公式δλ=λ0-λ,计算待测样品对应的δλ,结合标准曲线的线性方程即可高选择性识别汞离子并确定待测样品中汞离子的浓度。
上述步骤1中,所述含有氯金酸的无色凝胶中氯金酸的浓度为0.5~2.0mmol/l。
与现有技术相比,本发明具有以下有益效果:
1、本发明四羟基修饰的双脲类化合物合成步骤简单,产率高,且该化合物与硼酸盐在二甲亚砜与水的混合溶剂中通过硼氧键和脲基之间的氢键可形成可逆共价键凝胶,以形成的凝胶为基质,通过原位还原氯金酸制备金纳米颗粒,该凝胶的三维网络结构可防止纳米金颗粒发生团聚,制得的纳米金颗粒稳定性好,尺寸均匀,分散性好,平均粒径为20~30nm,且凝胶与纳米金颗粒的相容性较好,纳米金对成胶速度和成胶情况不会造成很大的影响。
2、本发明的可逆共价键凝胶和纳米金形成的复合溶液可以实现汞离子的高灵敏度、高选择性检测,检测耗时短、成本低,且复合溶液中纳米金颗粒不易发生团聚,稳定性好,对汞离子的检测带来了极大的方便,对环境和生物样品中汞离子进行高灵敏度和高选择性的检测有着非常重要意义。本发明获得了中国国家自然科学基金(基金号为21473110)的支持。
附图说明
图1是实施例4~12中形成的可逆共价键分子凝胶的照片。
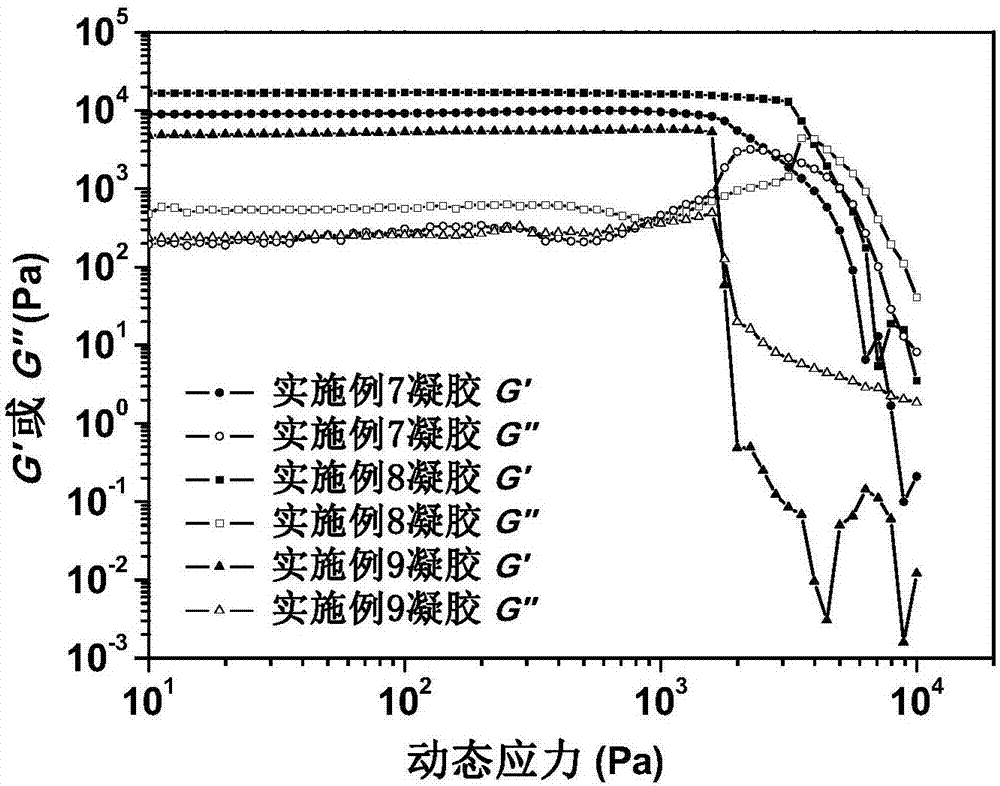
图2是实施例7~9中形成的可逆共价键分子凝胶的应力扫描曲线。
图3是实施例7中形成的可逆共价键分子凝胶的触变性行为曲线。
图4是实施例8中形成的可逆共价键分子凝胶的的触变性行为曲线。
图5是实施例9中形成的可逆共价键分子凝胶的触变性行为曲线。
图6是实施例9、13、14中形成的可逆共价键分子凝胶的应力扫描曲线。
图7是实施例9、15、16中形成的可逆共价键分子凝胶的应力扫描曲线。
图8是实施例17中含有纳米金颗粒的凝胶中分离出来的金颗粒的透射电镜图。
图9是基于实施例8的可逆共价键分子凝胶为基质检测不同浓度汞离子的紫外吸收光谱图。
图10是实施例17中复合溶液的表面等离子共振吸收峰的变化值δλ随汞离子浓度变化的标准曲线。
图11是四羟基修饰的双脲类化合物b、硼酸、氢氧化钠对汞离子检测结果的影响。
图12是采用实施例17的方法检测环境中的不同金属离子的照片。
具体实施方式
下面结合附图和实施例对本发明进一步详细说明,但本发明的保护范围不仅限于这些实施例。
实施例1
制备结构式如下的四羟基修饰的双脲类化合物a
取1.476g(16.20mmol)2-氨基-1,3-丙二醇溶于2ml甲醇中,将150ml含1.524g(8.10mmol)4,4'-二异氰酸基-3,3'-二甲基联苯的二氯甲烷溶液逐滴加入上述溶液中,常温搅拌反应16小时,过滤并用乙酸乙酯洗涤,常温真空干燥,得到四羟基修饰的双脲类化合物a。
所得化合物a经1hnmr、ftir表征确认,具体数据如下:1hnmr(600mhz,dmso-d6,tms),δ=2.17-2.28(6h,s,2-ch3),δ=3.40-3.46;3.49-3.55(8h,m,4-ch2-),δ=3.59-3.66(2h,m,2-ch-),δ=4.72-4.76(4h,t,4-oh),δ=6.59-6.66(2h,d,2-nh-),δ=7.32-7.36(2h,d,2-ph),δ=7.37-7.41(2h,s,2-ph),δ=7.83-7.88(2h,s,2-nh-),δ=7.91-7.95(2h,d,2-ph).ftir(kbr):υ=3312cm-1(o-h),υ=3041cm-1(c-h),υ=2970cm-1(n-h),υ=2883cm-1(c-h),υ=1639cm-1(c=o),υ=1593cm-1(c=c)。
实施例2
制备结构式如下的四羟基修饰的双脲类化合物b
本实施例中,用等摩尔4,4'-二异氰酸二苯甲烷替换实施例1中的4,4'-二异氰酸基-3,3'-二甲基联苯,其他步骤与实施例1相同,得到四羟基修饰的双脲类化合物b。
所得化合物b经1hnmr、ftir表征确认,具体数据如下:1hnmr(600mhz,dmso-d6,tms),δ=3.37-3.42;3.45-3.50(8h,m,4-ch2-),δ=3.55-3.61(2h,m,2-ch-),δ=3.72-3.75(2h,s,-ch-),δ=4.69-4.73(4h,t,4-oh),δ=5.79-6.01(2h,d,2-nh-),δ=7.00-7.06(4h,d,2-ph),δ=7.23-7.29(4h,s,2-ph),δ=8.50-8.54(4h,d,2-nh-).ftir(kbr):υ=3380cm-1(o-h),υ=3290cm-1(n-h),υ=3100,3031cm-1(c-h),υ=2876cm-1(c-h),υ=1630cm-1(c=o),υ=1572cm-1(c=c)。
实施例3
制备结构式如下的四羟基修饰的双脲类化合物c
本实施例中,用等摩尔1,4-苯二异氰酸酯替换实施例1中的4,4'-二异氰酸基-3,3'-二甲基联苯,其他步骤与实施例1相同,得到四羟基修饰的双脲类化合物c。
所得化合物b经1hnmr、ftir表征确认,具体数据如下:1hnmr(600mhz,dmso-d6,tms),δ=3.37-3.42;3.46-3.51(8h,m,4-ch2-),δ=3.55-3.61(2h,m,2-ch-),δ=4.68-4.73(4h,t,4-oh),δ=5.92-5.96(2h,d,2-nh-),δ=7.18-7.22(4h,s,2-ph),δ=8.37-8.43(2h,s,2-nh-).ftir(kbr):υ=3312cm-1(o-h),υ=3041cm-1(c-h),υ=2974cm-1(n-h),υ=2880cm-1(c-h),υ=1639cm-1(c=o),υ=1579cm-1(c=c)。
实施例4
将0.04g(0.090mmol)四羟基修饰的双脲类化合物a溶于344μl二甲亚砜中,超声至溶液澄清,然后加入556μl0.01g/ml(0.090mmol)硼酸的二甲亚砜溶液和100μl0.022g/ml(0.090mmol)氢氧化锂水溶液,常温震荡均匀,静置15分钟,即可形成不透明的可逆共价键分子凝胶。
实施例5
将0.04g(0.090mmol)四羟基修饰的双脲类化合物a溶于344μl二甲亚砜中,超声至溶液澄清,然后加入556μl0.01g/ml(0.090mmol)硼酸的二甲亚砜溶液和100μl0.036g/ml(0.090mmol)氢氧化钠水溶液,常温震荡均匀,静置15分钟,即可形成无色透明的可逆共价键分子凝胶。
实施例6
将0.04g(0.090mmol)四羟基修饰的双脲类化合物a溶于344μl二甲亚砜中,超声至溶液澄清,然后加入556μl0.01g/ml(0.090mmol)硼酸的二甲亚砜溶液和100μl0.232g/ml(0.090mmol)四丁基氢氧化铵水溶液,常温震荡均匀,静置15分钟,即可形成不透明的可逆共价键分子凝胶。
实施例7
将0.04g(0.092mmol)四羟基修饰的双脲类化合物b溶于330μl二甲亚砜中,超声至溶液澄清,然后加入570μl0.01g/ml(0.092mmol)硼酸的二甲亚砜溶液和100μl0.022g/ml(0.092mmol)氢氧化锂水溶液,常温震荡均匀,静置15分钟,即可形成无色透明的可逆共价键分子凝胶。
实施例8
将0.04g(0.092mmol)四羟基修饰的双脲类化合物b溶于330μl二甲亚砜中,超声至溶液澄清,然后加入570μl0.01g/ml(0.092mmol)硼酸的二甲亚砜溶液和100μl0.037g/ml(0.092mmol)氢氧化钠水溶液,常温震荡均匀,静置15分钟,即可形成无色透明的可逆共价键分子凝胶。
实施例9
将0.04g(0.092mmol)四羟基修饰的双脲类化合物b溶于330μl二甲亚砜中,超声至溶液澄清,然后加入570μl0.01g/ml(0.092mmol)硼酸的二甲亚砜溶液和100μl0.240g/ml(0.092mmol)四丁基氢氧化铵水溶液,常温震荡均匀,静置15分钟,即可形成半透明的可逆共价键分子凝胶。
实施例10
将0.04g(0.120mmol)四羟基修饰的双脲类化合物c溶于178μl二甲亚砜中,超声至溶液澄清,然后加入722μl0.01g/ml(0.120mmol)硼酸的二甲亚砜溶液和100μl0.028g/ml(0.120mmol)氢氧化锂水溶液,常温震荡均匀,静置15分钟,即可形成半透明的可逆共价键分子凝胶。
实施例11
将0.04g(0.120mmol)四羟基修饰的双脲类化合物c溶于178μl二甲亚砜中,超声至溶液澄清,然后加入722μl0.01g/ml(0.120mmol)硼酸的二甲亚砜溶液和100μl0.048g/ml(0.120mmol)氢氧化钠水溶液,常温震荡均匀,静置15分钟,即可形成无色透明的可逆共价键分子凝胶。
实施例12
将0.04g(0.120mmol)四羟基修饰的双脲类化合物c溶于178μl二甲亚砜中,超声至溶液澄清,然后加入722μl0.01g/ml(0.120mmol)硼酸的二甲亚砜溶液和100μl0.303g/ml(0.120mmol)四丁基氢氧化铵水溶液,常温震荡均匀,静置15分钟,即可形成半透明的可逆共价键分子凝胶。
实施例13
将0.04g(0.092mmol)四羟基修饰的双脲类化合物b溶于230μl二甲亚砜中,超声至溶液澄清,然后加入570μl0.01g/ml(0.092mmol)硼酸的二甲亚砜溶液和200μl0.120g/ml(0.092mmol)四丁基氢氧化铵水溶液,常温震荡均匀,静置15分钟,即可形成透明的可逆共价键分子凝胶。
实施例14
将0.04g(0.092mmol)四羟基修饰的双脲类化合物b溶于130μl二甲亚砜中,超声至溶液澄清,然后加入570μl0.01g/ml(0.092mmol)硼酸的二甲亚砜溶液和300μl0.080g/ml(0.092mmol)四丁基氢氧化铵水溶液,常温震荡均匀,静置30分钟,即可形成透明的可逆共价键分子凝胶。
实施例15
将0.036g(0.083mmol)四羟基修饰的双脲类化合物b溶于387μl二甲亚砜中,超声至溶液澄清,然后加入513μl0.01g/ml(0.083mmol)硼酸的二甲亚砜溶液和100μl0.217g/ml(0.083mmol)四丁基氢氧化铵水溶液,常温震荡均匀,静置15分钟,即可形成透明的可逆共价键分子凝胶。
实施例16
将0.045g(0.104mmol)四羟基修饰的双脲类化合物b溶于256μl二甲亚砜中,超声至溶液澄清,然后加入644μl0.01g/ml(0.104mmol)硼酸的二甲亚砜溶液和100μl0.271g/ml(0.104mmol)四丁基氢氧化铵水溶液,常温震荡均匀,静置15分钟,即可形成半透明的可逆共价键分子凝胶。
上述实施例4~12形成的可逆共价键分子凝胶的照片如图1所示,发明人研究了盐效应对实施例7~9形成的可逆共价键分子凝胶的力学强度及触变性的影响,结果见图2~5。由图2可见,在低剪切力范围内,实施例7~9形成的可逆共价键分子凝胶的储能模量g′均高于损耗模g″,表现出典型的软固体特性,三种凝胶的弹性模量和屈服应力按实施例8>实施例7>实施例9降低,此外,从图2中还可以看出,当剪切应力高于屈服值时,三种凝胶的g′和g″数值急剧下降,g″均明显高于g′,说明凝胶网络结构在高剪切作用下遭到破坏而表现明显的液态行为。由图3~5的测试结果来看,实施例9中形成的凝胶表现出独特的剪切触变性,体系在破坏与恢复10个作用循环过程中“凝胶-溶胶”相变几乎完全可逆,均保持了分子凝胶原有的粘弹性。而实施例7和8中形成的凝胶它们的“凝胶-溶胶”可逆性呈现出下降的趋势,这可能归因于高剪切力下,两个凝胶会变成碎片。
发明人进一步研究了实施例9、13、14中溶剂效应对形成的可逆共价键分子凝胶的流变学性能的影响,结果见图6。从图6中可以得出,二甲亚砜与水的体积比分别为9:1(实施例9)、8:2(实施例13)、7:3(实施例14)时,凝胶的屈服值依次为1778.0pa、891.2pa、630.9pa,而凝胶的g′和g″未发生明显变化。该结果表明:溶剂的微小改变将导致凝胶力学强度的显著变化。
凝胶的力学强度和粘弹性与胶凝剂的浓度密切相关,因此发明人还研究了实施例9、15、16中浓度效应对形成的可逆共价键分子凝胶的流变学性能的影响,结果见图7。由图7可见,四羟基修饰的双脲类化合物b的浓度分别为0.036g/ml(实施例15)、0.040g/ml(实施例9)和0.045g/ml(实施例16)时,所得凝胶的屈服值依次为223.8pa、777.0pa、6010.2pa,表明凝胶的力学强度随胶凝剂浓度的升高而增强。
实施例17
基于实施例8的可逆共价键分子凝胶为基质检测汞离子
1、将0.04g(0.092mmol)四羟基修饰的双脲类化合物b溶于330μl二甲亚砜中,超声至溶液澄清,然后加入570μl0.1g/ml(0.092mmol)硼酸的二甲亚砜溶液、100μl含3.7mg(0.092mmol)氢氧化钠和1.26mg(1.5×10-3mmol)氯金酸的水溶液,混合均匀,常温避光静置15分钟,得到含有氯金酸的无色凝胶。
2、在含有氯金酸的无色凝胶上加入250μl体积浓度为88%的水合肼的无水乙醇溶液,将瓶口封好,室温避光放置24小时,得到含有纳米金颗粒的紫色凝胶。由图8可见,所得凝胶中金颗粒的平均粒径为20~30nm。
3、将含有纳米金颗粒的凝胶上部剩余的水合肼的无水乙醇溶液倒掉,然后加入150μl超纯水将凝胶破坏,再加入350μl二甲亚砜使溶液澄清透明,得到凝胶和纳米金的复合溶液,采用紫外-可见分光光度计测定该复合溶液的表面等离子共振吸收峰λ0,再分别加入浓度为1、2、3…18、19、20μmol/l的氯化汞水溶液,采用紫外-可见分光光度计测定不同浓度汞离子对应体系的表面等离子共振吸收峰λ,结果见图9,并绘制δλ随汞离子浓度变化的标准曲线,其中δλ=λ0-λ,结果见图10。
由图9可见,随着汞离子浓度的增加,表面等离子共振吸收峰呈现蓝移,吸收强度略有增加,在556nm处观察到等消光点。由图10可见,当汞离子在较低浓度范围内(0~6μmol/l)时,δλ与汞离子浓度呈线性关系,线性方程为:y=0.07143+2x,其中y代表δλ,x为汞离子浓度,其相关系数r=0.9977。根据s/n=3计算出该方法的检出限为0.2μmol/l。
4、按照上述步骤3的方法用紫外-可见分光光度计测量待测样品对应体系的表面等离子共振吸收峰λ,根据公式δλ=λ0-λ,计算待测样品对应的δλ,结合标准曲线的线性方程即可高选择性识别汞离子并确定待测样品中汞离子的浓度。
发明人按照表1所示,考察了实施例17中四羟基修饰的双脲类化合物b、硼酸、氢氧化钠对汞离子(6μmol/l)检测结果的影响,实验结果见图11。
表1对照实验
注:表中“-”表示不含所在单元格中的物质,“√”表示含有所在单元格中的物质。
实验结果显示,本发明检测汞离子的方法中,四羟基修饰的双脲类化合物b、硼酸、氢氧化钠这三种物质缺一不可,表明本发明可逆共价键分子凝胶在汞离子的检测过程中扮演了重要的角色。
为了证明本发明的有益效果,发明人采用实施例17的方法分别对环境中的其他金属离子如铁离子、铬离子、镁离子、钴离子、钡离子、镍离子、钙离子、镉离子、铅离子、锌离子、铜离子的水溶液进行检测。实验结果表明,即使将铁离子、铬离子、镁离子、钴离子、钡离子、镍离子、钙离子、镉离子、铅离子、锌离子、铜离子的浓度增加至100μmol/l,体系的颜色也不发生任何变化,而汞离子浓度为6μmol/l时,体系的颜色马上由原来的紫色变为红色(见图12),说明该方法可实现汞离子的选择性检测。
- 还没有人留言评论。精彩留言会获得点赞!
- 辛夷水提物作为唯一活性成分在制备雌激素药物中的应用的制造方法与工艺
- 高固含量环境友好型聚氨酯灌浆用搅拌灌装装置的制造方法
- 一种聚氨酯文化石模具原料及聚氨酯文化石加工工艺的制造方法与工艺
- 聚氨酯反应釜的制造方法与工艺
- 一种发泡机用切换阀组的制造方法与工艺
- 一种发泡机用电动自洁式过滤器的制造方法与工艺
- (2R)‑5‑甲氧基‑1,2,3,4‑四氢‑2‑萘酚的制备方法与制造工艺
- 一种用于常温常湿条件下催化消除一氧化碳和甲醛的催化剂及其制备方法与制造工艺
- 氨基取代磷腈化合物制造方法、非水二次电池用电解液制造方法及非水二次电池制造方法与制造工艺
- 氨基取代磷腈化合物制造方法、非水二次电池用电解液制造方法及非水二次电池制造方法与制造工艺